Nanomaterialien zur Verbesserung der regenerativen Medizin
Wer hat noch nie einen Film gesehen, in dem ein Mensch seinen Körper regenerieren kann, nachdem er angeschossen oder erstochen wurde?
Ein berühmtes Beispiel ist die Selbstheilung von Wolverine. Auch wenn wir von einem solchen Kunststück noch weit entfernt sind, sind es manchmal genau diese Fantasien, die den wissenschaftlichen Fortschritt vorantreiben, und vielleicht können wir sie bald wahr werden lassen.
Ein großer Schritt in diese Richtung ist die Herstellung künstlicher Gewebe als Ersatz für verloren gegangene oder nicht mehr funktionsfähige natürliche Gewebe, wie z. B. eine Titanprothese.
Um jedoch das Niveau von Marvel-Charakteren bei der Regeneration unseres Körpers zu erreichen, müssen wir noch eine Stufe höher gehen und unsere Technologie auf die nächste Stufe bringen; und es scheint, als hätten wir den Boden unter den Füßen erreicht.
Wissenschaftler haben eine neue Strategie entwickelt, die dem menschlichen Körper hilft, sein eigenes Gewebe zu regenerieren, indem auf Nanomaterialien basierende Ansätze verwendet werden, um das Wachstum von Zellen, die Immunantwort und die Gewebeumbildung zu kontrollieren.
Dieses aufregende neue Wissenschaftsgebiet ist als regenerative Medizin bekannt .
Lassen Sie mich Ihnen mehr darüber erzählen!
Was haben Nanomaterialien mit regenerativer Medizin zu tun?
In einem unserer vorherigen Artikel Fortgeschrittene magnetische Nanopartikel zur Krebserkennung und -behandlung , haben wir gesehen, wie ein Material, wenn es auf sehr kleine Abmessungen geschrumpft wird, radikal andere Eigenschaften annehmen kann. Der Wissenschaft gelingt es Tag für Tag, neue Anwendungen für diese nanotechnologischen Eigenschaften zu finden.
Eines der großen Versprechen von Nanomaterialien ist die Fähigkeit, die Immunantwort zu „modulieren“, indem sie mit menschlichen Biomolekülen (Antikörpern, Zytokinen, Hormonen usw.) verbunden werden.
Aber was bedeutet diese „Modulation“?
Kontrolle der Immunantwort
Das Immunsystem ist die Armee unseres Körpers. Und wie bei jeder Armee werden Soldaten nicht nur zum Angriff und zur Zerstörung eingesetzt, sondern auch als Unterstützungsressourcen. Zum Beispiel kümmert sich das Immunsystem um alle Arten von Eventualitäten, wie z. B. die Erneuerung von Gewebe nach einer Verletzung, und hilft, Umweltungleichgewichte zu kontrollieren, indem es Stoffwechselgifte oder schädliche Fremdstoffe eliminiert.
Diese Kontrolle oder Modulation wird von einer endlosen Anzahl von Biomolekülen (z. B. Zytokinen, Interleukinen und Hormonen) orchestriert, deren Konzentration den Zellen als Signal dient, das ihnen sagt, wie sie sich jederzeit verhalten sollen.
Wenn wir beispielsweise bei einem Patienten ein künstliches Material verwenden, um eine Brandwunde abzudecken, ist es wünschenswert, dass es letztendlich in den Körper des Patienten integriert wird. Konkret möchten wir, dass sich die Zellen des Patienten ansiedeln und in das neue Material einwachsen, sodass es schließlich durch das eigene Gewebe des Patienten ersetzt wird.
Leider erkennt das Immunsystem das Material oft als eine unserem Körper fremde Einheit und versucht, es zu isolieren, indem es um es herum eine Wand aus faserigem Bindegewebe über einen als Fibrose bekannten Prozess bildet. Dies ist ein zellarmes Material, aber reich an Molekülen (Makromoleküle wie Kollagen oder Fibrin), die die Zellen strukturell stützen. Es hat Eigenschaften, die sich deutlich von denen des ursprünglichen Gewebes unterscheiden. Viele von Ihnen würden erkennen, wie steif sich ein Narbengewebe im Vergleich zu normaler Haut anfühlt. Eine Narbe in einem Gelenk kann sogar dessen Bewegung behindern.
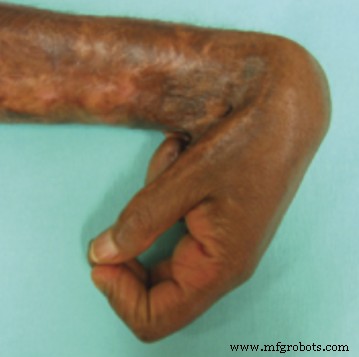
Abbildung 1 Hypertrophe Narbenbildung mit Gelenkkontraktur Aarabi S, Longaker MT, Gurtner GC (2007) Hypertrophe Narbenbildung nach Verbrennungen und Trauma:Neue Behandlungsansätze. PLoS Med 4(9):e234. doi:10.1371/journal.pmed.0040234 – http://www.plosmedicine.org/article/info%3Adoi%2F10.1371%2Fjournal.pmed.0040234
Hervorgehoben in meinem vorherigen Artikel Von PLA zum Biodruck:Science-Fiction-Tools für den medizinischen Bereich , besteht eine Strategie, um mit dieser Abwehr durch das Immunsystem umzugehen, darin, Biomaterialien zu verwenden, um Gerüste (unterstützende Strukturen, die von den eigenen Zellen des Patienten besiedelt werden) aus Molekülen wie Kollagen aufzubauen. Wenn wir ein Gerüst implantieren, das nur aus Kollagenfasern besteht, resorbiert der Körper leider dieses Material und ersetzt es im besten Fall durch Fibrose.
Das kann uns interessieren, wenn wir eine „künstliche Narbe“ erzeugen wollen, zum Beispiel um die Bauchdecke nach einem Leistenbruch zu reparieren; in dem wir ein Phasix™-Netz aus Poly-4-hydroxybutyrat (P4HB) verwenden konnten, um den Wanddefekt auszubessern.
Um eine funktionelle Integration eines Implantats zu erreichen, müssen wir die Zelldifferenzierung vorantreiben (d. h. jeder Zelle ihren spezifischen Typ und ihre spezifische Funktion geben) und die Möglichkeit vermeiden, dass das Immunsystem das Implantat abstößt. Wir können dies tun, indem wir Nanomaterialien als „Träger“ verwenden, um die Biomoleküle zu liefern, und als Signale, um diesen Prozess voranzutreiben.
Aber was wäre, wenn wir diese Biomoleküle immobilisieren oder an jeden beliebigen Ort lenken könnten?
Können wir das Immunsystem kontrollieren?
Beispielsweise kann die Kombination von Nanomaterialien und Antikörpern zur Stärkung der Immunantwort eingesetzt werden, etwa im Kampf gegen Krebs (Antikörper-modifizierte Eisenoxid-Nanopartikel).
Einige Nanomaterialien selbst haben bereits direkte hemmende oder stimulierende Wirkungen (je nach Material) auf die Immunantwort (Edelmetalle, Metalloxid-Nanopartikel, Ceroxid oder Dendrimere sind einige Beispiele). Indem wir also einfach die Oberfläche eines Implantats mit diesen Nanopartikeln beschichten, können wir tatsächlich einen Angriff des Immunsystems darauf stoppen. [1]
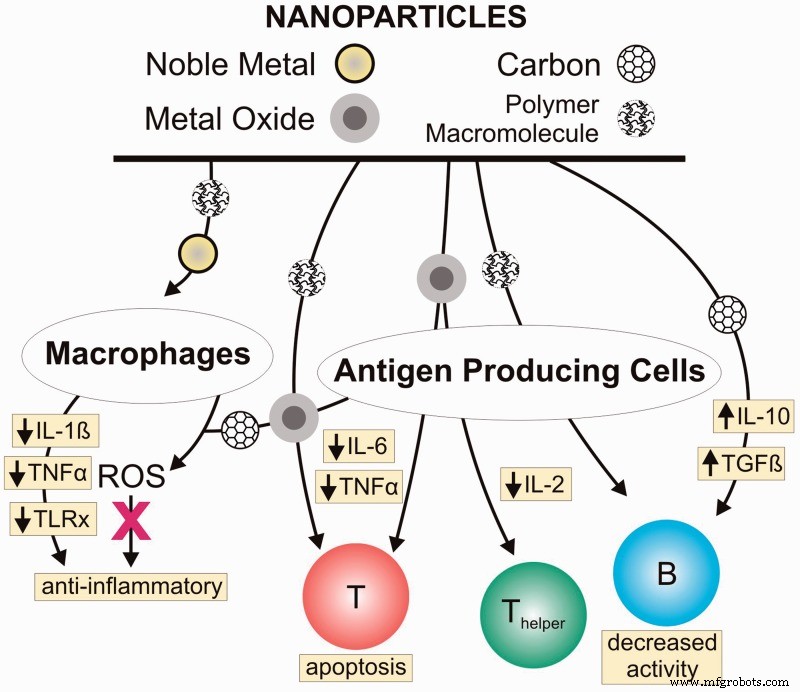
Abbildung 2 Nanomaterialien mit direkter Hemmwirkung auf die Immunantwort Ngobili Terrika A, Daniele Michael A. Nanoparticles and direct immunosuppression.1 May, 2016 Experimental Biology and Medicine 106 Volume:241 issue:10, pages:1064-1073; https://doi.org/10.1177/1535370216650053 https://journals.sagepub.com/doi/abs/10.1177/1535370216650053
Strategien zur Immobilisierung von Nanomaterialien und Biomolekülen auf Implantatoberflächen
Wie wir bereits erwähnt haben, gibt es zwei Hauptgründe, die Oberfläche eines Implantats zu beschichten:entweder um seine Biokompatibilität zu erhöhen (um zu verhindern, dass das Immunsystem es angreift) oder um Biomoleküle zu fixieren, die die Zellproliferation stimulieren und steuern (um die Implantat mit patienteneigenem Gewebe).
Die Idee, ein biologisch abbaubares Gerüst (mit Wachstumsfaktoren beschichtet) zu implantieren, das im Laufe der Zeit durch das Gewebe des Patienten ersetzt wird, ist ein Thema, das wir bereits in Von PLA zum Biodruck:Science-Fiction-Tools für den medizinischen Bereich . Solche Gerüste befinden sich noch in der Forschungsphase, aber es ist nur eine Frage von Jahren, bis sie möglicherweise in die klinische Praxis eintreten.

Die Erhöhung der Biokompatibilität von Fremdmaterialien ist eine aktuelle Notwendigkeit für die Industrie. Damit der menschliche Körper ein implantiertes Biomaterial nicht abstößt, müssen wir die Beschichtung (Nanomaterialien oder Biomolekül-Nanomaterial-Komplexe), die das Immunsystem regulieren, auf die Oberfläche unseres Implantats kleben. Wenn also eine Zelle des Immunsystems ihr zu nahe kommt, hemmt die Beschichtung die Zelle und verhindert die Entstehung einer Entzündungsreaktion um das Implantat herum.
Aber wie können wir eine solche Beschichtung herstellen?
Grundsätzlich gibt es zwei Möglichkeiten, die Beschichtung auf ein Implantat zu „kleben“:nicht-kovalente Immobilisierung und kovalente Immobilisierung.
Nicht-kovalente Immobilisierung (NCI):
NCI ist die einfachste und billigste Methode, um das Implantat zu beschichten, aber es hängt weitgehend davon ab, wie hydrophil das Implantatmaterial ist. Es basiert auf den elektrostatischen Ladungen, die eine Anziehungskraft zwischen dem Material, das wir implantieren, und der Beschichtung erzeugen würde.
Diese Methode bietet eine schnelle Freisetzung von Biomolekülen und ist daher am bequemsten, wenn wir an einer abrupten, aber kurzlebigen Reaktion interessiert sind. Sein größter Vorteil sind darüber hinaus die niedrigen Herstellungskosten.
NCI kann entweder durch Adsorption (winzige Partikel mit Größen zwischen 500 Å und 1 mm, die an der Oberfläche haften) oder durch Einschluss (in einer porösen Matrix eingeschlossene Partikel) aufgebracht werden. [2]
Beim Einschluss besteht die Matrix aus wasserlöslichen Polymeren wie Carrageenan, teilweise hydrolysiertem Kollagen (Gelatine), Alginat, Agar oder Zellulosetriacetat.[2, 3]
Aber was passiert, wenn das Implantatmaterial hydrophil und das Biomolekül hydrophob ist (oder umgekehrt)?
Eine einfache Idee kann eine effektive Lösung sein:die Verkapselung des Biomoleküls!

Einkapselung in die Umhüllung des Biomoleküls, die mit Polymeren wie Agarose, Poly(ethylenglykol) (PEG) oder Poly(N-vinylpyrrolidon) (PVP) leicht durchgeführt werden kann.
Ein Beispiel für diese Methode ist die Verwendung eines Polysulfongerüsts, das mit einer mit Biomolekülen angereicherten Agarosegellösung gefüllt ist, um die Regeneration von Nervenfasern zu steuern und Entzündungen zu reduzieren [4].
Wenn das Gerüst nicht ganz hydrophil ist, besteht die beste Strategie zur Immobilisierung des Biomoleküls außerdem darin, es in einer separaten wässrigen Phase über einen Prozess namens Wasser-in-Öl-in-Wasser (oder Doppelemulsion) einzukapseln. Wir können auch eine direkte Absorption auf der Materialoberfläche mit organischen Lösungsmitteln durchführen.
Ein Beispiel für ein hydrophobes Polymer, das häufig zur Immobilisierung von Biomolekülen wie Hormonfaktoren oder sogar Arzneimitteln verwendet wird, ist Poly(milch-co-glykolsäure) (PLGA).
Kovalente Immobilisierung (CI)
Die kovalente Immobilisierung besteht darin, eine irreversible Bindung zwischen unseren spezifischen Biomolekülen und dem Polymer herzustellen, aus dem unser Implantat besteht, indem sogenannte Vernetzungsmittel verwendet werden; das sind chemische Verbindungen, die auf eine physikalische Bedingung (Wärme, Licht…) reagieren und uns dabei helfen, eine Bindung herzustellen, die beispielsweise eine Polymerkette mit einer anderen verbinden könnte (wir könnten sie uns als Fesseln vorstellen, die durch Licht oder Wärme geschlossen werden beide Polymere verknüpfen).
Diese Methode führt zu einer viel weniger abrupten Wirkung auf das Immunsystem, obwohl sie viel länger anhält; Daher ist es vorzuziehen, es zu verwenden, wenn wir an einer langfristigen und stabilen Reaktion interessiert sind.
Der große Vorteil dieser Methode besteht darin, dass wir damit eine stratifizierte Gewebedifferenzierung durchführen können. Dies bedeutet, dass wir verschiedene Bindungspunkte in unserem Gerüst für verschiedene Faktoren entwerfen können, wodurch Regionen mit unterschiedlichen Biomolekülkonzentrationen geschaffen werden, um ein unterschiedlich strukturiertes Gewebe zu fördern.
Als Basiselement können Kollagen-Glykosaminoglykan (CG)-Gerüste verwendet werden (unter Verwendung von Carbodiimid als Vernetzer angesichts der Allgegenwart von NH2-Gruppen auf ihrer Oberfläche).
Ein Beispiel für eine kovalente Immobilisierung wäre die Konjugation von Polyethylenimin (PEI) mit Heparin zur Bildung einer Hülle, um die Biokompatibilität von NiTi-Legierungsoberflächen zu erhöhen [5].
Eine Vernetzungsmethode, die in den letzten Jahren an Bedeutung gewonnen hat, ist die Verwendung von Acrylaten zur Polymerisation von PEG-Hydrogelen. Acrylate sind funktionelle Gruppen, die gegenüber ultraviolettem Licht empfindlich sind. Diese Gruppen können Peptiden (oder anderen Wachstumsfaktoren) hinzugefügt werden, wodurch die Synthese durch Photopolymerisation von Gerüsten gesteuert wird, die aus Polymer-Biomolekül-Hybriden bestehen. Die Möglichkeit, diesen Prozess in den 3D-Druck zu integrieren, um unserem Gerüst ein Strukturmuster zu verleihen, macht die Photopolymerisation zu einer der relevantesten Methoden zur Immobilisierung von Biomolekülen.
Es wurden auch alternative Photolithographieverfahren entwickelt, beispielsweise verwendet das Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik eine Methode, die darin besteht, Wachstumsfaktoren mit Benzophenon (BP) an CG-Gerüste zu binden. [6, 7]
Ein anderes, selektiveres Ziel, aufgrund seiner geringeren Allgegenwart in Bezug auf die NH2-Gruppe, ist die SH-Gruppe. Crosslinker auf Sulfhydrylbasis werden häufig verwendet, um eine Beschichtung zu schaffen, die die Aktivierung des Komplements (eine sehr wichtige Komponente des Immunsystems) gegen unser Transplantat hemmt [8].
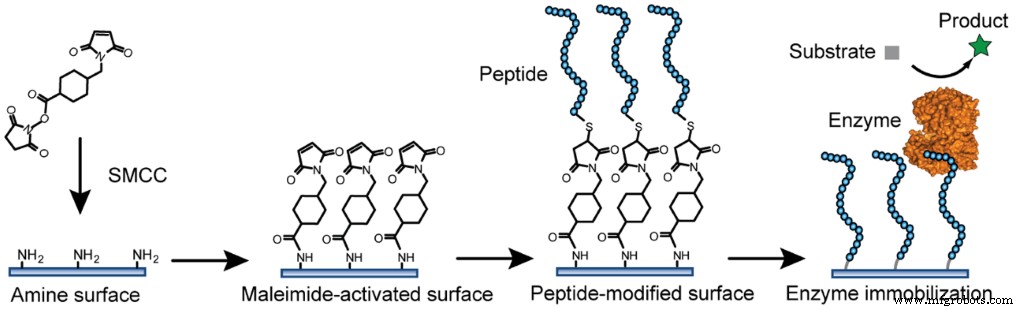
Abbildung 3 Beispiel einer Enzymimmobilisierung durch kovalente Bindung Fu J, Reinhold J, Woodbury NW (2011) Peptide-Modified Surfaces for Enzyme Immobilization. PLoS EINS 6(4):e18692. https://doi.org/10.1371/journal.pone.0018692 https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0018692
Schlussfolgerungen
Es gibt also eindeutig verschiedene Strategien, um Biomoleküle auf der Oberfläche eines Materials zu immobilisieren, um die Immunantwort oder den Differenzierungsprozess zu kontrollieren.
Bevor Sie sich für eine Immobilisierungsmethode entscheiden, ist es wichtig, die Eigenschaften des Materials, das Sie verwenden werden, und die Kurve des Freisetzungsprofils der Biomoleküle, die Sie erreichen möchten, zu kennen. Der beste Ansatz ist eine Kombination verschiedener Konjugationsmethoden, wobei zu berücksichtigen ist, dass das Immunsystem nicht statisch ist. Es zeigt eine dynamische Variation im Laufe der Zeit.
Die Beschichtung von Implantaten mit Nanomaterialien (oder Nanomaterial-Biomolekül-Komplexen) zur Erhöhung der Biokompatibilität von Implantaten ist heutzutage weit verbreitet. Diese Tatsache steht jedoch in scharfem Kontrast zu dem Fall der Herstellung von Gerüsten mit einer geschichteten Konzentration von eingekapselten oder gebundenen Biomolekülen. Trotz der enormen Aktivitäten auf diesem Gebiet gibt es heute nicht viele Unternehmen, die diese Gerüste anbieten, und es müssen noch viele regulatorische Maßnahmen angegangen werden, bevor diese Produkte auf den Markt gebracht werden.
Das bedeutet, dass wir noch etwas warten müssen, um eine vollständige narbenfreie Heilung durchführen zu können. Aber das Warten wird höchstwahrscheinlich nicht lange dauern. Diese vielversprechende Technologie könnte bereits in wenigen Jahren in der täglichen medizinischen Praxis eingesetzt werden.
Industrietechnik
- Wie Leitern die Sicherheit und Zuverlässigkeit erhöhen
- Graphen bringt Nanomaterialien an ihren Platz
- Wie KI IoT-Umgebungen verbessert
- Künstliches neuronales Netzwerk kann die drahtlose Kommunikation verbessern
- Biologische Verschlüsselungsschlüssel können das Sicherheitsniveau in der Post-Quanten-Ära erhöhen
- Verbessern Sie die funktionsübergreifende Zusammenarbeit mit Praxisgemeinschaften
- Grundprinzipien regenerativer Antriebe – Teil 2
- Der Wert des Wasserstrahlschneidens in der Medizin
- 5 reale Anwendungen von KI in der Medizin (mit Beispielen)
- Verbessern Sie das operative Know-how Ihres Unternehmens



