Ein hochempfindlicher CNTs/SnO2/CuO-Sensor bei Raumtemperatur für H2S-Gasmessanwendungen
Zusammenfassung
Gassensoren auf der Basis von Zinndioxid-Kohlenstoff-Nanoröhren-Verbundfilmen wurden durch ein einfaches, kostengünstiges Sol-Gel-Spin-Coating-Verfahren unter Verwendung von PEG400 als Lösungsmittel hergestellt. Nanostrukturiertes Kupfer wurde auf CNTs/SnO2 . beschichtet und dann wurde Kupfer bei 250 °C in Kupferoxid umgewandelt. Der spezifische Widerstand der fertigen Verbundfilme ist hochempfindlich gegenüber der Anwesenheit von H2 S, das sich bei Raumtemperatur leicht anheften oder lösen ließ. Die Ansprech- und Erholungszeit des Sensors beträgt 4 min bzw. 10 min, und der Empfindlichkeitswert beträgt 4,41. Inzwischen sind die CNTs/SnO2 /CuO-Sensor hat auch eine niedrige Nachweisgrenze, hohe Selektivität gegenüber H2 S und stabile Leistung mit unterschiedlichen Konzentrationen von H2 S.
Einführung
Mit der Entwicklung der Industrialisierung wird die Schadstoffbelastung immer ernster, so dass verschiedene Arten von Gassensoren umfassend untersucht wurden [1,2,3,4,5,6,7]. SnO2 als n-leitender und umweltfreundlicher Halbleiter wurde von vielen verschiedenen Forschern untersucht [8,9,10,11]. Es kann aufgrund seiner Fähigkeit, Moleküle in der Gasphase zu absorbieren, als ein ausgezeichnetes gasempfindliches Material angesehen werden, das weithin für die Entwicklung von Gassensoren verwendet wird. Der Mechanismus der Gasdetektion ist die Änderung der Materialleitfähigkeit durch die reversible Gas-Feststoff-Wechselwirkung an der Oberfläche von Zinndioxid [12]. Es gibt einige Methoden, die eingeführt wurden, um die Leistung von SnO2 . zu verbessern Gassensor, einschließlich Dotierung mit Metalloxid (z. B. TiO2 , La2 O3 ) [13, 14], katalytisch aktive Additive (z. B. Pt, Pd und Au) [9, 15,16,17,18] und Zugabe von Graphen und Kohlenstoffnanoröhren [8, 19, 20]. Es hat Anwendungen bei Umweltproblemen und industriellen Gasüberwachungsproblemen, wie z. B. SO2 [21], CO [20, 22], NO2 [23] und H2 S [24, 25], die ein großes Anliegen für die Umweltsicherheit darstellen.
Schwefelwasserstoff ist ein farbloses, giftiges Gas. Es gibt viele Quellen für Schwefelwasserstoff, normalerweise als Produkt des natürlichen Zersetzungsprozesses bestimmter chemischer Reaktionen und von Proteinen und einigen Verunreinigungen, die in verschiedenen Arten von Produktionsprozessen wie dem Bergbau und der Nichteisenmetallverhüttung, der Schwefelölexploration vorkommen , Gummi- und Zuckerindustrie, Abbau von Niedertemperatur-Kokskohle und Behandlung von Sümpfen, Kanälen und Abwasserkanälen. Schwefelwasserstoff ist ein gesundheitsschädliches Gas [26,27,28,29,30,31]. Auch geringe Konzentrationen von Schwefelwasserstoff können den menschlichen Geruchssinn schädigen. Hohe Konzentrationen von Schwefelwasserstoff können Riechnerven lähmen [30, 32]. Da das Gas mit der Nase tödlich entdeckt werden kann, ist der Nachweis von Schwefelwasserstoff erforderlich.
Studien zeigen, dass Kohlenstoffnanoröhren (CNTs) gute Kandidaten als potenzielle „Dotierstoffe“ von SnO2 . sind [19, 33]. CNTs haben eine große Oberfläche und können leicht molekular adsorbiert werden [34]. CNTs können auch die elektrostatische Ladungsübertragungsumgebung des Materials beeinflussen und so die Leistung von SnO2 . verbessern Sensoren.
Gassensoren basierend auf SnO2 Nachweis von Stickstoffdioxid, Kohlenmonoxid, Flüssiggas [35], Gasen flüchtiger organischer Verbindungen und anderen Gasen und Dämpfen. Um jedoch vernünftige Reaktionen zu erhalten, müssen die Betriebstemperaturen dieser Sensoren herkömmlicherweise über 200°C liegen. Bei Raumtemperatur gibt es kaum vernünftige Reaktionen. Franket al. [19] einen Gassensor für H2 . entwickeln S bei Raumtemperatur mit Zinndioxid-Kohlenstoff-Nanoröhren-Verbundfilmen. Obwohl die Ansprech- und Erholungszeit des Gassensors sehr kurz ist, ist die Empfindlichkeit gering.
In diesem Beitrag wird ein neuartiger Gassensor auf Basis von Kohlenstoff-Nanoröhrchen-Zinndioxid (CNTs/SnO2 ) wurden erfolgreich Verbundfilme mit Nano-Kupferoxid synthetisiert. Der Sensor kann H2 . erkennen S mit niedriger Konzentration mit einer Reaktionszeit von bis zu Dutzenden von Sekunden. Das Wichtigste ist, dass die Empfindlichkeit bei Raumtemperatur viel höher ist als bei anderen Gassensoren.
Experimenteller Abschnitt
Materialien und Methoden
Das CNT wurde von Chengdu Organic Chemicals Co. Ltd., Chinesische Akademie der Wissenschaften, bezogen. Wir behandelten Kohlenstoff-Nanoröhrchen zur Ansäuerung mit einem Volumenverhältnis von 3:1 von konzentrierter Schwefelsäure und konzentrierter Salpetersäure. Zum einen das SnCl4 als Rohstoff für das SnO2 B. durch Sol-Gel, wurde im EG bei einer Temperatur von 80°C unter magnetischem Rühren gelöst. Das CNT wurde der obigen Lösung zugesetzt und 3 h bei 80 °C magnetisch gerührt. Später betrug die Temperatur bis zu 120 °C für die Hydrolysereaktion etwa 3 h. Danach wurde das PEG-400 unter Magnetrührung zu der Lösung gegeben, um die Gewinnung von Oberflächenfilmen zu erleichtern. Das Schleuderbeschichtungsverfahren wurde verwendet, um die zusammengesetzten Oberflächenfilme in Siliciumdioxidsubstraten zu bilden. Wir verwendeten einen Rohrofen zur Wärmebehandlung bei 450°C für eine Stunde der Spin-Coating-Filme, die die CNTs/SnO2 . bilden sollen Verbundfolien. Danach wurde nanostrukturiertes Kupfer mit etwa 6 nm auf die Verbundfilme mit einem Vakuumaufdampfverfahren mit einem Strom von 23 Å und einer Verdampfungsrate von 2 /s aufgetragen. Dann wurde Kupfer bei 250 °C etwa 2 h lang in Kupferoxid umgewandelt. Schließlich verwendeten wir Vakuumverdampfung, um die Gold-Interdigitalelektroden zu bilden. Die Probe des Sensors ist in Abb. 1 dargestellt. Wir haben auch für SnO2 . vorbereitet und SnO2 /CuO-Nanokomposit in gleicher Weise für den Vergleich.
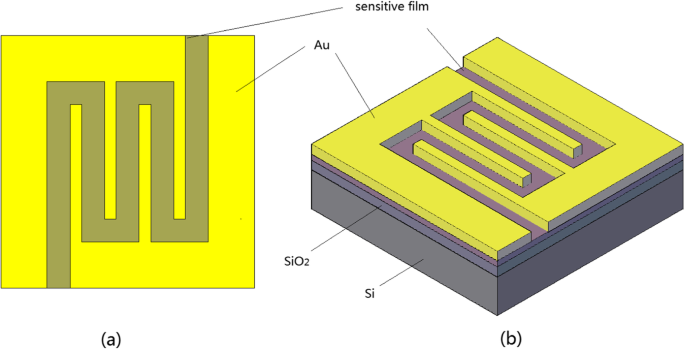
Schema von a Draufsicht auf Gassensor und b Stereogramm des Gassensors
Verfahren zur Gasmessung
Abbildung 2 zeigt das System zur Gasdetektion und Stickstoff wurde als Trägergas verwendet. Die ursprüngliche Konzentration von H2 S ist 1000 ppm. Die erforderliche Testkonzentration wurde durch die Mischung aus Trägergas und Analytgas erreicht, so dass der erforderliche ppm-Wert erreicht werden kann. Die Konzentration des Analytengases wurde durch digitale Durchflussmesser präzise kontrolliert, die die Flussrate von Trägergas und Analytengas kontrollierten. Es hält eine Durchflussrate von 400 sccm aufrecht, wenn das Gas durch die Testkammer strömt. Und die Durchflussraten von Trägergas und Analyt wurden geändert, um die erforderliche Konzentration durch die digitalen Durchflussmesser zu erhalten. Der Standard der Gasprüfung wurde bei Raumtemperatur, Atmosphärendruck und Stickstoffgasatmosphäre mit vernachlässigbarer relativer Luftfeuchtigkeit durchgeführt.
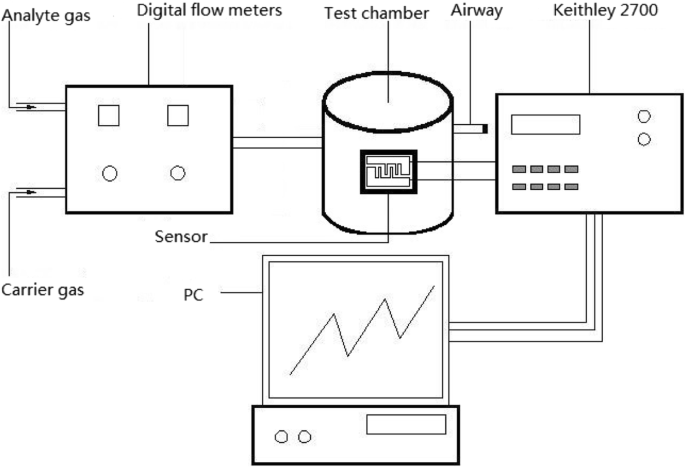
Der für die Gasdetektion verwendete Aufbau
Der Sensor wurde in der Testkammer aufbewahrt, die von Teflon hergestellt wurde. Die Prüfkammer besteht aus vier Extraktionselektroden, einem Gaszugang und einem Atemweg. Es kann über vier Sensorproben in der Prüfkammer platziert werden, sodass wir vier Sensoren gleichzeitig testen können. Der Keithley 2700 wurde verwendet, um die Widerstandsänderung der Sensoren zu erfassen. Durch die Kommunikation mit dem Computer über Software werden die Echtzeitdaten direkt auf dem Computer angezeigt.
Der Widerstand der Sensoren kann von Keithley 2700 in Echtzeit erfasst werden. Die Kurve der Widerstandsänderung kann erhalten und auf dem Computerbildschirm angezeigt werden. Im Folgenden sind die Formeln für Gasreaktion und Empfindlichkeit aufgeführt.
$$ \mathrm{Empfindlichkeit}=\frac{R_a-{R}_c}{\Updelta C}=\frac{\Updelta R}{\Updelta C} $$ (1) $$ \mathrm{Response}=\ frac{R_a-{R}_c}{R_c}=\frac{\Delta R}{R_c} $$ (2)wo R c repräsentiert den Widerstand des Geräts in einem Trägergas aus reinem N2 , R a der Widerstand des Gemisches aus Trägergas und Analytgas ist und ∆C ist die Änderung der Analytgaskonzentration.
Ergebnisse und Diskussion
FESEM wurde durchgeführt, um die morphologischen Eigenschaften der Proben zu erhalten, wie in Abb. 3 gezeigt. Abb. 3a zeigt die unberührten Kohlenstoffnanoröhren; in der Abbildung haben sie sich zu einer Gruppe zusammengeschlossen und die Struktur ist sehr intensiv, sodass Gase kaum in das Innere der Kohlenstoff-Nanoröhrchen gelangen können. Und es gibt viele Verunreinigungen auf der Oberfläche von Kohlenstoff-Nanoröhrchen. Aus Abb. 3b und c sind die Verunreinigungen verschwunden und die Kohlenstoffnanoröhren wurden nach der Oxidationsbehandlung lockerer. Das Pulver des ersten Schrittmaterials CNTs/SnO2 gesammelt und das FESEM-Bild davon ist in Abb. 3 d und e gezeigt. Die in der Abbildung zu findenden Kohlenstoff-Nanoröhrchen sind im Vergleich zu den Kohlenstoff-Nanoröhrchen in Abb. 3 c etwas dicker und gröber. Es ist eine Zinnoxidbeschichtung der Kohlenstoff-Nanoröhrchen. Wie in Abb. 3f gezeigt, wurde der hergestellte Verbundfilm untersucht. Auf der Oberfläche wurde eine poröse und gut lockere Struktur beobachtet. Es ist wahrscheinlich, dass es eine Kern-Schale-Struktur bildet, die aus den Kohlenstoffnanoröhren als Kern, dem Zinnoxid und dem Kupferoxid als Hülle besteht. Und die Kohlenstoffnanoröhren in diesen Bereichen spielen möglicherweise eine Rolle bei der Übertragungsladung.

FESEM-Bilder von a unberührte Kohlenstoff-Nanoröhrchen; b , c Kohlenstoff-Nanoröhrchen mit Oxidationsbehandlung; d , e CNTs/SnO2 Nanokomposit; und f CNTs/SnO2 /CuO-Nanokompositfolie
Die vorbereiteten Proben wurden durch XRD-Charakterisierung untersucht und die XRD-Kurven sind in Abb. 4 gezeigt. Wir können deutlich einen offensichtlichen Peak bei 2θ von 26° sehen, der ein typischer XRD-Peak für CNTs ist. Außerdem sind die Beugungspeaks bei 26,6°, 33,8°, 51,8°, 54,7° und 65,9° auf SnO2 . indiziert (JCPDS-Karte Nr. 41-1445). Und da der CuO-Gehalt zu gering ist, sind die CuO-Peaks nicht offensichtlich. Aber wir finden immer noch die schwachen Peaks bei 35,5°, 38,6°, 48,8°, 61,5° und 66,3° Indizierung auf CuO (JCPDS-Karte Nr. 89-2529).
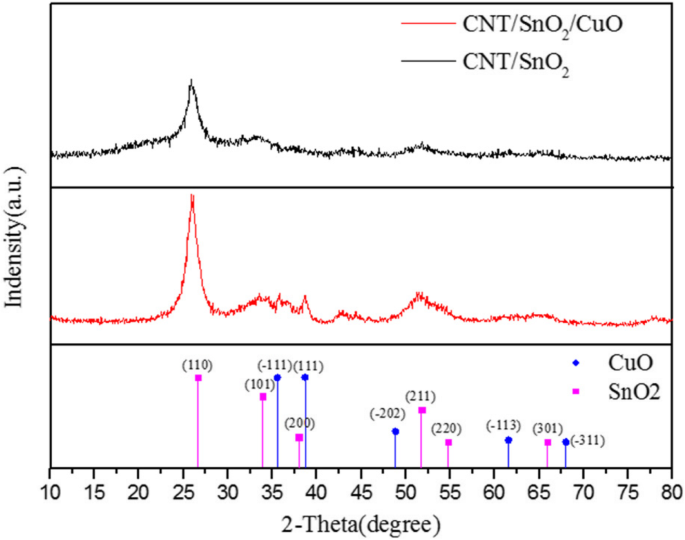
XRD-Muster der CNTs/SnO2 und CNTs/SnO2 /CuO-Nanokomposit
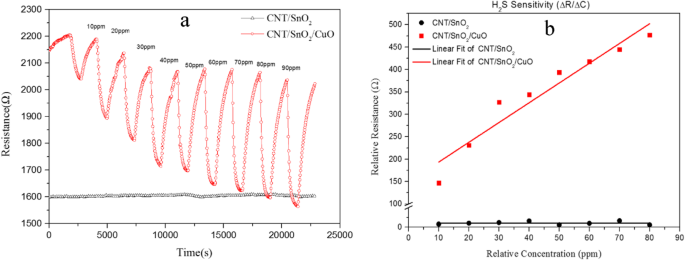
a Die Reaktion der CNTs/SnO2 und CNTs/SnO2 /CuO-Nanokomposit zu H2 S. b Die Empfindlichkeit der CNTs/SnO2 und CNTs/SnO2 /CuO zu H2 S
Die Reaktion der CNTs/SnO2 Nanokomposit und die CNTs/SnO2 /CuO-Nanokomposit zu Schwefelwasserstoff ist in Abb. 5a mit Konzentrationen von 10, 20, 40, 60 und 80 ppm gezeigt. Wenn Sensormaterialien unterschiedlichen Konzentrationen von H2 . ausgesetzt waren S bei Raumtemperatur zeigen sie den zeitlichen Verlauf des Widerstandssignals (Antwort) [19]. Beachten Sie, dass die CNTs/SnO2 Nanokomposit zeigt grundsätzlich keine Reaktion. Obwohl es einige kleine Unterschiede im Basislinienwiderstand der Konzentration von 20 bis 40 ppm gibt, sind die CNTs/SnO2 /CuO-Nanokomposit behält hauptsächlich die gute Reversibilität. Aus dem Diagramm ist ersichtlich, dass bei H2 S Gas wird in die Prüfkammer abgegeben (Gas an), die Ansprechzeit beträgt 4 min. Analog dazu, während die H2 S Gas wird aus der Prüfkammer entfernt (Gas aus), der Widerstand steigt mit einer Erholzeit von 10 min. Die Reaktionszeit und die Erholungszeit sind definiert als die Zeit, die der Sensorausgang benötigt, um 90 % der höchsten Reaktion bzw. 90 % des Minimums zu erreichen. In Abb. 5a können wir dies auch als Konzentration des H2 . erhalten S-Gas erhöht, die Variation des Widerstands verringert. Dies kann der Grund dafür sein, dass der Sensor mit zunehmender Gaskonzentration die Sättigungskonzentration erreicht. Abbildung 5 b zeigt die H2S-Empfindlichkeitswerte der CNTs/SnO2 und CNTs/SnO2/CuO aus Gl. (1). Aus den Diagrammen ist die Beziehung zwischen dem relativen Widerstand (ΔR) und der relativen Konzentration (ΔC) ungefähr linear. Der Empfindlichkeitswert von CNTs/SnO2/CuO beträgt 4,41, während CNTs/SnO2 5,95 × 10−4 beträgt. Im Vergleich zu CNTs/SnO2 zeigt sich die Empfindlichkeit des CNTs/SnO2/CuO-Nanokompositmaterials bei Raumtemperatur stark verbessert.
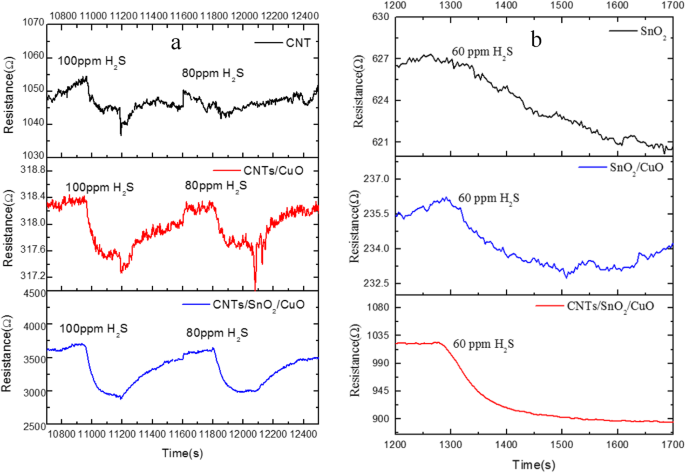
a , b Vergleich der Leistung von Nanokompositen beim Nachweis von H2 S
Außerdem ist der Leistungsvergleich von SnO2 , CNTs/CuO, SnO2 /CuO und CNTs/SnO2 /CuO-Nanokomposit beim Nachweis von H2 S ist in Abb. 6 dargestellt. Es zeigt, dass die CNTs/SnO2 /CuO-basierter Sensor hat die glatteren Ansprechkurven, die weniger Störungen bedeuten. Inzwischen CNTs/SnO2 /CuO-basierter Sensor zeigt eine höhere Empfindlichkeit bei der Erkennung von H2S.
Um die Wiederholbarkeit des Sensors zu untersuchen, testen wir die Ansprech- und Erholungseigenschaften bei 40 ppm H2 S und Raumtemperatur, wie in Abb. 7 gezeigt. Die Kurve zeigt, dass der Sensor des CNTs/SnO2 /CuO hat eine gute Wiederholbarkeit und Stabilität in der Konzentration von 40 ppm H2 S. Der erste reversible Zyklus der Reaktion weist einige Störungen im Erholungsbereich auf. Dies kann der Grund dafür sein, dass die Basislinie des Widerstands des Sensors nicht sehr glatt war. Im Laufe der Zeit wurde die Basislinie des Widerstands viel glatter, so dass der spätere reversible Zyklus der Reaktions- und Erholungskurve viel besser wurde. Die Ansprech- und Erholungszeit des Sensors kann etwas länger sein als bei einigen Sensoren, was mit einigen Faktoren zusammenhängen kann, einschließlich der Dicke der Sensorschicht, der Gasdiffusion und der Menge der Gasadsorption auf dem Sensormaterial bei unterschiedlichen Betriebsbedingungen Temperaturen [36,37,38]. Der Sensor der CNTs/SnO2 /CuO kann die Betriebstemperatur der Raumtemperatur sein. Bei Raumtemperatur kann die anorganische chemische Reaktion etwas langsam sein, was zu den Ergebnissen führt. Aus einem anderen Grund kann es die hohe Empfindlichkeit sein, die Zeit benötigt, um Gas zu absorbieren und Gas freizusetzen.
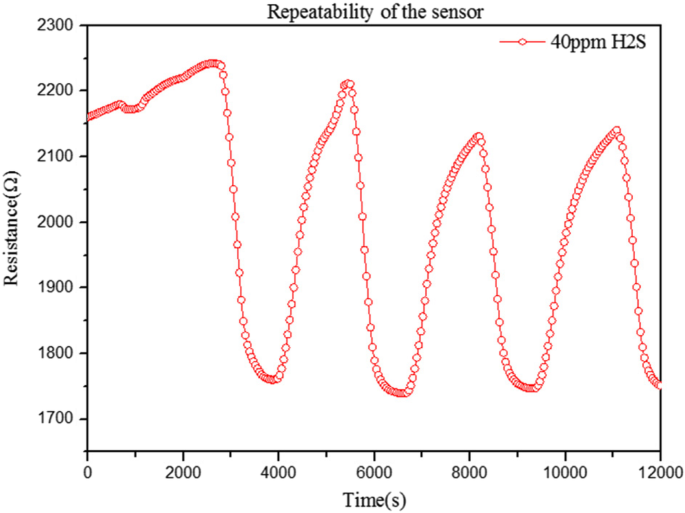
Reproduzierbarkeit des Sensors von CNTs/SnO2 /CuO in der Konzentration von 40 ppm H2 S
Abbildung 8 zeigt das Balkendiagramm, das die Gasselektivität von CNTs/SnO2 . veranschaulicht /CuO-Sensor bei 40 ppm gegenüber vier Gasen. Es ist offensichtlich, dass die Empfindlichkeit des Sensors gegenüber H2 S beträgt 19%, was die maximale Reaktion der vier Gase ist. Außerdem ist die Empfindlichkeit des Sensors gegenüber NH3 beträgt 4,1%, was die zweite maximale Antwort ist. Und die Empfindlichkeit der anderen beiden Gase ist viel geringer als die der ersteren, was fast keine Reaktion ist. Es zeigt sich, dass der Sensor eine bessere Selektivität gegenüber H2 . aufweist S als CO, SO2 , und NH3 . Dabei kommt es auf unterschiedliche Gase an, die bei der Reaktion mit Sensormaterialien unterschiedliche Energien aufweisen. Die Reaktion von H2 S-Moleküle mit den CNTs/SnO2 /CuO-Material könnte schneller und reaktionsschneller sein. Die CNTs/SnO2 /CuO-Sensor zeigt am empfindlichsten auf H2 S im Vergleich zu anderen Gasen.
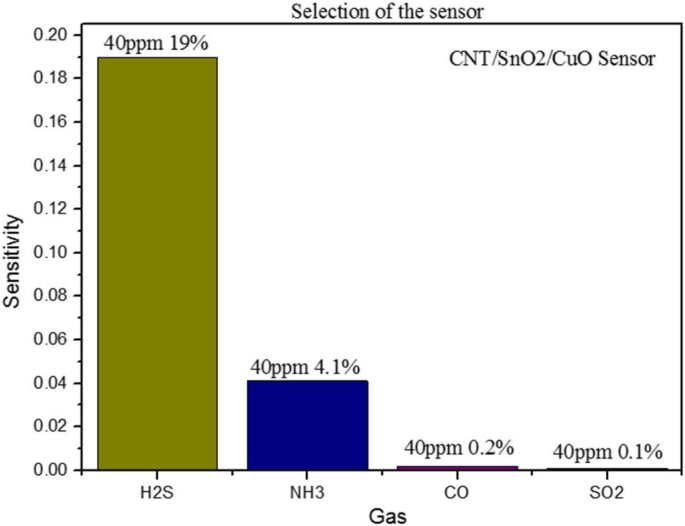
Selektivität des Sensors in 40 ppm für H2 S, NH4 , CO und SO2
Es wurde festgestellt, dass CNTs/SnO2 /CuO-basierter Sensor zeigt eine starke Abnahme des Widerstands von dünnen Filmen bei Einwirkung von H2 S-Gas. Es gibt zwei Hauptgründe, die den sensitiven und selektiven Nachweismechanismus von CNTs/SnO2 . erklären können /CuO-Nanokomposite. Zunächst die Kern-Schale-Struktur von CNTs/SnO2 Nanokomposite bieten eine größere Oberfläche, um die Gasmoleküle zu adsorbieren und zu diffundieren. Dann ist der Schlüssel zur Verbesserung der Leistung der Gassensorik die Bildung eines p-n-Heteroübergangs zwischen SnO2 und CuO. Das p-CuO/n-SnO2 Grenzfläche bildet eine Ladungsträgerverarmungsschicht, die einen hohen Widerstand von Sensormaterialien in Luft verursacht, wie in Fig. 9a gezeigt. Bei Exposition gegenüber H2 S-Gas, CuO wurde in CuS umgewandelt, was den p-n-Heteroübergang bricht. Daher wird die Verarmungsschicht, wie in Abb. 9b gezeigt, dünner und führt zu einem geringen Widerstand der Sensormaterialien.
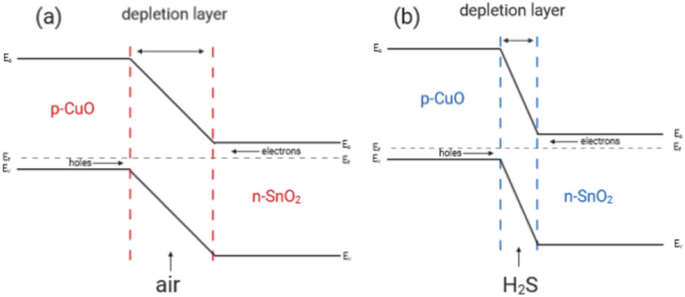
a , b Erfassungsmechanismen von SnO2 /CuO-Heteroübergang zum Nachweis von H2 S-Gas
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass die CNTs/SnO2 /CuO-Nanokomposit wurde auf einfache und kostengünstige Weise synthetisiert. Und der Sensor, der die CNTs/SnO2 . verwendet /CuO-Nanokomposit als aktives Material wurde entwickelt und unter Standardbedingungen bei Raumtemperatur getestet. Der Sensor hat eine schnelle Reaktion (4 min) und Erholung (10 min) bei Raumtemperatur. Und die CNTs/SnO2 /CuO-Gassensor konnte H2 . erkennen S-Konzentration so niedrig wie 10 ppm. Inzwischen sind die CNTs/SnO2 /CuO-Gassensor zeigt eine bessere Leistung als der von CNTs/SnO2 Sensor. Außerdem hat der Sensor eine gute Wiederholbarkeit und Stabilität in der Konzentration von 40 ppm H2 S und hat eine bessere Selektivität gegenüber H2 S als andere Gase. Daher sind die CNTs/SnO2 /CuO-Gassensor ist in vielen Situationen bei Raumtemperatur nützlich, z. B. in der Arbeitssicherheit.
Verfügbarkeit von Daten und Materialien
Alle Daten sind uneingeschränkt verfügbar.
Abkürzungen
- CNTs:
-
Kohlenstoff-Nanoröhrchen
- ZB:
-
Ethylenglykol
- FESEM:
-
Feldemissions-Rasterelektronenmikroskopie
- PEG:
-
Polyethylenglykol
- XRD:
-
Röntgendiffraktometer
Nanomaterialien
- Virtuelle Sensorfunktion und ihre Anwendungen
- Funktionsweise von Präsenzmeldern und ihre Anwendungen
- Türsensorfunktion und ihre Anwendungen
- Arbeiten und Anwendungen induktiver Sensoren
- IoT-Sensorfunktion und ihre Anwendungen
- Sensoren und Prozessoren konvergieren für industrielle Anwendungen
- Sensirion:Multigas-, Feuchtigkeits- und Temperaturmodul für Luftreiniger und HLK-Anwendungen
- Tragbarer Gassensor für Gesundheits- und Umweltüberwachung
- Ultradünne und hochempfindliche Dehnungssensoren
- Lab-On-Chip-Durchfluss- und Temperatursensor



