Eisen-Kohlenstoff-Gleichgewichtsdiagramm mit Erläuterung [Phasendiagramm]
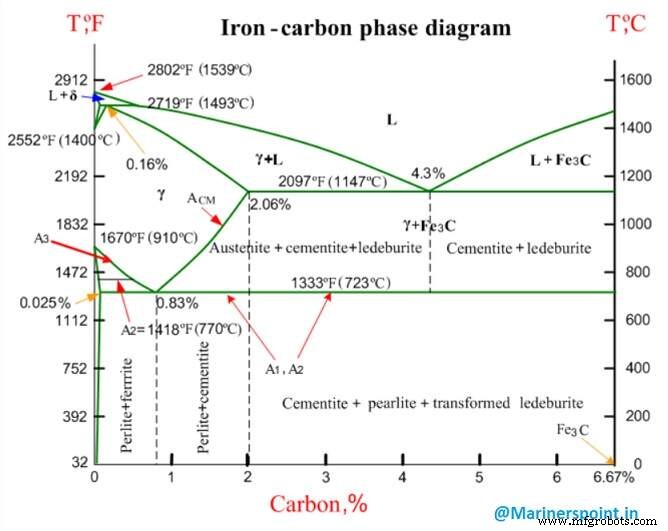
In diesem Artikel besprechen wir das Eisen-Kohlenstoff-Gleichgewichtsdiagramm , Verwendungen des Gleichgewichtsdiagramms, Arten des Eisen-Kohlenstoff-Gleichgewichtsdiagramms und verschiedene Phasen und Begriffe, die mit dem Eisen-Kohlenstoff-Phasendiagramm verbunden sind.
Was sind Phasendiagramme?
Phasendiagramme sind grafische Darstellungen der Phasen, die in einer Legierung unter verschiedenen Temperatur-, Druck- und chemischen Zusammensetzungsbedingungen vorhanden sind.
Die Erstarrung von Metalllegierungen wird anhand von Gleichgewichtsdiagrammen anschaulich. Dies sind grafische Darstellungen von Zustandsänderungen aufgrund von Temperatur- und Konzentrationsänderungen. Da dieses Diagramm die Art und Zusammensetzung von Legierungen sowie die Menge und Zusammensetzung der Phasen in einem bestimmten System angibt, wird es auch als Konstitutionsdiagramm oder Phasendiagramm bezeichnet
Eigenschaften und Verwendung des Gleichgewichtsdiagramms
Gleichgewicht bedeutet, dass Änderungen, die in einem System als Ergebnis eines Prozesses auftreten, der in eine Richtung abläuft, vollständig durch Änderungen aufgrund der Umkehrung des Prozesses im System kompensiert werden. Es wird also als dynamischer Zustand des Gleichgewichts zwischen atomaren Bewegungen betrachtet, bei dem die Resultierende Null ist.
Die Geschwindigkeiten der Temperatur- oder Zusammensetzungsänderungen waren während der experimentellen Arbeit extrem langsam, so dass die Legierung „zur Ruhe kam“, bevor eine Variable wie die Temperatur erneut geändert wurde. Der Zustand ist daher eher Ruhe als Veränderung.
Das Gleichgewichtsdiagramm zeigt Folgendes:
1. Temperatur, bei der die feste Legierung zu schmelzen beginnt und endet.
2. Mögliche Phasenänderungen, die als Ergebnis einer Änderung der Zusammensetzung oder Temperatur auftreten.
Welches Gleichgewichtsdiagramm stellt dar?
Das Diagramm beschreibt die geeigneten Bedingungen, damit zwei oder mehr Phasen im Gleichgewicht existieren. Beispielsweise beschreibt das Wasserphasendiagramm einen Punkt (Tripelpunkt), an dem Wasser gleichzeitig in drei verschiedenen Phasen koexistieren kann. Dies geschieht knapp über der Gefriertemperatur (0,01 °C) und 0,006 atm.
Verwendungen des Gleichgewichtsdiagramms in der Metallurgie
- Entwicklung der neuen Legierungen auf Basis von Anwendungsanforderungen.
- Herstellung dieser Legierungen.
- Entwicklung und Implementierung geeigneter Wärmebehandlungsverfahren zur Verbesserung der chemischen, physikalischen und mechanischen Eigenschaften dieser neuen Legierungen.
- Fehlerbehebung bei Problemen, die bei der Verwendung dieser neuen Legierungen auftreten, wodurch letztendlich die Produktvorhersagbarkeit verbessert wird.
Eisen-Kohlenstoff-Gleichgewichtsdiagramm
Das Eisen-Kohlenstoff-Gleichgewichtsdiagramm (auch Eisen-Kohlenstoff-Zustandsdiagramm genannt) ist eine grafische Darstellung der jeweiligen Gefügezustände der Legierung Eisen – Kohlenstoff (Fe-C) in Abhängigkeit von Temperatur und Kohlenstoffgehalt.
Das Eisen-Kohlenstoff-Phasendiagramm wird üblicherweise verwendet, um die verschiedenen Phasen von Stahl und Gusseisen vollständig zu verstehen. Stahl und Gusseisen sind sowohl Eisen- als auch Kohlenstofflegierungen. Außerdem enthalten beide Legierungen Spurenelemente in geringen Mengen.
Das Diagramm ist ziemlich komplex, aber da wir unsere Untersuchung auf Fe3C beschränken, werden wir nur bis zu 6,67 Gewichtsprozent Kohlenstoff betrachten.
Diagramm der Arten des Eisen-Kohlenstoff-Gleichgewichts
Das binäre Eisen-Kohlenstoff-Gleichgewichtsdiagramm ist die Grundlage von Stahl und Gusseisen. Es betrifft Umwandlungen, die in Legierungen mit Zusammensetzungen von reinem Eisen bis Zementit (6,67 Prozent Kohlenstoff) auftreten. Es gibt zwei Versionen des Eisen-Kohlenstoff-Gleichgewichtsdiagramms:
1. Eisen-Zementit-System. 2. Eisen-Graphit-System.
Diese beiden Systeme hängen von der Kühlgeschwindigkeit ab. Schnelles Abkühlen erzeugt Zementit und das System ist als Eisen-Zementit-System bekannt . In diesem System erreichen die in den erstarrten Phasen gebildeten Strukturen kein ausreichend vollständiges Gleichgewicht. Das Eisen-Zementit-System ist also ein metastabiles System eins.
Beim langsamen Abkühlen entsteht Graphit und das System ist bekannt als Eisen-Graphit-System . Die in der erstarrten Phase gebildeten Strukturen erreichen ein hinreichend vollständiges Gleichgewicht. Das ist also ein Stall eines.
Arten von Eisenlegierungen im Eisen-Kohlenstoff-Gleichgewichtsdiagramm
Die Gewichtsprozentskala auf der X-Achse des Eisen-Kohlenstoff-Phasendiagramms reicht von 0 % auf 6,67 % Kohlenstoff. Das Metall wird einfach als Eisen oder reines Eisen bis zu einem maximalen Kohlenstoffgehalt von 0,008 bezeichnet Gewichtsprozent Kohlenstoff. Bei Raumtemperatur liegt es im Ferrit vor Zustand.
Stahl ist eine Eisen-Kohlenstoff-Legierung mit einem Kohlenstoffgehalt von 0,008 bis 2,14 Prozent. Stahlsorten innerhalb dieses Bereichs sind als kohlenstoffarmer Stahl bekannt (oder Weichstahl), Stahl mit mittlerem Kohlenstoffgehalt und Stahl mit hohem Kohlenstoffgehalt .
Wenn der Kohlenstoffgehalt 2,14 überschreitet Prozent erreichen wir das Gusseisen Bühne. Gusseisen ist extrem hart, aber seine Sprödigkeit schränkt seine Anwendungen und Formgebungsverfahren stark ein.
EISEN-ZEMENTIT-SYSTEM
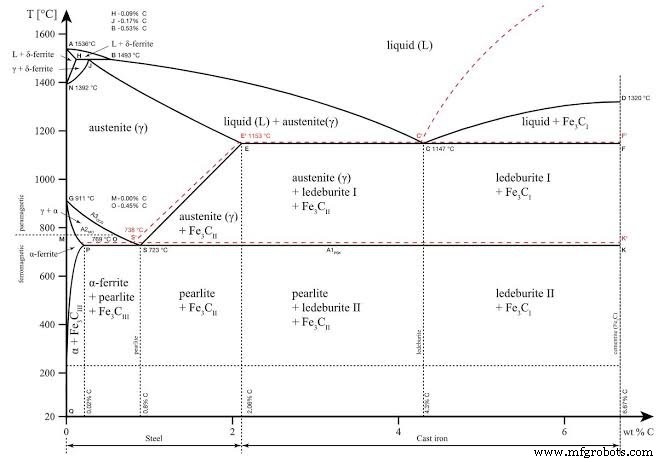
Wenn für Stähle mit unterschiedlichen Kohlenstoffgehalten eine Reihe von Zeit-Temperatur-Erwärmungskurven erstellt und die entsprechenden kritischen Punkte aufgetragen würden, würde man ein Diagramm ähnlich Abb. 2.14 erhalten. Dieses Diagramm, das nur unter langsamen Abkühlungsbedingungen gilt, ist als partielles Eisen-Kohlenstoff-Phasendiagramm bekannt . Anhand dieses Diagramms kann man leicht die richtigen Abschrecktemperaturen für jeden Kohlenstoffstahl erkennen. Die kritischen Punkte in Abb. 2.14 auf der Linie PSK sind mit A1, die auf der Linie GS mit A3 und die der Linie SE mit Acm bezeichnet. P>
Eisen-Kohlenstoff-Gleichgewichtsdiagramm mit Erläuterung
Austenit
Austenit , feste Lösung von Kohlenstoff und anderen Bestandteilen in einer bestimmten Form von Eisen, die als γ-(Gamma-)Eisen bekannt ist. Nehmen wir als Beispiel ein Stück 0,20-prozentigen Kohlenstoffstahl, das auf eine Temperatur von etwa 850 °C erhitzt wurde. Oberhalb von Ar3, Punkt (GS-Linie) ist dieser Stahl eine feste Lösung (interstitielle Art) von Kohlenstoff in Gamma-Eisen und wird Austenit genannt . Es hat ein kubisch flächenzentriertes Gitter und ist nichtmagnetisch.
Reiner Austenit kann bei einer Temperatur von 1130 °C bis zu etwa 2 % Kohlenstoff enthalten. Beim Abkühlen dieses Stahls beginnen die Eisenatome unterhalb des Punktes Ar3 (GS-Linie) ein kubisch-raumzentriertes Gitter zu bilden. Diese neue Struktur, die sich bildet, wird Ferrit oder Alpha-Eisen genannt und ist eine feste Lösung von Kohlenstoff in Alpha-Eisen, die bei Raumtemperatur bis zu 0,008 Prozent Kohlenstoff enthält.
Beim Abkühlen des Stahls auf Ar1 (PSK-Linie) wird zusätzlicher Ferrit gebildet. An der Arı-Linie wird der verbleibende Austenit in eine neue Struktur namens Perlit umgewandelt . Der Name Perlit ist auf seinen perlmuttartigen Glanz zurückzuführen. Es besteht aus abwechselnden Ferrit- und Zementitplatten und enthält etwa 87 Prozent Ferrit. Perlit kann entweder eine feine bis grobe lamellare oder körnige Struktur haben. Dies ist eine starke Substanz und kann mit Schneidwerkzeugen ziemlich gut geschnitten werden, d. h. der Perlitbestandteil in Stahl ist maschinell bearbeitbar.
Eutektoider Stahl
Wenn der Kohlenstoffgehalt des Stahls über 0,20 % ansteigt, sinkt die Temperatur, bei der der Ferrit zuerst vom Austenit abgestoßen wird, bis bei etwa 0,80 % Kohlenstoff (Punkt S) kein freier Ferrit vom Austenit abgestoßen wird. Dieser Stahl wird eutektoider Stahl genannt und ist 100 % Perlit .
Eutektoid Punkt
Was ist der eutektoide Punkt?
Der eutektoide Punkt in jedem Metall ist, wie bereits gesagt, die niedrigste Temperatur, bei der Änderungen in einer festen Lösung auftreten.
Wenn der Kohlenstoffgehalt des Stahls größer als Eutektoid (0,8 Prozent Kohlenstoff) ist, wird eine neue Linie im Eisen-Kohlenstoff-Phasendiagramm beobachtet, die mit Acm (S-Linie) bezeichnet ist. Die Linie bezeichnet die Temperatur, bei der anstelle von Ferrit erstmals Eisencarbid aus dem Austenit ausgeschieden wird.
Das Eisenkarbid (Fe3C) ist als Zementit bekannt . Es ist extrem hart, spröde und erscheint als parallele Platten (Lamellenschichten), als abgerundete Partikel (Sphäroide) oder als Hüllen um die Perlitkörner. Am Punkt C ist das eutektische Gemisch mit 4,3 Prozent Kohlenstoff als Ledeburit bekannt . Dies wird bei langsam abgekühlten Legierungen selten beobachtet, da es aufgrund seiner instabilen Natur während des Abkühlens nach dem Erstarren in andere Phasen zerfällt.
untereutektoid und übereutektoid
Stähle mit weniger als 0,80 Prozent Kohlenstoff werden als untereutektoid bezeichnet und solche, die mehr als 0,8 Prozent Kohlenstoff enthalten, werden als hypereutektoid bezeichnet Stähle. Diese Terminologie gilt nur für unlegierte und niedrig legierte Stähle. Bei hochlegierten Stählen ist die eutektoide Zusammensetzung verändert und das Gefüge ist möglicherweise gar nicht vorhanden.
Zunächst sei darauf hingewiesen, dass das normale Gleichgewichtsdiagramm eigentlich das metastabile Gleichgewicht zwischen Eisen und Eisenkarbid (Zementit) darstellt. Zementit ist metastabil, und das wahre Gleichgewicht sollte zwischen Eisen und Graphit liegen.
Obwohl Graphit reichlich in Gusseisen vorkommt (2-4 Gew.-% C), ist es normalerweise schwierig, diese Gleichgewichtsphase in Stählen (0,03-1,5 Gew.-% C) zu erhalten. Daher sollte das metastabile Gleichgewicht zwischen Eisen und Eisencarbid berücksichtigt werden, da es für das Verhalten der meisten Stähle in der Praxis relevant ist.
Eisen-Graphit-System
EISEN-GRAPHIT-SYSTEM
Es wurde bereits gesagt, dass Eisencarbid oder Zementit metastabil ist, obwohl es unter normalen Bedingungen dazu neigt, unbegrenzt zu bestehen. Wenn sich Zementit zersetzt, geschieht dies gemäß der Reaktion:
Fe3C <——–> 3Fe + C
In der stabilen Phase freier Kohlenstoff oder Graphit tritt anstelle der als Zementit bekannten Phase auf . Bei geringer Unterkühlung entsteht Graphit, wenn Gusseisen aus dem flüssigen Zustand erstarrt. Langsames Abkühlen fördert die Graphitierung . Schnelles Abkühlen unterdrückt teilweise oder vollständig die Graphitisierung und führt zur Bildung von Zementit.
Ein Eisen-Graphit-System (als gestrichelte Linie) ist in Abb. 2.14 dargestellt. Als Beispiel dient der Fall einer Kohlenstofflegierung mit 3,5 Gewichtsprozent Kohlenstoff
Am Punkt 1 befindet sich die Legierung im flüssigen Zustand. An Punkt 2 der Kühlleitung kann die auftretende Reaktion ausgedrückt werden als:
Bild
> Zwischen den Punkten 2 und 3 wird der überschüssige Kohlenstoff im Austenit als freier Graphit und nicht als Zementit ausgeschieden. An Punkt 3 findet die eutektoide Reaktion statt. Dies wird ausgedrückt als:
Bild
Der Mechanismus der eutektoiden Umwandlung muss eine einzelne feste Phase in zwei andere umwandeln, die beide eine vom Original abweichende Zusammensetzung haben.
Am Beispiel der eutektoiden Zersetzung von Eisen wandelt sich Austenit mit 0,8 % C in Ferrit (Eisen mit fast keinem Kohlenstoff) und Zementit (Fe3C mit 25 Atom-% Kohlenstoff). Daher müssen Kohlenstoffatome zusammendiffundieren, um Fe3C zu bilden, wobei Ferrit zurückbleibt. An den Korngrenzen des Austenits bilden sich Kerne kleiner Plättchen aus Ferrit und Zementit, und die Kohlenstoffdiffusion findet auf einer sehr lokalen Skala kurz vor der Grenzfläche statt (Schema unten).
So wachsen die Platten und verbrauchen dabei den Austenit, um Perlit zu bilden. Der Prozess der Graphitisierung wird durch Variieren der Abkühlgeschwindigkeit und durch geeignetes Legieren der metallischen Matrix gesteuert.
Im Eisen-Kohlenstoff-Gleichgewichtsdiagramm verwendete Begriffe
Eutectic Point
Der eutektoide Punkt in jedem Metall ist die niedrigste Temperatur, bei der Änderungen in festen Lösungen auftreten.
An diesen Stellen treten eutektische Reaktionen auf, bei denen eine flüssige Phase zu einem Gemisch aus zwei festen Phasen gefriert. Dies tritt auf, wenn eine flüssige Legierung eutektischer Zusammensetzung vollständig auf ihre eutektische Temperatur abgekühlt wird.
Eutektische Legierungen sind die Legierungen, die sich an dieser Stelle bilden. Legierungen auf der linken und rechten Seite dieses Punktes sind als untereutektische Legierungen und übereutektische Legierungen bekannt („hypo“ bedeutet im Griechischen weniger als, „hyper“ bedeutet größer als).
Austenit
Austenit, feste Lösung aus Kohlenstoff und anderen Bestandteilen in einer bestimmten Form von Eisen, bekannt als γ-(Gamma-)Eisen.
Diese Phase ist eine feste Lösung von Kohlenstoff in FCC Fe mit einer maximalen Löslichkeit von 2,14 % C. Bei weiterer Erwärmung wandelt sie sich bei 1395 °C in BCC-Ferrit um. γ-Austenit ist bei Temperaturen unterhalb der eutektischen Temperatur (727 °C) instabil, wenn es nicht schnell abgekühlt wird.
Alpha-Eisen oder Ferrit
α-Ferrit existiert bei niedrigen Temperaturen und niedrigem Kohlenstoffgehalt und ist eine feste Lösung von Kohlenstoff in BCC Fe. Diese Phase ist bei Raumtemperatur stabil. In der Grafik ist es als Splitter am linken Rand mit der Y-Achse auf der linken Seite und A2 auf der rechten Seite zu sehen. Diese Phase ist unterhalb von 768°C magnetisch.
Es hat einen maximalen Kohlenstoffgehalt von 0,022 % und wandelt sich bei 912 °C in γ-Austenit um, wie in der Grafik gezeigt.
Zementit
Zementit, eine metastabile Phase dieser Legierung mit einer festen Zusammensetzung von Fe3C, ist eine metastabile Phase dieser Legierung. Bei Raumtemperatur zersetzt es sich äußerst langsam in Eisen und Kohlenstoff (Graphit).
Diese Zersetzungszeit ist lang und dauert viel länger als die Lebensdauer der Anwendung bei Raumtemperatur. Andere Faktoren wie hohe Temperaturen und die Zugabe bestimmter Legierungselemente können diese Zersetzung beeinflussen, indem sie die Graphitbildung fördern.
Zementit ist hart und spröde und daher ideal für die Stahlbewehrung. Seine mechanischen Eigenschaften werden durch seine Mikrostruktur bestimmt, die durch die Mischung mit Ferrit bestimmt wird.
Wir haben versucht, alle Begriffe im Zusammenhang mit dem Eisen-Kohlenstoff-Phasendiagramm einschließlich der verschiedenen darin verwendeten Phasen und Begriffe abzudecken, um sie besser zu verstehen. Ich hoffe, Ihnen hat dieser Artikel über das Eisen-Kohlenstoff-Gleichgewichtsdiagramm gefallen . Bitte geben Sie Ihr Feedback im Kommentar unten ab.
Industrietechnik
- Schaltung mit Schalter
- 3D-Druck mit hochfestem Material – Kohlefaser-Nylon-Verbundstoff
- Bentley bringt Bentayga mit den weltgrößten Carbonlaufrädern auf den Markt
- Renndrohne mit vollständig geschlossenem Kohlefaser-Monocoque
- Elektroerosionsbearbeitung (EDM):Mechanik, Arbeitsprinzipien und Schaltungen (mit Diagramm)
- Eisenerzeugung durch Hochöfen und Kohlendioxidemissionen
- Was sind die Teile einer Schweißnaht? - Erklären Sie mit Diagramm
- Was ist das Eisen-Kohlenstoff-Phasendiagramm?
- 11 verschiedene Schweißverfahren anhand von Diagrammen
- Verschiedene Arten von Blechoperationen mit Diagramm



