Kalkstein – seine Verarbeitung und Anwendung in der Eisen- und Stahlindustrie
Kalkstein – seine Verarbeitung und Anwendung in der Eisen- und Stahlindustrie
Kalkstein ist ein natürlich vorkommendes und reichlich vorhandenes Sedimentgestein, das aus einem hohen Gehalt an Calciumcarbonat (CaCO3) in Form des Minerals Calcit besteht. Einige Kalksteine können einen geringen Prozentsatz an Magnesiumcarbonat (MgCO3) enthalten. Diese Kalksteine sind als dolomitische Kalksteine bekannt.
Kalkstein ist auch ein sehr wichtiges Industriemineral. Seine chemischen Eigenschaften machen es zu einem wertvollen Mineral für eine Vielzahl von Anwendungen in Industrie und Fertigung. Kalkstein ist auch einer der wichtigsten Rohstoffe für die Herstellung von Eisen und Stahl.
Kalkstein ist per Definition ein Gestein, das mindestens 50 Gew.-% CaCO3 in Form von Calcit enthält. Es können kleine Partikel von Quarz (Kieselerde), Feldspat (Alumosilikate), Tonmineralien, Pyrit (Eisensulfid), Siderit (Eisenkarbonat) und andere mit dem Kalkstein verbundene Mineralien vorhanden sein. Alle Kalksteine enthalten mindestens ein paar Prozent andere Materialien. Die Verunreinigungen in Kalkstein können aus Siliziumoxid (SiO2), Aluminiumoxid (Al2O3), Eisenoxid (Fe2O3), Schwefel (als Sulfide oder Sulfate), Phosphor (P2O5), Pottasche (K2O) und Soda (Na2O) bestehen. Kieselsäure und Tonerde sind die Hauptverunreinigungen von Kalkstein. Der Kalkstein, der zur Eisenherstellung verwendet wird, muss mindestens 85 % Calciumcarbonat und einen geringen Prozentsatz an Tonerde enthalten. In ähnlicher Weise muss Kalkstein, der für die Stahlherstellung verwendet wird, mindestens 92 % Calciumcarbonat und einen sehr geringen Prozentsatz an Verunreinigungen, insbesondere den Kieselerdeanteil, enthalten.
Die Hauptverwendungen von Kalkstein in der Eisen- und Stahlindustrie sind (i) als Flussmittel und (ii) andere Verwendungen, die als Entschwefelungsmittel, Beschichtung von Formen von Schweinegussmaschinen, Neutralisierung von saurem Wasser, Wasserbehandlung, Abwasser ( Abwasserbehandlung, Rauchgasbehandlung und Schlamm- und Abwasserbehandlung. Es ist auch ein Bestandteil der synthetischen Schlacke. Kalkstein wird normalerweise in drei Formen verwendet. Dies sind (i) roher Kalkstein, der auch die natürliche Form von Kalkstein ist, (ii) gebrannter Kalkstein oder Branntkalk oder einfach Kalk und (iii) als Kalkhydrat. Wenn Kalkstein als Flussmittel verwendet wird, dann wird er entweder als Rohkalkstein oder als kalzinierter Kalkstein verwendet. Hydratkalk wird im Allgemeinen aus gebranntem Kalk mit hohem Calciumgehalt hergestellt und enthält 72 % bis 74 % Calciumoxid mit 23 % bis 24 % chemisch gebundenem Wasser.
Verarbeitung von Kalkstein
Kalkstein muss nach seinem Abbau mehreren Verarbeitungen unterzogen werden, bevor er in verschiedenen Prozessen verwendet werden kann. Die grundlegenden Prozesse bei der Herstellung von Kalkstein sind (i) Abbau von Rohkalkstein, (ii) Aufbereitung von abgebautem Kalkstein für seine Verwendung durch Brechen und Klassieren, (iii) Kalzinieren von Rohkalkstein, (iv) Weiterverarbeitung des kalzinierten Kalksteins durch Hydratisierung zu Herstellung von Kalkhydrat, falls für die Verwendung erforderlich, und (v) verschiedene Transfer-, Lagerungs- und Handhabungsvorgänge. All diese Prozesse müssen möglicherweise nicht in jeder Anlage vorhanden sein.
Grundsätzlich werden in Eisen- und Stahlwerken drei Arten von Kalksteinprodukten verwendet. Sie sind (i) rohe Kalksteinprodukte, (ii) kalzinierte Kalkstein- oder Branntkalkprodukte und (iii) Kalkhydratprodukte. Die Verarbeitung von Kalkstein für diese Produkte ist unten beschrieben.
Der erste Prozess findet in Kalksteinminen statt, wo das abgebaute Erz zerkleinert und gesiebt wird, um die verschiedenen Größenfraktionen des Erzes zu trennen. Im Hüttenwerk wird stellenweise Rohkalk weiterverarbeitet. Beispiel Sinteranlage, wo der Rohkalkstein in Hammermühlen auf – 3 mm Größe zerkleinert wird (im Allgemeinen im Bereich von 85 % bis 90 %).
Das Kalzinieren von Kalkstein ist ein thermisches Behandlungsverfahren zur Durchführung der thermischen Zersetzung des rohen Kalksteins und zur Entfernung von LOI (Glühverlust) oder Kohlendioxid (CO2), einem Teil seiner Zusammensetzung. Der Kalzinierungsprozess besteht aus einer endothermen Reaktion, die im festen Zustand durchgeführt wird. Hochwertiger Kalk, der in der Stahlerzeugung verwendet wird, enthält im Allgemeinen etwa 90 % bis 95 % CaO. Aus 100 kg CaCO3 entstehen bei der vollständigen Kalzinierung theoretisch 56 kg CaO. In der Praxis variiert dies jedoch aufgrund mehrerer Faktoren. Da während der Kalzinierung von Kalkstein CO2 entfernt wird, ist der Kalk (i) porös, (ii) hat eine größere Oberfläche, (iii) hat eine hohe Reaktivität und (iv) ist hygroskopisch. Zur Herstellung von 1 t Branntkalk werden etwa 1,8 t Kalkstein benötigt.
Das Brennen von Kalkstein erfordert, da es sich um eine endotherme chemische Reaktion handelt, einen erheblichen Energieaufwand. Beim Erhitzen von Kalkstein wird das Calciumcarbonat gemäß der folgenden Gleichung zersetzt.
CaCO3 + ca. 42,5 kcal Wärme =CaO + CO2
Die Kalzinierung von Kalkstein ist ein einfacher einstufiger Brennprozess, der in einem Schachtofen oder Drehrohrofen durchgeführt wird. Es besteht aus fünf Prozessschritten. Diese sind (i) Wärmeübertragung von der Umgebung zur Partikeloberfläche, (ii) Wärmeleitung von der Oberfläche zur Reaktionsfront, (iii) chemische Kinetik an der Front, (iv) Diffusion des CO2 durch die poröse Oxidschicht zur Oberfläche und (v ) und dann in die Umgebung übertragen. Der Kalkstein wird in den Ofen geladen und während er durch den Ofen läuft, zersetzt oder kalziniert. Die Zersetzung von CaCO3 beginnt bei 810 Grad C.
Der Kalzinierungsprozess kann anhand eines teilweise zersetzten Stücks Kalkstein erklärt werden, dessen Profile des CO2-Partialdrucks und der Temperatur in Abb. 1 dargestellt sind. Die Probe besteht aus einem dichten Karbonatkern, der von einer porösen Schicht umgeben ist. Im Kalzinierofen wird bei einer Temperatur von Tgas Wärme durch Strahlung und Konvektion (symbolisiert durch „h“) auf die feste Oberfläche bei einer Temperatur von TOberfläche übertragen. Mittels Wärmeleitung (A) dringt Wärme durch die Oxidschicht, um die Reaktionsfront zu erreichen, wo die Temperatur Trc ist. Da die Reaktionsenthalpie um ein Vielfaches größer ist als die innere Energie, ist die weiter in den Kern strömende Wärme während der Reaktion vernachlässigbar. Daher ist die Kerntemperatur nur geringfügig niedriger als die Fronttemperatur. Nach Wärmezufuhr findet dann die chemische Reaktionskonstante (k) statt, deren treibende Kraft die Abweichung des CO2-Partialdrucks vom Gleichgewicht (p-eq – p-f) ist. Das freigesetzte CO2 diffundiert (Dp) durch die poröse Oxidschicht an die Oberfläche und gelangt schließlich durch Konvektion (B) in die Umgebung, wo der CO2-Partialdruck p-Oberfläche herrscht. Die chemischen und physikalischen Eigenschaften von Kalk werden durch die Kalzinierung beeinflusst, die wiederum von der Leitfähigkeit, dem Stoffübergangskoeffizienten und der Diffusionsfähigkeit der Kalkschicht beeinflusst wird.
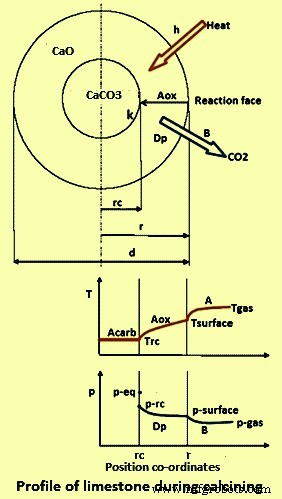
Abb. 1 Profil einer Kalksteinprobe während des Kalzinierens
Für die vollständige Kalzinierung von Kalkstein und um keinen Restkern aus unkalziniertem Kalkstein zu haben, ist es notwendig, dass die der Oberfläche des Kalksteins zugeführte Wärme über Wärmeleitung zum Kern vordringen muss. Im Kern muss zumindest kurzzeitig eine Temperatur von 900 Grad C erreicht werden, da die Atmosphäre im Inneren des Materials aus reinem CO2 besteht. Die Kalksteinoberfläche muss auf mehr als 900 Grad C erhitzt werden, um den erforderlichen Temperaturgradienten aufrechtzuerhalten und die isolierende Wirkung des kalzinierten Materials in der Kalksteinoberfläche zu überwinden. Bei der Herstellung von Branntkalk darf die Oberflächentemperatur jedoch 1.100 °C bis 1.150 °C nicht überschreiten, da es sonst zu einer Rekristallisation des CaO kommt, die zu einer geringeren Reaktivität führt und somit die Löscheigenschaften des Branntkalks verringert.
Um die Wärme aus den Verbrennungsgasen auf die Oberfläche des Kalksteins und dann von der Oberfläche auf den Kern des Kalksteins zu übertragen, ist eine gewisse Retentions- oder Verweilzeit erforderlich. Größere Kalksteinstücke benötigen eine längere Zeit zum Kalzinieren als kleinere Stücke. Prinzipiell verringert das Kalzinieren bei höheren Temperaturen die benötigte Verweilzeit. Zu hohe Temperaturen beeinträchtigen jedoch die Reaktivität des Produkts. Die Beziehung zwischen Kalzinierungstemperatur und Verweilzeit, die für verschiedene Kalksteingrößen benötigt wird, ist in Tab. 1 dargestellt.
| Tab 1 Zusammenhang zwischen Kalzinierungstemperatur und Verweilzeit | |||
| Sl. Nr. | Kalksteingröße | Kalzinierungstemperatur | Residenzzeit (ungefähr) |
| Einheit | mm | Grad C | Stunden |
| 1 | 50 | 1000 | 2.1 |
| 1200 | 0,7 | ||
| 2 | 100 | 1000 | 8.3 |
| 1200 | 2.9 | ||
Für den Kalzinierungsprozess werden mehrere verschiedene Ofentypen verwendet. Diese Öfen können Drehöfen oder Schachtöfen sein. Der auszuwählende Ofentyp hängt stark von den Eigenschaften des Kalksteins, der erwarteten Produktionsrate, den Brennstoffkosten, den Investitionskosten, dem verfügbaren Brennstoff, den örtlichen Bedingungen, der Infrastruktur und anderen Dingen ab. Generell sind vor der Auswahl des Kalzinierofens alle Daten inkl. Laboruntersuchungen auszuwerten.
Drehrohröfen, mit oder ohne Vorwärmer, verarbeiten in der Regel Kalkstein mit einer Materialgröße zwischen 10 mm und 50 mm. Die Wärmebilanz dieses Ofentyps ist etwas kategorisiert durch die hohen Verluste mit den Abgasen und durch den Ofenmantel. Typische Werte für die Abgasverluste liegen im Bereich um 25 % und für die Ofenmantelverluste im Bereich um 20 % des Gesamtwärmebedarfs. Nur etwa 60 % der in den Ofen mit Vorwärmer eingebrachten Brennstoffenergie wird für den Kalzinierungsprozess genutzt.
Bei vertikalen Einschachtöfen besteht ein Ungleichgewicht zwischen der Wärme, die aus der Kalzinierzone verfügbar ist, und der Wärme, die in der Vorwärmzone benötigt wird. Selbst bei dem idealen Kalzinierungsprozess kann die Temperatur der Abgase höher als 100 Grad C sein. Im Fall von Regenerativstromöfen (PFR) mit Gleichstrom wird die Wärme der Kalzinierungszone besser genutzt und der Verlust minimiert Wärme in den Abgasen, was zu einem geringeren Wärmeverbrauch pro Tonne Kalk führt.
Schematische Darstellung eines vertikalen Einschachtofens, die den Material- und Gasfluss, die Hauptkomponenten eines Kalkdrehofens und den Mechanismus der Wärmeübertragung in einem Drehrohrofen zeigt, sind in Abb. 2 dargestellt.
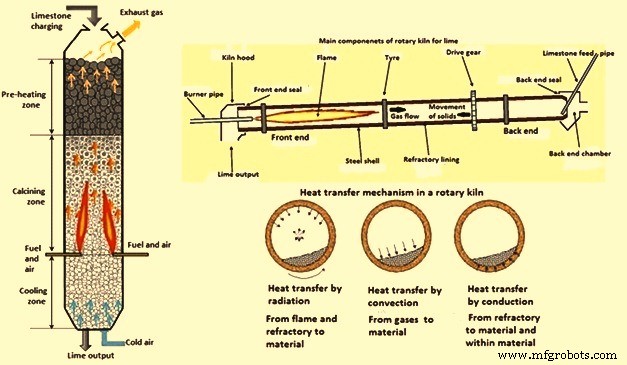
Abb. 2 Schematische Darstellung eines vertikalen Einschachtofens, Komponenten des Drehrohrofens und Wärmeübertragungsmechanismus in einem Drehrohrofen
Ein Vergleich der Daten für verschiedene Öfen, die typischerweise für die Kalksteinkalzinierung verwendet werden, mit wichtigen Verbrauchszahlen und typischer Rohmaterialgröße ist in Tab. 2 angegeben.
| Tab 2 Vergleich verschiedener Kalzinierofentypen | |||||
| Typ des Brennofens | Ofenkapazität | Kalksteingröße | Spezifischer Kraftstoffverbrauch | Spezifischer Stromverbrauch | Bemerkungen |
| tpd | mm | kcal/kg | kWh/Tonne | ||
| Rechteckiger GGR-Ofen | 100–400 | 30-120 | 810-870 | Ungefähr 20 | Es entsteht hochreaktiver Kalk |
| GGR-Rundofen | 300–800 | 30-160 | 810-870 | Ungefähr 20 | Es entsteht hochreaktiver Kalk |
| Feinkalkofen | 200–400 | 15-40 | 790-850 | Ungefähr 20 | Es entsteht hochreaktiver Kalk |
| Ringschachtofen | 200–600 | 15–200 | 910-980 | Ungefähr 30 | Hoher CO2-Gehalt im Abgas |
| Einschachtofen | 50–300 | 10-100 | 980–1100 | Ungefähr 35 | Es entsteht mittelharter Branntkalk |
| Drehrohrofen mit Vorwärmer | 300–1200 | 10-50 | 1150-1350 | Ungefähr 30 | Hoch reaktiver Kalk wird produziert, hohe Produktionsrate und wenig Schwefel |
| Lange Drehrohröfen ohne Vorwärmer | 300–1000 | 20-50 | 1600-1700 | Ungefähr 20 | Hohe Produktionsraten, reaktiver Kalk und wenig Schwefel |
| Suspensionskalzinierung | 300–1200 | 0,03-2 | 1300-1400 | Sehr feines Rohmaterial | |
Im Folgenden sind die Faktoren und Betriebsparameter aufgeführt, die einen Einfluss auf die Kalzinierung von Kalkstein haben.
Arten von Öfen – Es gibt zwei Arten von Öfen, die zum Kalzinieren von Kalkstein verwendet werden. Sie sind entweder vertikale Schachtöfen oder horizontale Drehrohröfen. Je nach Ofentyp ist die Größe der Kalksteinfüllung unterschiedlich. In vertikalen Öfen bewegt sich der Kalkstein nach unten und die heißen Gase strömen durch den Kalkstein nach oben, daher müssen die Steine groß genug sein, um einen Durchgang für die Verbrennungsgase nach oben zu ermöglichen. Diese Öfen verwenden normalerweise Kalksteingrößen im Bereich von 130 mm bis 200 mm. Bei diesen Ofentypen muss der Temperaturanstieg langsam sein und daher ist die resultierende Verweilzeit lang. Vertikalöfen sind brennstoffeffizient, aber in ihrer Kapazität begrenzt. Bei horizontalen Öfen dreht sich der Ofenkörper, wodurch der Kalkstein taumeln kann und alle Oberflächen heißem Gas ausgesetzt werden. Die typische Kalksteingröße für diese Ofentypen liegt zwischen 25 mm und 40 mm. Die Gleichmäßigkeit der Kalksteingröße zum Beschicken des Ofens ist sehr wichtig für einen gleichmäßigen Kalzinierungsprozess. Aus praktischer Sicht ist eine enge Dimensionierung jedoch aufgrund der erforderlichen mehrfachen Siebung teuer. Kalkstein kleiner Größe wie 6 mm und kleiner mit einem bestimmten Feinanteil in einem horizontalen Ofen neigt dazu, in der Masse umzukippen, wodurch die Exposition von Partikeln gegenüber heißen Gasen verringert wird. Dieser Prozess führt zu einer ungleichmäßigen Belichtung, wodurch die Qualität des Branntkalks verringert wird. In Vertikalöfen blockiert das Vorhandensein von sehr kleinem Kalkstein die Hohlräume zwischen Kalkstein, was den Gasdurchgang und damit die Wärmeübertragung stört und eine ungleichmäßige Kalzinierung verursacht. Darüber hinaus neigen kleine Kalksteinpartikel (weniger als 3 mm) dazu, sich zu zersetzen und die Erzeugung von Feinanteilen zu verursachen, die von Staubabscheidern entfernt werden müssen.
Größe und Abstufung von Kalkstein - Während des Kalzinierungsprozesses schreitet die Dissoziation von Kalkstein normalerweise allmählich von der Oberfläche in das Innere des Kalksteins fort. Je größer der Kalkstein ist, desto schwieriger ist er zu kalzinieren und es erfordert auch mehr Zeit. Ein breiter Bereich der Partikelgrößenverteilung in der Ofenbeschickung stört auch die Wärmeverteilung im Ofen. Die kleinen Steine sammeln sich zwischen den von großen Steinen in Schachtöfen gebildeten Hohlräumen und blockieren so den Zug und den Fluss von Verbrennungsflammen und -gasen. Auch während des Kalzinierens eines großen Bereichs von Kalksteingrößen kalzinieren Temperaturen, die die kleineren Größen angemessen ohne übermäßiges Kalzinieren kalzinieren, nur die äußere Hülle des Kalksteins mit größeren Abmessungen. Daher sind Kalksteine mit eingeschränkter Abstufung, unabhängig von der Größe, viel einfacher zu kalzinieren. Die Größe des Kalksteins ist auch ein kritisches Element beim Kalzinierungsprozess. Wenn der Kalkstein in den Ofen eintritt, wird er den heißen Gasen innerhalb des Ofens ausgesetzt. Die Geschwindigkeit der Wärmedurchdringung ist abhängig von der Temperatur des Kalksteins und der umgebenden Gase. Außerdem braucht die Wärme Zeit, um in den Kalkstein einzudringen. Je kleiner der Kalkstein ist, desto kürzer ist die Zeit der Wärmedurchdringung. Bei Kalksteinmehl kann diese Zeit den Bruchteil einer Minute betragen.
Kristallstruktur und Dichte von Kalkstein – Die kristalline Struktur von Kalkstein beeinflusst die Kalzinierungsgeschwindigkeit, die innere Festigkeit von Kalkstein sowie die resultierende Kristallgröße von CaO im Kalk. Die kleineren Kristalle agglomerieren während des Kalzinierens und bilden größere Kristalle, wodurch eine Schrumpfung und Volumenreduktion verursacht wird. Höhere Ofentemperaturen unterstützen den Agglomerationsprozess. Je größer die Agglomeration ist, desto größer ist die Volumenschrumpfung des Endprodukts. Die Dichte von Kalkstein und seine Kristallstruktur sind etwas verwandt. Die Form der Kristalle bestimmt den Hohlraum zwischen den Kristallen und damit die Dichte des Kalksteins. Größere Hohlräume ermöglichen einen leichten Durchtritt von CO 2 -Gasen während des Kalzinierens, führen aber auch zu einer Volumenverringerung während des Kalzinierens. Einige Kalksteinarten zerfallen aufgrund ihrer kristallinen Struktur beim Kalzinierungsprozess. Diese Kalksteinsorten sind nicht zum Kalzinieren geeignet. Es gibt einige andere Kalksteinarten, die sich umgekehrt verhalten und beim Brennen so dicht werden, dass sie das Entweichen von CO2 verhindern und porenfrei werden. Auch diese Kalksteinarten sind nicht zum Brennen geeignet.
Kalztemperatur – Die Kalzinierung von Kalkstein beginnt bei etwa 810 °C bei atmosphärischem Druck und in einer Atmosphäre, die zu 100 % aus CO2 besteht. Die Dissoziation schreitet fortschreitend von der äußeren Oberfläche zur inneren Oberfläche fort. Damit die Dissoziation in das Innere des Kalksteins eindringen kann, sind höhere Temperaturen notwendig. Die Temperaturen müssen weiter erhöht werden, damit eine Dissoziation des Kalksteinkerns stattfinden kann. Je größer der Kalkstein ist, desto höher ist die Temperatur, die für die Dissoziation des Kerns aufgrund des zunehmenden Innendrucks benötigt wird, wenn das CO2-Gas sein Entweichen erzwingt. Eine Temperaturerhöhung übt einen viel größeren Einfluss auf die Dissoziationsgeschwindigkeit aus als die Temperaturerhaltung. Außerdem beträgt die zum Kalzinieren erforderliche theoretische Temperatur etwa 1.000 °C. In der Praxis sind die im Ofen aufrechterhaltenen Temperaturen jedoch viel höher (etwa 1.350 °C). Die richtige Temperatur im Ofen hängt von der Kalksteingröße sowie vom Ofentyp und vom verwendeten Brennstoff ab. Der Ofenbediener experimentiert normalerweise, um die genaue Temperatur für die spezielle Größe und Qualität des verwendeten Kalksteins zu bestimmen. Im Allgemeinen ist es besser, die niedrigste Temperatur bei einer möglichst kurzen Verweilzeit zu verwenden, um eine vollständige Kalzinierung zu erreichen. Höhere Kalzinierungstemperaturen verursachen eine verstärkte Schrumpfung und Volumenverringerung. Höhere Kalzinierungstemperaturen verursachen auch eine Karbonisierung der Oberfläche von kalziniertem Kalkstein, wobei CO2 aus dem Stein sowie als Verbrennungsprodukt freigesetzt wird, wodurch der Kalk nicht porös und somit weniger reaktiv wird.
Temperaturanstiegsrate – Der Temperaturanstieg muss allmählich und gleichmäßig erfolgen. Dies ist besonders wichtig, wenn Kalkstein großer Größe (100 mm bis 150 mm) verwendet wird. Beim Kalzinieren von großformatigem Kalkstein muss der Kalkstein während des Prozesses porös bleiben. Wenn die Temperatur ansteigt, wird die äußere Kalksteinschicht auf Dissoziationstemperatur erhitzt, wobei CO2 aus dem Kalkstein entweicht und Kapillarkanäle hinterlässt, die den Kalk porös machen. Beim Entweichen des Gases schrumpft das Volumen des Kalksteins um bis zu 40 %. Diese Volumenschrumpfung schränkt den Gasdurchgang aus dem Zentrum des Kalksteins ein und verhindert, dass zusätzliches CO2-Gas entweicht. Eine zu lange Verweilzeit erleichtert die Vereinigung von CaO und CO2 zurück zu CaCO3 (Karbonisierung) bei Temperaturen über 1350°C. Wenn der Temperaturanstieg sehr schnell ist, wird die äußere Schicht der Kalksteinstücke sehr schnell kalziniert. Mit steigender Temperatur schrumpft die Oberfläche von Kalksteinstücken und die durch das Entweichen von CO2 entstandenen Poren schließen sich. Dadurch entsteht ein erhöhter Innendruck im Kalkstein. Da das Gas nicht entweichen kann, lässt es den Kalkstein explodieren und zerfallen. Dies führt zur Produktion unerwünschter Feinstoffe, die die Qualität des resultierenden Branntkalks verringern.
Zeit der Kalzinierung – Es wurde festgestellt, dass unabhängig von der Art des Kalksteins und seiner Qualität eine höhere Brenntemperatur und eine längere Brenndauer einen härter gebrannten Branntkalk ergeben, der eine hohe Schrumpfung, eine hohe Dichte, eine geringe Porosität und eine geringe chemische Reaktivität aufweist. Das Gegenteil findet bei niedrigeren Brenntemperaturen mit kürzerer Kalzinierungsdauer statt, was zur Herstellung der erwünschten, weichgebrannten, hochreaktiven Kalke mit geringer Schrumpfung und Dichte und hoher Porosität führt. Die Kalzinierung von kleinen und großen Steinen in Bezug auf ihre relative Erwärmungs- und Kalzinierungszeit ist direkt proportional zum Quadrat der Dicke (oder dem durchschnittlichen Durchmesser bei unregelmäßig geformten Steinen). Die Verweilzeit im Ofen hängt von der Größe des Kalksteins sowie der Kalzinierung ab Temperatur. Die Größe des Kalksteins ist das kritischste Element für die Kalzinierung. Wenn der Kalkstein in den Ofen eintritt, wird er den heißen Gasen innerhalb des Ofens ausgesetzt. Die Geschwindigkeit der Wärmedurchdringung basiert auf dem Temperaturunterschied zwischen dem Kalkstein und dem Temperatur der Gase. Zusätzlich zu diesem Temperaturunterschied braucht Wärme Zeit, um den Kalkstein zu durchdringen. Je kleiner die Größe des Kalksteins ist, desto kürzer ist die Zeit für die Wärmedurchdringung. Bei pulverisiertem Kalkstein kann sich diese Zeit verkürzen auf weniger als 1 Minute. Wenn die Verweilzeit zu kurz ist, bleibt der Kern des Kalksteins unkalziniert, während die äußere Oberfläche kalziniert wird. Wenn die Verweilzeit zu lang ist, wird die n Die Oberfläche der Kalksteinstücke schrumpft und die durch das Austreten von CO2-Gas entstandenen Poren schließen sich, wodurch eine undurchlässige Oberfläche entsteht. Diese Art von Kalk wird als hartgebrannter oder totgebrannter Kalk bezeichnet. Dieser Kalk hat eine sehr geringe Reaktivität und löscht nicht gut. Darüber hinaus bedeutet eine längere Aufbewahrungszeit weniger Produktion und höhere Produktionskosten.
CO2-Konzentration im Ofen – Die CO2-Konzentration in der Ofenatmosphäre steigt mit der Freisetzung aus Kalkstein während der Kalzinierung. Für eine ordnungsgemäße Kalzinierung muss das CO2 kontinuierlich entfernt werden. Wenn CO2 nicht entfernt wird, bewirkt eine Kombination aus hoher CO2-Konzentration und hoher Kalzinierungstemperatur eine Karbonisierung der kalzinierten Kalksteinstücke und wandelt CaO wieder in CaCO3 um. Außerdem reagiert das CO2 auch mit den Kalksteinverunreinigungen.
Chemische Reaktivität – Es besteht ein Zusammenhang zwischen Porosität, Dichte und Porengrößenverteilung. Diese Faktoren haben einen großen Einfluss auf solche standardmäßig messbaren Eigenschaften von Branntkalk wie Reaktivität, verfügbarer Kalk sowie die Korngrößenverteilung und die Oberfläche. Es wurde festgestellt, dass eine Verweilzeit von 1 Stunde bis 4 Stunden sehr wenig oder keine Wirkung auf die Porosität, Oberfläche oder Reaktivität im Kalzinierungstemperaturbereich von 950 °C bis 1070 °C hat und die Schüttdichte von Branntkalk konstant bleibt . Überhöhte Kalzinierungstemperaturen und längere Kalzinierungsperioden führen zu einem harten Brennen des Kalksteins und dies führt zur Produktion von Kalk mit geringer Reaktivität.
Schrumpfverhalten – Das Schwinden von Branntkalk kann aus den Dichten des Kalksteins und des Kalks unter Berücksichtigung des Glühverlusts (LOI) berechnet werden. Sie wird nach der Formel S =100*{[100/Ds-(100-L)/Dl]/100*Ds} berechnet, wobei S die prozentuale Schrumpfung, Ds die Dichte des Kalksteins in Gramm/cm³ und Dl die Dichte von Branntkalk in Gramm/cm³ und L ist der Glühverlust von Kalkstein in Prozent. Das Schwinden des Kalksteins hat großen Einfluss auf die Schüttdichte der Kalksteincharge im Ofen. Je höher die Schwindung ist, desto geringer sind die Hohlräume in der Kalksteinschüttung. Dies führt zu einer Verdichtung des Kalksteins im Ofen, was zu einem hohen Druckabfall im Ofenbett mit dem damit verbundenen Einfluss auf den Abzug von Rauchgasen aus dem Ofen führt.
Qualität und Art des Kraftstoffs – Die Qualität und Art des Brennstoffs hat großen Einfluss auf die Effizienz des Ofens und die Qualität des produzierten Kalks. Feste Rohbrennstoffe wie Holz, Holzkohle und Steinkohle werden schon sehr früh eingesetzt. In den Öfen werden Kohlenstaub, Produktionsgas, Erdgas und Heizöl eingesetzt. Erdgas ist der bequemste Brennstoff und Erzeugergas ist der problematischste. Die endgültige Wahl des Kraftstoffs wird auch von Umwelterwägungen bestimmt, da einige Kraftstoffe eine höhere Tendenz haben, die Umwelt durch schädliche Emissionen zu belasten. Typischerweise verwenden vertikale Öfen Öl oder Erdgas als Brennstoff, während horizontale Drehöfen Kohle verwenden. Beide Ofentypen können jedoch jeden dieser Brennstoffe verwenden. Sowohl Öl als auch Kohle enthalten bestimmte Prozentsätze an Schwefelverbindungen, die zwischen 0,5 % und 3 % liegen können. Schwefel verbindet sich normalerweise bei geeigneten Temperaturen mit CaO und erzeugt Calciumsulfid oder Calciumsulfat. Dies geschieht im Allgemeinen auf der Oberfläche von kalziniertem Material und macht das Material nicht porös, wodurch seine Reaktivität verringert wird. Außerdem führt ein hoher Anteil an Asche in der Kohle zu Ablagerungen auf den feuerfesten Materialien im Drehrohrofen, wodurch der Fluss der Kalksteinbeschickung im Ofen gestört wird. Der Ofen muss periodisch gekühlt und die angesammelte Asche manuell entfernt werden, was ein sehr mühsamer und kostspieliger Vorgang ist. Erdgas ist der sauberste Brennstoff und wird hauptsächlich in Vertikalöfen verwendet.
Die dritte Art der Verarbeitung von Kalkstein besteht in der Herstellung von Kalkhydrat, einem trockenen Pulver, das durch Behandlung von Branntkalk mit ausreichend Wasser zur Befriedigung seiner chemischen Affinität zu Wasser erhalten wird, wodurch die Oxide in Hydroxide umgewandelt werden. Kalkhydrat wird manchmal auch gelöschter Kalk genannt. Für die Rauchgasentschwefelung erfordert die Eigenschaft des Kalkhydrats eine erhöhte mittlere Feinheit, eine größere Oberfläche und ein höheres Volumen der Poren. Die Hydratationsreaktion ist chemisch einfach, aber stark exotherm mit einer Wärmeentwicklung von etwa 276 kcal/kg CaO. Die Reaktion ist unten angegeben.
CaO + H2O =Ca(OH)2 + Wärme
Zum Vergleich:Die exotherme Wärme, die bei der Hydratisierung von 1.000 Tonnen gebranntem Kalk mit hohem Calciumgehalt entsteht, entspricht dem Gesamtheizwert von etwa 35 Tonnen Kohle. Die Begriffe Hydratation und Slaking werden häufig synonym verwendet. Es gibt jedoch einen bestimmten und deutlichen Unterschied. Hydratation wird normalerweise als ein Prozess definiert, bei dem ungefähr stöchiometrische Mengen Wasser und Kalk reagieren, um ein Produkt, Hydrat, zu bilden, das ein trockenes Pulver ist. Es enthält weniger als 1 % freie Feuchtigkeit und wird als Pulver gehandhabt. Löschen hingegen ist definiert als ein Prozess, bei dem Kalk mit einer überschüssigen Menge Wasser umgesetzt wird, um eine Kalkaufschlämmung zu bilden, die als Flüssigkeit gehandhabt wird.
Eine schnelle Hydratation neigt dazu, feinere Teilchen zu erzeugen, da Hydratkristallen geringere Agglomerationschancen gegeben werden. Die schnellste Reaktion ist jedoch nicht unbedingt die beste Voraussetzung. Im Prinzip verläuft eine typische hochreaktive Kalkreaktion in drei verschiedenen Phasen (Abb. 3). Diese Phasen werden als (i) kinetisch, (ii) transitorisch und (iii) Diffusion bezeichnet. Die kinetische Phase ist normalerweise sehr kurz (weniger als 10 Sekunden) und zeigt einen starken Temperaturanstieg, der bis zu 50 % des gesamten Temperaturanstiegs ausmachen kann. Die Länge der Übergangsphase (häufig weniger als eine Minute) kann sich aufgrund der Größe der dem Hydrator zugeführten Kalkklumpen ändern. Es zeigt einen sichtbaren Knick des Temperaturanstiegs. In der Diffusionsphase steigt die Temperatur wieder stark an, bis sie schnell abflacht, um das Ende der Reaktion anzuzeigen.
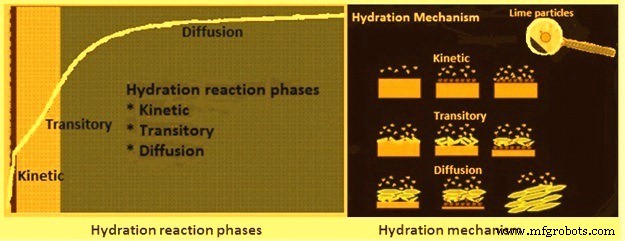
Abb. 3 Hydratationsreaktionsphasen und Hydratationsmechanismus
Der Hydratationsmechanismus ist auch in Abb. 3 dargestellt. Der Hydratationsmechanismus von Kalkpartikeln zeigt, dass die Reaktion nach dem ersten Kontakt mit Wasser aufgrund des ungehinderten Kontakts zwischen Kalk und Wasser innerhalb weniger Sekunden sehr stark einsetzt. Nachdem die erste Schicht aus teilweise hydratisiertem Kalk auf der Oberfläche erzeugt wurde, wirkt sie als Schutzschild für die darunter liegenden Branntkalkschichten, da sie dazu neigt, in der Nähe der Teilchenoberfläche zu bleiben. Die Schicht aus teilhydratisiertem Kalk verzögert also das Eindringen von Wasser. Wenn Ca(OH)2-Kristalle allmählich ihre endgültige Form annehmen, beginnen sie sich zu trennen. Dies verbessert das Eindringen von Wasser, was den Reaktionsverlauf wieder aufnimmt. Der andere wichtige Faktor ist, dass die Entwicklung der Reaktion von der Stückgröße des Branntkalks abhängt.
Anwendung von Kalkstein und Kalk in Eisen- und Stahlwerken
Bei der Herstellung von Eisen im Hochofen (BF) wird Kalkstein entweder beim Sintern oder als direkte Beschickung im Hochofen hinzugefügt. Kalkstein wird normalerweise während der Eisenherstellung hinzugefügt, um entweder neutrale oder leicht basische BF-Schlacke zu erhalten. Die Zugabe von Kalkstein durch Sinterung ist ein bevorzugterer Weg, da während des Sinterprozesses CO 2 aus Kalkstein ausgetrieben wird. Beim Sintern wird Kalkstein in Hammerbrechern auf -3 mm (im Bereich von 85 % bis 90 %) zerkleinert, bevor er in die Sintermischung eingemischt wird. Bei direkter Beschickung des Hochofens werden Kalksteinbrocken mit einer Größe von 10 mm bis 40 mm verwendet.
Bei der Kalksteinzugabe durch Sintern wird heute auch direkt gebrannter Kalkstein (Kalk) verwendet. Die Verwendung von Branntkalk im Sinterverfahren hat die Vorteile (i) Verbesserung der Bindungseigenschaften der Sintermischung, (ii) Verbesserung der Produktivität der Sintermaschine, (iii) Verbesserung der Sinterfestigkeit und (iv) Verringerung der Volumen der Abgase mit den damit verbundenen Vorteilen.
Ein hoher Gehalt an Kieselsäure (SiO2) in dem zum Sintern verwendeten Kalkstein wird bevorzugt, da SiO2 der Wirkung von Aluminiumoxid (Al2O3) im Hochofen entgegenwirkt.
Die zweite Hauptverwendung von Kalkstein ist die Stahlherstellung. Es wird zur Aufrechterhaltung der Schlackenbasizität (CaO/SiO2) von etwa 3 verwendet. In der Stahlerzeugung wird Kalkstein in kalzinierter Form verwendet. Für die Verwendung bei der Stahlerzeugung soll der SiO2-Gehalt (aufgrund seiner sauren Natur) im Kalkstein sehr niedrig sein, vorzugsweise weniger als 1 %. Außerdem soll die Reaktivität des Kalks sehr gut sein, da weniger Zeit zur Verfügung steht, da der Prozess der Stahlherstellung ein sehr schneller Prozess ist. Der gesamte Stahlherstellungsprozess dauert weniger als 20 Minuten.
Kleinere Verwendungen von Kalk (entweder kalziniert oder hydratisiert) sind Entschwefelungsmittel, Beschichtung von Formen von Schweinegussmaschinen, Neutralisierung von saurem Wasser, Wasserbehandlung, Abwasserbehandlung, Rauchgasbehandlung und Schlamm- und Abwasserbehandlung usw. Kalk wird manchmal auch als Bestandteil von synthetischer Schlacke hinzugefügt.
Herstellungsprozess
- Anwendung von Niob in der Stahlindustrie
- Anwendung von Molybdänmetall und seinen Legierungen
- Direktreduziertes Eisen und seine Produktionsprozesse
- Tundish und seine Rolle beim Stranggießen von Stahl
- Entlademöglichkeiten für direktreduziertes Eisen und dessen Heißtransport
- Wissenswerte Branchentrends auf dem Eisen- und Stahlmarkt
- CNC-Maschinen und ihre Vorteile in der Industrietechnik
- Ein Überblick über Werkzeugstahl und seine Anwendungen
- Ein Überblick über Werkzeugstahl und seine begleitenden Anwendungen
- Rohstoffe für die Herstellung von Eisen und Stahl



