Au-beschichtete GaAs-Nanopillar-Arrays, hergestellt durch metallunterstütztes chemisches Ätzen
Zusammenfassung
GaAs-Nanosäulen-Arrays wurden erfolgreich durch metallunterstütztes chemisches Ätzen unter Verwendung von Au-Nanodot-Arrays hergestellt. Die Nanodot-Arrays wurden auf Substraten durch Vakuumabscheidung durch eine poröse Aluminiumoxidmaske mit einer geordneten Anordnung von Öffnungen gebildet. Durch Verwendung eines Ätzmittels mit hoher Säurekonzentration und niedriger Oxidationsmittelkonzentration bei relativ niedriger Temperatur konnte der Bereich um die Au/GaAs-Grenzfläche selektiv geätzt werden. Unter optimalen Bedingungen wurden mit Au bedeckte GaAs-Nanosäulen-Arrays mit einer geordneten Periodizität von 100 nm und Säulenhöhen von 50 nm gebildet.
Hintergrund
III-V-Verbindungshalbleiter haben aufgrund ihrer hervorragenden Eigenschaften, einschließlich der überlegenen Ladungsträgermobilität und der direkten Bandlücke, als Materialien der nächsten Generation und potenzielle Alternativen zu Halbleitern auf Siliziumbasis Aufmerksamkeit auf sich gezogen. Nanostrukturen mit geordneter Periodizität und/oder hohem Aspektverhältnis gelten aufgrund ihrer geringen Kosten und hohen Umwandlungseffizienz im Vergleich zu herkömmlichen dünnschichtbasierten Geräten als wichtiges Element in verschiedenen Anwendungen, einschließlich optischer und optoelektronischer Bauelemente [1,2,3,4] . Im Allgemeinen werden zur Herstellung niederdimensionaler Halbleiter (z. B. Nanodrähte) Trockenprozesse wie Molekularstrahlepitaxie, Dampf-Flüssigkeit-Feststoff-Epitaxie und metallorganische Dampfphasenepitaxie verwendet [1, 5, 6, 7]. Obwohl diese Verfahren viele Vorteile haben, einschließlich einer hohen Musterungsgenauigkeit, umfassen ihre Nachteile hohe Kosten und Größenbeschränkungen des Musterungsbereichs in praktischen Anwendungen. Daher werden alternative Methoden benötigt, die eine einfache und kostengünstige Herstellung von Nanostrukturen ermöglichen.
Das metallunterstützte chemische Ätzen, das von Li und Bohn im Jahr 2000 vorgeschlagen wurde [8], ist aufgrund seiner relativen Einfachheit und geringen Kosten ein häufig verwendetes Herstellungsverfahren. Jüngste Studien haben gezeigt, dass metallunterstütztes chemisches Ätzen angewendet werden kann, um komplexe Nanostrukturen wie tiefe, gerade Nanoporen, helikale Nanoporen, geneigte Kanäle, Zykloiden und Spiralen herzustellen [4, 9,10,11,12]. Seit dem Bericht von Li et al. berichten jedoch die meisten Studien über die Herstellung von Silizium-Nanostrukturen; wenige Untersuchungen haben sich auf die Nanofabrikation von III-V-Verbindungshalbleitern konzentriert [13, 14], und die Bildung geordneter Strukturen im Nanometerbereich auf GaAs-Substraten ist besonders wenig verstanden. Um den Anwendungsbereich des metallunterstützten chemischen Ätzens zu erweitern, ist es wünschenswert, ein Nanofabrikationsverfahren für III-V-Verbindungshalbleiter zu entwickeln, das nicht von den Abmessungen der resultierenden Muster abhängt.
In einer früheren Studie haben wir Mikrobump-Arrays aus InP [15] und Linienmuster und Säulenarrays aus GaAs [16] unter Verwendung von metallunterstütztem chemischem Ätzen hergestellt. Die Abmessungen der resultierenden Muster (z. B. Periodizität und Breite der Linienmuster) reichten jedoch von mehreren Mikrometern bis zu mehreren zehn Mikrometern. Nach unserem besten Wissen hat aus den folgenden Gründen keine Studie über die Bildung geordneter GaAs-Nanostrukturen mit Submikrometer- oder kleinerer Periodizität durch metallunterstütztes chemisches Ätzen berichtet:(1) Form und Größe von Edelmetallen lassen sich nur schwer kontrollieren als Katalysator im Nanometerbereich verwendet wird und (2) das Ätzphänomen von GaAs im Vergleich zu Silizium weniger gut verstanden ist. Daher haben wir versucht, den Ätzmechanismus von GaAs auf der Nanometerskala aufzuklären. In dieser Studie zeigen wir, dass geordnete Nanosäulen-Arrays mit einer Periodizität von 100 nm auf GaAs-Substraten durch metallunterstütztes chemisches Ätzen mit einem strukturierten Au-Katalysator hergestellt werden können. Die Auswirkungen der Ätzmittelzusammensetzung und der Ätzzeit auf die Morphologie des geätzten GaAs-Substrats werden ebenfalls untersucht.
Methoden
Das Prinzip der Herstellung von GaAs-Nanosäulen-Arrays durch metallunterstütztes chemisches Ätzen ist in Abb. 1 schematisch dargestellt. Eine poröse Aluminiumoxid-Durchgangslochmaske mit einer geordneten Anordnung von Öffnungen wurde durch zweistufige Anodisierung gefolgt von zweischichtiger Anodisierung hergestellt [ 17]. Die erste Anodisierung wurde auf elektrochemisch poliertem Aluminium (99,99 % Reinheit) bei einer konstanten Spannung von 40 V in 0,3 mol dm –3 . durchgeführt Oxalsäure bei 30 °C für 3 h. Die Anodisierungsspannung von 40 V ist als Selbstordnungsbedingung bekannt, die eine hochgeordnete Porenanordnung in anodischem Aluminiumoxid erzeugt [18].
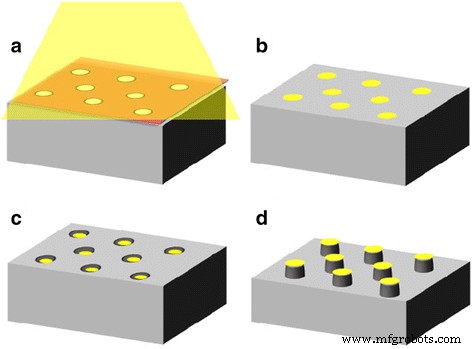
Schematisches Modell der Herstellung von GaAs-Nanosäulen-Arrays. a Vakuumabscheidung von Au auf einem GaAs-Substrat durch eine poröse Aluminiumoxidmaske. b Abnehmen der Maske. c , d Chemisches Ätzen von GaAs unter Verwendung von Au-Nanodot-Arrays als Katalysator
Nach der ersten Anodisierung wurde die erste anodisierte Aluminiumoxidschicht in einer Mischlösung aus Phosphorsäure und Chromsäure bei 80 °C entfernt. Anschließend wurde die zweite Anodisierung 1,5 Minuten lang unter den gleichen Bedingungen wie die erste Anodisierung durchgeführt. Nach dem Prinzip der zweischichtigen Anodisierung wurde die Probe bei einer konstanten Spannung von 40 V in 12 mol dm −3 . erneut anodisiert Schwefelsäure bei 5 °C für 8 Minuten, um eine Opferschicht aus Aluminiumoxid herzustellen. Die poröse Aluminiumoxidmaske mit Durchgangslöchern wurde durch Auflösen der Opferaluminiumoxidschicht in 2 Gew.-% Phosphorsäure bei 30 °C für 20 Minuten gebildet. Weiteres chemisches Ätzen wurde in 5 Gew.-% Phosphorsäure bei 30 °C für 15 Minuten durchgeführt, um den Porendurchmesser der Aluminiumoxidmaske zu erhöhen.
Nach dem Spülen der Aluminiumoxidmaske in destilliertem Wasser wurde die erhaltene Aluminiumoxidmaske auf ein n-Typ-GaAs-Substrat [Si-dotiert, 2,35–2,67 × 10 –3 Ω cm, (100) Kristallorientierung]. Anschließend wurde eine 30 nm dicke Au-Schicht durch die Aluminiumoxidmaske unter Verwendung eines Vakuumabscheidungssystems nach der Widerstandsheizformel (ULVAC KIKO Inc., VPC-410) mit einem Druck unter 1 × 10 -3 Pa (Abb. 1a). Die Dicke der Au-Schicht wurde mit einer Quarzkristall-Mikrowaage gemessen und die Abscheidungsrate von Au betrug 0,02 nm s –1 . . Nach der Metallabscheidung wurde die Aluminiumoxidmaske in 5 Gew.-% Phosphorsäure bei 25 °C 30 Minuten lang entfernt (Abb. 1b).
Das Au-beschichtete GaAs-Substrat wurde in HF mit KMnO4 . chemisch geätzt (Abb. 1c). KMnO4 wirkt in einer sauren Lösung als Oxidationsmittel [19,20,21,22]. Die Morphologien der Aluminiumoxidmaske, der abgeschiedenen Au-Schicht und des geätzten GaAs-Substrats wurden durch Feldemissions-Rasterelektronenmikroskopie (FE-SEM; JEOL JSM-6701F) bewertet. Die chemische Zusammensetzung des geätzten GaAs-Substrats wurde durch Schneckenelektronenspektroskopie (AES; JEOL JAMP-9500F) bewertet. Auger-Elektronenspektren werden leicht von ausgewählten Punkten oder Bereichen der Oberfläche aufgenommen. Hier wurde ein AES-Elementar-Mapping-Bild mit einer Beschleunigungsspannung und einem Emissionsstrom von 30 kV bzw. 15 nA aufgenommen.
Ergebnisse und Diskussion
Beim metallunterstützten chemischen Ätzen ist es wichtig, die Abmessungen des Metallkatalysators genau zu kontrollieren, um das gewünschte Design auf der Substratoberfläche zu erhalten. Da die Morphologie der resultierenden Struktur von dem anfänglichen geometrischen Muster und den Abmessungen des Metallkatalysators abhängt, ist ein strukturierter Metallkatalysator erforderlich, um geordnete Nanostrukturen auf Halbleiteroberflächen herzustellen. In dieser Studie wurde eine Aluminiumoxidmaske mit einer geordneten Anordnung von Öffnungen verwendet, um die Größe und Anordnung des Metallkatalysators zu kontrollieren. Für einen trockenen Metallabscheidungsprozess ist die Dicke der Maske kritisch, da die Metallabscheidung durch eine dicke Maske mit schmalen Öffnungen physikalisch schwierig ist. Bei porösem Aluminiumoxid kann die Dicke der Maske mit hoher Reproduzierbarkeit durch Änderung der Anodisierungszeit eingestellt werden. Hier wurde eine ungefähr 300 nm dicke poröse Aluminiumoxidmaske mit Durchgangslöchern auf einem GaAs-Substrat hergestellt. Die Aluminiumoxidmaske wurde mit ihrer Oberfläche nach oben gerichtet eingesetzt. Der obere und der untere Durchmesser der Öffnungen in der Aluminiumoxidmaske betrugen ungefähr 80 nm bzw. 70 nm. Der etwas größere Durchmesser der oberen Öffnung im Vergleich zur unteren Öffnung wurde dem chemischen Ätzen während der Herstellung der Aluminiumoxidmaske zugeschrieben.
Abbildung 2 zeigt ein typisches gut geordnetes Au-Nanodot-Array auf einem GaAs-Substrat. Das Nanopunkt-Array entspricht der Konfiguration des selbstgeordneten Poren-Arrays in der anodischen Aluminiumoxidmaske, wie in Fig. 2a gezeigt. Obwohl die Kontrollierbarkeit der Au-Abscheidung weiter verbessert werden sollte, ist die hier gezeigte Metallabscheidung durch die Aluminiumoxidmaske im Hinblick auf die Einfachheit und Effizienz des Herstellungsprozesses für die großtechnische Herstellung von geordneten Edelmetallpunktmustern auf Halbleitersubstraten geeignet. Beachten Sie, dass jeder Au-Nanopunkt fast den gleichen Durchmesser von ungefähr 70 nm hatte; dieser Durchmesser wurde durch die Porengröße des unteren Teils der Aluminiumoxidmaske bestimmt, während die Höhen der Au-Nanopunkte hauptsächlich durch die Abscheidungszeit bestimmt wurden. In dieser Studie wurde die Höhe jedes Au-Nanopunkts auf ~30 nm eingestellt, wie in Abb. 2b gezeigt.

a Oberfläche und b REM-Querschnittsbilder eines Au-Nanodot-Arrays, das auf einem GaAs-Substrat durch eine anodische poröse Aluminiumoxidmaske gebildet wurde
Nach der Bildung von Au-Dot-Arrays auf GaAs-Substraten wurden die Proben in eine Lösung aus HF und KMnO4 . eingetaucht zum metallunterstützten chemischen Ätzen. Beim herkömmlichen metallunterstützten chemischen Ätzen erfolgt das Ätzen lokal an der Grenzfläche zwischen dem Katalysator und dem darunter liegenden Substrat, was zur Bildung von Poren oder Gräben in senkrechter Richtung zum Substrat führt, und der Metallkatalysator sinkt in den Halbleiter ein, wie in gezeigt Abb. 1c. Es wird angenommen, dass die Verwendung eines Ätzmittels, das aus einer hohen Säurekonzentration und einer niedrigen Oxidationsmittelkonzentration besteht, einen reibungslosen Verbrauch der erzeugten positiven Löcher fördert (h + ) an der Grenzfläche Metall/Halbleiter. In dieser Studie wird erwartet, dass die Oxidation von GaAs an der Au/GaAs-Grenzfläche direkt durch das erzeugte h + .
Abbildung 3 zeigt ein typisches SEM-Bild der geätzten GaAs-Oberfläche unter Verwendung des strukturierten Au-Katalysators. Chemisches Ätzen wurde in einer Lösung mit 0,001 mol dm –3 . durchgeführt KMnO4 und 20 mol dm −3 HF bei einer relativ hohen Temperatur von 45 °C. In dieser Studie wurde die Konzentration von KMnO4 war niedrig (0,001 mol dm −3 ), um seitliches Ätzen zu unterdrücken. Nach früheren Berichten von DeJarld et al. und Cheung et al. stieg die laterale Ätzrate mit zunehmendem Oxidationsmittel (KMnO4 ) Konzentration [19, 21].

SEM-Bild der oberen Oberfläche des GaAs-Substrats nach Au-unterstütztem chemischem Ätzen in einer Lösung mit 0,001 mol dm –3 KMnO4 und 20 mol dm −3 HF für 600 s bei 45 °C
Au-Katalysatoren, die als kreisförmige helle Flecken erkannt wurden, wurden in vielen Bereichen des GaAs-Substrats in Poren beobachtet, wie in Abb. 3 gezeigt. Der Durchmesser der in Abb. 3 beobachteten Poren stimmte mit der Größe der gezeigten abgeschiedenen Au-Nanopunkte überein in Fig. 2. Diese Ergebnisse zeigen, dass konventionelles metallunterstütztes chemisches Ätzen, das in Fig. 1c schematisch gezeigt ist, nur an der Au/GaAs-Grenzfläche auftrat und anisotrop senkrecht zum Substrat, dh in der <100>-Richtung, verlief.
Beim metallunterstützten chemischen Ätzen beeinflussen die Ätzmittelzusammensetzung und die Ätztemperatur die Dynamik der Trägerdiffusion, Oxidation und Produktentfernung [19]. Um neue Anwendungen geätzter GaAs-Substrate zu erschließen, haben wir versucht, GaAs-Nanosäulen-Arrays herzustellen, indem wir die Bedingungen des metallunterstützten chemischen Ätzens ändern. Abbildung 4 zeigt typische Querschnitts-REM-Bilder von geätzten GaAs-Oberflächen, die mit dem strukturierten Au-Katalysator erhalten wurden. Durch Erhöhung der Konzentration von KMnO4 , die Morphologie der resultierenden Struktur könnte geändert werden. In allen Fällen wurden über die gesamte Probenfläche hexagonal angeordnete GaAs-Nanosäulen erhalten. Die Säulenspitzen waren durch seitliches Ätzen leicht verjüngt. Die Periodizitäten der GaAs-Nanosäulen-Arrays betrugen ungefähr 100 nm, entsprechend denen der als Katalysator verwendeten Au-Punkt-Arrays und den Poren des porösen Aluminiumoxids, das als Anfangsmaske verwendet wurde. Unseres Wissens sind die Abmessungen (z. B. Periodizität) der Strukturen, die in dieser Studie auf GaAs durch metallunterstütztes chemisches Ätzen erhalten wurden, kleiner als die für andere GaAs-Strukturen berichteten [19,20,21,22].

SEM-Bilder von GaAs-Nanosäulen-Arrays, die durch Au-unterstütztes chemisches Ätzen in Lösungen mit 0,01 mol dm –3 . hergestellt wurden KMnO4 und 5, 10 oder 20 mol dm −3 HF für 5 s bei a 20 und b 45 °C
Als das Ätzen bei einer relativ niedrigen Temperatur von 20 °C durchgeführt wurde, wurde an der Spitze jeder Säule ein Au-Katalysator beobachtet, wie durch Pfeile angezeigt. Abbildung 4a zeigt, dass die Ätzrate mit steigender HF-Konzentration bei derselben Oxidationsmittelkonzentration zunahm. Bei der hohen HF-Konzentration von 20 mol dm −3 , war die verbleibende GaAs-Säulenhöhe am höchsten.
Entgegen der Erwartung, dass die Oxidation von GaAs an der Au/GaAs-Grenzfläche durch das erzeugte h + , wurde im Fall von Fig. 4 keine chemische Auflösung im Kontaktbereich zwischen dem Au-Katalysator und dem darunterliegenden GaAs-Substrat beobachtet. Das Ätzmuster wird als von der Temperatur des Ätzmittels abhängig angesehen. Bei niedriger Temperatur (z. B. 20 °C) ist die Rate von h + Es wird angenommen, dass der Verbrauch an der Au/GaAs-Grenzfläche niedriger ist als die Rate von h + Injektion; also h + diffundiert in den Bereich, der Au-beschichtetes GaAs umgibt. Schließlich bildete sich unter dem Kontaktbereich zwischen dem Au-Katalysator und dem darunterliegenden GaAs-Substrat eine GaAs-Nanosäule, da auf der freigelegten GaAs-Oberfläche ortsselektives Ätzen auftrat. Mit anderen Worten, die Au-Nanopunkte dienten auch als Schutzmaske, um die Auflösung des GaAs-Substrats zu verhindern. Dieses Ätzphänomen, wie es in Abb. 1d schematisch dargestellt ist, wird als inverses metallunterstütztes chemisches Ätzen bezeichnet [19, 22]. Im Jahr 2010 demonstrierten wir auch die Bildung von InP-Mikrobump-Arrays durch inverses metallunterstütztes chemisches Ätzen unter UV-Bestrahlung [15]. Im Gegensatz zum herkömmlichen metallunterstützten chemischen Ätzen verläuft das inverse metallunterstützte chemische Ätzen in den Oberflächen freiliegender III–V-Verbindungshalbleiter um metallbeschichtete Bereiche herum durch die Diffusion von h + aus Metallkatalysator und anschließendem ortsselektiven chemischen Ätzen. Ein so einzigartiges Ätzverhalten wurde bei Siliziummaterialien nicht beobachtet.
Wenn metallunterstütztes chemisches Ätzen bei einer hohen Temperatur von 45 °C durchgeführt wird, wird das erzeugte h + wird erwartet, dass es verbraucht wird, sobald es die Grenze zwischen Au, GaAs und Ätzmittel erreicht, was zu einer Förderung des vertikalen Ätzens führt. Aber auch in diesem Fall trat ein inverses metallunterstütztes chemisches Ätzen auf. Wie in Fig. 4b gezeigt, nahm die Ätzrate mit zunehmender HF-Konzentration auf die gleiche Weise wie das Ätzverhalten von Fig. 4a zu. Bei einer hohen Ätztemperatur von 45 °C und einer hohen HF-Konzentration von 20 mol dm −3 , wurden die Au-Katalysatoren von den Spitzen der GaAs-Säulen abgelöst, weil das überschüssige h + die durch die relativ hohe Temperatur selbst in der kurzen Ätzzeit von 5 s erzeugt wurde, förderte das seitliche Ätzen von GaAs in Gegenwart des Au-Katalysators. Die Formkontrollierbarkeit der Säulen wird durch die zusätzliche Optimierung der Ätzbedingungen (z. B. Ätzmittelzusammensetzung, Konzentration und Temperatur) verbessert. Versuche, die Auswirkungen der Konzentration des Oxidationsmittels auf die Bildung von h + . zu klären und Morphologie von geätztem GaAs sind derzeit im Gange.
Um den Einfluss der Ätzzeit auf die Geometrie der geätzten GaAs-Struktur zu untersuchen, wurde das chemische Ätzen auf 20 mol dm –3 . verlängert HF und 0,01 mol dm −3 KMnO4 bei einer relativ niedrigen Temperatur von 20 °C. Wie im Querschnittsbild in Abb. 5a gezeigt, erreichte die Tiefe der GaAs-Nanosäulen ~50 nm. Eines der bemerkenswerten Merkmale der in dieser Studie erhaltenen GaAs-Nanosäulen-Arrays besteht darin, dass die Spitze jeder Säule mit Au bedeckt war, wie im Einschub von Abb. 5a gezeigt. Abbildung 6 zeigt die AES-Elementaranalyse derselben Probe. Die AES-Karten für Ga und Au des geätzten GaAs zeigen das Vorhandensein von Au an der Spitze jeder Säule selbst nach metallunterstütztem chemischem Ätzen für 10 s.

SEM-Querschnittsbilder eines GaAs-Nanosäulen-Arrays, hergestellt durch Au-unterstütztes chemisches Ätzen bei 20 °C für a 10 und b 60 s in einer Lösung mit 20 mol dm −3 HF und 0,01 mol dm −3 KMnO4 . Einschub zeigt ein Oberflächenbild eines mit Au bedeckten GaAs-Nanosäulen-Arrays

a Bild des GaAs-Substrats nach Au-unterstütztem chemischem Ätzen und entsprechende AES-Karten für b Ga und c Au. Die Ätzbedingungen waren die gleichen wie in Abb. 5a
Da die Säulenhöhe hauptsächlich durch die Ätzzeit bestimmt wurde, wurde das Ätzen weiter von 10 s auf 1 min verlängert, um Arrays von höheren Säulen auf GaAs zu bilden. Die verlängerte Ätzzeit von 1 min führte jedoch zu einer verringerten Säulenhöhe, wie in Abb. 5b gezeigt. Die Abnahme der Säulenhöhe wurde dem seitlichen Ätzen in Gegenwart eines Au-Katalysators und dem anschließenden Ablösen der als Katalysator verwendeten Au-Punkte zugeschrieben.
Obwohl metallunterstütztes chemisches Ätzen, das die Diffusion von h + aus Metallkatalysatoren, noch nicht vollständig abgeschlossen ist, bietet die Nanofabrikation von III-V-Verbindungshalbleitern durch metallunterstütztes chemisches Ätzen eine vielversprechende Alternative für das Design geordneter dreidimensionaler Strukturen ohne den Einsatz von Trockenprozessen. Darüber hinaus haben die erhaltenen GaAs-Nanosäulen-Arrays mit Au-Kappe potenzielle technologische und wissenschaftliche Anwendungen in optoelektronischen Geräten wie Solarzellen, die plasmonische Nanostrukturen verwenden, um das Einfangen von Licht zu verbessern [23, 24].
Schlussfolgerungen
Zusammenfassend haben wir die Herstellung geordneter GaAs-Nanosäulen-Arrays auf GaAs (100)-Substraten durch Au-unterstütztes chemisches Ätzen demonstriert. Au-Nanodot-Arrays mit hexagonalen Gittermustern und geordneten Periodizitäten von 100 nm wurden durch Vakuumabscheidung durch eine poröse Aluminiumoxidmaske gebildet. Die Au-Nanopunkte hatten Durchmesser von ungefähr 70 nm, entsprechend dem Durchmesser des unteren Teils der Aluminiumoxidmaske, und dienten als Katalysator und Schutzmaske. Bei relativ niedriger Temperatur könnten Au-bedeckte GaAs-Nanosäulen-Arrays durch ortsselektives Ätzen in der umgebenden freiliegenden GaAs-Oberfläche gebildet werden. Diese Ergebnisse liefern den ersten Beweis für die präzisere Kontrolle von Nanostrukturen auf GaAs-Substraten mit einem praktikablen Ansatz basierend auf metallunterstütztem chemischem Ätzen. Die in dieser Mitteilung vorgestellte unkonventionelle Lithografietechnik zur Nanofabrikation von III-V-Verbindungshalbleitern überwindet die Nachteile konventioneller Methoden und hat potenzielle technologische und wissenschaftliche Anwendungen in verschiedenen Forschungsbereichen.
Abkürzungen
- AES:
-
Auger-Elektronenspektroskopie
- FE-REM:
-
Feldemissions-Rasterelektronenmikroskopie
Nanomaterialien
- Chemische Eigenschaften von Titan
- C#-Arrays
- C++-Arrays
- C-Arrays
- C Mehrdimensionale Arrays
- Java-Arrays
- Aufklärung der morphologischen Evolution und Ätzkinetik poröser Silizium-Nanodrähte beim metallunterstützten chemischen Ätzen
- Auswirkungen des Mikroumgebungs-pH-Werts von Liposomen auf die chemische Stabilität des beladenen Arzneimittels
- Erhöhte Biokompatibilität in anodischen TaO x Nanotube-Arrays
- MATLAB - Arrays



