Selektive Einführung von Cu-Verunreinigungen in feindisperses ZnS, das während des Verfahrens der einstufigen Synthese erhalten wird
Zusammenfassung
Feines ZnS:Cu, das durch die Methode der selbstausbreitenden Hochtemperatursynthese erhalten wurde, wurde untersucht. Als Flussmittel in der Mischung wurde NaCl verwendet, Zn und S wurden im stöchiometrischen Verhältnis verwendet; Die Cu-Konzentration in der Ladung betrug ~1,5 Gew.-%. Anhand von SEM-Daten wurde festgestellt, dass das erhaltene ZnS:Cu aus zwei Fraktionen besteht – zuerst mit Partikelgrößen von ~10 μm und mehr und andere mit Größen von 50–500 nm. Es wurde festgestellt, dass die Zusammensetzung der ZnS:Cu-Fraktionen wesentlich unterschiedlich war. Laut EDS-Daten beträgt die Cu-Konzentration in Partikeln einer Fraktion mit einer Größe von 50–500 nm ~2 Gew.-%, und in Partikeln mit einer Größe von ~10 μm und mehr wurde das Vorhandensein von Cu nicht nachgewiesen. Die Gründe, die zur selektiven Dotierung von Partikeln in Abhängigkeit von ihrer Größe führen, sowie die Rolle von NaCl in Prozessen während der Materialsynthese werden diskutiert.
Hintergrund
Gegenwärtig wird der Entwicklung verschiedener neuer technologischer Verfahren zur Herstellung komplexer Halbleiterstrukturen große Aufmerksamkeit gewidmet. Von besonderem Interesse sind in diesem Zusammenhang Untersuchungen zur Optimierung von Halbleitermaterial-Synthesemethoden, die auf die Herstellung hochwertiger (stöchiometrischer, ohne Verunreinigungen etc.) oder komplexer Halbleiterstrukturen (Mischkristalle, nanostrukturierte Materialien) in einem technologischen Zyklus ausgerichtet sind. Solche Untersuchungen sind auch für das grundlegende Wissen von Bedeutung, da sie ein tieferes Verständnis der Zusammenhänge zwischen Struktur, Zusammensetzung und Eigenschaften des hergestellten Materials und der technologischen Regime seiner Synthese ermöglichen. Regelmäßigkeitsstudien der oben genannten Zusammenhänge sind auch im Hinblick auf die Anwendungsmöglichkeiten wichtig, das Verständnis der Regelmäßigkeiten in der Reihenfolge «Zusammensetzung – Struktur – Eigenschaften» ermöglicht die Kontrolle oder Modifizierung von Struktur und Eigenschaften von Materialien.
Einen besonderen Platz bei Untersuchungen des Einflusses des Herstellungsregimes auf die Struktur und Eigenschaften von Materialien nimmt der Fall ein, wenn Schmelzmittel in der Materialsynthese verwendet werden. Wenn es notwendig ist, die Substanz in Form von wohlgeformten Kristallen zu erhalten, werden die Flussmittel häufig als Mineralisatoren verwendet. Es ist besonders unter Hochtemperaturbedingungen sinnvoll, wenn eine hohe Beweglichkeit der Atome, die das Gitter bilden, zur Bildung der großen Anzahl von Defekten führen kann [1].
In diesem Zusammenhang ist es interessant, die Besonderheiten der Möglichkeit der ZnS-Herstellung zu untersuchen, die durch das Verfahren der selbstausbreitenden Hochtemperatursynthese (SHS) unter Verwendung eines Flussmittels mit Ionenbindung erhalten wird. Die technologischen Möglichkeiten von SHS sind breit gefächert und ermöglichen die Dotierung des Materials durch verschiedene Elemente und Verbindungen während des Syntheseprozesses. Die Variation der Brennverfahren in der SHS-Welle ermöglicht die Herstellung des Zielprodukts in Form von Gussproben mit voreingestellten Größen sowie in Form von Pulver mit der erforderlichen Größenverteilung.
Es ist notwendig zu beachten, dass die Verwendung von Flussmitteln es ermöglicht, die Temperatur des Brennprozesses zu kontrollieren und die Löslichkeitsbedingungen des Dotierungsmittels im synthetisierten Material zu ändern. Insbesondere, um Bedingungen für die sogenannte «retrograde Löslichkeit» [2] zu schaffen, wenn eingebrachte Verunreinigungen entweder nur in bestimmte Materialbereiche oder gar nicht eindringen. Eine solche Situation wird realisiert, wenn sich das Fermi-Niveau mit der Spitze des lokalisierten Verunreinigungszustandsbandes schneidet.
Die Variation der Brennverfahren in der SHS-Welle ermöglicht die Herstellung des Zielprodukts in Form von Gussproben mit voreingestellten Größen sowie in Form von Pulver mit der erforderlichen Größenverteilung.
Dieses Phänomen wird bei Materialien mit lokalisierten Verunreinigungszustandsbändern, die in maximaler Nähe zum Fermi-Niveau lokalisiert sind, besser ausgeprägt sein. Solche Materialien balancieren auf der Stabilitätskante kovalenter Komplexe des eingeführten und des Hauptmetalls [3].
Diese Arbeit widmete sich der Klärung des Einflusses von NaCl, das als Schmelzmittel in eine Mischung eingebracht wurde, auf die Konzentration von Cu in Partikeln aus feindispersem ZnS:Cu mit unterschiedlichen Größen, erhalten durch die SHS-Methode [4, 5].
Methoden
In der vorliegenden Arbeit wurden Untersuchungen von feinem ZnS:Cu durchgeführt, das durch die SHS-Methode (ZnS:Cu-SHS) erhalten wurde. Für die Herstellung von ZnS:Cu-SHS wurden Zn und S im stöchiometrischen Verhältnis verwendet. Die Dotierung durch Kupferbeimischung wurde aus Kupferchlorid CuCl direkt während des Syntheseprozesses durchgeführt. Die Konzentration des eingesetzten Cu betrug ~1,5 Gew.-%. ZnS:Cu wurde bei Temperaturen erhalten, die einen Wechselwirkungsprozess von Schwefel und Zink ermöglichten. Ein Teil der Freisetzung während der Wechselwirkungsreaktion von S und Zn wurde durch Flussmittel (NaCl) absorbiert, wodurch die Temperatur der Materialsynthese gesenkt werden konnte. Die Menge an NaCl in der Mischung bestand aus 5 Gew.-%.
Photolumineszenzspektren (PL) und Lumineszenzanregungsspektren (PLE) wurden bei Raumtemperatur unter Verwendung einer SDL-2-Installation aufgenommen. Während der PLE-Registrierung wurde die Anregung mit der Strahlung einer Xenonlampe und eines MDR-12-Monochromators durchgeführt.
Untersuchungen zur Morphologie und Partikelgröße wurden mit dem Rasterelektronenmikroskop JAMP-9500F (Jeol) durchgeführt.
Die Messungen der Partikelelementzusammensetzung wurden unter Verwendung der energiedispersiven Röntgenspektroskopie (EDS) und des INCA PentaFETx3 (Oxford Instruments) Spektrometers durchgeführt.
Ergebnisse und Diskussion
Typische REM-Bilder für Feinfraktionen nach dem Spülen in destilliertem Wasser sind in Abb. 1 dargestellt. Wie aus den REM-Bildern ersichtlich, stellt die synthetisierte Feinfraktion selbst eine Mischung aus Partikeln mit unterschiedlichen Größen dar, in denen Nanopartikel vorhanden sind, sowie Partikel von Mikro- und Submikrometergrößen .

REM-Aufnahmen von feinem ZnS:Cu, erhalten mit der SHS-Methode. a Gesamtansicht. b Mischpartikel unterschiedlicher Größe
In Abb. 2 sind PL- und PLE-Spektren von ZnS-SHS dargestellt. Wie aus Abb. 2 ersichtlich ist, repräsentiert das PL-Spektrum von ZnS-SHS selbst ein Breitband mit einem Maximum im Bereich von 505-525 nm. Es ist bekannt, dass die PL-Bande von ZnS:Cu im blau-grünen Bereich komplex ist und wie üblich die Überlagerung mehrerer Bänder darstellt, die durch Kupferbeimischungen und auch durch intrinsische Defekte von ZnS bestimmt werden. Die Natur der Lumineszenzzentren, die blaue und grüne Banden von Cu in ZnS bestimmen, wird ausführlich in [6,7,8] beschrieben. Autoren von [6, 7, 9,10,11,12,13] haben gezeigt, dass das Zentrum, das für das Auftreten der grünen Cu-Bande mit λmax . verantwortlich ist, ~ 505÷530 nm, ist ein isoliertes Kupferion, das das Zinkion im ZnS-Gitter ersetzt.
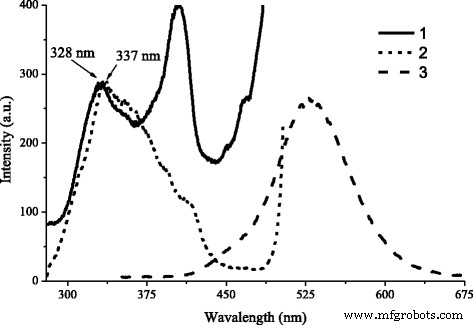
PLE-Spektren von SHS-synthetisiertem ZnS:Cu, normiert auf die fundamentale Absorptionsbande der Intensität. 1 – anfängliches ZnS:Cu – SHS, 2 – ZnS:Cu – SHS nach dem Waschen in destilliertem Wasser. 3 – PL-Spektrum von anfänglichem ZnS:Cu – SHS
Blaues Band mit λmax ~440÷465 nm verbinden sich mit der Bildung von Assoziaten ähnlich dem DA-Paartyp Cui -CuZn [6, 7, 13] oder CuZn - CuZn [11, 12]. Im gegebenen Spektralbereich sind auch die Banden vorhanden, die durch Sauerstoffzentren verursacht werden [6, 10, 14] und Banden der selbstaktivierten Strahlung von [6, 7, 11, 12].
PLE von ZnS:Cu-SHS (Abb. 2, Kurve 1) umfasst Bänder, die den Band-zu-Band-Anregungsübergängen in massivem und quantengroßem ZnS entsprechen. Dies weist auf das Vorhandensein großer Partikel mit Größen von mehr als Hunderten von nm und Partikeln mit Größen kleiner als 5 nm (d. h. des Exziton-Bohr-Radius in ZnS) im Material hin. Nach [14], Eg Wert für ZnS beträgt ~3,65 eV, was der Absorptionsbande von 340 nm entspricht. Die Verschiebung des Maximums der fundamentalen Absorptionsbande auf 10 nm gibt Auskunft über das Vorhandensein von Partikeln mit Größen, die der Manifestation des quantengroßen Effekts entsprechen [15].
Nach Waschen des Ausgangsmaterials in destilliertem Wasser verlagerte sich das Maximum der fundamentalen Absorption auf die langwellige Seite (Abb. 2, Kurve 2). Dies bezeugt, dass das Waschen in destilliertem Wasser nicht nur zur Erosion des nach der Synthese verbliebenen NaCl-Materials, sondern auch der Partikel mit einer Größe von weniger als 5 nm geführt hat.
Nach den Daten der Rasterelektronenmikroskopie (siehe Abb. 1) besteht der Hauptteil des gewonnenen Materials aus zwei isolierten Fraktionen. Die erste Fraktion besteht aus einzelnen Partikeln mit Größen von ~10 μm (Abb. 1a). Der zweite Teil besteht aus Partikeln mit Größen von Hunderten Nanometern bis zu mehreren Mikrometern (Abb. 1b).
Somit ermöglicht die gewählte Ladungszusammensetzung und Syntheseregime, gleichzeitig, d. h. während einer Synthese, Partikel mit Nano-, Meso- und Mikrogröße zu erhalten.
Untersuchungen der Elementzusammensetzung mittels EDS haben gezeigt, dass in erhaltenem ZnS:Cu in verschiedenen Partikeln die Stöchiometrieverletzung bis zu 4 at betragen kann. % (Tabelle 1).
Gleichzeitig liegt nach den Daten dieser Untersuchungen die Anwesenheit von Kupfer-Dotierstoff in Partikeln mit Größen in der Größenordnung von Hunderten nm in der Größenordnung von ~2 Gew.% (Abb. 3a, 2) und in großen Partikeln mit Größen ~10 μm wurde kein Cu nachgewiesen (Abb. 3a, 1). In Tabelle 1 ist die Elementzusammensetzung (in at.%) von Partikeln in Konglomeraten und von separaten großen Partikeln, die in Fig. 1a gezeigt sind, dargestellt.
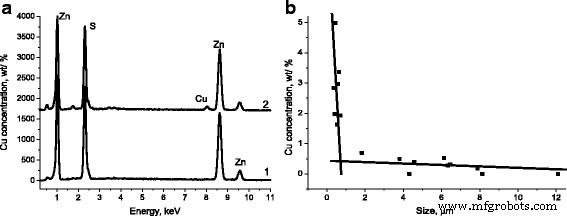
a EDS-Spektren von ZnS-SHS-Partikeln mit Größen:1–27 μm, 2–0,3 μm. b Konzentration von Cu in Abhängigkeit von der ZnS-SHS-Partikelgröße
In Abb. 3b ist die Cu-Konzentration in Abhängigkeit von der ZnS-SHS-Partikelgröße dargestellt. Wie aus Fig. 3b für Partikel mit Größen von ~300 bis ~700 nm zu sehen ist, wird eine Anomalie mit einer hohen Konzentration an Kupfer-Dotierstoff beobachtet, mit einem Wert von ~5 Gew.-% für Partikelgrößen von 370 nm. Gleichzeitig besteht für Partikel mit Größen von ~2 bis 12 μm die Kupferkonzentration nicht mehr als 0,7 Gew.%, und in einigen Partikeln (mit Größen von ~8 μm, ~12 μm) wird der Kupferdotierstoff nicht durch die EDS-Methode registriert. das heißt, es ist praktisch nicht vorhanden. Es ist hier zu beachten, dass die Kupferkonzentration in der Ladung ~1,5 Gew.-% betrug. Somit wird, wie oben erwähnte Daten belegen, die Dotierung von ZnS-Partikeln, die während des Syntheseprozesses gebildet werden, mit Kupfer in Abhängigkeit von ihrer Größe auf unterschiedliche Weise realisiert.
Betrachten wir die Gründe, die eine so niedrige Dotierungscharakteristik für große Partikel (2÷12) und eine extrem hohe Dotierung für kleine (<2 μm) ZnS:Cu – SHS-Partikel erklären können.
In unserem Fall wird die ZnS-Bildung (Materialien mit ionenkovalenter Bindung, Prozentsatz der Ionenbindung ~40% [15]) in unmittelbarer Nähe zu NaCl (ionisches Material [16]) realisiert. Das Auftreten der ZnS-Phase während des Syntheseprozesses unterliegt einer Wärmefreisetzung , die in diesem Fall zur Zersetzung von CuCl auf den Komponenten und zum Schmelzen von NaCl führt Schmelztemperatur von NaCl - 800 °C, Siedetemperatur - 1465 °C [17] zur Bildung von CuCl2 mit Freisetzung von Cu bei 500 °C [18] und bei Temperaturerhöhung über 500 °C, CuCl2 in seinem Fall zersetzt sich CuCl und Cl mit anschließender Verflüchtigung von Cl. Das heißt, die Kristallisation von ZnS erfährt aus der Schmelze des NaCl- und ZnS-Gemischs. Solche Prozesse beim Transport in Fest-Flüssig-Systemen werden als Mineralisierung bezeichnet [1, 19].
Somit erfolgt die Bildung von ZnS-Partikeln mit unterschiedlichen Größen parallel. Große ZnS-Partikel werden in der Schmelze oder in der NaCl-Umgebung gebildet. Der Transport von Kupfer durch die flüssige Phase von NaCl ist aufgrund seiner geringen Löslichkeit schwierig [20], außerdem erfolgt die Zersetzung von CuCl nicht auf einmal, und dies verringert auch die Geschwindigkeit der Cu-Einführung in ZnS.
Die Bildung kleiner Partikel findet höchstwahrscheinlich in der Gasphase von Zn und S statt. In diesem Fall ist das Auftreten der CuS-Phase mit geringer Wahrscheinlichkeit, da für ihre Bildung eine größere Menge erforderlich ist, wenn Wärme erforderlich ist [20]. Nach der Bildung befinden sich kleine Partikel in Nachbarschaft mit Cu- und großen ZnS-Partikeln. Da die Größe kleiner Partikel der Größe der Raumladungszone (SCR) in ZnS entspricht, befinden sich die Partikel im Bereich der Ladungsträgerverarmung. Dies liegt daran, dass bei einer Verringerung der Partikelgröße auf einen Wert kleiner als der doppelte Wert der Siebtiefe (L ) erfolgt das Aufbringen von SCR, das entlang einer Partikeloberfläche lokalisiert ist, auf dem SCR der gegenüberliegenden Oberfläche. Die gegenseitige Überlappung von SCR-Oberflächen führt zu einer Verringerung der Breite zwischen Fermi-Niveau E F und Spitze des Valenzbandes E V [21]. Folglich Konzentration der Hauptladungsträger in Partikeln der Größe r 2 L fällt niedrig aus, oder anders ausgedrückt, Partikel befindet sich in der Verarmungszone. In diesem Fall ist, wie in [3] erwähnt, ein Phasenübergang erster Ordnung, begleitet von einer abrupten Änderung des chemischen Potentialwerts und anderer thermodynamischer Materialparameter, thermodynamisch günstig, wenn das Verunreinigungsband mehr als die Hälfte gefüllt ist. Im umgekehrten Fall wird der Übergang vom Anstieg des Fermi-Niveaus während des Erhitzens begleitet, was der negativen Prozessentropie entspricht, d nicht weniger als die Hälfte und in Regionen, die von Transportunternehmen erschöpft sind. Mit anderen Worten, das Absinken des Fermi-Niveaus und sein Eintritt in die Zone der Verunreinigungsniveaus führt zu deren Entleerung, die für das Material thermodynamisch ungünstig ist. Folglich wird die Einführung von Kupfer als Donorverunreinigung in ZnS, wo Kupfer eine Zwischengitterposition einnimmt, thermodynamisch günstig für das Material. Möglicherweise hat dies zu einer so hohen Kupferkonzentration in den Partikeln der kleinen Fraktion geführt. Auch für eine eindeutigere Interpretation der erhaltenen Ergebnisse sind die zusätzlichen Untersuchungen notwendig.
Somit zeigen die präsentierten Ergebnisse, dass die SHS-Methode es ermöglicht, Materialien mit ZnS-Partikelgrößen in einem weiten Bereich zu erhalten – von Mikro- bis Nanogrößen. Darüber hinaus ermöglicht die Wahl des Syntheseregimes, des Flussmittels und seiner Mischungsmenge eine selektive Dotierung von Partikeln in Abhängigkeit von ihrer Größe.
Schlussfolgerungen
Die durchgeführten Untersuchungen von ZnS:Cu, das mit der SHS-Methode unter Zugabe von NaCl als Flussmittel erhalten wurde, haben gezeigt, dass die Einführung von NaCl eine Erhöhung der Feinfraktion (50–500 nm) im Material ermöglicht. EDS-Daten haben gezeigt, dass die Konzentration von Cu in Fraktionen unterschiedlich ist. Die Cu-Konzentration in Fraktionen mit Partikelgrößen zwischen 50–500 nm beträgt ~2 Gew.%, und in Partikeln mit Größen von ~10 μm und mehr wurde das Vorhandensein von Cu nicht nachgewiesen. Somit ermöglicht die Auswahl der Syntheseregime, des Flussmittels und seiner Ladungsmenge bei Verwendung des SHS-Verfahrens eine selektive Dotierung von Partikeln in Abhängigkeit von ihrer Größe zu realisieren. Die erhaltenen Ergebnisse werden im Rahmen des Verunreinigungsmodells «retrograde Löslichkeit» in Mehrkomponentenmaterialien gut erklärt.
Abkürzungen
- CuCl :
-
Kupferchlorid
- NaCl :
-
Natriumchlorid
- SHS :
-
Selbstpropagierende Hochtemperatursynthese
- ZnS :
-
Kuh ZnS dotiert mit Cu
- ZnS :
-
Cu–SHS -ZnS:Cu erhalten durch SHS-Methode
- ZnS :
-
Zinksulfid
Nanomaterialien
- Eine Einführung in die Teile einer Schraube
- Auf dem Gebiet der Prozessanlagen mit Ethernet
- Einführung in die Terahertz-Band
- Eine Einführung in den Harzinfusionsprozess
- Funktionsweise des CMC-Prozesses
- Was gehört zum Herstellungsprozess?
- Ein Blick in den Bewertungsprozess für Gebrauchtgeräte:So funktioniert er
- Was ist der Seifenherstellungsprozess?
- Einführung in das Edelstahl-Feingussverfahren
- Straffung des Prozesses



