Antibabypille
Hintergrund
Orale Kontrazeptiva oder Antibabypillen wurden von mehr als 60 Millionen Frauen weltweit verwendet und werden von vielen als der gesellschaftlich bedeutendste medizinische Fortschritt des 20. Jahrhunderts angesehen. Die Antibabypille ist eine Tablette, die eine Frau täglich einnimmt, um eine Schwangerschaft zu verhindern. Die Antibabypille bewirkt dies, indem sie die Entwicklung der Eizelle im Eierstock der Frau während ihres monatlichen Menstruationszyklus hemmt. Während des Menstruationszyklus einer Frau veranlasst ein niedriger Östrogenspiegel normalerweise die Hypophyse, ein Hormon auszusenden, das die Entwicklung einer Eizelle einleitet. Die Antibabypille setzt genügend synthetisches Östrogen frei, um zu verhindern, dass dieses Hormon während des monatlichen Zyklus freigesetzt wird. Die Antibabypille enthält auch ein zweites synthetisches Hormon, Gestagen, das die Dicke des Zervixschleims erhöht und die Entwicklung der Gebärmutterschleimhaut verhindert, um eine Schwangerschaft weiter zu verhindern. Studien haben gezeigt, dass die Antibabypille zu 99% eine Schwangerschaft verhindert. Die Ergebnisse der Studien zur Sicherheit der Verhütungsmittel variieren. Einige Studien zeigen, dass seine Anwendung das Risiko für bestimmte Krebsarten erhöht, während andere zeigen, dass dieses Risiko minimal ist. Es gibt auch Behauptungen, dass die Antibabypille das Risiko für Schlaganfälle und Herzinfarkte erhöht.
Verlauf
Die Planned Parenthood Federation of America beauftragte Dr. Gregory Pincus und Dr. John Rock 1950 mit der Entwicklung einer einfachen und zuverlässigen Verhütungsmethode. In den nächsten Jahren arbeiteten die Ärzte an der Formulierung einer Antibabypille bei der Worcester Foundation for Experimental Biology in Massachusetts. Sie testeten ihre Erfindung an 6.000 Frauen in Puerto Rico und Haiti. Die Erfindung wurde dann 1960 in den USA als Enovid-10 vermarktet.
Viele führen den Wandel der sozialen Landschaft in den Vereinigten Staaten während der 1960er Jahre auf die weit verbreitete Akzeptanz und Anwendung der Antibabypille zurück. Als sexuelle Beziehungen außerhalb der Ehe und aus anderen Gründen als der Geburt von Kindern gesellschaftlich akzeptierter wurden und Frauen, die eine Karriere anstrebten, nach Methoden der Familienplanung suchten, war das Umfeld reif für die Einführung dieser diskreten, einfach anzuwendenden Form der Verhütung.
Trotz ihrer Popularität begann die Öffentlichkeit kurz nach der Einführung der Antibabypille Bedenken hinsichtlich Nebenwirkungen und Sicherheit zu äußern. Bereits 1961 kursierten Berichte, wonach die Antibabypille das Risiko für einen Schlaganfall oder Herzinfarkt bei Frauen durch Blutgerinnung erhöht. 1965 stellte die Federal Food and Drug Administration (FDA) einen Wissenschaftler der Johns Hopkins School of Hygiene and Public Health zur Verfügung, um die Nebenwirkungen der Antibabypille zu untersuchen. Die Agentur richtete auch einen beratenden Ausschuss für Geburtshilfe und Gynäkologie ein, um den Zusammenhang zwischen oralen Kontrazeptiva und der Blutgerinnung zu untersuchen sowie zu untersuchen, ob die Antibabypille das Risiko für Brust-, Gebärmutterhals- oder Endometriumkrebs erhöht. Das Komitee, das erste von der FDA eingerichtete Beratungsgremium, berichtete 1966, dass es keine Beweise dafür gefunden habe, dass die Antibabypille für den Menschen unsicher wäre.
Unzufrieden forderte die FDA eine größere Studie über die Auswirkungen der Antibabypille auf die Blutgerinnung. Die Agentur stellte außerdem fest, 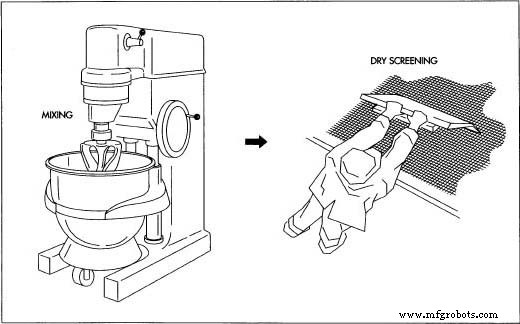 In einem so genannten Nassgranulationsverfahren werden die Wirkstoffe mit einem Verdünnungsmittel und ein Sprengmittel in einem großen Mixer. Nach dem Mischen wird die Pulvermasse durch ein Maschensieb gedrückt. jedoch, dass die Antibabypille nicht lange genug verwendet wurde, um eine Studie über ihren Zusammenhang mit Krebs zu beobachten. Gleichzeitig hat die Weltgesundheitsorganisation (WHO) auch festgestellt, dass die Auswirkungen der Antibabypille auf die Blutgerinnung eine Studie rechtfertigen. 1968 zeigte eine britische Studie eine Zunahme von Blutgerinnseln bei Frauen, die orale Kontrazeptiva einnahmen. Die FDA verlangte, dass Packungen mit Antibabypillen Warnhinweise enthalten. Im Jahr 1969 kam die Agentur zu dem Schluss, dass die Östrogenmenge die Blutgerinnung beeinflusst und dass Antibabypillen mit niedrigeren Östrogendosen genauso wirksam waren wie ihre östrogenreichen Gegenstücke. Die Agentur begann, Ärzten zu raten, ihren Patienten die niedrigstmögliche Östrogendosis zu verschreiben.
In einem so genannten Nassgranulationsverfahren werden die Wirkstoffe mit einem Verdünnungsmittel und ein Sprengmittel in einem großen Mixer. Nach dem Mischen wird die Pulvermasse durch ein Maschensieb gedrückt. jedoch, dass die Antibabypille nicht lange genug verwendet wurde, um eine Studie über ihren Zusammenhang mit Krebs zu beobachten. Gleichzeitig hat die Weltgesundheitsorganisation (WHO) auch festgestellt, dass die Auswirkungen der Antibabypille auf die Blutgerinnung eine Studie rechtfertigen. 1968 zeigte eine britische Studie eine Zunahme von Blutgerinnseln bei Frauen, die orale Kontrazeptiva einnahmen. Die FDA verlangte, dass Packungen mit Antibabypillen Warnhinweise enthalten. Im Jahr 1969 kam die Agentur zu dem Schluss, dass die Östrogenmenge die Blutgerinnung beeinflusst und dass Antibabypillen mit niedrigeren Östrogendosen genauso wirksam waren wie ihre östrogenreichen Gegenstücke. Die Agentur begann, Ärzten zu raten, ihren Patienten die niedrigstmögliche Östrogendosis zu verschreiben.
In den frühen 1970er Jahren wurde ein orales Kontrazeptivum eingeführt, das nur Gestagen enthält. Diese Form des oralen Kontrazeptivums, auch Minipille genannt, verhinderte eine Schwangerschaft allein durch Veränderungen der Gebärmutter und des Gebärmutterhalses. Es wurde eine Eizelle produziert, aber die durch die Minipille verursachten Veränderungen machten es der Eizelle schwierig, sich mit den Spermien des Mannes zu vereinigen. Während die Minipille die von Östrogen ausgehenden Risiken eliminiert, hat sie sich bei der Schwangerschaftsverhütung als weniger wirksam erwiesen als östrogenhaltige Pillen. In den 1970er Jahren wurden Pillen auf den Markt gebracht, die durchweg niedrigere Östrogendosen enthielten.
1982 wurde eine zweiphasige Antibabypille eingeführt, gefolgt von einer dreiphasigen Pille im Jahr 1984. Diese niedrig dosierten Pillen enthielten unterschiedliche Verhältnisse von Gestagen zu Östrogen. 1988 nahmen alle drei Pharmaunternehmen, die noch immer hochdosierte Antibabypillen herstellten, auf Antrag der FDA ihre hochdosierten Produkte vom Markt. Bis 1990 wurde die Östrogenmenge in der Antibabypille um mindestens zwei Drittel reduziert. Studien zeigen, dass das Risiko einer Blutgerinnung bei Frauen, die die Antibabypille einnehmen, entsprechend abgenommen hat. Weitere Studien haben gezeigt, dass hochdosierte Antibabypillen tatsächlich das Risiko einer Frau für Eierstock- und Endometriumkrebs, gutartige Zysten der Eierstöcke und Brüste sowie entzündliche Erkrankungen des Beckens senken. Das Risiko für Brust- oder Gebärmutterhalskrebs ist noch umstritten.
Die Pille ist für bestimmte Gruppen von Frauen, einschließlich Raucherinnen, immer noch unsicher; sind fettleibig; eine Vorgeschichte von gesundheitlichen Problemen haben 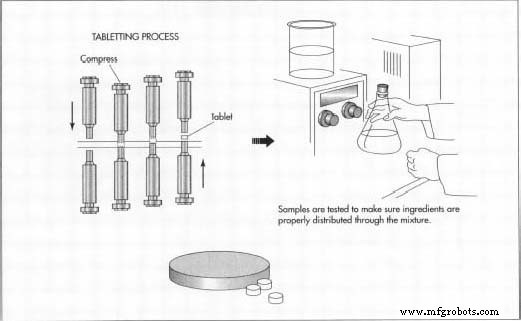 Nach dem Test wird die Mischung in Tablettenform geformt und verpackt. wie Diabetes, Bluthochdruck oder hoher Cholesterinspiegel; oder wenn Sie in der Vorgeschichte Blutgerinnsel, Herzinfarkt, Schlaganfall, Lebererkrankungen, Brustkrebs oder Krebs der Fortpflanzungsorgane haben.
Nach dem Test wird die Mischung in Tablettenform geformt und verpackt. wie Diabetes, Bluthochdruck oder hoher Cholesterinspiegel; oder wenn Sie in der Vorgeschichte Blutgerinnsel, Herzinfarkt, Schlaganfall, Lebererkrankungen, Brustkrebs oder Krebs der Fortpflanzungsorgane haben.
Die Antibabypille kann nicht nur eine Schwangerschaft verhindern, sondern auch die Symptome des prämenstruellen Syndroms lindern. Es gibt heute mindestens 30 Sorten von Antibabypillen auf dem Markt.
Rvaw-Materialien
Die Hauptbestandteile der Antibabypille sind Pulver, die synthetische Versionen der Hormone Östrogen und Gestagen enthalten.
Der Herstellungsprozess
Prozess
- In einem Verfahren, das als Nassgranulation bekannt ist, werden die Wirkstoffe – die Pulver, die synthetische Versionen von Östrogen und Gestagen enthalten – zusammen mit einem Verdünnungsmittel und einem Sprengmittel (Produkte, die die Pulver verdünnen und sie in Flüssigkeit auflösen) gemischt. in einem großen Mixer, der dem Mixmaster ähnelt, der in vielen Küchen zu finden ist. Für größere Chargen kann ein sogenannter Doppelschalenmischer verwendet werden.
- Bindemittelhaltige Lösungen (das Material, das den Inhalt der Tablette zusammenhält) werden in die Pulvermasse eingerührt, die angefeuchtet wird, bis sie die Konsistenz von braunem Zucker annimmt.
- Die Pulvermasse (bekannt als Nassgranulation) wird durch ein Maschensieb gepresst.
- Das feuchte Material wird dann auf flache, mit großen Papierblättern bedeckte Schalen gelegt und in Trockenschränke gestellt.
- Ein Schmiermittel in Form eines feinen Pulvers wird auf das getrocknete Material gesiebt (sogenannte Trockengranulation).
- Das Schmiermittel und das Trockengranulat werden dann in einem Mischer unter Verwendung einer Drehbewegung gemischt.
- Tabletten werden aus der Mischung geformt, typischerweise unter Verwendung einer Methode, die als Direktverpressung bekannt ist. Direktverpressung verwendet Stahlstempel und -matrizen in großen Maschinen, die Tabletten direkt aus der pulverförmigen Mischung pressen. Die physikalische Zusammensetzung der pulverförmigen Mischung wird in keiner Weise verändert. Das Stanz- und Matrizensystem ist oft computergesteuert.
- Die Tabletten werden auf Einhaltung der Bundesvorschriften geprüft und für den Versand an Apotheken verpackt.
Qualitätskontrolle
Wie Medikamente unterliegen auch die Antibabypillen den strengen Vorschriften der FDA. Die Herstellung von Antibabypillen erfolgt in einer hochsterilen Umgebung und während des gesamten Produktionsprozesses werden Proben genommen, um sicherzustellen, dass jede Tablettencharge den Bundesvorschriften entspricht. Zu den untersuchten Faktoren gehören Gewicht, Färbung und andere kosmetische Bedenken. Viele computergestützte Tablet-Maschinen können Gewichtsinformationen bereitstellen. Auch die Tablettenstanz- und Matrizensysteme werden regelmäßig überprüft. Darüber hinaus wird die Umgebung, in der die Tabletten hergestellt werden, streng kontrolliert, um das Eindringen von Verunreinigungen zu vermeiden.
Die Zukunft
Eine relativ neue Innovation im Bereich der Geburtenkontrolle ist die Einführung von Norplant, einem Verhütungsmittel, das nach dem gleichen Konzept der Pille funktioniert, jedoch unter die Haut des Oberarms eingeführt wird und jeweils die richtige Dosierung in das Körpersystem freisetzt Tag. Eine weitere Innovation, die in den Vereinigten Staaten neu ist, obwohl sie in Europa verwendet wurde, ist RU486, eine Art der Empfängnisverhütung, die nach dem Geschlechtsverkehr eingenommen werden kann, um eine Schwangerschaft zu verhindern.
Herstellungsprozess



