Künstliche Haut
Hintergrund
Die Haut, das größte Organ des menschlichen Körpers, schützt den Körper vor Krankheiten und körperlichen Schäden und hilft, die Körpertemperatur zu regulieren. Es besteht aus zwei Hauptschichten, der Epidermis und der Dermis. Die Epidermis oder äußere Schicht besteht hauptsächlich aus Zellen:Keratinozyten, Melanozyten und Langerhans. Die Dermis, die hauptsächlich aus Bindegewebsfasern wie Kollagen besteht, versorgt die Epidermis mit Nährstoffen.
Wenn die Haut durch Krankheiten oder Verbrennungen ernsthaft geschädigt wurde, kann der Körper nicht schnell genug handeln, um die notwendigen Ersatzzellen herzustellen. Wunden, wie zum Beispiel Hautgeschwüre bei Diabetikern, heilen möglicherweise nicht und Gliedmaßen müssen amputiert werden. Verbrennungsopfer können an Infektionen und Plasmaverlust sterben. Hauttransplantate wurden entwickelt, um solche Folgen zu verhindern und Missbildungen zu korrigieren. Bereits im 6. Jahrhundert
Bis zum Ende des 20. Jahrhunderts wurden Hauttransplantate aus Patientenhaut (Autotransplantate) oder Leichenhaut (Allotransplantate) hergestellt. An erster Stelle standen Infektionen oder im Fall von Kadaverhaut Abstoßung. Während Hauttransplantate von einem Körperteil eines Patienten zu einem anderen immun gegen Abstoßung sind, werden Hauttransplantate von einem Spender zu einem Empfänger aggressiver abgestoßen als jedes andere Gewebetransplantat oder Transplantat. Obwohl die Haut von Kadavern während der anfänglichen Heilungsphase eines Verbrennungsopfers Schutz vor Infektionen und Flüssigkeitsverlust bieten kann, ist häufig eine anschließende Transplantation der eigenen Haut des Patienten erforderlich. Der Arzt ist auf die Haut des Patienten beschränkt, ein entscheidender Nachteil bei schweren Verbrennungsopfern.
Mitte der 1980er Jahre schlossen sich Medizinforscher und Chemieingenieure aus den Bereichen Zellbiologie und Kunststoffherstellung zusammen, um Tissue Engineering zu entwickeln, um das Auftreten von Infektionen und Abstoßungen zu reduzieren. Einer der Katalysatoren für das Tissue Engineering war der wachsende Mangel an verfügbaren Organen für Transplantationen. Im Jahr 1984 teilte Joseph Vacanti, ein Chirurg der Harvard Medical School, seine Frustration über den Mangel an verfügbaren Lebern mit seinem Kollegen Robert Langer, einem Chemieingenieur am Massachusetts Institute of Technology. Gemeinsam überlegten sie, ob im Labor neue Organe gezüchtet werden könnten. Der erste Schritt bestand darin, die körpereigene Gewebeproduktion zu duplizieren. Langer hatte die Idee, ein biologisch abbaubares Gerüst zu konstruieren, auf dem Hautzellen mit Fibroblasten gezüchtet werden könnten, Zellen, die aus gespendeten neonatalen Vorhäuten gewonnen wurden, die während der Beschneidung entfernt wurden.
In einer von anderen Forschern entwickelten Variante dieser Technik werden die extrahierten Fibroblasten zu Kollagen hinzugefügt, einem faserigen Protein, das im Bindegewebe vorkommt. Wenn die Verbindung erhitzt wird, geliert das Kollagen und fängt die Fibroblasten ein, die sich wiederum um das Kollagen herum anordnen und kompakt, dicht und faserig werden. Nach einigen Wochen werden Keratinozyten, die ebenfalls aus der gespendeten Vorhaut gewonnen werden, auf das neue Hautgewebe ausgesät, wo sie eine epidermale Schicht bilden.
Ein künstliches Hauttransplantat bietet mehrere Vorteile gegenüber denen, die vom Patienten und Kadavern stammen. Es macht Gewebe überflüssig 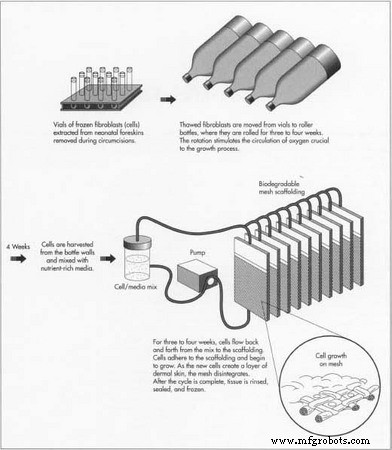 eingeben. Künstliche Haut kann in großen Mengen hergestellt und für die Lagerung und den Versand eingefroren werden, um sie bei Bedarf zur Verfügung zu stellen. Jede Kultur wird auf Krankheitserreger untersucht, wodurch die Wahrscheinlichkeit einer Infektion stark eingeschränkt wird. Da künstliche Haut keine immunogenen Zellen wie dendritische Zellen und kapillare Endothelzellen enthält, wird sie vom Körper nicht abgestoßen. Schließlich wird die Rehabilitationszeit deutlich verkürzt.
eingeben. Künstliche Haut kann in großen Mengen hergestellt und für die Lagerung und den Versand eingefroren werden, um sie bei Bedarf zur Verfügung zu stellen. Jede Kultur wird auf Krankheitserreger untersucht, wodurch die Wahrscheinlichkeit einer Infektion stark eingeschränkt wird. Da künstliche Haut keine immunogenen Zellen wie dendritische Zellen und kapillare Endothelzellen enthält, wird sie vom Körper nicht abgestoßen. Schließlich wird die Rehabilitationszeit deutlich verkürzt.
Rohstoffe
Die zur Herstellung von künstlicher Haut benötigten Rohstoffe fallen in zwei Kategorien, die biologischen Komponenten und die notwendige Laborausstattung. Der größte Teil des gespendeten Hautgewebes stammt von neonatalen Vorhäuten, die während der Beschneidung entfernt wurden. Eine Vorhaut kann genug Zellen ergeben, um vier Hektar Transplantatmaterial herzustellen. Fibroblasten werden von der Hautschicht des gespendeten Gewebes getrennt. Die Fibroblasten werden unter Quarantäne gestellt, während sie auf Viren und andere infektiöse Krankheitserreger wie IIV, Hepatitis B und C und Mykoplasmen getestet werden. Die Krankengeschichte der Mutter wird aufgezeichnet. Die Fibroblasten werden in Glasfläschchen gelagert und in flüssigem Stickstoff bei –94 °F (–70 °C) eingefroren. Die Fläschchen werden gefroren gehalten, bis die Fibroblasten zum Züchten von Kulturen benötigt werden. Bei der Kollagenmethode werden auch Keratinozyten aus der Vorhaut extrahiert, getestet und eingefroren.
Wenn die Fibroblasten auf Netzgerüsten gezüchtet werden sollen, entsteht ein Polymer durch die Kombination von Milchsäure- und Glykolsäuremolekülen, den gleichen Elementen, die zur Herstellung von auflösenden Nähten verwendet werden. Die Verbindung durchläuft eine chemische Reaktion, die zu einem größeren Molekül führt, das aus sich wiederholenden Struktureinheiten besteht.
Bei der Kollagenmethode wird eine kleine Menge Rinderkollagen aus der Strecksehne junger Kälber extrahiert. Das Kollagen wird mit einem sauren Nährstoff vermischt und in einem Kühlschrank bei 39,2 °F (4 °C) gelagert.
Die Laborausrüstung umfasst Glasfläschchen, Schläuche, Rollflaschen, Pfropfkartuschen, Formen und Gefrierschränke.
Der Herstellungsprozess
Prozess
Der Herstellungsprozess ist täuschend einfach. Seine Hauptfunktion besteht darin, die extrahierten Fibroblasten vorzutäuschen, dass sie sich im menschlichen Körper befinden, damit sie auf natürliche Weise miteinander kommunizieren, um neue Haut zu bilden.
Gittergerüstmethode
- 1 Fibroblasten werden aufgetaut und expandiert. Die Fibroblasten werden aus den Fläschchen in Rollflaschen überführt, die Liter-Soda-Flaschen ähneln. Die Flaschen werden drei bis vier Wochen lang auf die Seite gedreht. Die Rollbewegung ermöglicht die Zirkulation von Sauerstoff, der für den Wachstumsprozess unerlässlich ist.
- 2 Zellen werden in ein Kultursystem überführt. Die Zellen werden aus den Rollflaschen entnommen, mit einem nährstoffreichen Medium kombiniert, durch Röhrchen in dünne, kassettenartige Bioreaktoren geleitet, in denen das biologisch abbaubare Netzgerüst untergebracht ist, und mit Elektronenstrahlen sterilisiert. Wenn die Zellen in die Kassetten fließen, haften sie am Netz und beginnen zu wachsen. Die Zellen werden drei bis vier Wochen lang hin und her geströmt. Jeden Tag wird übrig gebliebene Zellsuspension entfernt und frische Nährstoffe werden hinzugefügt. Sauerstoff, pH, Nährstofffluss und Temperatur werden durch das Kultursystem gesteuert. Wenn die neuen Zellen eine Hautschicht bilden, zerfällt das Polymer.
- 3 Wachstumszyklus abgeschlossen. Wenn das Zellwachstum auf dem Netz abgeschlossen ist, wird das Gewebe mit nährstoffreicheren Medien gespült. Ein Kryoschutzmittel wird hinzugefügt. Kassetten werden einzeln gelagert, etikettiert und eingefroren.
Collagen-Methode
- 4 Zellen werden in ein Kultursystem überführt. Eine kleine Menge des kalten Kollagens und Nährmediums, ungefähr 12% der kombinierten Lösung, wird den Fibroblasten zugesetzt. Die Mischung wird in Formen abgefüllt und auf Raumtemperatur kommen gelassen. Wenn sich das Kollagen erwärmt, geliert es, fängt die Fibroblasten ein und erzeugt das Wachstum neuer Hautzellen.
- 5 Keratinozyten hinzugefügt. Zwei Wochen nachdem das Kollagen zu den Fibroblasten hinzugefügt wurde, werden die extrahierten Keratinozyten aufgetaut und auf die neue dermale Haut ausgesät. Sie werden mehrere Tage lang wachsen gelassen und dann der Luft ausgesetzt, wodurch die Keratinozyten zur Bildung von Epidermisschichten angeregt werden.
- 6 Wachstumszyklus abgeschlossen. Die neue Haut wird in sterilen Behältern aufbewahrt, bis sie gebraucht wird.
Die Zukunft
Die Mediziner setzen auf die Technologie der künstlichen Haut als Vorreiter bei der Organrekonstruktion. Es ist zu hoffen, dass dieses sogenannte Engineered Structural Tissue eines Tages beispielsweise Kunststoff- und Metallprothesen ersetzen wird, die derzeit als Ersatz für geschädigte Gelenke und Knochen verwendet werden. Ohren und Nasen werden rekonstruiert, indem Knorpelzellen auf Polymergewebe ausgesät werden. Die Regeneration von Brust- und Harnröhrengewebe wird derzeit im Labor untersucht. Durch diese Technologie ist es möglich, dass eines Tages Leber, Nieren und sogar Herzen aus menschlichem Gewebe gezüchtet werden.
Herstellungsprozess



