Selbstdotierter hochporöser Kohlenstoff mit hohem Graphitgehalt für die Elektrokatalyse von Sauerstoffreduktionsreaktionen
Zusammenfassung
Die großtechnische Produktion von aktiven und stabilen porösen Kohlenstoffkatalysatoren für die Sauerstoffreduktionsreaktion (ORR) aus proteinreicher Biomasse wurde zu einem heißen Thema in der Brennstoffzellentechnologie. Hier berichten wir über eine einfache Strategie zur Synthese stickstoffdotierter poröser Nanokohlenstoffe durch einen einfachen zweistufigen Pyrolyseprozess in Kombination mit der Aktivierung von Zinkchlorid und einem Säurebehandlungsprozess, bei dem vorzugsweise Kidneybohne durch Niedertemperaturkarbonisierung verwendet wurde als einzige Kohlenstoff-Stickstoff-Quelle. Die Ergebnisse zeigen, dass dieses Kohlenstoffmaterial eine ausgezeichnete elektrokatalytische ORR-Aktivität sowie eine höhere Haltbarkeit und Methanol-Toleranz im Vergleich zu den Pt/C-Katalysatoren des Standes der Technik für die ORR aufweist, was hauptsächlich auf den hohen Graphit-Stickstoff-Gehalt zurückzuführen ist , hohe spezifische Oberfläche und poröse Eigenschaften. Unsere Ergebnisse können die Synthese von Hochleistungs-ORR-Elektrokatalysatoren auf Kohlenstoffbasis fördern, die aus weit verbreiteter natürlicher Biomasse gewonnen werden.
Hintergrund
Platin (Pt)-basierte Materialien, die hochmodernen Katalysatoren für Brennstoffzellen, leiden unter hohen Preisen, begrenzten Ressourcen, unzureichender Haltbarkeit und Methanol-toleranten Eigenschaften im Elektrokatalyseprozess der Sauerstoffreduktionsreaktion (ORR) [1] . Zu diesem Zweck wurden in letzter Zeit große Anstrengungen unternommen, um nach hochaktiven, langlebigen und kostengünstigen Alternativen zu Pt-basierten ORR-Elektrokatalysatoren zu suchen [2]. Unter den verschiedenen Nicht-Pt-Katalysatoren sind heteroatomdotierte poröse Kohlenstoffe (HDPC) eine neue Art von metallfreien Katalysatoren mit hoher Aktivität und Haltbarkeit für die ORR dank ihrer geringen Kosten, Ungiftigkeit und Erneuerbarkeit [3,4, 5,6], und daher werden die eingehenden Untersuchungen bis heute mit Spannung erwartet. HDPC wird im Allgemeinen durch chemische Methoden oder natürliche Template synthetisiert, sie können jedoch die Anforderungen an kostengünstige, einfache Synthese und hervorragende Leistung nicht erfüllen [7, 8]. Daher ist die Suche nach einer vernünftigen und effektiven Methode zur Synthese des HDPC-Materials immer noch ein bedeutendes wissenschaftliches Thema, um eine hocheffiziente Katalyse zur Sauerstoffreduktion zu realisieren.
Wie bereits berichtet, proteinangereicherte Biomasse (z. B. Nori [9], Süßkartoffelrebe [10], Pomeloschale [11], Enoki-Pilz [12], Coprinus comatus [13] und Lemna minor [14]) kann in großem Umfang als Single-Source-Vorstufe für HDPC-Katalysatoren für die ORR verwendet werden. Wir schlagen kürzlich eine Strategie vor, um den HDPC-Katalysator mit poröser 3D-Netzwerkstruktur durch Hochtemperatur-Karbonisierung von Bioabfällen aus Fischschuppen mit einem Aktivator aus Zinkchlorid zu bilden [6]. Interessanterweise stellen wir fest, dass die Vorbehandlung von Biomasse im ersten Schritt nicht nur dazu beitragen kann, die Eigenschaften der Kohlenstoffstruktur des endgültigen ORR-Katalysators zu verbessern, sondern auch seinen Oberflächenstickstoffgehalt und die Dotierungseffizienz von Stickstoffatomen in die Kohlenstoffstruktur erhöht. Basierend auf diesem Ergebnis berichten wir hier zunächst über eine Strategie zur Herstellung von stark mit Graphit-Stickstoff dotiertem porösem Kohlenstoff (KB350Z-900) durch direkte Umwandlung von Biomasse aus weißen Kidneybohnen (KB) mit einem Prozess der zweistufigen Karbonisierung, gefolgt von Zinkchlorid Aktivierungs- und Säurebehandlungsverfahren. Die KB-Biomasse, die heute zu den bekanntesten Speisebohnen zählt, kann in verschiedenen Ländern reichlich und günstig gewonnen werden. Der Gesamtgehalt an biologischem Protein in dehydratisierter KB-Biomasse beträgt im Allgemeinen 20–30%. Nach unserem besten Wissen wird selten über die ORR-Aktivität des dotierten Kohlenstoffkatalysators berichtet, der aus KB-Biomasse gewonnen wird. Die Rolle von ZnCl2 im Aktivierungsprozess kann hauptsächlich die schnelle Dehydratisierung und katalytische Dehydroxylierung von KB-Biomasse anregen, so dass der Wasserstoff und Sauerstoff innerhalb der KB-Biomasse unter Bildung von Wasserdampf freigesetzt werden. Dieser Prozess kann die Bildung von mehr Mikro-/Meso-Poren erleichtern und schließlich mit Stickstoff selbstdotierte Kohlenstoffmaterialien mit hoher Porosität erzeugen. Der erhaltene Katalysator auf Kohlenstoffbasis weist eine hohe elektrokatalytische Aktivität, Langzeitbeständigkeit und Methanoltoleranz auf, was eine vielversprechende Alternative zum Katalysator auf Pt-Basis für die ORR im alkalischen Medium sein könnte.
Methoden
Zuerst wurde weiße Kidneybohne (KB) mit entionisiertem Wasser gewaschen und bei 80 °C in einem Vakuumtrockenschrank vollständig getrocknet. Anschließend wurde KB im Fließ-N2 . vorbehandelt Atmosphäre bei 350 °C für 2 h zur effektiven Zersetzung des Proteins zum KB350-Vorläufer. Die schnellste Zersetzung der weißen KB-Biomasse erfolgt zwar bei etwa 300 °C (Zusatzdatei 1:Abbildung S1), jedoch wurde eine Temperatur von 350 °C als Karbonisierungstemperatur im ersten Schritt gewählt, um die Zersetzungstemperatur von Tyrosin (344 .) zu überschreiten °C), die höchste unter den Aminosäuren in Bioprotein. KB350 und Zinkchlorid (ZnCl2 ) wurden durch Kugelmahlen bei 500 U/min im Massenverhältnis 1:1 mechanisch gemischt. Die erhaltene Mischung wurde in einem Röhrenofen bei verschiedenen Temperaturen (700, 800, 900 oder 1000 °C) 2 h lang mit einer Heizrate von 10 °C min − 1 . pyrolysiert . Der produzierte Nanokohlenstoff wird im Folgenden KB350Z-X genannt (X = 700, 800, 900 oder 1000). Als Kontrolle wurde KB-Z-900 auf ähnliche Weise durch Pyrolyse einer mechanischen Mischung aus KB und ZnCl2 . hergestellt bei gleichem Massenverhältnis. Die direkte Pyrolyse von KB bei 900 °C für 2 h wurde verwendet, um KB900 herzustellen. Alle vorbereiteten Proben wurden in 0,5 mol l − 1 . weiter nachbehandelt HCl-Lösung für 2 h. Das Ziel der Säureauslaugung besteht darin, Zn-Spezies und metallische Verunreinigungen vor dem elektrochemischen Testen effektiv zu entfernen.
Die Daten der Raman-Spektroskopie wurden mit einem Renishaw inVia-Gerät mit einem angeregten λ von 514,5 nm getestet. Feldemissions-Rasterelektronenmikroskopie-(FE-SEM)-Bilder wurden von Hitachi UHR S4800 (Japan) erhalten. Hochauflösende Transmissionselektronenmikroskopie (HR-TEM) wurde auf dem FEI Tecnai F30-Instrument durchgeführt und die Beschleunigungsspannung beträgt 300 kV. Röntgenphotoelektronenspektroskopie (XPS) wurde unter Verwendung eines Kratos XSAM800 Spektrometers durchgeführt. Ein Micromeritics Analyzer (ASAP 2010) wurde verwendet, um N2 . zu messen Adsorptions-/Desorptionsisothermen bei 77 K.
Elektrochemische Messungen wurden an einer Zennium-E-Workstation (Deutschland) mit einem herkömmlichen Drei-Elektroden-System durchgeführt. Als Arbeitselektrode, Referenzelektrode, bzw. Hilfselektrode. Die Herstellung von Arbeitselektroden bezieht sich auf unsere früheren Berichte [6]. Im Allgemeinen 5,0 μl von 10 mg ml − 1 Dispersion wurde auf die GC-RDE-Oberfläche übertragen und natürlich getrocknet. Die Massenbeladung aller getesteten Proben wurde auf ~ 400 μg cm − 2 . eingestellt . Alle Potentiale (gegen SCE) wurden in die Potentiale gegen die reversible Wasserstoffelektrode (RHE) umgewandelt.
Ergebnisse und Diskussion
Wir haben zuerst die Raman-Spektren von KB900-, KB-Z-900- und KB350Z-900-Katalysatoren getestet, um ihre Unterschiede in den strukturellen Eigenschaften zu verstehen. Die Raman-Spektren sind in Abb. 1a dargestellt. Das Intensitätsverhältnis (ID /IG ) von „D“-Band zu „G“-Band wurde verwendet, um die ungeordneten und graphitischen Grade zu charakterisieren. Das ID /IG ist 0,85 nur für KB350Z-900, aber das ID /IG ist 0,94 für KB900 bzw. 0,88 für KB-Z-900. Es könnte zeigen, dass mit KB350Z-900 im Vergleich zu Katalysatoren auf Stickstoff/Kohlenstoff-Basis (NC) wie hergestellt ein höherer Graphitgrad erzielt werden kann, was direkt durch Vergleich der Raman-Intensität bestätigt werden kann. Außerdem ist die Verwendung von ZnCl2 Aktivator bei der Synthese von NC-basierten Katalysatoren kann die Erhöhung des Graphitgrades während des Pyrolyseprozesses aufgrund eines niedrigsten ID . erleichtern /IG Verhältnis von KB350Z-900. Die Vorbehandlung von KB im ersten Schritt bei 350 °C kann den Graphitgrad von NC-basierten Katalysatoren weiter verbessern, was dazu beitragen kann, mehr mit Graphit und Stickstoff dotierte Kohlenstoffstrukturen herzustellen. N2 Adsorptions-Desorptions-Isothermen wurden verwendet, um die Wirkung von ZnCl2 . zu untersuchen Aktivator und Vorbehandlung im ersten Schritt auf die spezifische Oberfläche und Porenverteilung von NC-basierten Katalysatoren. Abbildung 1b zeigt deutlich eine Langmuir-IV-Isothermenkurve mit einer Hystereseschleife vom Typ H2, was zeigt, dass die mesoporösen Strukturen auch in den hergestellten Katalysatoren enthalten sind (z. B. KB-Z-900 und KB350Z-900). Die BET-spezifische Oberfläche beträgt etwa 380 m 2 g − 1 für KB-Z-900 und 1132 m 2 g − 1 für KB350Z-900 bzw. Ein höheres Gesamtporenvolumen von KB350Z-900 beträgt ~ 0,62 m 3 g − 1 , und die Meso- und Makroporenfläche von KB350Z-900 beträgt ~ 664 m 2 g − 1 (Einschub in Abb. 1b). Die Vorbehandlung von KB im ersten Schritt bei 350 °C kann die Bildung von mehr Meso- und Makroporen und die Erhöhung der spezifischen BET-Oberfläche fördern, was die Freilegung aktiver Zentren und die Diffusion von Sauerstoffmolekülen während des elektrochemischen Tests weiter ermöglicht. Transmissionselektronenmikroskopie(TEM)-Bilder (Abb. 1c, d) bestätigen auch, dass in KB350Z-900 eine große Anzahl von Mikro-/Makroporen und amorphen Kohlenstoffstrukturen beobachtet werden können. Bezeichnenderweise bilden sich aufgrund eines höheren Anteils an N-Dotierung defekte und exponierte Kanten in der Kohlenstoff-Nanostruktur, die auch effektiv reaktive Stellen für die ORR bieten sollen [15].
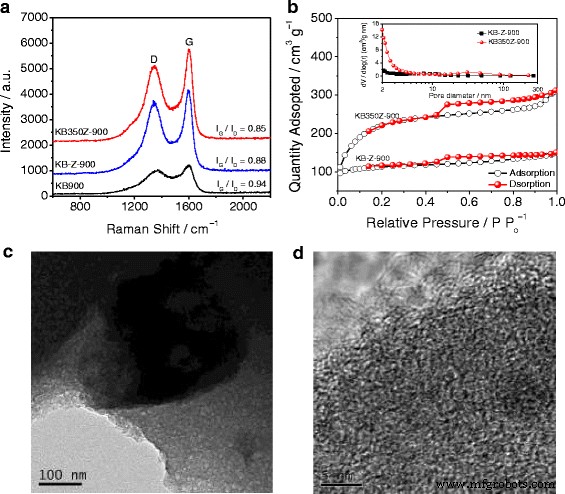
a Raman-Spektren von KB900, KB-Z-900 und KB350Z-900. b Stickstoffadsorptions-Desorptions-Isothermen und entsprechende BJH-Porengrößenverteilungen (Einschub) von KB-Z-900 und KB350Z-900. c Niedrige Auflösung und d hochauflösende Transmissionselektronenmikroskopie-Bilder von KB350Z-900
Abbildung 2a, b zeigen, dass die Stickstoffatome erfolgreich in die Kohlenstoffstruktur von drei Arten von ORR-Katalysatoren dotiert werden. Der Oberflächenstickstoffgehalt aus der XPS-Analyse beträgt 1,23, 1,92 bzw. 2,70 Atom-% für KB-900, KB-Z-900 bzw. KB350Z-900. Es zeigt an, dass der Stickstoffverlust durch die Aktivierung von ZnCl2 . verringert werden kann und zweistufiger Karbonisierungsprozess [6]. Die XPS-Spektren von N1 von KB-900 und KB-Z-900 können an drei Peaks angepasst werden (siehe Zusatzdatei 1:Abbildung S2), die Pyridin-N, Graphit-N und oxidiertem-N zugeschrieben werden können [6, 7,8, 12, 13]. Das XPS-Spektrum von N1 von KB350Z-900 kann jedoch nur in zwei Peaks eingepasst werden (siehe Zusätzliche Datei 1:Abbildung S2), zentriert bei 398,5 und 401,1 eV, die Pyridin-N bzw. Graphit-N zugeordnet werden können. Insbesondere wird die oxidierte N-Spezies im XPS-Spektrum von N1 von KB350Z-900 nicht beobachtet, und der Prozentsatz der graphitischen N-Spezies beträgt bis zu 88,8 Atom-% des Gesamtstickstoffgehalts. Der Gehalt an Graphit-N-Spezies folgt der Reihenfolge KB350Z-900 > KB-Z-900 > KB-900, was bedeutet, dass ZnCl2 Der Aktivierungsprozess kann einfach sein, um die Erhöhung des Graphit-N-Gehalts im NC-Material zu erleichtern, und die Verwendung der KB350-Vorstufe, die aus der Vorbehandlung des KB-Materials im ersten Schritt stammt, kann die Bildung von oxidierten N-Spezies effektiv reduzieren.
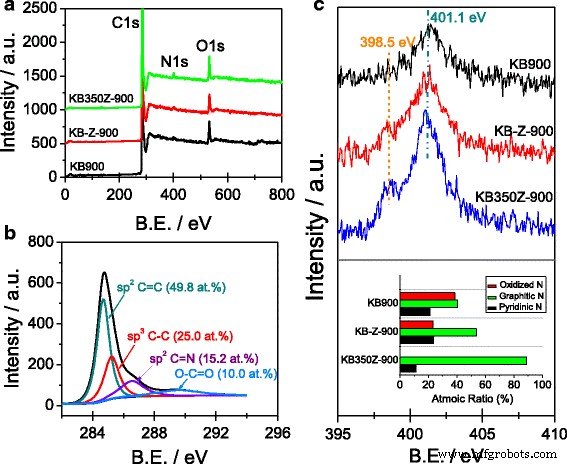
a XPS-Umfrage von KB900, KB-Z-900 und KB350Z-900; b C1s XPS-Spektrum von KB350Z-900; c N1 s XPS-Spektren von KB900, KB-Z-900 und KB350Z-900
CV-Kurven (siehe Abb. 3a), erhalten in N2 im Vergleich zu O2 gesättigte KOH-Lösungen zeigen, dass KB350Z-900 die höchste ORR-Spitzenstromdichte und das positivste Spitzenpotential (0,90 V) im Vergleich zu KB-Z-900 und KB-900 aufweist, was auf den hohen Gehalt an Graphit-N-Spezies zurückzuführen sein kann im Inneren des Katalysators [13, 16]. Darüber hinaus erhaltene LSV-Kurven (Abb. 3b) in O2 gesättigte KOH-Lösung weisen ferner darauf hin, dass sich das ORR-Halbwellenpotential und die begrenzte Stromdichte von KB350Z-900 denen des erstklassigen 20 Gew.-% Pt/C-Katalysators annähern. Die Tafel-Methode wurde verwendet, um die Strompotentialkurven (j-E) im kinetischen Bereich zu analysieren. Die ORR-Stromdichte ist im Potenzialbereich von 0,8–1,0 V (vs. RHE) nahezu unabhängig von der Elektrodenrotationsrate, was darauf hindeutet, dass die Stromdichte in diesem Bereich mit niedrigem Überpotenzial von der elektrochemischen kinetischen Stromdichte dominiert wird. Die Tafel-Plots von E als Funktion von log (j) sind in (Zusatzdatei 1:Abbildung S3) dargestellt. Eine Tafel-Steigung von 143 mV Dekade − 1 wird für KB350Z-900 erhalten. Die Abweichung der Tafel-Steigungen sowohl für KB350Z-900 als auch für Pt/C-Katalysatoren impliziert, dass ihre intermediäre Adsorption einem anderen Modell folgen könnte [17]. Höhere Tafel-Steigungen (absoluter Wert) entsprechen einem schnellen Anstieg des Überpotentials mit der Stromdichte, was wahrscheinlich zu einer relativ geringeren katalytischen Aktivität der ORR führt [18]. Die elektrokatalytische ORR-Aktivität von KB350Z-900 kann jedoch im Vergleich zu den zuvor berichteten kohlenstoffbasierten Katalysatoren, die aus anderer Biomasse oder Biomaterial stammen, besser sein [9,10,11,12,13,14]. Die Untersuchung des Temperatureffekts der Pyrolyse auf NC-Katalysatoren über das ZnCl2 Aktivierung zeigt auch, dass die ORR-Aktivität der Reihenfolge KB350Z-900 > KB350Z-800 > KB350Z-1000 > KB350Z-700 folgt, was auf die beste elektrokatalytische Aktivität von KB350Z-900 hinweist, da höhere oder niedrigere Temperaturen die ORR-Aktivität verschlechtern. im alkalischen Medium [19]. Es kann hauptsächlich auf einen wichtigen Grund zurückgeführt werden, dass eine hohe Porosität und spezifische Oberfläche sowie ein hoher Oberflächen-N-Gehalt und ein hoher Prozentsatz an N-Spezies von KB350Z-900 den schnellen Transport von O2 . erleichtern können -Molekül und die Freilegung zugänglicher aktiver Zentren [6], die dazu beitragen können, die elektrokatalytische Aktivität gegenüber der ORR zu erhöhen.
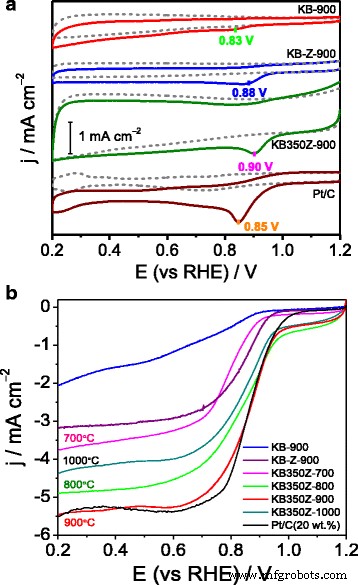
a CV-Kurven von KB900, KB-Z-900 und KB350Z-900 in N2 im Vergleich zu O2 gesättigte KOH-Lösung; b LSV-Kurven der hergestellten Katalysatoren und JM Pt/C-Katalysator
Darüber hinaus sind in Abb. 4a, b LSV-Kurven für ORR von KB-Z-900 und KB350Z-900 bei unterschiedlichen Drehzahlen (400–3600 U/min) dargestellt. Die gute Linearität der Koutecky-Levich-Plots (Abb. 4c) weist auf die ORR-Kinetik erster Ordnung in Bezug auf gelöstes O2 . hin Konzentration. Die durchschnittliche Elektronentransferzahl (n) der ORR auf KB-Z-900 und KB350Z-900 wird gemäß der Koutecky-Levich-Gleichung auf ~ 3,93 bzw. ~ 3,98 (Einschub in Abb. 4c) geschätzt ]. Die Koutecky-Levich-Gleichung lautet wie folgt:
$$ 1/{j}_d=1/{j}_k+1/B{\omega}^{1/2} $$ $$ \mathrm{B}=0,62\mathrm{nF}{\mathrm{C }}_{\mathrm{O}}{\mathrm{D}}_{\mathrm{O}}^{2/3}{\nu}^{-1/6}{\upomega}^{1/ 2} $$wo F ist die Faraday-Konstante, C O ist die O2 Sättigungskonzentration im Elektrolyten, D O ist die O2 Diffusionskoeffizient im Elektrolyten, ν die kinetische Viskosität des Elektrolyten ist und ω die Elektrodenrotationsgeschwindigkeit ist und 0,62 eine Konstante ist, wenn die Rotationsrate in U/min ausgedrückt wird. Es deutet darauf hin, dass der ORR-Prozess auf KB-Z-900 und KB350Z-900 hauptsächlich einem direkten Vier-Elektronen-Transfer-Pfad zur Herstellung von H2 . folgt O (z. B. O2 + 2 H2 O + 4e − → 4 OH − ), die der durch einen Pt/C-Katalysator katalysierten ORR sehr ähnlich ist [21].
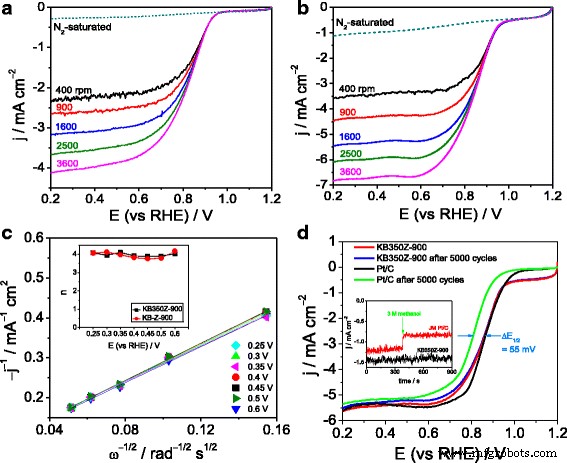
a LSV-Kurven von KB-Z-900 in N2 im Vergleich zu O2 gesättigte KOH-Lösung bei unterschiedlichen Rotationsgeschwindigkeiten; b LSV-Kurven von KB350Z-900 in N2 im Vergleich zu O2 gesättigte KOH-Lösung bei unterschiedlichen Rotationsgeschwindigkeiten; c Koutecky-Levich-Plots von jd − 1 gegen ω − 1/2 erhalten von (b ) bei den angegebenen Potentialen (0,25–0,6 V). Einschub ist die Auftragung von n gegen das Potenzial, die aus (a ) und (b ); d LSV-Kurven von KB350Z-900 und JM Pt/C vor und nach CV für 5000 Zyklen in O2 gesättigte KOH-Lösung; Einschub:amperometrische i-t-Kurven bei 0,9 V gegen RHE für Tests auf Methanoltoleranz
Hier verwenden wir den beschleunigten Alterungstest (AAT) durch kontinuierliches CV-Scannen für 5000 Zyklen in einem Potenzialbereich von 0,2 bis 1,2 V gegenüber RHE, um die elektrochemische Stabilität von KB350Z-900 und Pt/C-Katalysator in einem O2 zu bewerten -gesättigter KOH-Elektrolyt. Nach dem CV-Test ist das Halbwellenpotential der ORR an der KB350Z-900-katalysierten Elektrode nur um 2 mV negativ verschoben, aber das reduzierte Halbwellenpotential der ORR an der JM Pt/C-katalysierten Elektrode beträgt etwa 55 mV (Abb. 4d). Darüber hinaus wird auch für den Pt/C-Katalysator eine höhere Verschlechterung der begrenzten Stromdichte festgestellt, was auf eine bessere elektrokatalytische Stabilität von KB350Z-900 gegenüber der ORR hinweist. Amperometrische i-t-Kurven bei 0,9 V in O2 -gesättigter KOH-Elektrolyt (Einschub in Abb. 4d) bestätigen, dass die Elektrooxidationsreaktion von 3 M Methanol bei KB350Z-900 kaum auftritt, was auf eine gute methanoltolerante Leistung von KB350Z-900 und die vielversprechenden Anwendungen in Alkali-Methanol-Brennstoffzellen hindeutet.
Schlussfolgerungen
Hier entwickeln wir ein einfaches und einfaches Verfahren zur großtechnischen Herstellung von hochporösen Kohlenstoffen, die mit stark graphitischem Stickstoff dotiert sind, aus der zweistufigen Pyrolyse von Kidneybohnen-Biomasse in Kombination mit der Aktivierung von Zinkchlorid und einem Säurebehandlungsprozess, der als Elektrokatalysator zur Sauerstoffreduktion im alkalischen Medium. Zuerst stellen wir fest, dass eine große BET-Oberfläche (~ 1132 m 2 g − 1 ) ist erhältlich bei KB350Z-900 mit einem hohen Porenvolumen von ~ 0,62 m 3 g − 1 . Zweitens kann ein zweistufiger Pyrolyseprozess mit Zinkchlorid-Aktivierung dazu beitragen, den Gehalt an graphitischem Stickstoff im Inneren des kohlenstoffbasierten Katalysators signifikant zu erhöhen. Wir beobachten auch, dass die katalytische ORR-Aktivität dieses Kohlenstoffmaterials mit der des modernen kommerziellen 20 Gew.-%-Pt/C-Katalysators, aber auch der Elektrokatalysestabilität des ersteren gegenüber der ORR und der methanoltoleranten Leistung, gut vergleichbar ist. besser sind, was auf vielversprechende Anwendungen in alkalischen Brennstoffzellen hindeutet. Die hervorragende ORR-Leistung von KB350Z-900 ist hauptsächlich auf den hohen Gehalt an graphitischem Stickstoff, die hohe spezifische Oberfläche und die porösen Eigenschaften zurückzuführen. Unsere Ergebnisse können die großtechnische Produktion von hochaktiven und stabilen kohlenstoffbasierten ORR-Elektrokatalysatoren aus weit verbreiteter natürlicher Biomasse weiter fördern.
Nanomaterialien
- IBM-Wissenschaftler erfinden ein Thermometer für die Nanoskala
- Kohlenstoff-Nanoröhren erweitern die Grenzen der flexiblen Elektronik
- Ozeankohlenstoff auf atomarer Skala
- Wie die Luft- und Raumfahrtindustrie Kohlefaser für ihre Bedürfnisse nutzt
- 5 Tipps zum Finden des besten Herstellers von Kohlefaserteilen
- Das Design der Emissionsschicht für Elektronenvervielfacher
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Sauerstoffreduktionsreaktion auf PtCo-Nanokatalysator:(Bi)Sulfat-Anionenvergiftung
- Hochaktive und stabile Fe-N-C-Sauerstoffreduktions-Elektrokatalysatoren aus Elektrospinnen und In-situ-Pyrolyse
- Einfache Herstellung von Kohlenstoff-Nanoröhrchen-Cu2O-Nanokompositen als neue Katalysatormaterialien für die Reduktion von P-Nitrophenol



