In-situ-Herstellung von Aktivkohle aus Desmostachya bipinnata aus Bioabfällen zur Verbesserung der Superkondensatorleistung
Zusammenfassung
Hier demonstrieren wir die Herstellung von hochkapazitiver Aktivkohle (AC) unter Verwendung eines Bioabfall-Kushagrases (Desmostachya bipinnata ), indem ein chemischer Prozess gefolgt von einer Aktivierung durch KOH verwendet wird. Die so synthetisierte mehrschichtige Aktivkohle wurde durch Röntgenpulverbeugung, Transmissionselektronenmikroskopie und Raman-Spektroskopietechniken bestätigt. Die chemische Umgebung der vorbereiteten Probe wurde durch FTIR- und UV-Vis-Spektroskopie untersucht. Die Oberfläche und Porosität des so synthetisierten Materials wurden durch die Brunauer-Emmett-Teller-Methode ermittelt. Alle elektrochemischen Messungen wurden mittels zyklischer Voltammetrie und galvanometrischer Lade-/Entladungsmethode (GCD) durchgeführt, aber aufgrund der Genauigkeit der Technik konzentrieren wir uns hauptsächlich auf GCD. Darüber hinaus zeigt das AC-Material wie synthetisiert eine maximale spezifische Kapazität von 218 F g –1 . im Potenzialfenster von − 0,35 bis + 0,45 V. Außerdem weist der Wechselstrom eine ausgezeichnete Energiedichte von ~ 19,3 Wh kg −1 . auf und Leistungsdichte von ~ 277.92 W kg −1 , jeweils im gleichen Betriebspotentialfenster. Es hat auch eine sehr gute Kapazitätserhaltungsfähigkeit selbst nach 5000. Zyklen gezeigt. Der hergestellte Superkondensator zeigt eine gute Energiedichte bzw. Leistungsdichte und eine gute Kapazitätserhaltung bei bemerkenswert höheren Lade-/Entladeraten mit ausgezeichneter Zyklenstabilität. Künftig ist Aktivkohle aus Bioabfällen aus Kusha-Gras (DP-AC) vielversprechend und kann aufgrund seiner hervorragenden elektrochemischen Eigenschaften in Superkondensatoranwendungen eingesetzt werden. Hier stellen wir uns vor, dass unsere Ergebnisse einen einfachen und innovativen Ansatz zur Synthese von Aktivkohle aus Bioabfall aus Kusha-Gras (DP-AC) als aufkommendes Superkondensator-Elektrodenmaterial veranschaulichen und seine praktische Anwendung in Bereichen der elektrochemischen Energiespeicherung erweitern.
Einführung
In den letzten Jahren wurde der Entwicklung vielversprechender nachhaltiger Energiespeichermodelle, die Umwandlungs- und Speichergeräte umfassen, viel Aufmerksamkeit gewidmet, um den globalen Energiebedürfnissen gerecht zu werden [1,2,3]. Energiespeicher wie Batterien und Superkondensatoren spielen eine sehr wichtige, effiziente und erschwingliche Rolle bei der Erzeugung erneuerbarer und nachhaltiger Energiequellen und sind praktikable Alternativen zu herkömmlichen nicht erneuerbaren Optionen. Superkondensatoren haben sich aufgrund ihrer langen Lebensdauer, der hohen Leistungsdichte und der ultraschnellen Lade-/Entladezeit als vielversprechendste nachhaltige Energiespeichergeräte erwiesen [4,5,6,7,8]. Darüber hinaus wurde aufgrund des aufstrebenden Forschungsgebiets von kohlenstoffbasierten Nanomaterialien wie Graphen, Nanotubes, Nanodots und Quantendots auch die intensive Entwicklung von Superkondensator-Energiespeichern verstärkt [9,10,11]. Studien zeigen, dass sich viele Forschungsarbeiten auf die Synthese von Materialien und ihren Verbundwerkstoffen mit anderen Hybriden konzentriert haben, die eine hohe Kapazität, ein breites Potenzialfenster, eine geringere Impedanz und eine gute kapazitive Rückhaltung aufweisen [12]. Auch die Herstellung von Elektroden hat mit hoher Massenbeladung von aktiviertem Material und Masse-zu-Strom-Kollektor-Verhältnis große Aufmerksamkeit auf sich gezogen [13, 14].
Superkondensatoren auf Basis von Kohlenstoffmaterialien wurden umfassend untersucht und bieten breite Potenzialfenster, die zu einer hohen Energiedichte in Gegenwart organischer Elektrolyte führen [15, 16]. Daher weisen Superkondensatoren auf Kohlenstoffbasis einen hohen Widerstand und eine niedrige Kapazität auf. Organische Elektrolyte sind jedoch giftig, brennbar und vergleichsweise teuer [15]. Kohlenstoffnanoröhren, Graphen usw. sind in gewissem Maße exorbitant in Bezug auf die Methoden zur Herstellung und Verfügbarkeit von Urmaterialien und beschränken ihre großtechnischen Anwendungen. Daher wurden Forschungen durchgeführt, die sich mit mehreren Änderungen für verschiedene Kohlenstoffmaterialien befassten, um das potenzielle Fenster, die Superkapazitätsleistung und eine geringere Impedanz mit einer umweltfreundlichen, kostengünstigen und einfach anzuwendenden Methode zu erhöhen [17, 18].
Aktivkohle mit hoher Oberfläche, reichlich funktionellen Assoziaten und ausreichender Porosität wurde in den letzten Jahrzehnten in großem Umfang für Adsorption, Gasspeicherung, Gastrennung, Katalysatorträger, Lösungsmittelentfärbung, Lösungsmittelrückgewinnung, Elektroden und Superkondensatoren verwendet. Seine poröse Struktur und andere Eigenschaften wie hohe Oberfläche, Porenvolumen, Anwesenheit verschiedener Arten von funktionellen Gruppen und Verteilung der Porengrößen spielen eine entscheidende Rolle bei den absorbtionsbezogenen Anwendungen der Aktivkohle [18]. Abhängig von der Porengröße kann Aktivkohle in unterschiedlichen Anwendungsgebieten eingesetzt werden, beispielsweise werden Mikroporen bei der Adsorption kleinerer Moleküle verwendet, während Mesoporen in großem Umfang bei der Adsorption größerer Moleküle verwendet werden [19, 20].
Viele Faktoren beeinflussen die Eigenschaften der Aktivkohle wie Rohstoffe, Syntheseweg, Aktivierungsreagenz und Umgebungsbedingungen während des Aktivierungsprozesses. AC wird synthetisiert, indem verschiedene Syntheserouten und Vorstufen angenommen werden, die als Bioabfall/natürlich verfügbar sind, wie Kokosnussschalen [21], Neem [22], Maisstärke [23], recyceltes Altpapier [24], Altreifen [25], und Bananenfasern [26]. AC wird hauptsächlich durch physikalische und chemische Aktivierungsprozesse synthetisiert [19]. Normalerweise beinhaltet die erste hauptsächlich die Karbonisierung und die weitere Aktivierung in einer inerten Atmosphäre oder die Anwesenheit von Gas wie CO2 oder Oxidationsmittel [27], wobei der chemische Aktivierungsprozess zunächst die Entwicklung der porösen Strukturen durch Zugabe von Aktivierungsmitteln wie ZnCl2 . beinhaltet , NaOH, H3 PO4 , und KOH [12, 28, 29, 30]. Studien zufolge ist ZnCl2 ist aufgrund von Umweltbedenken und inkompetenter Erholung kein sehr bevorzugter Wirkstoff. Daher wird die durch ZnCl2 . aktivierte AC für pharmazeutische und agro-lebensmittelindustrielle Zwecke nicht geeignet, da sie die Ergebnisse wahrscheinlich verunreinigen [20]. Unter anderen chemischen Reagenzien ist KOH weit verbreitet, da es zu ACs mit großer Oberfläche und gut definierten Poren führt. González et al. berichteten über die KOH-Aktivierung von Kirschkernen, die zu mikroporösen ACs mit großen Kapazitäten führt [31]. Yushinet al. synthetisierten die ACs auf Holzsägemehlbasis durch hydrothermale Karbonisierung, gefolgt von einer Aktivierung aus KOH, und untersuchten ihre Superkondensatorleistung [32]. Ranganathanet al. illustrierte die Synthese von ACs aus Altpapier unter Verwendung von KOH als Aktivierungsmittel. Es weist eine spezifische Kapazität von 180 F g −1 . auf im KOH-Elektrolyt [24]. Er et al. verwendeten eine schnelle Mikrowellenerhitzungstechnik, um ACs aus Koksen zu synthetisieren, und untersuchten das KOH-Koks-Massenverhältnis und die Aktivierungszeit [33]. Die Aktivierungsmittel spielen während des Prozesses eine entscheidende Rolle, wie Dehydratisierungsmittel verhindern das Fortschreiten mehrerer Zwischenprodukte. Es erhöht auch die Dichte poröser Strukturen und reduziert die Aktivierungszeit sowie die Temperatur [24, 34, 35].
In der vorliegenden Arbeit wird Kushagras (Desmostachya bipinnata ) wurde als umweltfreundlicher, kostengünstiger und zahlreicher kohlenstoffhaltiger Vorläufer für die Synthese von Aktivkohle verwendet. Um AC zu synthetisieren, wurde aufgrund seiner besseren Zuverlässigkeit ein chemischer Prozess mit KOH als Aktivierungsmittel verwendet. Das so synthetisierte AC-Material wurde durch UV-sichtbares, Fourier-Transform-Infrarot- und Raman-Spektroskopie charakterisiert. Um auf die Validierung der Strukturmerkmale zuzugreifen, wurde das synthetisierte Material außerdem durch Rasterelektronenmikroskopie (REM), energiedispersive Spektroskopie (EDAX), TEM und XRD-Techniken charakterisiert. Für den Anwendungszweck wurden elektrochemische und galvanometrische Ladungstechniken angewendet, indem eine geringfügige Modifikation der Elektrode mit einem Drei-Elektroden-System durchgeführt wurde. Aufgrund der Zuverlässigkeit der GC-Technik wurde sie für andere Berechnungen wie Superkapazität, Energiedichte und Stromdichte verwendet. Es zeigt, dass hergestelltes AC aufgrund wohldefinierter poröser Merkmale ausgezeichnete Superkapazitätseigenschaften aufweist. Fortan ist diese Studie die erste ihrer Art, die sich mit der Herstellung von hochkapazitiver Aktivkohle (AC) unter Verwendung eines Bioabfall-Kushagrases (Desmostachya bipinnata ).
Methoden
Materialien
Kusha-Gras (Desmostachya bipinnata; DP) wurde aus dem Botanischen Garten des BHU Campus, Varanasi, Indien, gesammelt, während Kaliumhydroxid (KOH), Glaskohlenstoffelektrode (GCE) und Aluminiumoxidpulver von Sigma-Aldrich bezogen wurden. Wässrige Lösungen, die in allen Experimenten verwendet wurden, wurden unter Verwendung von entionisiertem Wasser hergestellt (DI > 18 MΩ cm −1 , Millipore Q-System).
Zur Charakterisierung der so synthetisierten Proben wurden verschiedene analytische Techniken eingesetzt. Um auf die strukturellen Merkmale und kristallinen Eigenschaften der Aktivkohle im synthetisierten Zustand zuzugreifen, wurde eine Pulver-Röntgenbeugung auf einem PANalytical-Röntgendiffraktometer unter Verwendung von CuKα . durchgeführt Strahlung (λ = 1,540 Å) bei 2θ ~ 10°–80°. Die Mikrostrukturen und Oberflächenmorphologien des synthetisierten Materials wurden mit einem Transmissionselektronenmikroskop (TEM, TECHNAI G 2 betrieben bei 200 kV) und einem Rasterelektronenmikroskop (Dual FIB:FEI Nanolab betrieben bei 200 kV). Eine TEM-Probe wurde hergestellt durch Tropfengießen einer Suspension von DP-AC-Pulver über ein kohlenstoffbeschichtetes Gitter, gefolgt von einer Ultraschallsuspension in DI-Wasser. Darüber hinaus wurden einige zusätzliche strukturelle Merkmale der Aktivkohle im synthetisierten Zustand durch Raman-Spektroskopie bestätigt. Die Messung der Raman-Streuung wurde mit einer 532-nm-He-Ne-Laseranregung unter Verwendung eines Raman-Spektrometers (Renishaw in Via, UK) durchgeführt. Darüber hinaus wurde das Fourier-Transform-Infrarot-(FTIR)-Spektrometer (Bruker ALPHA II) verwendet, um das Vorhandensein der funktionellen Gruppen zu untersuchen, die an die so hergestellte Probe gebunden sind. Die optischen Eigenschaften wurden durch UV-sichtbares Licht-Absorptionsspektroskopie, aufgenommen durch Leuchtstofflampen (λ = 365 nm) (PerkinElmer, Lambda 25). Die Oberfläche und die Porengrößenverteilung der so hergestellten Aktivkohleprobe wurden durch Verwendung einer Flüssigstickstoff-Adsorptions-/Desorptionsanalyse nach einer automatischen Brunauer-Emmett-Teller (BET)-Methode (micromeritics FlowPrer 060, Gemini VII, USA) gemessen.
Synthese von Aktivkohle
Kurz gesagt, Kusha-Gras (DP) wurde geschnitten und mehrmals vorsichtig mit entionisiertem Wasser gewaschen, bis sich herausstellte, dass der Überstand farblos war. DP wurde 5 h in einem Ofen bei 100 °C gehalten und weitere 2 h in einem Muffelofen bei 700 °C karbonisiert. Zur Aktivierung wurde es in bewährtem KOH (w/w 1:4) mit Hilfe von Mörser-Pistill angemischt und anschließend die homogene Mischung gesammelt. Weiter wurde es in einem Röhrenofen bei 700 °C für 2 h in Argonatmosphäre gehalten. Die Mischung wurde weiter auf Raumtemperatur abgekühlt und die erhaltene Mischung wurde mehrmals mit DI-Wasser gewaschen, bis der pH-Wert einen Wert von ~ 7 erreichte. Schließlich erhielten wir das Produkt als Aktivkohle und bewahrten es für weitere Experimente in einem Gefäß auf und Messungen. Der Gesamtprozess ist in Abb. 1 dargestellt.
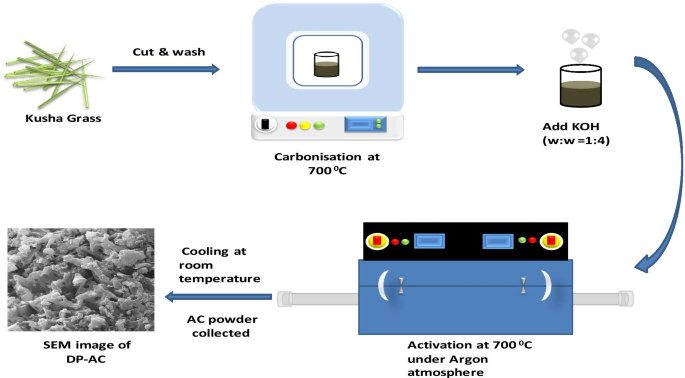
Illustration des strategischen Weges zur Synthese von Aktivkohle aus Kusha-Gras (Desmostachya bipinnata )
Elektrodenvorbereitung
Eine Glaskohlenstoffelektrode (GCE) mit einem Durchmesser von ~ 0,3 cm wurde mit einer Aluminiumoxidaufschlämmung (0,05 μm) poliert. Im nächsten Schritt wurde DI-Wasser zur Reinigung der Oberfläche des GCE verwendet. Es wurde 3–4 Mal mit DI-Wasser gewaschen und weitere 15–20 Minuten in DI-Wasser und Ethanol beschallt. Für die Abscheidung von AC wurde 1 mg aktives Material (AC) in DI-Wasser (1 ml) gelöst und 15 min beschallt. Darüber hinaus wurden 10 μL der vorbereiteten Lösung mit Hilfe einer Mikropipette über GCE gegossen und im Lampenlicht ohne Kontakt in der Nähe getrocknet, um eine Kontamination zu verhindern.
Elektrochemische Tests
Elektrochemische Experimente wurden an der Mehrkanal-Workstation CHI-660C mit einem Drei-Elektroden-System unter Verwendung von pt-Draht, Ag/AgCl und einer Glaskohlenstoffelektrode als Gegen-, Referenz- bzw. Arbeitselektrode durchgeführt. Zur Durchführung der Messungen wurde ein alkalischer wässriger 6 M KOH-Elektrolyt verwendet. Zyklische Voltammetrie bei verschiedenen Abtastraten (10–200 mV s −1 ) wurde mit dem Sweep-Potentialfenster von − 0,35 V bis + 0,45 V durchgeführt. Auf die verschiedenen elektrochemischen Parameter wurde mit den folgenden Gleichungen zugegriffen [35,36,37].
Die spezifische Kapazität wurde bewertet als
$$C_{{\text{s}}} =\frac{{I_{{{\text{Durchschnitt}}}} }}{\nu \times m}$$ (1)wobei \(I_{{{\text{Avg}}}}} =I_{\max} - I_{\min}\) und auch m und ν repräsentieren die Masse des Ladematerials (g) bzw. die Scanrate (v/s). Außerdem C s hat eine Einheit von F g −1 .
Da die galvanometrische Ladungs-Entladungs-Technik (GCD) zuverlässiger ist und genauere Ergebnisse liefert, haben wir die GCD-Technik für weitere Berechnungen übernommen. Wir haben die spezifische Kapazität mit der Gleichung berechnet
$$C_{{\text{s}}} =\frac{{I \times\Updelta t}}{{\Updelta V\times m}}$$ (2)wo ich , ∆t , ∆V , und m repräsentieren den Strom (A ), Entladezeit (s ), Spannungsfenster (V ) und Masse des Ladematerials (g ) bzw.
Außerdem ist die Energiedichte (E ) und Leistungsdichte (P ) wurden durch die Gleichungen abgeleitet
$$E =\frac{{c_{{\text{s}}} { } \times\Delta V^{{2{ }}} }}{7.2}\quad { }\left( {\text{Wh /kg}} \right)$$ (3) $$P =\frac{E \times 3600 }{{\Delta t}} \quad \left( {{\text{W}}/{\text{kg }}} \right).$$ (4)Ergebnisse und Diskussion
Röntgenbeugung
Um auf Informationen bezüglich der Graphitisierung von Aktivkohlematerial im synthetisierten Zustand zuzugreifen, wurde die XRD-Technik verwendet. Das XRD-Profil (Abb. 2a) zeigt deutlich die charakteristischen Peaks von Aktivkohlematerial bei 22° und 43° [38, 39]. Die Intensität und Position der Peaks zeigen den geringen Graphitisierungsgrad, die Regelmäßigkeiten der kristallinen Struktur und die Bildung von K2 CO3 (2θ = 36,52°) als Zwischenprodukt [40,41,42]. Außerdem können die erhaltenen charakteristischen Peaks den Reflexionsebenen (002) und (100) für den DP-AC zugeordnet werden. Der breite Peak im Spektrum legt den amorphen Kohlenstoff fest, während die Schärfe des bei 22° zugeordneten Peaks die erhöhte Translationsordnung in der Kohlenstoffprobe bei hoher Temperatur zeigt. Diese Ergebnisse bestätigen die erfolgreiche Bildung von wie synthetisiertem AC-Material.
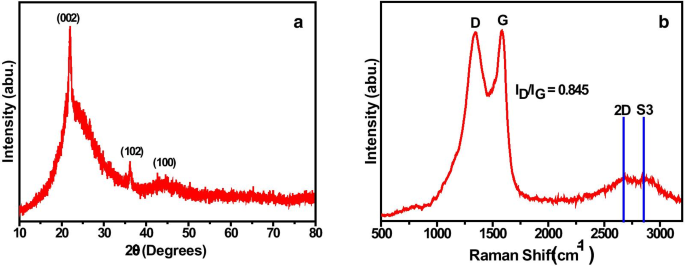
a XRD-Muster und b Raman-Spektrum von Aktivkohle wie synthetisiert
Raman-Analyse
Darüber hinaus wurde das Material durch Raman-Spektroskopie charakterisiert, eine am deutlichsten ausgeprägte Technik zur Charakterisierung verschiedener kohlenstoffhaltiger Materialien. Im Raman-Spektrum von Aktivkohlematerial werden zwei intensivste Peaks beobachtet, die bei 1346 cm −1 . positioniert sind (D-Peak) und 1587 cm −1 (G-Peak) wie in Abb. 2b gezeigt. Der D-Peak ist das Merkmal von Gitterfehlern, Kantenfehlern, ungepflegter Ausrichtung und niedrigsymmetrischer graphitischer Struktur in Aktivkohlematerial [43], und der zweite Peak, dh der G-Peak, zeigt das Auftreten von C=C-Streckschwingungen [ 10]. Außerdem zeigt es zwei weitere Bänder bei höheren Wellenzahlen 2678 cm −1 (2D) und 2840 cm −1 (S3) aufgrund des Obertons von Kohlenstoff und zeigt das Vorhandensein von wenig geschichtetem Kohlenstoffmaterial und die graphitische Natur von Aktivkohlematerial [44].
Außerdem wurde der Graphitisierungsgrad durch die Gleichung berechnet
$$R =\frac{{I_{{\text{D}}} }}{{I_{{\text{G}}} }}$$ (6)wo R , ich D, und ich G stellen den Graphitisierungsgrad dar, die Intensität des D-Peaks bei 1346 cm −1 , und die Intensität des G-Peaks bei 1587 cm −1 , bzw. Nach der Berechnung wird der Wert von R hat sich zu ~ 0.84 herausgestellt, was auf einen höheren Graphitisierungsindex in gewissem Maße hinweist [10].
Morphologische Charakterisierung und energiedispersive Röntgenanalyse (EDX)
Um die mikrostrukturellen Merkmale und die Oberflächenmorphologie des synthetisierten Materials zu untersuchen, wurden rasterelektronenmikroskopische (REM) Bilder wie in Abb. 3a, b gezeigt analysiert. Die Morphologie weist auf das Vorhandensein großer unregelmäßiger Poren in dem so synthetisierten DP-AC hin. Das Auftreten unregelmäßiger und ungeordneter Porenstrukturen auf der Oberfläche erklärt den heftigen Angriff des Reagenz KOH. Während der Pyrolyse entwickelte DP-AC-Poren sind entscheidend, um die Oberfläche und das Porenvolumen der Aktivkohle zu erhöhen, indem sie die Diffusion von KOH-Molekülen in die Poren fördern und dadurch die Kohlenstoffreaktion erhöhen, die hier als zusätzliche Poren in der AC angenommen wird. Die großporige Struktur auf der Oberfläche des Aktivkohlematerials war für Ladungsspeicheranwendungen wie Superkondensatoren von Vorteil. Darüber hinaus wurde die Elementaranalyse des so synthetisierten Aktivkohlematerials (Abb. 3c) mittels energiedispersiver Röntgenspektroskopie durchgeführt und enthüllt die Existenz von Kohlenstoff-, Sauerstoff- und Kaliumelementen darin.

a REM-Bild (Balkenskala 10 μm), b SEM-Bild (Balkenskala 2 μm) und c EDAX-Profil der vorbereiteten Probe
Transmissionselektronenmikroskopie (TEM) und Partikelgrößenverteilung
Um weitere strukturelle Informationen und Kristallqualitätsdimensionen der präparierten Probe zu authentifizieren, wurde ferner Transmissionselektronenmikroskopie (TEM) durchgeführt. TEM-Bilder lassen auf das Vorhandensein mehrerer Strukturen mit Porengröße schließen, die in Abb. 4a, b als transparente Stellen (gelb eingekreist) zu sehen sind. Darüber hinaus zeigt das SAED-Muster die amorphe Natur des Aktivkohlematerials, wie im Einschub von Fig. 4a gezeigt.
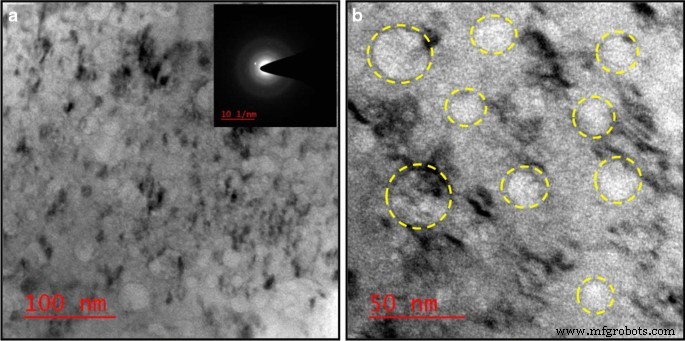
a TEM-Bild (Balkenskala 100 nm) (Einschub:SAED-Muster), b TEM-Bild, das verschiedene Größen poröser Strukturen (Balkenskala 50 nm) des Aktivkohlematerials wie synthetisiert zeigt
UV-sichtbare Lichtabsorption und FTIR-Analyse
Das UV-sichtbare Absorptionsspektrum des so synthetisierten Aktivkohlematerials wurde aufgezeichnet und ist in Abb. 5a dargestellt. Es besitzt aufgrund der elektronischen Übergänge zwischen dem bindenden und antibindenden π . einen charakteristischen Absorptionspeak bei 264 nm -Orbitale.
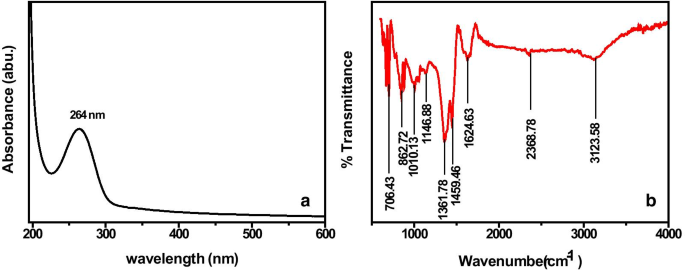
a UV-sichtbares Spektrum und b FTIR-Spektrum der aus Kusha-Gras gewonnenen Aktivkohleprobe nach der Synthese
Die chemischen Oberflächeneigenschaften von Aktivkohlematerial wie synthetisiert wurden durch FTIR-Spektroskopie analysiert und sind in Abb. 5b gezeigt. Sie gibt Auskunft über die zugehörigen funktionellen Gruppen im Aktivkohlematerial. Das Auftreten einer Absorptionsbande bei 3115 cm −1 und ein kleiner Peak bei 2368,78 cm −1 aufgrund der -OH-Streckschwingung der funktionellen Hydroxylgruppen [10, 45, 46]. Der Peak bei 1624,63 cm −1 assoziiert ist −C=C Streckung der aromatischen Ringe, die durch die Zersetzung von C-H-Bindungen zu einer stabileren –C=C-Gruppe bei höheren Aktivierungstemperaturen gebildet werden können [47]. Die starken Absorptionsbanden bei 1459,46, 1361,78, 1146,88, 1010,13 und 862,72 cm −1 bestätigen das Vorhandensein von –C–C (konjugiert mit –C=C), –CH3 Vibration, C–N-Streckung, C–O-Streckung des Esters bzw. – C–O-symmetrische Streckung [39, 43, 47,48,49] im synthetisierten Aktivkohlematerial. Darüber hinaus ist der starke Absorptionspeak bei 706,43 cm −1 Attribute auf –C=C-Biegen in dem wie synthetisierten DP-AC.
WET-Analyse
N2 Adsorptions- und Desorptionsisothermen
Die Porosität im Kohlenstoffmaterial wurde durch Aktivierung durch ein Reagenz KOH während der Synthese erzeugt. Porenstruktur und Oberfläche werden als wesentliche Faktoren für die Superkondensator- bzw. Ultrakondensatorfähigkeit der Materialien angesehen [11]. Das so synthetisierte DP-AC wurde von N2 . analysiert Adsorptions-Desorptionstest nach dem BET-Prinzip für Porenstruktureigenschaften und Oberfläche. Abbildung 6a zeigt die Stickstoffadsorptions-Desorptions-Isotherme von DP-AC, aktiviert durch K2 CO3 . Die Form von N2 Die Adsorptions-Desorptions-Isotherme wird als gemischte Isotherme angenommen, d. h. sie umfasst die Isothermen II und IV. Die Isotherme vom Typ II, die als Kombination der Isothermen vom Typ I und II angenommen wird, weist auf die Existenz einer mikroporösen Natur hin. Der erste Teil (konkave Form) zeigt die vollständige Bedeckung der Monoschicht und die weitere Absorption der Multischicht [11]. Daher zeigt die Typ-II-Isotherme eine gute Übereinstimmung sowohl in mikroporösen als auch in mikroporösen Strukturen. Bei dem relativ höheren Druck bedeutet die Kurvenaufnahme bemerkenswert Isothermen vom Typ IV mit einer Hystereseschleife. Darüber hinaus wird die Typ-IV-Isotherme einer einschichtigen und mehrschichtigen Adsorption zugeschrieben, die mit einer Kapillarkondensation einhergeht, die in sich verjüngenden schlitzartigen Poren stattfindet. Außerdem wurden die Oberfläche und der Porengrößendurchmesser unter Verwendung der BET-Gleichung (Gl. 7) bewertet.
$$\frac{1}{{Q\left( {\left( {\frac{{P_{0}}}{P}} \right) - 1)} \right)}} =\frac{1} {{Q_{m} C}} + \frac{C - 1}{{Q_{m} C}}\left( {\frac{P}{{P_{0} }}} \right)$$ ( 7)wo (P /P 0 ) steht für den relativen Druck und Q , Q m , und C repräsentieren das Gewicht des adsorbierten Gases, des Adsorbats als Monoschicht bzw. die BET-Konstante. Die Oberflächenparameter wie BET-Oberfläche, Mikro- und Mesoporenoberfläche, Gesamtporenvolumen, Mikro- und Mesoporenvolumen und durchschnittlicher Porendurchmesser von DP-AC wurden abgeleitet und sind in Zusatzdatei 1:Tabelle S2 von Supplementary . zusammengefasst Informationsbereich.
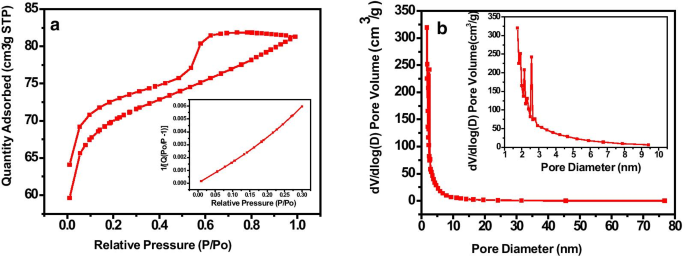
a N2 Isotherme der Adsorptions-Desorptions-Analyse (Einschub, der eine Beziehung zwischen dem relativen Druck (P /P 0 ) gegen 1/[Q (P 0 /P − 1)]), b BJH-Plot; Porengrößenverteilungsdiagramm von Aktivkohlematerialien (Einschub zeigt vergrößerte Ansicht, die die Existenz von Mesoporen für DP-AC zeigt)
Die Porengrößenverteilung des DP-AC
Abbildung 6a (Einschub) zeigt eine gerade Linie für die absorbierte Menge im Vergleich zum relativen Druck (P /P 0 ), was eine gute Übereinstimmung für die Berechnung der Gesamtoberfläche ist. Abbildung 6b zeigt die Porengrößenverteilung gegenüber dem Differenzvolumen. Um die Porengrößenverteilung zu untersuchen, wurde eine BJH-Analyse durchgeführt. Der durchschnittliche Porendurchmesser und die Breite der hergestellten Aktivkohleprobe wurden als ~ 3,3 nm bzw. ~ 2,3 nm ermittelt. Das entsprechende durchschnittliche Porenvolumen betrug 0,126 cm 3 . g −1 . Abbildung 6b (Einschub) zeigt die vergrößerte Ansicht des BJH-Differenzvolumens und der Verteilung des Porengrößendurchmessers für DP-AC. Die BET-Isothermenkurve zeigt, dass die Oberfläche einen Wert von ~ 738,56 m 2 . besitzt g −1 , die auf die Existenz von Meso- und Makroporen in der so synthetisierten Probe schließen lässt. Materialien mit einem hohen Oberfläche-zu-Volumen-Verhältnis und vielen Mesoporen stimulieren eine ausreichende Ladungsspeicherung (Energiedichte) bzw. eine schnelle Ladungsübertragungskinetik (Leistungsdichte) und spielen eine entscheidende Rolle bei der fortschrittlichen Energiespeicherung.
Elektrochemische Analyse
Zyklische Voltammetrie (CV), galvanostatische Ladung/Entladung (GCD) und elektrochemische Impedanzspektroskopie (EIS) wurden verwendet, um die elektrochemische Leistung von DP-AC für Superkondensatoren zu beobachten. Alle Untersuchungen wurden mit einem Drei-Elektroden-System in 6 M KOH als Elektrolytlösung durchgeführt.
Die elektrochemische Leistungsbewertung unter Verwendung von CV ist in Abb. 7a zusammengefasst. Die Abbildung zeigt CV-Kurven bei unterschiedlichen Abtastraten im Bereich von 10–200 mV s −1 innerhalb des Potenzialfensters von 0,35 V bis + 0,45 V und zeigt die rechteckige Form der zyklischen Volumenkurve von AC. Abbildung 7b zeigt ein gemeinsames Merkmal einer elektrochemischen Energiespeichervorrichtung. Eine niedrige Scanrate weist einen höheren Wert der spezifischen Kapazität auf als eine höhere Rate, da bei einer niedrigen Scanrate die Ionen im Elektrolyten in die zugänglichen Poren der Elektrode diffundieren können, was eine gute Wechselwirkung zwischen den Ionen und Poren der Elektrode ermöglicht auftreten. Bei höheren Raten führen eine schlechte Zugänglichkeit oder eine geringere Verfügbarkeit der Zeit für Hydroxylionen, um vom Elektrolyten auf die Elektrodenoberfläche zu gelangen, und somit führen Ionen zu einer Abnahme der spezifischen Kapazität [50, 51]. Wir haben eine maximale spezifische Kapazität bei 10 V s −1 . beobachtet Abtastrate, während die Abtastrate von 160 auf 10 V s −1 . verringert wird . Eine große Oberfläche und eine hohe Porosität spielen eine entscheidende Rolle, um eine hohe Kapazität zu besitzen. Darüber hinaus trägt die geschlossene rechteckige Form des CV zur Optimierung des kombinierten Mikroporen- und Mesoporenvolumens sowie einer guten elektrischen Leitfähigkeit bei. Von nun an die höchste spezifische Kapazität, C SP as ~ 220,70 F g −1 wurde bei 10 mV s −1 . gefunden für DP-AC berechnet nach Gl. 1.
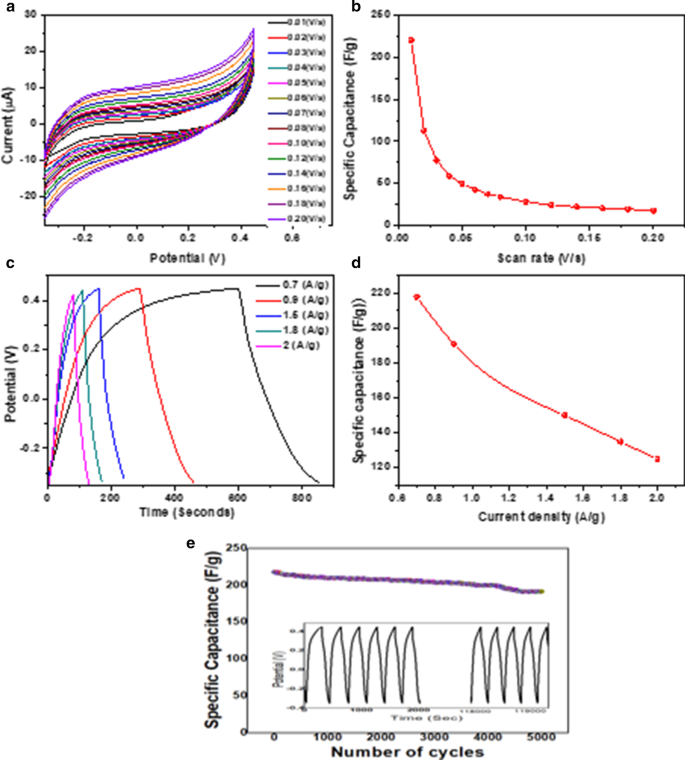
a Zyklisches Voltammogramm (CV) bei verschiedenen Abtastraten, b spezifische Kapazität durch CV, c galvanostatische Lade-Entlade-Kurven bei unterschiedlichen Stromdichten, d spezifische Kapazität durch GCD, e Zyklenstabilität des DP-AC-Elektrodenmaterials wie synthetisiert bis zum 5000. Zyklus mit Anfangs- und Endzyklen bei einer Stromdichte von 0,7 A g −1
Diese hervorragenden Leistungen von DP-AC sind auf seine poröse blattartige Struktur zurückzuführen, die eine entscheidende Rolle für Elektrolytionen spielt und einen schnellen Ladungstransport und -speicherung ermöglicht.
Darüber hinaus wurden die elektrochemische Kapazität und die kolumbische Effizienz aus der elektrochemischen Leistung des Elektrodenmaterials abgeleitet, indem die galvanostatische Ladungs-/Entladungstechnik in einem festen Potenzialfenster bei kontrollierten Stromsituationen bei verschiedenen Stromdichten von 0,7, 0,9, 1,5, 1,8 und 2 A . angewendet wurde g −1 . Es zeigt ein fast dreieckförmiges galvanometrisches Profil (Abb. 7c), das die EDLC-Charakteristik in der DP-AC-Elektrode anzeigt. Das maximale C SP wurde abgeleitet als 218 F g −1 bei einer Stromdichte von 0,7 A g −1 für DP-AC aus Gl. 2. Abbildung 7d zeigt die Variation der spezifischen Kapazität mit der Stromdichte [52,53,54]. Mit zunehmender Stromdichte nimmt die spezifische Kapazität langsam ab. Es ist bekannt, dass es für die Elektrolytionen schwierig ist, schnell in die entsprechenden Poren des Elektrodenmaterials zu diffundieren, wenn der Ladestrom schneller wird. Da außerdem die Zyklenstabilität des Materials ein entscheidender Parameter für die praktische Verwendung des Superkondensators ist, wurde die Zyklenfestigkeit des DP-AC-Elektrodenmaterials durchgeführt. Abbildung 7e zeigt, dass ~ 88 % der anfänglichen spezifischen Kapazität erhalten bleiben und weist auf ihre Fähigkeit zum schnellen Laden und Entladen ohne kaum Verschlechterung selbst nach dem 5000 Material.
Um die Leistungsfähigkeit des synthetisierten DP-AC-Materials für Energiespeicheranwendungen im praktischen Leben weiter zu validieren, werden Energie- und Leistungsdichten als zwei wichtige Parameter betrachtet und aus dem Lade-/Entladeprofil unter Verwendung von Gl. 3 und 4. Es weist eine maximale Energiedichte von 19,3 Wh kg −1 . auf mit einer einigermaßen guten Leistungsdichte von 277 W kg −1 bewertet im Bereich − 0,35 V bis + 0,45 V und ist in Abb. 8a dargestellt. Damit haben wir in Anlehnung an das Ragone-Plot einen Superkondensator mit erhöhter Energiedichte und ohne Leistungsdichteverlust entwickelt, der praktisch einsetzbar ist. Außerdem bemerkenswertes C SP in einem breiten Potentialfenster zeigt eine ausreichende Erhöhung der Energiedichte von DP-AC wie synthetisiert. Einige erweiterte Berechnungen in Bezug auf die Superkondensatorleistung wurden abgeleitet und daher in Zusatzdatei 1:Tabelle.S1 angezeigt.
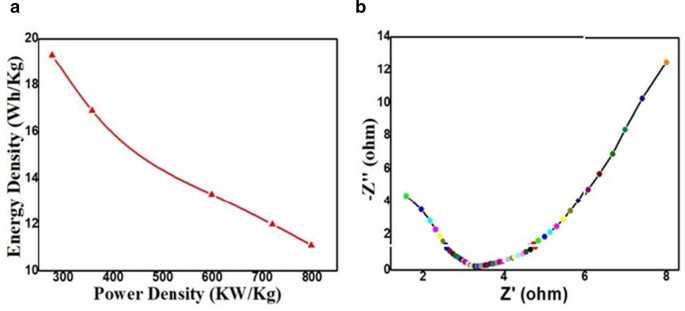
a Ragone-Diagramm für den GCD-Kondensator und b Nyquist-Plot der Impedanz für DP-AC wie synthetisiert
Electrochemical impedance spectroscopy (EIS) technique has been adopted to investigate the interfacial properties such as capacitive and resistive characters of the as-synthesized material at the electrode–electrolyte interface [52] through Nyquist plot (Fig. 8b) and Bode plot (Additional file 1:Fig.S1). Fig. 8b illustrates the Nyquist plot between – Z” (imaginary part) and Z’ (real part) measured in the frequency range of 0.01 Hz to 0.1 GHz at an AC amplitude of 5 mV in the open circuit potential. It shows electric resistance of 1.58 Ω along a small diameter of semicircle confirming high conductivity and low internal resistance. The intersection between the curve and horizontal axis represents the total electric resistance of the device. The diameter of the semicircle at high frequency owes to the charge transfer resistance between electrode material and electrolyte, and tail slope at low frequency attributes to the ionic diffusion rate in the electrolyte [55,56,57]. Therefore, an electrode with as-synthesized DP-AC suits well for supercapacitor applications.
Schlussfolgerung
In summary, a very new facile and low-cost synthesis strategy has been illustrated in the present study for the development of activated carbon material with well-developed pores and high surface area from a natural precursor Kusha grass. It demonstrates a sustainable, eco-friendly, easy-to-employ, without any complex post-synthesis procedure for the energy storage application like a supercapacitor. The fabricated DP-AC with excellent properties has been used as an electrode material for electrochemical supercapacitors. The route enables a bit of modification of the electrode system with a loading of 1 × 10 −5 g DP-AC sample and exhibits a significantly high collector current–mass ratio. The highest specific capacitance has been observed with the CV technique as 220.70 F g −1 and with GCD as 218 F g −1 in a wide operating potential window, which is comparably higher than reported works on the ground of green synthesis (Table 1). The fabricated supercapacitor shows a good energy density and power density as 19.3 Wh kg −1 and 277.92 W kg −1 , respectively, and good retention in capacitance at remarkably higher charging/discharging rates with excellent cycling stability. Henceforth, bio-waste Kusha grass-derived activated carbon (DP-AC) with optimal electrochemical performance can be explored successfully at a real scale, and electrochemical electrical energy store devices with Kusha grass-based AC material may be realized in a short period.
Verfügbarkeit von Daten und Materialien
The used datasheets and materials are available from the corresponding authors on reasonable request.
Abkürzungen
- DP:
-
Desmostachya bipinnata
- AC:
-
Aktivkohle
- KOH:
-
Kaliumhydroxid
- GCE:
-
Glaskohlenstoffelektrode
- XRD:
-
Röntgenpulverbeugung
- TEM:
-
Transmissionselektronenmikroskopie
- SEM:
-
Rasterelektronenmikroskopie
- EDAX:
-
Energiedispersive Röntgenspektroskopie
- FTIR:
-
Fourier-Transformations-Infrarotspektroskopie
- WET:
-
Brunauer–Emmett–Teller
- Lebenslauf:
-
Zyklische Voltammetrie
- GCD:
-
Galvanostatic charge–discharge
- EIS:
-
Elektrochemische Impedanzspektroskopie
Nanomaterialien
- Benchmarking Ihrer Schmierleistung für verbesserte Zuverlässigkeit
- 3 Schlüssel für eine verbesserte Anlagenleistung
- Bewertung der Vorteile von DevOps für IoT-Leistungstests
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Aktivkohlefasern mit hierarchischer Nanostruktur aus Baumwollhandschuhabfällen als Hochleistungselektroden für Superkondensatoren
- Monodisperse Kohlenstoff-Nanosphären mit hierarchischer poröser Struktur als Elektrodenmaterial für Superkondensatoren
- Magnetische Kohlenstoff-Mikrosphären als wiederverwendbares Adsorptionsmittel zur Entfernung von Sulfonamid aus Wasser
- Ein einfacher Ansatz zur Synthese von fluoreszierenden Kohlenstoffquantenpunkten aus Tofu-Abwasser
- Selbstdotierter hochporöser Kohlenstoff mit hohem Graphitgehalt für die Elektrokatalyse von Sauerstoffreduktionsreaktionen
- Na4Mn9O18/Carbon Nanotube Composite als elektrochemisches Hochleistungsmaterial für wässrige Natrium-Ionen-Batterien



