Photolumineszenzstudie des Einflusses von additivem Ammoniumhydroxid in hydrothermal gewachsenen ZnO-Nanodrähten
Zusammenfassung
Wir berichten über den Einfluss von Ammoniumhydroxid (NH4 OH) als Wachstumsadditiv auf Zinkoxid-Nanomaterialien durch die optische Reaktion, die durch Photolumineszenz (PL) erhalten wird. Für das Wachstum von ZnO-Nanodrähten (NWs) auf einer kernlosen Au-Oberfläche wird ein hydrothermaler Niedertemperaturprozess verwendet. Eine Änderung der ZnO-NW-Dichte um mehr als zwei Größenordnungen wird durch vorsichtige Zugabe von NH4 . nachgewiesen OH in der Wachstumslösung. Darüber hinaus zeigen wir durch systematische experimentelle Studien und PL-Charakterisierungsdaten, dass die Zugabe von NH4 OH kann die optische Reaktion von hergestellten ZnO-NWs verschlechtern. Erhöhung der Basizität der Wachstumslösung durch Zugabe von NH4 OH kann die optische Reaktion von NWs durch langsames Ätzen seiner Oberflächen langsam verschlechtern, wodurch die Punktdefekte in ZnO-NWs erhöht werden. Die vorliegende Studie zeigt die Bedeutung von Wachstumsnährstoffen, um qualitätskontrollierte, dichte einstellbare ZnO-NWs auf kernlosen leitfähigen Substraten zu erhalten.
Hintergrund
Bedeutende Entwicklungen in der Synthese funktioneller Nanomaterialien über Bottom-up-Ansätze bieten nun hochwertige Materialien für die Entwicklung effizienter elektronischer Geräte der nächsten Generation [1,2,3,4,5]. Das Forschungsgebiet des ZnO hat nach der erfolgreichen Demonstration des Wachstums einkristalliner Nanostrukturen (Nanobelt) ein Wiederaufleben des Interesses gezeigt [6]. Danach stößt der Einsatz hochwertiger, einkristalliner halbleitender ZnO-Nanostrukturen für den Aufbau von Hochleistungselektronik weiterhin auf enormes Forschungsinteresse im Bereich Displays [7, 8], Logikschaltungen [9, 10], Sensoren [ 11, 12] und Optoelektronik [13]. Das erneute Interesse an ZnO-Material wurde hauptsächlich durch seine Biokompatibilität, einfache Nanostrukturherstellung und große Familie erreichbarer Nanomorphologien getrieben [14, 15]. Unter den verschiedenen ZnO-Nanoarchitekturen wurden eindimensionale (1D) ZnO-Nanodrähte (NWs) und Nanostäbe (NRs) umfassend als aktives halbleitendes Material in nanoskaligen Bauelementen wie Feldeffekttransistoren (FETs) [16], Nanogeneratoren ( NGs) [17] oder Sensoren [12].
Idealerweise ist ein gut stöchiometrisches ZnO ein Isolator. In seiner nichtstöchiometrischen Form kann es sich jedoch abhängig von der Anzahl der erzeugten nativen Punktdefekte und/oder der Menge des eingeführten Dotierungsmittels wie ein Halbleiter oder ein Leiter verhalten. Es wurde gezeigt, dass in nanostrukturiertem ZnO Defekte eine zentrale Rolle bei der Definition der Leistungsfähigkeit elektronischer Bauelemente spielen, wie bei Sensoren [18] und/oder Nanogeneratoren [17, 19], indem sie die freie Ladungsdichte, die Lebensdauer der Minoritätsträger und Lumineszenzeffizienz. So wurde beispielsweise gezeigt [18], dass hochempfindliche UV-Sensoren erhalten werden können, indem die Zahl der Oberflächendefekte in ZnO-NWs erhöht wird. Diese Oberflächendefekte können als Einfangzentren für freie Elektronen wirken und führen zur Bildung einer Oberflächenverarmungsschicht. Je größer die Tiefe der Verarmungsregion an der NW-Oberfläche ist, desto höher ist die UV-Empfindlichkeit. Andererseits hat eine zu große Anzahl von Defekten nachteilige Auswirkungen auf die Leistung des NG-Geräts [17, 19]. Daher ist eine perfekte Kontrolle über die Qualität des hergestellten ZnO-Nanomaterials für den Bau eines leistungsstarken elektronischen Geräts unerlässlich.
Verschiedene Bottom-up-Wachstumstechniken, einschließlich Flammentransportansatz [20,21,22,23], Dampf-Flüssig-Feststoff (VLS) [24], elektrochemische Abscheidung [25] und hydrothermale und/oder chemische Badabscheidung [16, 26,27,28,29] wurden für die Synthese von 1D-ZnO-NWs verwendet. Dennoch sind die meisten Techniken durch ihren Hochtemperaturprozess begrenzt, der nicht mit sehr geringen Kosten auf große Geräteflächen skaliert werden kann, beispielsweise auf Kunststoffsubstraten. Der Bedarf an einer einfachen, industriell skalierbaren und substratunabhängigen Synthese von ZnO-NWs hat zu erheblichen Fortschritten in Richtung des hydrothermalen Wachstumsprozesses geführt [16, 17]. Hydrothermales Wachstum (HTG) ist ein Niedertemperaturprozess, bei dem einkristallines 1D-Material auf verschiedenen Substraten, einschließlich Kunststoffen oder sogar Textilfasern, hergestellt werden kann [30]. Im Allgemeinen zeigen HTG-gezüchtete ZnO-NWs in den Photoemissionsspektren einen intensiven Bandpeak auf dem Defektniveau, der sich je nach Art der Defekte im Nanomaterial von blauer zu roter Wellenlänge ausdehnt [31]. In der Literatur werden viele verschiedene Punktdefekte wie Sauerstoff- und Zinkleerstellen (VO und VZn ) und Interstitial (Oi und Zni ), Antisiten (OZn und ZnO ), und Wasserstoffverunreinigungen wurden als Ursache für die Emissionsbande auf Defektniveau in der Photolumineszenz (PL) identifiziert [32]. Das sichtbare PL-Band besteht aus drei Gaußschen Komponenten bei 2,52, 2,23 und 2,03 eV, die jeweils als blaues IB gekennzeichnet sind , grün IG , und orange IO Spitzenemission [33]. Die Herkunft dieser Fehlerzustände ist jedoch auch nach jahrelangen Untersuchungen noch immer umstritten. Unabhängig von der Ursache von Defekten in ZnO sagt jedoch das Verhältnis des Band-zu-Band-Übergangs (UV-Emission) zur defektbezogenen Spitzenintensität im PL-Spektrum die optische Reaktion des hergestellten Nanomaterials voraus [18, 34].
Ein Wachstumsprozess mit einer in-situ-Integration von ZnO-NWs über einer Metallelektrode ohne ZnO-Keimschicht kann den Ladungstransportprozess über die Metall-Halbleiter-(MS)-Kontaktschnittstelle und folglich die Geräteleistung verbessern [35]. Ammoniumhydroxid (NH4 .) OH) wurde häufig für das Wachstum von ZnO-NWs auf Au-Metalloberflächen eingesetzt [35, 36]. In unserer vorherigen Arbeit haben wir beispielsweise gezeigt, dass NH4 OH kann zur gleichzeitigen Abstimmung der NW-Dichte und der elektrischen Eigenschaften von ZnO-NWs verwendet werden, die auf einer kernlosen Au-Oberfläche gewachsen sind [5]. Berichten Sie jedoch über die Auswirkungen der Zugabe von NH4 OH über der optischen Reaktion des hergestellten ZnO-Nanomaterials auf der Au-Oberfläche wird in der Literatur selten gefunden. In diesem Bericht untersuchen wir die optische Reaktion von ZnO-Material, indem wir die defektbezogene Emission und UV-Emission im PL-Spektrum von NWs analysieren, die in verschiedenen NH4 . gewachsen sind OH-Konzentrationen. Zwei dominante Peaks, die im PL-Diagramm zu sehen sind, sind bei 3,24 eV (382 nm) und 2,23 eV (556 nm) zentriert, die als ultraviolette (UV) Emission (IUV .) bezeichnet werden ) und grüne Defektemission (IG ) Spitzen. Das extrahierte Verhältnis IUV /IG liefert einen qualitativen Index der Strahlungsdefektmenge im hergestellten Nanomaterial. Die Wirkung von NH4 OH wird weiter bestätigt, indem eine weitere Reihe von Experimenten und PL-Charakterisierungen durchgeführt werden. In dieser zweiten Versuchsreihe haben wir ZnO-NWs ohne NH4 . gezüchtet OH und führte dann eine Nachwachstumsbehandlung von NWs in Ammoniaklösung mit unterschiedlichem pH-Wert durch. Wir haben einen ähnlichen Trend der Abnahme des Verhältnisses IUV . festgestellt /IG für beide Probenserien, d. h. diejenigen, die in verschiedenen NH4 gezüchtet wurden OH-Konzentration und die anderen nach dem Wachstum in NH4 . behandelt OH.
Methoden
Die ZnO-NWs werden durch hydrothermalen Wachstumsprozess auf (100)-orientierten Si-Wafern gezüchtet. Eine Probe von 2 × 2 cm 2 starres Silizium wird zuerst in Piranha-Lösung (1:1 H2 .) gereinigt SO4 und H2 O2 ) für 10 Minuten, gefolgt von einem 2-minütigen Eintauchen in Flusssäure (50 %), um das während der Piranha-Reinigung gebildete dünne Oxid zu entfernen, und schließlich in entionisiertem (DI) Wasser gespült. Auf diesen Reinigungsschritt folgt das Trocknen mit Stickstoffgas und ein abschließender Brennschritt wird bei ~ 200 °C durchgeführt, um jegliche adsorbierte Feuchtigkeit vor der Metallabscheidung zu entfernen. Anschließend wird eine Goldschicht (~ 200 nm dick) durch Gleichstromsputtern bei Raumtemperatur abgeschieden. Um die Haftung zwischen Gold und Silizium zu verbessern, scheiden wir mit derselben Technik eine Titanschicht (~ 100 nm) ab. Der Reaktant-Vorläufer für HTG besteht aus einem 1:1-Verhältnis von Zinknitrat-Hexahydrat (Zn (NO3 )2 ‚6H2 O, 98% Sigma Aldrich) und Hexamethylentetramin (HMTA, Sigma Aldrich). Während des Wachstums wurden die Substrate mit der Vorderseite nach unten in einen Teflonbecher getaucht, in einem Edelstahl-Autoklavenreaktor versiegelt und für 15 h in einen vorgeheizten Konvektionsofen bei 85 °C gestellt. Der Autoklav wird aus dem Ofen genommen und kühlt auf natürliche Weise ab. Anschließend werden die Substrate gründlich mit fließendem DI-Wasser gespült und in N2 . getrocknet Gasstrom. In den Experimenten wurde die Konzentration von NH4 OH wird von 0 bis 50 mM variiert. Zur morphologischen Charakterisierung der ZnO-NWs wird ein Hitachi S-4150 Rasterelektronenmikroskop (REM)-System verwendet. Um die optische Reaktion der erhaltenen NWs mit verschiedenen NH4 . zu verfolgen OH-Konzentrationen, Photolumineszenz (PL)-Messungen wurden durchgeführt; bei Raumtemperatur (RT) durch Pumpen mit 1,5 mW die 325 nm lange Linie eines He-Cd-Lasers durch einen akustooptischen Modulator bei einer Frequenz von 55 Hz zerhackt. Weitere experimentelle Details zu PL-Messungen finden sich in Lit. [33].
Ergebnisse und Diskussionen
Um die vorliegende Studie durchzuführen, werden ZnO-NWs unter Verwendung des HTG-Prozesses mit verschiedenen NH4 . gezüchtet OH-Konzentration bei 85 °C. Die Parameter des Wachstumsprozesses sind in Tabelle 1 aufgeführt und weitere Details zum Wachstum finden sich in Lit. Boubeniaet al. [5]. Die erhaltenen Wachstumsergebnisse bei Variation von NH4 OH-Konzentrationen (von 0 bis 50 mM in Schritten von 10 mM) in der Wachstumslösung sind in Abb. 1a–f dargestellt; zeigt typische Querschnitts- und Draufsicht-REM-Bilder, die von den ZnO-NW-Proben aufgenommen wurden. Eine Änderung der NW-Dichte um mehr als zwei Größenordnungen wird durch vorsichtige Zugabe von NH4 . erreicht OH in der Wachstumslösung. Der Mechanismus hinter der NW-Dichtevariation mit NH4 OH-Addition findet sich in Boubenia et al. [5], wo die Autoren die Hypothese aufstellten, dass die Menge an Ammoniumhydroxid einen direkten Einfluss auf die Konzentration von Zn(II)-Komplexen hat, was die Zn-Löslichkeit in der Lösung stark beeinflusst. Folglich kann die Übersättigung der Wachstumslösung und damit die Anzahl der Keime über dem Substrat kontrolliert werden. Darüber hinaus bestimmt/konditioniert zusammen mit der Dichte das Aspektverhältnis (AR) der Nanostrukturen ihre Anwendung in der flexiblen Elektronik, wo hohe Oberflächen-Volumen-Verhältnisse für eine erhöhte Belastungsabsorption benötigt werden. Darüber hinaus ist die Anzahl der Oberflächendefektzustände direkt proportional zum AR der NWs, was einen direkten Einfluss auf die optische Reaktion des Nanomaterials hat. Daher Variation der AR von NW mit steigendem NH4 Die OH-Konzentration wird auch unter Verwendung von SEM-Bildern berechnet. Abbildung 1g zeigt eine Grafik, die den Trend der Dichte- und AR-Variation bei Zugabe von NH4 . darstellt OH in der Wachstumslösung. Anhand von Abb. 1g ist zu erkennen, dass als NH4 Die OH-Konzentration steigt, sowohl die NW-Dichte als auch die AR steigen, bis die Werte bei einer Ammoniumhydroxid-Konzentration von 40 mM gesättigt sind. Raman-Spektroskopie-Messungen bei Raumtemperatur, durchgeführt an ZnO-NWs, die mit verschiedenen NH4 . gezüchtet wurden OH-Konzentrationen, bestätigen Sie die Wurtzit-Kristallstruktur des hergestellten Nanomaterials (Zusatzdatei 1:Abbildung S1) [5].
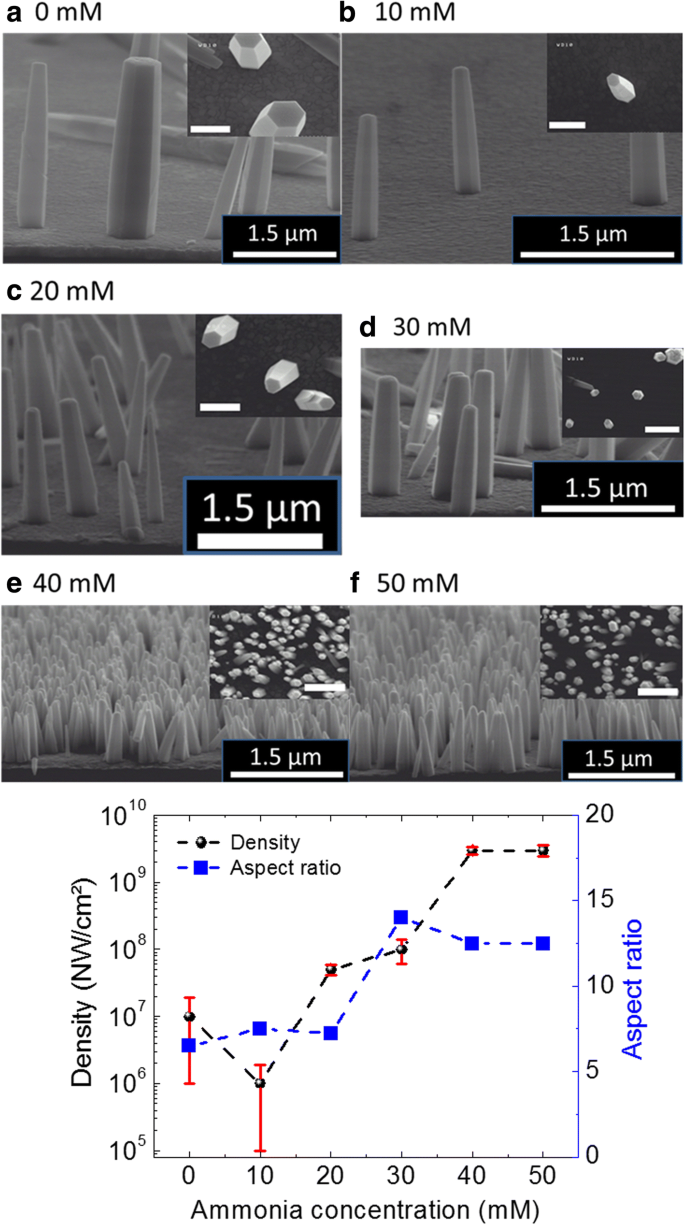
SEM-Bilder von NWs, die für verschiedene Konzentrationen von Ammoniak gezüchtet wurden. a 0 mM, b 10 mM, c 20 mm, d 30 mM, e 40 mM und f 50 mm. Der Einsatz in jedem Panel (a –e ) zeigt das REM-Bild in Draufsicht, das von derselben Probe aufgenommen wurde. Der Maßstabsbalken im Einschub beträgt 500 nm. g Die Variation der Dichte und des Seitenverhältnisses von NWs mit der Änderung von NH4 OH-Konzentration
Abbildung 2a zeigt die bei RT gemessenen PL-Spektren für NWs, die mit verschiedenen Ammoniumhydroxidkonzentrationen gezüchtet wurden. Das PL-Spektrum von ZnO-NWs weist zwei Emissionsbänder auf:eine Lichtemission am nahen Bandrand (NBE) und eine breite tiefe (sichtbare) Emission. Die in der vorliegenden Studie verwendete Anregungsenergie beträgt 3,81 eV, wodurch die Ladungsträgerpopulation des Leitungsbandminimums sichergestellt wird. Der starke und schmale UV-Emissionspeak, der für alle Fälle bei 3,24 eV zentriert ist, resultiert aus der Verschmelzung der verschiedenen Exzitonen-bezogenen Emission nahe der Bandkante, einschließlich der Rekombination freier Exzitonen und ihrer longitudinalen optischen (LO)-Phonon-Replikate, [37] freie zu neutrale Akzeptorübergänge, [38] und Donor-Akzeptor-Paar-Rekombination [39], abhängig von der lokalen Gitterkonfiguration und dem Vorhandensein von Defekten [40,41,42]. In Abb. 2a können wir auch eine breite Emission im sichtbaren Bereich beobachten, die sich von der grünen zur orangen Farbwellenlänge ausdehnt. Das Vorhandensein eines breiten sichtbaren Emissionspeaks kann mit der Hypothese der Existenz multipler Defekte und/oder Defektkomplexe erklärt werden, die dominant an der Oberfläche von ZnO-Nanostrukturen vorhanden sind [34, 43]. Trotz einer Reihe von Berichten über das Vorhandensein sichtbarer Emission im PL-Spektrum von ZnO gibt es jedoch in der Literatur keinen klaren Konsens über die Peakpositionen im sichtbaren Bereich oder ihren Ursprung. Es ist auch zu beachten, dass es aufgrund der großen Unterschiede in Dichte und Aspektverhältnis von Probe zu Probe (Abb. 1g) schwierig ist, dieselbe Materialmenge für so unterschiedliche Proben zu untersuchen. Daher können wir die Emissionsintensität dieser Proben nicht direkt vergleichen. Nichtsdestotrotz sagt das Verhältnis der Größe der UV-Emissionsspitzenintensität in Bezug auf die defektbezogene Spitzenintensität im PL-Spektrum die optische Reaktion des hergestellten Nanomaterials voraus. Alle sichtbaren Spektren können erfolgreich an drei defektbezogene sichtbare Lumineszenzzustände angepasst werden, nämlich blau, grün und orange. In Abb. 2b ist beispielsweise die Gaußsche Anpassung von 40 mM NH4 . dargestellt OH-Probe für die blauen, grünen und orangen Zustände, die entsprechend eingefärbt sind, um ihre relativen Unterschiede hervorzuheben. Es ist hier zu beachten, obwohl die PL-Intensität sowohl für den UV- als auch für den sichtbaren Emissionspeak aufgrund des Unterschieds in der produzierten Masse für variierendes NH4 . variiert OH in Lösung bleibt der prozentuale Beitrag für die blauen, grünen und orangen Zustände gleich. In Abb. 2b ist der prozentuale Beitrag jedes Fehlerzustands für die 40 mM-Probe dargestellt, was zeigt, dass der Hauptbeitrag der sichtbaren Emission mit dem grünen Fehlerzustand zusammenhängt. Um die optische Reaktion des hergestellten Nanomaterials zu verfolgen, ist es daher angemessen, das Intensitätsverhältnis der UV-Emission (IUV ) in den grünen Defektzustand (IG .) ), die den höchsten prozentualen Beitrag in den sichtbaren Spektren zu haben scheint.
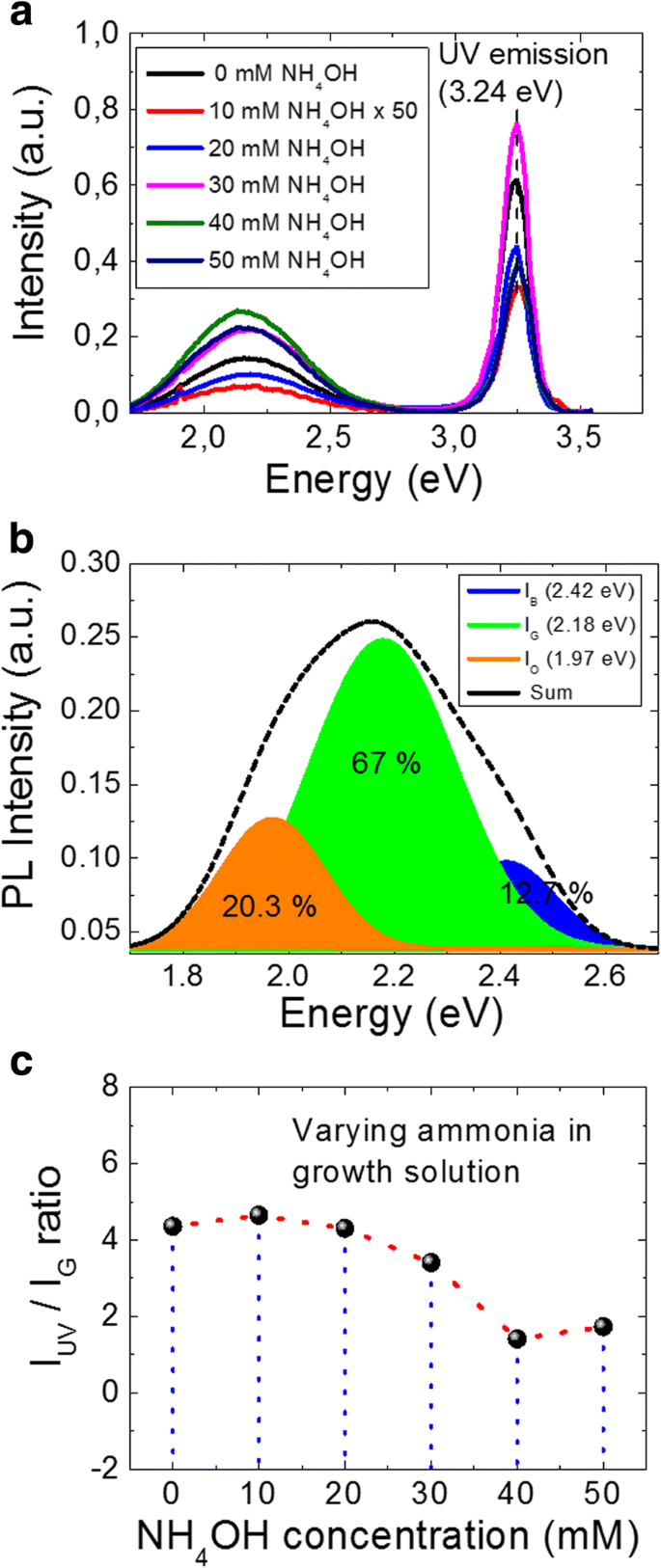
Die Ergebnisse der PL-Messungen. a Die PL-Spektren der unter verschiedenen Ammoniumhydroxidkonzentrationen gewachsenen ZnO-NWs. b Entfaltete Gaußsche Anpassung für die 40-mM-Probe an blaue, grüne und orange Emissionszustände und ihre prozentualen Beiträge zur sichtbaren Emission. c Das Intensitätsverhältnis von UV- und grünem Emissionspeak als Funktion von NH4 OH-Konzentration
Abbildung 2c zeigt das extrahierte IUV /IG Verhältnis für jeden Fall von NWs, die mit unterschiedlichen Ammoniakkonzentrationen angebaut wurden, während Tabelle 2 die extrahierten Werte darstellt. Anhand von Abb. 2c ist zu erkennen, dass die IUV /IG Verhältnis nimmt nach 20 mM NH4 smoothly sanft ab OH in der Wachstumslösung. Zum Beispiel das IUV /IG Der Wert für 40 mM Ammoniak ist dreimal niedriger als der der Probe "kein Ammoniak", was auf eine Zunahme der sichtbaren Defektzustände bei Zugabe von Ammoniak hinweist. Dominant kann es zwei mögliche Gründe für die beobachtete experimentelle Zunahme von Defektzuständen im sichtbaren Bereich geben:(i) Zunahme des Aspektverhältnisses und (ii) Zunahme der Lösungsbasizität bei Zugabe von Ammoniumhydroxid. Betrachtet man den ersten Punkt, kann das Seitenverhältnis die Intensität der Emission im sichtbaren Bereich stark beeinflussen. Djurisic et al. führten eine eingehende PL-Analyse von ZnO-Nanostrukturen durch und kamen zu dem Schluss, dass die grüne Lumineszenz in ZnO-PL-Spektren wahrscheinlich von einigen nicht-paramagnetischen Defekten oder Defektkomplexen herrührt und dass der größte Teil von Oberflächendefekten stammt [34]. Aus Abb. 1g ist ersichtlich, dass das Seitenverhältnis stark ansteigt (L /d ) über 20 mM NH4 OH-Addition, wobei L und d sind die Länge bzw. der Durchmesser des NW. Ein großer AR bedeutet eine beträchtliche Zunahme des Oberflächen-Volumen-Verhältnisses, was zu einer erhöhten Emission von Defekten führt. Ein ähnlicher Anstieg der Defektpegelemission mit dem Anstieg von AR wurde in Lit. berichtet. [44] führt zu einer Abnahme des IUV /Ivis Verhältnis. Die Autoren sind jedoch nicht davon überzeugt, dass die Zunahme von AR der einzige Grund für die beobachtete Zunahme der Defektemissionsintensität sein kann. Sie wiesen außerdem darauf hin, dass die erhaltenen Ergebnisse sehr empfindlich auf die experimentellen Bedingungen wie Anregungsdichte und Strahlungsfläche reagieren können [44].
Ein weiterer möglicher Grund für die beobachtete Zunahme der Defektzustände in den NWs kann die Zugabe von NH4 . sein OH selbst. Chenet al. haben gezeigt, dass in hydrothermal gewachsenen ZnO-NWs (unter Verwendung einer ZnO-Keimschicht) verschiedene Defekte durch Zugabe von NH3 . induziert werden können Moleküle während der Wachstumsphase [45]. Obwohl die Zugabe von NH4 OH ist nicht entscheidend für das Wachstum von ZnO-NWs unter Verwendung einer ZnO-Keimschicht, für das keimlose Wachstum von ZnO-NWs auf Au-Oberflächen die Zugabe von NH4 OH spielt eine Schlüsselrolle bei der Kontrolle der Zahl der Nukleationsstellen auf der Au-Oberfläche. Alenezi et al. erklärten die ZnO-NW-Dichtevariation auf der blanken Au-Oberfläche, indem sie feststellten, dass ohne NH4 OH, hauptsächlich Zn 2+ Ionen sind verfügbar, während sie Ammoniumhydroxid verwenden, sind sie begrenzt, was die Rate der homogenen Keimbildung erheblich verringert und die heterogene begünstigt. Ähnliche Beobachtungen werden von Boubenia et al. [5], wobei mehr als zwei Ordnungen der NW-Dichte durch sorgfältige Kontrolle von NH4 . variiert werden können OH-Konzentration in der Wachstumslösung. Die Autoren behaupten außerdem, dass die Dichte freier Ladungsträger zunimmt, während die Feldeffektmobilität abnimmt, wenn das NH4 Die OH-Konzentration steigt, was auf die Entstehung zusätzlicher Punktdefekte bei Zugabe von NH4 . hinweist OH in der Wachstumslösung. Es werden jedoch keine PL-Daten gezeigt, um die berichteten elektrischen Ergebnisse zu bestätigen. Die in Abb. 2 gezeigten PL-Ergebnisse stimmen vollständig mit den elektrischen Ergebnissen überein, die von Boubenia et al. [5], wie in Tabelle 2 erwähnt, wobei die freie Ladungsdichte von 4,3 × 10 16 . ansteigt bis 2 × 10 17 cm − 3 als NH4 Die OH-Konzentration steigt von 0 auf 40 mM in der Wachstumslösung. Daher können wir annehmen, dass die Zugabe von NH4 OH in der Wachstumslösung erzeugt zusätzliche Punktdefekte in den ZnO-NWs. Um diese Hypothese zu bestätigen, führten wir jedoch eine weitere Reihe von Experimenten durch, bei denen die gewachsenen ZnO-NWs ohne Zugabe von NH4 OH, werden in Lösung mit zunehmender Basizität behandelt. Die Einzelheiten zu den Behandlungsversuchen nach dem Wachstum sind in Tabelle 3 aufgeführt.
Die erhaltenen experimentellen Ergebnisse für die Nachwachstumsbehandlung von NWs in Ammoniaklösung sind in den Fig. 1 und 2 gezeigt. 3 und 4. Abbildung 3 zeigt die entsprechenden SEM-Bilder der Proben, die in verschiedenen NH4 . behandelt wurden OH-Konzentrationen. Aus dem vorliegenden Datensatz ist ersichtlich, dass die Oberfläche von NW mit zunehmendem NH4 . rauer wird OH-Konzentration, die sogar zur Bildung von Nanohügeln an der polaren Oberfläche von ZnO-NWs für 100 und 200 mM behandelte Proben führt. Der schlimmste Fall ist bei Proben zu sehen, die mit 100 und 200 mM NH4 . behandelt wurden OH, wo einige NWs aus der Basis herausgebrochen zu sein scheinen und horizontal über dem Substrat liegen. Bei weiterer Erhöhung der Molarität von NH4 OH-Lösung, mehr als 90% der NWs sind gebrochen (Daten nicht gezeigt).

REM-Bilder von gewachsenen (unberührten) ZnO-NWs und nach dem Wachstum behandelten NWs in verschiedenen NH4 OH-Konzentrationen
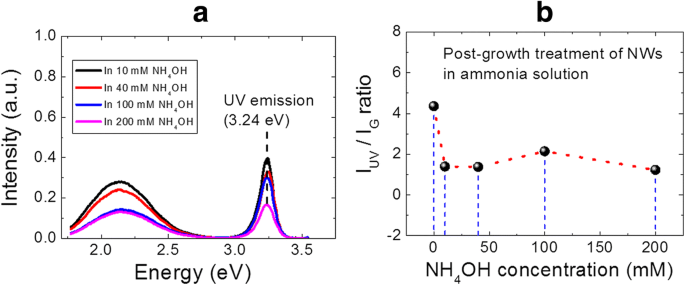
a Die PL-Spektren der ZnO-NWs, die in Lösungen mit verschiedenen Ammoniumhydroxidkonzentrationen behandelt wurden. b Das Intensitätsverhältnis von UV- und Grünemissionspeaks als Funktion von NH4 OH-Konzentration, extrahiert aus a
Die resultierenden PL-Daten aus den nach dem Wachstum behandelten Proben sind in Abb. 4 dargestellt. Abb. 4a zeigt die bei RT gemessenen PL-Spektren für NWs, die mit verschiedenen Ammoniumhydroxidkonzentrationen behandelt wurden, während das extrahierte IUV /IG Diagramm ist in Abb. 4b gezeigt. Es ist zu beachten, dass die Peakposition sowohl für die UV- als auch für die sichtbare Emission nach NH4 . nicht geändert wurde OH-Behandlung, was darauf hinweist, dass während der NH4 . kein zusätzlicher Punktdefekt mit unterschiedlichem Energieniveau gebildet wird OH-Behandlung. Die kontinuierliche Verringerung der PL-Intensität des UV-Emissionspeaks mit der Zunahme von NH4 OH-Konzentration, zeigt deutlich die Entfernung von ZnO-Nanomaterial aufgrund eines langsamen Ätzens der NWs in basischem Medium [46]. Außerdem ist es interessant, in Abb. 4b einen klaren und starken Abfall des IUV . zu erkennen /IG Verhältnis, da die NWs in NH4 . behandelt werden OH-Lösung. Wichtig ist hier zu erwähnen, dass für die vorliegende Studie die experimentellen Bedingungen wie Anregungsdichte, Strahlungsfläche, Anfangsmasse des ZnO-Nanomaterials etc. festgelegt sind. Daher ist das beobachtete IUV /IG Verhältnistrend kann vollständig mit dem durch die Zugabe von NH4 eingeführten Effekt zusammenhängen OH und nicht auf Veränderungen der experimentellen Bedingungen [47]. Die erhaltenen experimentellen Ergebnisse stützen eindeutig die im vorherigen Abschnitt aufgestellte Hypothese zur Erzeugung zusätzlicher Punktdefekte durch Zugabe von NH4 OH in der Wachstumslösung. Wir glauben, dass die Erhöhung der Basizität der Wachstumslösung durch die Zugabe von NH4 OH kann die optische Reaktion von NWs langsam verschlechtern, indem es langsam seine Oberflächen ätzt, was das Niveau von Punktdefekten in ZnO-NWs erhöht.
Schlussfolgerungen
Zusammenfassend demonstrierten wir einen einfachen, kostengünstigen und skalierbaren Bottom-up-Prozess für ein keimfreies Wachstum von ZnO-NWs auf metallischen Au-Oberflächen. Durch vorsichtige Zugabe von Ammoniumhydroxid in die Wachstumslösung kann die ZnO-NW-Dichte über zwei Größenordnungen gesteuert werden. Folgen der Zugabe von NH4 Die OH über der optischen Reaktion der erhaltenen NWs wurden unter Verwendung der Photolumineszenztechnik untersucht. Das sichtbare Emissionsspektrum für jedes NH4 OH-Konzentration, wurde erfolgreich in die blauen, grünen und orangefarbenen Defektzustände entfaltet. Darüber hinaus wurde auch der prozentuale Beitrag jedes Defektzustands dargestellt, was zeigt, dass der Hauptbeitrag der sichtbaren Emission vom grünen Defektzustand stammt. Um die optische Reaktion des hergestellten Nanomaterials zu verfolgen, verglichen wir dabei das Intensitätsverhältnis der UV-Emission (IUV ) in den grünen Defektzustand (IG .) ). Es wurde beobachtet, dass das IUV /IG Das Verhältnis nimmt nach Zugabe von 20 mM NH4 . stark ab OH, was auf die Entstehung zusätzlicher Punktdefekte bei Zugabe von NH4 . hinweist OH in der Wachstumslösung. Die experimentellen Ergebnisse wurden durch die Literaturdaten zur Erhöhung der freien Ladungsdichte mit NH4 . gut unterstützt OH-Zugabe. Nichtsdestotrotz wurde die vorgeschlagene Hypothese weiter bestätigt, indem eine weitere Reihe von Experimenten durchgeführt wurde, bei denen die gewachsenen ZnO-NWs ohne Zugabe von NH4 OH, wurden in Lösungen mit zunehmender Basizität behandelt. Ein deutlicher und starker Abfall des IUV /IG Verhältnis, da die NWs in NH4 . behandelt wurden OH-Lösung, zeigte, dass die Erhöhung der Basizität der Wachstumslösung bei Zugabe von NH4 OH kann die optische Reaktion von NWs durch Ätzen seiner Oberflächen langsam verschlechtern, was das Niveau von Punktdefekten in ZnO-NWs erhöht. Die vorliegende Studie ist wichtig, um die optische Reaktion von ZnO-NWs zu kontrollieren, die direkt auf metallischen Au-Elektroden für elektronische und optoelektronische Anwendungen aufgewachsen werden können.
Nanomaterialien
- Die Untersuchung eines neuartigen, durch Nanopartikel verbesserten wurmähnlichen Mizellensystems
- First-Principles-Studie zur Stabilität und dem STM-Image von Borophen
- In-vitro-Studie zum Einfluss von Au-Nanopartikeln auf HT29- und SPEV-Zelllinien
- Amorphe Silizium-Nanodrähte, die durch Glühen auf Siliziumoxid-Film gewachsen sind
- Einfluss von Wasser auf die Struktur und die dielektrischen Eigenschaften der mikrokristallinen und Nano-Cellulose
- Abstimmung der Oberflächenmorphologien und -eigenschaften von ZnO-Filmen durch das Design der Grenzflächenschicht
- Eine zweistufige Methode zur Untersuchung des Einflusses der Aggregation/Agglomeration von Nanopartikeln auf den Elastizitätsmodul von Polymer-Nanokompositen
- Herstellung und Charakterisierung von ZnO-Nano-Clips durch das Polyol-vermittelte Verfahren
- Einfluss des Substrats auf die Wellenlänge und Stärke der LSP-Kopplung
- Selbst gesätes MOCVD-Wachstum und dramatisch verstärkte Photolumineszenz von InGaAs/InP-Kern-Schale-Nanodrähten



