Die potenzielle Anwendung von BAs für einen Gassensor zum Nachweis von SO2-Gasmolekülen:eine DFT-Studie
Zusammenfassung
Verschiedene atmosphärische Gasmoleküle (z. B. N2 , O2 , CO2 , H2 O, CO, NEIN, NEIN2 , NH3 , und SO2 ) werden durch Dichtefunktionalrechnungen auf dem reinen hexagonalen Borarsenid (BAs) absorbiert. Für jedes Gasmolekül wurden verschiedene Adsorptionspositionen berücksichtigt. Die stabilste Adsorption hing von Position, Adsorptionsenergie, Ladungstransfer und Austrittsarbeit ab. SO2 Gasmoleküle hatten die beste Adsorptionsenergie, den kürzesten Abstand für die BAs-Oberfläche im atmosphärischen Gasmolekül und einen gewissen Ladungstransfer. Die Berechnung der Austrittsarbeit war wichtig, um die Möglichkeiten zur Anpassung der elektronischen und optischen Eigenschaften zu erforschen. Unsere Ergebnisse präsentierten BAs Materialien können der potenzielle Gassensor von SO2 . sein mit hoher Empfindlichkeit und Selektivität.
Einführung
BAs (hexagonales Borarsenid) besteht aus Elementen der Gruppen III und V. Die Gruppen der III–V-Elemente haben ausgezeichnete Eigenschaften, wie ausgezeichnete photoelektrische Eigenschaften, mechanische Eigenschaften und eine große Bandlücke [1]. Die vielversprechenden Anwendungsmöglichkeiten von 2D-Materialien [2,3,4,5] wurden in neueren Studien gut dokumentiert [6,7,8,9,10,11,12,13,14,15,16,17,18,19 ,20]; diese Materialien wurden verwendet, um verschiedene Biomoleküle [21, 22], Schadstoffe [23, 24] und Gasmoleküle [25, 26] zu erkennen, um geeignete Sensoren zu entwickeln. Wir hatten immer mehr die Gruppen der III–V-Elementmaterialien gefunden, zum Beispiel BN, AlN, GaN, GaAs und BP, und es gibt immer mehr Studien für die Gasmoleküle durch theoretische Berechnungen. Strak et al. [27] entdeckten, dass AlN(0001) ein leistungsfähiger Katalysator für die Hochdruck-Hochtemperatur-Synthese von Ammoniak ist, und die Arbeiten bestätigten auch die Möglichkeit einer effizienten Synthese von Ammoniak an der AlN(0001)-Oberfläche. Diaoet al. [28] präsentierte die Adsorption von H2 O, CO2 , CO, H2 , und N2 auf (10–10) Oberflächen von reinen und Zn-dotierten GaAs-Nanodrähten; die Wirkung der Adsorption von CO2 und N2 auf Absorptionskoeffizienten war am größten. Chenget al. [29] zeigten die Adsorption der meisten Gasmoleküle an reinem SP und dotiertem SP anhand einer ersten prinzipiellen Untersuchung und kamen zu dem Schluss, dass N-BP besser als Gassensor für SO2 . geeignet ist , NEIN und NEIN2 aufgrund der Existenz des Desorptionsprozesses. Kamaraj und Venkatesan [30] untersuchten die Struktur und die elektronischen Eigenschaften der BAs mittels DFT und LDA; Obwohl bei der experimentellen Synthese und theoretischen Untersuchung von BAs beträchtliche Fortschritte erzielt worden waren, statteten die Ergebnisse der BAs-Nanoblätter das System mit vielversprechenden Anwendungen in der Nanoelektronik und Photovoltaik aus.
In dieser Arbeit haben wir zunächst die Gassensoreigenschaften untersucht, um die Möglichkeiten von BAs als Gassensoren durch Berechnungen der Dichtefunktionaltheorie (DFT) voll auszuschöpfen. Wir haben die Adsorptionseigenschaften atmosphärischer Gase vorhergesagt (z. B. CO2 , O2 , N2 , H2 O, NEIN, NEIN2 , NH3 , CO und SO2 ) zu BAs auf der Grundlage von First-Principles-Berechnungen. Unsere Arbeit zeigte das scheinbare Adsorptionsverhalten, moderate Ladungstransfers und einzigartige Transmissionseigenschaften von SO2 Adsorption an BAs. Die Ergebnisse legten nahe, dass einlagige BAs ein großes Potenzial für SO2 . besitzen Sensoranwendung.
Theorie und Methode der Simulation
Das System wurde als 4 × 4-Superzelle aus BAs und darauf adsorbierten atmosphärischen Gasmolekülen modelliert. In DMol 3 [31] Berechnungsverfahren wurden Austauschkorrelationsfraktionen innerhalb eines General Gradient Approximation (GGA) mit dem Perdew-Burke-Ernzerhof (PBE) berechnet [32]. Die Brillouin-Zone wurde unter Verwendung eines 5 × 5 × 1 Monkhorst-Pack-K-Punkt-Gitters und einer Methfessel-Paxton-Verschmierung von 0,01 Ry beprobt. Alle Atomstrukturen wurden entspannt, bis die Gesamtenergie und die Hellmann-Feynman-Kraft auf 1.0 × 10 −5 . konvergierten eV und 0,06 eV/Å [33].
Um die Wechselwirkung zwischen Gasmolekülen und Adsorptionsschichtoberfläche zu bewerten, berechneten wir die Adsorptionsenergie (E Anzeige ) von adsorbierten Systemen, die definiert wurde als:
$$ {E}_{\mathrm{ad}}={E}_{\mathrm{BAs}+\mathrm{Gas}\mathrm{Molekül}}-\left({E}_{\mathrm{BAs} }+{E}_{\mathrm{Gas}\ \mathrm{Molekül}}\right) $$wo E BAs + Gasmolekül ist die Gesamtenergie des BAs-adsorbierten Systems, E BAs ist die Energie von BAs und E Gasmolekül ist die Energie eines Gasmoleküls. Alle Energien wurden für optimierte Atomstrukturen berechnet. Der Ladungstransfer wurde durch Mullikens Populationsanalyse untersucht.
Ergebnis und Diskussion
In dieser Arbeit wurden drei Adsorptionsstellen für BAs betrachtet, nämlich die Spitze eines Boratoms (B), die Spitze eines Arsenatoms (As) und das Zentrum eines hexagonalen B-As (Mitte), wie in Abb. 1a . gezeigt . Wir haben das Vorhandensein der Atmosphäre untersucht und den besten Gassensor gefunden.
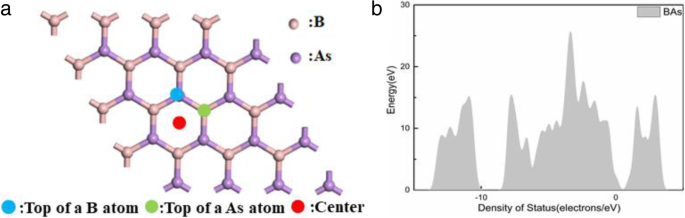
a Schematische Ansicht der Top-Sites und der Center-Site auf BAs. b Die DOS der BAs
Zunächst wurde die geometrische Struktur der reinen BAs-Monoschicht optimiert, und wie in Abb. 1b gezeigt, betrug die BAs-Bindungslänge 1.967 Å. In der Bandstruktur des BAs-Faltblatts war eine indirekte Bandlücke von 1.381 eV zu erkennen, die kleiner war als die der Volumenstruktur. Diese Werte stimmten gut mit den zuvor gemeldeten Werten überein (Abb. 2) [34, 35].
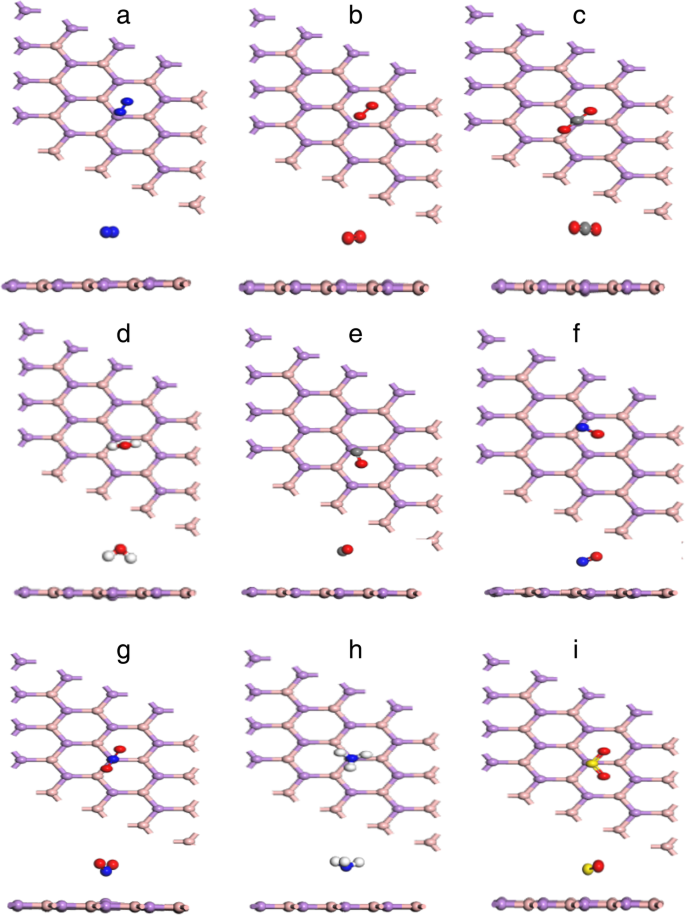
Die energetisch günstigsten Adsorptionskonfigurationen der Gasmoleküle:N2 (a ), O2 (b ), CO2 (c ), H2 O (d ), CO (e ), NEIN (f ), NO2 (g ), NH3 (h ) und SO2 (ich ) auf Monolayer-BAs
Inzwischen hatten wir die Adsorptionsenergie, den Ladungstransfer und den Abstand zwischen den Molekülen und der BAs-Oberfläche analysiert. Das Endergebnis ist in Tabelle 1 dargestellt.
N 2 Adsorption: Adsorption von N2 Gasmolekül auf BAs wurde für drei Konfigurationen von N2 . untersucht /BAs, d.h. Oberseite des B-Atoms, Oberseite des As-Atoms und das Zentrum eines hexagonalen Rings über der BAs-Oberfläche, und der nächste Abstand betrug 3.764 Å, 3.549 Å und 3.65 Å und die entsprechende Adsorptionsenergie war − 0.24 eV, − 0.27 eV bzw. − 0,24 eV. Das Zentrum hatte die beste Adsorptionsenergie und die stabilste Struktur. Die Adsorptionsenergie von N2 BAs war −0,24 eV, der Ladungstransfer von BAs zu N 2 Gasmolekül war 0,014e, und der Abstand der N2-BAs betrug 3,65 . Abb. 3a zeigte, dass es viele Linien unter dem Fermi-Energieniveau gab und die entsprechende Zustandsdichte mehrere Spitzen unter dem Fermi-Energieniveau aufwies. Wie in der Abbildung gezeigt, ist der N2 Gasmolekül hatte vier Peaks, die einen gewissen Einfluss auf BAs hatten, hauptsächlich von − 5 bis 0 eV, und große Beiträge zur DOS hatten. Insgesamt ist die Wirkung von N2 Die Adsorption von Gasmolekülen auf BAs war schlecht.
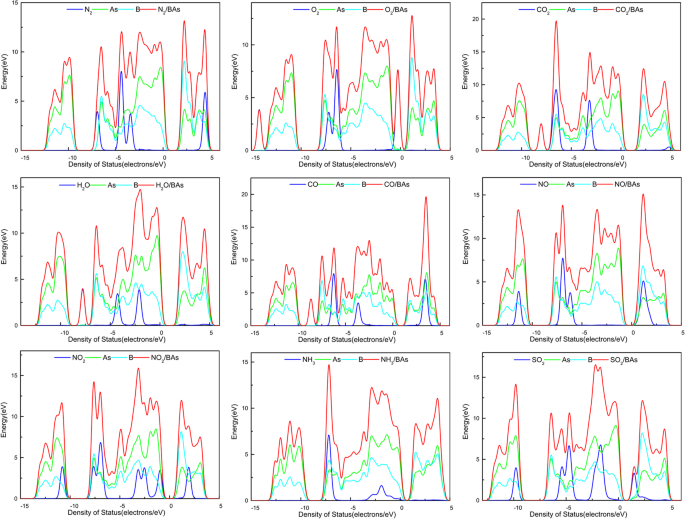
Zustandsdichte (DOS) von N2 /BAs (a ), O2 /BAs (b ), CO2 /BAs (c ), H2 O/BAs (d ), CO/BAs (e ), NO/BAs (f ), NO2 /BAs (g ), NH3 /BAs (h ) und SO2 /BAs (i )
O 2 Adsorption: O2 Gasmoleküle neigten dazu, am zentralen Punkt zu adsorbieren. Die Adsorptionsenergie von O2 /BAs war − 0.35 eV, und der Abstand von O2 -BAs war 2,90 . Die Gesamtbandstruktur und DOS für O2 /BAs wurden in Abb. 3 aufgetragen. Es war offensichtlich, dass eine zusätzliche Linie den Nullpunkt kreuzte und die Bandlücke verringerte; O2 Gasmoleküls hatte einen Peak bei − 1 bis 0 eV und hatte einen Einfluss auf die Zustandsdichte oberhalb des Fermi-Niveaus. Die Populationsanalyse für den Mulliken-Ladungstransfer zeigte, dass − 0.172e von der BAs-Oberfläche auf das O2 . übertragen wurde Gasmolekül, was darauf hindeutet, dass O2 Gasmoleküle fungierten als Akzeptor. Im Allgemeinen ist die O2 Gasmoleküladsorption auf BAs war besser als N2 .
CO 2 Adsorption: CO2 Gasmoleküle neigten dazu, oben auf dem As-Atom zu adsorbieren. Die Adsorptionsenergie von CO 2 /BAs war −0,28 eV, der Ladungstransfer von BAs zu CO 2 Gasmolekül war −0.018e, und der Abstand des CO 2 -BAs war 3,55 Å. Wie in Abb. 3 gezeigt, hatte die Struktur im Vergleich zu unberührten BAs keine offensichtliche Änderung, und es gab einige offensichtliche Wellenberge der Energie von − 9 eV in DOS, die einen großen Beitrag zur DOS leisteten. Dieser Punkt hat auch die Adsorption von CO2 . hervorgehoben Gasmolekül durch BAs. Die Ergebnisse zeigten, dass der Adsorptionseffekt und die Empfindlichkeit von BAs gegenüber CO2 Gasmolekül waren allgemein.
H 2 O-Adsorption: H2 O-Gasmoleküle neigten dazu, oben auf dem As-Atom zu adsorbieren. Die Adsorptionsenergie von H 2 O/BAs war −0,38 eV, der Ladungstransfer von BAs zu H 2 O-Gasmolekül war −0.03e, und der Abstand von H 2 O-BAs betrug 3,63 Å. Wie in Abb. 3 gezeigt, gab es keine großen Veränderungen in der Struktur im Vergleich zu unberührten BAs. Das Fermi-Niveau von Al-G stieg offensichtlich an und bewegte sich in das Valenzband. Im Allgemeinen ist die H2 Die Adsorption von O-Gasmolekülen an BAs wurde ignoriert.
CO-Adsorption: Das CO-Gasmolekül neigte dazu, oben auf dem As-Atom zu adsorbieren. Die Adsorptionsenergie von CO/BAs betrug −0,27 eV, der Ladungstransfer von BAs auf das CO-Gasmolekül betrug −0,024e und der Abstand der CO-BAs betrug 3,50 . Die Gesamtzustandsdichte (DOS) und die Bandstruktur für BAs-CO wurden in Abb. 3 aufgetragen. CO-Gasmolekül und As-Atom spielten eine große Rolle bei der Wirkung eines Peaks von 3 bis 4 eV auf die DOS. Es gab jedoch keine Abweichung der DOS im Bereich von − 7 bis 4 eV, was darauf hindeutet, dass CO wöchentlich an BAs adsorbiert wurde. Es gab einen offensichtlichen Wellenberg der Energie von − 3 bis 1 eV und 3 eV, der große Beiträge zur DOS hatte. Die Populationsanalyse für den Mulliken-Ladungstransfer zeigte, dass eine Ladung von − 0.024e von der BAs-Oberfläche auf das CO-Gasmolekül übertragen wurde, und legte nahe, dass das CO-Gasmolekül als Akzeptor fungiert. Insgesamt war die Wirkung der CO-Gasmoleküladsorption auf BAs nicht besonders.
KEINE Adsorption: NO-Gasmoleküle neigten dazu, oben auf dem B-Atom zu adsorbieren. Die Adsorptionsenergie von NO/BAs betrug – 0,18 eV, der Ladungstransfer betrug – 0,01e vom NO-Gasmolekül zu BAs und der Abstand der NO-BAs betrug 2,86 Å. Es gab viele Linien auf dem Fermi-Energieniveau. Es stellte sich heraus, dass die Energielücke im mittleren Band den Bandlückenwert reduziert. Aus dem Zustandsdichtediagramm ergab sich ein zusätzlicher Wellenpeak oberhalb des Fermi-Energieniveaus, aber es gab nur eine geringe Änderung unterhalb des Fermi-Energieniveaus, relativ stabil in Abb. 3. Die Vermischung der Orbitale verursachte einen geringen Ladungstransfer und eine Umverteilung über die wechselwirkenden Region. Die Populationsanalyse für den Mulliken-Ladungstransfer zeigte, dass eine Ladung von 0,01e von der BAs-Oberfläche auf das NO-Molekül übertragen wurde, was darauf hindeutet, dass NO als Donor fungiert. Es gab keine Abweichung der DOS im Bereich von − 7 bis 4 eV, was darauf hindeutet, dass NO wöchentlich an BAs adsorbiert wurde.
NEIN 2 Adsorption: NEIN2 Gasmoleküle neigten dazu, oben auf dem As-Atom zu adsorbieren. Die Adsorptionsenergie von NO2 /BAs war − 0.43 eV, und der Abstand von NO2 -BAs war 2,47 . Das Interessante war, dass der Nullpunkt in der Bande direkt nach der Adsorption von NO2 . eine gerade Linie kreuzte Gasmolekül, was bedeutete, dass das BAs, ein Halbleiter, in das Goldattribut umgewandelt wurde; die Bandlücke betrug 0 eV. Es gab keine große Änderung im Ganzen, und es wurde ein Peak bei etwa − 3 eV aufgrund von NO2 . erzeugt Gasmolekulare Adsorption. Es gab einen offensichtlichen Wellenberg der Energie von − 7 eV und 2 eV, der große Beiträge zur DOS hatte. Im Allgemeinen ist die Adsorption von NO2 von BAs war besser als die einiger oben genannter Moleküle.
NH 3 Adsorption: NH3 Gasmoleküle neigten dazu, oben auf dem As-Atom zu adsorbieren. Die Adsorptionsenergie von NH 3 / BA war -0,34 eV, der Ladungstransfer von NH 3 Gasmoleküls zu BA betrug 0,007e, und der Abstand von NH 3 -BA war 3,27 Å. Es gab keine klare Änderung im Energieband und in der Zustandsdichte, außer dass es einen offensichtlichen Peak der Adsorption von NH3 . gab Gasmolekül unterhalb des Fermi-Niveaus. Das NH3 Gasmolekül hatte einen geringen Einfluss auf BAs bei − 8 bis − 4 eV und bildete einen 15 eV-Peak. Der Adsorptionseffekt und die Empfindlichkeit seiner BAs gegenüber NH3 Gasmolekül waren allgemein.
SO 2 Adsorption: SO2 Gasmolekül neigte dazu, am zentralen Punkt zu adsorbieren, die Adsorptionsenergie von SO2 /BAs war − 0.92 eV, und die Populationsanalyse für Mulliken-Ladungstransfer zeigte, dass − 0.179e Ladung von der BAs-Oberfläche auf das SO2 . übertragen wurde Gasmolekül, was darauf hindeutet, dass SO2 Gasmolekül wirkt als Akzeptor. Der Abstand des SO2 /BAs war 2,46 Å. Im Vergleich zu anderen Gasmolekülen ist das SO2 /BAs hatten die größte Adsorptionsenergie, den zweitgrößten Elektronentransfer und den kürzesten Abstand des SO2 -BAs. Wie in Abb. 3 gezeigt, hatte das Valenzband von BAs einen offensichtlichen Anstieg und eine verringerte Bandlücke, und aufgrund des adsorbierten SO2 Gasmoleküls konnte anhand der Zustandsdichte festgestellt werden, dass es einen weiteren Wellenpeak bei − 7.5 eV und einen gewissen Transfer auf dem Fermi-Niveau gab. Die Adsorption von SO2 von BAs hatte die ausgezeichnete Wirkung.
Abb. 4i zeigt das Elektronendichtediagramm von SO2 /BAs und die lokale Elektronenüberlappung zwischen BAs und SO2 Gasmolekül. Auf dieser Grundlage zogen wir den Schluss, dass die Adsorption von SO2 durch BAs war physikalische Adsorption. Die in Abb. 5 gezeigte Berechnung von WF war von großer Bedeutung, um die Möglichkeit zu untersuchen, die elektronischen und optischen Eigenschaften (wie Absorptionsspektren und Energieverlustfunktionen) durch Adsorption kleiner Moleküle zu regulieren. Die Austrittsarbeit wurde in der Festkörperphysik als die minimale Energie definiert, die erforderlich ist, um ein Elektron aus dem Inneren eines Festkörpers an die Oberfläche des Objekts zu bewegen. Die Austrittsarbeit von reinen BAs betrug 4,84 eV. NO und NH3 Gasmoleküle waren Donatoren beim Ladungstransfer, und ihre Austrittsarbeit nahm ab; die Austrittsarbeit betrug 4,80 eV bzw. 4,68 eV. Die Austrittsarbeit von N2 /BAs, CO2 /BAs und CO/BAs war das gleiche wie bei BAs. Die Austrittsarbeit von O2 /BAs, NO2 /BAs und SO2 /BAs war höher als BAs. In Kombination mit der obigen Adsorptionsenergie, dem Abstand der Gasmoleküle und der BAs-Oberfläche, dem Ladungstransfer und der Austrittsarbeit fanden wir heraus, dass SO2 Gasmolekül war am besten geeignet für BAs-Materialien.
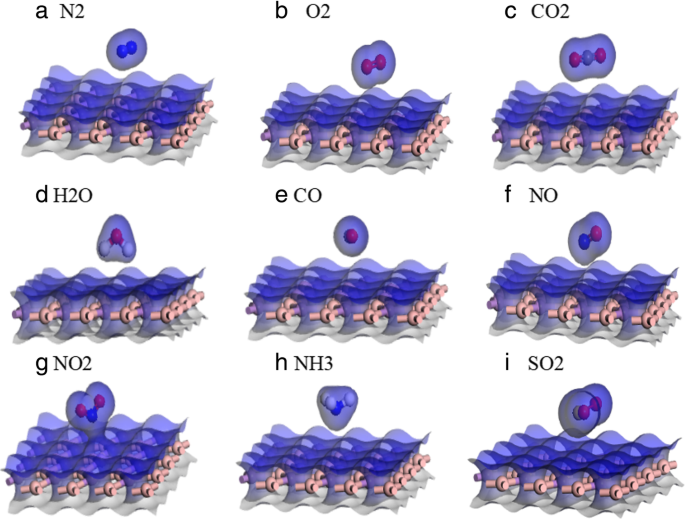
Elektronendichte für reines N2 /BAs (a ), O2 /BAs (b ), CO2 /BAs (c ), H2 O/BAs (d ), CO/BAs (e ), NO/BAs (f ), NO2 /BAs (g ), NH3 /BAs (h ) und SO2 /BAs (i )
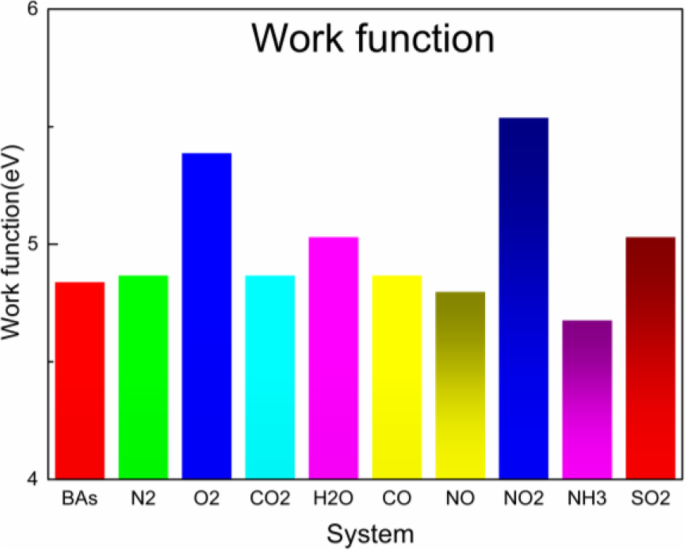
Austrittsarbeit von BAs N2 /BAs, O2 /BAs, CO2 /BAs, H2 O/BAs, CO/BAs, NO/BAs, NO2 /BAs, NH3 /BAs und SO2 /BAs
Schlussfolgerung
Wir haben die strukturellen und elektronischen Eigenschaften von BAs mit den Adsorbentien N2 . vorgestellt , O2 , CO2 , H2 O, CO, NEIN, NEIN2 , NH3 , und SO2 Gasmolekül, unter Verwendung der Methode der Dichtefunktionaltheorie. In der Adsorptionsenergie ist SO2> NEIN2> H2 O > O2> NH3> CO2> CO > N2> NO und SO2 < NEIN2 < NEIN
Abkürzungen
- BAs:
-
Hexagonales Borarsenid
- DOS:
-
Dichte der Zustände
- WF:
-
Arbeitsfunktion
Nanomaterialien
- Auswahl der Lösungsmittelfarbstoffe bester Qualität für eine perfekte Anwendung
- 10 Faktoren, um den perfekten Schalter für Ihre Anwendung zu finden
- Das Potenzial für die Integration visueller Daten in das IoT
- Was ist das beste Gas für das MIG-Schweißen?
- So wählen Sie den richtigen Sensor für Abfüllanwendungen aus
- Tragbarer Gassensor für Gesundheits- und Umweltüberwachung
- WiFi-RSSI-Sensor-Tracker für die ISS
- Mq-3-Gassensor:Der ultimative Leitfaden zu einem Alkoholsensor
- Das richtige Elektrodenmaterial für Ihre Widerstandsschweißanwendung
- So wählen Sie den richtigen Filter für Ihre Anwendung aus



