Eine neue Methode ohne organisches Lösungsmittel zu zielgerichtetem Nanowirkstoff für eine verbesserte Wirksamkeit bei Krebs
Zusammenfassung
Da die hydrophobe Gruppe für die Synthese der arzneistoffbeladenen Nanopartikel immer essentiell ist, verlassen sich die meisten Verfahren stark auf organische Lösungsmittel, die möglicherweise nicht vollständig entfernt werden und eine potenzielle Gefahr für die Patienten darstellen könnten. In dieser Studie haben wir mit 10 Hydroxycamptothecin (HCPT) beladene, mit Folat (FA) modifizierte Nanonadeln (HFNDs) vollständig „grün“ synthetisiert für eine hocheffiziente Krebstherapie mit hoher Wirkstoffbeladung, Targeting-Eigenschaft und Bildgebungsfähigkeit. Es sollte beachtet werden, dass bei dem Herstellungsverfahren kein organisches Lösungsmittel verwendet wurde. Die In-vitro-Zellaufnahmestudie und die In-vivo-Verteilungsstudie zeigten, dass die HFNDs mit FA auf der Oberfläche eine offensichtlich zielgerichtete Eigenschaft zeigten und leichter in die HeLa-Zellen eindrangen als die Chitosan-HCPT-Nanonadeln ohne FA-modifizierte (NDs). Die Zytotoxizitätstests zeigten, dass die HFNDs eine bessere Abtötungsfähigkeit für HeLa-Zellen besaßen als das einzelne Medikament oder die NDs in der gleichen Dosis, was auf ihre gute Antikrebswirkung hindeutet. Das In-vivo-Antikrebs-Experiment zeigte außerdem die ausgeprägten Antikrebswirkungen und die geringeren Nebenwirkungen der HFNDs. Diese neue Methode ohne organisches Lösungsmittel wird zu einem vielversprechenden System zur nachhaltigen Wirkstoffabgabe für die Krebsdiagnose und -behandlung führen.
Hintergrund
Im Laufe der letzten zwei Jahrzehnte konzentrierte sich die Forschung darauf, die suboptimalen pharmakokinetischen Eigenschaften der Chemotherapie zu verbessern, um deren Wirksamkeit zu erhöhen [1, 2]. Es wurden bedeutende Fortschritte erzielt und viele multifunktionale Wirkstoffabgabesysteme auf Nanopartikelbasis erfolgreich hergestellt, die eine breite Palette kombinierter Eigenschaften aufweisen, wie z ,9,10], pH-Empfindlichkeit [11, 12] und anhaltende Wirkstofffreisetzung [9, 13].
In den letzten Jahren hat die nicht-sphärische Partikelform aufgrund ihrer potenziellen Wirkung auf die Wirkstoffabgabe immer mehr Aufmerksamkeit auf sich gezogen [14,15,16,17,18,19]. Es gibt bereits Hinweise darauf, dass die Form einen Einfluss auf viele Eigenschaften der Partikel hat, wie beispielsweise die Bioverteilung und den Abbau [20,21,22]. Vor allem erwies sich die zelluläre Internalisierung als stark formabhängig [23,24,25]. Denn die Partikel müssen in der Lage sein, in Krebszellen einzudringen und auf ihre therapeutischen Ziele einzuwirken, um sie abzutöten. Und viele Studien haben ergeben, dass die Krebszellen Partikel mit einem hohen Aspektverhältnis bevorzugen [10, 26].
Die meisten dieser Methoden basieren jedoch stark auf organischen Lösungsmitteln, hauptsächlich aufgrund der hydrophoben Gruppe, die in den Herstellungsprozessen von Nanopartikeln benötigt wird [27]. Diese organischen Lösungsmittel können in den Partikeln zurückbleiben und können durch herkömmliche Verfahren, wie Destillation bei vermindertem Druck oder Gefriertrocknung, nicht vollständig entfernt werden. Dadurch verbleiben Spuren organischer Lösungsmittel im Arzneimittel, die als Restlösungsmittel bezeichnet werden. Obwohl Restlösungsmittel sehr gering sind und den speziellen Anweisungen in Pharmakopöen entsprechen können, die die maximal zulässigen Mengen von Restlösungsmitteln in pharmazeutischen Produkten streng kontrollieren, sammeln sich die Restlösungsmittel im Körper an und können die Krankheit verschlimmern oder andere schwerwiegende Folgen haben Probleme. Daher streben die Hersteller danach, die Menge der im Arzneimittelherstellungsprozess verwendeten organischen Lösungsmittel zu minimieren. Daher wird es für die Medizin, die menschliche Gesundheit und die Umwelt ein ziemlich großer Sprung sein, „grüne“ Chemie in der pharmazeutischen Industrie einzusetzen, obwohl sie mit vielen Schwierigkeiten konfrontiert ist.
In dieser Studie haben wir HCPT-beladene, Folat (FA)-modifizierte Nanonadeln (HFNDs) mit einem hohen Aspektverhältnis und scharfen Enden über eine vollständig umweltfreundliche Methode ohne Verwendung von organischen Lösungsmitteln entwickelt. Die pH-kontrollierte Fällung des HCPT und FA-modifizierten Chitosan (CS-FA) führt zur Nukleation von Nanonadeln mit nanokristallinem HCPT als Kern, umhüllt mit CS-FA als sterischen Stabilisatoren. Es wurde festgestellt, dass die HFNDs gute Ziel- und Bildgebungseigenschaften aufweisen. Anschließend wurden In-vitro- und In-vivo-Studien systematisch untersucht. Diese Ergebnisse unterstreichen das große Potenzial von FA-modifizierten, bildgebenden Nanonadeln für eine hocheffiziente Chemotherapie sowie für Anwendungen in der Krebsdiagnostik.
Methoden
Materialien
Alle Chemikalien sind von analytischer Qualität und werden wie erhalten ohne weitere Reinigung verwendet. In allen Experimenten wurde entionisiertes (DI) Wasser verwendet. FA wurde von Bio Basic Inc. bezogen. 10-Hydroxycamptothecin (HCPT; Reinheit> 99%) wurde von Lishishen Pharmaceutical Co., Ltd. bezogen. Chitosan (Mw =70.000, 90% Deacetylierungsgrad) wurde von Zhejiang Aoxing bezogen. N -Hydroxysuccinimid (NHS) und 1-(3-Dimethylaminopropyl)-3-ethylcarbodiimid-Hydrochlorid (EDC) wurden von Sigma-Aldrich bezogen.
Synthese des FA-Chitosan-Konjugats
FA (10 mg), Chitosan (20 mg), EDC (4 mg) und NHS (4 mg) wurden in 2 ml PBS-Pufferlösung (pH 5,5) gegeben und 12 h bei RT gerührt, um die CS-FA-Suspension zu erhalten . Dann wurde die Suspension gegen eine Pufferlösung (pH 10) dialysiert, um überschüssige FA-Moleküle zu entfernen. Die verbleibende Suspension wurde zentrifugiert (5000 U/min) und für 24 h lyophilisiert, um das trockene CS-FA-Pulver zu erhalten.
Vorbereitung von HFNDs
HCPT (10 μg) wurde in 200 μl wässriger NaOH-Lösung (0,1 M) gelöst, um Lösung A zu erhalten, und CS-FA (10 μg) wurde in 200 μl HCl (0,1 M) gelöst, um Lösung B zu erhalten. Danach Lösung A und Lösung B wurden tropfenweise in reines Wasser (1 ml) unter kräftigem Rühren 30 s lang zugegeben, und die Mischung wurde 6 min lang in einem Eisbad beschallt (200 W). Die Suspension wurde zentrifugiert (10.000 U/min, 5 min) und 24 h lyophilisiert. Für die Herstellung von NDs wurde die Chitosanlösung verwendet, um die Lösung B zu ersetzen.
Charakterisierung
Die Morphologie der HFNDs wurde durch SEM (UV-70) bei 15 kV untersucht. Die Größen- und Zeta-Potentialwerte wurden mit einer Malvern Zetasizer Nano-ZS-Maschine (Malvern Instruments, Malvern) bestimmt. Zur Ermittlung der Mittelwerte wurden drei parallele Messungen durchgeführt. Die Kristallinität von HFNDs wurde mit XRD (X’pert PRO) analysiert. Der Gehalt an FA in HFNDs wurde durch UV-Spektrophotometrie (Beckman DU800) bestimmt. Alle Proben wurden bei 281 nm untersucht. Zur Bestimmung der FS-Konzentration wurde zuvor die Standardkurve gezogen. Der Gehalt an HCPT in HFNDs wurde durch Fluoreszenzspektrophotometrie bei 383 nm bestimmt. Zur Bestimmung der HCPT-Konzentration wurde zuvor die Standardkurve gezogen. Der Inhalt und die Einschlusseffizienz wurden nach Gl. (1, 2, 3 und 4):
$$ \mathrm{Droge}\ \mathrm{Laden}\ \mathrm{Inhalt}\ \mathrm{of}\ \mathrm{HCPT}\ \left(\%\right)=\left(\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{HCPT}\ \mathrm{in}\ \mathrm{HFNDs}\right)/\left(\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{HFNDs}\right) \times 100\% $$ (1) $$ \mathrm{Entrapment}\ \mathrm{Effizienz}\ \mathrm{of}\ \mathrm{HCPT}\left(\%\right)=\left(\mathrm{ Gewicht}\ \mathrm{of}\ \mathrm{Droge}\ \mathrm{in}\ \mathrm{HFNDs}\right)/\left(\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{Fütterung} \ \mathrm{Droge}\right)\times 100\% $$ (2) $$ \mathrm{Prozentsatz}\ \mathrm{of}\ \mathrm{F}\mathrm{A}\ \mathrm{in}\ \mathrm{die}\ \mathrm{Konjugation}\ \left(\%\right)=\left(\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{FA}\ \mathrm{in}\ \mathrm {Konjugation}\right)/\left(\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{Konjugation}\right)\times 100\% $$ (3) $$ \mathrm{Droge}\ \mathrm {Laden}\ \mathrm{Inhalt}\ \mathrm{of}\ \mathrm{F}\mathrm{A}\ \left(\%\right)=\left(1-\mathrm{Droge}\ \mathrm{ Laden}\ \mathrm{Inhalt}\ \mathrm{ von}\ \mathrm{HCPT}\right) \times \mathrm{Prozent}\ \mathrm{von}\ \mathrm{F}\mathrm{A}\ \mathrm{in}\ \mathrm{der}\ \mathrm {Konjugation}\mal 100\% $$ (4)In-vitro-Studie zur Wirkstofffreisetzung
Die In-vitro-Studie zur Wirkstofffreisetzung von HFNDs wurde unter Verwendung der Dialysetechnik durchgeführt. Die HFNDs wurden in einer PBS-Pufferlösung (10 ml) dispergiert und in einen vorgequollenen Dialysebeutel (MWCO 3500 Da) gegeben. Der Dialysebeutel wurde dann in PBS (0,1 M, 200 ml, pH 7,4) eingetaucht und in einem Schüttelinkubator (100 U/min) bei 37 °C kontinuierlich oszilliert. Alle Proben wurden durch Fluoreszenzspektrophotometrie untersucht.
Konfokale Bildgebung von Zellen
Die konfokale Abbildung von Zellen wurde unter Verwendung eines konfokalen Laserscanning-Mikroskops von Leica durchgeführt. Die Bildgebung von HCPT wurde unter 382-nm-Laseranregung durchgeführt und die Emission wurde im Bereich von 500–550 nm gesammelt. HeLa-Zellen wurden ausgesät und bei 37 °C für 24 h vorinkubiert (5% CO2 .) ) vor der Inkubation mit den HFNDs für 8 h.
Zelluläre Aufnahme gemessen durch Fluoreszenzmessung
HeLa-Zellen wurden in eine 24-Well-Platte ausgesät (1 × 10 6 ml/Vertiefung). Die Platte wurde dann bei 37 °C für 24 h in einer befeuchteten Atmosphäre (5% CO2 .) inkubiert ). Die Zellen wurden dann mit NDs und HFNDs bei äquivalenten Konzentrationen von HCPT inkubiert. Die arzneimittelbehandelten Zellen wurden 6 h bei 37 °C inkubiert, anschließend zweimal mit PBS gewaschen und durch Trypsin-(0,05%)/EDTA-Behandlung verdaut. Die Suspensionen wurden 4 min zentrifugiert (1000 U/min, 4 °C). Die Zellpellets wurden mit PBS gewaschen, um die Hintergrundfluoreszenz im Medium zu entfernen. Nach zwei Wasch- und Zentrifugationszyklen wurden die Zellen mit 2 ml PBS resuspendiert und durch kräftige Beschallung vollständig zerstört. Die Menge an HCPT in der beschallten Mischung wurde durch Fluoreszenzspektroskopie (Anregung bei 382 nm) analysiert. Leerzellen in Abwesenheit des Arzneimittels wurden gemessen, um den Autofluoreszenzspiegel der Zellen als Kontrolle zu bestimmen.
Zytotoxizitätstests
Die Zytotoxizität von HFNDs wurde durch MTT-Assay bestimmt. Kurz gesagt, eine angemessene Anzahl von HeLa-Zellen in der exponentiellen Phase wurde in fünffacher Ausführung in eine 96-Well-Mikroplatte mit flachem Boden ausplattiert und 24 h in Gegenwart von Wirkstoff/Partikeln inkubiert. In dieser Studie wurden 20 μL 3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazoliumbromid (MTT)-Lösung (5 mg/ml in PBS) in jede Vertiefung gegeben. und die Platten wurden weitere 4 h bei 37 °C inkubiert. Danach wurde ein Volumen von 150 μL Dimethylsulfoxid (DMSO) zugegeben und die Platte wurde 30 min bei 37 °C auf einem Wasserbad geschüttelt. Die Absorption bei 570 nm wurde mit einem Microplate Reader (Modell 680; Bio-Rad) gemessen.
Bioverteilung
Für die In-vivo-Fluoreszenzbildgebung wurde DiR in die NDs und HFNDs eingekapselt. DiR-NDs und DiR-HFNDs wurden HeLa-Tumor-tragenden Nacktmäusen über Schwanzvenen in einer äquivalenten Dosis von DiR-HCPT pro Kilogramm Körpergewicht der Maus intravenös verabreicht. In vorbestimmten Zeitintervallen wurden die Mäuse anästhesiert und mit dem Maestro-In-vivo-Bildgebungssystem (Cambridge Research &Instrumentation, Woburn, MA, USA) abgebildet. Nach 24 Stunden wurden die Mäuse getötet und der Tumor sowie die Hauptorgane (Milz, Leber, Niere, Lunge und Herz) herausgeschnitten, gefolgt von Waschen der Oberfläche mit 0,9 % NaCl für die Ex-vivo-Bildgebung.
Tumorhemmung in vivo
Wenn das HeLa-Tumorvolumen der HeLa-Tumor-tragenden Mäuse ungefähr 60 mm 3 . betrug , wurden die Mäuse nach dem Zufallsprinzip in vier Gruppen eingeteilt und alle 3 Tage durch intravenöse Injektion von 0,9 % NaCl, freiem HCPT, NDs und HFNDs in einer Dosis von 80 μg HCPT pro Maus behandelt. Das Tumorvolumen und das Körpergewicht wurden alle 3 Tage überwacht. Das Tumorvolumen wurde nach folgender Formel berechnet:Tumorvolumen = 0.5 × Länge × Breite 2 .
Nach 21 Tagen wurden die Mäuse getötet, gefolgt von der Exzision und dem Wiegen der Tumoren. Dann wurden die Tumore über Nacht bei 4 °C in 4 % Paraformaldehyd fixiert, in Paraffin eingebettet, geschnitten (4 μm), mit Hämatoxylin und Eosin (H&E) gefärbt und mit einem digitalen Mikroskopiesystem beobachtet.
Statistische Analyse
Die statistische Signifikanz der Behandlungsergebnisse wurde mit dem t . von Student Test (zweiseitig); P < 0,05 wurde in allen Analysen als statistisch signifikant eingestuft (95% Konfidenzniveau).
Ergebnisse und Diskussion
Synthese des FA-Chitosan-Konjugats
Zuerst haben wir FA durch eine Amidierungsreaktion zwischen der Carboxylendgruppe von FA und dem Amidogen von Chitosan an Chitosan konjugiert (Abb. 1). Die Struktur der Konjugation (CS-FA) wurde durch Fourier-Transformations-Infrarot-(FT-IR)-Spektroskopie bestätigt. Wie in Abb. 2 gezeigt, wurde der Peak bei 1605/cm im IR-Spektrum von CS-FA stärker als der von Chitosan, entsprechend der C=O-Streckschwingung der neuen Amidobindung. Das Ergebnis zeigte, dass FA erfolgreich über eine Amidobindung an das Amidogen von Chitosan konjugiert wurde. Um den Prozentsatz von FA in der Konjugation zu untersuchen, wurde eine Standardkurve durch Ultraviolett-Spektrophotometrie erstellt. Und der Prozentsatz von FA wurde mit 23,4 ± 2,5% berechnet.
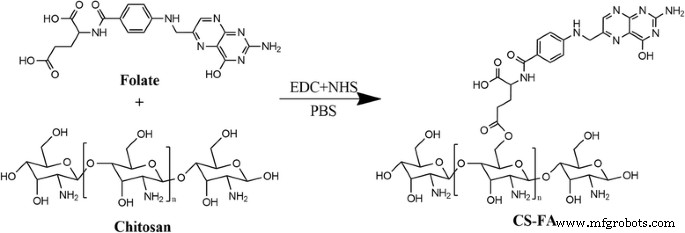
Syntheseroute des CS-FA-Konjugats
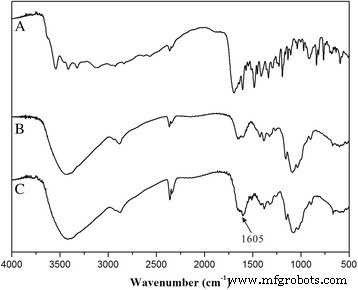
FTIR-Spektren von (a ) FA, (b ) Chitosan und (c ) CS-FA
Vorbereitung von HFNDs
Es ist allgemein bekannt, dass HCPT in Wasser extrem schlecht löslich ist, sich jedoch in Alkali lösen kann. Das Chitosan ist genau das Gegenteil:löslich in Säuren und unlöslich in Wasser. Und das CS-FA zeigte eine ähnliche Löslichkeit wie das Chitosan. Daher wurden das HCPT und das CS-FA in Alkali bzw. Säuren gelöst. Wenn die beiden Lösungen gemischt wurden, fand eine Neutralisationsreaktion statt. Die hergestellte Mischung wurde so eingestellt, dass sie neutral war, was ein schlechtes Lösungsmittel sowohl für HCPT als auch für CS-FA wäre. Die durch pH-Änderungen ausgelöste Abnahme der Löslichkeit bot die Möglichkeit zur Nukleation von HCPT-Nanonadeln und der begleitenden Kopräzipitation von CS-FA auf den wachsenden HCPT-Nanonadeln (Abb. 3a). Die dynamische Nukleation und Präzipitation der Nanonadeln unter Ultraschall sowie die aktive Okklusion des weichen Bestandteils CS-FA führten zur Bildung von HFNDs anstelle von HCPT-Bulkkristallen. Um die Formulierungsbedingungen zu optimieren, wurde ein Bedingungsexperiment entworfen, um die Wirkung des Verhältnisses von HCPT zu CS-FA, der Ultraschallleistung, des pH-Werts der hergestellten Mischung und der Konzentration der hergestellten Mischung auf die Morphologie von HFNDs zu untersuchen (Tabelle 1).
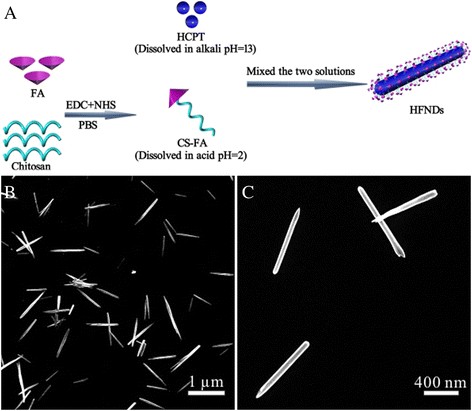
a Illustration der völlig grünen Methode zur Herstellung von HFNDs. b , c Die REM-Bilder von HFNDs
Abbildung 4 zeigt die Morphologie der Partikel unter verschiedenen Bedingungen. Wenn CS-FA zu viel war, lagerte sich überschüssiges CS-FA an der Oberfläche der produzierten Partikel an (Abb. 4a). Während CS-FA zu wenig war, konnte CS-FA das Wachstum der HCPT-Nanonadeln, die zur Aggregation neigten, nicht stoppen (Abb. 4b). Da die Nukleation durch pH-Änderungen ausgelöst wurde, spielte der pH-Wert der hergestellten Mischung eine wichtige Rolle im Herstellungsprozess. Der pH-Wert sollte auf neutral eingestellt werden, sonst würde die Kristallisation beschädigt (Abb. 4c). Auch die Ultraschallleistung hatte einen großen Einfluss auf die Morphologie der HFNDs. Die Nanonadeln würden bei niedriger Leistung aggregieren (Abb. 4d) und bei hoher Leistung in Fragmente zerfallen (Abb. 4e). Darüber hinaus wurde festgestellt, dass die Konzentration der hergestellten Mischung einen großen Einfluss auf die Größe der HFNDs hat. Die Größe nahm durch Erhöhung der Konzentration ab (Abb. 3b und 4f).
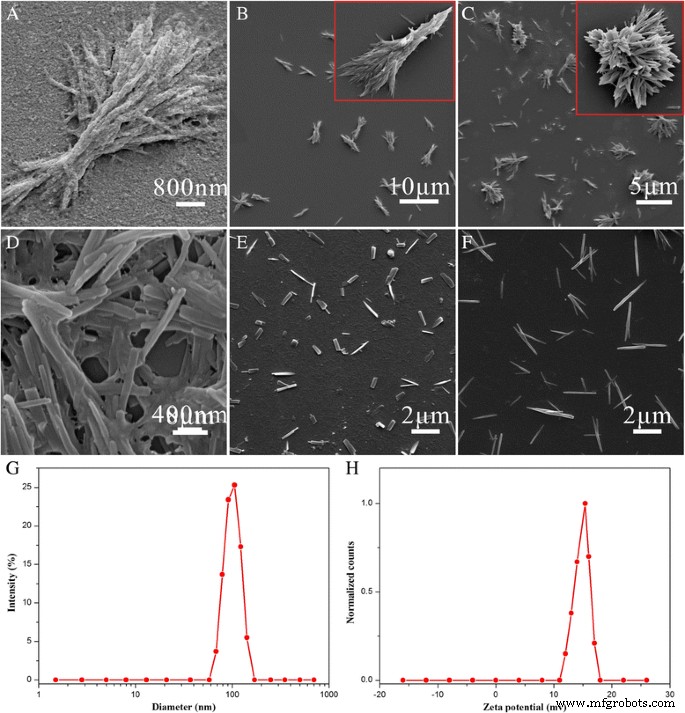
a –f Die REM-Bilder von HFNDs unter verschiedenen Bedingungen (siehe Details in Tabelle 1). g Partikelgrößenverteilung der HFNDs. h Zetapotential der HFNDs
Abbildung 3b, c zeigt die optimierte nadelförmige Morphologie der HFNDs mit einer durchschnittlichen Länge von etwa 800 nm und einer Breite von etwa 80 nm. Das Ergebnis der DLS-Messung zeigt eine Größe von 104,3 ± 5,7 nm (Abb. 4g) und ein Zetapotential von +16,3 ± 1,9 mv (Abb. 4h). Darüber hinaus zeigte eine HFND-Dispersion mit 2 Gew.-% eine gute Stabilität für mindestens 2,5 Tage. Da es keine Fluoreszenzsignale von CS-FA gibt, können wir den HCPT-Wirkstoffbeladungsgehalt der HFNDs unter Verwendung der Fluoreszenzeigenschaften von HCPT messen. Der HCPT-Wirkstoffbeladungsgehalt der HFNDs betrug 70,2 ± 3,1% und die Einkapselungseffizienz betrug 83,1%. Und der FA-Gehalt der HFNDs betrug 7,0%, der über den Prozentsatz von FA in CS-FA berechnet wurde.
XRD-Analyse
Bekanntlich beeinflusst die Wirkstoffform stark die Eigenschaften der Nanopartikel. Daher ist es von großer Bedeutung, die Form von HCPT in den HFNDs zu verstehen. Röntgenbeugung wurde verwendet, um die Form von HCPT innerhalb der HFNDs nachzuweisen (Abb. 5). Es ist klar, dass reines HCPT viele scharfe kristalline Peaks aufweist, die für die Eigenschaften einer hohen Kristallinität repräsentativ sind. Während die breiten Peaks von semikristallinem Chitosan im XRD-Muster der HFNDs noch vorhanden waren, gehörte die Mehrheit der Peaks zu HCPT, was auf die hohe Kristallinität von HCPT hindeutet. Kurz gesagt legen die XRD-Ergebnisse nahe, dass sich HCPT in HFNDs im kristallinen Zustand befindet. Darüber hinaus hatte sich die Wachstumskinetik von HCPT innerhalb der HFNDs verändert, hauptsächlich aufgrund der aktiven Okklusion und der einschränkenden Wirkung von CS-FA. Um die Wirkung von CS-FA im Kristallisationsprozess zu untersuchen, wurden die HCPT-Kristalle ohne das Vorhandensein von CS-FA hergestellt. Abbildung 6 zeigt die Morphologie der HCPT-Kristalle. Sie waren stäbchenförmig und hatten eine Länge von mehr als 10 μm, was sich völlig von der von HFNDs unterschied. Dies zeigte weiter, dass CS-FA die Wachstumskinetik von HCPT innerhalb der HFNDs verändert hatte.
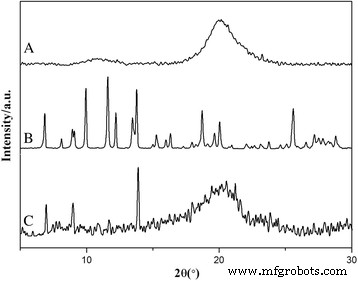
Die XRD-Muster von (a ) Chitosan, (b ) HCPT und (c ) MHNDs

Das REM-Bild von HCPT-Volumenkristallen
In-vitro-Studien zur Wirkstofffreisetzung
Da das Arzneimittelfreisetzungsverhalten eine wichtige Eigenschaft für ein Arzneimittelabgabesystem ist, wurden die in vitro-Freisetzungsstudien der HFNDs unter Verwendung einer Dialysetechnik zusammen mit freien HCPT-Pulvern durchgeführt. Alle Proben wurden durch Hochleistungsflüssigkeitschromatographie (HPLC) untersucht. Die Freisetzungsprofile sind in Abb. 7 dargestellt. Das Profil von freiem HCPT zeigte, dass mindestens 30 % des Arzneimittels zum ersten Probenahmezeitpunkt von 1 h und fast 100 % nach 18 h freigesetzt wurden. Das Freisetzungsprofil der HFND scheint jedoch eine bemerkenswert verlängerte und anhaltende Freisetzung der beiden Medikamente über 48 Stunden zu sein. Die verlängerte Wirkstofffreisetzung kann darauf zurückgeführt werden, dass die polymere Hülle von CS-FA die Wirkstofffreisetzung im Kern begrenzen könnte. Diese Vorteile könnten die Anwendung der HFNDs für ein nachhaltiges Arzneimittelabgabesystem fördern.
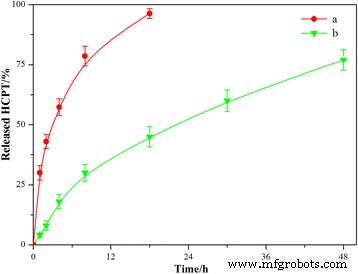
In-vitro-Wirkstofffreisetzungsprofile der MHNDs in PBS (pH 7,4) bei 37 °C. (a ) Kostenlose HCPT; (b ) HFNDs
Mobilfunkaufnahme
Unabhängig davon, wie das Wirkstoffabgabesystem die Zieltumorstelle durch systemische Verabreichung oder durch direkte lokale Verabreichung erreicht, ist es von großer Bedeutung, wenn sie in den Tumorbereich eindringen können, um auf ihr intrazelluläres Ziel einzuwirken. Konfokale Laser-Scanning-Mikroskopie (CLSM) wurde durchgeführt, um die zelluläre Aufnahme von HFNDs zu beurteilen. Um ihre Effizienz der zellulären Aufnahme durch HeLa-Zellen zu bewerten, wurden die HFNDs und die HCPT-beladenen Nanonadeln (NDs; Wirkstoffbeladung = 64,7%) mit HeLa-Zellen für 8 h bei 37 °C inkubiert (die NDs wurden mit HCPT und Chitosan über die gleiche Methode wie die HFNDs). Wie in Abb. 8 gezeigt, wurde eine viel intensivere Fluoreszenzemission von HCPT von den HFND-exponierten Zellen nachgewiesen als von denen, die nach 8 Stunden Inkubation den NDs ausgesetzt waren, was zeigt, dass die FA auf der Oberfläche der Partikel stark ansteigen konnte die zelluläre Aufnahme.
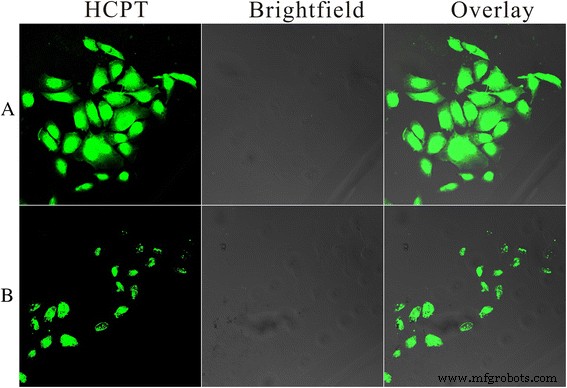
Intrazelluläre Arzneimittelabgabe für 8 h bei 37 °C. Konfokale Laser-Scanning-Mikroskopie-Bilder von HeLa-Zellen, die mit a . inkubiert wurden HFNDs und b NDs
Um weiter zu bestätigen, dass die zelluläre Internalisierungsrate der HFNDs schneller war, wurden Fluoreszenzmessungen durchgeführt, um den Unterschied der Fluoreszenzemissionsintensität von HCPT in den HeLa-Zellen zu quantifizieren. In Übereinstimmung mit den CLSM-Beobachtungen wurden HFNDs im zellulären Internalisierungsprozess viel bevorzugter als NDs (Abb. 9). Dadurch wurde die Targeting-Eigenschaft von HFNDs weiter bestätigt.
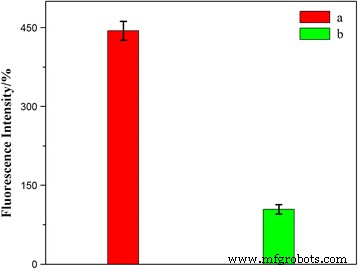
Fluoreszenzmessungen der mit HFNDs inkubierten HeLa-Zellen (a ) und NDs (b ) über eine 8-stündige Inkubationszeit bei 37 °C; P < 0.05
Zytotoxizitätstests
Um die Möglichkeit der Verwendung der HFNDs für die lokale Wirkstoffabgabe weiter zu untersuchen, testeten wir die Abtötungsfähigkeit der HFNDs für Krebszellen. Die Zytotoxizität von HFNDs wurde unter Verwendung des MTT-Assays mit den HeLa-Zellen bewertet. Die freien HCPT und NDs, die äquivalente Konzentrationen von HCPT enthielten, wurden als Kontrolle verwendet. Die HCPT-Konzentrationen betrugen 0,50, 1,00, 2,00, 4,00, 8,00 und 16 μg/ml. Wie in Abb. 10 gezeigt, war die Zytotoxizität von HCPT höher als die von NDs, hauptsächlich aufgrund der viel schnelleren Wirkstofffreisetzungsrate von HCPT als der von NDs. Trotzdem war die Zytotoxizität der HFNDs höher als die von HCPT. Dies lag wahrscheinlich an der zielgerichteten Eigenschaft von FA auf der Oberfläche der HFNDs, die den Partikeln helfen könnte, in die Zellen einzudringen und sie abzutöten. Somit zeigten die HFNDs den Krebszellen eine überraschend gute Abtötungsfähigkeit. Diese Ergebnisse bestätigen, dass FA auf der Oberfläche der HFNDs die zelluläre Aufnahme der Partikel und damit ihre Abtötungsfähigkeit für Krebszellen durch Bindung an FA-Rezeptoren erhöhen kann.
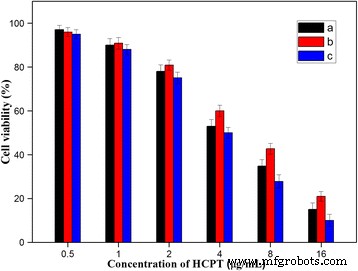
In-vitro-Zelllebensfähigkeit von HeLa-Zellen, die mit (a ) kostenloses HCPT, (b ) NDs und (c ) HFNDs nach Inkubation von 24 h. P < 0.05
Bioverteilung
Um die Tumorzielfähigkeit von Dual-Drug-Nanonadeln zu bewerten, wurde DiR als Nahinfrarot-Fluoreszenzsonde verwendet, die bei der äquivalenten DiR-Konzentration in freie HCPT, NDs und HFNDs eingekapselt werden sollte. 0,9% NaCl, DiR-NDs und DiR-HFNDs wurden intravenös in die Mäuse-tragenden Tumoren injiziert, die aus humanen Zervixkarzinom-HeLa-Zellen stammten, und ihre in-vivo-Bioverteilung wurde untersucht.
Wie in Abb. 11a dargestellt, wurde in der DiR-ND-Gruppe ein starkes Fluoreszenzsignal in der DiR-HFND-Gruppe sichtbar gemacht, während an Tumorstellen keine Fluoreszenzsignale nachgewiesen wurden. Wenn die Gesamtfluoreszenzzahlen die ganze Zeit reduziert wurden, wurde die Intensität des Signals an der Tumorstelle von 1 auf 12 h erhöht, was darauf hindeutet, dass sich die HFNDs während dieser Zeit in Tumoren anreicherten. Nach 24 h wurden die Mäuse getötet und das Tumorgewebe sowie das normale Gewebe für die ex vivo-Bildgebung und -Analyse isoliert (Abb. 11b, c). Die Fluoreszenzintensität im Tumorgewebe von mit DiR-HFNDs behandelten Mäusen war signifikant höher als bei den anderen Mäusen. Es wurde bestätigt, dass die Einführung von FA den Nanonadeln eine ausgezeichnete Wirksamkeit bei der Tumor-Targeting-Wirkung bot, was zu einer hocheffizienteren Krebsbehandlung führte.
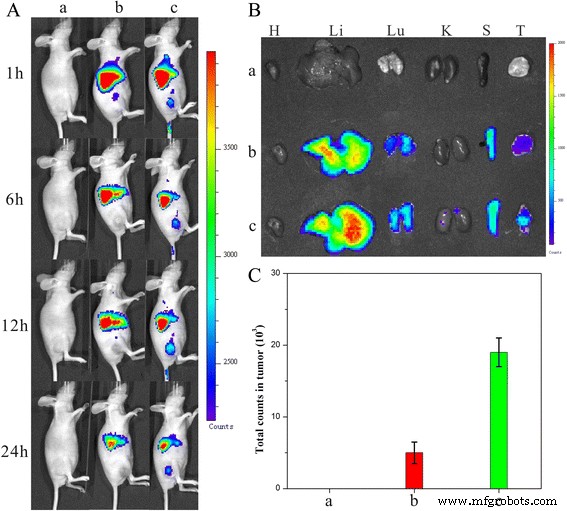
a Verteilung und Tumorakkumulation von DiR-Nanopartikeln in HeLa-Tumor-tragenden Mäusen, die eine intravenöse Injektion der angegebenen Formulierungen erhalten. b Ex-vivo-Fluoreszenzbildgebung des Tumors und des normalen Gewebes, das von den eingeschläferten HeLa-Tumor tragenden Nacktmäusen gewonnen wurde. Die Bilder wurden 24 h nach der Injektion aufgenommen. H, Li, Lu, K, S und T stehen für Herz, Leber, Lunge, Niere, Milz bzw. Tumor. c DiR-Fluoreszenzintensität in Tumorgeweben, die 24 h nach der systemischen Injektion gesammelt wurden. P < 0,05. (a ) 0,9% NaCl, (b ) DiR-NDs und (c ) DiR-HFNDs
Tumorhemmung in vivo
Um die in-vivo-Antitumorwirkungen zu bewerten, erzeugten wir HeLa-Tumor-Xenotransplantate in Kunming-Mäusen und bewerteten das Tumorwachstum nach der intravenösen Verabreichung von 0,9% NaCl, freiem HCPT, NDs und HFNDs mit der gleichen Konzentration von HCPT. Im Vergleich zu den Mäusen, die mit 0,9% NaCl als Kontrolle behandelt wurden, nahm die Wachstumsrate der Tumore bei Mäusen, die freie HCPT oder NDs erhielten, allmählich ab (Abb. 12a), was auf die signifikant wirksame Hemmung des Tumorwachstums hinweist. Bemerkenswert ist, dass die HFNDs zur stärksten Hemmung des Tumorwachstums führten. Am Ende des Experiments wurden die Tumoren herausgeschnitten und gewogen. Wie in Abb. 12c gezeigt, wurde festgestellt, dass die Nanonadeln mit zwei Wirkstoffen im Vergleich zu den anderen Gruppen eine überlegene therapeutische Wirksamkeit aufwiesen (P < 0,05). Ein zusätzlicher Beweis für die verstärkte Antikrebswirkung der Dual-Drug-Nanonadeln wurde in den histologischen Bildern gezeigt (Abb. 12d). Bei allen Arzneimittelabgabesystemen sollte die systemische Toxizität, die normalerweise bei der freien HCPT-vermittelten Behandlung auftritt, berücksichtigt werden, um Sicherheit und Wirksamkeit zu gewährleisten. In dieser Arbeit führte die Verabreichung des freien HCPT zu Antriebslosigkeit/Faulheit und starkem Körpergewichtsverlust von Mäusen (Abb. 12b), was auf die unerwünschten Nebenwirkungen der Chemotherapie hinweist. Im Gegensatz dazu wurden bei den mit NDs und HFNDs behandelten Mäusen keine offensichtlichen Nebenwirkungen gezeigt. Insgesamt wurde darauf hingewiesen, dass die HFNDs mit den überlegenen Antikrebswirkungen sowie der geringeren Toxizität die Wirksamkeit der Lebensqualitätstherapie erheblich verbessern würden.
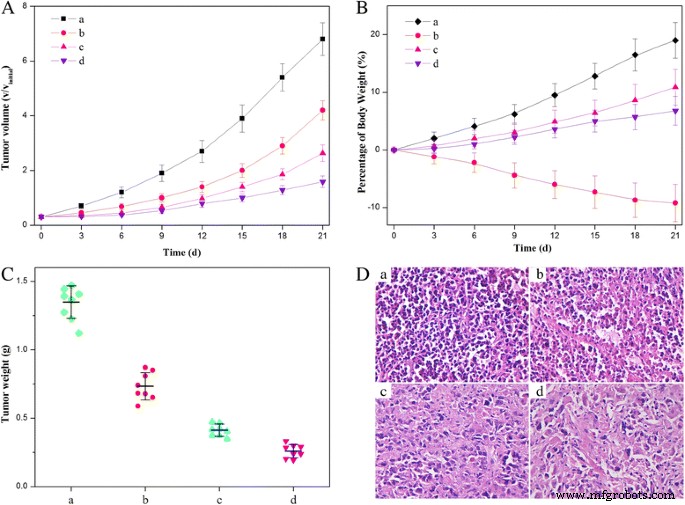
Antikrebswirkung verschiedener (Nano-)Formulierungen. a Volumenänderung des Tumors bei Mäusen während der Behandlung. b Gewichtsveränderung der tumortragenden Mäuse während der Behandlung. c Gewichte von HeLa-Tumoren nach Behandlung mit verschiedenen Formulierungen. d Histologischer Schnitt des Tumors der Mäuse nach der Behandlung. (a ) 0,9% wässrige NaCl-Lösung, (b ) kostenloses HCPT, (c ) NDs und (d ) HFNDs. Alle Formulierungen verwendeten die gleiche HCPT-Konzentration in Mäusen-tragenden HeLa-Tumoren. P < 0.05
Schlussfolgerungen
Die vorliegende Studie präsentiert einen vollständig grünen Ansatz, um FA-modifizierte, HCPT-beladene Nanonadeln für die hocheffiziente Chemotherapie mit hoher Wirkstoffbeladung, Targeting-Eigenschaft und Bildgebungsfähigkeit zu erhalten. Das Profil der Wirkstofffreisetzung zeigte, dass die HFNDs eine anhaltende und verlängerte Freisetzung zeigten. Das CLSM zeigte die effektivere zelluläre Internalisierung von HFNDs als von NDs. Das MTT-Experiment zeigte, dass die HFNDs nicht nur eine viel höhere Zytotoxizität zeigten als die einzelnen Medikamente und NDs. Dies veranschaulichte die gute Targeting-Eigenschaft der HFNDs. Diese Arbeit öffnet eine Tür, um neue Dosierungen von Nanopartikeln mit vollständig grüner Methode zu entwickeln, die in Zukunft einen starken Einfluss auf den Umweltschutz haben könnten.
Nanomaterialien
- Herstellungsverfahren für künstliche Moleküle gewinnt den besten Posterpreis
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Lieferant für die Automatisierung der medizinischen Montage nimmt neuen Namen für den US-Betrieb an
- Folatrezeptor-gerichtete Bioflavonoid-Genistein-beladene Chitosan-Nanopartikel für eine verbesserte Antikrebswirkung bei Gebärmutterhalskrebs
- Hochleitfähige PEDOT:PSS transparente Lochtransportschicht mit Lösungsmittelbehandlung für Hochleistungs-Silizium/organische Hybridsolarzellen
- Nachbehandlungsmethode zur Synthese monodisperser binärer FePt-Fe3O4-Nanopartikel
- Herstellung und Charakterisierung eines neuen anodischen Tio2-Kohlenstoff-Nanofaser-Verbundkatalysators für eine Direkt-Methanol-Brennstoffzelle mittels Elektrospinnverfahren
- S-dotierter Sb2O3-Nanokristall:ein effizienter Katalysator für sichtbares Licht für den organischen Abbau
- Fragen und Antworten:Eine neue Methode für den 3D-Druck winziger Gelstrukturen
- Die Herausforderung der 5S-Methode für die Industrie 4.0



