Manipulation der Schwefelungstemperatur zur Synthese eines α-NiS-Nanosphärenfilms zur Langzeitkonservierung von nicht-enzymatischen Glukosesensoren
Zusammenfassung
In dieser Studie wurden Alpha-Nickelsulfid (α-NiS)-Nanosphärenfilme durch Elektroplattieren des Nickel-Nanoblattfilms auf dem Indium-Zinn-Oxid (ITO)-Glassubstrat und durch Schwefeln des nickelbeschichteten ITO-Glassubstrats synthetisiert. Zuerst haben wir die Nickel-Nanoblatt-Filme auf den ITO-Glassubstraten galvanisch abgeschieden, die in 0,5 × 1 cm 2 . geschnitten wurden Größe. Zweitens wurden die Nanoblatt-Nickelfilme in vakuumversiegelten Glasampullen mit Schwefelplatten bei unterschiedlichen Tempertemperaturen (300, 400 und 500 °C) für 4 h in vakuumversiegelten Glasampullen getempert. Die α-NiS-Filme wurden mit Röntgenbeugung (XRD), variablem Vakuum-Rasterelektronenmikroskop (VVSEM), Feldemissions-Rasterelektronenmikroskopie/energiedispersivem Spektrometer (FE-SEM/EDS), zyklischem Voltammogramm (CV), elektrochemischen . untersucht Impedanzspektroskopie (EIS), Ultraviolett/sichtbar/nahes Infrarot (UV/sichtbar/NIR) Spektren und Photolumineszenz (PL) Spektren. Auf der Oberfläche der α-NiS-Filme wurden bei einer Glühtemperatur von 400 °C für 4 Stunden viele Nanokugeln beobachtet. Wir haben auch die hochauflösende Transmissionselektronenmikroskopie (HR-TEM) für die Analyse der α-NiS-Nanosphären verwendet. Wir zeigten, dass unser α-NiS-Nanosphärenfilm eine lineare Stromantwort auf verschiedene Glukosekonzentrationen aufwies. Darüber hinaus wurden unsere α-NiS-Nanosphärenfilme bei Raumtemperatur fünfeinhalb Jahre lang aufbewahrt und waren immer noch nützlich zum Nachweis von Glukose in niedriger Konzentration.
Hintergrund
In den letzten zehn Jahren wurde Nickelsulfid (NiS) als gut leitfähig akzeptiert. Es kann als Kathodenmaterial für Lithium-Akkus geschmolzen werden [1,2,3]. Darüber hinaus wurde NiS in Solarspeichern eingesetzt [4, 5]. Es wurde auch nachgewiesen, dass es hervorragende Eigenschaften für die Anwendung in Photokatalysatoren besitzt [6, 7]. NiS-Film kann auch für nicht-enzymatische Glukosesensoren verwendet werden [8, 9]. Über den Glukosenachweis wurden viele Erfassungsverfahren zum Nachweis von Glukose entwickelt. Zu den am weitesten verbreiteten und historisch bedeutsamen Methoden gehörten Kupferjodometrie, Hochleistungsflüssigkeitschromatographie (HPLC), Glukoseoxidase (GC), Kapillarzonenelektrophorese (CZE) und nicht-enzymatischer Glukosesensor [10]. Ein nicht-enzymatischer Glukosesensor wird in Zukunft eine wichtige Anwendung für den Glukosenachweis sein [11]. Wir sind an der Synthese von NiS-Filmen interessiert und erforschen diese Art von Material für eine der wichtigen Anwendungen des nicht-enzymatischen Glukosesensors. In der Sensorkonservierungsstudie kann der nicht-enzymatische Glukosesensor länger konserviert werden als der enzymatische Glukosesensor [12]. In diesem Artikel werden wir den Syntheseprozess des α-NiS-Films beschreiben und unsere Proben demonstrieren, die zum Nachweis von Glukose durch zyklische Voltammogramm (CV)-Messungen und Amperometrie verwendet werden können. Wir fanden auch heraus, dass es keine Berichte über die Aufbewahrung von nicht-enzymatischen Glukosesensoren bei Raumtemperatur für fünfeinhalb Jahre gab. In diesem Artikel haben wir gezeigt, dass unsere α-NiS-Nanosphärenfilme in unserem Labor fünfeinhalb Jahre lang bei Raumtemperatur aufbewahrt wurden und immer noch zum Nachweis von Glukose in verschiedenen Konzentrationen in verschiedenen Lösungen (0,1 M NaOH und Krebs-Puffer) nützlich waren.
Methoden
Vorbereitung der α-NiS-Filme
Für die Herstellung des α-NiS-Films war die Synthesebedingung ein zweistufiger Prozess:Der erste Schritt war die Herstellung des Nickel-Nanoblatt-Films [13, 14] und der zweite Schritt war der Syntheseprozess des α-NiS-Films durch eine Methode des physikalischen Dampftransports (PVT) zum Sulfurieren des Nickel-Nanoblatt-Films [15, 16]. Im ersten Schritt wurde ein Nickel-Nanoblatt-Film über ein einfaches Elektroabscheidungsverfahren synthetisiert. Wir verwendeten eine Platin-Ebenen-Anode und eine Indium-Zinn-Oxid (ITO)-Glaskathode, die in einem kathodischen Elektrotauchlackierungsprozess behandelt wurden, um den Nickel-Nanoblatt-Film herzustellen. Nickelfilme wurden galvanisch auf ITO-beschichteten leitenden Glassubstraten abgeschieden, die in 0,5 × 1 cm 2 . geschnitten wurden Größe. Jeder hatte einen Widerstand von < 15 Ω/cm 2 . 0,1 M Nickelsulfat-Hexahydrat (NiSO4 .) .6H2 O, Sigma-Aldrich, ≥ 98,5%) und 0,05 M Natriumhydroxid (NaOH, SHOWA, 96%) wurden verwendet, um eine Vorläuferlösung in bidestilliertem Wasser herzustellen. Wir haben die Nickelschicht im potentiostatischen Modus verwendet. Wir stellen das Elektrotauchlackierungspotential auf 3,0 V DC mit einer Lösung von pH 7,7 ein. Hochwertige Nickelschichten wurden bei 40 °C für 10 Minuten galvanisch abgeschieden. Nach der Aufnahme von Nickelfilmen wurden die Nickel-Nanoblatt-Filme in vakuumversiegelten Glasampullen mit Schwefelschichten getempert. Die α-NiS-Filme wurden bei verschiedenen Tempertemperaturen (300, 400 und 500 °C) 4 h lang getempert. Wir möchten die optimale Dauer der Glühzeit bestätigen und haben die α-NiS-Schichten bei einer Glühtemperatur von 400 °C für verschiedene Zeiten (3 und 6 h) getempert.
Charakterisierung des α-NiS-Films
Die Morphologie von α-NiS-Filmen wurde unter Verwendung von XRD (SHIMADZU XRD-6000) unter Verwendung von Cu Kα-Strahlung, variabler Vakuum-Rasterelektronenmikroskopie (VVSEM) (HITACHI S-3000N) und FE-SEM/EDS (HITACHI S-4800) charakterisiert. bei 3,0 kV. Die elektrochemischen Eigenschaften von α-NiS-Filmen wurden unter Verwendung von CV-Messungen und Amperometrie mit einer Ag/AgCl-Referenzelektrode durch einen Potentiostaten (Jiehan, ECW-5000) in einer Drei-Elektroden-Konfiguration gemessen. Der α-NiS-Film wurde durch CV-Messungen und Amperometrie in einer 15-ml-Lösung von 0,1 M NaOH mit unterschiedlichen Glucosekonzentrationen bewertet. Die Impedanzmessungen von α-NiS-Filmen wurden mithilfe einer elektrochemischen Impedanzspektroskopie (EIS) (Zennium IM6) in 0,1 M KCl mit 1,5 mM Fe(CN)6 . abgeschätzt 3−/4− . Der α-NiS-Film wurde durch CV-Messungen und Amperometrie in Krebs-Puffer (115 mM NaCl, 2 mM KCl, 25 mM NaHCO3 .) bewertet , 1 mM MgCl2 , 2 mM CaCl2 , 0,25% Rinderserumalbumin [pH 7,4]; Äquilibriert mit 5 % CO2 ) [17]. Die Absorptionsspektren der &agr;-NiS-Filme wurden mit einem UV/Sicht-/NIR-Spektrophotometer (HITACHI U-3501) gemessen, nachdem die &agr;-NiS-Filme in destilliertem Wasser unter Verwendung eines Ultraschall-Dispergierers dispergiert worden waren. Die Photolumineszenz (PL)-Spektren wurden mit einem Fluoreszenzspektrometer (RF-5301PC) mit einem Xenon-Laser bei Raumtemperatur erhalten. Schließlich wurde die Kristallstruktur der α-NiS-Nanokügelchen mit einem HR-TEM-System (JEOL TEM-2010 HR-TEM) untersucht.
Ergebnisse und Diskussion
Wir erhielten die Nickel-Nanoblatt-Filme durch das Elektroabscheidungsverfahren. Wir stellen die DC-Elektroabscheidung auf das Potenzial von 3,0 V DC und 4,0 V DC ein. Wir hielten die Galvanisierungslösung 10 Minuten lang bei 40 °C und beobachteten den galvanisch abgeschiedenen Nickelfilm auf dem ITO-Glassubstrat. Abbildung 1 zeigt die Ergebnisse der galvanischen Abscheidung von Nickelschichten. Wie in Abb. 1a, b zu sehen, hatte die beobachtete Oberfläche des Nickel-Nanoblatt-Films eine durchschnittliche Korngröße von 0,01–0,3 μm bei einem Abscheidungspotential von 3,0 V DC. Der Querschnitt des Nickel-Nanoblatt-Films mit einer Dicke von ungefähr 500 nm wurde im Einschub von Fig. 1b gezeigt. Es wurde beobachtet, dass auf der Oberfläche des Nickelfilms eine durchschnittliche Korngröße von 0,5–1,0 μm bei einem Abscheidungspotential von 4,0 V DC auftrat. Abbildung 1d zeigt die XRD-Muster für die Nickelfilme. Beugungspeaks entsprechend XRD-Mustern für verschiedene Nickelfilme wurden durch Vergleich mit der Karte des Joint of Committee on Powder Diffraction Standards (JCPDS870712) bestätigt. Daher haben wir bestätigt, dass die Endprodukte Nickelfilme waren, wenn die Filme auf dem ITO-Glassubstrat beobachtet wurden.
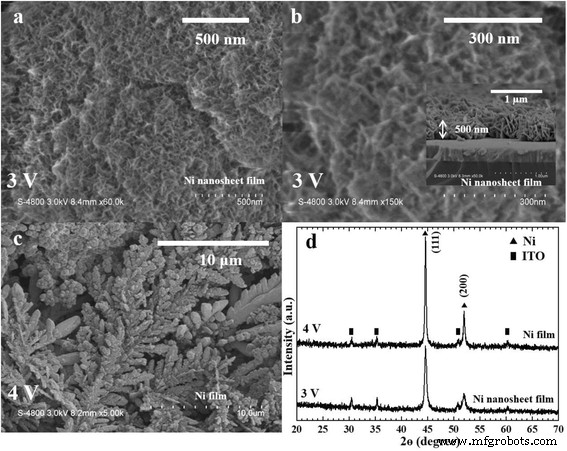
FE-REM-Aufnahmen der Nickelschichten. a , b Die Draufsicht des Nickel-Nanoblatt-Films wurde bei 3,0 V DC galvanisch abgeschieden. Einschub:Querschnitt des Nickel-Nanoblatt-Films. c Die Draufsicht des Nickelfilms wurde bei 4,0 V DC galvanisch abgeschieden. d Die XRD-Muster von Nickelfilmen wurden bei verschiedenen Potentialen (3,0 und 4,0 V DC) galvanisch abgeschieden.
Wir waren der Ansicht, dass der Nickel-Nanoblatt-Film besser als der Nickel-Film war, um die Nanostruktur des &agr;-NiS-Films zu entwickeln. Wir haben die Nickel-Nanoblatt-Filme in unseren Experimenten geschwefelt, um Nano-NiS-Filme zu erhalten. Nachdem Nickelschichten in vakuumversiegelten Glasampullen getempert wurden, erhielten wir die α-NiS-Schichten. Abbildung 2 zeigt die Ergebnisse der Steuerung der verschiedenen Schwefelungstemperaturen zur Synthese von α-NiS-Filmen. Abbildung 2a XRD-Muster zeigten, dass drei α-NiS-Filme bei drei verschiedenen Tempertemperaturen (300, 400 und 500 °C) synthetisiert wurden. Im XRD-Muster jeder Probe beobachteten wir, dass die Beugungspeaks der verschiedenen α-NiS-Filme die gleiche Phase hatten. Beugungspeaks entsprechend XRD-Mustern von α-NiS-Filmen wurden durch Vergleich mit Karten des Joint of Committee on Powder Diffraction Standards (JCPDS750613) bestätigt. Daher bestätigten wir, dass die Endprodukte α-NiS-Filme waren. Abbildung 2b–d zeigten die unterschiedlichen Morphologien der α-NiS-Filme bei drei verschiedenen Tempertemperaturen (300, 400 und 500 °C) für 4 Stunden. Die EDS-Ergebnisse von α-NiS-Filmen mit den Gewichtsprozentsätzen (Gew.-%) der Elemente Schwefel (S) und Nickel (Ni) wurden in den Einfügungen von Abb. 2b–d gezeigt. Abbildung 2b zeigte unregelmäßig geformte Partikel auf der Oberfläche des α-NiS-Films bei einer Glühtemperatur von 300 °C. Wir haben beobachtet, dass die Partikel in Abb. 2b ungefähr 0,5–2 μm groß sind. Das EDS-Ergebnis des α-NiS-Films bei einer Glühtemperatur von 300 °C, 34,99 Gew. % S und 65,01 Gew. % Ni mit einem Molverhältnis von 0,99 (S/Ni) wurde im Einschub von Abb. 2b gezeigt. Wir beobachteten kugelförmige Partikel und eine poröse Struktur von α-NiS mit einer ungefähren durchschnittlichen Größe von 0,1–0,2 μm auf der Oberfläche des α-NiS-Films bei einer Glühtemperatur von 400 °C in Abb. 2c. Das EDS-Ergebnis des α-NiS-Films bei einer Glühtemperatur von 400 °C, 35,75 Gew. % S und 64,25 Gew. % Ni mit einem Molverhältnis von 1,02 (S/Ni) wurde im Einschub von Abb. 2c gezeigt. Wir beobachteten auch kettenartige Partikel von α-NiS mit einer ungefähren durchschnittlichen Größe von 1–5 μm auf der Oberfläche des α-NiS-Films bei der Schwefelungstemperatur von 500 °C in Abb. 2d. Das EDS-Ergebnis des α-NiS-Films bei einer Glühtemperatur von 500 °C, 36,22 Gew. % S und 63,22 Ge % Ni mit einem Molverhältnis von 1,04 (S/Ni) wurde im Einschub von Abb. 2c gezeigt. Wir beobachteten, dass sich die Morphologien (unregelmäßig geformte Partikel, Nanokugeln und kettenförmige Partikel) der Probenoberflächen bei unterschiedlichen Tempertemperaturen (300, 400 und 500 °C) änderten. Im Allgemeinen beobachteten wir eine unterschiedliche Wachstumsentwicklung und Nanostrukturbildung bei den unterschiedlichen Tempertemperaturen. Forscher (Denholme et al.) präsentierten auch, dass die Temperatur die Wachstumskinetik des NiS2 . beeinflusst Filme kontrollierten die unterschiedlichen Morphologien durch Temperaturparameter im Ni-S-System [15]. Dies war auf den S-Dampfdruck zurückzuführen. In ähnlicher Weise wurde begründet, dass der S-Dampf an Reaktionen über Dampf-Feststoff- oder Dampf-Flüssig-Feststoff-Mechanismen an der Ni-Metalloberfläche in S-Dampf- und Ni-Transportreaktionen teilnimmt. Somit wurde die Reaktion in einem geschlossenen System durchgeführt und war vom Dampfdruck der Reaktanten abhängig. Der Dampfdruck war abhängig von der Reaktionstemperatur und dem stöchiometrischen Verhältnis der Reaktanten. Wir dachten, dass die unterschiedlichen Morphologien von NiS im S-Dampfdruck signifikant zunahmen, wenn die Temperaturen mit unterschiedlichen Steigerungen der Ni- und S-Reaktionsrate anstiegen.
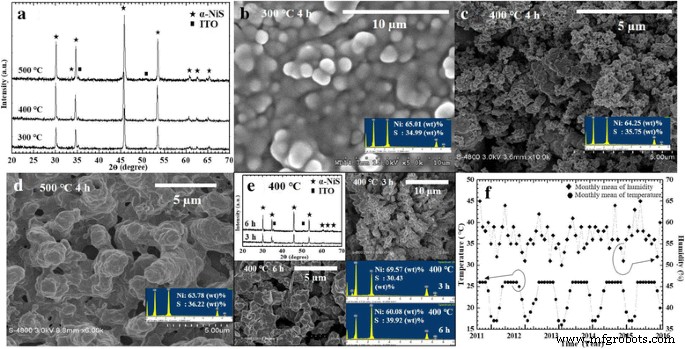
a Das XRD-Muster zeigt die α-NiS-Nanosphärenfilme bei verschiedenen Tempertemperaturen (300, 400 und 500 °C). Die Draufsichtbilder der α-NiS-Filme wurden bei b . getempert 300, c 400 und d 500 °C für 4 h. Einschub:Die EDS-Spektren befanden sich im Einschub von b –d . e Die Bilder zeigten, dass XRD-Muster (oben links), FE-SEM-Bilder (oben rechts, 3 h; unten links, 6 h) und EDS-Spektren (unten rechts) der α-NiS-Filme bei unterschiedlichen Temperzeiten (3 und 6 .) h). f Die Kurven zeigten die Aufzeichnungen über Temperatur- und Feuchtigkeitsmessungen in unserem Labor für Konservierungstests der Bedingungen
Wir wollen auch die optimale Dauer der Glühzeit bestätigen. Die α-NiS-Filme wurden für andere Zeiten (3 und 6 h) bei 400 °C getempert. Die Ergebnisse sind in Abb. 2e dargestellt. Wir beobachteten, dass sich die XRD-Muster der verschiedenen α-NiS-Filme in derselben Phase befanden und durch JCPDS750613-Karten im Einschub (oben links) von Abb. 2e bestätigt wurden. Wir beobachteten, dass die Partikel auf der Oberfläche des α-NiS-Films bei der Schwefelungstemperatur von 400 °C für 3 h im Einschub (oben rechts) von Abb. 2e ungefähr 0,5–1 μm groß waren. Das EDS-Ergebnis des α-NiS-Films bei einer Glühtemperatur von 400 °C, 30,43 Gew. % S und 69,57 Gew. % Ni für 3 h mit einem Molverhältnis von 0,8 (S/Ni) wurde im Einschub gezeigt (unten rechts) von Abb. 2e. Wir beobachteten, dass die Partikel auf der Oberfläche des α-NiS-Films bei der Schwefelungstemperatur von 400 °C für 6 h im Einschub (unten links) von Abb. 2e ungefähr 0,5–2 μm groß waren. Das EDS-Ergebnis des α-NiS-Films bei einer Glühtemperatur von 400 °C, 39,92 Gew. % S und 60,08 Gew. % Ni für 6 h mit einem Molverhältnis von 1,21 (S/Ni) wurde im Einschub gezeigt (unten rechts) von Abb. 2e. Wie im Einschub (EDS-Ergebnis) von Abb. 2c zu sehen ist, zeigte sich, dass für die 4-h-Probe kein Überschuss oder kein Mangel an S vorlag, was nahe am stöchiometrischen Verhältnis von 1 (S/Ni) lag. Schließlich wurde das REM-Bild von Abb. 2c mit mehr Nanokügelchen auf der Oberfläche des α-NiS-Films für die Temperzeit 4 h mit zwei REM-Bildern für unterschiedliche Temperzeiten (3 und 6 h) mit größeren Partikeln in den Einsätzen (oben) verglichen rechts und unten links) von Fig. 2e. Wir haben bestätigt, dass die optimale Temperzeit 4 Stunden beträgt.
Nach der Synthese von α-NiS-Nanosphärenfilmen haben wir einen Teil der α-NiS-Nanosphärenfilme fünfeinhalb Jahre lang in kleinen Plastikbehältern mit Plastikabdeckungen in unserem Labor mit Klimaanlage platziert. Der Zeitpunkt des Konservierungstests für unsere α-NiS-Nanosphärenfolien war vom 1. August 2011 bis 31. Dezember 2016. Wie in Abb. 2f zu sehen, zeigten die Kurven die Temperatur (16–26 °C) und die relative Luftfeuchtigkeit (50–65 %) ), die in unserem Labor für den Konservierungstest vom 1. August 2011 bis 31. Dezember 2016 aufgenommen wurden. Nach Abschluss des Konservierungstests wollten wir die α-NiS-Nanosphärenfilme, die noch die aktuellen Reaktionen bei unterschiedlichen Glucosekonzentrationen zeigten, durch CV-Messungen und Amperometrie bestätigen in einer Lösung im Januar 2017. Wir haben einige Veröffentlichungen über die Messung des elektrochemischen Verhaltens von NiS-Proben für einen nicht-enzymatischen Glukosesensor untersucht. Viele Forscher maßen die Proben durch CV-Messungen und Amperometrie in einer 0,1 M NaOH-Lösung, weil sie die Ergebnisse leicht mit der gleichen Bedingung vergleichen konnten [8,9,10,11,12]. Abbildung 3 zeigt die CV- und Amperometrieeigenschaften von α-NiS-Filmen. Die Fläche der Arbeitselektrode betrug 0,2 × 0,5 cm 2 . zum Nachweis von Glucose auf der Oberfläche eines α-NiS-Nanosphärenfilms in allen Experimenten. Die Oxidations-Reduktions-(Redox-)Reaktion der α-NiS-Filme wurde unter Verwendung des CV-Verfahrens durch eine Ag/AgCl-Referenzelektrode mit einem Potentiostaten abgeschätzt. Die CV-Eigenschaften von α-NiS-Filmen wurden zwischen 0 und 0,8 V für 1 Zyklus von einem Potentiostaten gescannt. Die Proben wurden in einer Drei-Elektroden-Konfiguration mit einer Abtastrate von 20 mVs –1 . gemessen . In Bezug auf die Konzentration von NaOH haben wir 0,1 M für die Lösung gewählt, weil wir die folgende Formel (1) gesehen haben, dass je mehr OH − Anionen, die wir hatten, desto mehr e − Anionen in Lösung [8].
$$ \mathrm{NiS}+{\mathrm{OH}}^{-}\leftrightarrow \mathrm{NiS}\mathrm{OH}+{\mathrm{e}}^{-} $$ (1)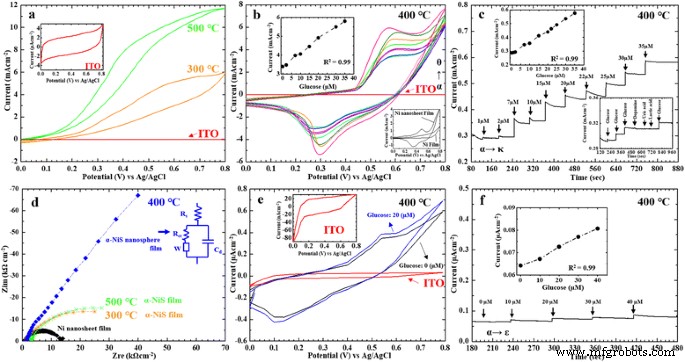
a Drei CVs im Bild:Die rote Kurve zeigte den CV von blankem ITO; die orangefarbenen und grünen Kurven waren die CVs von α-NiS-Filmen bei verschiedenen Glühtemperaturen (300 und 500 °C). Einschub:Lebenslauf aus blankem ITO/Glas. b VK von Nano-NiS/ITO in 0,1 M NaOH mit unterschiedlichen Glucosekonzentrationen:(α) 0 μM, (β) 2 μM, (γ) 7 μM, (δ) 10 μM, (ε) 15 μM, (ζ) 20 μM, (η) 30 μM und (θ) 35 μM. Einschub:oben links – Diagramm des Oxidationsspitzenstroms gegen die Glukosekonzentration; unten – CVs des Ni-Films und des Ni-Nanoblatt-Films. c Der α-NiS-Nanosphärenfilm wurde durch Amperometrie in 0,1 M NaOH mit verschiedenen Glucosekonzentrationen bewertet:(α) 1 μM, (β) 2 μM, (γ) 7 μM, (δ) 10 μM, (ε) 15 μM, (ζ) 20 μM, (η) 22 μM, (θ) 25 μM, (ι) 30 μM und (κ) 35 μM. Einschub:oben links – Darstellung der aktuellen Reaktionen gegenüber den Glukosekonzentrationen; unten – chronoamperometrische Reaktion von NiS/ITO in 0,1 M NaOH mit 2 μM Glukose und in Gegenwart von 2 μM Dopamin, Harnsäure und Milchsäure bei einem angelegten Potenzial von 0,6 V DC. d Nyquist-Diagramme des Nickel-Nanoblattfilms, des α-NiS-Nanosphärenfilms und des α-NiS-Films bei unterschiedlichen Tempertemperaturen (300 und 500 °C) in 0,1 M KCl mit 1,5 mM Fe(CN)6 3−/4− . e CV von Nano-NiS/ITO bei Krebs mit unterschiedlichen Glukosekonzentrationen:(α) 0 μM und (β) 20 μM. Einschub:oben links – Lebenslauf von blankem ITO/Glas. f Der α-NiS-Nanosphärenfilm wurde durch Amperometrie in Krebs-Puffer mit verschiedenen Glucosekonzentrationen bewertet:(α) 0 μM, (β) 10 μM, (γ) 20 μM, (δ) 30 μM und (ε) 40 μM. Einschub:oben – Darstellung der aktuellen Reaktionen im Vergleich zu den Glukosekonzentrationen
Gemäß der obigen Formel (1) haben wir angenommen, dass je mehr e − Anionen, die wir in einer Lösung hatten, zeigte der größere Stromwert in einem Potentiostaten. In Abb. 3a gab es drei Kurven. Die rote CV-Kurve des blanken ITO wurde im Einschub von Abb. 3a gezeigt. Die orangefarbenen und grünen CV-Kurven zeigten die Redoxreaktion der α-NiS-Filme bei verschiedenen Glühtemperaturen (300 und 500 °C). Wir haben beobachtet, dass die CV-Kurven in Abb. 3a keine negativen Reduktionspotentiale aufwiesen. Wir fanden auch, dass zwei α-NiS-Filme keine Stromreaktionen auf unterschiedliche Glukosekonzentrationen zeigten. Wie in Abb. 3b zu sehen ist, wurde der α-NiS-Nanosphärenfilm durch CV-Messungen in einer Lösung von 0,1 M NaOH mit unterschiedlichen Glucosekonzentrationen (2, 7, 10, 15, 20, 30 und 35 μM) bei bewertet eine Abtastrate von 20 mVs −1 . Offensichtlich haben wir das Redoxpotential des α-NiS-Nanosphärenfilms in Abb. 3b gesehen. Die ähnlichen Redoxkurven von Nano-NiS-Filmen wurden in der anderen Veröffentlichung gefunden [8]. Forscher (Padmanathan et al. 2015) berichteten, dass die Erklärung des Reaktionsmechanismus die beiden Redox-Gleichungen waren. (2) und (3) zum Erfassen von Glukose von Nano-NiS-Filmen. Die beiden Gleichungen wurden unten gezeigt [8]:
$$ {\mathrm{Ni}}^{\mathrm{II}}\to {\mathrm{Ni}}^{\mathrm{II}\mathrm{I}}+{\mathrm{e}}^{- } $$ (2) $$ {\mathrm{Ni}}^{\mathrm{II}\mathrm{I}}+\mathrm{Glukose}\to {\mathrm{Ni}}^{\mathrm{II} }+\mathrm{Gluconolacton} $$ (3)Wie in Abb. 3b zu sehen ist, wurden die unterschiedlichen Stromwerte der Oxidationspeaks offensichtlich bei 0,6 V geändert. Wir haben beobachtet, dass eine gestrichelte Linie eine lineare Beziehung zu den unterschiedlichen Stromreaktionen von Oxidationspeaks gegenüber unterschiedlichen Glukosekonzentrationen im Einschub (links) von Abb. 3b aufwies. Die CV-Kurven für den Nickel-Nanoblatt-Film und den Nickel-Film wurden auch im Einschub (unten) von Fig. 3b gezeigt. Die Stromantworten der CV-Kurve für den Nickel-Nanoblatt-Film waren von 0 bis 0,8 V im Einschub (unten) von Fig. 3b größer als der des Ni-Films. Wir dachten, dass wir den Nickel-Nanoblatt-Film als Vorläufer im Syntheseprozess des α-NiS-Nanosphären-Films verwendet haben, und wir hatten mehr Möglichkeiten, größere Stromantworten in der CV-Kurve zu erhalten. Abbildung 3c zeigt, dass die unterschiedlichen Stromreaktionen des α-NiS-Nanosphärenfilms zum Nachweis von Glukose bei unterschiedlichen Konzentrationen (1, 2, 7, 10, 15, 20, 22, 25, 30 und 35 μM) durch Amperometrie dienten. Wir beobachteten die unterschiedlichen Stromantworten der Glukosekonzentrationen von 1 bis 35 μM mit einer linearen Beziehung mit einem Korrelationskoeffizienten von 0,99 im Einschub (links) von Abb. 3c. Es wurde beschrieben von:
$$ I\left[{\mathrm{mAcm}}^{-2}\left]=0,0084\right[\mathrm{Glukose}\right]\upmu\mathrm{M}+0,2821 $$ (4)Der Sensitivitätswert wurde auf 8,4 μA μM –1 . geschätzt cm −2 für die Gl. (4). Die chronoamperometrische Reaktion eines α-NiS-Nanosphärenfilms in 0,1 M NaOH mit 2 μM Glukose und 2 μM Dopamin, 2 μM Harnsäure und 2 μM Milchsäure bei einem angelegten Potenzial von 0,6 V DC wurde im Einschub (unten) von Abb. gezeigt . 3c. Wir haben gezeigt, dass unser α-NiS-Nanosphärenfilm ein nicht-enzymatischer Glukosesensor in 0,1 M NaOH mit Anti-Interferenz-Fähigkeit gegenüber Dopamin, Harnsäure und Milchsäure ist.
In Bezug auf die elektrochemischen Ergebnisse der α-NiS-Nanosphärenfilme kamen wir zu dem Schluss, dass nur eine 400 °C-Probe viele kleine Nanopartikel und eine poröse Struktur auf der Oberfläche des α-NiS-Nanosphärenfilms in Abb. 2c aufwies. Die kleineren Nanopartikel und die poröse Struktur wurden auf der Oberfläche des &agr;-NiS-Nanosphärenfilms abgeschieden, sodass der Nanosphärenfilm eine größere Oberfläche und höhere Reaktionen bei der elektrochemischen Detektion bereitstellte. Wir beobachteten, dass die Proben 4 h lang bei 400 °C getempert wurden, wobei die aktuellen Reaktionen bei niedrigen Glukosekonzentrationen erfolgten. Nur eine 400 °C-Probe mit einer guten Glukosereaktion war auf viele kleine Nanopartikel und eine poröse Struktur auf der Oberfläche des α-NiS-Nanosphärenfilms zurückzuführen.
Abbildung 3d zeigt, dass die elektrochemische Impedanzspektroskopie (EIS) von α-NiS-Filmen in einer Lösung von 0,1 M KCl (mit 1,5 mM Fe(CN)6 3−/4− ). Wir haben beobachtet, dass die Warburg (W ) war die Impedanz des &agr;-NiS-Nanosphärenfilms größer als bei zwei anderen &agr;-NiS-Filmen. Die Elemente des EIS-Modells des α-NiS-Nanosphärenfilms waren R s = 133 Ω, R ct = 42.1 Ω, C d = 22,1 μF und W = 11,7 kΩ. Die elektrochemische Impedanz des Ni-Nanoblattfilms wurde auch in Fig. 3d gezeigt und hatte den niedrigeren Impedanzwert in diesen Mustern. Wir haben auch die Werte unseres nicht-enzymatischen Glukosesensors für Stabilität, Standardabweichung (SD) der Stabilität und Wiederverwendbarkeit berechnet (siehe Tabelle 1). Aus den Werten der SD der Stabilität in Tabelle 1 haben wir festgestellt, dass der durchschnittliche Stabilitätswert (0,011 mA/min) der 14-fachen Messung größer war als der durchschnittliche Stabilitätswert (0,006 mA/min) der 13-fachen Messung. Wir gingen davon aus, dass der numerische Wert der Wiederverwendbarkeit ungefähr 13 (SD ≤ 0,002 mA/min) betrug.
Nach Abschluss der Messung des elektrochemischen Verhaltens von NiS-Proben in 0,1 M NaOH haben wir auch viele Arbeiten auf einen physiologischen Zustand untersucht. Diese Forscher verwendeten verschiedene Lösungen wie phosphatgepufferte Kochsalzlösung (PBS), Annexin-V-Bindungspuffer, aECF-Lösung und Krebs-Puffer für die Anwendung von Zellkulturen [17,18,19,20,21]. Einige Forscher wählten Krebs-Puffer als Zellkulturpuffer bei niedriger Glukosekonzentration [20, 21]. Der lineare Bereich unseres α-NiS-Nanosphärenfilms zum Nachweis einer niedrigen Glukosekonsekration lag zwischen 1 und 35 μM in 0,1 M NaOH, daher hatte die Verwendung unseres Sensors zum Nachweis einer niedrigen Glucosekonsekration in Krebs-Puffer für einen physiologischen Zustand eine praktische Bedeutung für uns . Der &agr;-NiS-Nanosphärenfilm wurde verwendet, um Glukose bei verschiedenen Konzentrationen in Krebs-Puffer nachzuweisen. Wir haben unseren α-NiS-Nanosphärenfilm verwendet, um die unterschiedlichen Glukosekonzentrationen (0 und 20 μM) durch ein zyklisches Voltammogramm (CV) in Krebs-Puffer (115 mM NaCl, 2 mM KCl, 25 mM NaHCO3) nachzuweisen , 1 mM MgCl2 , 2 mM CaCl2 , 0,25% Rinderserumalbumin [pH 7,4]; Äquilibriert mit 5 % CO2 , eingestellt auf pH 7,4 mit 0,01 M NaOH) [20]. Wie im Einschub von Fig. 3e zu sehen ist, zeigte es die Hintergrund-CV-Kurve von bloßem ITO. Abbildung 3e zeigt auch die CV-Kurven der NiS/ITO-Elektrode in Krebs-Puffer mit 0 und 20 μM Glukose. Wir haben die CV-Kurven mit unterschiedlichen Stromantworten nahe 0,6 V offensichtlich beobachtet. Wie in Abb. 3f zu sehen ist, wurde der α-NiS-Nanosphärenfilm durch Amperometrie in Krebs-Puffer (eingestellt auf pH 7,4 mit 0,01 M NaOH) zum Nachweis verschiedener Glukosekonzentrationen bewertet:(α) 0 μM, (β) 10 μM, (γ ) 20 μM, (δ) 30 μM und (ε) 40 μM. Die eingefügte Figur zeigt die Auftragung des Oxidationsspitzenstroms gegen die Glucosekonzentration. Eine Kurve der amperometrischen Antwort wurde im Einschub (oben) von Abb. 3f gezeigt, die eine lineare Beziehung mit einem Korrelationskoeffizienten von 0,99 zeigte. Es wurde von I[μAcm −2 . beschrieben ] = 0,0004[Glukose]μM + 0,0638.
Abbildung 4 zeigt die UV-/Sicht-/NIR-Absorptions- und -Fluoreszenzspektren. Wir haben die UV/Visible/NIR-Absorption der α-NiS-Filme im Spektralbereich von 300–800 nm (Abb. 4a–c) für verschiedene Tempertemperaturen (300, 400 und 500 °C) aufgezeichnet. Um die Energielücke zu bestimmen (E g ) der Nanokugeln, die folgende Abhängigkeit des Absorptionskoeffizienten (α ) auf der Photonenenergiegleichung wurde verwendet [22]:
$$ \alpha hv=A{\left( hv-{E}_{\mathrm{g}}\right)}^m $$ (5)wo E g war die Energielücke, A war die Konstante mit separaten Werten für verschiedene Übergänge, hν war die Photonenenergie und m war ein Exponent, der die Werte 1/2, 3/2, 2 und 3 annahm, die mit der Natur des elektronischen Übergangs zusammenhängen. Es war für die Absorption verantwortlich. Es zeigte die (αhν ) 2 gegen hν Plot im Einschub von Abb. 4a–c. Wenn m =1/2, erlaubten diese Absorptionsspektren von α-NiS-Filmen die richtigen Werte für den direkten Übergang. Wie im Einschub von Abb. 4a–c zu sehen ist, haben wir drei Energielücken (E g )-Werte (1.08, 1.8 und 0.66 eV) der α-NiS-Filme. Wir haben gepunktete Linien verwendet, um die Kurven von 0,6 bis 2,8 eV im Einschub von Abb. 4a–c anzupassen. Wie im Einschub von Abb. 4a–c zu sehen ist, haben wir auch beobachtet, dass die höchste Energielücke (E g ) des α-NiS-Nanosphärenfilms betrug etwa 1,8 eV bei einer Glühtemperatur von 400 °C. In dieser Studie wurden auch Fluoreszenzgeräte verwendet, um die optischen Eigenschaften der Proben zu untersuchen. Bisherige Forscher konzentrierten sich auf die Fluoreszenzspektren der α-NiS-Partikel, die durch die unterschiedlichen Phasen, Formen, Strukturen und das Oberflächen-Volumen-Verhältnis beeinflusst wurden [23]. Wie in Abb. 4d zu sehen ist, haben wir die Fluoreszenzspektren von α-NiS-Filmen mit ultravioletten Emissionen bei unterschiedlichen Tempertemperaturen (300, 400 und 500 °C) beobachtet. Die PL-Spektren der Proben zeigten die scharfen Emissionspeaks bei 448 nm und die Emissionspeaks bei 369 nm (anregt bei λ ex = 277 nm) [23, 24]. Aufgrund der Ergebnisse zu den optischen Eigenschaften unserer α-NiS-Filme waren wir der Ansicht, dass unterschiedliche Glühtemperaturen eine Chance haben, unterschiedliche Korngrößen auf dem NiS-Film zu erhalten. Bei den Nanopartikeln mit Quanteneinschluss beeinflusste eine Erhöhung der Nanopartikelgröße die Abnahme der Bandlücke mit der Temperatur von 400 auf 500 °C [25]. Die optischen Eigenschaften von NiS änderten sich mit unterschiedlicher Korngröße, sodass sich die optischen Eigenschaften von NiS mit unterschiedlichen Temperaturen signifikant änderten [25]. Die unterschiedlichen optischen Eigenschaften des NiS-Films bei unterschiedlichen Temperaturen sollten auf den Größeneffekt zurückzuführen sein, der die auf die Bandlücke beeinflusste Partikelgröße verringert.
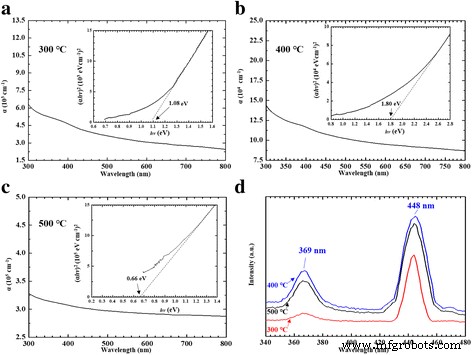
UV-/Sicht-/NIR-Absorptionsspektren und (αhν ) 2 gegen hν Plot in den Abbildungen zur Synthese von α-NiS-Filmen bei a 300, b 400 und c 500 °C. d Fluoreszenzspektren der α-NiS-Filme wurden bei verschiedenen Tempertemperaturen (300, 400 und 500 °C für 4 h) hergestellt
Wir haben erwogen, die HR-TEM-Analyse auf einen α-NiS-Nanosphärenfilm zu konzentrieren, da wir viele α-NiS-Nanosphären für die nicht-enzymatischen Glukosesensoren bei einer Glühtemperatur von 400 °C erhalten haben. Wie in Abb. 5 zu sehen ist, beobachteten wir, dass die α-NiS-Nanokügelchen 4 h lang bei 400 °C getempert wurden. Die Informationen über die Mikrostruktur der so hergestellten α-NiS-Nanokügelchen wurden durch HR-TEM erhalten. Abbildung 5a, b zeigten HR-TEM-Bilder der Nanokügelchen. Der Durchmesser der Nanokugel betrug 150 bis 250 nm. Abbildung 5c HR-TEM-Bild zeigte auch klare Gitterstreifen mit einem Zwischenraum von 0,7786 nm, die dem Abstand zwischen zwei benachbarten (101) Ebenen der α-NiS-Nanosphäre entsprachen. Abbildung 5d zeigte ein SAED-Muster der Nanokugel, und die Flecken des Beugungsrings wurden auf (101) der α-NiS-Nanostruktur indiziert.

a –c HR-TEM-Bilder der α-NiS-Nanosphäre. d Das SAED-Muster der α-NiS-Nanosphäre wurde 4 h lang bei 400 °C getempert
Schlussfolgerung
Zusammenfassend wurden die α-NiS-Nanosphärenfilme mit XRD-, VVSEM-, FE-SEM-, EDS-, EIS-, UV-, PL- und HR-TEM-Geräten untersucht. Wir beobachteten, dass der α-NiS-Nanosphärenfilm gebildet wurde, indem die Glühtemperatur 4 h lang auf 400 °C in vakuumversiegelten Glasampullen kontrolliert wurde. Die Energielücke (E g ) des α-NiS-Nanosphärenfilms betrug ungefähr 1,8 eV. Nachdem wir unsere α-NiS-Nanosphärenfilme fünfeinhalb Jahre lang in unserem Labor konserviert hatten, beobachteten wir durch CV-Messungen und Amperometrie in verschiedenen Lösungen (0,1 M NaOH und Krebs Puffer). Der lineare Bereich zum Nachweis von Glukose lag zwischen 1 und 35 μM in 0,1 M NaOH. Für einen physiologischen Zustand lag der lineare Bereich zum Nachweis von Glukose ungefähr zwischen 0 und 40 μM in Krebs-Puffer.
Abkürzungen
- Lebenslauf:
-
Zyklisches Voltammogramm
- EDS:
-
Energiedispersives Spektrometer
- FE-REM:
-
Feldemissions-Rasterelektronenmikroskopie
- HR-TEM:
-
Hochauflösende Transmissionselektronenmikroskopie
- NiS:
-
Nickel sulfide
- PL:
-
Photolumineszenz
- PVT:
-
Physical vapor transport
- SD:
-
Standard deviation
- UV/Visible/NIR:
-
Ultraviolet/visible/near-infrared
- VVSEM:
-
Variable vacuum scanning electron microscopy
- wt%:
-
Percentage by weight
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Der Bedarf an hochgenauen Ultra-Niederdrucksensoren
- Die Gesundheitssensoren von Maxim für ultrakleine Wearables
- Analoge Sensoren auf dem Raspberry Pi mit einem MCP3008
- Schneidelösung für die Filmindustrie – digitale Schneidemaschine
- IBM-Wissenschaftler erfinden ein Thermometer für die Nanoskala
- Wie 0G-Netzwerksensoren die Kühlkette von Impfstoffen schützen
- So wählen Sie den richtigen Sensor für Abfüllanwendungen aus
- Material für die nächste Generation intelligenter Sensoren
- Neues mathematisches Tool kann die besten Sensoren für den Job auswählen
- Die langfristigen Vorteile der vorbeugenden Wartung Ihres Lkw



