Hochselektiver und empfindlicher Nachweis von Hg2+ basierend auf Förster-Resonanzenergietransfer zwischen CdSe-Quantenpunkten und g-C3N4-Nanoblättern
Zusammenfassung
In Gegenwart von Hg 2+ , wurde ein Fluoreszenzresonanzenergietransfersystem (FRET) zwischen CdSe-Quantenpunkten (QDs) (Donor) und g-C3 . konstruiert N4 (Rezeptoren). Nanokomposite aus g-C3 N4 unterstützt von CdSe QDs (CdSe QDs/g-C3 N4 Nanoblätter) wurden über einen elektrostatischen Wechselwirkungsweg in einer wässrigen Lösung hergestellt. Die Nanokomposite wurden durch Röntgenphotoelektronenspektroskopie, Röntgenbeugung, Fourier-Transformations-Infrarotspektroskopie und Transmissionselektronenmikroskopie charakterisiert. Die Ergebnisse zeigten, dass der g-C3 N4 Nanoblätter wurden zufällig durch CdSe-QDs mit einem durchschnittlichen Durchmesser von etwa 7 nm dekoriert. Die Machbarkeit des FRET-Systems als Sensor wurde durch die Hg(II)-Detektion in Wasser demonstriert. Bei pH 7 wurde ein linearer Zusammenhang zwischen der Fluoreszenzintensität und der Hg(II)-Konzentration (0–32 nmol/l) mit einer Nachweisgrenze von 5,3 nmol/l beobachtet. Die neue Nachweismethode hat sich beim Nachweis von Hg 2+ . als sensitiv erwiesen in Wasserlösungen. Darüber hinaus zeigte die Methode eine hohe Selektivität für Hg 2+ über mehrere Metallionen, darunter Na + , Mg 2+ , Ca 2+ , Pb 2+ , Cr 3+ , Cd 2+ , Zn 2+ , und Cu 2+ . Die CdSe-QDs/g-C3 N4 Nanoblatt-Konjugat zeigte eine wünschenswerte Langzeitstabilität und Reversibilität als neuartiger FRET-Sensor. Die neuartige FRET-basierte Fluoreszenzdetektion bot eine attraktive Assay-Plattform zur Quantifizierung von Hg 2+ in komplexen Wasserlösungen.
Hintergrund
Die Hauptursache für Quecksilbervergiftungen beim Menschen waren verschmutzte natürliche Gewässer [1]. Hg 2+ Ionenmetabolismus durch aquatische Mikroben produziert Methylquecksilber, ein starkes Neurotoxin, das mit kognitiven und Bewegungsstörungen in Verbindung gebracht wird [2]. Daher sind schnelle, kostengünstige, einfache und auf komplexe Umgebungen anwendbare Quecksilbernachweismethoden erforderlich. Insbesondere Nanomaterialien mit einzigartigen optischen Eigenschaften können verwendet werden, um optische Sensoren mit hoher Empfindlichkeit und Selektivität zu entwickeln [3]. Halbleiter-Quantenpunkte (QDs), fluoreszierende Metall-Nanocluster (NCs), Edelmetall-Nanopartikel (NPs) und Kohlenstoff-Nanopunkte (CDs) wurden häufig beim Design von Hg 2+ . verwendet optische Sensoren aufgrund ihrer besonderen Eigenschaften wie einfache Synthese, hohe Stabilität, Funktionalisierung und Biokompatibilität. Viele Fluoreszenzsensoren für Hg 2+ berichtet worden [4,5,6,7,8]. Huang et al. [9] entwickelten einen zeitgesteuerten Förster-Resonanzenergietransfer-(FRET)-Sensor für Hg 2+ Erkennung. Darüber hinaus wurden verschiedene FRET-Systeme zum Nachweis von Hg 2+ . entwickelt [10,11,12]. Bemerkenswerterweise könnten FRET-Systeme auf ähnliche Weise unter Verwendung von Nanopartikeln wie QDs sowie organischen und anorganischen NPs aufgebaut werden [13,14,15]. Unter den Nanopartikeln g-C3 N4 Nanoblätter hatten breites Interesse geweckt [16, 17]. Obwohl g-C3 N4 Nanoblätter wurden als Sensoren verwendet, ein FRET-Detektionssystem mit g-C3 N4 Nanoblätter und CdSe-QDs für Metallionen wurden nicht beschrieben. FRET-basierte Fluoreszenzsensorsysteme bieten mehrere Vorteile [18].
In der vorliegenden Studie wurde ein neuer FRET-basierter Fluoreszenzsensor zum Nachweis von Quecksilberionen in wässrigen Medien mit g-C3 . entwickelt N4 Nanoblätter und CdSe-QDs-Partikel als Vehikel. Der vorgeschlagene Mechanismus ist in Abb. 1 dargestellt.
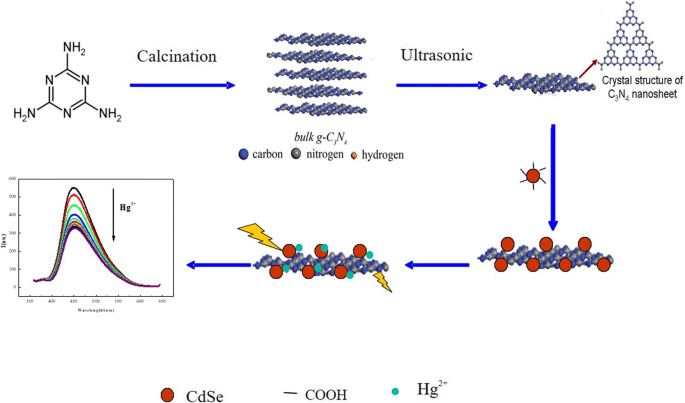
Die Mechanismen der FRET-basierten Detektion von Quecksilberionen
Methoden
Materialien
Quecksilber(II)-chlorid (HgCl2 .) ) wurde vom Tong Ren Chemical Research Institute (Guizhou, China) bezogen. Harnstoff- und CdSe-QDs wurden von der Aladdin Reagent Company (Shanghai, China) bezogen. Andere Reagenzien und Chemikalien waren von analytischer Reagensqualität und wurden ohne weitere Reinigung verwendet. Alle Lösungen wurden unter Verwendung von gereinigtem Wasser aus einem Milli-Q-Gradienten-Wasserreinigungssystem (Millipore Inc., USA; nominaler Widerstand 18,2 MÙ cm) hergestellt.
Charakterisierung
Ein Röntgendiffraktometer (Rigaku D/max-2400) wurde verwendet, um Beugungsmuster zu erhalten. Ultraviolett-sichtbare (UV-vis) Spektren wurden auf einem UV-vis 800 Spektrophotometer bei Raumtemperatur aufgenommen. Fourier-Transformations-Infrarot-(FTIR)-Spektren wurden auf einem Nicolet-nexus670-Spektrometer unter Verwendung von KBr aufgezeichnet. Fluoreszenzmessungen wurden bei Raumtemperatur mit einem RF-5301PC-Fluoreszenzspektrometer durchgeführt. Röntgenphotoelektronenspektroskopie (XPS)-Messungen wurden unter Verwendung eines multifunktionalen Spektrometers (Thermo Scientific) durchgeführt.
Aufbau des FRET-Sensors zwischen den g-C3 N4 Nanoblätter und CdSe-QD-Partikel
In einem typischen Verfahren ist g-C3 N4 (125 mg, das gemäß unserem vorherigen Bericht [19] synthetisiert wurde) wurde in 250 ml Wasser (1:1) dispergiert und 5 h bei Umgebungstemperatur mit Ultraschall behandelt. Dann wurden CdSe-QDs (1,838 g, 0,0216 Mol) durch Beschallung für 2 Stunden in der Lösung gelöst. Da die Amingruppe am g-C3 N4 Nanoblätter und CdSe-QDs hatten eine Carboxylgruppe, g-C3 N4 Nanoblätter und CdSe-QDs-Nanopartikel würden durch elektrostatische Wechselwirkung kombiniert. Alle Lösungen wurden in Milli-Q-Gradientenwasser (pH =7) hergestellt. Die CdSe-QDs/g-C3 N4 Nanoblatt-Konjugat-Emissionsspektren wurden aufgezeichnet. Alle Proben wurden bei 334 nm angeregt, was nahe der minimalen Akzeptorabsorption lag.
Fluoreszenznachweis von Hg 2+
Hg 2+ wurde bei Raumtemperatur in Wasser abgeschreckt. Während eines typischen Vorgangs 10 μl CdSe-QDs/g-C3 N4 Nanoblatt-Konjugate wurden zu 3 ml Reinstwasser gegeben und dann die berechnete Menge an Hg 2+ wurde hinzugefügt. Die Emissionsspektren der CdSe-QDs/g-C3 N4 Nanoblatt-Konjugate wurden 2 Minuten später bei Raumtemperatur aufgezeichnet.
Störungs- und Wettbewerbsanalysen
Die Reaktion der FRET-Nanosonde auf andere Metallionen (Na + , Mg 2+ , Ca 2+ , Pb 2+ , Cr 3+ , Cd 2+ , Zn 2+ , und Cu 2+ ) wurde durch Fluoreszenzspektroskopie untersucht. Die Studien wurden mit den CdSe QDs/g-C3 . durchgeführt N4 Nanoblatt-Konjugate, die bei 450 nm emittieren. Die Konjugatlösung wurde in eine Quarz-Fluoreszenzküvette mit optischem Weg von 1 cm gegeben. Die Fluoreszenzintensität wurde bei einer Emissionswellenlänge von 450 nm unter einer Anregungswellenlänge von 334 nm in Gegenwart jeder möglichen Interferenz (32 nM) gemessen. Kompetitionsassays wurden auch für alle zuvor analysierten möglichen Interferenzen durchgeführt. Für Konkurrenzexperimente:32 nM Hg 2+ wässrige Lösungen wurden hergestellt.
Ergebnisse und Diskussion
Charakterisierung
Die Struktur und Morphologie von g-C3 N4 Nanoblätter wurden durch TEM, XPS und XRD charakterisiert. Das TEM-Bild in Abb. 2a zeigte, dass der g-C3 N4 nanosheet besaß eine graphenähnliche Morphologie, die hauptsächlich aus wenigen Schichten besteht [19]. Abbildung 2a zeigt die XRD-Muster von g-C3 N4 Nanoblätter. Der starke XRD-Peak zentriert bei 27,4 ° entsprach dem typischen Peak der graphitischen Zwischenschichtstapelung (002) von g-C3 N4 . Der kleine Peak bei 13,1° entsprach dem periodischen Strukturpackungsmerkmal in der Ebene innerhalb der Blätter [20, 21]. Die XPS-Messung wurde verwendet, um die Valenzzustände von g-C3 . zu analysieren N4 Nanoblätter. Das XPS-Spektrum in Abb. 2c zeigte das an N gebundene C-C bei 284,8 und 288,0 eV, und das N1 s-Spektrum lag bei 397,04 eV. In Abb. 2d der Peak bei 811 cm −1 wurde der Schwingung des Triazinrings zugeschrieben. Die Spitzen um 1000 cm −1 repräsentierten die Streckmoden von CN-Heterocyclen und den Peak bei 1800 cm −1 entsprach C–NH–C. Die Spitzen bei 300–3600 cm −1 entsprach N–H- und O–H-Streckschwingungen [22].
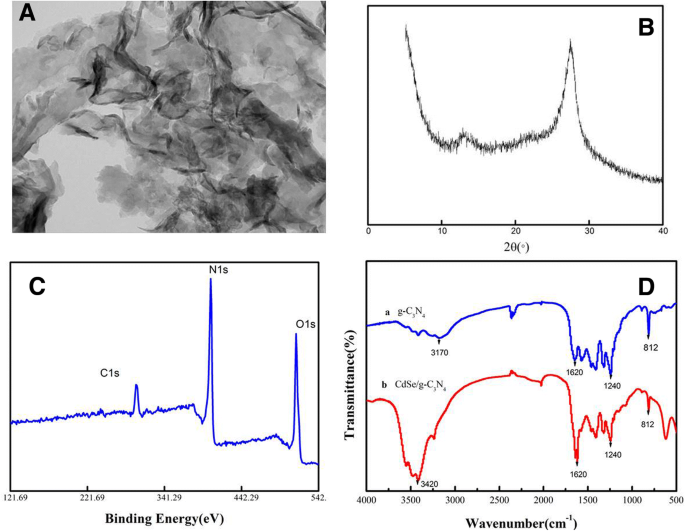
Charakterisierung des so hergestellten g-C3 N4 Nanoblatt. a TEM-Bild. b XRD-Bild. c XPS-Spektrum. d FTIR-Spektrum
UV-Vis- und Fluoreszenzeigenschaften von CdSe-QDs/g-C3 N4 Nanoblätter
Fluoreszenz- und UV-Vis-Absorptionsspektren wurden aufgenommen, um die optischen Eigenschaften von CdSe-QDs/g-C3 . zu bewerten N4 Nanoblätter. Wie in Abb. 3a gezeigt, wurde im UV-Vis-Absorptionsspektrum ein großer Peak bei etwa 334 nm beobachtet. Darüber hinaus wurden die Fluoreszenzemissions- und Anregungspeaks bei 452 und 334 nm in der synchronen Fluoreszenzspektroskopie in Abb. 3b beobachtet und waren mit der Emissionsfluoreszenz und ultravioletten Lichtanregung von Nanoblättern verbunden. Die Emissionspeaks zeigten eine Verschiebung gegenüber dem reinen g-C3 N4 Nanoblätter bei 14–16 nm (Emissions- und Anregungspeaks wurden bei 438 und 310 nm beobachtet, wie in Abb. 3c dargestellt), was dem FRET zugeschrieben werden konnte. Der Einfluss der Anregungswellenlängen auf die Fluoreszenzintensitäten wurde ebenfalls bestätigt.
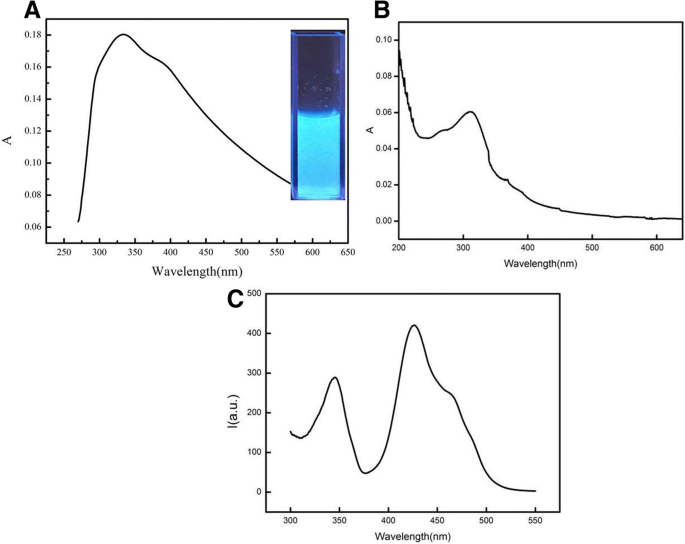
Das UV-Vis-Absorptions- und Fluoreszenzspektrum von CdSe QDs/g-C3 N4 konjugiert
Einfluss des pH-Werts auf die Fluoreszenz der CdSe-QDs/g-C3 N4 Nanoblatt-Konjugate
Abbildung 4 zeigt die Fluoreszenz der CdSe-QDs/g-C3 N4 Nanoblatt-Konjugate bei unterschiedlichen pH-Werten. Der pH-Wert stieg mit der Fluoreszenzintensität von 3 auf 7 an. Allerdings nahm die Fluoreszenzintensität allmählich ab, wenn der pH-Wert von 7 auf 10 variierte, was auf den Einfluss des pH-Werts auf die Änderung der Oberflächenladung aufgrund der Protonierung-Deprotonierung aufgrund der Existenz von Aminogruppen in der Struktur von . zurückgeführt werden könnte gC3 N4 Nanoblätter. In dieser Studie wurden die CdSe-QDs/g-C3 N4 Nanoblatt-Konjugate wurden zum Nachweis von Hg 2+ . durchgeführt Ionen, und als optimaler pH-Wert wurde ein pH-Wert von 7 gewählt. Die Fluoreszenzemissionen wurden bei pH 7 mit unterschiedlichen Konzentrationen von NaCl gemessen, um die Stabilität der CdSe-QDs/g-C3 . zu erhalten N4 Nanoblatt-Konjugate unter Bedingungen hoher Ionenstärke. Bei hoher Ionenstärke wurde nur eine geringfügige Änderung der Fluoreszenzintensitäten der CdSe-QDs/g-C3 . beobachtet N4 Nanoblatt-Konjugate. Das Ergebnis zeigte, dass eine hohe Ionenstärke minimale Auswirkungen auf die Fluoreszenzintensitäten der Konjugate hatte.
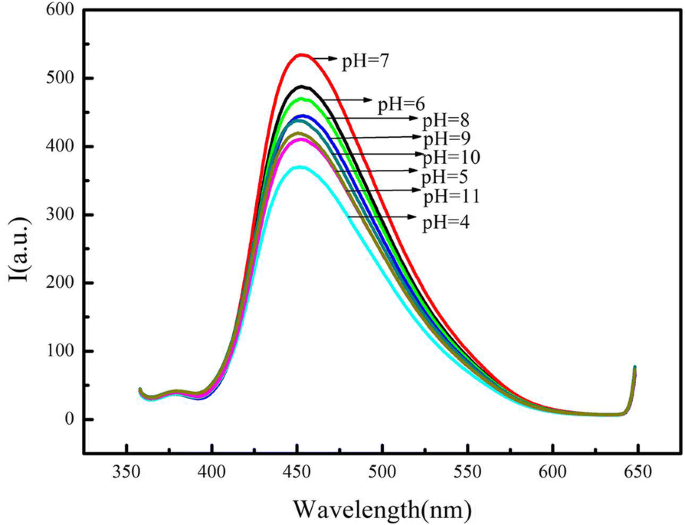
Die Wirkung des pH-Werts auf die Fluoreszenz von CdSe QDs/g-C3 N4 Nanoblätter-Konjugate
Selektivität von CdSe-QDs/g-C3 N4 Nanosheet-FRET-System zum Nachweis von Quecksilberionen
Die Selektivität ist ein wichtiger Parameter eines neuen Sensorsystems. Die Selektivität der CdSe QDs/g-C3 N4 Nanoblatt-FRET-Sensor wurde unter Verwendung verschiedener Metallionen (z. B. Cu 2+ , Mg 2+ , Na + , Ca 2+ , Hg 2+ , Cr 3+ , Pb 2+ , Cd 2+ , und Zn 2+ ); die Ergebnisse sind in Abb. 5a dargestellt. Im Vergleich zur Blindprobe ohne Ionen ist das Fluoreszenzverhältnis von Hg 2+ deutlich erhöht, während sich die Fluoreszenzintensität anderer Metallionen geringfügig veränderte oder gleich blieb. Diese Ergebnisse zeigten, dass der FRET-Sensor eine höhere Selektivität aufwies als die anderen (Abb. 5b). Somit sind die CdSe-QDs/g-C3 N4 zeigte eine hohe Selektivität gegenüber Hg 2+ . Dieses Phänomen war im Vergleich zu reinem g-C3 . deutlich N4 Nanoblatt, das für Cu 2+ . selektiv war und Hg 2+ [23, 24].
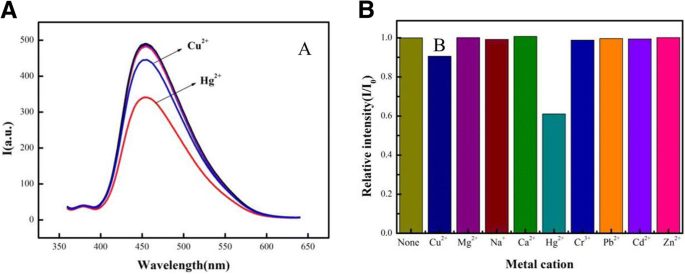
Die Selektivitätsexperimente für die CdSe-QDs/g-C3 N4 Nanoblätter FRET-Sensor
Machbarkeit des FRET-Fluoreszenzverfahrens beim Nachweis von Hg 2+
Um die Praktikabilität des FRET-Sensors zu untersuchen, wurden die CdSe QDs/g-C3 N4 Nanoblatt-Fluoreszenzdetektion von Hg 2+ wurde durchgeführt. Das Vorhandensein von Hg 2+ führte zu einer verringerten Fluoreszenzintensität, wie in Abb. 6 gezeigt, die veranschaulicht, dass Hg 2+ könnte den FRET-Sensor effektiv löschen. Um die Empfindlichkeit zu untersuchen, muss die Reaktion des Sensors auf verschiedene Hg 2+ Konzentrationen wurden durch Fluoreszenzspektroskopie weiter ausgewertet und die Ergebnisse sind in Abb. 6a gezeigt. Die Fluoreszenzintensität von g-C3 N4 Nanoblätter nahmen mit steigendem Hg 2+ . allmählich ab Konzentrationen. Abbildung 6b erklärt, dass das I /Ich 0 war abhängig von der Konzentration von Hg 2+ , wo ich 0 und ich waren die Fluoreszenzintensität in Abwesenheit bzw. Anwesenheit von Hg 2+ . Außerdem ist die Beziehung von I /Ich 0 zwischen den Konzentrationen von Hg 2+ war linear und die lineare Regressionsgleichung war I = − 9.6 × 10 7 + 550.5(R 2 = 0,9882), wie im Einschub von Abb. 6b gezeigt. Im Vergleich zu kürzlich berichteten Lumineszenzmethoden hatte die vorgeschlagene Methode eine niedrigere Nachweisgrenze und eine höhere Empfindlichkeit [25, 26]. Die g-C3 N4 Nanoblätter und CdSe-QDs zeigten keine offensichtliche Löschreaktion auf andere Metallionen außer Hg 2+ , was auf eine relativ hohe Selektivität für diese Methode hindeutet.
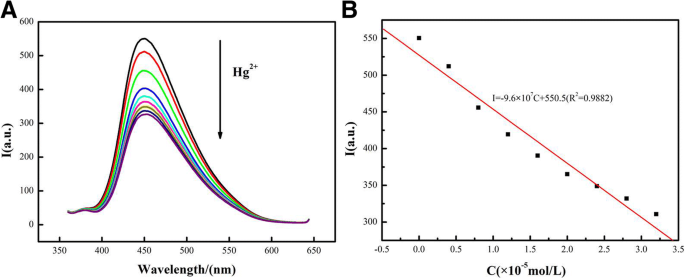
Die Sensoreigenschaften der CdSe QDs/g-C3 N4 Nanoblatt-Konjugate und die Abhängigkeit der Fluoreszenzintensität von der Konzentration von Hg 2+ (CHg 2+ :1, 0 nM; 2, 4 nM; 3, 8 nM; 4, 12 nM; 5, 16 nM; 6, 20 nM; 7, 24 nM; 8, 28 nM; 9, 32 nM)
Die anderen koexistierenden Kationen, die den Nachweis von Quecksilberionen beeinflussen, wurden ebenfalls nachgewiesen. Die Reaktion der CdSe QDs/g-C3 N4 Nanoblatt-basiertes Sensorsystem für Hg 2+ -Ionen in Gegenwart von Alkali-, Erdalkali- und anderen Übergangsmetallionen wurde in Tabelle 1 gezeigt. Die Koexistenz der meisten Metallionen beeinträchtigte die Bindung von Hg 2+ . nicht , was darauf hindeutet, dass die Interferenz dieser koexistierenden Ionen auf dem Hg 2+ Sensor war vernachlässigbar.
Darüber hinaus ist die Langzeitstabilität eine überlegene Eigenschaft von Sensoren. Die Extinktion und die Fluoreszenz während der kontinuierlichen Untersuchung alle 3 Tage innerhalb von 2 Wochen zeigten, dass die Aktivität von CdSe QDs/g-C3 N4 Nanoblätter blieben über 92% der anfänglichen Effizienz, obwohl sie bei Umgebungsbedingungen gelagert wurden. Die Ergebnisse zeigten, dass die CdSe-QDs/g-C3 N4 Nanoblätter als FRET-Sensoren hatten eine gute Langzeitstabilität.
Verglichen mit früheren Berichten über Fluoreszenzassays für Hg 2+ (Ergebnisse sind in Tabelle 2 aufgeführt), die CdSe-QDs/g-C3 N4 Nanoblatt-Fluoreszenzsonde auf FRET-Basis mit einer Hg(II)-Konzentration im Bereich von 0–32 nmol/L bei pH =7 wies eine Nachweisgrenze bei 5,3 nmol/L auf. Somit erzielte unsere Methode eine überlegene Nachweisgrenze und einen linearen Bereich.
Anwendung des FRET-Sensors
Die CdSe-QDs/g-C3 N4 Nanoblätter als FRET-Sensor boten erfolgreich eine gute Plattform zum Nachweis von Hg 2+ in realen Proben aufgrund ihrer Empfindlichkeit und Selektivität. Nun, See- und Leitungswasser wurden als echte Proben für die Analyse ausgewählt, in denen die Rückgewinnung von Hg 2+ lagen im Bereich von 95,4–101,6 % (Tabelle 3). Die relative Standardabweichung (RSD) von Hg 2+ lag im Bereich von 0,64–1,72 %. Das Ergebnis zeigte eindeutig, dass die entwickelte Methode effizient zum Nachweis von Hg 2+ . eingesetzt werden kann bei praktischen Anwendungen. Die akzeptablen Werte für RSD und relativer Fehler bestätigten die hohe Empfindlichkeit, hohe Präzision und hohe Zuverlässigkeit des vorgeschlagenen FRET-Sensors für Hg 2+ Bestimmung in praktischen Anwendungen.
Schlussfolgerungen
Es wurde ein FRET-basiertes System zum Nachweis von Hg 2+ . entwickelt innerhalb von g-C3 N4 Nanoblätter/CdSe-QDs. Die Nachweisgrenze für Hg 2+ ion betrug 5,3 nM, mit einer linearen Reaktion im Bereich von 0 bis 32 nM. Die Anwendbarkeit dieses Sensors wurde durch die Messung des Gehalts an Hg 2+ . nachgewiesen in echten Mustern. Angesichts der Langzeitstabilität, der geringen Kosten und der einfachen Herstellung der CdSe-QDs/g-C3 N4 Nanoblatt-Konjugaten könnte der Fluoreszenzassay als Umweltsensor verwendet werden. Diese Strategie würde einen alternativen Ansatz für die Konstruktion von FRET-basierten Sensoren für Hg 2+ . bieten in wässrigen Medien, einschließlich Umwelt- und biologischen Proben.
Highlights
- 1.
Das Fluoreszenzresonanzenergietransfersystem (FRET) wurde zwischen CdTe-Quantenpunkten (QDs) (Donor) und g-C3 . konstruiert N4 (Akzeptor) in Gegenwart von Hg 2+ zum ersten Mal.
- 2.
Die Nanokomposite von g-C3 N4 unterstützt von CdSe QDs (CdSe QDs /g-C3 N4 ) wurden über einen einfachen elektrostatischen Wechselwirkungsweg in wässriger Lösung hergestellt.
- 3.
Die Machbarkeit des FRET-Systems als Sensor zum Nachweis von Hg (II) in wässriger Lösung wurde demonstriert. Bei pH 7 wurde eine lineare Beziehung zwischen der Intensität der gelöschten Fluoreszenz und der Konzentration von Hg (II) im Bereich von 0–32 nmol/L beobachtet. Die Nachweisgrenze lag bei 5,3 nmol/l.
- 4.
Die neuartige FRET-basierte Fluoreszenzdetektion kann eine attraktive Assay-Plattform für die Quantifizierung von Hg 2+ . bieten in komplexen Wasserlösungen.
Abkürzungen
- FRET:
-
Förster-Resonanz-Energieübertragung
- FTIR:
-
Fourier-Transformations-Infrarot
- UV–vis:
-
Ultraviolett – sichtbar
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgendiffraktometer
Nanomaterialien
- Demonstration eines flexiblen Graphen-basierten Biosensors für den empfindlichen und schnellen Nachweis von Eierstockkrebszellen
- N,N-Dimethylformamid, das die Fluoreszenz von MXen-Quantenpunkten für die empfindliche Bestimmung von Fe3+ reguliert
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Sensibler nichtenzymatischer elektrochemischer Glukosenachweis basierend auf hohlporösem NiO
- Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
- Abhängigkeit der Hüllendicke des Energietransfers zwischen den Teilchen in Kern-Schale-ZnSe/ZnSe-Quantenpunkten mit Europiumdotierung
- Hochempfindlicher chemischer Ethanolsensor basierend auf neuartigem Ag-dotiertem mesoporösem α-Fe2O3, hergestellt durch modifiziertes Sol-Gel-Verfahren
- Synthese und Eigenschaften von wasserlöslichen blau emittierenden Mn-legierten CdTe-Quantenpunkten
- Dual emittierende und farbabstimmbare Mn-dotierte InP/ZnS-Quantenpunkte über eine Wachstumsdotierungsmethode
- Ultradünne und hochempfindliche Dehnungssensoren



