Korrosion in Kohlenstoffstählen
Korrosion in Kohlenstoffstählen
Gemäß ISO 8044:2010 ist „Korrosion die physikalisch-chemische Wechselwirkung zwischen einem Metall und seiner Umgebung, die zu einer Veränderung der Eigenschaften des Metalls führt und die zu erheblichen Funktionsbeeinträchtigungen des Metalls, der Umgebung oder des technischen Systems führen kann denen sie einen Teil bilden“. Korrosion tritt auf, wenn sich die Eigenschaften des Metalls oder Systems ändern, was zu einem unerwünschten Ergebnis führen kann. Dies kann von der reinen Sehbehinderung bis zum kompletten Ausfall technischer Anlagen reichen, die große wirtschaftliche Schäden verursachen und sogar Menschen gefährden.
Korrosion kann allgemein als die Zerstörung oder Verschlechterung von Metall durch direkte chemische und elektrochemische Reaktion mit seiner Umgebung definiert werden. Einfach ausgedrückt ist metallische Korrosion die Umkehrung der Galvanik. Das zu korrodierende Metall bildet die Anode, während die Kathode das zu galvanisierende ist. Metallkorrosion tritt auf, da in vielen Umgebungen die meisten Metalle nicht von Natur aus stabil sind und dazu neigen, in eine stabilere Kombination zurückzukehren, wofür die in der Natur vorkommenden Metallerze bekannte Beispiele sind
Kohlenstoffstahl ist das am weitesten verbreitete Konstruktionsmaterial. Es hat eine relativ begrenzte Korrosionsbeständigkeit. Die Kosten der Korrosion von Kohlenstoffstahl für die Gesamtwirtschaft sind sehr hoch. Da die Kohlenstoffstähle die größte verwendete Einzelklasse von Legierungen darstellen, sowohl hinsichtlich der Tonnage als auch der Gesamtkosten, ist die Korrosion von Kohlenstoffstählen ein Problem von enormer praktischer Bedeutung. Bei Kohlenstoffstahl kann der typische Korrosionsprozess als die thermodynamisch begünstigte Umkehrreaktion des Metallgewinnungs-(Extraktions-)Prozesses angesehen werden, wie in Abb. 1 gezeigt.
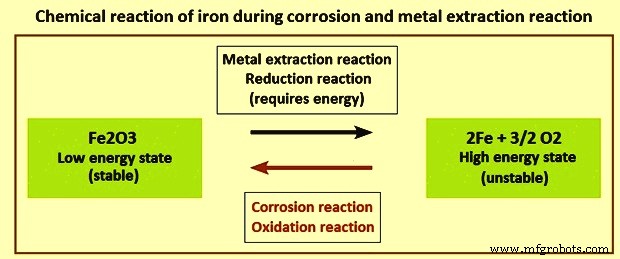
Abb. 1 Chemische Reaktion von Eisen während der Korrosions- und Metallextraktionsreaktion
Kohlenstoffstahl (der Weichstähle einschließt) hat naturgemäß einen begrenzten Legierungsgehalt, normalerweise weniger als 2 Gew.-% für die Gesamtheit aller Zusätze. Leider bewirken diese Zugabemengen im Allgemeinen keine bemerkenswerten Änderungen im allgemeinen Korrosionsverhalten. Eine mögliche Ausnahme von dieser Aussage sind wetterbeständige Stähle, bei denen kleine Zusätze von Kupfer, Chrom, Nickel und/oder Phosphor in bestimmten Umgebungen zu einer erheblichen Verringerung der Korrosionsrate führen. Bei den Gehalten an verschiedenen Elementen, in denen sie im Kohlenstoffstahl vorhanden sind, haben die Elemente keine signifikante Wirkung auf die Korrosionsrate in der Atmosphäre, neutralen Gewässern oder Böden. Lediglich bei Säureangriff ist eine Wirkung zu beobachten. In diesem Fall erhöhen die Anwesenheit von Phosphor und Schwefel die Angriffsgeschwindigkeit deutlich. Tatsächlich scheinen in Säuresystemen die reinen Eisen den besten Widerstand gegen Angriffe zu zeigen.
Korrosionsreaktionen finden statt, wenn Bedingungen thermodynamisch günstig für die chemischen Reaktionen sind. Wenn dies geschieht, dann steuern möglicherweise andere Faktoren die Geschwindigkeit der Reaktion (Kinetik der Reaktion). Die Korrosionsgeschwindigkeit hängt stark von der Umgebung ab, in der die Kohlenstoffstähle verwendet werden. Bei der Lösung eines bestimmten Korrosionsproblems kann oft eine dramatische Änderung der Angriffsrate erreicht werden, indem die korrosive Umgebung verändert wird. Da Korrosion ein so facettenreiches Phänomen ist, ist es im Allgemeinen nützlich zu versuchen, die verschiedenen Arten basierend auf der Umgebungsbasis zu kategorisieren, wie z. B. atmosphärische Korrosion, wässrige Korrosion, Korrosion in Böden, Beton und Kesseln usw.
Arten von Korrosionsreaktionen
Man unterscheidet zwischen Korrosionsarten, die normalerweise die Wechselwirkung zwischen Metall und Umgebung beschreiben, und Korrosionsformen, die das phänomenologische Erscheinungsbild beschreiben.
Chemische Reaktion – Es handelt sich um eine typische chemische Korrosionsreaktion bei hohen Temperaturen, bei der das Metall mit heißen Gasen reagiert und eine Oxidschicht bildet.
Metallphysikalische Reaktion – Das Beispiel der Metallo-physikalischen Reaktion ist die Versprödung durch Wasserstoff, der in das Metall eindiffundiert und möglicherweise zum Versagen eines Bauteils führt. Versprödung kann das Ergebnis eines unvorsichtigen Herstellungsprozesses sein. Es kann auch durch Korrosionsprozesse (Metallauflösung) wie korrosionsinduzierte wasserstoffunterstützte Rissbildung ausgelöst werden.
Elektrochemische Reaktion – Es ist die häufigste Art von Korrosionsreaktion. Die Reaktion impliziert einen elektrischen Austausch durch Elektronen im Metall und Ionen in einem leitenden Elektrolyten, beispielsweise einem Wasserfilm auf seiner Oberfläche.
Die Gesamtreaktion kann in zwei Teilreaktionen unterteilt werden, nämlich (i) Metallauflösung, auch bekannt als Oxidation oder anodische Reaktion (Fe =Fe2+ + 2 e-), und (ii) Reduktion oder kathodische Reaktion, eine Reaktion, bei der hauptsächlich der vorhandene Sauerstoff beteiligt ist in der Luft mit Wasser (O2 + 2 H2O + 4 e- =4 OH). Diese beiden Teilreaktionen können auf der Metalloberfläche in einer ziemlich homogenen Verteilung stattfinden, was zu einem gleichmäßigen Angriff führt, oder sie können lokal und getrennt auftreten, was zu lokalisierten Korrosionsformen wie Lochfraßkorrosion führt.
Der Mechanismus und die elektrochemische Natur der Korrosionsreaktion definieren die notwendigen Voraussetzungen für das Auftreten von Korrosion (Abb. 2). Diese Voraussetzungen sind (i) ein leitfähiges Metall, (ii) ein Elektrolyt (ein dünner Feuchtigkeitsfilm auf der Oberfläche reicht bereits aus) und (iii) Sauerstoff für die kathodische Reaktion.
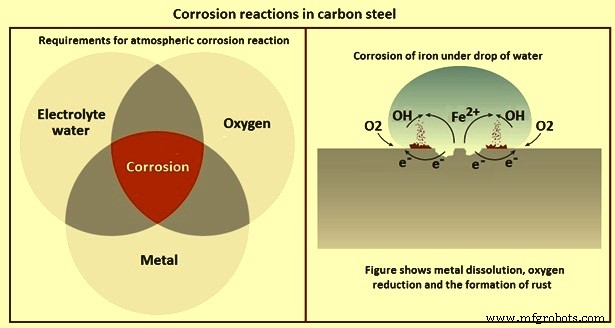
Abb. 2 Korrosionsreaktionen in Kohlenstoffstahl
Abb. 2 zeigt auch den grundlegenden Korrosionsmechanismus von Eisen unter einem Wassertropfen. Sowohl Eisenlösungs- als auch Sauerstoffreduktionsreaktionen laufen mit leichter Abscheidung an der Oberfläche ab und ihre Produkte (Fe-Ionen und OH-Ionen) reagieren im Wassertropfen zu Rotrost (Korrosionsprodukt). Das einfache Modell der Korrosionsreaktion von Bild 2 erklärt viele Korrosionsformen und leitet auch Maßnahmen zur Korrosionsminderung ab. Indem eine der Teilreaktionen verhindert oder verlangsamt wird, kann die Gesamtkorrosionsrate reduziert werden.
Korrosionsformen
Es gibt sechs Hauptformen von Korrosion (Abb. 3). Diese sind (i) gleichmäßige Korrosion/flache Lochfraßkorrosion, (ii) Lochfraßkorrosion, (iii) umweltbedingte Rissbildung, (iv) Spaltkorrosion, (v) interkristalline (intergranulare) Korrosion und (vi) galvanische Korrosion .
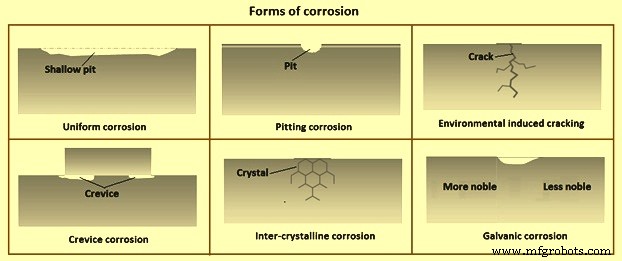
Bild 3 Korrosionsformen
Gleichmäßige Korrosion/flache Lochfraßkorrosion – Gleichmäßige Korrosion ist eine Form der Korrosion, bei der die Oberfläche nahezu gleichmäßig abgetragen wird. Die Teilreaktionen (Metallauflösung und Sauerstoffreduktion) sind statistisch über die Oberfläche verteilt, was zu einer mehr oder weniger homogenen Auflösung des Metalls und einer gleichmäßigen Bildung von Korrosionsprodukten (z. B. Rotrost auf Kohlenstoffstahl) führt. Das Ausmaß dieser Korrosionsform lässt sich aufgrund bisheriger Erfahrungen in der Regel gut abschätzen. Die Korrosionsrate wird normalerweise in Mikrometer pro Jahr angegeben. Anhand dieser Durchschnittswerte ist es möglich, die Lebensdauer eines Bauteils zu berechnen und somit die Lebensdauer durch Erhöhung der Dicke zu erhöhen.
Auf ungeschütztem Kohlenstoffstahl und auf verzinktem Stahl findet unter atmosphärischen Bedingungen eine gleichmäßige Korrosion statt. In der Realität ist es unwahrscheinlich, dass ein rein homogener Korrosionsangriff stattfindet. Gerade bei komplexen Stahlteilen gibt es immer Bereiche, die schneller korrodieren als andere, was zu einer mehr oder weniger rauen Oberfläche mit unregelmäßigem Belag von Korrosionsprodukten führt.
Lochkorrosion – Lochkorrosion ist eine lokalisierte Form der Korrosion, die zur Bildung kleiner Löcher oder Vertiefungen im Stahl führt. Diese Korrosionsform findet sich vor allem bei passiven Metallen, die ihre Korrosionsbeständigkeit einer nur wenige Nanometer dicken Oxidschicht an der Oberfläche verdanken. Der korrosionsinitiierende Prozess beginnt mit einem lokalen Durchbruch der Passivschicht. An Stählen kann beispielsweise durch Chloridionen ein lokaler Korrosionsangriff ausgelöst werden. Lochkorrosion kann ziemlich problematisch sein. Während an der Oberfläche gleichmäßige Korrosion deutlich erkennbar ist, zeigt sich Lochfraßkorrosion oft nur als kleine Nadelstiche an der Oberfläche. Die Menge des unter den Nadellöchern entfernten Materials ist im Allgemeinen unbekannt, da sich verborgene Hohlräume bilden können, wodurch Lochfraßkorrosion schwieriger zu erkennen und vorherzusagen ist. Technisch gesehen gibt es keine vernünftige Möglichkeit, Lochfraßkorrosion zu kontrollieren. Diese Korrosionsform muss durch konstruktive Überlegungen und die Verwendung des richtigen Materials von vornherein ausgeschlossen werden.
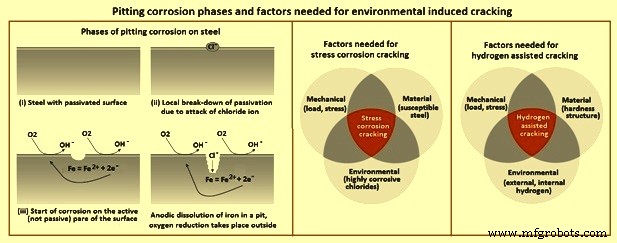
Abb. 4 Phasen der Lochfraßkorrosion und erforderliche Faktoren für umweltbedingte Rissbildung
Umweltbedingte Rissbildung – Es gibt zwei Arten von umweltbedingter Rissbildung. Dies sind (i) Spannungskorrosionsrisse und (ii) wasserstoffunterstützte Risse (Abb. 4).
Spannungsrisskorrosion ist ein kombinierter mechanischer und elektrochemischer Korrosionsprozess, der zur Rissbildung bestimmter Materialien führt. Es kann zu einem unerwarteten plötzlichen Sprödversagen von normalerweise duktilen Metallen führen, die Spannungen ausgesetzt sind, die weit unter ihrer Streckgrenze liegen. Eigenspannungen in einem Material können ausreichen, um einen Angriff von Spannungsrisskorrosion auszulösen.
Spannungsrisskorrosion ist nicht einfach eine Überlagerung von Korrosion und mechanischen Spannungen, sondern kann als autokatalytischer, sich selbst beschleunigender Prozess verstanden werden, der zu hohen Metallauflösungsraten führt (anodische Reaktion). Anfänglich bildet sich eine kleine Vertiefung, die sich aufgrund der aufgebrachten Spannungen oder Eigenspannungen im Material zu einem Riss entwickelt. Die Rissbildung eröffnet eine neue aktive (nicht passive) Metalloberfläche, die wiederum sehr leicht korrodiert. Dies führt zu weiterer Rissausbreitung und wiederum zur Freilegung neuer hochaktiver Metalloberflächen im Riss. Die Metallauflösung im Riss schreitet schnell voran, bis ein mechanisches Versagen auftritt.
Spannungsrisskorrosion ist eine sehr spezifische Form der Korrosion, die nur auftritt, wenn die folgenden drei unterschiedlichen Anforderungen gleichzeitig erfüllt sind (Bild 4), nämlich (i) mechanisch (Belastung, Spannung), (ii) Material (anfällige Legierung, z. B. Stahl). ) und (iii) Umgebung (stark ätzend, Chloride). Es ist allgemein bekannt, dass bestimmte Stahlsorten in rauen Umgebungen wie Schwimmbädern Spannungsrisskorrosion erleiden können. In den meisten dieser Fälle wird die Korrosion durch Chloride ausgelöst, die die Passivschicht angreifen.
Wasserstoffunterstützte Rissbildung wird durch die Diffusion von Wasserstoffatomen in den Stahl verursacht. Das Vorhandensein von Wasserstoff im Gitter schwächt die mechanische Integrität des Metalls und führt zu Risswachstum und Sprödbruch bei Spannungsniveaus unterhalb der Streckgrenze. Wie die Spannungsrisskorrosion kann sie ohne erkennbare Warnzeichen zum plötzlichen Versagen von Stahlteilen führen. In gängigen Anwendungen ist eine Wasserstoffschädigung meist nur für hochfesten Stahl mit einer Zugfestigkeit von etwa 1 MPa oder höher relevant.
Bei der Spannungsrisskorrosion müssen drei verschiedene Bedingungen (Bild 4) gleichzeitig vorliegen. Dies sind (i) Mechanik (Belastung, Spannung), (ii) Material (Härtestruktur), (iii) Umgebung (externer Wasserstoff, interner Wasserstoff).
Die Wasserstoffquelle kann der Produktionsprozess wie Stahlherstellung, Beizen und Elektroverzinken (primärer Wasserstoff) sein. Eine sekundäre Quelle kann der während eines Korrosionsprozesses gebildete Wasserstoff sein. Während des Korrosionsprozesses wird Wasserstoff gebildet und diffundiert in das Material. Diese Wasserstoffaufnahme führt zu einer Abnahme der Zähigkeit bzw. Duktilität des Stahls.
Spaltkorrosion – Spaltkorrosion bezieht sich auf Korrosion, die in Rissen oder Spalten auftritt, die zwischen zwei Oberflächen (aus demselben Metall, verschiedenen Metallen oder sogar einem Metall und einem Nichtmetall) gebildet werden. Diese Korrosionsart wird durch den eingeschränkten Zutritt von Sauerstoff aus der Luft durch Diffusion in den Spaltbereich ausgelöst, was zu unterschiedlichen Konzentrationen an gelöstem Sauerstoff im gemeinsamen Elektrolyten (der sogenannten Belüftungszelle) führt. Auch hier finden die beiden Teilreaktionen an unterschiedlichen Stellen der Oberfläche statt. Die Sauerstoffreduktion findet in den durch die Umgebungsluft gut zugänglichen Außenbereichen mit höheren Sauerstoffkonzentrationen statt, während die anodische Metallauflösung im Spaltbereich erfolgt, was zu lokalen Angriffen (z. B. Lochfraß) führt. Es kann auch unter Unterlegscheiben oder Dichtungen auftreten, wenn das Eindringen von Wasser darunter nicht verhindert wird.
Es gibt untere und obere Grenzen für die Größe eines Spaltes, in dem Korrosion induziert werden kann. Wenn der Spalt zu eng ist, wird kein Korrosionselektrolyt eingebracht. Wenn der Spalt zu breit ist, um den Sauerstoffeintrag zu reduzieren, kann sich die Belüftungszelle und folglich unterschiedliche Sauerstoffkonzentrationen nicht entwickeln. Die kritische Spaltbreite hängt jedoch von mehreren Faktoren ab, wie z. B. der Art der verwendeten Stähle, der korrodierenden Umgebung und den Nass-/Trockenzyklen.
Interkristalline (intergranulare) Korrosion – Interkristalline Korrosion ist eine Sonderform der Punktkorrosion, bei der der korrosive Angriff auf einem recht schmalen Pfad bevorzugt entlang der Korngrenzen im Metallgefüge erfolgt. Die häufigste Folge dieser Korrosionsform ist ein schneller mechanischer Zerfall (Dehnbarkeitsverlust) des Materials. Normalerweise kann dies durch die Verwendung des richtigen Materials und des richtigen Produktionsprozesses verhindert werden.
Ein bekanntes Beispiel ist die sogenannte Sensibilisierung von Edelstahl. Wenn bestimmte Qualitäten dieses Materials für eine beträchtliche Zeit, z.B. Während eines Schweißprozesses werden chromreiche Karbide gebildet, was zu einer Chromverarmung an den Korngrenzen führt. Folglich besitzen die Korngrenzen eine geringere Korrosionsbeständigkeit als das Restmaterial, was zu einem lokalen Korrosionsangriff führt.
Galvanische (Kontakt-) Korrosion – Galvanische Korrosion bezieht sich auf Korrosionsschäden, bei denen zwei unterschiedliche Metalle eine elektrisch leitende Verbindung haben und in Kontakt mit einem gemeinsamen korrosiven Elektrolyt sind. Im elektrochemischen Korrosionsmodell findet eine der beiden Teilreaktionen (anodische Metallauflösung und kathodische Sauerstoffreduktion) fast ausschließlich an einem Metall statt. Normalerweise wird das unedlere Metall aufgelöst (anodische Metallauflösung), während der edlere Teil nicht durch Korrosion angegriffen wird (dient nur als Kathode für die Sauerstoffreduktion). Wo galvanische Korrosion stattfindet, ist die Korrosionsgeschwindigkeit des unedleren Metalls höher als in einer freien korrodierenden Umgebung ohne Kontakt zu einem anderen Metall.
Anhand thermodynamischer Daten und unter Berücksichtigung gemeinsamer Erfahrungen aus typischen Anwendungen lässt sich vorhersagen, welche Materialkombinationen von galvanischer Korrosion betroffen sind. Ein positives Beispiel für das Phänomen der galvanischen Korrosion ist die Art und Weise, wie Zink Kohlenstoffstähle und niedriglegierte Stähle schützt. Zink ist das unedlere Metall, das Stahl aktiv schützt, indem es selbst korrodiert.
Atmosphärische Korrosion von Kohlenstoffstahl
Die Korrosion von Kohlenstoffstahl in der Atmosphäre und in vielen wässrigen Umgebungen lässt sich am besten vom Standpunkt der Filmbildung und des Abbaus verstehen. Es ist eine unausweichliche Tatsache, dass Eisen in Gegenwart von Sauerstoff und/oder Wasser gegenüber seinen Oxiden thermodynamisch instabil ist. Die Frage ist also nie, ob der Stahl korrodiert, sondern wie schnell. Ohne Filmbildung und bei konstanter Umgebung ist eine konstante Oxidationsgeschwindigkeit zu erwarten. Wenn andererseits der sich bildende Korrosionsproduktfilm den Stahl von der korrosiven Umgebung isoliert, dann wird nach der anfänglichen Filmbildungsperiode eine Korrosionsrate von Null erwartet. Ein fest haftender Film, der nur einen Diffusionstransfer der Reaktanden zulässt, zeichnet sich durch eine mit der Quadratwurzel der Einwirkzeit abnehmende Korrosionsgeschwindigkeit aus. Da die obigen Idealisierungen selten bei der Korrosion von Kohlenstoffstählen angetroffen werden, ist es offensichtlich, dass andere Faktoren wirksam sind, die dazu neigen, eine stabile Filmbildung zu stören. Diese Faktoren können extern sein, wie Erosion durch Wind oder Regen, oder sie können intern in der Folie selbst sein, wie Spannungen, die durch die unterschiedlichen spezifischen Volumina von Metall und Oxid verursacht werden.
Die Korrosion von Eisen in der Atmosphäre erfolgt durch die Bildung von Oxidhydraten. Die Halbzellenreaktionen können durch die Gleichungen (i) 1/2O2 + H2O + 2e ausgedrückt werden =2(OH)- (kathodisch) und (ii) Fe =(Fe)2+ + 2e (anodisch). Dann können weitere Reaktionen auftreten, wie (i) (Fe)2+ + 2(OH)- =Fe(OH)2 und (ii) 2Fe(OH)2 + H2O + 1/2O2 =2Fe(OH)3 .
Die Oxidhydrate können während Trockenperioden Wasser verlieren und in die wasserfreien Eisen(II)- und Eisen(III)-Oxide zurückverwandelt werden. Zusätzlich bildet sich oft eine Schicht aus Magnetit (Fe3O4) oder FeO·Fe2O3 zwischen den Schichten aus Eisenoxid (FeO) und Hämatit (Fe2O3). Tatsächlich bilden die verschiedenen Oxide und Hydroxide des Eisens ein ziemlich kompliziertes System von Verbindungen. Es wurde festgestellt, dass die Verbindung FeOOH in drei verschiedenen Kristallformen plus einer amorphen Form existiert. Das Vorkommen der verschiedenen Oxidarten ist abhängig vom pH-Wert, der Sauerstoffverfügbarkeit, verschiedenen Luftschadstoffen und der Zusammensetzung des Kohlenstoffstahls, wie bei kupfer- und phosphorhaltigen Verwitterungsstählen. Die tatsächliche Beschaffenheit des Korrosionsfilms ist wichtig, da FeO und FeOOH anscheinend stärker haften als Fe3O4 und Fe2O3 und daher eher den Korrosionsangriff verlangsamen, aber die höheren Oxide und Oxyhydroxide anfälliger für Abplatzungen sind.
Da die Korrosionsraten von Kohlenstoffstählen in unterschiedlichen atmosphärischen Umgebungen (ländlich, städtisch, industriell und marine usw.) erheblich variieren, ist es nur logisch zu bestimmen, welche der Faktoren zu diesen Unterschieden beitragen. Obwohl die Vorhersage der Korrosivität nicht möglich ist, scheinen Feuchtigkeit, Temperatur und die Gehalte an Chlorid, Sulfat und wahrscheinlich anderen atmosphärischen Schadstoffen jeweils einen Einfluss auf die Korrosionsrate von Kohlenstoffstählen auszuüben.
Auswirkungen von Feuchtigkeit und Luftschadstoffen – Da atmosphärische Korrosion ein elektrolytischer Prozess ist, ist die Anwesenheit eines Elektrolyten erforderlich. Dies bedeutet nicht, dass die Stahloberfläche mit Wasser überspült werden soll. Tatsächlich reicht ein sehr dünner absorbierter Wasserfilm aus. Während einer tatsächlichen Belichtung verbringt der Stahl einen Teil der Zeit mit Wasser überflutet aufgrund von Regen oder Spritzern und einen Teil der Zeit mit einem dünnen adsorbierten Wasserfilm bedeckt. Der Zeitanteil, der mit dem dünnen Wasserfilm bedeckt ist, hängt ganz stark von der relativen Luftfeuchtigkeit an den Expositionsorten ab. Verschiedene Studien haben diese Zeit der Nässe gezeigt, obwohl ein wichtiger Faktor bei der Schätzung der Korrosionsraten nicht isoliert betrachtet werden kann. Ein Beispiel für diese Tatsache ist in Abb. 5 dargestellt, in der die Gewichtszunahme von Eisen als Funktion der relativen Luftfeuchtigkeit für eine Exposition von 55 Tagen in einer Atmosphäre mit 0,01 % Schwefeldioxid aufgetragen ist. In der unteren rechten Ecke von Abb. 5 ist die gemessene Korrosionsrate für Eisen dargestellt, das die gleiche Zeit in einer schwefeldioxidfreien Umgebung bei 99 % relativer Luftfeuchtigkeit ausgesetzt war.
Ein weiteres interessantes Merkmal ist das offensichtliche Vorhandensein eines kritischen Feuchtigkeitsniveaus, unterhalb dessen die Korrosionsrate gering ist. Die kritische Luftfeuchtigkeit in einer schwefeldioxidhaltigen Umgebung liegt bei etwa 60 %. Dieses Verhalten steht im Gegensatz zu dem von Stahl in Kontakt mit Meersalzpartikeln, wie in Abb. 5 gezeigt. In Abb. 5 zeigt die Korrosionsrate einen stetigen Anstieg mit zunehmender Feuchtigkeit. Obwohl nur wenige Daten vorliegen, erscheint es plausibel, dass Stickoxide in der Umwelt ebenfalls eine beschleunigende Wirkung auf die Korrosion von Kohlenstoffstahl haben. Tatsächlich ist zu vermuten, dass jeder gasförmige atmosphärische Bestandteil, der zu einer starken elektrolytischen Aktivität fähig ist, die Korrosionsrate von Kohlenstoffstahl erhöhen kann. Kurz gesagt, es ist ersichtlich, dass Chloridionen eine beschleunigende Wirkung auf die atmosphärische Korrosion haben,
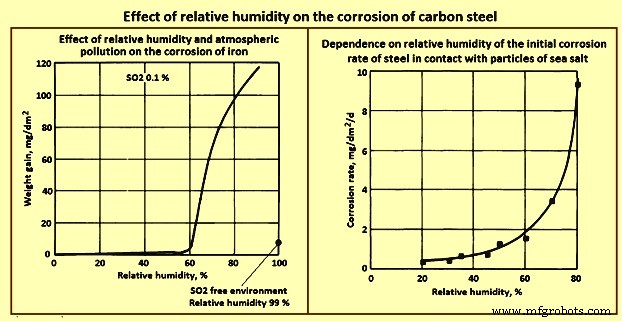
Abb. 5 Einfluss der relativen Luftfeuchtigkeit auf die Korrosion von C-Stählen
Korrosionsschutz von Kohlenstoffstählen
Korrosionsschutz (Abb. 6) ist oft eine notwendige Überlegung bei der Auswahl von Kohlenstoffstahl für eine bestimmte Konstruktionsanwendung. Korrosion kann die Tragfähigkeit eines Bauteils verringern, entweder durch generelle Verringerung seiner Größe (Querschnitt) oder durch Lochfraß, der nicht nur den wirksamen Querschnitt im Bereich mit Lochfraß verringert, sondern auch Spannungserhöhungen einführt, die Risse initiieren können. Offensichtlich verlängert jede Maßnahme, die Korrosion verringert oder beseitigt, die Lebensdauer eines Bauteils und erhöht seine Zuverlässigkeit. Die Wirtschaftlichkeit, die Umgebungsbedingungen, der für die voraussichtliche Lebensdauer des Teils erforderliche Schutzgrad, die Folgen eines unerwarteten Betriebsausfalls und die Bedeutung des Aussehens sind die Hauptfaktoren, die nicht nur bestimmen, ob ein Stahlteil vor Korrosion geschützt werden muss, sondern auch am meisten effektive und wirtschaftliche Methode, um diesen Schutz zu erreichen.
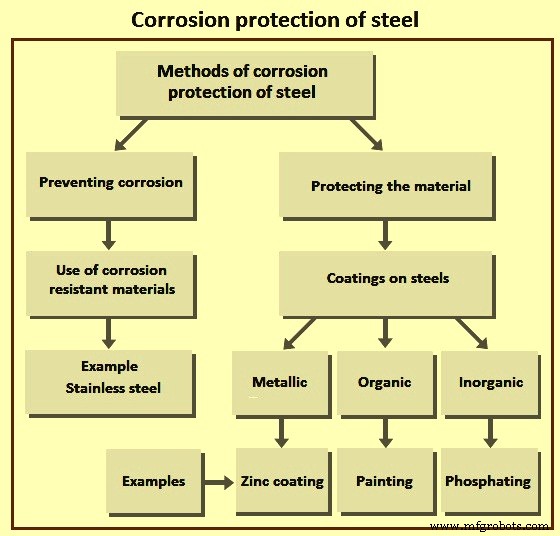
Bild 6 Korrosionsschutz von Stahl
Es gibt zwei Methoden, um die Korrosion von Stählen zu minimieren. Die erste besteht darin, die Reaktionsphasen zu trennen, und die zweite besteht darin, die Reaktivität der Reaktionsphasen zu verringern. Die Trennung der reagierenden Phasen kann durch metallische, anorganische oder organische Beschichtungen und Filmbildungsinhibitoren erfolgen. Die Reaktivität kann durch Legieren, anodischen oder kathodischen Schutz und chemische Behandlung der Umgebung verringert werden. Einige Schutzmethoden kombinieren zwei oder mehr Formen.
In den meisten Umgebungen beträgt die Korrosionsrate von Kohlenstoffstahl in einer ländlichen Umgebung im Freien typischerweise etwa 20 Mikrometer pro Jahr und steigt in Küstenumgebungen auf mehr als 100 Mikrometer pro Jahr an. Sie ist normalerweise zu hoch für eine zufriedenstellende Anwendung. Das Produktdesign berücksichtigt im Allgemeinen keinen Grundmaterialverlust. Daher sind für Kohlenstoffstahl kosteneffiziente Korrosionsschutzlösungen erforderlich. In alkalischer Umgebung bleibt Stahl jedoch normalerweise stabil. Dies erklärt, warum beispielsweise Bewehrungsstäbe aus Kohlenstoffstahl bereits im alkalischen Milieu des umgebenden Betons sehr gut vor Korrosion geschützt sind.
Beschichtungsschutz von Kohlenstoffstahl
Es werden verschiedene Arten von Beschichtungen aufgebracht, um die Korrosionsbeständigkeit von Kohlenstoffstählen zu verbessern. Die Beschichtungspraktiken reichen von Ölen für kostengünstigen, temporären Schutz bis hin zu Dampfabscheidung für langfristige Korrosions-, Hitze- und Verschleißbeständigkeit. Aus wirtschaftlichen Gründen ist vor der Auswahl einer Beschichtung die gewünschte Schutzart zu ermitteln.
Ein wirksamer vorübergehender Schutz während des Versands oder der Lagerung kann durch Beschichten des Kohlenstoffstahls mit Mineralöl, Lösungsmitteln in Kombination mit Inhibitoren, Emulsionen von Beschichtungen auf Erdölbasis oder Wachsen erreicht werden. Diese Arten von Beschichtungen werden nach dem Säurebeizen oder zwischen Beschichtungssequenzen aufgebracht. Von diesen Beschichtungen wird kein langfristiger Korrosionsschutz erwartet.
Die Oberflächenvorbereitung ist für alle Beschichtungsprozesse wichtig. Oxide auf der Stahloberfläche sind durch Beizen oder Strahlen zu entfernen. Das Entfetten ist nach der Oxidentfernung oder nach einer vorübergehenden Beschichtung des Stahls erforderlich und kann auf verschiedene Weise erfolgen. Idealerweise wird direkt nach der Reinigung mit dem ersten Schritt des Beschichtungsprozesses begonnen.
Beschichtungsverfahren – Diese werden verwendet, um Beschichtungen aus Zink, Aluminium, Blei, Zinn und einigen Legierungen dieser Metalle auf Kohlenstoffstähle aufzubringen. Das Schmelztauchverfahren besteht aus dem Eintauchen des Stahls in ein geschmolzenes Bad des Beschichtungsmetalls.
Verzinken oder Verzinken ist eine gute Wahl für den Korrosionsschutz von Kohlenstoffstahl. Für das Aufbringen von Zinküberzügen auf Stahl stehen mehrere geeignete Verfahren zur Verfügung. Die Korrosionsrate von Zink ist mit etwa 0,5 Mikrometer pro Jahr in ländlicher/städtischer Atmosphäre mehr als zehnmal niedriger als die von Stahl und steigt in Küstenumgebungen auf bis zu etwa 5 Mikrometer pro Jahr an. Die niedrigen Korrosionsraten sind das Ergebnis der Bildung stabiler Schichten aus Korrosionsprodukten, die Karbonate (aus CO2 in der Luft) und Chloride (falls sie in der Atmosphäre vorhanden sind) enthalten. Bedingungen, bei denen die Bildung solcher unlöslicher Korrosionsprodukte nicht möglich ist, führen zu viel höheren Korrosionsraten, schränken die Eignung von Zink als Schutzbeschichtung ein. Dazu gehören Dauernässe oder die Belastung durch hohe Konzentrationen industrieller Schadstoffe wie Schwefeldioxid. In diesen Umgebungen werden bevorzugt lösliche Korrosionsprodukte gebildet, die durch Niederschläge abgewaschen werden können. Zusätzlich zu verringerten Korrosionsraten bietet Zink auch einen kathodischen oder Opferschutz für den darunter liegenden Stahl. Wo Kratzer, Absplitterungen oder andere Beschädigungen der Zinkbeschichtung den Stahl freilegen, findet eine besondere Form der galvanischen Korrosion statt. Zink, ein weniger edles Metall als Stahl, korrodiert bevorzugt und trägt dadurch dazu bei, dass die freiliegende Stahloberfläche geschützt bleibt.
Zinküberzüge werden bei atmosphärischer Korrosion ziemlich homogen verbraucht. Dementsprechend verdoppelt sich bei einer gegebenen Anwendung normalerweise auch die Verdoppelung der Schichtdicke, bis das Zink verbraucht ist und Rotrost auf dem Stahlsubstrat auftritt. Zink ist in alkalischen Umgebungen nicht stabil und wird in Lösungen mit einem pH-Wert von 10 oder höher leicht angegriffen.
Die Verfahren der Zinkbeschichtung sind Elektroverzinkung, Feuerverzinkung und Sherardisierung. Das Sherardisieren ist ein Verfahren zur Zinkbeschichtung unter Verwendung eines thermischen Diffusionsprozesses.
Aluminium-Feuertauchbeschichtungen (Aluminieren) verleihen Kohlenstoffstählen Korrosions- und Hitzebeständigkeit. In vielen Umgebungen schützt Aluminium Stahl galvanisch ähnlich wie Zink. Auch Zink-Aluminium- und Aluminium-Zink-Legierungen werden durch Schmelztauchen auf Stahl aufgebracht. Das Erhitzen von aluminiertem Stahl führt zur Bildung einer intermetallischen Eisen-Aluminium-Verbindung, die einer Oxidation bei Temperaturen bis zu etwa 800 °C widersteht
Feuerverzinnte Beschichtungen bieten eine dekorative und ungiftige Barrierebeschichtung. Zinn schützt das Stahlsubstrat nicht galvanisch. Aus diesem Grund werden häufig Lacke oder andere organische Beschichtungen verwendet, um Poren in der Zinnbeschichtung zu füllen und einen verbesserten Barriereschutz bereitzustellen.
Schmelztauchbleibeschichtungen werden manchmal auf Stahl verwendet, der Schwefelsäuredämpfen oder anderen aggressiven chemischen Umgebungen ausgesetzt ist. Terne Plate, eine Blei-Zinn-Legierungsbeschichtung, bietet mehr Schutz als reine Bleibeschichtungen und ist lötbar.
Galvanische Beschichtungen werden auf Stahl für Korrosionsbeständigkeit, Aussehen, Lötbarkeit oder andere spezielle Anforderungen aufgebracht. Eine Vielzahl von Materialien wird auf Stahl galvanisiert, darunter Zink, Aluminium, Chrom, Kupfer, Cadmium, Zinn und Nickel. Mehrschichtige Beschichtungen können auch galvanisch aufgebracht werden. Ein Beispiel ist das Kupfer-Nickel-Chrom-Beschichtungssystem, das für glänzende Automobilverkleidungen verwendet wird.
Plattierte Metalle – Kohlenstoffstähle können mit korrosionsbeständigeren Materialien wie Kupfer und rostfreien Stählen durch Kaltwalzenbonden, Heißwalzenbonden, Heißpressen, Explosionsbonden und Extrusionsbonden verbunden werden. Das resultierende lamellare Verbundmaterial hat spezifische Eigenschaften, die in einem einzelnen Material nicht erhältlich sind.
Thermische Spritzbeschichtungen – Diese Beschichtungen bieten einen wirksamen Langzeit-Korrosionsschutz für Stähle in einer Vielzahl von korrosiven Umgebungen. Sie werden durch eines von mehreren Verfahren aufgebracht, einschließlich Drahtflammspritzen, Pulverflammspritzen und Lichtbogenspritzen. Zink, Aluminium und Zink-Aluminium-Legierungen sind die gebräuchlichsten Beschichtungsmaterialien, die durch thermische Spritztechniken aufgetragen werden. Austenitische rostfreie Stähle, Aluminiumbronzen und MCrAlY-Beschichtungsmaterialien (wobei M =Co, Ni oder Co/Ni) wurden ebenfalls für spezifische Anwendungen verwendet. Für maximale Korrosionsbeständigkeit werden thermisch gespritzte Beschichtungen mit einem organischen Decklack versiegelt. Thermische Spritzbeschichtungen werden häufig zum Korrosionsschutz in Schiffsanwendungen eingesetzt.
Aufdampfbeschichtungen – Diese werden manchmal zum Schutz von Kohlenstoffstahl verwendet, obwohl die Kosten für solche Beschichtungen sehr hoch sein können. Bei der Dampfabscheidung, sei es physikalische Dampfabscheidung oder chemische Dampfabscheidung, wird das Beschichtungsmaterial in Form von einzelnen Atomen oder Molekülen auf das Substrat transportiert. Durch Aufdampfen kann eine Vielzahl von Beschichtungsmaterialien aufgebracht werden. Bei ausreichender Dicke ist die Beschichtung im Wesentlichen porenfrei und dicht und bietet somit einen hervorragenden Barriereschutz. Eine wohlbekannte Anwendung für dampfabgeschiedene Beschichtungen auf Stahl sind ionendampfabgeschiedene Aluminiumbeschichtungen auf Stahlflugzeugen und Luft- und Raumfahrtkomponenten.
Phosphat- oder Chromat-Umwandlungsbeschichtungen – Diese werden verwendet, um die Korrosionsbeständigkeit von Stählen zu erhöhen. Sie selbst bieten eine etwas bessere Korrosionsbeständigkeit als blanker Stahl. Häufiger werden sie in Verbindung mit einem anderen Beschichtungssystem verwendet. Konversionsbeschichtungen werden nach der Feuerverzinkung aufgebracht und bieten einen guten Korrosionsschutz, wenn sie mit einem organischen Beschichtungssystem überzogen werden.
Beim Phosphatieren wird Stahl in eine saure Lösung getaucht, die Metall(Zn, Fe)-Phosphatsalze enthält. Die Lösung reagiert mit der Stahloberfläche und bildet eine mikrokristalline Phosphatschicht auf der Oberfläche. Dadurch entsteht eine raue Oberfläche mit hervorragenden Ölrückhalteeigenschaften.
Organische Beschichtungen – Diese Beschichtung besteht aus Lacken, die häufiger zum Korrosionsschutz von Stählen verwendet werden als jede andere Beschichtungsart. Richtig aufgetragen bieten die Lacke hervorragenden Schutz zu relativ geringen Kosten. Für die Applikation der Lacke stehen verschiedenste Beschichtungsmaterialien und Auftragsverfahren zur Verfügung.
Keramische Beschichtungen – Zu den keramischen Beschichtungen, die zum Schutz von Stahl verwendet werden, gehören Silikatzemente und Porzellanemails. Monolithische Zementauskleidungen bieten eine gute Chemikalienbeständigkeit und Wärmedämmung. Sie können durch Gießen oder Sprühen aufgetragen werden. Porzellanemails sind Glasbeschichtungen, die bei oder über 425 °C auf die Stahloberfläche aufgeschmolzen werden, um eine glasartige Beschichtung mit guter Korrosionsbeständigkeit und hoher Härte bereitzustellen. The composition of the enamel can be varied to provide desired properties, such as improved resistance to alkalis.
Other nonmetallic materials coatings – These coatings are sometimes used as coatings or linings for steel in corrosion applications. These include rubbers (both natural and synthetic) and other elastomers and such plastic materials as epoxies, phenolics, and vinyls. A wide variety of properties and resistances to specific environments are available. Rubber linings have been used for many years in steel storage tanks for hydrochloric acid and sulphuric acid. Plastic linings are employed for plating tanks and similar applications.
Multi-layer coatings – When the corrosion protection provided by the metallic coating is not sufficient, then the steel can be further protected by additional coatings, mainly organic paint with or without metallic flakes. An example of this is the multi-layer coating on fasteners consisting of an electro-plated Zn alloy coating with an additional organic top coat.
Herstellungsprozess



