Gold-Nanobiosensor basierend auf der lokalisierten Oberflächenplasmonenresonanz kann humane Brucellose diagnostizieren und stellt eine schnelle und kostengünstige Methode vor
Zusammenfassung
Brucellose gilt als die häufigste bakterielle Zoonose der Welt. Obwohl der Laborbefund heute die zuverlässigste Diagnose ist, haben die aktuellen Labormethoden viele Einschränkungen. Diese Forschung zielte darauf ab, die Leistung einer neuartigen Technik basierend auf der lokalisierten Oberflächenplasmonenresonanz (LSPR) zu entwickeln und zu bewerten, um bestehende Mängel zu beseitigen oder zu reduzieren. Zu diesem Zweck wurden glatte Lipopolysaccharide aus Brucella melitensis . extrahiert und Brucella abortus und durch kovalente Wechselwirkungen auf der Oberfläche der Goldnanopartikel fixiert. Nach einigen Optimierungsprozessen wurde dynamische Lichtstreuung verwendet, um die Sonde zu charakterisieren. Der Nachweis von eingefangenem Anti-Brucella-Antikörper erfolgte durch Messung der Rotverschiebung des LSPR-Peaks gefolgt von der Bestimmung des Cutoff-Werts, was auf einen signifikanten Unterschied zwischen Kontrollen und richtig positiven Patienten hindeutete (P Wert < 0,01). Darüber hinaus wurden 40 Seren von echten negativen Proben und positiven Patienten verwendet, um die Leistung dieser Methode zu bewerten, indem ihre Ergebnisse mit dem Goldstandard (Kultur), dem Standard-Röhrchen-Agglutinationstest und den Anti-Brucellose-IgM- und IgG-Werten (ELISA) verglichen wurden. Sensitivität, Spezifität, positiver prädiktiver Wert und negativer prädiktiver Wert zeigten eine angemessene Leistung der LSPR-basierten Methode (85 %, 100 %, 100 % bzw. 86 %). Die aktuellen Forschungsergebnisse liefern eine vielversprechende schnelle, bequeme und kostengünstige Methode zum Nachweis der Anti-Brucella-Antikörper in Humanseren, die in medizinischen Labors weit verbreitet zur schnellen und effektiven Diagnose von Brucellose eingesetzt werden kann.
Einführung
Brucellae sind langsam wachsende gramnegative Kokkobazillen, die zur Familie der Brucellaceae gehören [1]. Brucellen umfassen fakultativ intrazelluläre Bakterien, die eine Vielzahl von Haus- und Wildtieren infizieren [2]. Die Entdeckung neuer Brucella-Arten in den letzten Jahren hat die Gattung stark erweitert. Derzeit gibt es zwölf Arten der Gattung, von denen vier Brucella enthalten. Melitonie , B. Abort , B. suis , und B. canis sind die Hauptursachen der Erkrankung beim Menschen [3]. B. Melitonie gilt als die virulenteste Spezies des Menschen [3]. Obwohl Brucellose beim Menschen nicht zum Tod führt und nur ein Ausnahmefall einer Übertragung von Mensch zu Mensch ist, führt die unaufhörliche Epidemie der menschlichen Brucellose weltweit zu ernsthaften Bedenken für die öffentliche Gesundheit und wirtschaftlichen Schäden durch den Verlust der Produktivität der Tiere. Wichtig ist, dass das abnehmende Potenzial der Brucellose beim Menschen und das komplizierte Behandlungsprotokoll der Krankheit diese Bakterien zu Kandidaten für die biologische Kriegsführung gemacht haben [4, 5].
Brucellose beim Menschen wird als „Fehlerkrankheit“ [6] bezeichnet, da ihr klinisches Erscheinungsbild unspezifisch ist und sich mit einem breiten Spektrum anderer Krankheiten überschneidet; Daher ist eine labortechnische Bestätigung der Diagnose für die korrekte Behandlung eines Patienten unerlässlich [7, 8]. Obwohl Kultur, serologische Tests und Nukleinsäure-Amplifikationstests die Diagnose einer Brucellose stellen können, haben diese Methoden viele Einschränkungen. In der Kultur als Goldstandard ist die Haupteinschränkung, die die richtige Diagnose und Behandlung des Patienten verzögert, die lange Inkubationszeit. Fortschrittliche automatisierte Blutkultursysteme (z. B. Bactec- und BacTAlert-Systeme) können akute Brucellose-Fälle erkennen, benötigen jedoch 5 bis 7 Tage Inkubation, und sogar die Inkubation und Durchführung von Blind-Subkulturen für langwierige Proben müssen verlängert werden [9]. Die mangelnde Spezifität und falsch positive Ergebnisse insbesondere bei wiederholt mit Brucella-Organismen exponierten Personen sind die Haupteinschränkungen serologischer Tests [9, 10]. Obwohl sie eine ausgezeichnete Sensitivität, Spezifität, Sicherheit und schnelle Diagnose der Krankheit durch Nukleinsäure-Amplifikationsassays aufweisen, sind die klinische Bedeutung dieser Methoden und ihre begrenzten therapeutischen Implikationen aufgrund der langfristigen Beständigkeit positiver biomolekularer Testergebnisse bei Patienten nicht klar die sich vollständig erholt haben [9, 11]. Daher ist es notwendig, eine Methode zu entwickeln, die alle oben genannten Einschränkungen des Tests überwindet und gleichzeitig deren Vorteile verbessert.
Die Verbesserung von Biosensor-Geräten mit niedrigen Nachweisgrenzen ist zu einem wichtigen Bestandteil der Forschung zum Nachweis von Biomarkern geworden, da in den letzten zehn Jahren eine Vielzahl von Studien der Suche nach geeigneten Verfahren gewidmet wurde, um die Empfindlichkeit verschiedener Nachweisplattformen in der Biosensorik zu verbessern [12, 13] . Biosensoren werden verwendet, um einen Analyten nachzuweisen und zu quantifizieren, indem sie ein Signal aus Wechselwirkungen erzeugen, die biologische Komponenten umfassen. Die erhöhte Sensitivität optischer Transducer in Kombination mit der unvergleichlichen Spezifität der biomolekularen Wechselwirkungen hatte in letzter Zeit zur Entwicklung vieler verschiedener optischer Biosensoren geführt [14]. Aufgrund der einfachen Anwendung, der Empfindlichkeit gegenüber niedrigen Temperaturen und der zuverlässigen Signalerzeugung, die durch eine Rotverschiebung der Absorptionsbande als Reaktion auf biologische Wechselwirkungen belegt wird, sind die Tests, die auf den einzigartigen optischen Eigenschaften von Nanopartikeln basieren, zum Nachweis biologischer Marker kostengünstig [ 15,16,17]. Diese Nachweismethoden verwenden die biophysikalischen Eigenschaften von Molekülen wie Molekulargewicht, Ladung und Brechungsindex, um die Aktivität eines bestimmten Moleküls zu überwachen. Oberflächenplasmonenresonanz ist ein Phänomen, das durch die kollektive Oszillation von Oberflächenelektronen nach Einwirkung von einfallendem Licht verursacht wird und verwendet wurde, um oberflächengebundene Biomoleküle schnell und einfach nachzuweisen [18, 19]. Die SPR besteht aus zwei Hauptmethoden, der lokalisierten (LSPR) oder der propagierenden (PSPR) [20, 21]. Unter ihnen haben sich optische Biosensoren auf Basis lokalisierter Oberflächenplasmonen aufgrund ihres erheblichen Anwendungspotenzials bemerkenswert entwickelt [12, 22]. Diese Technik kommt von der Wechselwirkung zwischen Oberflächenelektronen leitfähiger Nanopartikel, die kürzer sind als die einfallende Lichtwellenlänge, und der Lichtwelle, die auftritt, wenn im Leitungsband einfallendes Licht mit Oberflächenelektronen wechselwirkt [23, 24]. Im Vergleich zu anderen ähnlichen Plattformen haben die auf lokalisierter Oberflächenplasmonenresonanz basierenden Biosensoren mehrere Vorteile (z. B. Oberflächenplasmonenresonanz), wie z umgebendes Medium und Fähigkeit, durch sich frei ausbreitendes Licht angeregt zu werden [12]. Daher gelten in der Nanobiosensortechnologie LSPR-basierte Nanobiosensoren als eines der leistungsfähigsten Werkzeuge zum Nachweis von Biomolekülen.
Kurzum:Einerseits sind laborbasierte Strategien nach wie vor die wichtigste Grundlage für die Diagnose der Brucellose. Andererseits unterliegen die derzeitigen klinischen Verfahren vielen Einschränkungen. Daher wird der Vorschlag einer neuen alternativen Methode, die die Unzulänglichkeiten bestehender Techniken überwinden kann, als eine der Hauptkomponenten von Behandlungsprotokollen angesehen. Daher zielte diese Studie darauf ab, einen schnellen, bequemen, kostengünstigen, sicheren und empfindlichen LSPR-basierten Nanobiosensor zum Nachweis von Anti-Brucella-Antikörpern in biologischen Proben zur Diagnose von Brucellose vorzustellen. Dazu wurden die Lipopolysaccharide (LPS) von B. melitensis und B. abortus auf Gold-Nanopartikel (GNPs) beschichtet und die Spezifität, Sensitivität, positiver Vorhersagewert (PPV) und negativer Vorhersagewert (NPV) der Technik bewertet durch Vergleich der Ergebnisse, die mit einem Serumkulturtest erzielt wurden. Darüber hinaus führte die aktuelle Studie einen enzymgekoppelten Immunadsorptionstest zur Messung der Anti-Brucellae-Antikörper (sowohl IgM als auch IgG) und einen Standard-Röhrchen-Agglutinationstest durch, um die Fähigkeit der derzeit entwickelten Technologie zum Nachweis von Brucellose im Gegensatz zu herkömmlichen Methoden zu beurteilen.
Methoden
Bakterienkultur und LPS-Extraktion
Die glatten Stämme von B. Melitonie und B. Abort wurden in Luria-Bertani kultiviert [3] Agar. Im nächsten Schritt wurden Bakterien geerntet und LPS mit einer modifizierten Heiß-Phenol-Wasser-Methode extrahiert [25]. Um die Qualität des extrahierten LPS zu bestätigen, wurde eine Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese (SDS-PAGE, Sigma-Aldrich, St. Louis, Missouri, USA) mit Silbernitratfärbung angewendet. Die LPS-Quantifizierung wurde mit 1,9-Dimethylmethylenblau (Sigma-Aldrich, St. Louis, Missouri, USA) mit Salmonella typhimurium . durchgeführt als Standard. Zur Beurteilung der Protein- und Nukleinsäurekontamination wurden die Bradford-Methode und die Absorption bei 260 nm verwendet.
Synthese sphärischer Goldnanopartikel
Eine chemische Reduktion von Goldsalz (HAuCl4 ) wurde verwendet, um die Gold-Nanopartikel zu synthetisieren, was ein schnelles, kostengünstiges und grünes Syntheseverfahren für Au-Nanopartikel bei Raumtemperatur ist [26]. Nach dem beschriebenen Verfahren wurden 15 mg Natriumcitrat (Sigma-Aldrich, St. Louis, Missouri, USA) in 50 ml destilliertem entionisiertem Wasser gelöst und in einem Eisbad aufbewahrt und auf einem Magnetrührer (150 U/min) gemischt. . Gleichzeitig wurden 600 µl Goldsalzlösung (17,3 mM) zugegeben. Anschließend wurden 1,2 ml Natriumborhydrid-Lösung (20 mM) zugegeben. Die Lösung wurde 2 h unter ähnlichen Bedingungen gemischt und dann zur späteren Anwendung bei 4 °C aufbewahrt. Nach früheren Studien wirkt Natriumcitrat bei dieser Art der Synthese gleichzeitig als Reduktionsmittel (treibt die Reduktion von AuIII zu Au0), Verkappungsmittel (elektrostatische Stabilisierung der kolloidalen Lösung der Goldnanopartikel) und pH-Mediator (verändert die Reaktivität von Au an der Reaktion beteiligte Spezies). In diesem Assay zeigt die Herstellung einer rot gefärbten Lösung aus einer gelb gefärbten Lösung von HAuCl4 die Bildung von Gold im Oxidationszustand Null.
Rasterelektronenmikroskopie (REM) wurde verwendet, um die Morphologie von Goldnanopartikeln zu untersuchen, und Zetasizer NanoZS90 (Malvern Instruments Ltd, Malvern, Worcestershire, UK) wurde verwendet, um die Größenverteilung zu beurteilen. Als Grundprinzip für die Partikelgrößenmessung wurde die dynamische Lichtstreuung (DLS) bei einem Streuwinkel von 90° verwendet. Zetasizer Nano verwendet einen Laser mit einer Wellenlänge von 633-nm. Mit dieser Technik wird die durch Brownsche Bewegung verursachte Ausbreitung von Partikeln gemessen und durch die Stokes-Einstein-Beziehung in eine Größenverteilung umgewandelt [27]. Das Zeta-Potential wurde auch angelegt, um die elektrische Oberflächenladung von Nanopartikeln zu bestimmen. Die Absorptionsspektren der Nanopartikel wurden mit einem Cary 500 UVeviseNIR-Spektrophotometer (Ultraviolett – sichtbares nahes Infrarot) (Varian, Australien) aufgenommen.
Konstruktion einer Nanosonde (Biosensor)
Carboxylierung von Gold-Nanopartikeln
Goldnanopartikel wurden mit Thioglykolsäure-Linkern beschichtet, um die Oberfläche von GNPs für die Beladung mit LPS vorzubereiten. Kurz gesagt, 1 ml TGA-Lösung (1 mM) wurde mit 1 ml Goldnanopartikellösung gemischt und 24 h bei Raumtemperatur aufbewahrt. Zur Isolierung beschichteter Goldnanopartikel wurde die Lösung 15 min bei 12.000 g zentrifugiert. Danach wurden zwei Waschschritte mit doppelt destilliertem entionisiertem Wasser verwendet, um überschüssiges TGA zu entfernen. Schließlich wurde Spektrophotometrie verwendet, um die Beschichtung von Thioglykolsäure auf der Oberfläche der GNPs zu beurteilen.
Optimierung der Beschichtung von Thioglykolsäure auf Goldnanopartikeln
Die Beschichtung mit TGA erfolgte zu unterschiedlichen Zeiten, einschließlich 12, 18, 24, 36 und 48 h, um das Beschichtungsverhältnis von TGA auf Goldnanopartikeln zu optimieren. Anschließend wurde die optische Dichte gemessen und grafisch dargestellt, um die beste Inkubationszeit zu erhalten.
Kovalente Bindung von LPS an TGA-modifizierte Goldnanopartikel
Um die kovalente Bindung zwischen der Carboxylgruppe von TGA und der Amingruppe von LPS zu stimulieren, wurden die Carboxylgruppen durch EDC (der beliebteste Nulllängen-Crosslinker für biochemische Konjugationen) und N-Hydroxysuccinimid (NHS)-Moleküle aktiviert [28]. Sedimentierte Goldnanopartikel wurden in 0,1 mM EDC/NHS-Lösung suspendiert und 30 Minuten bei Raumtemperatur inkubiert. Im nächsten Schritt wurden 2 ml Phosphatpuffer-Kochsalzlösung (PBS) mit 0,05 % Tween-20 (PBST) (pH 7,4) hinzugefügt. Nach einem kräftigen Vortex wurden die Nanopartikel 15 Minuten lang bei 12.000 U/min zentrifugiert. Nach der Zentrifugation wurde die LPS-Lösung nach dem Entfernen des Überstands zugegeben. Anschließend wurde die Mischung 10 min im Ultraschallbad inkubiert, gefolgt von einer 3 h langen Inkubation bei Raumtemperatur. Danach wurden 2 ml PBST zugegeben und kräftig gevortext, gefolgt von einer 15-minütigen Zentrifugation bei 12.000 U/min, und der Überstand wurde entfernt. Schließlich wurden die Nanosonden dann in 500 µl PBS resuspendiert und die LSPR-Spektren wurden mit einem Spektrophotometer gemessen. Nach der Bestätigung der LPS-Anheftung an die Goldnanopartikel wurde die Lösung für weitere Studien bei 4 °C aufbewahrt. Abbildung 1 zeigt die chemischen Wechselwirkungsgleichungen der TGA-modifizierten Goldnanopartikel-Synthese und der LPS-Anlagerung.
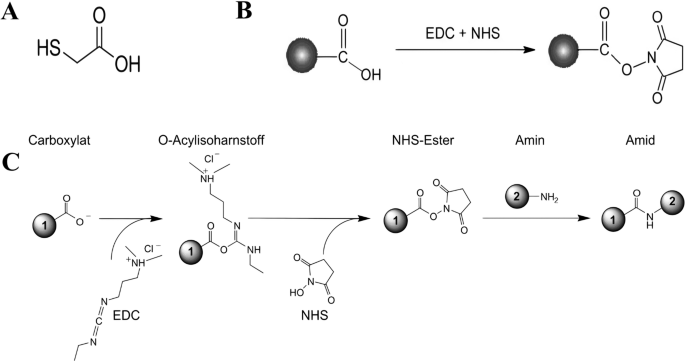
Chemische Wechselwirkungen der LPS-Anlagerung an die Goldnanopartikel. A TGA-Molekül, B EDC + NHS-Interaktion und C Kovalente Bindung von LPS an TGA-modifizierte Goldnanopartikel. Nummer 1:Nanopartikel; Nummer 2:LPS
Optimierung der LPS-Konzentration
Um die Bindung von LPS an aktivierte TGA-Carboxylgruppen zu maximieren, wurde das LPS-zu-Au-Nanopartikel-Verhältnis optimiert, indem die Peakverschiebung in den LSPR-Spektren als Funktion der LPS-Konzentrationen (100, 150, 200, 300 und 560 µg .) bewertet wurde /ml) in einer festen Menge der Au-Nanopartikel.
Nachweis von Anti-LPS-Antikörpern durch Nanoprobe
100 µl der verdünnten Proben (1:50 in PBS) wurden mit 200 µl des Biosensors vermischt und durch Pipettieren vermischt. Im nächsten Schritt wurden die Biosensoren nach 30-minütiger Inkubation bei Raumtemperatur 15 min bei 12.000 g zentrifugiert. Schließlich wurden die Biosensoren in 200 µl PBS suspendiert und die Extinktion wie zuvor beschrieben gemessen. Zur Validierung der Nanobiosensor-Funktion wurden auch positive und negative Kontrollen aus einem kommerziell erhältlichen ELISA-Kit (Pishtazteb Zaman, Iran) bereitgestellt.
Ethikerklärung
Die Verwendung von Humanseren wurde von den Ethikkommissionen der Fasa University of Medical Sciences Fasa, Iran (IR.FUMS.1396.324) genehmigt. Die Identitäten der Serenspender wurden kodiert und niemandem, der an dieser Studie beteiligt war, bekannt gegeben. Darüber hinaus wurden alle Verfahren gemäß den nationalen Vorschriften unter ethischen Richtlinien durchgeführt. Darüber hinaus stammten alle Proben von Probanden, die die schriftliche Einverständniserklärung unterzeichnet hatten.
Evaluieren der Funktion der entworfenen Methode
Vierzig Proben mit 20 Fällen (richtig positiv) und 20 Kontrollen (richtig negativ) wurden bereitgestellt, um die Funktionalität der entwickelten Methode zu bewerten. Aus diesem Grund wurde die Leistung der entwickelten Methode in der vorliegenden Studie mit den Kulturergebnissen verglichen. Darüber hinaus wurden verfügbare kommerzielle Kits (Pishtaz Teb, Teheran, Iran) verwendet, um die Serumspiegel von IgM- und IgG-Antikörpern zu bestimmen. Die Probenvorbereitung und Antikörperbewertung erfolgte nach Herstellerprotokoll (Spezifität:99,85 %, Sensitivität:99,4 %). Darüber hinaus wurde der Standardröhrchen-Agglutinationstest mit allen Serumproben durchgeführt, um die Leistung der LSPR-basierten Methode zu vergleichen und zu validieren. Um die Leistung der entwickelten Methode zu bewerten, wurden die erhaltenen Ergebnisse der LSPR-basierten Methode mit den genannten konventionellen Tests verglichen, wobei Sensitivität, Spezifität, positiver Vorhersagewert und negativer Vorhersagewert basierend auf der gemeinsamen Formel wie folgt berechnet wurden:
$$\begin{ausgerichtet} {\text{Empfindlichkeit}} &=\frac{{{\text{Zahl}}\,{\text{of}}\,{\text{Wahr}}\,{\text {Positives}}}}{{{\text{Zahl}}\,{\text{of}}\,{\text{Wahr}}\,{\text{Positives}}\, + \,{\text {Zahl}}\,{\text{von}}\,{\text{Falsch}}\,{\text{Negative}}}} \\ {\text{Spezifität}} &=\frac{{{\ text{Zahl}}\,{\text{von}}\,{\text{Wahr}}\,{\text{Negativen}}}}{{{\text{Zahl}}\,{\text{of }}\,{\text{Wahr}}\,{\text{Negative}}\, + {\text{Zahl}}\,{\text{von}}\,{\text{Falsch}}\, {\text{Positives}}}} \\ {\text{PPV}} &=\frac{{{\text{Zahl}}\,{\text{of}}\,{\text{Wahr}}\ ,{\text{Positives}}}}{{{\text{Zahl}}\,{\text{of}}\,{\text{Wahr}}\,{\text{Positives}}\, + \ ,{\text{Zahl}}\,{\text{von}}\,{\text{Falsch}}\,{\text{Positives}}}} \\ {\text{NPV}} &=\frac {{{\text{Zahl}}\,{\text{von}}\,{\text{Wahr}}\,{\text{Negative}}}}{{{\text{Zahl}}\,{ \text{of}}\,{\text{Wahr}}\,{\text{Negatives}}\, + \,{\text{Zahl}}\,{\text{of}}\,{\text {False}}\,{\text{Negatives}}}} \\ \end{aligned}$$Statistische Analyse
Diese Studie wurde als klassisches diagnostisches Leistungsexperiment analysiert, indem die Übereinstimmung eines vorgeschlagenen Tests, des LSPR-Nanosensors, und eines Referenzstandardtests, der Kultur und einiger konventioneller Tests, einschließlich ELISA und SAT, bewertet wurde, um ihre Fähigkeit zur Identifizierung einer Zielerkrankung zu bestimmen . Cutoff-Werte wurden aus dem Durchschnitt der Kontrollseren (richtig negativ) plus zweifachen Standardabweichungswerten (2SD) berechnet. Zur Ermittlung der Normalität und Bewertung der Datenverteilung wurde der Kolmogorov-Smirnov-Test durchgeführt. Basierend auf den Normalitätsergebnissen, die die parametrische Verteilung zeigten, wurde der ANOVA-Test verwendet, um Gruppen zu vergleichen. Alle statistischen Analysen wurden mit GraphPad Prism für Windows Version 8 und SPSS für Windows Version 9 durchgeführt.
Ergebnisse
Lipopolysaccharid-Extraktionsanalyse
SDS-PAGE zeigte, dass die Ausbeute der LPS-Extraktion ungefähr 1 Prozent des verwendeten Bakterien-Feuchtgewichts betrug. Darüber hinaus betrug die Nukleinsäurekonzentration ≤ 0,2% der LPS-Konzentration. Wichtig ist, dass die Bradford-Methode das Fehlen jeglicher Proteinkontaminationen nachgewiesen hat.
Charakterisierung von Goldnanopartikeln
Die Größenverteilung der Nanopartikel bestimmt die Qualität eines Biosensors. Nanopartikel müssen nach den bisherigen Studien eine bestimmte Größe besitzen. In dieser Hinsicht führt die entsprechend kleine Größe der Nanopartikel zu einer geeigneten kolloidalen Stabilität, hohen Oberflächen-zu-Volumen-Verhältnissen und einer schnellen Bewegung für hohe Bindungsraten führt zu einer hohen Affinität, einer hohen Empfindlichkeit und einer hohen Selektivität in Wechselwirkung mit biologischen Zielen. Darüber hinaus müssen die Nanopartikel so groß wie möglich sein, um die Anwesenheit verschiedener Liganden auf der Partikeloberfläche zu ermöglichen und auch multivalente Wechselwirkungen zu erzielen [29,30,31]. Wie Gu et al. berichtet, ist die Vergleichbarkeit der Größe von Nanopartikeln mit der Größe biologischer Targets bei der Interaktion von Proteinen besonders wichtig [32]. Entsprechend der Größe der Anti-Brucella-Antikörper, die 2–5 nm beträgt [33], wurden in dieser Studie Goldnanopartikel mit einer durchschnittlichen Größe von 10 nm hergestellt und die Größenverteilung der Nanopartikel mit einem Zetasizer NanoZS90-Instrument bestimmt, das a . verwendet Laser mit einer Wellenlänge von 633-nm. Diese Technik profitiert von der Stokes-Einstein-Gleichung, die die durch Brownsche Bewegung verursachte Partikeldiffusion in eine Größenverteilung umwandeln kann. Gemäß Abb. 2 war das BSP gleichmäßig auf einer 10-nm-Skala verteilt. Zeta-Potentialwerte enthüllten Details über die Oberflächenladung und Stabilität der BSP. Die Partikel waren negativ geladen und ihr Zetapotential betrug ungefähr – 28 mV. Darüber hinaus zeigt Tabelle 1 die maximale Absorptionswellenlänge von GNPs. Visuelle und ultraviolette Wellenlängen wurden mit einem Spektrophotometer gemessen und die maximale Absorption betrug 530 nm. Wir haben die Turkevich-Methode verwendet, um Gold-Nanopartikel herzustellen. Die Vorteile dieser Methode sind die Herstellung von Gold-Nanopartikeln, einschließlich eines einfachen und kostengünstigen Herstellungsprozesses, der Möglichkeit, die Größe der Nanopartikel zu kontrollieren, und der richtigen kolloidalen Stabilität [34].
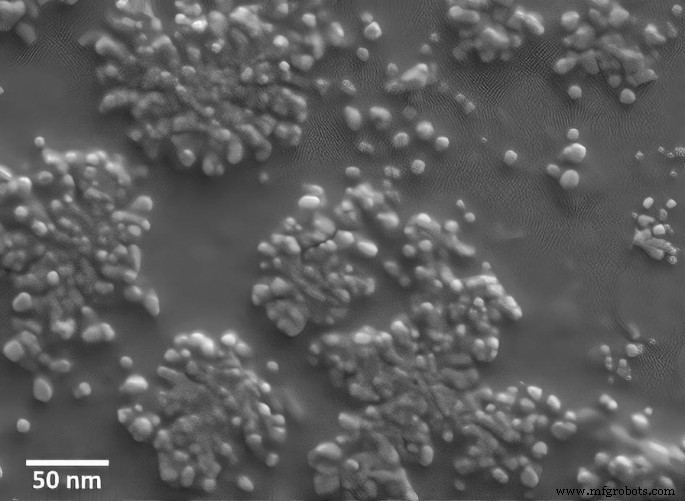
Struktur von Goldnanopartikeln unter REM. Die gleichmäßige Verteilung von Gold-Nanopartikeln spiegelt sich gut in der Abbildung wider.
Charakterisierung der Nano-Bio-Sonde
Wie oben erwähnt, wurden in dieser Studie TGA-Moleküle verwendet, um die Goldnanopartikel mit LPS zu verbinden, was zu einer leichten Abnahme des LSPR-Peaks bei 530 nm um 4,55 % führte. Außerdem wurden in der vorliegenden Studie mehrere Inkubationszeiten durchgeführt, um die maximale TGA-Adhäsion an den Goldnanopartikeln zu bestimmen. Gemäß den in Abb. 3 gezeigten Ergebnissen führte eine 24 Stunden lange TGA-Inkubation mit GNPs zur maximalen TGA-Beschichtung auf der Oberfläche der Goldnanopartikel.
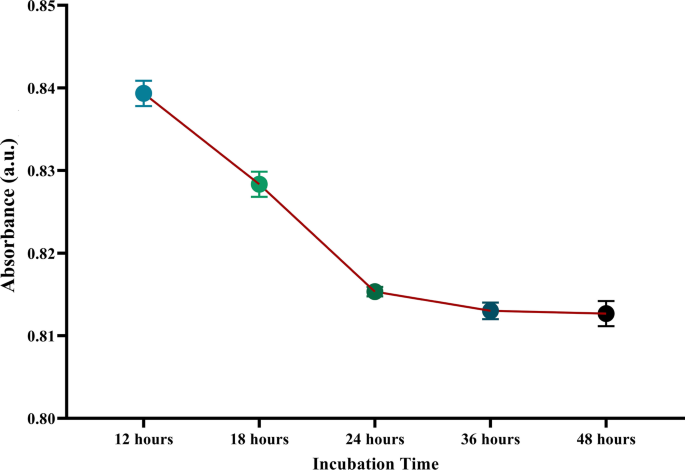
Optimierung der Beschichtung von Goldnanopartikeln mit Thioglykolsäure. Wie die Abbildung zeigt, gibt es trotz der Verlängerung der angrenzenden Zeit keine signifikante Änderung der Extinktion nach 24 h Inkubation. Daher wurden 24 h als optimierte Zeit für das Auftragen von Thioglykolsäure auf GNPs ausgewählt. Das Y -Achse zeigt die Absorptionsintensität bei 530 nm (maximale Absorption von Nanopartikeln). Die Versuche wurden in dreifacher Ausführung durchgeführt. Die Daten werden als Mittelwert ± SEM dargestellt. a.u.:Absorptionseinheit
Zur Bestimmung der optimierten Konzentration von LPS wurden in der vorliegenden Studie Konzentrationen von 100, 150, 200, 300 und 560 µg/ml untersucht. Wie in Abb. 4 gezeigt, nimmt die Extinktion mit zunehmender Konzentration ab. Den Ergebnissen zufolge wählte die vorliegende Studie eine LPS-Konzentration von 300 ug/ml, um die Oberfläche von TGA-modifizierten GNPs zu beschichten, da es keine merkliche Abnahme der Absorptionsspitzenintensität durch Erhöhung der LPS-Konzentration gab.
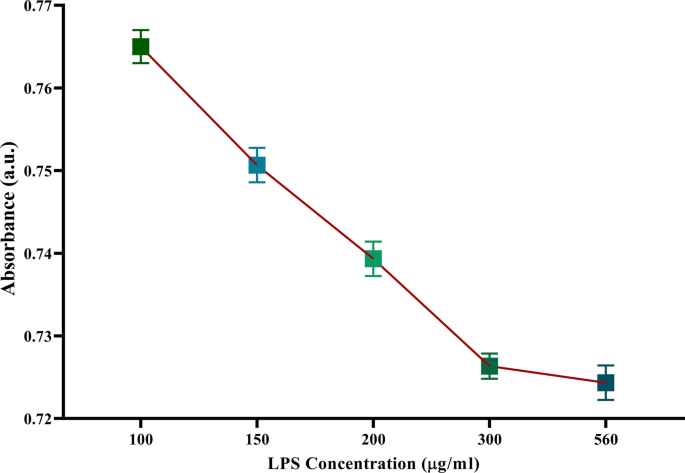
Optimierung der LPS-Konzentration. Mit steigender LPS-Konzentration nahm die Extinktion signifikant ab. Bei einer Erhöhung der LPS-Konzentration von mehr als 300 mg/ml gab es jedoch keine signifikante Verringerung der LSPR-Absorption. Daher wurde die genannte Konzentration als optimierte Konzentration gewählt. Das Y -Achse zeigt die Absorptionsintensität bei 530 nm (maximale Absorption von Nanopartikeln). Die Versuche wurden in dreifacher Ausführung durchgeführt. Die Daten werden als Mittelwert ± SEM dargestellt. a.u.:Absorptionseinheit
Bewertung der Nano-Bio-Probe-Funktionen
Da es sich bei der LSPR-Technik um eine oberflächensensitive optische Methode handelt, kann sie die Wechselwirkung zwischen Anti-LPS-Antikörpern und Antigenen in der Oberfläche der Goldnanopartikel durch das Bild von Veränderungen des LSPR-Absorptionspeaks erkennen, die durch elektrostatische Wechselwirkung zwischen Antikörper und Antigen. Um die korrekte Funktion des Biosensors zu bestätigen, wurde in dieser Studie eine Positivkontrolle hergestellt, die aus Anti-Brucella-LPS-Antikörpern mit einem Titer von 1:80 und einer Negativkontrolle bestand, und das LSPR-Spektrum des Biosensors nach Inkubation mit den Kontrollen aufgezeichnet. Wie in Abb. 5 gezeigt, beeinflusste die Inkubation mit negativer Kontrolle die Absorption von LSPR nicht. Die Inkubation mit positiver Kontrolle verursachte jedoch eine Verschiebung der maximalen LSPR-Extinktion, die früher als Rotverschiebung bekannt war. Daher begrenzt die Bindung von Anti-Brucella-Antikörpern an die LPS-Antigene das Auftreffen von Licht auf die Oberfläche von Nanosonden.
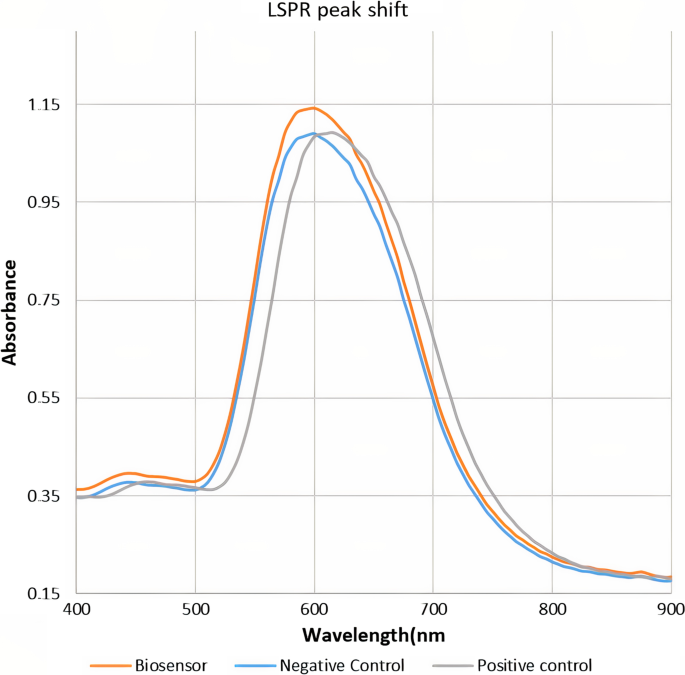
Peak der LSPR-Nanoprobe in Gegenwart von positiven und negativen Kontrollen. Kontrollen wurden aus kommerziell erhältlichen ELISA-Kits bereitgestellt
Bestimmung des Cutoff-Werts
Zu diesem Zweck erhielt diese Studie 40 Seren von richtig positiven und negativen Probanden basierend auf der Kultur und den klinischen Beobachtungen. Wie in Abb. 6 gezeigt, betrug der Rotverschiebungs-Durchschnitt in echt negativen Proben (Kontrollen) 1,70 nm, was sich signifikant von richtig positiven Patienten unterschied (P Wert < 0,001). Darüber hinaus zeigten die Ergebnisse, dass die Rotverschiebung von 4,38 nm als Cutoff-Wert verwendet werden sollte. Interessanterweise wiesen nur 5 % der Kontrollen eine Rotverschiebung über dem Cutoff-Wert auf, und die Rotverschiebung bei allen Patienten lag über dem Cutoff-Wert, was darauf hindeutet, dass die Leistung der Methode akzeptabel und die Bestimmung des Cutoff-Werts zuverlässig ist.
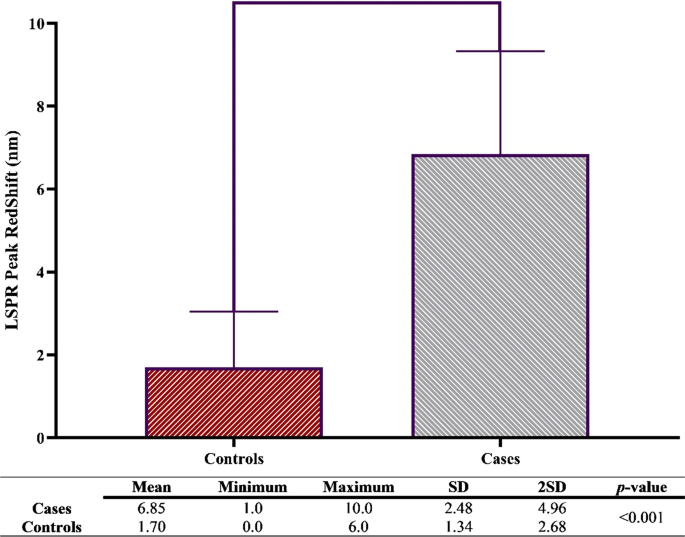
LSPR-Peak-Rotverschiebung in den Seren von echten Patienten und Kontrollpersonen. Bei der Interaktion zwischen Antikörpern, die in den Seren infizierter Individuen präsentiert wurden, fand eine Rotverschiebung statt, die sich im Vergleich zu Kontrollen signifikant unterschied. Darüber hinaus zeigt die Abbildung die für die Definition des Cutoff-Punktes wertvollen SD- und 2SD-Werte. Die Experimente wurden dreifach für jede Probe durchgeführt. P Wert < 0.05 wurde als signifikant angesehen
Validierung der Biosensor-Funktion
In den vorherigen Schritten führte diese Studie eine schnelle und kostengünstige Methode zur Identifizierung von Anti-Brucella-Antikörpern in den Proben ein. Es ist jedoch erforderlich, die Funktionalität einer neuen Methode zu überprüfen. Zu diesem Zweck führte diese Studie eine Reihe von Teilstudien durch, darunter Standard-Röhrchen-Agglutinationstests, Anti-IgG- und Anti-IgM-Spiegel in den Seren negativer und positiver Proben basierend auf den Kulturergebnissen. Wie in Tabelle 2 gezeigt, war die Sensitivität des aktuellen Verfahrens geringer als die von SAT allein. Wichtig ist, dass die Spezifität der LSPR-basierten Methode das akzeptableste Ergebnis zeigte, das 100 % betrug. Ähnlich wie bei der Spezifität war der positive prädiktive Wert der aktuellen Methode höher als bei anderen konventionellen Tests (100%). Letztendlich betrug der NPV von SAT-, IgG-, IgM- und LSPR-basierten Methoden 90 %, 90 %, 81 % bzw. 86 %.
Diskussion
Brucellose gilt wahrscheinlich als die erste Infektion des Menschen nach der Domestikation von Rindern, Schafen und Ziegen [35]. Brucellose ist die weltweit am weitesten verbreitete bakterielle Zoonose mit 500.000 neuen menschlichen Krankheitsfällen, die jedes Jahr weltweit diagnostiziert werden [9, 36]. Die Symptome der Brucellose beim Menschen sind nicht pathognomonisch, da die Infektion jedes Organ des Körpers betreffen kann [37]. Obwohl die Laborergebnisse immer noch ein zuverlässiger Faktor bei der Erkennung von Krankheiten sind, haben die aktuellen Strategien, einschließlich Kultur-, Serologie- und Nukleinsäureamplifikationstests, schwerwiegende Mängel gezeigt [9, 38, 39, 40]. Daher versucht diese Studie, eine neue diagnostische Methode basierend auf LSPR einzuführen, um die Einschränkungen zu beseitigen.
In den letzten Jahren wurde die lokalisierte Oberflächenplasmonenresonanz als Grundlage für die Entwicklung von Biosensoren verwendet. Die Vorteile der aktuellen Forschung zu Goldnanopartikeln und Fortschritte in der Nanotechnologie wurden als Hauptfaktoren zur Verbesserung der diagnostischen Leistung angesehen. Die einzigartigen Farb- und optischen Eigenschaften von GNPs aufgrund ihrer plasmonischen und einstellbaren Effekte sind zwei herausragende und vorteilhafte Eigenschaften dieser Partikel im Vergleich zu anderen Partikeln [12, 41].
In dieser Studie wurde eine Rotverschiebung des LSPR-Peaks als Indikator für die Interaktion zwischen LPS-Antigenen und Anti-Brucella-Antikörpern verwendet. Mit anderen Worten, im Vergleich zu den Kontrollproben verursachte die Anwesenheit von Antikörpern im Serum der Fallproben eine deutliche Rotverschiebung des LSPR-Absorptionspeaks, was als Indikator für Brucellose angenommen werden kann. Obwohl es einen signifikanten Unterschied in der Rotverschiebung zwischen Kontroll- und Fallproben gibt, kann dieser Unterschied die Konzentration von Antikörpern im Serum nicht quantifizieren, was als eine der gravierenden Einschränkungen dieser Methode angesehen werden kann. Wir müssen jedoch bedenken, dass einige gängige Methoden, wie zum Beispiel ELISA-bezogene Strategien, normalerweise als Grenzwert angesehen werden [42, 43].
Wichtig ist, dass diese Studie die Leistung der LSPR-basierten Technik validiert hat, indem die erhaltenen Ergebnisse mit anderen aktuellen Methoden durch die Bewertung verschiedener Parameter verglichen wurden. Der erste analysierte Parameter war die Sensitivität, die die Wahrscheinlichkeit eines positiven Brucellose-Tests bei einem Patienten bestimmt [44]. Wie Yagupsky et al. diskutiert [9], ist die Sensitivität der Blutkultur, die als aktueller Goldstandard gilt, insbesondere bei chronischen Erkrankungen und fokalen Infektionen herabgesetzt. In addition, this method also faced other serious limitations, such as laboratory safety problems, the slow-growth of bacteria, and a positive result is indisputable evidence of the disease [45, 46]. This LSPR-based technique represented a reliable and competitive result compared to the conventional methods in sensitivity such as culture, SAT, and ELISA-dependent kits. At the same time, specificity, that is the probability of a negative test if the patient is not infected, was evaluated [45, 47]. As results showed, compared to the other diagnostic strategy, the designed LSPR-based technique had the most significant outcome in terms of specificity. It is an important characteristic of this method because the previous studies had questioned the validity and specificity of serodiagnostic methods of human brucellosis since asymptomatic and self-limiting episodes of this infection occur in zoonosis endemicity areas [48,49,50]. However, like antibody-related methods, the current method resists the possible long-term persistence of anti-Brucella antibodies within the serum, even after complete recovery from brucellosis.
Similar to previous studies, positive predictive value was defined as the ratio of the true positive results to the sum of all positive results [51]. Similarly, the NPV was described as the ratio of the true negative results to the sum of all negative results [51]. Compared to conventional diagnostic strategies, the current designed method represented the most wonderful PPV outcomes, demonstrating its ability to distinguish between infected and non-infected individuals. In addition, the evaluation of the NPV results revealed the promising potential of the LSPR-based method to exclude non-patients from real patients.
Conclusion
This study introduced a rapid, simple, low cost, reliable, and economical method for diagnosing brucellosis. Although there are some minor limitations, including the qualitative outcomes and the possibility of being positive in recovered individuals, the advantages discussed show that it has good capabilities compared to the current laboratory-based diagnostic procedures.
Availability of data and materials
The datasets used and/or analyzed during the current study are available from the corresponding author on reasonable request.
Abbreviations
- LPS:
-
Lipopolysaccharides
- GNPs:
-
Gold nanoparticles
- DLS:
-
Dynamic light scattering
- LSPR:
-
Localized surface plasmon resonance
- SAT:
-
Standard tube agglutination test
- ELISA:
-
Enzyme-linked immunosorbent assay
- PPV:
-
Positive predictive value
- NPV:
-
Negative predictive value
- PSPR:
-
Propagating surface plasmon resonance
- SDS-PAGE:
-
Sodium dodecyl sulfate–polyacrylamide gel electrophoresis
- SEM:
-
Scanning electron microscopy
- TGA:
-
Thioglycolic acid
- NHS:
-
N-hydroxysuccinimide
- EDC:
-
N -(3-dimethylaminopropyl)-N ′-ethylcarbodiimide hydrochloride
- PBS:
-
Phosphate buffer saline
Nanomaterialien
- Synthese von elektrisch leitfähigem Siliziumdioxid-Nanofaser/Gold-Nanopartikel-Verbundmaterial durch Laserpulse und Sputtertechnik
- Lokalisierte Oberflächenplasmonenresonanz-Abhängigkeit von falsch ausgerichtetem abgeschnittenem Ag-Nanoprismen-Dimer
- Abstimmung der Oberflächenchemie von Polyetheretherketon durch Goldbeschichtung und Plasmabehandlung
- Auswirkung der Verteilung von Goldnanopartikeln in TiO2 auf die optischen und elektrischen Eigenschaften von farbstoffsensibilisierten Solarzellen
- Bildung und Lumineszenzeigenschaften von Al2O3:SiOC-Nanokompositen auf der Basis von durch Phenyltrimethoxysilan modifizierten Aluminiumoxid-Nanopartikeln
- Abstimmung der Oberflächenmorphologien und -eigenschaften von ZnO-Filmen durch das Design der Grenzflächenschicht
- Die Kopplungseffekte von Oberflächenplasmonpolaritonen und magnetischen Dipolresonanzen in Metamaterialien
- Polarisationsunempfindlicher Oberflächenplasmonen-Polarisations-Elektroabsorptionsmodulator auf Basis von Epsilon-nahezu Null Indiumzinnoxid
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Magnetischer Goldnanopartikel-markierter monoklonaler Heparanase-Antikörper und seine anschließende Anwendung für die Tumor-Magnetresonanztomographie



