Hydrothermal-unterstützte Sinterstrategie für poröses und hohlstrukturiertes LiNb3O8-Anodenmaterial
Zusammenfassung
Porös- und hohlstrukturiertes LiNb3 O8 Anodenmaterial wurde erstmals durch eine hydrothermal unterstützte Sinterstrategie hergestellt. Die Phasenentwicklung wurde untersucht und der Bildungsmechanismus der porösen und hohlen Struktur vorgeschlagen. Die Bildung der einzigartigen Struktur kann der lokalen Existenz einer flüssigen Phase aufgrund der Verflüchtigung des Li-Elements zugeschrieben werden. Als Anodenmaterial beträgt die anfängliche Entladekapazität 285,1 mAhg –1 bei 0,1 C, die größte bisher gemeldete Entladekapazität für LiNb3 O8 . Selbst nach 50 Zyklen kann die reversible Kapazität immer noch 77,6 mAhg −1 . aufrechterhalten bei 0,1 C etwa das 2,5-fache von LiNb3 O8 Proben, die mit traditionellen Festkörpermethoden hergestellt wurden. Die signifikante Verbesserung der Li-Speicherkapazität ist auf die spezielle poröse und hohle Struktur zurückzuführen, die eine hohe Dichte an aktiven Zentren und kurze parallele Kanäle für eine schnelle Interkalation von Li + . bietet Ionen durch die Oberfläche.
Hintergrund
In den letzten Jahren wurde hohlen und porösen Strukturen aufgrund ihrer weit verbreiteten Anwendungen in Katalyse, Energie, Umwelttechnik, Wirkstoffabgabe und Sensorsystemen große Aufmerksamkeit geschenkt [1,2,3,4]. Im Vergleich zu anderen neuen Energiebatterien haben sich Lithium-Ionen-Batterien (LIBs) als vorherrschende Stromquelle für tragbare Elektronik kommerziell durchgesetzt und zeigen aufgrund ihrer hohen Energiedichte, langen Lebensdauer und Umweltfreundlichkeit ein großes Potenzial für groß angelegte Anwendungen [5 ]. Um eine hohe elektrochemische Leistung zu erzielen, haben die Elektroden von LIBs immer offene Strukturen, die eine hohe Dichte an aktiven Zentren und parallele Kanäle für eine schnellere Interkalation von Li + . bieten können Ionen durch die Oberfläche [6]. Es ist jedoch eine Herausforderung, Nanomaterialien mit offenen Strukturen einschließlich poröser und hohler Architekturen zu synthetisieren.
Um die Leistung von LIBs zu verbessern, wurde nach Hochleistungselektrodenmaterialien gesucht, einschließlich Anoden- und Kathodenmaterialien. LiFePO4 [7], LiCoO2 [8], LiMn2 O4 [9], LiVPO4 F [10] und verschiedene Hybridmaterialien [11, 12] wurden ernsthaft als Kandidaten für Kathodenmaterialien in Betracht gezogen. Für Anodenmaterialien wurden viele verschiedene Materialien als Alternativen zu graphitbasierten Anodenmaterialien untersucht, wie Übergangsmetalloxide (TMOs) [13], Molybdändisulfid (MoS2 ) und Graphen-basierte Hybride [14]. In der neueren Literatur wurde gezeigt, dass Niob eine überlegene elektrochemische Leistung aufweist [15]; einige traditionelle Verbindungen, die mit Nb-Elementen dotiert sind, und neue Verbindungen auf Nb-Basis sind gut entwickelt [16,17,18,19]. Nb-basierte Oxide gelten als vielversprechende Anodenmaterialien für LIBs mit verbesserter Sicherheit. Im Vergleich zu Li4 Ti5 O12 (mit einer theoretischen Kapazität von 175 mAhg −1 ), Nb-basierte Oxide haben eine relativ hohe theoretische Kapazität von 389 mAhg −1 . Es ist auch bemerkenswert, dass die beiden Nb-Redoxpaare Nb 5+ /Nb 4+ und Nb 4+ /Nb 3+ , kann die Bildung von Festelektrolytgrenzflächen (SEI) während der Zyklen unterdrücken [19]. LiNb3 O8 , ein bekanntes Material, erscheinen immer im Herstellungsprozess von LiNbO3 als Verunreinigungsphase aufgrund von Li-Verflüchtigung [20]. Jianet al. zuerst eingeführt LiNb3 O8 Material, das durch eine Festkörperreaktion als Anode für LIBs hergestellt wurde. Es zeigt sich, dass das so hergestellte LiNb3 O8 Probe kugelgemahlen mit Acetylenruß (LiNb3 O8 -BM) die anfänglichen Entlade-/Ladekapazitäten erheblich verbessert (351 und 212 mAhg −1 .) ) als die des vorbereiteten LiNb3 O8 Probe (250 und 170 mAhg −1 ) bei 0,05 °C; nach 50 Zyklen erreichte die Kapazität 150 mAhg −1 für LiNb3 O8 -BM bei 0,1 C, nur 30 mAhg −1 für LiNb3 O8 Probe [18]. Poröses LiNb3 O8 Nanofasern zeigten aufgrund der großen Oberfläche, der kleinen Nanokristalle und der porösen Struktur mit einer anfänglichen Entladungskapazität von 241,1 mAhg −1 . auch eine verbesserte Kapazität und Zyklizität bei 0,1 °C [19]. Aufgrund der Schwierigkeit, eine reine Phase zu erhalten, ist LiNb3 . als neuartiges Anodenmaterial mit hoher theoretischer Kapazität O8 wurde selten untersucht.
In diesem Artikel wird porös- und hohlstrukturiertes LiNb3 O8 Anodenmaterial wurde erfolgreich durch einen hydrothermal unterstützten Sinterprozess hergestellt. Die Phasenentwicklung wurde untersucht und der Bildungsmechanismus der porösen und hohlen Struktur vorgeschlagen. Die morphologischen und elektrochemischen Eigenschaften von LiNb3 O8 als Anodenmaterial wurden ebenfalls eingehend untersucht.
Methoden
Vorbereitung von Proben
LiNb3 O8 Pulver wurden durch das hydrothermal unterstützte Sinterverfahren hergestellt. Lithiumhydroxid-Monohydrat (LiOH·H2 O, Aladdin, ACS, ≥98,0 % und Niobpentoxid (Nb2 .) O5 , Aladdin, AR, 99,9%) wurden ohne weitere Reinigung als Rohstoffe bezogen. Zuerst 3,5 mmol Nb2 O5 wurde in 35 ml LiOH·H2 . dispergiert O transparente wässrige Lösung (Molverhältnis von Li:Nb = 8:1) mit Magnetrührer für 1 h. Dann wurde die Suspensionslösung in einen 50 ml Teflon-ausgekleideten Hydrothermalsynthese-Autoklavenreaktor gegeben. Danach wurde der Reaktor verschlossen und 24 h bei 260 °C gehalten und dann auf natürliche Weise auf Raumtemperatur abgekühlt. Schließlich wurden die so hergestellten Produkte zentrifugiert und mit entionisiertem Wasser und Ethanol gespült. Nach dem Trocknen in einem Ofen bei 60 °C für 12 h wurden die weißen Li-Nb-O-Pulver gesammelt und bei verschiedenen Temperaturen von 500 bis 800 °C für 2 h mit einer Anstiegsrate von 5 °C/min kalziniert.
Charakterisierung
Die thermische Zersetzungscharakteristik von Li-Nb-O-Pulver wurde mit einem thermogravimetrischen und Differentialscanningkalorimeter (TG/DSC, Netzsch STA 409 PC/PG) von Raumtemperatur auf 1200 °C mit einer Anstiegsrate von 10 °C/min unter . untersucht N2 Atmosphäre. Die Kristallstrukturen der kalzinierten Pulver wurden mittels Röntgenpulverdiffraktometrie (XRD; Bruker D8 Discover) mit Cu Kα . analysiert Strahlung. Die Morphologien der kalzinierten Pulver wurden durch Rasterelektronenmikroskopie (REM; JSM-6700F) charakterisiert. Die Analyse mit Röntgenphotoelektronenspektroskopie (XPS) wurde auf einem Thermo-Fisher Escalab 250Xi-Instrument durchgeführt.
Elektrochemische Messungen
Die LiNb3 O8 Elektroden wurden durch Auftragen einer Aufschlämmung von LiNb3 . hergestellt O8 Pulver, Ruß und Polyvinylidenfluorid (PVDF) mit einem Gewichtsverhältnis von 8:1:1 auf eine Aluminiumfolie. Anschließend wurde die Elektrode über Nacht bei 120 °C in einem Vakuumofen getrocknet. Die Anoden wurden in Scheiben mit einem Durchmesser von 16 mm gestanzt. Für die elektrochemischen Messungen wurden CR2025-Knopfzellen in einem mit Argon gefüllten Handschuhfach unter Verwendung von Lithiumfolie als Gegenelektrode und einer mikroporösen Polypropylenmembran (Celgard 2320) als Separator zur Isolierung der beiden Elektroden zusammengebaut, und dann die 1,0-M- LiPF6 Elektrolyt wurde in einer Mischung aus Ethylencarbonat und Dimethylcarbonat (1:1, bezogen auf das Volumen) gelöst. Galvanostatische Ladungs-Entladungs-Tests der Zellen wurden unter Verwendung eines elektrischen Testsystems von Land (Wuhan Land Electronics Co., Ltd., China) zwischen 0 und 3 V (gegen Li/Li + .) durchgeführt ) bei unterschiedlichen Stromdichten von 0,1–1 C (1 C = 389 mAhg −1 .) ). Zyklische Voltammetrie (CV)-Kurven wurden auf einer elektrochemischen Workstation (CHI604E, Shanghai Chenhua Instruments Co., Ltd., China) im Spannungsbereich von 1–3 V aufgezeichnet.
Ergebnisse und Diskussion
Abbildung 1 zeigt die TG/DSC-Kurven des Pulvers, das nach der hydrothermalen Reaktion ohne weitere Kalzinierung erhalten wurde. Der Gewichtsverlust des Pulvers ist sehr gering, etwa 5 %, selbst wenn die Temperatur 1100 °C erreicht, aber der Verlust tritt während des gesamten Kalzinierungsprozesses auf. Dies ist auf die Verdampfung des Li-Elements aufgrund seiner niedrigen Schmelztemperatur zurückzuführen, was durch die DSC-Ergebnisse mit endothermem Reaktionsprozess während des gesamten Kalzinierungsprozesses bestätigt wird. Bei 330 °C tritt ein endothermer Peak auf, der auf die Bildung von LiNbO3 . zurückzuführen sein kann . Bei 580 °C tritt eine exotherme Reaktion auf, die aus der Reaktion zwischen LiNbO3 . resultiert und Nb2 O5 um LiNb3 zu bilden O8 . Wie aus der DSC-Kurve hervorgeht, wird die exotherme Reaktion jenseits von 1100 °C aufgrund der Zersetzung von LiNb3 . stark O8 .
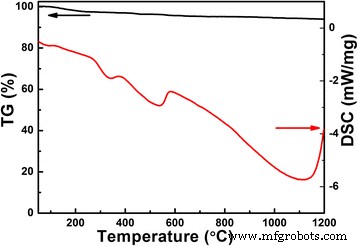
TG/DSC-Kurven des Li-Nb-O-Pulvers von Raumtemperatur bis 1200 °C bei einer Heizrate von 10 °C/min in N2
Die XRD-Muster von Li-Nb-O-Pulvern, die bei verschiedenen Temperaturen kalziniert wurden, sind in Abb. 2 gezeigt. Es ist ersichtlich, dass die Hauptphasen LiNbO3 . sind und Nb2 O5 bei 500 °C. Mit steigender Kalzinierungstemperatur erscheint der Beugungspeak bei 30,26°, der als (410)-Ebene des monoklinen LiNb3 . indiziert werden kann O8 . Die Reaktion kann durch Gl. (1) nicht Gl. (2) [21]:
$$ {\mathrm{LiNb}\mathrm{O}}_3+{Nb}_2{\mathrm{O}}_5\to {\mathrm{LiNb}}_3{\mathrm{O}}_8 $$ (1) $$ {\mathrm{LiNb}\mathrm{O}}_3\to {\mathrm{LiNb}}_3{\mathrm{O}}_8+{Li}_2\mathrm{O}\uparrow $$ (2)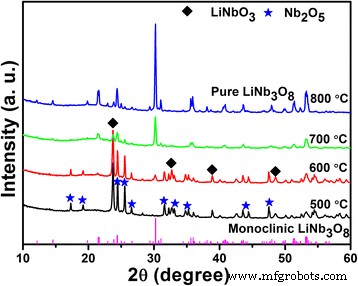
XRD-Muster des Li-Nb-O-Pulvers, das 2 h lang bei verschiedenen Temperaturen kalziniert wurde
Bei 700 °C ist das monokline LiNb3 O8 ist die vorherrschende Phase mit fast vernachlässigbarer Verunreinigung. Die reine Phase von LiNb3 O8 wird bei 800 °C erhalten, wobei alle Beugungspeaks auf die monokline Phase (JCPDS-Karte Nr. 36–0307), eine Raumgruppe von P21/a, indiziert sind. Verglichen mit der traditionellen Festkörpermethode ist die reine Phase von LiNb3 O8 wird leichter mit dem hydrothermal unterstützten Sinterverfahren erhalten.
Die REM-Bilder von LiNb3 O8 Bei 800 °C kalziniertes Pulver mit unterschiedlichen Vergrößerungen sind in Abb. 3 dargestellt. Die poröse und hohle Struktur, die einer Wabe ähnelt, wird von LiNb3 . gebildet O8 Nanopartikel mit einer Länge von mehreren Mikrometern. Die Struktur ist nicht flach, mit deutlicher Krümmung und bildet sogar geschlossene tubbyartige Strukturen. Sie unterscheidet sich vollständig von der Partikelaggregation, die aus herkömmlichen Festkörperreaktionen resultiert. Die Größe der LiNb3 O8 Partikel etwa 200 nm groß ist, wie in Abb. 3c gezeigt. Die kleine Partikelgröße und die einzigartige Struktur sind für die Ioneninterkalation von Vorteil [6]. Die Bildung der einzigartigen Struktur kann der Lithiumverflüchtigung während des Kalzinierungsprozesses zugeschrieben werden, wie durch TG-DSC-Ergebnisse bewiesen. Als leichte Verflüchtigung des Li-Elements wandert das überschüssige Li-Element, das im Pulver vorhanden ist, leicht an die Oberfläche der Partikel und geht in eine flüssige Phase über. Die lokale Existenz einer flüssigen Phase fördert die Bildung von neuem LiNb3 O8 Partikel an der Stelle und fördert auch die Bildung von Netzwerken zwischen den Partikeln.

a –c REM-Bilder von LiNb3 O8 Pulver mit verschiedenen Vergrößerungen
Um die elementare Zusammensetzung und den elektronischen Zustand weiter zu bestätigen, wurde das porös- und hohlstrukturierte LiNb3 O8 Pulver werden durch XPS analysiert, wie in Abb. 4 gezeigt. Die XPS-Daten wurden unter Verwendung von C 1s als Referenz mit einer Bindungsenergie von 284,6 eV kalibriert. In Abb. 4a entsprechen zwei Peaks bei 207,1 und 209,8 eV Nb 3d5/2 und 3d3/2 , entsprechend Nb 5+ Zustand in LiNb3 O8 [22]. Die XPS-Spektren von O 1s in Abb. 4b können in zwei Peaks bei 530.3 und 532 eV entfaltet werden. Ersteres wird den Nb-O-Bindungen zugeordnet, und letzteres ist mit Nichtgitter-Sauerstoff verwandt [22, 23].
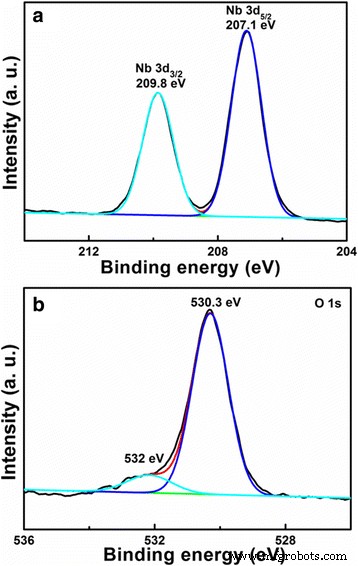
XPS-Spektren von (a ) Nb 3d und (b ) O 1s für das porös- und hohlstrukturierte LiNb3O8
Untersuchung der elektrochemischen Leistung von LiNb3 . wie hergestellt O8 Probe wurden die Tests der CV- und galvanostatischen Entladungs-Ladungs-Zyklen durchgeführt. Die ersten drei CV-Kurven von LiNb3 O8 Pulver mit einer Abtastrate von 0,1 mV/s im Bereich von 3~1 V sind in Fig. 5 gezeigt. Im ersten Zyklus werden zwei ausgeprägte Peaks (Li-Insertion) bei 1,13 und 1,30 V beobachtet; ersteres ist auf die partielle Reduktion von Nb 4+ . zurückzuführen bis Nb 3+ , während letztere mit der vollständigen Valenzvariation von Nb 5+ . in Verbindung gebracht werden kann bis Nb 4+ [18, 19]. Wie in Fig. 5 zu sehen ist, unterscheiden sich die nachfolgenden Zyklen stark vom ersten Zyklus. Das Verschwinden der Peaks bei 1,13 und 1,30 V impliziert, dass der Phasenübergang im ersten Zyklus irreversibel ist. Nur die Oxidationspeaks (Li-Extraktion) bei 1,71 und 1,96 V bleiben beim Zyklen stabil, was auf die Strukturänderung des LiNb3 . hindeutet O8 Probe in nachfolgenden Zyklen ist reversibel.
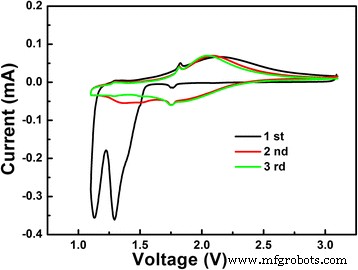
Die ersten drei CV-Kurven des LiNb3 O8 Pulver mit einer Scanrate von 0,05 mV/s zwischen den Spannungsbereichen von 3–1 V
Abbildung 6 zeigt die Entladungs-Ladungs-Kurven des LiNb3 O8 Pulver bei 0,1 C (hier 1 C = 389 mAhg −1 ) zwischen 3 und 1 V im ersten, zweiten, zehnten, dreißigsten und fünfzigsten Zyklus. In der ersten Entladungskurve sind zwei offensichtliche Potenzialplateaus bei ungefähr 1,13 und 1,30 V zu beobachten, was in guter Übereinstimmung mit den CV-Ergebnissen ist, dass zwei Phasenreaktionen, Nb 4+ → Nb 3+ und Nb 5+ → Nb 4+ , stattfinden. In den folgenden Zyklen werden jedoch die Plateaus des ersten Zyklus durch schräge Kurven ersetzt, was unterschiedliche Reaktionen zwischen dem ersten und den folgenden Zyklen impliziert. Gleichzeitig ist die anfängliche Entladekapazität des LiNb3 O8 Probe ist 285,1 mAhg −1 bei 0,1 C, die größte bisher gemeldete Entladekapazität für LiNb3 O8 Anodenmaterialien [18, 19]. 4.4 Li pro Einheitsformel kann in das LiNb3 . eingefügt werden O8 Material, das einer Zusammensetzung von Li5,4 . entspricht Nb3 O8 . Die Ladekapazität im ersten Zyklus beträgt jedoch 106,4 mAhg −1 , was darauf hinweist, dass nur 1,6 Li reversibel extrahiert werden können. Der große Verlust von 2,8 Li ist derzeit nicht eindeutig.
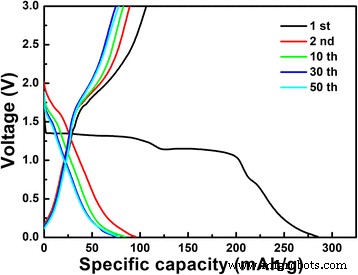
Galvanostatische Lade-Entlade-Profile des LiNb3 O8 Pulver bei 0,1 C zwischen 3 und 1 V
Abbildung 7 zeigt die Zyklenleistung von LiNb3 O8 Proben mit unterschiedlichen Stromraten bis zu 50 Zyklen. Die anfänglichen Entladekapazitäten von LiNb3 O8 Pulver mit Raten von 0,1, 0,5 und 1 C sind 285,1, 250 und 228 mAhg −1 , bzw. Bei einer aktuellen Rate von 0,1 C kann die reversible Kapazität immer noch 77,6 mAhg −1 . aufrechterhalten , etwa das 2,5-fache von LiNb3 O8 Proben, die mit der traditionellen Festkörpermethode hergestellt wurden (ca. 30 mAhg −1 bei 0,1 C, Ref.-Nr. [18]). Die deutliche Verbesserung der Li-Speicherkapazität ist auf die spezielle poröse und hohle Struktur von LiNb3 . zurückzuführen O8 Probe, die eine hohe Dichte an aktiven Zentren und kurze parallele Kanäle für eine schnellere Interkalation von Li + . bietet Ionen durch die Oberfläche [6]. Wenn die Raten auf 0,5 und 1 C steigen, bleiben die Entladekapazitäten nach 50 Zyklen 39,7 und 29,4 mAhg −1 , bzw. Es wird erwartet, dass die Kapazitätsstabilität durch geeignete Oberflächenmodifikation auf LiNb3 . verbessert werden kann O8 Material.
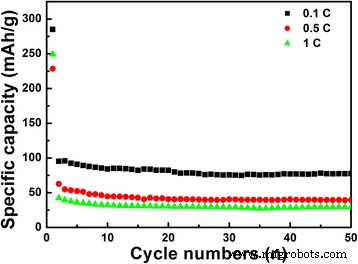
Fahrleistung des LiNb3 O8 Pulver mit verschiedenen Stromstärken von 0,1 C, 0,5 C und 1 C
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass poröses und hohl strukturiertes LiNb3 O8 Anodenmaterial wurde erfolgreich durch die hydrothermal-unterstützte Sinterstrategie hergestellt. Die Phasenentwicklung wurde untersucht und der Bildungsmechanismus der porösen und hohlen Struktur vorgeschlagen. Die Bildung der einzigartigen Struktur kann der lokalen Existenz einer flüssigen Phase aufgrund der Li-Verflüchtigung zugeschrieben werden. Als Anodenmaterial beträgt die anfängliche Entladekapazität 285,1 mAhg –1 bei 0,1 C, die größte bisher gemeldete Entladekapazität für LiNb3 O8 . Nach 50 Zyklen kann die reversible Kapazität immer noch 77,6 mAhg −1 . aufrechterhalten , etwa das 2,5-fache von LiNb3 O8 Proben, die mit traditionellen Festkörpermethoden hergestellt wurden. Die deutliche Verbesserung der Li-Speicherkapazität ist auf die spezielle poröse und hohle Struktur von LiNb3 . zurückzuführen O8 Pulver, das eine hohe Dichte an aktiven Zentren und kurze parallele Kanäle für eine schnelle Interkalation von Li + . bietet Ionen durch die Oberfläche.
Nanomaterialien
- Feuerfestes Metallpulver und der Sinterprozess davon
- Ein Leitfaden zum Aufbau und zur Messung einer schlanken Wartungsstrategie
- Eine fehlerhafte Wartungsstrategie beheben:PM-Optimierung und FMEA
- TOTAL entwickelt Wartungs- und Inspektionsstrategie
- Materialinnovationsschlüssel für 7nm und darüber hinaus
- Fortschritte der Strategie für die digitale Transformation bei Öl und Gas
- Nano- und Batterieanode:Ein Rückblick
- Die Auswirkungen des Li/Nb-Verhältnisses auf die Herstellung und photokatalytische Leistung von Li-Nb-O-Verbindungen
- MoS2/Acetylene Black Composite mit wenigen Schichten als effizientes Anodenmaterial für Lithium-Ionen-Batterien
- Herstellung und photokatalytische Leistung von Hohlstruktur-LiNb3O8-Photokatalysatoren



