Herstellung hierarchischer ZnO@NiO-Kern-Schale-Heterostrukturen für verbesserte photokatalytische Leistung
Zusammenfassung
ZnO@NiO-Kern-Schale-Heterostrukturen mit hoher photokatalytischer Effizienz und Wiederverwendbarkeit wurden durch elektrochemische Abscheidung auf Kohlenstofffasergewebe-Substraten hergestellt. Ihre photokatalytischen Eigenschaften wurden durch Messung des Abbaus von Rhodamin B und Methylorange (MO) unter Bestrahlung mit ultraviolettem Licht untersucht. Die Photoabbaueffizienz der ZnO@NiO-Heterostrukturen gegenüber beiden Farbstoffen war besser als die der reinen ZnO-Nanostäbchen und NiO-Nanoblätter. Die höhere Leistung könnte der Bildung eines p-n-Heteroübergangs zwischen ZnO und NiO zugeschrieben werden. Insbesondere die ZnO@NiO-Heterostruktur, die nach der Abscheidung von NiO für 10 Minuten gebildet wurde, baute 95 % des MO unter Bestrahlung mit ultraviolettem Licht für 180 Minuten ab. Die hohe Photoabbaueffizienz der ZnO@NiO-Heterostrukturen wurde auch der hohen Trenneffizienz photogenerierter Ladungsträger zugeschrieben, was durch den höheren Photostrom der ZnO@NiO-Heterostrukturen (achtfach) im Vergleich zu dem der reinen ZnO-Nanostäbe bestätigt wurde. Darüber hinaus wurde die hohe Photoabbaueffizienz der ZnO@NiO-Heterostrukturen über drei aufeinanderfolgende Abbauexperimente aufrechterhalten und ging nach dem dritten Zyklus auf 90 % zurück.
Hintergrund
In den letzten Jahrzehnten hat die Halbleiterphotokatalyse als eine Art „grüne Technologie“ aufgrund ihrer Anwendungsmöglichkeiten im Umweltschutz und in der Energieerzeugung viel Aufmerksamkeit auf sich gezogen [1,2,3]. Typische untersuchte Halbleiter sind TiO2 [4], ZnO [5,6,7], Cu2 O [8, 9], CdS [10, 11] und C3 N4 [12]. Unter diesen wurde ZnO aufgrund seiner hohen Elektronenbeweglichkeit, seiner vielfältigen Morphologien, seiner einfachen Herstellung, seiner geringen Kosten und seiner nicht toxischen Natur am meisten systemisch untersucht [13, 14]. ZnO mit direkter großer Bandlücke (3,37 eV) weist aufgrund der nativen Defekte, einschließlich Zink-Interstitials und Sauerstoff-Leerstellen, normalerweise eine n-Leitfähigkeit auf. ZnO als Photokatalysator weist jedoch mehrere Beschränkungen auf:(1) seine große Bandlücke begünstigt die Verwendung von ultraviolettem Licht hauptsächlich für das Auftreten von Photoabbau; (2) eine schnelle interne Rekombination photogenerierter Elektron-Loch-Paare führt zu einer geringen Photoabbaueffizienz [15, 16]; (3) das Auftreten einer starken Photokorrosion während des photokatalytischen Prozesses behindert einen wirksamen Abbau organischer Schadstoffe. Daher bleibt die Entwicklung einer Hochleistungs-Photokatalyse auf Basis von ZnO eine Herausforderung.
Viele Forschungsgruppen haben sich mit der Verbesserung der Trenneffizienz photogenerierter Ladungsträger und der Erweiterung des spektralen Ansprechbereichs beschäftigt, beispielsweise durch Dotieren [17], Beladen von Edelmetallen [5, 18, 19, 20] und Kombination mit anderen Halbleitern [21, 22,23,24,25,26,27,28,29,30,31]. Als potenzieller Kandidat hat Nickeloxid, ein Halbleitermaterial vom p-Typ (Eg = 3.5 eV) mit einer Steinsalz- oder kubischen Struktur, aufgrund seiner elektronischen Struktur, seiner hohen Lochbeweglichkeit und seiner geringen Gitterfehlanpassung mit ZnO großes Interesse auf sich gezogen. Somit kann es verwendet werden, um einen p-n-Heteroübergang mit ZnO herzustellen. Darüber hinaus kann der ZnO@NiO-Heteroübergang eine Typ-II-Bandstruktur bilden. Das Leitungsband (CB) von ZnO liegt zwischen dem Valenzband (VB) und dem CB-Band von NiO; eine solche Konfiguration kann die Rekombination photogenerierter Elektron-Loch-Paare behindern, was möglicherweise zu einer verbesserten photokatalytischen Effizienz führt. Zhanget al. [32] berichteten über die Synthese von p-Typ-NiO/n-ZnO-Nanofasern mit Heteroübergang mithilfe eines Sol-Gel-Prozesses und einer Elektrospinntechnologie und deren Verwendung als Photokatalysatoren. Letztere zeigten höhere katalytische Aktivitäten als reine NiO- und ZnO-Nanofasern. Luo et al. [33] berichteten, dass ZnO-Nanonadeln, die direkt aus einem porösen Ni-Schaum oder einer NiO-Oberfläche gewachsen waren, eine 2,5-fach höhere photokatalytische Leistung aufwiesen als reines ZnO. Leiet al. stellten hierarchische poröse ZnO/NiO-Mikrohohlkugeln her, die eine überlegene Adsorptionskapazität für den Kongo aufweisen [34]. Trotz der verbesserten photokatalytischen Effizienz, die berichtet wurde, weist die Verwendung aktueller ZnO@NiO-Heterostrukturen als Photokatalysatoren immer noch Nachteile auf, wie den komplexen Syntheseprozess, die Schwierigkeiten bei der Abtrennung des Photokatalysators vom Reaktionsmedium und die anschließende Wiederverwendung der Photokatalysatoren. Insbesondere die Abtrennung der Photokatalysatoren aus der Lösung nach der Reaktion ist eine Herausforderung in praktischen photokatalytischen Prozessen.
In der vorliegenden Arbeit wird ein Kohlefasergewebe als Substrat gewählt, um ZnO@NiO-Heterostrukturen durch elektrochemische Abscheidung zu synthetisieren. Eine solche Konfiguration ermöglicht eine leichte Abtrennung des Photokatalysators von der Lösung und eine Wiederverwendung des Photokatalysators. Die Photostromantwort der hierarchischen ZnO@NiO-Kern-Schale-Heterostrukturen wird ebenfalls diskutiert.
Methoden
Materialvorbereitung
ZnO-Nanostäbe wurden über ein elektrochemisches Abscheidungsverfahren auf einem Kohlefasergewebe gezüchtet. Vor der Verwendung wurde das Kohlefasertuch durch sequentielle Beschallung in Aceton, Ethanol und entionisiertem Wasser gereinigt. Eine gemischte wässrige Lösung (Elektrolyt) von 5 mM Zinknitrat-Hexahydrat (Zn(NO3 )2 ·6H2 O) und 5 mM Hexamethylentetramin, Kohlefasergewebe, eine 2 cm × 2 cm große Platinplatte und Ag/AgCl in einer gesättigten KCl-Lösung wurden als Arbeits-, Gegen- bzw. Referenzelektroden verwendet. Die Elektrolysezelle wurde in ein Wasserbad gestellt, um eine konstante Temperatur von 90 °C aufrechtzuerhalten. Die Reaktion wurde 30 min bei einem konstanten Potenzial von – 0,9 V gegen die Referenzelektrode durchgeführt. Nach der Reaktion wurden die Proben mehrmals mit entionisiertem Wasser gewaschen und in einem Ofen bei 60 °C 24 h lang getrocknet.
Eine Schicht aus NiO-Nanoblättern wurde durch elektrochemische Abscheidung auf einem Kohlefasergewebe abgeschieden, und 0,01 Mol Nickelnitrat-Hexahydrat (Ni(NO3 )2 ·6H2 O) wurde in 500 ml entionisiertem Wasser gelöst. Die Reaktion wurde bei einem konstanten Potential von – 1 V gegenüber der Referenzelektrode für 10 Minuten durchgeführt. Nach der Reaktion wurden die Proben aus der Lösung genommen und mehrmals mit entionisiertem Wasser gewaschen, gefolgt von einem Tempern bei 400 °C in einem Ofen für 2 Stunden an der Luft.
Zur Herstellung der ZnO@NiO-Heterostrukturen wurde auf den ZnO-Nanostäben durch elektrochemische Abscheidung eine NiO-Schicht abgeschieden. Die Abscheidungszeit wurde von 5 bis 10 und 15 Minuten variiert. Die resultierenden Proben werden jeweils als ZN1, ZN2 und ZN3 bezeichnet. Der Herstellungsprozess der ZnO@NiO-Heterostrukturen ist in Abb. 1 dargestellt. Es wurde derselbe Prozess verwendet, der für die Abscheidung einer NiO-Schicht auf einem Kohlenstoffgewebesubstrat verwendet wurde.

Herstellungsprozess hierarchischer ZnO@NiO-Heterostrukturen
Materialcharakterisierung
Die Morphologien und Strukturen der ZnO-Nanostäbe, NiO-Nanoblätter und ZnO@NiO-Heterostrukturen wurden durch Feldemissions-Rasterelektronenmikroskopie (FESEM; NoVaTM Nano SEM 250, FEI), Röntgenbeugung (XRD; Bruker D8 Advance) und Transmission charakterisiert Elektronenmikroskopie (TEM; Tecnai G2 F20, FEI). Die chemische Oberflächenzusammensetzung und die Zustände von ZN2 wurden mit einem Röntgen-Photoelektronenspektrometer (Thermo ESCALAB 250XI) mit einer monochromatischen Al Kα-Quelle (1486,6 eV) bestimmt. Photolumineszenz (PL)-Messungen wurden mit einem JY-630 Mikro-Raman-Spektrometer unter Verwendung der 325-nm-Linie eines He-Cd-Lasers als Anregungsquelle durchgeführt.
Photokatalytische Aktivität
Die photokatalytische Aktivität der Proben (ZnO, NiO und ZnO@NiO) wurde durch Untersuchung des Photoabbaus von Rhodamin B (RhB) und Methylorange (MO) untersucht. Der photokatalytische Aufbau (XPA Serie-7, Nanjing) wurde mit einer 500W Quecksilberlampe als Lichtquelle ausgestattet. Typischerweise wurde die auf dem Kohlefasergewebesubstrat gewachsene Photokatalysatorprobe (2 cm × 1,5 cm) in ein Quarzröhrchen gegeben, das mit 20 ml wässriger RhB- oder MO-Lösung (5 mg/l) gefüllt war. Die Lösung wurde zunächst 60 Minuten im Dunkeln gehalten, um ein Adsorptions-Desorptions-Gleichgewicht zwischen dem Photokatalysator und dem Farbstoff zu gewährleisten. Danach wurde die Bestrahlung mit UV-Licht eingeleitet. In bestimmten Beleuchtungsintervallen wurde die Konzentration des Farbstoffs durch Messung der Absorption der Farbstofflösung bei 464 nm (für MO) und 554 nm (für RhB) auf einem UV-Vis-Spektrophotometer (TU-1900/1901, Peking) bestimmt. . Die Experimente wurden bei Raumtemperatur durchgeführt.
Charakterisierung der Photostrom-Antwort
Alle elektrochemischen Messungen wurden unter Verwendung eines typischen Drei-Elektroden-Systems durchgeführt. A 0,5 M Na2 SO4 Als Elektrolyt wurde eine wässrige Lösung (mit einem auf ~~7,0 gepufferten pH-Wert) verwendet. Als Lichtquelle für den Photostromtest wurde eine 10 W UV-Lampe verwendet.
Ergebnisse und Diskussion
Die XRD-Muster der ZnO-Nanostäbchen, NiO-Nanoblätter und ZnO@NiO-Nanokomposite, die auf einem Kohlefasergewebe aufgewachsen sind, sind in Abb. 2 gezeigt. Die breiten Beugungspeaks bei 25,7 ° und 43,7 ° konnten dem Kohlenstoffgewebe zugeschrieben werden. Die beobachteten Beugungspeaks der ZnO-Nanostäbchen konnten den Kristallebenen (100), (002), (101), (102), (110), (103) und (112) von hexagonalem Wurtzit ZnO zugeordnet werden. Die bei 37.0° und 42.9° beobachteten Beugungspeaks im XRD-Muster von NiO-Nanoblättern konnten den Kristallebenen (111) und (200) von kubischem NiO zugeordnet werden. Die XRD-Muster der ZN1-, ZN2- und ZN3-Heterostrukturen zeigten Beugungspeaks der hexagonalen Struktur von ZnO und der kubischen Struktur von NiO. Darüber hinaus verstärkten sich die Beugungspeaks von NiO allmählich, wenn die Abscheidungszeit für die Herstellung der zusammengesetzten Heterostrukturen von 5 auf 15 Minuten zunahm. Darüber hinaus wurden keine anderen charakteristischen Peaks beobachtet, und es wurde keine Kristallphasenumwandlung von ZnO nach der NiO-Abscheidung beobachtet, was die hohe Reinheit der hergestellten Verbundstoffe bestätigt.
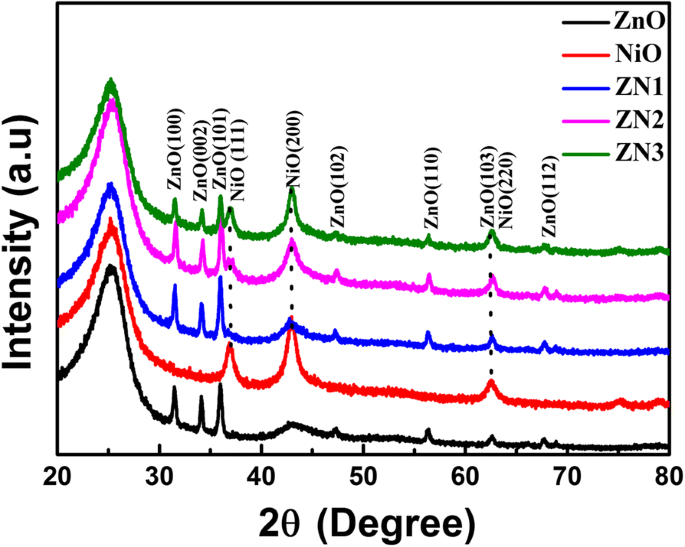
XRD-Muster von ZnO-, NiO- und ZnO@NiO-Verbundwerkstoffen
Abbildung 3a zeigt repräsentative REM-Aufnahmen von oben des Kohlefasergewebesubstrats. Die Fasern hatten eine glatte Oberfläche (Einschub in Abb. 3a). Wie in Fig. 3b zu sehen ist, wuchs NiO mit einer blattartigen Struktur gleichmäßig auf dem Kohlefasergewebe. Im Gegensatz dazu wuchs ZnO als Nanostäbchen auf dem Kohlefasergewebe (Abb. 3c). ZnO-Nanostäbe mit glatter Oberfläche und Durchmessern von 200 nm wurden in großer Ausbeute erhalten (Einschub in Abb. 3c). Die FESEM-Bilder der ZnO@NiO-Komposite sind in Abb. 3d–f dargestellt. Der Durchmesser der Heterostrukturen wurde bei der Abscheidung von NiO-Nanoblättern größer. Eine Verlängerung der Abscheidungszeit von NiO auf 10 min (Abb. 3e) erhöhte die Dichte der abgeschiedenen NiO-Nanoblätter. Als die Abscheidungszeit auf 15 min verlängert wurde (Abb. 3f), war die Oberseite der Nanokomposite miteinander verbunden, was auf eine weitere Zunahme der abgeschiedenen NiO-Menge hindeutet, die mit den XRD-Ergebnissen übereinstimmt.

REM-Bilder von a Carbongewebe, b NiO-Nanoblätter, c ZnO-Nanostäbe, d ZN1, e ZN2 und f ZN3
Die EDS-Elementabbildungen in Abb. 4b und c, die dem SEM in Abb. 4a der ZN2-Probe entsprechen, zeigen deutlich die gleichmäßige räumliche Verteilung der Elemente Zink (Zn), Nickel (Ni) und Sauerstoff (O), was darauf hindeutet, dass NiO Nanoblätter, die gleichmäßig auf den Oberflächen von ZnO-Nanostäbchen verteilt sind. Die oben genannten Elemente im hierarchischen ZnO@NiO werden auch durch die EDX-Messung in Abb. 4 bestätigt, was mit den Beobachtungen des SEM übereinstimmt.
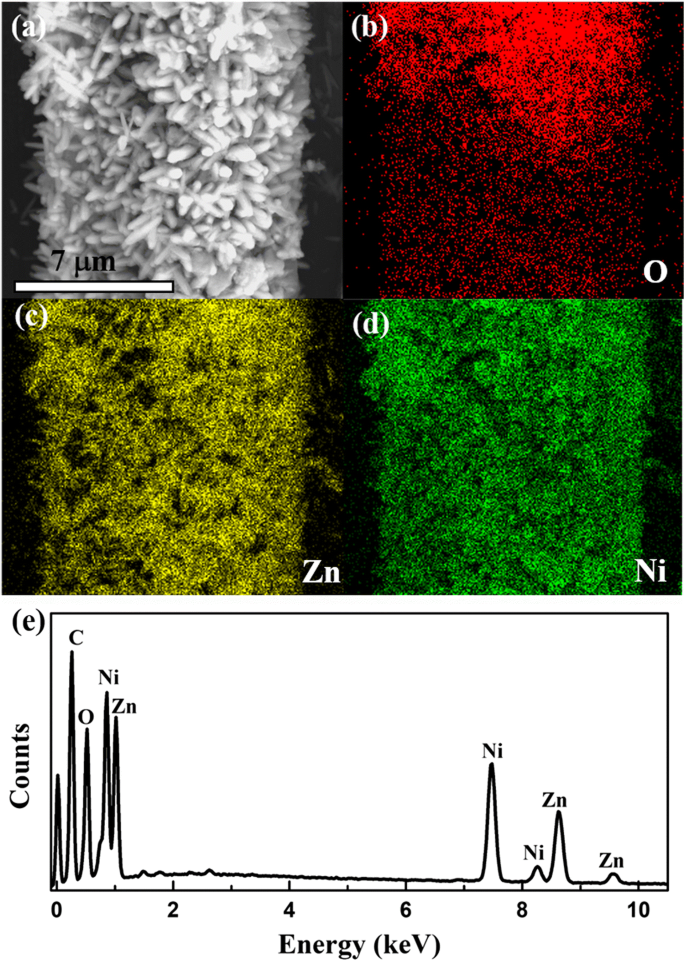
Typische energiedispersive Röntgenspektroskopie (EDS)-Elementarabbildungsbilder von ZN2. a Das entsprechende REM-Bild des Mapping-Bereichs. b O-Mapping. c Zn-Mapping. d Ni-Mapping. e EDS-Bilder
Wie in einem repräsentativen TEM-Bild in Abb. 5 zu sehen ist, haben die ZnO@NiO-Heterostrukturen (ZN2) eine Kern-Schale-Struktur, die aus ZnO-Nanostäbchen als Kern und NiO-Nanoblättern als Hülle besteht. Der Durchmesser der stäbchenförmigen Morphologien betrug ~ 200–300 nm. Das hochauflösende TEM-Bild in Abb. 5b zeigt die Grenzflächen der kristallinen ZnO- und NiO-Kristallgitter. Der Netzebenenabstand von 0,26 nm stimmt mit dem Gitterabstand der (002)-Ebene von hexagonalem Wurtzit ZnO überein, während der Gitterabstand von 0,241 nm dem Gitterabstand der (111)-Ebene von kubischem NiO entspricht. Darüber hinaus weisen die ausgeprägte Grenzfläche und Kontinuität der Gittersäume, die zwischen den NiO- und ZnO-Nanostrukturen in Abb. 5b beobachtet werden, auf die Bildung eines p-n-Heteroübergangs zwischen NiO und ZnO in der ZN2-Nanostruktur hin.

a TEM-Bild der ZnO@NiO-Heterostruktur (ZN2). b Hochauflösendes TEM des Bildes von ZN2
Röntgen-Photoelektronenspektroskopie-(XPS-)Muster von ZN2 sind in Abb. 6 dargestellt. In den XPS-Übersichtsspektren wurden Peaks beobachtet, die den vier Elementen Zn, O, Ni und C entsprechen (Abb. 6a). Der C1s-Peak mit einer Bindungsenergie von 284,6 eV wurde als Standardreferenz für die Kalibrierung verwendet und wird hauptsächlich auf Kohlenwasserstoff-Verunreinigungen zurückgeführt, die typischerweise in XPS-Spektren vorhanden sind [15]. In Abb. 6b wurden die XPS-Peaks bei 529,5 eV dem Gittersauerstoff zugeschrieben, während der Energiepeak bei 532,2 eV nicht adsorbiertem O2 . zugeordnet wurde oder Oberflächen-Hydroxyl-Spezies [35]. In Abb. 6c wurden die beiden Peaks, die bei Bindungsenergien von 1022,3 und 1045,2 eV zentriert waren, dem Zn 2p3/2 . zugeschrieben und Zn 2p1/2 stellt [36] fest, was darauf hindeutet, dass Zn in Form von Zn 2+ . existierte . Abbildung 6d zeigt die Ni 2p-XPS-Signale von ZN2, die in fünf Peaks entfaltet werden konnten. Die Peaks bei 854.0, 856.1 und 861.1 eV, entsprechend dem Ni 2p3/2 Zustand, könnte Ni-O zugeschrieben werden. Die verbleibenden beiden Peaks bei 873,1 und 879,6 eV wurden dem Ni 2p1/2 . zugeschrieben Zustand [32].
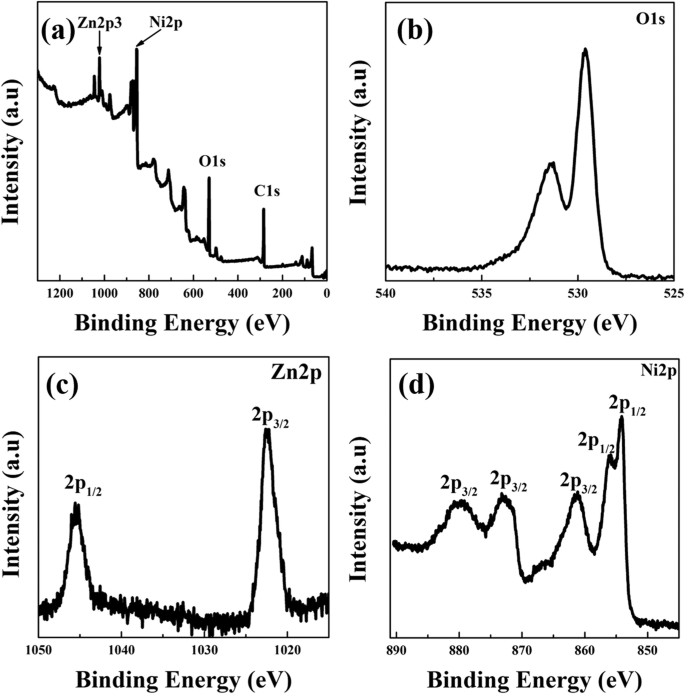
XPS-Spektren von ZN2. a Vermessungsspektren. b O 1s. c Zn 2p. d Ni 2p-Spektren
Um die potenzielle Anwendbarkeit der ZnO@NiO-Nanokomposite zu untersuchen, wurden die photokatalytischen Aktivitäten der Proben durch Messung des Abbaus des RhB-Farbstoffs unter Bestrahlung mit ultraviolettem Licht untersucht. Die charakteristische Absorption von RhB bei 554 nm wurde verwendet, um seine Konzentration während des Abbauprozesses zu überwachen. Nach 180 Minuten wurden 95 % des RhB in Gegenwart von ZN2 abgebaut. Im Vergleich dazu degradierten die ZnO-Nanostäbchen und NiO-Nanoblätter nur 38 % bzw. 33 % des RhB (Abb. 7a). Darüber hinaus war die Photoabbauaktivität der ZnO@NiO-Nanokomposite viel höher als die der ZnO-Nanostäbchen und NiO-Nanoblätter. Um die Photoabbauaktivität zu messen, wurde eine Auftragung der Photoabbauratenkonstante von RhB gegen die Abbauzeit verwendet. Die Reaktion kann wie folgt als kinetisches Modell pseudo-erster Ordnung beschrieben werden [9]:
$$ \ln \left(\frac{C}{C_0}\right)=-kt, $$wobei C 0 stellt die anfängliche Konzentration von RhB dar, C bezieht sich auf die Konzentration von RhB bei verschiedenen Bestrahlungszeiten t , und k ist die Reaktionsgeschwindigkeitskonstante. Die linearen Diagramme von ln(C /C 0 ) gegen die Zeit des Photoabbaus von RhB über ZnO, NiO, ZN1, ZN2 und ZN3 sind in Abb. 7b gezeigt. Die Geschwindigkeitskonstante (k ) entspricht der Steigung der linearen Anpassungen. Das berechnete k für den Abbau von RhB über ZN2 betrug 0,01656 min −1 , die höher war als die berechneten für die Reaktionen an ZnO-Nanostäbchen (0,00257 min −1 ) und NiO-Nanoblätter (0,00208 min −1 .) ). Insgesamt nahm die photokatalytische Aktivität in der Reihenfolge ZN2 > ZN3 > ZN1 > ZnO-Nanostäbchen > NiO-Nanoblätter ab. Die experimentellen Ergebnisse legen nahe, dass die Abscheidung der NiO-Schicht auf den ZnO-Nanostäben den Ladungstransfer erleichtert und somit die photokatalytische Aktivität signifikant verbessert. Gemäß den BET-Ergebnissen (dargestellt in der zusätzlichen Datei 1) nehmen die spezifischen Oberflächen von ZnO@NiO-Verbundwerkstoffen zunächst mit zunehmender Abscheidungszeit von NiO zu und nehmen dann ab, wenn die Abscheidungszeit weiter zunimmt; somit zeigt ZN2 die höchste photokatalytische Aktivität.
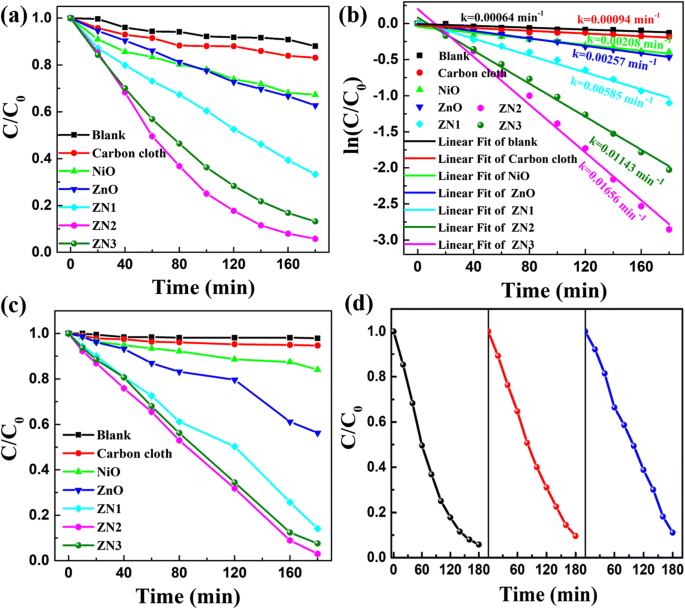
a Diagramme der relativen Konzentration (C/C0 ) von RhB gegen die Zeit für den Abbau von RhB über ZN1-, ZN2-, ZN3- und ZnO-Nanostäbchen und NiO-Nanoblättern unter UV-Licht-Bestrahlung. b Entsprechende Diagramme von − ln(C t /C 0 ) gegen die Bestrahlungszeit. c Diagramme der relativen Konzentration (C /C 0 ) von MO gegen die Zeit für den Abbau von MO über ZnO-, NiO- und ZnO@NiO-Heterostrukturen unter UV-Bestrahlung. d Wiederholter photokatalytischer Abbau von RhB über ZN2
Der photokatalytische Abbau des MO-Farbstoffs unter Bestrahlung mit ultraviolettem Licht wurde ebenfalls untersucht und die Ergebnisse sind in Abb. 7c dargestellt. Ebenso nahm die photokatalytische Aktivität in der Reihenfolge ZN2 > ZN3 > ZN1 > ZnO-Nanostäbchen > NiO-Nanoblätter ab. Daraus konnte geschlossen werden, dass die ZnO@NiO-Nanokomposite eine überlegene photokatalytische Aktivität gegenüber den ZnO-Nanostäbchen und NiO-Nanoblättern aufweisen. Die photokatalytische Stabilität von ZN2 wurde durch wiederholten photokatalytischen Abbau von RhB unter UV-Licht bestimmt. Wie in Abb. 7d zu sehen ist, blieb die Abbauausbeute über die wiederholten Zyklen hoch (~ 95 %), wobei nach dem dritten Zyklus eine leichte Abnahme auf 90 % beobachtet wurde. Diese Ergebnisse belegen die hohe photokatalytische Effizienz und Wiederverwendbarkeit der ZnO@NiO-Heterostrukturen, die wichtige Attribute für ihren praktischen Einsatz in realen Anwendungen zur Eliminierung organischer Schadstoffe aus Abwasser sind.
Die entsprechenden Photostromantworten sind in Abb. 8a gezeigt. Mehrere Ein-Aus-Lichtzyklen wurden verwendet, um die Trenneffizienz der Ladungsträger zu untersuchen. Die NiO-Nanoblätter zeigten sowohl unter dunklen Bedingungen als auch bei heller Beleuchtung keine Stromänderungen, während die ZnO-Nanostäbchen unter ultravioletter Bestrahlung eine geringe Photostromantwort zeigten. Im Gegensatz dazu zeigten die ZnO@NiO-Komposite eine höhere Photostromdichte. Und die Photostromdichte nahm in der Reihenfolge ZN2 > ZN3 > ZN1 > ZnO-Nanostäbchen > NiO-Nanoblätter ab. Die schnellen Photostromantworten implizierten, dass der Ladungstransport in den Proben sehr schnell war. Die verbesserte Photostromantwort der ZnO@NiO-Komposite kann der Bildung inniger Grenzflächenkontakte zwischen den ZnO-Nanostäben und NiO-Nanoblättern zugeschrieben werden. Daraus wird abgeleitet, dass die photoangeregten Elektronen in den NiO‐Nanoblättern erzeugt und unter ultravioletter Bestrahlung effizient vom CB von NiO auf die benachbarten ZnO‐Nanostäbchen übertragen werden können, wobei ZnO als effiziente Elektronensenke und Elektronentransporter dient und so die Rekombination photogenerierter Elektron−Loch hemmt Paare. Es ist erwähnenswert, dass der Photostrom der ZnO@NiO-Komposite anfangs mit zunehmender Abscheidungszeit von NiO zunahm und dann abnahm, wenn die Abscheidungszeit weiter verlängert wurde. Es ist möglich, dass die Grenzflächenkontaktfläche zwischen den ZnO-Nanostäben und NiO-Nanoblättern zunächst zunimmt und dann mit zunehmender Abscheidungszeit von NiO abnimmt, was mit dem Ergebnis der photokatalytischen Aktivität übereinstimmt.
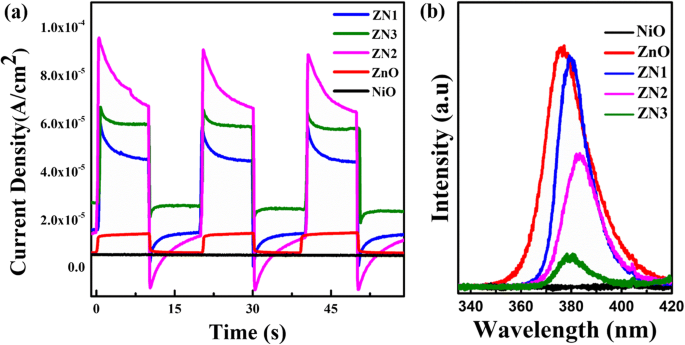
a Photostromantwort von NiO-Nanoblättern, ZnO-Nanostäbchen und ZnO@NiO-Heterostruktur unter UV-Lampenbestrahlung (10 W). b PL-Spektren von reinen ZnO-Nanostäbchen, NiO-Nanoblättern und ZnO@NiO-Komposit
Abbildung 8b zeigt die typischen PL-Spektren von reinen ZnO-Nanostäbchen, NiO-Nanoblättern und ZnO@NiO-Heterostrukturen, die unter denselben Bedingungen bei Raumtemperatur gemessen wurden. Bei reinen ZnO-Nanostäbchen wird ein starker Emissionspeak bei 378 nm beobachtet, der der Emission von ZnO nahe der Bandkante entspricht. Bei NiO-Nanoblättern wird kein Emissionspeak beobachtet. Darüber hinaus ist die PL-Emissionsintensität von ZnO@NiO-Kompositen im Vergleich zu reinen ZnO-Nanostäbchen offensichtlich abgeschwächt, was darauf hindeutet, dass die Rekombination photogenerierter Elektron-Loch-Paare eingeschränkt ist. Die Ergebnisse von Photostrom und PL zeigen, dass das ZnO@NiO-Nanokomposit die Trenneffizienz und die Grenzflächenladungstransfereffizienz photogenerierter Elektron-Loch-Paare bemerkenswert verbessern kann.
Die verbesserte photokatalytische Aktivität der ZnO@NiO-Heterostrukturen wurde der schnellen Ladungsträgertrennung und dem schnellen Ladungsträgertransport an der Grenzfläche der ZnO@NiO-Heterostrukturen aufgrund der Typ-II-Bandausrichtung zwischen ZnO und NiO zugeschrieben. Dieser vorgeschlagene Mechanismus stimmt mit dem in früheren Berichten überein [8, 10, 22]. Abbildung 9 zeigt ein vorgeschlagenes Energiebandstrukturdiagramm der ZnO@NiO-Heterostruktur. ZnO ist ein Halbleiter vom n-Typ, während NiO ein Halbleiter vom p-Typ ist. Wenn sich ZnO und NiO verbinden, entsteht ein p-n-Heteroübergang, und an der Grenzfläche zwischen NiO und ZnO wird aufgrund von Elektronen- und Lochtransfers ein inneres elektrisches Feld erzeugt. Bei Bestrahlung mit UV-Licht werden die Elektronen im VB zum CB angeregt und hinterlassen Löcher im VB. Die Bandausrichtung der p-Typ-NiO- und n-Typ-ZnO-Heteroübergänge ist vorteilhaft für die Übertragung der durch Licht erzeugten Elektronen von der CB von NiO auf die CB von ZnO, dann können sich die Elektronen mit den gelösten Sauerstoffmolekülen verbinden und die Superoxid-Radikalanionen (• O2 − ), die eine wichtige Rolle in der gesamten photokatalytischen Reaktion spielen. Umgekehrt können die durch Licht erzeugten Löcher von der VB von ZnO auf die VB von NiO übertragen werden, und die Löcher werden leicht von OH − . eingefangen an der Katalysatoroberfläche, um weiter die Hydroxylradikalspezies (•OH) zu ergeben, die ein extrem starkes Oxidationsmittel für die Zersetzung des organischen Farbstoffs ist. Daher zeigten die ZnO@NiO-Nanokomposite eine überlegene photokatalytische Leistung gegenüber den ZnO-Nanostäbchen und NiO-Nanoblättern.
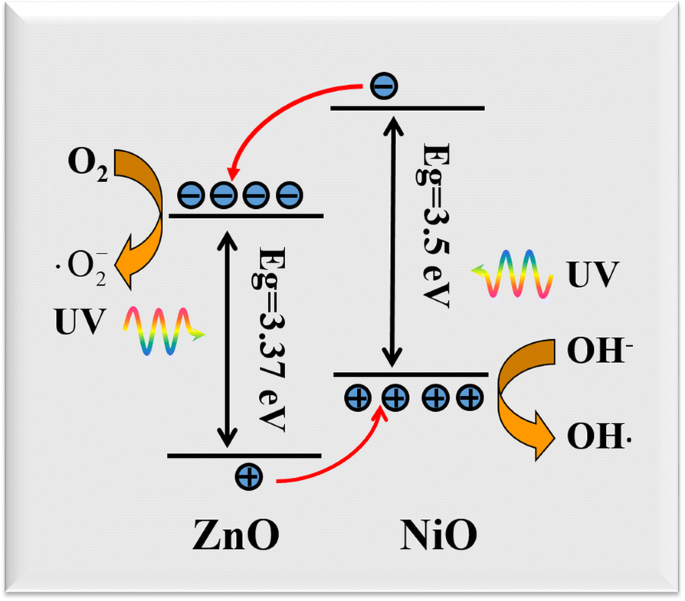
Schema der Energiebandausrichtung zwischen ZnO und NiO
Schlussfolgerungen
ZnO@NiO-Heterostrukturen wurden erfolgreich durch ein einfaches elektrochemisches Abscheidungsverfahren hergestellt. Die photokatalytische Aktivität der ZnO@NiO-Nanokomposite war der von ZnO-Nanostäbchen und NiO-Nanoblättern hinsichtlich des Abbaus von MO- und RhB-Farbstoffen unter UV-Licht-Bestrahlung überlegen. Die hohe photokatalytische Leistung wurde der hohen Trenneffizienz der photoerzeugten Elektron-Loch-Paare vom p-n-Heteroübergang zugeschrieben, wie durch die Photostromantwortmessungen bestätigt wurde. Die Ergebnisse zeigten, dass in den ZnO@NiO-Heterostrukturen mehr freie Ladungsträger erzeugt und getrennt werden konnten, was zu einer höheren Trenneffizienz im Vergleich zu der in den ZnO-Nanostäbchen und NiO-Nanoblättern erzielten führte. Darüber hinaus konnten die ZnO@NiO-Heterostrukturen mit minimaler Abnahme der photokatalytischen Aktivität leicht recycelt werden. Die hohe photokatalytische Effizienz und Wiederverwendbarkeit der ZnO@NiO-Heterostrukturen, die eine einfache Trennung aus der Lösung ermöglichen, haben wichtige Anwendungen bei der Eliminierung organischer Schadstoffe aus Abwasser.
Abkürzungen
- CB:
-
Leitungsband
- EDS:
-
Energiedispersive Röntgenspektroskopie
- MO:
-
Methylorange
- PL:
-
Photolumineszenz
- RhB:
-
Rhodamin B
- SEM:
-
Rasterelektronenmikroskopie
- TEM:
-
Transmissionselektronenmikroskopie
- VB:
-
Valenzband
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Benchmarking Ihrer Schmierleistung für verbesserte Zuverlässigkeit
- 3 Schlüssel für eine verbesserte Anlagenleistung
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität
- Hierarchische Heterostruktur von ZnO@TiO2-Hohlkugeln für eine hocheffiziente photokatalytische Wasserstoffentwicklung
- Durch sichtbares Licht angetriebene photokatalytische Leistung von N-dotierten ZnO/g-C3N4-Nanokompositen
- Herstellung und photokatalytische Leistung von Hohlstruktur-LiNb3O8-Photokatalysatoren
- Herstellung von PPy-beschichteten MnO2-Hybrid-Mikromaterialien und ihre verbesserte zyklische Leistung als Anode für Lithium-Ionen-Batterien
- Ein neuartiger Bi4Ti3O12/Ag3PO4-Heteroübergang-Photokatalysator mit verbesserter photokatalytischer Leistung
- Die Herstellung und hocheffiziente Absorption elektromagnetischer Wellen von CoFe/C-Kern-Schale-strukturierten Nanokompositen
- Herstellung und Charakterisierung von ZnO-Nano-Clips durch das Polyol-vermittelte Verfahren



