Verwendung von Omniscan-beladenen Nanopartikeln als tumorgerichtetes MRT-Kontrastmittel bei oralem Plattenepithelkarzinom durch Gelatinase-Stimuli-Strategie
Zusammenfassung
In dieser Studie wurde das tumorgerichtete MRT-Kontrastmittel mit Gelatinase-Stimuli-Nanopartikeln (NPs) und Omniscan (Omn) im Doppelemulsionsverfahren hergestellt. Die Größe, Verteilung, Morphologie, Stabilität, Wirkstoffbeladung und Verkapselungseffizienz von Omn-NPs wurden charakterisiert. Die makroskopischen und mikroskopischen morphologischen Veränderungen von NPs als Reaktion auf Gelatinasen (Kollagenasen IV) wurden beobachtet. Die MR-Bildgebung mit Omn-NPs als Kontrastmittel wurde in den oralen Plattenepithelkarzinommodellen mit Omn als Kontrolle ausgewertet. Wir fanden klare Hinweise darauf, dass die Omn-NPs durch Gelatinasen transformiert wurden und das Signal der T1-gewichteten MRT-Sequenz zeigte, dass das Tumor-zu-Hintergrund-Verhältnis bei Omn-NPs signifikant höher war als bei Omn. Der Spitzenzeitpunkt nach der Injektion lag bei Omn-NPs viel später als bei Omn. Diese Studie zeigt, dass Omn-NPs als MRT-Kontrastmittel mit verbesserter Spezifität und verlängerter Zirkulationszeit auf der Grundlage einer relativ einfachen und universellen Strategie viel versprechend sind.
Einführung
Das Plattenepithelkarzinom der Mundhöhle (OSCC) ist der häufigste bösartige Tumor im Mund-, Kiefer- und Gesichtsbereich; Aufgrund der besonderen Lage des OSCC beeinträchtigt die operative Behandlung zwangsläufig die Funktionen und Ästhetik des orofazialen Bereichs. Eine frühzeitige und genaue Diagnose von OSCC ermöglicht eine individuellere und angemessenere chirurgische Behandlung und führt daher zu einer geringeren Morbidität nach der Behandlung sowie zu einer besseren Prognose für den Patienten. Eine korrekte Diagnose und Staging, die sich auf die Behandlungsplanung der Krankheit auswirkt, erfordert den Einsatz bildgebender Verfahren [1].
Die MRT ist ein nicht-invasives Bildgebungsverfahren ohne ionisierende Strahlung. Es kann verwendet werden, um hochauflösende und dreidimensionale Bilder von Weichgeweben bereitzustellen. Die multiparametrische MRT wurde in klinischen Studien getestet und hat sich bei der Tumorlokalisation als nützlich erwiesen [2]. Während verschiedene Verbindungen als MRT-Kontrastmittel bewertet wurden, sind Gadolinium(Gd)-Komplexe nach wie vor die am häufigsten verwendeten und machen im Wesentlichen alle derzeit in der Klinik verwendeten Mittel aus [3]. Die bestehenden Gd-basierten MRT-Kontrastmittel sind jedoch nicht tumorspezifisch und nicht in der Lage, einen präzisen Nachweis und eine genaue Charakterisierung des Tumors zu ermöglichen. Aufgrund der geringen Größe können die meisten dieser Wirkstoffe in den intravaskulären und interstitiellen Räumen verteilt und über die Nierenfiltration schnell ausgeschieden werden [3]. Um die Spezifität in Tumorgeweben zu verbessern und die Zirkulationszeit im Blutfluss des MRT-Kontrastmittels zu verlängern, haben Forscher versucht, variable neue MRT-Kontrastmittel zu entwickeln und zu synthetisieren [4,5,6,7,8].
In der jüngeren Vergangenheit wurden viele mit Methoxy-Poly(ethylenglycol)(mPEG) und/oder Polycaprolacton (PCL) verwandte Nanopartikel (NPs) entworfen und untersucht [9,10,11]. Diese NPs wurden verwendet, um Medikamente zu verabreichen, sie unterstützten die Löslichkeit von Medikamenten, verbesserten den therapeutischen Prozess, indem sie die Zirkulationszeit verlängerten und die Aufnahme in Tumoren durch die verbesserte Permeabilität und Retentionswirkung verbesserten. mPEG und PCL sind von der US-amerikanischen Food and Drug Administration zugelassene Copolymere, die eine sehr geringe Immunogenität, Antigenität und Toxizität aufweisen und für medizinische Anwendungen umfassend untersucht werden [12]. Es ist bekannt, dass die Biokompatibilität und die biologische Abbaubarkeit wichtige Eigenschaften beim Einsatz von Nanopartikeln in der Medizin-, Umwelt- und Verfahrenstechnik sind [13, 14]. In unserer vorherigen Arbeit haben wir ein Gelatinase-Stimuli-Wirkstoffabgabesystem basierend auf mPEG und PCL mit tumorspezifischen Gelatinasen-spaltbaren Peptiden entwickelt, die zwischen mPEG und PCL eingefügt wurden [12]. Therapeutische Medikamente wie Docetaxel, miR-200c wurden auf dieses Nanopartikel geladen. Die In-vitro- und In-vivo-Studien zeigten, dass die Medikamente spezifisch in das Tumorgewebe abgegeben werden können [15]. Unsere NPs basieren auf einer relativ einfachen tumorgerichteten Strategie. Der Effekt der verbesserten Permeabilität und Retention (EPR) könnte die Nanopartikel in Tumorgewebe anreichern. Gelatinasen (Matrix-Metalloproteasen-2/9 MMP2/9, Collagenasen IV), die in Tumoren weit verbreitet sind, würden die NPs trennen und die beladenen Medikamente freisetzen. Im Gegensatz zur aktiven Targeting-Strategie haben unsere NPs das Potenzial, variable therapeutische und diagnostische Medikamente zu laden, was einfacher und universeller wäre.
In dieser Studie haben wir die gleiche Art von NP mit Omn, einem weit verbreiteten MRT-Kontrastmittel [16], beladen, um das Ziel zu erreichen, ein tumorgerichtetes, biokompatibles und biologisch abbaubares MRT-Kontrastmittel zu etablieren. Die Wirksamkeit von Omn-NPs als MRT-Kontrastmittel wurde im Xenograft-Modell des humanen oralen Plattenepithelkarzinoms mit Omn allein als Kontrolle bewertet.
Materialien und Methoden
Materialien
Methoxy-polyethylenglycol-NHS (mPEG-NHS, Mn 5000) wurde von Beijing Jiankai Technology Co (Beijing, China) bezogen. Das durch Gelatinase spaltbare Peptid (Sequenz:H2N-PVGLIG-COOH) wurde von Shanghai HD Biosciences Co (Shanghai, China) synthetisiert. Omniscan (Gadodiamid-Injektion) wurde von GE Healthcare (Irland) bezogen. Collagenasen IV wurden von Sigma (USA) bezogen.
Synthese von Omn-beladenen Gelatinasen-Stimuli-NPs
Gelatinasen-spaltbares Copolymer mPEG-Pep-PCL und mPEG-PCL ohne Peptid wurden durch ringöffnende Copolymerisation wie in unserer vorherigen Arbeit [17] synthetisiert. Die Omn-NPs wurden durch eine Doppelemulsionslösungsmittelverdampfungstechnik formuliert. Kurz gesagt wurden 10 mg mPEG-Pep-PCL-Copolymer in 1 ml Dichlormethan (DCM) gelöst. Dann wurden 0,1 ml, 0,2 ml bzw. 0,3 ml Omn zugegeben. Diese Mischung wurde in 3 ml einer 3% (w/v) wässrigen Polyvinylalkohol (PVA)-Lösung durch Beschallung (XL2000, Misonix, Farmingdale, NY, USA) für 60 s emulgiert, um eine Öl/Wasser (o/w)-Emulsion zu erhalten . Diese Emulsion wurde dann in 5 ml wässriger Lösung, die 0,5% (w/v) enthielt, durch Beschallung mit PVA für 60 s emulgiert. Die gebildete W/O/W-Emulsion wurde bei Raumtemperatur in einem Abzug leicht gerührt, bis das organische Lösungsmittel verdampft war. Die resultierende Lösung wurde filtriert, um nicht eingebaute Arzneimittel zu entfernen. Leer-NPs wurden auf die gleiche Weise wie beschrieben hergestellt, ohne Omn hinzuzufügen. Omn-beladene mPEG-PCL-NPs (Con-Omn-NPs) wurden mit 10 mg mPEG-PCL-Copolymer synthetisiert und 0,2 mL Omn folgten den gleichen Schritten.
Partikelgrößenmessung und Morphologieuntersuchung von NPs
Die Partikelgrößen und Stabilität von Omn-NPs und Blank-NPs wurden durch dynamische Lichtstreuung (DLS) (Brookhaven Instruments Corporation, USA) gemessen. Omn-NPs und Blank-NPs wurden bei Raumtemperatur aufbewahrt. Die Partikelgrößen wurden alle 2 Tage durch DLS bestimmt, um die Stabilität der Omn-NPs zu bewerten (insgesamt für 6 Tage). Die Werte waren der Durchschnitt von Dreifachmessungen für eine einzelne Probe. Die Morphologieuntersuchung von Omn-NPs und Blank-NPs wurde unter Verwendung eines Transmissionselektronenmikroskops (TEM) (JEM-100S, JEOL, Japan) durchgeführt. Ein Tropfen richtig verdünnter NPs-Suspension wurde auf ein mit einer Nitrozellulosemembran bedecktes Kupfergitter gegeben und bei Raumtemperatur luftgetrocknet. Die Probe wurde vor der Untersuchung mit Phosphorwolfram-Natrium-Lösung 1% (w/v) negativ gefärbt.
Der Inhalt des Wirkstoffladens und die Effizienz der Kapselung
Der Wirkstoffbeladungsgehalt und die Einkapselungseffizienz von Omn-NPs wurden durch Berechnung der Konzentration von Gadoliniumionen analysiert. Ein Milliliter Omn-NPs wurde durch konzentrierte Salpetersäure gespalten, und dann wurde die Mischung mit verdünnter Salpetersäure verdünnt. Die Probe wurde durch induktiv gekoppelte Plasma-Atomemissionsspektrometrie (ICP-AES, Optima 5300DV, PerkinElmer, USA) getestet.
$$ \mathrm{Droge}\ \mathrm{Laden}\ \mathrm{Inhalt}\%=\frac{\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{der}\ \mathrm{Droge}\ \ mathrm{in}\ \mathrm{Nanopartikel}}{\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{der}\ \mathrm{Nanopartikel}} $$$$ \mathrm{Kapselung}\ \mathrm{Wirkungsgrad }\%=\frac{\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{das}\ \mathrm{Medikament}\ \mathrm{in}\ \mathrm{Nanopartikel}}{\mathrm{Gewicht}\ \mathrm{von}\ \mathrm{der}\ \mathrm{Ernährung}\ \mathrm{Droge}} $$Makroskopische Veränderungen und mikroskopische morphologische Veränderungen von NPs als Reaktion auf Collagenase
Omn-beladene mPEG-PCL-NPs (Con-Omn-NPs) und mPEG-Pep-PCL-NPs (Omn-NPs) wurden mit Hank-Lösung enthaltend Collagenase IV (0,34 mg/ml) bei 37 °C für 24 Stunden inkubiert. Veränderungen der Transparenz der Lösung wurden mit bloßem Auge beobachtet.
Die mikroskopische Morphologiebewertung von Con-Omn-NPs und Omn-NPs (inkubiert mit oder ohne Collagenase) wurde unter Verwendung eines TEM durchgeführt. Für die TEM wurde ein Tropfen NPs-Suspension auf ein mit einer Nitrozellulosemembran bedecktes Kupfergitter gegeben und vor der Beobachtung luftgetrocknet.
In V itro C ellular U ptake
Humane orale Plattenepithelkarzinomlinien (HSC3) wurden freundlicherweise vom Neunten Krankenhaus von Shanghai zur Verfügung gestellt. Die Tumorzellen wurden in einer 24-Well-Platte mit einer Dichte von 5 × 10 5 . ausgesät Zellen pro Vertiefung und 24 h kultiviert. Dann wurden Cumarin-6-beladene mPEG-Pep-PCL-NPs (12,5 µg/ml berechnet durch Cumarin-6) in das Kulturmedium gegeben und 0,5 und 1 Stunde bei 37 °C inkubiert. Das Kulturmedium wurde abgesaugt und dreimal mit PBS gewaschen. Die Zellen wurden 20 min mit absolutem Ethanol (1 ml pro Vertiefung) immobilisiert, dann dreimal mit PBS gewaschen. Die Zellen wurden durch Immunfluoreszenz-Zytochemie und konfokales Laser-Scanning-Mikroskop (LSM710, Carl Zeiss MicroImaging GmbH, Berlin, Deutschland) beobachtet. Die Anregungs- und Emissionswellenlänge betrug 460 nm für Cumarin-6.
Tiere
Alle Tierversuche wurden in voller Übereinstimmung mit den Richtlinien des Leitfadens für die Pflege und Verwendung von Labortieren durchgeführt, der von den US-amerikanischen National Institutes of Health veröffentlicht wurde (NIH-Publikation Nr. 85-23, überarbeitet 1985) und wurde vom Ethics Review Board für . genehmigt Tierstudien des Nanjing Stomatological Hospital, Medizinische Fakultät der Universität Nanjing. BALB/c-Mäuse (5–6 Wochen, 18–22 g) wurden vom Model Animal Research Center der Nanjing University gekauft. Die Tiergesundheit, einschließlich Körpergewicht und Hautzustand, wurde zweimal wöchentlich überwacht. Ulzerationen, eine Verringerung der Tiermobilität und Gewichtsverlust, wurden während des Experiments nicht beobachtet.
OSCC-Modelleinrichtung
Die Tumorzellen wurden in Dulbecco modifiziertem Eagle-Medium (DMEM) mit 10 % fötalem Rinderserum (FBS), 100 µE/ml Penicillin und 100 µg/ml Streptomycin bei 37 °C in einer angefeuchteten Atmosphäre mit 5 % CO . kultiviert 2 und 95% Luft. Um ein Xenotransplantatmodell des menschlichen OSCC zu erstellen, wurden die menschlichen OSCC-Zellen HSC3 (1 × 10 6 Zellen in 50 µl Phosphatpuffer-Kochsalzlösung (PBS)) wurden in die rechte Achselhöhle von Nacktmäusen (3 Mäuse pro Gruppe) subkutan geimpft. Wir haben die Tumordimension jeden zweiten Tag mit einem Messschieber gemessen. Als der Tumordurchmesser etwa 0,4–0,5 cm betrug, waren die Mäuse bereit für In-vivo-MR-Bildgebungsexperimente.
In-vivo-MRT-Studie mit Omn-NPs und Omn als Kontrastmittel
Für In-vivo-Studien teilten wir die Mäuse in zwei Gruppen (A und B). Mäusen in Gruppe A wurden Omn-NPs durch die Schwanzvene injiziert, während Mäusen in Gruppe B die gleiche Omn-Konzentration wie die geladenen NPs injiziert wurde. Beide Gruppen wurden mit einem Bruker Biospin 7.0 T MRT-Scanner (Bruker BioSpin, Ettlingen, Deutschland) gescannt. Die Parameter wurden wie folgt eingestellt:Sichtfeld (FOV), 3,5 × 2,5 cm; Scheibendicke 0,8 mm; TR, 745,2 µm; TE, 7,5 µm. Die axialen Schnitte der Maus wurden unter Verwendung einer T1-gewichteten Spin-Echo-Sequenz akquiriert. Bilder wurden vor und zu verschiedenen Zeitpunkten nach der intravenösen Verabreichung von zwei Kontrastmitteln aufgenommen.
Expression von MMP2/9 in Tumor- und Normalgewebe
Nach einer in-vivo-MRT-Untersuchung wurden Tumorgewebe, Herz, Leber, Milz, Lunge, Niere und Muskelgewebe aus dem OSCC-Mäusemodell für die immunhistochemische (IHC) Färbung für MMP2 und MMP9 ausgewählt. Alle Gewebe wurden seziert und in 10 % neutral gepuffertem Formalin fixiert, routinemäßig zu Paraffin verarbeitet und in einer Dicke von 5 µm geschnitten. Die IHC-Untersuchung für die semiquantitative Expression (–, + und ++) von MMP2/9 wurde unter Verwendung von Lichtmikroskopie durchgeführt.
Statistische Analyse
Die statistische Analyse wurde mit t . von Student durchgeführt Prüfung. Die Daten wurden als Mittelwert ± SD und einem Wert von p . aufgeführt <0,05 wurde als statistisch signifikant angesehen.
Ergebnisse und Diskussion
Charakterisierung von mPEG-Pep-PCL-Nanopartikeln
Die 1 H-NMR(CDCl3 )Spektren von mPEG-Pep-PCL-Copolymeren bestätigten, dass das Peptid erfolgreich mit mPEG konjugiert wurde und die mPEG-Pep-Konjugate erfolgreich mit PCL konjugiert wurden ( 1a ). Das Molverhältnis von hydrophilem Block zu hydrophobem Block (mPEG/PCL) im mPEG-Pep-PCL-Copolymer betrug etwa 0,95 basierend auf dem Integralverhältnis von -CH2-O- (4,04 ppm) im PCL-Segment zu -CH2-CH2-O ( 3,65 ppm) im mPEG-Segment von 1 H-NMR-Messung.
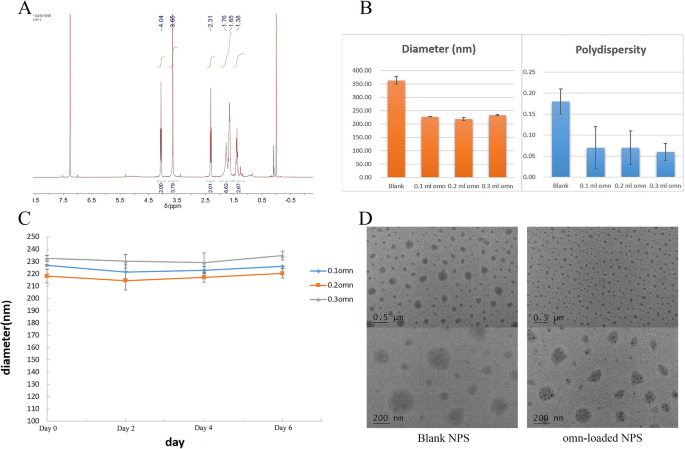
a 1 H-Kernresonanzspektren (300 MHz, 25 μC) von PEG-Pep-PCL in CDCl3. b Der Durchmesser und der Polydispersitätsindex von Blank-NPs und Omn-beladenen NPs (0,1 ml, 0,2 ml, 0,3 ml). c Die Stabilität von Omn-beladenen NPs (0,1 ml, 0,2 ml, 0,3 ml). d TEM-Aufnahmen von Blank-NPs und Omn-beladenen NPs. Die Fehlerbalken stellen die Standardabweichungen von drei separaten Messungen dar.
Partikelgrößen und Stabilität von NPs
Die Partikelgrößen und der Polydispersitätsindex (PDI) wurden mittels DLS bestimmt (Abb. 1b). Es wurden keine signifikanten Unterschiede in der Partikelgröße zwischen den drei Omn-NPs gefunden (p> 0,05), während zwischen Omn-NPs und Blank-NPs signifikante Unterschiede gefunden wurden (p <0,05). Für den PDI wurden keine signifikanten Unterschiede zwischen diesen Omn-NPs gefunden (p> 0,05), aber es gab signifikante Unterschiede zwischen Omn-NPs und Blank-NPs (p <0,05).
Bezüglich der Stabilität von Omn-NPs wurden in allen drei Omn-NPs keine Ausfällung und offensichtliche Größenänderungen beobachtet (Abb. 1c), was darauf hindeutet, dass Omn-NPs stabil waren.
Morphologische Studien von NPs
Die TEM-Aufnahmen von Blank-NPs und Omn-NPs sind in Abb. 1d dargestellt. Die abgeflachte Form konnte auch sowohl in Blank-NPs als auch in Omn-NPs beobachtet werden und die Omn-NPs waren aufgrund ihrer unterschiedlichen Größe viel kleiner als Blank-NPs. Darüber hinaus konnte das Omn in den NPs deutlich unterschieden werden, das in den NPs als dunkle Partikel erschien. Dieser Omn-Partikel konnte innerhalb der NPs verstreut beobachtet werden.
Drug Loading Content und Verkapselungseffizienz
Der Wirkstoffbeladungsgehalt und die Einkapselungseffizienz der drei Omn-NPs sind in Tabelle 1 gezeigt. Das Ergebnis zeigte, dass 0,3 ml Omn die höchste Wirkstoffbeladung aufwiesen, aber die Einkapselungseffizienz war ziemlich gering und 0,1 ml Omn hatte die höchste Einkapselungseffizienz und relativ nah Medikamentenbeladung mit 0,2 µl und 0,3 µl Omn. Unter Berücksichtigung sowohl der Wirkstoffbeladung als auch der Verkapselungseffizienz wurden 0,1 µl Omn-NPs in der abschließenden In-vivo-MRT-Studie verwendet. Die geringe Verkapselungseffizienz zeigte auch, dass das von uns hinzugefügte Omn im Reaktionssystem für NPs ausreichend war.
Makroskopische und mikroskopische morphologische Veränderungen von Omn-NPs und Con-Omn-NPs als Reaktion auf Collagenase IV
Um die Spaltung von NPs als Reaktion auf Gelatinase (Kollagenase IV) zu überprüfen, wurden die makroskopischen und mikroskopischen morphologischen Veränderungen von Omn-NPs und Con-Omn-NPs nach Inkubation mit Hanks Lösung mit 2 µmg/ml Collagenase IV bewertet. A1 und B1 zeigten die transparenten Lösungen von Con-Omn-NPs vor und nach der Inkubation mit Collagenase IV, und A2 und B2 zeigten keine Veränderung der mikroskopischen Morphologie der Con-Omn-NPs unter Verwendung von TEM vor und nach der Inkubation. C1 und D1 zeigten die Lösungen von Omn-NPs vor und nach der Inkubation mit Collagenase IV. D1 zeigte, dass die Flüssigkeit nach 24 Stunden trübe wurde, als es in den Omn-NP-Lösungen zu Ausfällungen kam. D2 zeigte die TEM-Bilder von Omn-NPs als Reaktion auf Kollagenasen IV, die Strukturen der NPs wurden aufgebrochen (Abb. 2). Dieses Ergebnis zeigte, dass unsere NPs Gelatinase-Stimuli waren:Die Spaltung des Peptids würde die NPs aufbrechen und die beladenen Medikamente würden freigesetzt. Und die Eigenschaft, das Peptid zu spalten, um die beladenen Medikamente freizusetzen, wurde auch durch die Wirkstofffreisetzung und in unserer früheren Forschung gezeigt [12, 18].

a1 , a2 , b1 , b2 , c1 , c2 , d1 , d2 Makroskopische und mikroskopische morphologische Veränderung von Omn-beladenen mPEG-PCL-NPs (Con-Omn-NPs) und Omn-beladenen mPEG-Pep-PCL-NPs (Omn-NPs) nach Inkubation mit Collagenase IV
In-vitro-Studien zur zellulären Aufnahme
Die zelluläre Aufnahme von Cumarin-6-beladenen NPs ist in Abb. 3 gezeigt. Die grüne Fluoreszenz von Cumarin-6 wurde im Zytoplasma der HSC3-Zellen gezeigt, was darauf hindeutet, dass Cumarin-6 zusammen mit den NPs in das Zytosol eintrat. Da Cumarin-6 ursprünglich in den NPs eingeschlossen war, zeigte dies, dass unsere NPs Zellmembranbarrieren effektiv durchdringen und sich über Endocytose im Zellzytoplasma verteilen konnten.
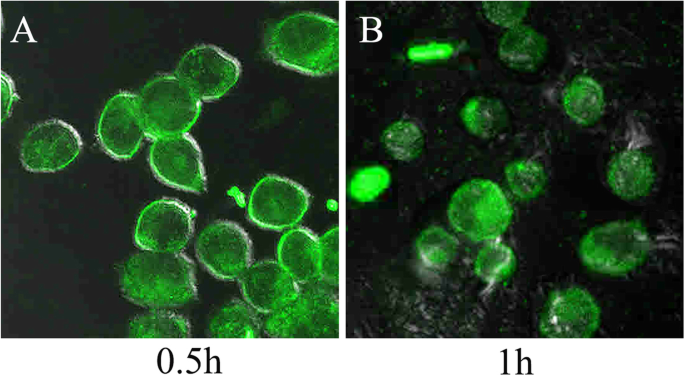
a, b In-vitro-Studien zur zellulären HSC3-Aufnahme von Nanopartikeln. Konfokalmikroskopische Aufnahmen von HSC3-Zellen nach Inkubation mit Cumarin-6-beladenen NPs
MRT-Bildgebung in vivo mit Omn-NPs und Omn als Kontrastmittel
Bilder wurden aufgenommen, bevor Omn-NPs und Omn intravenös in einer Dosis von 0,025 µmmol/kg (Gd 3+ ) von 2 Gruppen. Bilder nach Kontrastmittelgabe wurden dann 5 min, 15 min, 30 min, 60 min, 90 min, 120 min, 150 min und 180 min nach der Injektion erhalten (Abb. 4a). Das Signal von Tumor-zu-Hintergrund (TBR ) wurde berechnet und als quantifizierbarer Indikator für die Bewertung mit Omn-Nps im Vergleich zu Omn verwendet. Die Ergebnisse zeigten, dass die maximale TBR für Omn-NPs 2,23 ± 0,10 und 1,48 ± 0,01 für Omn betrug, die Zeit bis zur Spitze 30 min für Omn-NPs und 5 min für Omn betrug und die Signalverstärkungsdauer 180 min für Omn betrug. NPs und 30 min für Omn (Abb. 4b). Es gab einen signifikanten Unterschied für die maximale TBR und die Retentionszeit zwischen den beiden Gruppen (p <0,05). Obwohl unsere Omn-NPs eine relativ geringe Wirkstoffbeladung aufwiesen, wurde eine überlegene verbesserte in-vivo-MR-Bildgebung im Vergleich zu Omn allein demonstriert. Dies bewies auch, dass unsere Omn-NPs Gelatinase-Stimuli und tumorspezifisch waren.
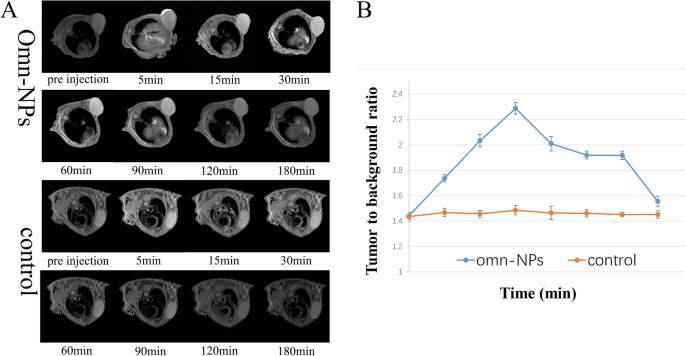
a , b Axiale MRT-Bilder und Liniendiagramm des Tumor-zu-Hintergrund-Verhältnisses des Xenograft-Modells des menschlichen OSCC an den angegebenen Tumorpositionen, aufgenommen mit einer T1-gewichteten Sequenz. Die Fehlerbalken stellen die Standardabweichungen von drei separaten Messungen dar.
Obwohl in letzter Zeit fortschrittliche bildgebende Verfahren wie die Einzelphotonen-Emissions-Computertomographie [19], die Positronen-Emissions-Tomographie (PET) [20] und die optische Bildgebung [21] bei der Diagnose von OSCC verwendet wurden, ist die MRT immer noch die am weitesten verbreitete und zuverlässigste Instrumente zum Staging von Kopf-Hals-Tumoren nach dem TNM-Krebs-Staging-System [1] und Gadoliniumchelate sind immer noch die am häufigsten verwendeten MRT-Kontrastmittel [22].
Um das Ziel zu erreichen, den Tumor spezifisch für das MRT-Kontrastmittel anzuzielen, wurden aktive und passive Targeting-Strategien verwendet [2, 23, 24]. Active Targeting [12] ist zu einem großen Schwerpunkt in der Krebsdiagnose geworden. Targeting-Liganden wie Aptamer [25], Peptid [8], Antikörper [6] und Folat [26] werden an makromolekulare und supramolekulare multimere Gd-Komplexe konjugiert, um an bestimmte Rezeptoren zu binden, die von Tumorzellen oder Gefäßen überexprimiert werden. Die Biokompatibilitäts- und Bioabbaubarkeitseigenschaften dieser makromolekularen und supramolekularen sind jedoch nicht klar und ihre nicht biologische Abbaubarkeit behindert die klinische Anwendung. Unsere Omn-NPs bestehen jedoch aus PEG, PCL, Gelatinase-Spaltungspeptid und Omn. PEG und PCL haben ausgezeichnete Biokompatibilitäts- und Bioabbaubarkeitseigenschaften, und Omn ist ein klinisch weit verbreitetes MRT-Kontrastmittel; Daher wird von unseren Omn-NPs eine ausgezeichnete biologische Sicherheit erwartet.
Die Modifikation des Polymers mit hydrophilem mPEG könnte die Blutzirkulation verlängern und die Akkumulation von NPs in Tumoren erhöhen. Die PEGylierung könnte die Serumproteinadhärenz reduzieren und eine Tarnoberfläche schaffen, um die Zirkulationszeit zu verlängern, indem die Aufnahme durch die retikuloendothelialen Systeme vermieden wird [12, 17]. Die Konzentration der eingekapselten Medikamente stieg spezifisch an den Tumorstellen an und es wurde eine signifikant verlängerte Dauer der Verstärkung in dieser Studie beobachtet. Daher war der Spitzenzeitpunkt der TBR viel später und die Bildgebungslatenzzeit war in der Omn-NPs-Gruppe viel länger als in der Omn-Gruppe.
Darüber hinaus minimieren eine verbesserte Spezifität und eine verlängerte Anreicherungsdauer die injizierte Dosis von Gadoliniumionen und reduzieren somit das Risiko einer nephrogenen systemischen Fibrose, ein Problem bei der Entwicklung von gadoliniumbasierten Kontrastmitteln [27, 28].
IHC-Färbung für MMP2 und MMP9
Die Ergebnisse der IHC-Färbung für MMP2 und MMP9 von Normalgeweben aus Organen und Tumorgeweben sind in Abb. 5 gezeigt. Die Ergebnisse zeigten, dass die Expressionsniveaus von MMP2 und MMP9 in Tumorgeweben (++) betrugen, während in den meisten Normalgeweben waren (− ). In den Tumorgeweben waren Zellplasma und extrazelluläre Matrix sichtbar braun gefärbt, was auf eine höhere MMP2/9-Expression hinweist.
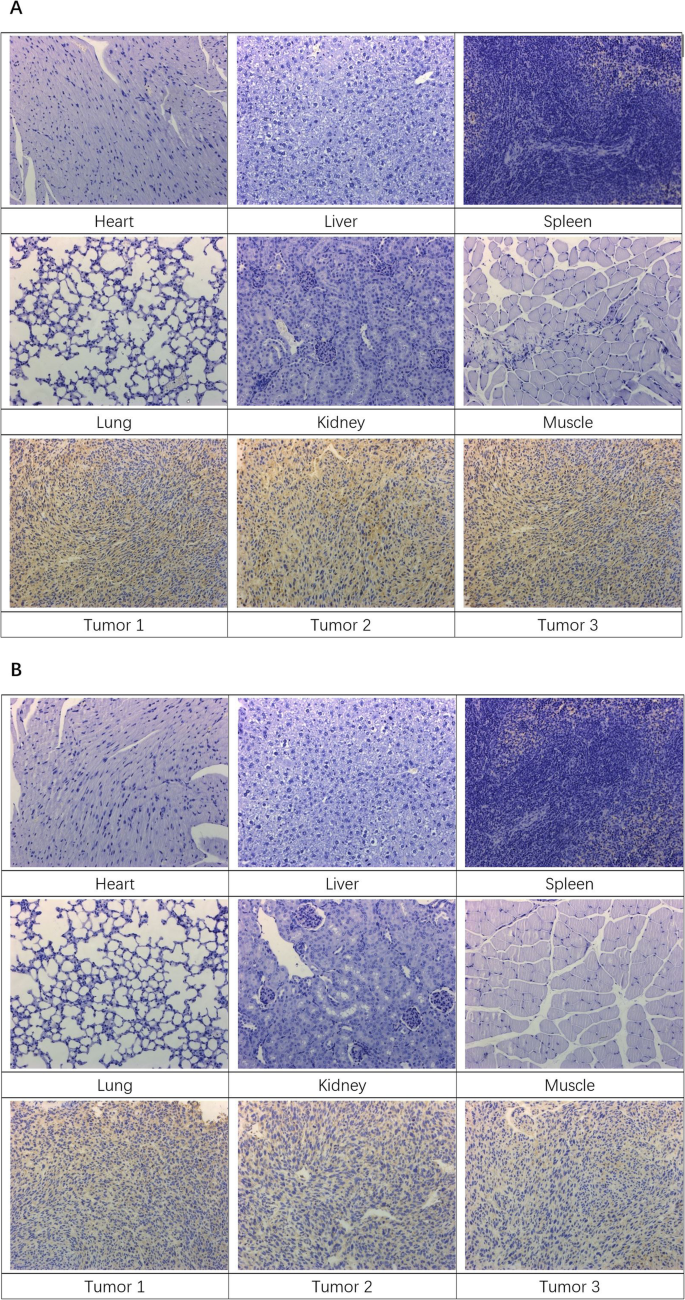
a , b IHC-Färbung für MMP2 und MMP9 in Normal- und Tumorgewebe von Xenotransplantat-Mäusen Modell von humanen oralen Plattenepithelkarzinomlinien
Die Matrix-Metalloproteinase (MMP)-Familie spielt eine Schlüsselrolle bei der Krebsinvasion und -metastasierung, MMP2/9, die auch als Kollagenasen IV und Gelatinasen A/B bekannt sind, gelten als die wichtigsten krebsbezogenen MMPs. Studien haben eine Korrelation zwischen der Expression von Gelatinasen und schlechten Ergebnissen vieler Tumoren, einschließlich OSCC, gezeigt [29, 30]. Die hohe Expression von MMP2/9 wurde auch in unserer Studie beobachtet. Aufgrund ihrer weit verbreiteten Expression und ihrer engen Verwandtschaft mit Krebs sind die MMPs zweifellos wichtige Anti-Krebs-Targets. Daher konnten unsere Omn-NPs bei fast allen Tumoren eingesetzt werden. Seine Einfachheit und Universalität hat ein gutes klinisches Anwendungspotenzial.
Schlussfolgerungen
In dieser Studie entwarfen und synthetisierten wir ein neuartiges MRT-Kontrastmittel-Verabreichungssystem, das auf Tumoren ausgerichtet ist, um Defekte der derzeit in der Klinik verwendeten Kontrastmittel auszugleichen. Das höhere MRT-T1-Tumor-zu-Hintergrund-Verhältnis und die verlängerte Blutzirkulationszeit wurden für Omn-NPs als für Omn im OSCC-Mäusemodell gefunden. Diese Studie zeigt, dass Omn-NPs als tumorspezifisches MRT-Kontrastmittel vielversprechend sind, um die Spezifität zu verbessern und die Zirkulationszeit im Tumorgewebe zu verlängern. In Anbetracht der hervorragenden Biokompatibilität und biologischen Abbaubarkeit von PEG und PCL und der Tatsache, dass Omn ein klinisch weit verbreitetes MRT-Kontrastmittel ist, hat dieses tumorspezifische MRT-Kontrastmittelabgabesystem ein gutes klinisches Anwendungspotenzial. Darüber hinaus werden weitere Anstrengungen unternommen, um den Wirkstoffgehalt und die Verkapselungseffizienz von Omn in unseren NPs für eine bessere Empfindlichkeit zu erhöhen.
Verfügbarkeit von Daten und Materialien
Die Daten, die die Ergebnisse dieser Studie stützen, sind auf Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- NPs:
-
Nanopartikel
- Omn:
-
Omniscan
- OSCC:
-
Plattenepithelkarzinom der Mundhöhle
- MMP:
-
Matrix-Metalloproteinase
- Gd:
-
Gadolinium
- mPEG:
-
Methoxy-poly(ethylenglycol)
- PCL:
-
Poly (ε-caprolacton)
- Pep:
-
Peptid
- Omn-NPs:
-
Omniscan-beladene mPEG-Pep-PCL-NPs
- Con-Omn-NPs:
-
Omniscan-beladene mPEG-PCL-NPs
- MRT:
-
Magnetresonanztomographie
- EPR:
-
Verbesserte Durchlässigkeit und Retention
- DCM:
-
Dichlormethan
- PVA:
-
Polyvinylalkohol
- DLS:
-
Dynamische Lichtstreuung
- PDI:
-
Polydispersitätsindex
- TEM:
-
Transmissionselektronenmikroskop
- ICP-AES:
-
Induktiv gekoppelte Plasma-Atomemissionsspektrometrie
- DMEM:
-
Dulbecco's modifiziertes Eagle's Medium
- FBS:
-
Fötales Rinderserum
- IHC:
-
Immunhistochemisch
- PBS:
-
Phosphatgepufferte Kochsalzlösung
Nanomaterialien
- In-vitro-Studie zum Einfluss von Au-Nanopartikeln auf HT29- und SPEV-Zelllinien
- Silica-Nanopartikel für die intrazelluläre Proteinzufuhr:ein neuartiger Syntheseansatz unter Verwendung von grün fluoreszierendem Protein
- Förderung des SH-SY5Y-Zellwachstums durch Goldnanopartikel, die mit 6-Mercaptopurin und einem Neuronen-penetrierenden Peptid modifiziert sind
- Nah-Infrarot-emittierende Cr3+/Eu3+ codotierte Zink-Gallogermanat-Persistenz-lumineszierende Nanopartikel für die Zellbildgebung
- Wirkung des sauren Peptisierungsmittels auf das Anatas-Rutil-Verhältnis und die photokatalytische Leistung von TiO2-Nanopartikeln
- Graphenoxid-basierte Nanokomposite, dekoriert mit Silbernanopartikeln als antibakterielles Mittel
- Artesunat-beladene und Nahinfrarot-farbstoffkonjugierte Albumin-Nanopartikel als hocheffizienter, auf Tumoren ausgerichteter photochemo-theranostischer Wirkstoff
- Der Apoptose-Effekt von mit Lithocholsäure modifizierten Goldnanopartikeln auf Leberkrebszellen
- Autophagie-Inhibitor (LY294002) und 5-Fluorouracil (5-FU) Kombinations-basiertes Nanoliposom für verbesserte Wirksamkeit gegen Plattenepithelkarzinom des Ösophagus
- Ein neuartiges Kontrastmittel auf Basis magnetischer Nanopartikel für den Cholesterinnachweis als Alzheimer-Biomarker



