Funktionelles poröses Polymer auf Triphenylphosphin-Basis als effizienter heterogener Katalysator für die Synthese cyclischer Carbonate aus CO2
Zusammenfassung
Durch Friedel-Crafts-Alkylierung von Triphenylphosphin und α-Dibrom-p . wurde ein neuartiges poröses Polymer auf Triphenylphosphin-Basis (TPDB) mit einer großen Brunauer-Emmett-Teller (BET)-Oberfläche synthetisiert -Xylol. Anschließend wurden die funktionellen Hydroxylgruppen durch Nachmodifizierung von TPDB mit 3-Brom-1-propanol (BP) und Triethanolamin (TEA) erfolgreich auf das Polymergerüst aufgepfropft. Die resultierende Probe TPDB-BP-TEA wurde durch verschiedene Techniken wie FT-IR, TG, SEM, EDS-Mapping, ICP-MS und N2 . charakterisiert Adsorption – Desorption. Dieses neue Polymer wurde als Katalysator in der lösungsmittelfreien Cycloadditionsreaktion von CO2 . getestet mit Epoxiden, die eine hervorragende Leistung mit hoher Ausbeute, Selektivität und stabiler Recyclingfähigkeit für mehrere Katalysezyklen zeigten. Die Ergebnisse des Vergleichsexperiments zeigen, dass die Bromidionen und Hydroxylgruppen sowie die große Oberfläche Schlüsselfaktoren für die Verbesserung der katalytischen Aktivität dieses neuen Katalysators sind.
Hintergrund
Ionische Flüssigkeiten (ILs) haben aufgrund ihrer spezifischen Eigenschaften wie vernachlässigbare Flüchtigkeit, ausgezeichnete thermische Stabilität, bemerkenswerte Löslichkeit und die Vielfalt der Strukturen große Aufmerksamkeit als alternative Reaktionsmedien/Katalysatoren auf sich gezogen [1,2,3]. Insbesondere könnten ILs mit verschiedenen funktionellen Gruppen in ihren Kationen oder Anionen entworfen und modifiziert werden, um die für Zielreaktionen erforderlichen Funktionalitäten zu erhalten [4, 5]. Es wurde über viele IL-katalysierte organische Reaktionen berichtet, unter denen Cycloadditionen ein heißes Thema sind [6, 7]. Da Kohlendioxid (CO2 ) eine potenziell reichlich vorhandene, billige, ungiftige, nicht brennbare und erneuerbare Kohlenstoffressource in der organischen Synthese ist, wurden große Anstrengungen unternommen, um wirksame Verfahren für CO2 . zu entwickeln chemische Fixierung. Vor kurzem wurde die Cycloaddition von CO2 mit Epoxiden zur Synthese wertvoller cyclischer Carbonate gilt als eine der vielversprechendsten Strategien zur effektiven Fixierung von CO2 [8,9,10,11]. Die Produkte cyclische Carbonate haben umfangreiche Anwendungen als aprotische Lösungsmittel, Vorstufen, Kraftstoffadditive und grüne Reagenzien gefunden. Obwohl sich ILs als ausgezeichnete Katalysatoren für die Cycloaddition von CO2 . erwiesen haben Unter metallfreien/lösemittelfreien Bedingungen litten diese homogenen Katalysatoren unweigerlich unter einigen Problemen der Katalysatorrückgewinnung und Produktreinigung.
Die porösen Materialien mit großer Oberfläche eröffnen neue Möglichkeiten für das Design und die Synthese neuer heterogener Katalysatoren [12,13,14]. In den letzten Jahrzehnten wurden neben traditionellen porösen Zeolithen und Aktivkohle eine Reihe nützlicher poröser Materialien wie metallorganische Gerüste (MOFs) [15, 16], kovalente organische Gerüste (COFs) [17, 18] und poröse organische Polymere [19, 20] wurden entwickelt und als Katalysatorträger für die heterogene Katalyse eingesetzt. Unter diesen porösen Materialien haben IL-haltige poröse organische Polymere aufgrund ihrer geringen Gerüstdichte, ihrer hohen chemischen Stabilität und der Fähigkeit, eine breite Palette nützlicher funktioneller Gruppen in das poröse Gerüst einzuführen, besondere Aufmerksamkeit auf sich gezogen [21,22,23]. Zum Beispiel haben He et al. haben eine Reihe neuartiger heterogener Katalysatoren durch Immobilisierung von Imidazolium-basierten ILs auf einem mesoporösen Polymer vom FDU-Typ entwickelt, die eine gute katalytische Aktivität im CO2 . zeigen Cycloadditionsreaktion [24]. Jedoch leidet das mehrstufige IL-Modifikationsverfahren unweigerlich unter der geringen IL-Beladungsmenge und der inhomogenen Verteilung der ILs. Neben der Post-Modifikationsstrategie ist die direkte Synthese von IL-haltigen Polymeren durch radikalische Polymerisation ein alternativer Ansatz. Wang und Mitarbeiter berichteten beispielsweise über eine templatfreie radikalische Selbstpolymerisationsmethode zur Synthese einer mesoporösen hierarchischen poly(ionischen Flüssigkeit)s [25]. Die erhaltenen Poly(ionischen Flüssigkeiten) weisen eine hohe Aktivität, einfaches Recycling und Wiederverwendung bei der Cycloaddition von CO2 . auf . Obwohl verschiedene ionische Polymere mit zahlreichen funktionellen Spezies erhalten werden können, machen die hohe BET-Oberfläche und die hohe IL-Beladungsmenge immer noch nicht gleichzeitig diese Copolymerisationstechnik peinlich. Daher ist der Einbau von IL-Gruppen in poröse organische Polymergerüste mit einem hohen stabilen Gehalt und einer großen Oberfläche immer noch eine große Herausforderung.
In diesem Artikel berichteten wir über die Synthese eines ionischen porösen Polymers auf Triphenylphosphin-Basis mit großer Oberfläche, großem Porenvolumen und reichlich Bromidionen und Hydroxylgruppen für die Cycloaddition von CO2 mit Epoxiden. Zuerst Triphenylphosphin (PPh3 ) und α-Dibrom-p -Xylol (DB) wurden durch Friedel-Crafts-Alkylierung mit wasserfreiem FeCl3 . zu einem porösen Polymer (TPDB) umgesetzt als Förderer. Dann kann die TPDB leicht mit 3-Brom-1-propanol (BP) bzw. Triethanolamin (TEA) funktionalisiert werden, um ein funktionelles poröses Polymer (TPDB-BP-TEA) zu liefern. TPDB-BP-TEA wurde durch den Einsatz von FTIR, TG, SEM, EDS-Mapping, ICP-MS und N2 . charakterisiert Adsorption – Desorption. Systematische katalytische Tests zeigen, dass das poröse Polymer ein ausgezeichneter Katalysator für die Cycloaddition von CO2 . ist zu Epoxiden, mit den Vorteilen hoher Aktivität und Selektivität, einfacher Rückgewinnung und stetiger Wiederverwendung.
Experimentell
Materialien und Methoden
Alle Chemikalien waren von chemischer Qualität und wurden wie gekauft verwendet. Die Thermogravimetrie (TG)-Analyse wurde mit einem STA409-Instrument bei einer Heizrate von 10 K/min in Stickstoff durchgeführt. Fourier-Transformations-Infrarot-Spektren (FT-IR) wurden auf einem Agilent Cary 660 FT-IR-Spektrometer im Bereich 4000–400 cm −1 . aufgenommen Region mit den getesteten Proben in KBr-Scheiben gepresst. Rasterelektronenmikroskopie-(SEM)-Bilder wurden auf einem SUPERSCAN SSX-550-Elektronenmikroskop (Shimadz, Japan), das bei 20 kV betrieben wurde, aufgenommen. Die Elementverteilung von Phosphor (P), Sauerstoff (O) und Stickstoff (N) wurde durch ein Hitachi S-4800-Feldemissions-Rasterelektronenmikroskop, begleitet von energiedispersiver Röntgenspektrometrie, charakterisiert. Das BELSORP-MINI-Instrument wurde verwendet, um die Stickstoffsorptionsisothermen bei der Temperatur von flüssigem Stickstoff (77 K) zu messen. Die spezifischen Oberflächen wurden mit der Brunauer-Emmett-Teller (BET)-Methode bestimmt und die Porenverteilung wurde mit der BJH-Methode aus Adsorptionszweigen von Isothermen berechnet. Der Gehalt an P-Element wurde durch ICP-MS unter Verwendung des Agilent 7700-Spektrometers bestimmt. Die CHN-Elementaranalyse wurde auf einem Elementaranalysator Vario EL cube durchgeführt.
Katalysatorvorbereitung
Synthese von TPDB
TPDB wurde nach der bisherigen Literatur [26] hergestellt. PPh3 (4 mmol, 1,05 g) und α-Dibrom-p -Xylol (DB, 4 mmol, 1,06 g) wurden in 20 ml 1,2-Dichlorethan (DCE) gelöst. Dann wasserfreies FeCl3 (16 mmol, 2,59 g) wurde in die obige Lösung gegeben, um die Alkylierung zwischen PPh3 . zu katalysieren und DB. Das Reaktionsgemisch wurde zunächst 5 h bei 45°C gerührt und dann weitere 48 h bei 80°C umgesetzt. Nach Abschluss wurde das resultierende braune Gel abfiltriert und mit DCE bzw. Methanol 24 h lang mit Soxhlet extrahiert. Das vernetzte Polymer TPDB wurde nach dem Trocknen bei 60 °C unter Vakuumbedingungen erhalten.
Synthese von TPDB-BP
Das erhaltene Polymer TPDB (1 g) wurde in 15 ml Acetonitril dispergiert und 3-Brom-1-propanol (BP, 0,8 g) wurde in die Lösung gegeben. Das Reaktionsgemisch wurde 24 h bei 80 °C umgesetzt. Das feste Produkt TPDB-BP wurde filtriert, dreimal mit Acetonitril gewaschen und bei 60 °C unter Vakuumbedingungen getrocknet.
Synthese von TPDB-BP-TEA
TPDB-BP (1 g) wurde in 15 ml Aceton dispergiert und dann wurde Triethanolamin (TEA, 0,8 g) dazugegeben. Das Reaktionsgemisch wurde 24 h bei 60 °C umgesetzt. Nach Abschluss wurde das feste Produkt TPDB-BP-TEA filtriert und dreimal mit Aceton gewaschen, gefolgt von 12 h Trocknen im Vakuum bei 60 °C. Das Ergebnis der ICP-MS-Analyse offenbarte 3,7 Gew.-% des P-Elements in TPDB. CHN-Elementaranalyse-Ergebnisse (Gew.-%) C 64,91 %, H 5,54% und N 1,65%.
Katalytischer Test
Die Cycloadditionsreaktion wurde in einem Edelstahl-Autoklavenreaktor (25 ml) mit einem Magnetrührer durchgeführt. In einem typischen Versuch wurden Propylenoxid (PO, 20 mmol) und der Katalysator TPDB-BP-TEA (0,1 g) in den Autoklavenreaktor gegeben. CO2 wurde dann auf 1 MPa geladen und die Reaktionstemperatur wurde auf 120 °C eingestellt. Die Reaktionsmischung wurde 6 h lang umgesetzt, danach wurde der Reaktor auf Umgebungstemperatur abgekühlt und Ethylalkohol wurde dazugegeben, um die Reaktionsmischung zu verdünnen. Der feste Katalysator wurde abfiltriert und das Filtrat wurde durch Gaschromatographie (GC) unter Verwendung von Biphenyl als internem Standard analysiert, um die Ausbeute zu berechnen. GC war mit einem FID und einer DB-Wachs-Kapillarsäule (SE-54 30 m × 0,32 mm × 0,25 μm) ausgestattet. Die GC-Spektren sind in Zusatzdatei 1 dargestellt:Abbildungen S1–S5.
Ergebnisse und Diskussion
Synthese und Charakterisierung von Katalysatoren
Gemäß dem in Schema 1 veranschaulichten Syntheseverfahren wurde ein poröses organisches Polymer TPDB durch Friedel-Crafts-Alkylierung von PPh3 . hergestellt durch Verwendung von DB als Crosslinker und FeCl3 als Förderer. TPDB wurde dann mit BP funktionalisiert, was das funktionalisierte Polymer TPDB-BP lieferte. Eine weitere Modifikation von TPDB-BP mit TEA ergab das resultierende TPDB-BP-TEA, das gründlich durch TG, FT-IR, SEM, EDX und N2 . charakterisiert wurde Adsorptions-/Desorptionsanalyse. TPDB erwies sich als stabil bis ca. 300 °C, wie durch TG belegt (Abb. 1, Kurve a). Nach der Modifikation mit BP und TEA nahm die Thermostabilität der erhaltenen Proben TPDB-BP und TPDB-BP-TEA leicht auf 250 °C ab (Abb. 1, Kurven b und c). Das Ergebnis der ICP-MS-Analyse ergab 3,7 Gew.-% des P-Elements in TPDB-BP-TEA, und die CHN-Elementaranalyse zeigt C 64,91 Gew.-%, H 5,54 Gew.-% und N 1,65 Gew.-% für TPDB-BP-TEA.
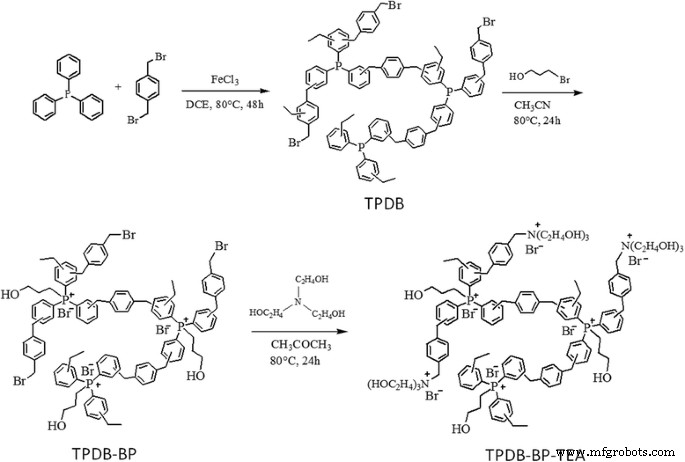
Synthese des porösen organischen Polymers TPDB-BP-TEA. Zuerst Triphenylphosphin (PPh3 ) und α-Dibrom-p -Xylol (DB) wurden durch Friedel-Crafts-Alkylierung mit wasserfreiem FeCl3 . zu einem porösen Polymer (TPDB) umgesetzt als Förderer. Anschließend kann die TPDB leicht mit 3-Brom-1-propanol (BP) und Triethanolamin (TEA) funktionalisiert werden, um ein funktionelles poröses Polymer (TPDB-BP-TEA) zu liefern
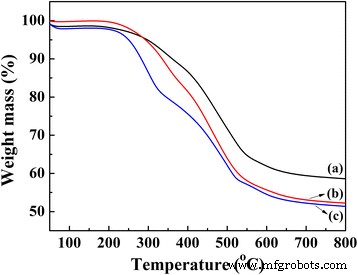
TG-Kurven von (a) TPDB, ( b) TPDB-BP und ( c) TPDB-BP-TEA. TPDB erwies sich als stabil bis 300 °C, wie durch TG belegt (Kurve a). Nach der Modifizierung mit BP und TEA verringerte sich die Thermostabilität der erhaltenen Proben TPDB-BP und TPDB-BP-TEA leicht auf 250 °C
Abbildung 2 zeigt die FT-IR-Spektren des TPDB-Polymers und nach seiner schrittweisen Modifikation. Die unterschiedlichen Banden entsprechend dem P–C=C (1674 cm −1 ) in PPh3 und aromatische Ringdehnungsschwingungen (1603–1438 cm −1 ) sowie zu den Streckschwingungen von C‐H im aromatischen Ring (916, 880, 745, 720 und 690 cm −1 ) sind im FT-IR-Spektrum von TPDB vorhanden, was auf das Vorhandensein von sowohl PPh3 und DB-Gruppen. Nach der Modifikation von BP sind die beobachteten Banden ähnlich. TPDB-PA zeigt jedoch eine breite Absorptionsbande mittlerer Intensität bei 3378 cm −1 , was der Streckschwingung des –OH entspricht. Nachdem TPDB-BP durch TEA weiter modifiziert wurde, war die Intensität der –OH-Vibration bei 3351 cm −1 für TPDB-BP-TEA signifikant erhöht, was wahrscheinlich auf den Einfluss der reichlich vorhandenen organischen Gruppen (−N(CH2CH2OH)3 ). Außerdem erschienen die neuen Bänder bei 1062 und 1030 cm −1 werden den Streckschwingungen von C–N bzw. C–O in TEA zugeordnet. Die breiten XPS-Spektren in Abb. 3 zeigen das Vorhandensein von P-, C-, N-, Br- und O-Elementen auf TPDB-BP-TEA an. Diese Beobachtungen legen nahe, dass die BP- und TEA-Gruppen erfolgreich auf das Gerüst von TPDB aufgepfropft wurden.
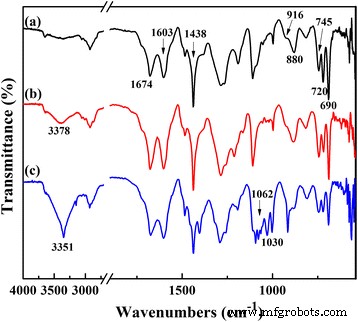
FT-IR-Spektren von (a) TPDB, (b) TPDB-BP und (c) TPDB-BP-TEA. Die unterschiedlichen Banden entsprechend dem P–C=C (1674 cm −1 ) in PPh3 und aromatische Ringdehnungsschwingungen (1603–1438 cm −1 ) sowie zu den Streckschwingungen von C‐H im aromatischen Ring (916, 880, 745, 720 und 690 cm −1 ) zeigt das Vorhandensein von PPh3 . an und DB-Gruppen in TPDB. TPDB-PA zeigt eine breite Absorptionsbande mittlerer Intensität bei 3378 cm −1 , was der Streckschwingung des –OH entspricht. Nach weiterer Modifikation durch TEA, die Intensität der –OH-Vibration bei 3351 cm −1 für TPDB-BP-TEA signifikant erhöht. Außerdem erschienen die neuen Bänder bei 1062 und 1030 cm −1 werden den Streckschwingungen von C–N bzw. C–O in TEA zugeordnet
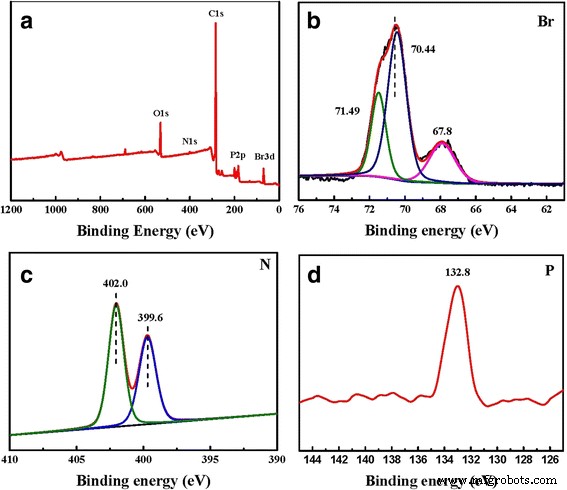
a Breites XPS-Spektrum, b Br-Spektrum, c N-Spektrum und d P-Spektrum von TPDB-BP-TEA. Die breiten XPS-Spektren in Abb. 3 zeigen die Anwesenheit von P-, C-, N-, Br- und O-Elementen auf TPDB-BP-TEA
Die Proben wurden weiter durch SEM- und EDS-Kartierung charakterisiert (Abb. 4). TPDB zeigt eine amorphe Morphologie (Abb. 4a). Wenn das BP an das TPDB-Gerüst angebunden wurde, weist TPDB-BP auch die amorphe Morphologie mit nanoskaliger Hohlstruktur auf (Abb. 4b). Nach der weiteren Modifizierung mit TEA zeigt TPDB-BP-TEA keine wesentlichen Veränderungen in der Struktur, aber seine Oberfläche wurde mit einigen agglomerierten Blöcken rauh (Abb. 4c). Das EDS-Mapping-Bild bestätigt die homogene Verteilung der P- und Br-Elemente im Polymergerüst von TPDB (Abb. 4d, e). Die Br-Menge nahm offensichtlich zu (Abb. 4f) und ein neues Element O wurde nach der Modifizierung von TPDB mit BP beobachtet (Abb. 4g). Nach der weiteren Modifikation von TPDB-BP mit TEA wurde ein neues Element N beobachtet (Abb. 4i), und die Menge des O-Elements stieg im Bild von TPDB-BP-TEA signifikant an (Abb. 4h). Diese Bilder bestätigen die erfolgreiche Immobilisierung von BP und TEA auf dem TPDB-Framework, die mit der FT-IR-Analyse übereinstimmte.
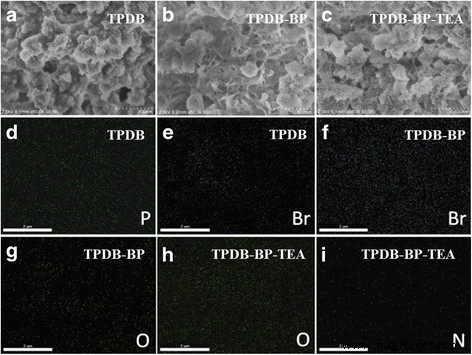
SEM- und EDS-Mapping-Bilder von a , d , und e TPDB, b , f , und g TPDB-BP und c , h , und i TPDB-BP-TEA. TPDB, TPDB-BO und TPDB-BP-TEA zeigen alle eine amorphe Morphologie (a ). Nach der Modifikation mit BP und TEA zeigt TPDB-BP-TEA keine wesentlichen Veränderungen in der Struktur, aber seine Oberfläche wurde mit einigen agglomerierten Blöcken rau (c ). EDS-Mapping-Bild validiert die homogene Verteilung der P- und Br-Elemente im Polymergerüst von TPDB (d , e ). Die Menge an Br hat sich offensichtlich erhöht (f ) und ein neues Element O wurde beobachtet (g ) nach der Modifikation von TPDB mit BP. Nach der weiteren Modifikation von TPDB-BP mit TEA wurde ein neues Element N beobachtet (i ), und die Menge an O-Element stieg im Bild von TPDB-BP-TEA signifikant an (h ). Diese Bilder bestätigen die erfolgreiche Immobilisierung von BP und TEA auf dem TPDB-Framework
BET-Oberflächen und Porengrößenverteilungen der Polymere TPDB und TPDB-BP-TEA wurden durch Analyse von N2 . gemessen Adsorptions- und Desorptionsisothermen bei 77 K. Wie in Abb. 5 gezeigt, zeigen TPDB und TPDB-BP-TEA eine anfänglich hohe Aufnahme, gefolgt von einem allmählichen Anstieg der Stickstoffadsorption und dem steilen Anstieg des hohen P/P 0 Region zeigt an, dass das Material aus Mikroporen und Mesoporen besteht. TPDB bietet eine hohe BET-Oberfläche von 493,15 m 2 /g, Porenvolumen von 0,54 cm 3 /g und eine durchschnittliche Porengröße von 4,38 nm. Nach der zweistufigen Modifikation verringerten sich die BET-Oberfläche und das Porenvolumen auf 227,12 m 2 /g und 0,41 cm 3 /g bzw. Die Abnahme von Oberfläche und Porengröße war wahrscheinlich darauf zurückzuführen, dass der Modifikationsprozess zu einem leichten Verlust der Porenwirksamkeit geführt hat, während die integrale Porenstruktur des Katalysators unverändert bleibt.
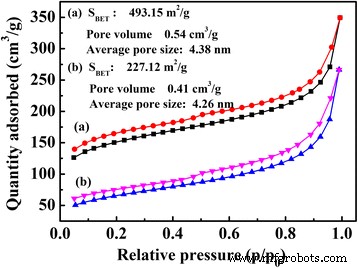
Stickstoffadsorptions-Desorptions-Isothermen von (a) TPDB und (b) TPDB-BP-TEA. BET-Oberflächen und Porengrößenverteilungen der Polymere TPDB und TPDB-BP-TEA wurden durch Analyse von N2 . gemessen Adsorptions- und Desorptionsisothermen bei 77 K. Der steile Anstieg des hohen P/P0 Region zeigt an, dass das Material aus Mikroporen und Mesoporen besteht. TPDB bietet eine hohe BET-Oberfläche von 493,15 m 2 /g, Porenvolumen von 0,54 cm 3 /g und eine durchschnittliche Porengröße von 4,38 nm. Nach der zweistufigen Modifikation verringerten sich die BET-Oberfläche und das Porenvolumen auf 227,12 m 2 /g und 0,41 cm 3 /g bzw.
katalytische Leistung von Katalysatoren
Die katalytische Leistung aller Proben wurde zuerst bewertet, indem die Cycloaddition von CO2 . durchgeführt wurde und PO unter milden Bedingungen ohne die Hilfe von Metallen, Lösungsmitteln und externen homogenen Cokatalysatoren, und die Ergebnisse sind in Tabelle 1 gezeigt. Anfänglich wurde kein cyclisches Carbonatprodukt ohne Verwendung eines Katalysators nachgewiesen (Eintrag 1). Bei Verwendung von TPDB als Katalysator wurde eine Ausbeute von 44% an cyclischem Carbonat mit einer geringen Selektivität von 59% beobachtet und 1,2-Propandiol wird als Hauptnebenprodukt gebildet (Nr. 2). TPDB-BP zeigte eine leicht erhöhte Ausbeute von 51% bei 93% Selektivität (Eintrag 3). Interessanterweise bot TPDB-BP-TEA nach der weiteren Modifizierung mit TEA eine sehr hohe Ausbeute von 97% bei 100% Selektivität (Eintrag 4). In der Literatur ist bekannt, dass Br-Anionen als die wichtigsten aktiven Zentren für Cycloadditionsreaktionen wirken [27,28,29,30]. Darüber hinaus könnte das Vorhandensein von –OH-Gruppen an festen Materialien die Ringöffnung von Epoxiden aufgrund von Wasserstoffbrückenbindungen effizient fördern [31,32,33]. Daher hängt die hervorragende Leistung von TPDB-BP-TEA vernünftigerweise mit seinen reichlich vorhandenen Br-Anionen und -OH-Gruppen zusammen, wie die EDS-Kartierung in Abb. 4f nahelegt. Darüber hinaus können die große Oberfläche und die poröse Struktur des Katalysators im Prinzip den Massen- und Energietransfer an der Grenzfläche beschleunigen.
Der Einfluss der Reaktionsparameter, wie zum Beispiel anfängliches CO2 Druck, Reaktionszeit und Temperatur wurde unter Verwendung von TPDB-BP-TEA als Katalysator untersucht, und die Ergebnisse sind in Abb. 6 zusammengefasst. Die Ausbeute stieg bemerkenswert von 58 auf 97 %, wenn CO2 Der Druck wurde von 0,6 auf 1,0 MPa erhöht und danach wurde die Ausbeute konstant gehalten. Die katalytische Reaktion endete in 4 h, während eine längere Reaktionszeit zu einer leichten Abnahme der Ausbeute führte. Dies ist möglicherweise auf Nebenreaktionen wie die Polymerisation von PC zurückzuführen. Darüber hinaus war in dieser Studie eine Reaktionstemperatur von 120 °C für die Synthese von cyclischem Carbonat optimal. Abgesehen von PO zeigt TPDB-BP-TEA eine hocheffiziente Aktivität für die Cycloaddition verschiedener Epoxide (Tabelle 2), einschließlich Epichlorhydrin, Allylglycidylether und Styroloxid (GC-Spektren sind in Zusatzdatei 1 gezeigt:Abbildungen S1–S5). Als sehr anspruchsvolle Substrate für diese Reaktion erfordern interne Epoxide drastische Bedingungen für eine effiziente Umwandlung, da die „scheinbare“ größenselektive Katalyse in porösen heterogenen Systemen offensichtlich ist [34,35,36]. Hier zeigt Cyclohexenoxid eine relativ niedrige Ausbeute von 74 % mit 59 % Selektivität gegenüber porösem TPDB-BP-TEA-Katalysator, was wahrscheinlich an der inhärenten Inertheit von Cyclohexenoxid liegt.
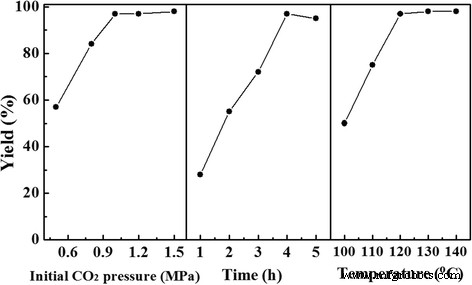
Einfluss von Reaktionsparametern auf die Cycloadditionsreaktion von CO2 mit Propylenoxid. Die Ausbeute stieg bemerkenswert von 58 auf 97 %, wenn die CO2 Der Druck wurde von 0,6 auf 1,0 MPa erhöht und danach wurde die Ausbeute konstant gehalten. Die katalytische Reaktion endete in 4 h, während eine längere Reaktionszeit zu einer leichten Abnahme der Ausbeute führte. Dies ist möglicherweise auf Nebenreaktionen wie die Polymerisation von PC zurückzuführen. Die optimale Reaktionstemperatur war 120 °C
Wie in Fig. 7 dargestellt, wird TPDB-BP-TEA leicht durch Filtration oder Zentrifugation gewonnen und behält seine Aktivität im fünffachen Recyclingtest unter milden Bedingungen gut bei. Die Reaktionsbedingungen sind die gleichen wie in Tabelle 1. Um das Auslaugen des Katalysators zu überprüfen, wurde weiterhin ein Heißfiltrationsversuch durchgeführt. Nachdem der TPDB-BP-TEA-Katalysator nach 2 h aus der Reaktionslösung entfernt wurde (Ausbeute 59%), zeigte der Überstand in den nächsten 4 h keine weitere Reaktivität, was auf die heterogene Natur des vorliegenden Katalysators hinweist. ICP-MS- und CHN-Analysen für den recycelten Katalysator zeigen 3,84 Gew. % P, 67,72 Ge % C, 5,83 Ge % H und 1,52 Gew. % N, die dem frischen Katalysator sehr ähnlich sind. Das FT-IR-Spektrum des wiedergewonnenen Katalysators (Abb. 8) weist auf die gut erhaltenen Textureigenschaften im Vergleich zum frischen Katalysator hin, was seine gute Recyclingfähigkeit erklärt.
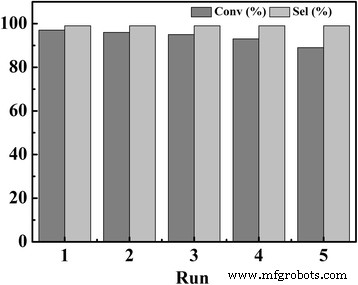
Katalytische Wiederverwendbarkeit von TPDB-BP-TEA für die Cycloaddition von CO2 mit PO. Als fester Katalysator wird TPDB-BP-TEA leicht durch Filtration oder Zentrifugation zurückgewonnen und behält seine Aktivität im fünffachen Recyclingtest unter milden Bedingungen gut.
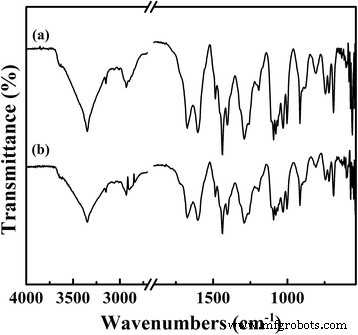
FT-IR-Spektren von (a) frischem TPDB-BP-TEA und (b) wiederverwendetem TPDB-BP-TEA. Das FT-IR-Spektrum des wiedergewonnenen Katalysators deutet auf die gut erhaltenen Textureigenschaften im Vergleich zum frischen hin, was seine gute Recyclingfähigkeit erklärt.
Schlussfolgerungen
Ein poröses organisches Polymer mit großer Oberfläche, hoher Dichte an ionischen Zentren und funktionellen –OH-Gruppen wird durch Friedel-Crafts-Alkylierung und Nachmodifizierungsreaktion entwickelt. Die resultierende Probe TPDB-BP-TEA könnte als hocheffizienter heterogener Katalysator für die Synthese cyclischer Carbonate durch Cycloaddition von CO2 . verwendet werden und Epoxide unter metall- und lösemittelfreien Bedingungen. An verschiedenen Substraten werden relativ hohe Ausbeuten und Selektivitäten erzielt, und der Katalysator kann leicht abgetrennt und mit sehr konstanter Aktivität wiederverwendet werden. Die zahlreichen Bromidionen und Hydroxylgruppen, die poröse Struktur und die große Oberfläche sind für die hervorragende Leistung des Katalysators bei der Cycloaddition von CO2 . verantwortlich . Der Ansatz in dieser Arbeit bietet einen idealen Weg für einen einfachen Zugang zu einer Reihe von porösen, funktionalisierbaren Polymeren, die nicht nur für die chemische Fixierung von CO2 . verwendet werden können in Feinchemikalien, ist aber auch vielversprechend für eine Vielzahl potenzieller katalytischer Anwendungen.
Nanomaterialien
- Die Entwicklung der 3D-Drucktechnologie von HP:Von Polymer zu Metall AM
- 6 Tipps zur optimalen Nutzung Ihres PM-Programms
- Foster ist jetzt exklusiver Distributor für SK Functional Polymer
- Grüne Eintopf-Synthese von Ag-dekorierten SnO2-Mikrosphären:ein effizienter und wiederverwendbarer Katalysator für die Reduktion von 4-Nitrophenol
- Ein hochempfindlicher elektrochemischer DNA-Biosensor aus Acryl-Gold-Nanokomposit zur Bestimmung des Geschlechts von Arowana-Fischen
- Nachbehandlungsmethode zur Synthese monodisperser binärer FePt-Fe3O4-Nanopartikel
- Entwicklung der Kontaktfläche bei Normallast für raue Oberflächen:von atomaren zu makroskopischen Skalen
- Kontrollierte Synthese von BaYF5:Er3+, Yb3+ mit unterschiedlicher Morphologie zur Verbesserung der Aufkonversionslumineszenz
- Was bringt 5G für das IoT/IIoT?
- Erwägen Sie die Umstellung von CO2 auf Stickstoff in Ihrer Brauerei?



