Funktionalisiertes Nanoadsorbens für die Affinitätstrennung von Proteinen
Zusammenfassung
Thiol-funktionalisierte Silica-Nanosphären (SiO2 -SH NS) mit einem durchschnittlichen Durchmesser von 460 nm wurden auf einem hydrothermalen Weg synthetisiert. Anschließend wird das vorbereitete SiO2 -SH NSs wurden durch SnO2 . modifiziert Quantenpunkte für SnO2 /SiO2 zusammengesetzte NSs mit offensichtlicher Fluoreszenz, die verwendet werden könnten, um das Zielprotein zu verfolgen. Das SnO2 /SiO2 NSs wurden durch reduziertes Glutathion (GSH) weiter modifiziert, um SnO2 . zu erhalten /SiO2 -GSH-NSs, die spezifisch Glutathion S . trennen können -Transferase-markiertes (GST-markiertes) Protein. Darüber hinaus wird die Peroxidaseaktivität von Glutathionperoxidase 3 (GPX3) von SnO2 . getrennt /SiO2 -GSH-NSs in vitro wurden evaluiert. Die Ergebnisse zeigen, dass das präparierte SnO2 /SiO2 -GSH-NSs weisen eine vernachlässigbare unspezifische Adsorption, eine hohe Konzentration an Proteinbindung (7,4 mg/g) und gute Wiederverwendungseigenschaften auf. In der Zwischenzeit kann das durch diese NSs getrennte GST-markierte GPX3 seinen Redoxzustand und seine Peroxidaseaktivität beibehalten. Daher ist das vorbereitete SnO2 /SiO2 -GSH-NSs könnten vielversprechende Anwendungen bei der schnellen Trennung und Reinigung von GST-markierten Proteinen finden.
Hintergrund
Die einfache Trennung und Reinigung von Proteinen ist sehr wichtig für die xenobiotische Biotransformation, den Arzneimittelstoffwechsel, die Biosynthese von Prostaglandinen und Steroidhormonen und den Abbau aromatischer Aminosäuren [1,2,3,4,5,6]. Die aufgetrennten Proteine können für die Antigen- und Impfstoffherstellung, molekulare Immunologie und strukturelle sowie biochemische und zellbiologische Studien verwendet werden. Glutathion S -Transferase (GST) stellt eine Hauptgruppe von Entgiftungs-Isoenzymen dar, die im GST-Genfusionssystem und im Arzneimittelwirkungs-Targeting-Feld oder als Tumormarker verwendet werden können [7, 8]. Zur Reinigung verschiedener Proteine stehen derzeit verschiedene Methoden wie Fällung, Chromatographie, Ultrafiltration und Dialyse zur Verfügung, wobei insbesondere die Affinitätstrennung auf Basis der natürlichen biologischen Affinität zwischen biologischen Makromolekülen und komplementären Liganden von außerordentlicher Bedeutung ist [9,10,11,12 ,13,14]. Die erfolgreiche Produktion und Reinigung von löslichen und natürlichen Fusionsproteinen voller Länge wird jedoch immer noch durch verschiedene Hindernisse wie die Notwendigkeit einer Vorbehandlung zur Entfernung der Zelltrümmer und kolloidalen Verunreinigungen, eine relativ lange Betriebszeit und die Proteinlöslichkeit verzögert. Diese Nachteile konnten glücklicherweise durch den Einsatz von Nanomaterialien überwunden werden, um die Trennung und Reinigung der Zielproteine zu unterstützen [15,16,17,18,19]. Zum Beispiel magnetisches SiO2 -NiO-Nanokomposit ist in der Lage, His-markierte Proteine zu trennen [20]. Nanomaterialien haben jedoch noch immer kurze Wege bei der Trennung verschiedener Proteine, da sie gegenüber Visualisierungs- und Fluoreszenztechniken, die als empfindliche biomolekulare und medizinische Diagnosewerkzeuge zur Bekämpfung der biologischen Kriegsführung verwendet werden können, oft inaktiv sind [21,22,23]. In diesem Sinne ist es zwingend erforderlich, Nanomaterialien mit Fluoreszenzreaktionen zu finden, um ihre Anwendung bei der Trennung und Reinigung von rekombinanten Proteinen wie Glutathionperoxidase 3 (GPX3) zu fördern.
Besonderes Augenmerk legen wir auf nanoskaliges SnO2 Quantenpunkte (QDs), weil SnO2 . als n-Typ-Halbleiter mit großer Bandlücke (3,6 eV) mit guter chemischer Stabilität und Biokompatibilität zeigt optische Extinktion im sichtbaren Spektralbereich. Hier etablieren wir einen intelligenten Weg zur Einführung von fluoreszierendem SnO2 QDs auf der Oberfläche von Silica-Nanosphären (NSs), in der Hoffnung, ein gewünschtes SnO2 . zu entwickeln /SiO2 Nanostruktur mit potenzieller Anwendung bei der Trennung und Reinigung von GST-markierten Proteinen. Erstens, Thiol-funktionalisierte Silica-Nanosphären (SiO2 -SH NS) wurden auf einem hydrothermalen Weg hergestellt. Resultierendes SiO2 -SH NSs wurden mit SnO2 . vermischt Quantenpunkte für SiO2 /SnO2 zusammengesetzte NS mit offensichtlicher Fluoreszenzabsorption. Das SiO2 /SnO2 NSs wurden durch reduziertes Glutathion (GSH) weiter modifiziert, um SiO2 . zu erhalten /SnO2 -GSH-NSs mit Potenzial für die Affinitätstrennung von GST-markiertem Protein. Die Fähigkeit und die Peroxidaseaktivität des hergestellten SnO2 /SiO2 -GSH-NSs bei der Trennung von GST-markierten Proteinen wurden durch SDS-PAGE-Analyse bewertet.
Experimentell
Material und Methoden
Hexadecyltrimethylammoniumbromid (CTAB), Zinn(IV)chlorid (SnCl4 .) ), Triethylamin (TEA) und Isopropanol wurden von Tianjin Kermel Chemicals Reagent Company (Tianjin, China) bereitgestellt. AgNO3 wurde von Tianjin Fuchen Technology Development Co., Ltd. (Tianjin, China) gekauft. 3-Mercaptopropyl-trimethoxysilan (MPS) wurde von Alfa-Aesar (Shanghai, China) angeboten. Tetraethylorthosilikat (TEOS) wurde von Tianjin Fuchen Chemicals (Tianjin, China) geliefert. Dihydronicotinamidadenindinukleotidphosphat (NADPH), Thioredoxin und Thioredoxinreduktase wurden von Sigma (Beijing, China) bezogen. Glutathion Sepharose 4B (Stockholm, USA) stammte von GE Healthcare. Dithiothreitol (DTT) war von Aladdin Industrial Corporation (Inalco SPA, Italien) erhältlich. Alle chemischen Reagenzien waren analytische Reagenzien und wurden ohne weitere Reinigung verwendet.
Vorbereitung von SnO2 Quantenpunkte
In einer typischen Synthese [24] werden 3,5 g SnCl4 ·5H2 O wurde zu 50 ml H2 . hinzugefügt 0, dann wurden 5 ml Ammoniak unter Rühren in die Lösung gegeben. Anschließend wurde der durch Zentrifugation erhaltene Niederschlag mehrere Male mit entionisiertem Wasser gewaschen, um das überschüssige Cl − . zu entfernen Ionen. Dreißig Milliliter entionisiertes Wasser wurden in den erhaltenen Niederschlag gegeben, und dann wurde der pH-Wert der Lösung mit 2 mol/l Ammoniak auf 12 eingestellt. Die gemischte Lösung wurde in einen mit Teflon ausgekleideten Edelstahlautoklaven überführt, verschlossen und 24 h auf 150°C erhitzt. Nach Beendigung des Erhitzens wurde die gemischte Lösung abgekühlt, zentrifugiert und vollständig mit Ethanol-Isopropanol (Volumenverhältnis 1:1) gewaschen, um SnO2 . zu erhalten QDs.
Vorbereitung von SnO2 /SiO2 -SH NS
Bei einer typischen Synthese 0,2 g SnO2 QDs und 0,09 g CTAB wurden in dem gemischten Lösungsmittel von H2 . gelöst O (42,5 ml) und absoluter Alkohol (7 ml) unter magnetischem Rühren (200 G, r .) = 180 mm). In die resultierende Lösung wurden 2,7 ml TEA unter zusätzlichem 20-minütigem Rühren gegeben. Die gemischte Lösung wurde 5 h auf 60 °C erhitzt, während 3,5 ml TEOS und 0,35 ml MPS langsam zugetropft wurden, gefolgt von einer Zentrifugation (12.800 G, r .). = 180 mm) und vollständig mit HCl-Ethanol (30 ml) und Wasser (30 ml) gewaschen, um SnO2 . zu erhalten /SiO2 -SH NS dreimal, die in Wasser dispergiert wurde (0,12 g/ml).
Oberflächenmodifikation von SnO2 /SiO2 -SH NS
Vier Milliliter 0,12 g/ml SnO2 /SiO2 -SH NSs wurde dreimal mit PBS (0,01 mol/l, pH = 7,4) gewaschen. Diese SnO2 /SiO2 -SH NSs wurden in 30 ml 16,7 mg/ml GSH-Lösung gegeben und bei 37 °C für 24 h (120 U/min) mit einem konstanten Temperaturoszillator oszilliert. Am Ende der Oszillation wurde die gemischte Lösung zentrifugiert, um SnO2 . bereitzustellen /SiO2 -GSH-NSs; dann wurde das Präzipitat dreimal vollständig mit 30 ml PBS (0,01 mol/l, pH = 7,4) gewaschen, um überschüssiges GSH durch physikalische Adsorption zu entfernen, wodurch das gewünschte SnO2 . erhalten wurde /SiO2 -GSH-NS. Das resultierende SnO2 /SiO2 -GSH-NSs wurden Alkohol hinzugefügt (25 %, v /v ) und bei 4 °C gelagert.
Trennung von GST-markierten Proteinen
Die gemischten Proteine wurden aus dem Zelllysat von Escherichia coli . gewonnen , das durch Wasserlyse erfolgt (Konzentration 0,01 mol/l, pH 7,4). Für die In-vitro-Proteinexpression die Proteinregion, die die kodierende Sequenz von Glutathionperoxidase 3 (GPX3, Aminosäuren 37–206), Offene Stomata 1 (OST1) und ABA-insensitiv 2 (ABI2, Aminosäuren 100–423) in Arabidopsis thaliana wurde kloniert und im Leseraster in das Plasmid pGEX-6p1 eingefügt (GPX3 wurde als Kontrolle verwendet). pGEX-GPX3-, pGEX-OST1- und pGEX-ABI2-Konstrukte wurden in E. coli BL21 (DE3) Zellen. Die rekombinanten GST-markierten Proteine wurden mit Glutathion Sepharose 4B und SnO2 . gereinigt /SiO2 -GSH-NS. Die zum Klonieren der Gene verwendeten Primer waren wie folgt:für GPX3 Vorwärtsprimer, 5'-GATGGATCTCGCCATCGACGGTGGAACAA-3'; reverser Primer, 5'-CACCTCGAGTCAAGCAGATGCCAATAGCTT-3'; für OST1, Vorwärtsprimer, 5'- GCCGAATTCATGGATCGACCAGCAGTGA-3'; reverser Primer, 5'-CCCCTCGACTCACATTGCGTACACAATC-3'; für ABI2 Vorwärtsprimer, 5'- GCGGAATTCGAGAGTAGAAGTCTGTTTG-3'; reverser Primer, 5′- GCGCTCGAGTCAATTCAAGGATTTGCTC-3′.
Nach dem Waschen mit PBS-Lösung (0,01 mol/L, pH = 7.4) wird das vorbereitete SnO2 /SiO2 -GSH-NSs wurden direkt in 1000 μL E eingebracht. coli Lysat und geschüttelt bei 4 °C für 2 h (Rotationsgeschwindigkeit:90 U/min), um das SnO2 /SiO2 -GSH-NSs zum Einfangen von GST-markierten Proteinen. Nach Beendigung des Schüttelns wurden diese NSs durch Zentrifugation aus der Lösung isoliert und vollständig mit PBS-Lösung gewaschen, um alle restlichen nicht eingefangenen Proteine zu entfernen. Das GST-markierte proteingebundene SnO2 /SiO2 -GSH-NSs wurden dreimal mit 300 μl und 0,5 mol/l GSH-Lösung gewaschen, um GST-markierte Proteine von ihrer Oberfläche zu trennen. Getrennt gesammelte Proteinlösungen wurden durch Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese (SDS-PAGE) nachgewiesen. Die Konzentration der aufgetrennten Proteine wurde mit dem BCA Protein Assay Kit bestimmt. Das SnO2 /SiO2 -GSH-NSs können mehrmals verwendet werden, um die Zielproteine mit derselben Methode zu trennen.
Messung der Glutathionperoxidase-Aktivität
Die abgetrennte GPX3-Aktivität wurde durch die spektrometrische Bestimmung des NADPH-Verbrauchs bei 340 nm gemessen, wie von Delaunay et al. [25]. Das GST-Tag wurde durch PreScission-Protease von GST-markiertem GPX3 abgeschnitten, und dann wurde das GPX3 für die Aktivitätsanalyse verwendet. Erstens 98 μl Reaktionspufferlösung (einschließlich 100 mmol/l Tris-Cl, 0,3 mmol/l NADPH, 1,34 μmol/l Thioredoxin und 0,18 μmol/l Thioredoxin-Reduktase aus E. coli Lysat) wurde in ein Röhrchen gegeben; nach vollständigem Mischen wurden 1,35 μmol gereinigtes GPX3 in die resultierende Reaktionspufferlösung gegeben. Dann wurde die gemischte Lösung in 2 μL H2 . gegeben O2 (5 mmol/L) zur Initiierung der Reaktion und der NADPH-Verbrauch bei 340 nm wurde durch spektrometrische Bestimmung erfasst.
Analyse der Redoxzustände von gereinigtem GPX3
Das GST-Tag wurde von GST-markiertem GPX3 durch PreScission-Protease abgeschnitten. Das abgetrennte GPX3 wurde mit 5 mmol/l H2 . behandelt O2 und 1 mmol/L DTT für 10 Minuten, um die Redoxzustände des gereinigten GPX3 zu ändern. Das resultierende GPX3 wurde für die in vitro-Analyse von Redoxzuständen verwendet. Extrakte wurden durch nicht reduzierendes 15% SDS-PAGE-Gel bewertet.
Charakterisierung
Die Morphologie und Zusammensetzung des hergestellten SnO2 /SiO2 -GSH-NSs wurden durch Transmissionselektronenmikroskopie (TEM, JEM-2010, Japan), Rasterelektronenmikroskopie (SEM, JSM 5600LV, Japan), Röntgenbeugung (XRD, X' Pert Philips, Holland) und Fluoreszenzspektrometer ( FL, FluoroSENS, Großbritannien, bei der Anregungswellenlänge von 260 nm). Die getrennten GST-markierten Proteine wurden mit Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese (SDS-PAGE, Power PAC 300, China) mit einer Vorkonzentrationsspannung von 70 V und einer Trennspannung von 120 V nachgewiesen. Der Oszillator mit konstanter Temperatur stammte von Shanghai ChemStar Instruments , Co., Ltd. (ATS-03M2R, China). Die Konzentration der aufgetrennten Proteine wurde mit dem BCA Protein Assay Kit (Beijing CoWin Biotech, China) bestimmt.
Ergebnisse und Diskussion
TEM-, SEM-, XRD- und Fluoreszenzanalysen von SnO2 QDs und SnO2 /SiO2 -GSH-NSs
Abbildung 1 zeigt die hochauflösenden TEM (HRTEM)-Bilder und das XRD-Muster des synthetisierten SnO2 QDs. Es ist ersichtlich, dass das synthetisierte SnO2 QDs sind kugelförmig und haben einen durchschnittlichen Durchmesser von 5 nm, was eine enge Partikelgrößenverteilung aufweist (Abb. 1a), und ihr Gitterabstand in der (110)-Ebene beträgt 0,29 nm (Abb. 1b). Das gut aufgelöste Gitterbild zeigt, dass das präparierte SnO2 QDs haben eine hochgeordnete kristalline Struktur. Entsprechendes ausgewähltes Bereichselektronenbeugungsmuster von SnO2 QDs (Abb. 1c) können auf eine einzelne Cassiterit-Phase indiziert werden, die mit dem relevanten XRD-Muster übereinstimmt (Abb. 1d). Die charakteristischen Peaks bei 2 Theta = 26,6° (110), 33,9° (101), 38,0° (200), 51,8° (211), 65,9° (301) und 78,7° (321) stimmen mit dem Standard überein XRD-Daten von Kassiterit SnO2 (JCPDS-Karte Nr. 41-1445). Außerdem weisen die intensiven XRD-Peaks darauf hin, dass das präparierte SnO2 QDs sind gut kristallisiert und das Fehlen anderer charakteristischer Peaks deutet darauf hin, dass sie keine Hämatit- oder Hydroxidverunreinigungen enthalten.
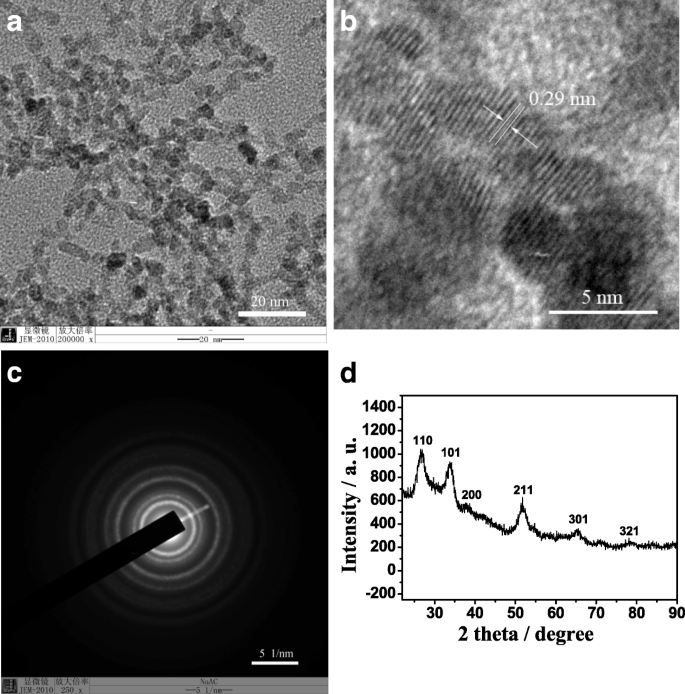
TEM (a ), HRTEM (b ) Bilder, ausgewähltes Bereichselektronenbeugungsmuster (c ) und XRD-Muster (d ) von präpariertem SnO2 QDs
Abbildung 2 zeigt die SEM- und TEM-Bilder von SnO2 /SiO2 -GSH-NS. Es ist ersichtlich, dass das präparierte SnO2 /SiO2 -GSH-NS sind kugelförmig und haben einen durchschnittlichen Durchmesser von etwa 430 nm, und ihre Oberfläche scheint etwas rau zu sein (Abb. 2a, b). Inzwischen ist zu erkennen, dass das SnO2 QDs (ca. 5–15 nm) werden auf der Oberfläche von SiO2 . modifiziert Mikrokügelchen (Abb. 2c, d), was mit den entsprechenden REM-Bildern übereinstimmt. Es wird angezeigt, dass das SnO2 und Siliciumdioxid-NSs wurden aggregiert.

SEM (a , b ) und TEM (c , d ) Bilder des präparierten SnO2 /SiO2 -GSH-NSs
Abbildung 3a zeigt das XRD-Muster des synthetisierten SnO2 /SiO2 -GSH-NS. Die Hauptpeaks bei 2 Theta = 110°, 101°, 200°, 211°, 301° und 321° stimmen mit denen von SnO2 . überein (Abb. 1d). Außerdem SnO2 /SiO2 -GSH-NSs zeigen einen intensiven charakteristischen Peak von amorphem Siliziumdioxid um 23° (JCPDS-Karte Nr. 76-0933), was darauf hindeutet, dass SnO2 mit sichtbarem Licht wurde erfolgreich auf der Oberfläche von SiO2 . eingeführt NS. Abbildung 3b zeigt das Fluoreszenzspektrum von SnO2 /SiO2 -GSH-NSs bei 368 nm. Es ist ersichtlich, dass SnO2 /SiO2 -GSH zeigt eine intensive Fluoreszenzemission, die auf Sauerstoffleerstellen von SnO2 . zurückgeführt wird . Abbildung 3c zeigt die Fluoreszenzbildgebung von SnO2 /SiO2 -GSH-NSs, wenn diese NSs verwendet werden, um GST-getaggtes GPX3 in E zu trennen. Spule lysieren. Es ist zu erkennen, dass dort, wo das präparierte SnO2 /SiO2 -GSH-NSs werden verwendet. Es zeigt an, dass SnO2 wurde auf der Oberfläche von SiO2 . modifiziert und das SnO2 /SiO2 -GSH NSs haben gute Fluoreszenzeigenschaften.
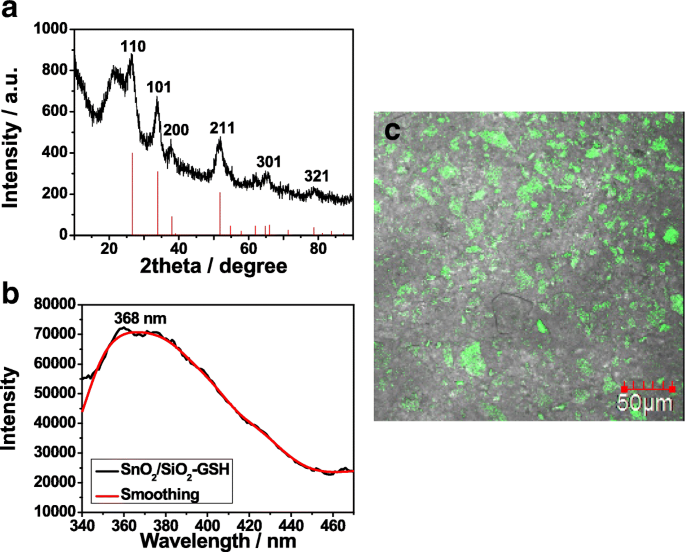
XRD-Muster (a ), Fluoreszenzspektrum (b ) und Fluoreszenzbildgebung (c ) von präpariertem SnO2 /SiO2 -GSH-NSs
SDS-PAGE-Analyse
Um die Fähigkeit des präparierten SnO2 . abzuschätzen /SiO2 -GSH-NSs bei der Trennung von GST-markierten Proteinen führten wir eine SDS-PAGE-Analyse durch. Abbildung 4 zeigt das SDS-PAGE-Analyseergebnis des GST-getaggten GPX3, getrennt durch SnO2 /SiO2 -GSH-NS. Es ist zu erkennen, dass das SnO2 /SiO2 -GSH-NSs können Zielproteine von E effizient anreichern. coli Lysat, und insbesondere die Menge der dissoziierten Proteine neigt dazu, mit zunehmender GSH-Konzentration im Bereich von 10–100 mmol/l zuzunehmen (Spuren 3–6 in Abb. 4a). Es ist klar, dass die Zielproteine durch das präparierte SnO2 . spezifisch getrennt werden können /SiO2 -GSH-NSs aus dem E. coli Lysat und es gab kaum unspezifische.
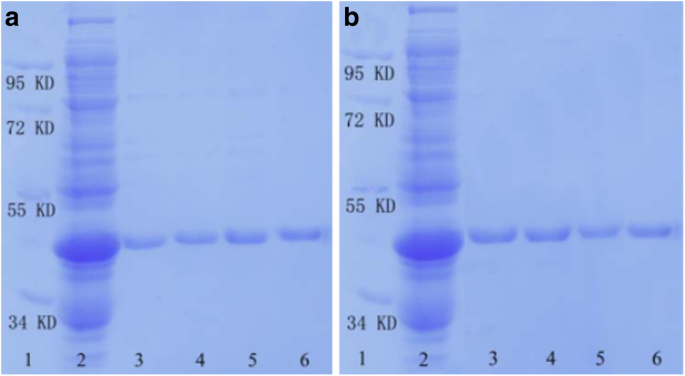
SDS-PAGE-Analyse gereinigter GST-markierter Proteine, getrennt durch SnO2 /SiO2 -GSH-NS. a Spur 1, Markierung; Spur 2, E. coli Lysat; Bahnen 3–6 beziehen sich auf die vom SnO2 . abgewaschenen Fraktionen /SiO2 -GSH-NSs mit unterschiedlichen Konzentrationen an GSH-Lösung (Spur 1, 10 mmol/l; Spur 2, 20 mmol/l; Spur 3, 50 mmol/l; Spur 4, 100 mmol/l). b Spur 1, Markierung; Spur 2, E. coli Lysat; Spur 3, 1. Trennung; Spur 4, 2. Trennung; Spur 5, 3. Trennung; und Spur 6, die Fraktionen, die von der Glutathion-Sepharose 4B abgewaschen wurden
Um die wiederverwendeten Eigenschaften des präparierten SnO2 . zu untersuchen /SiO2 -GSH-NSs haben wir sie wiederholt verwendet, um GST-getaggtes GPX3 zu trennen. Wie in Abb. 4b gezeigt (Spur 1 bezieht sich auf den Marker, Spur 2 bezieht sich auf GST-GPX3-enthaltende E. coli Lysat, Spur 3 bezieht sich auf die erste Trennung, Spur 4 bezieht sich auf die zweite Trennung, Spur 5 bezieht sich auf die dritte Trennung und Spur 6 bezieht sich auf die von Glutathion Sepharose 4B abgewaschenen Fraktionen), das synthetisierte SnO2 /SiO2 -GSH-NSs weisen eine besondere Selektivität gegenüber GST-markiertem GPX3 auf, das aus E extrahiert wurde. coli Lysat, und ihre Spezifität und Affinität bleiben nach drei Zyklen wiederholter Trennung unberührt.
Um die Universalität des synthetisierten SnO2 . zu testen /SiO2 -GSH-NSs zur Reinigung von GST-getaggten Proteinen haben wir drei Arten von GST-getaggten Proteinen (GST-getaggtes GPX3, GST-getaggtes OST1 und GST-getaggtes ABI2) ausgewählt, um Experimente durchzuführen. Wie in Abb. 5 gezeigt, können GST-markierte GPX3-, OST1- und ABI2-Proteine spezifisch durch SnO2 . getrennt werden /SiO2 -GSH-NSs aus dem E. coli Lysat (Bahnen 3, 6, 9); dann können wir sowohl GPX3 erhalten (das GST-Tag von SnO2 abschneiden) /SiO2 -GSH-NSs, die GST-getaggtes GPX binden3) und GST-Tag, eluiert von SnO2 /SiO2 -GSH-NSs (Spur 13, das GPX3; Spur 14, das GST-Tag), das eine ähnliche Wirkung mit Glutathion-Sepharose 4B (Spur 2, 5, 8, 11, 12) hat. Die Konzentrationen von gereinigten Proteinen durch SnO2 /SiO2 -GSH-NS betrugen 7,4 mg/g (GST-getaggt GPX3), 7,1 mg/g (GST-getaggt OST1) und 6,8 mg/g (GST-getaggt ABI2), was darauf hindeutet, dass SnO2 /SiO2 -GSH-NSs eignen sich gut, um GST-markierte Proteine aus dem E. coli lysieren. Um die Bindungskapazität zwischen dem präparierten SnO2 /SiO2 -GSH NSs und das andere Material, Glutathione Sepharose 4B (erworben in Stockholm, USA) wurde als Vergleichsexperimentmaterial verwendet. Die Gesamtproteine, die durch Glutathion-Sepharose 4B gereinigt wurden, betrugen 7,1 mg/ml (GST-getaggtes GPX3), 6,9 mg/ml (GST-getaggtes OST1) bzw. 5,6 mg/ml (GST-getaggtes ABI2). Es ist ersichtlich, dass die Bindungskapazität des hergestellten SnO2 /SiO2 -GSH NSs ist höher als die von Commodity 4B.
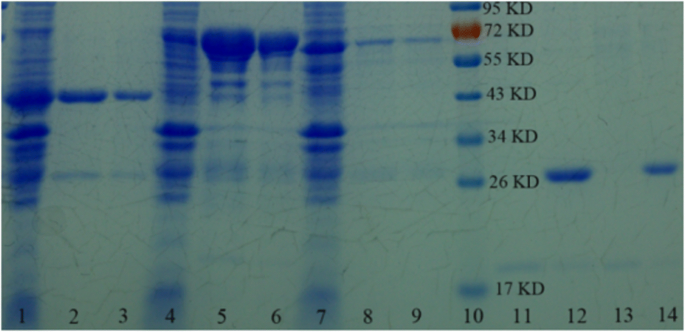
SDS-PAGE-Analyse der gereinigten rekombinanten GPX3-, OST1- und ABI2-Proteine. Bahnen 1, 4 und 7, E. coli Lysat; Bahnen 2, 5 und 8, die Proteine, die von kommerzieller Glutathion-Sepharose 4B (GE Healthcare, USA) eluiert wurden; Spuren 3, 6 und 9, die von SnO2 . eluierten Proteine /SiO2 -GSH-NSs; Spur 10, die Markierung; Bahnen 11 und 13, GPX3, erhalten nach dem Abschneiden des GST-Tags von Glutathion-Sepharose 4B-gebundenem GST-GPX3 und SnO2 /SiO2 -GSH NSs gebundenes GST-markiertes GPX3; Spuren 12 und 14, GST-Tag eluiert von Glutathion Sepharose 4B und SnO2 /SiO2 -GSH-NSs
Analyse des Redoxzustands und der Peroxidaseaktivität von GST-markiertem GPX3
Um den Redoxzustand und die Aktivität von GST-markiertem GPX3 zu analysieren, getrennt durch das präparierte SnO2 /SiO2 -GSH NSs schneiden wir das GST-Tag ab, um das separierte GPX3 zu erhalten. Abbildung 6a zeigt gegebene In-vitro-Assays des GPX3-Redoxzustands (entsprechend einem repräsentativen Gel aus drei unabhängigen Experimenten). Spuren 1 und 2 beziehen sich auf GPX3, das erhalten wurde, nachdem das GST-Tag von Glutathion-Sepharose 4B-gebundenem GST-markiertem GPX3 abgeschnitten wurde (Spur 1 ist das oxidierte GPX3 und Spur 2 ist das reduzierte GPX3); Bahnen 3 und 4 beziehen sich auf GPX3, das erhalten wurde, nachdem das GST-Tag von SnO2 . abgeschnitten wurde /SiO2 -GSH-gebundenes GST-markiertes GPX3 (Spur 3 ist das oxidierte GPX3 und Spur 4 ist das reduzierte GPX3); Spur 5 bezieht sich auf die Markierung. Wie in Abb. 6a gezeigt, trennte sich das gereinigte GPX3 von Glutathion-Sepharose 4B (Bahnen 1 und 2) und SnO2 . /SiO2 -GSH-NSs (Bahnen 3 und 4) haben den oxidierten und den reduzierten Zustand, und das reduzierte GPX3 wandert langsamer als das oxidierte Gegenstück. Dies stimmt gut mit unseren früheren Erkenntnissen überein, dass GPX3 in vitro in oxidiertem und reduziertem Zustand vorliegt und seine reduzierte und oxidierte Form als Ergebnis der Modifikation der reduzierten Cys-Reste getrennt werden kann [26,27,28].
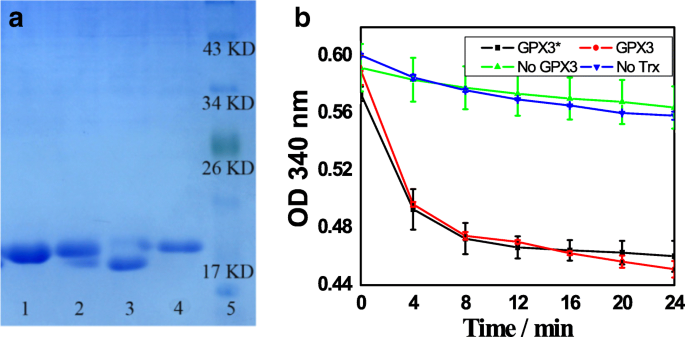
a In-vitro-Assays des GPX3-Redoxzustands:Bahnen 1 und 3 (das oxidierte GPX3) und 2 und 4 (das reduzierte GPX3) beziehen sich auf GPX3, das nach dem Abschneiden des GST-Tags von Glutathion-Sepharose 4B und SnO2 /SiO2 -GSH-gebundenes GST-markiertes GPX3 bzw.; Spur 5, Markierung. b Assays der Peroxidase-Aktivität von GPX3
Abbildung 6b zeigt die Assays der Peroxidase-Aktivität von GPX3:Linie GPX3*, vollständiger Assay des gereinigten GPX3 in Gegenwart von Glutathion-Sepharose 4B, Thioredoxin, Thioredoxin-Reduktase, NADPH und H2 O2; Linie GPX3, vollständige Reaktion zwischen SnO2 /SiO2 -GSH NSs trennten GPX3, Thioredoxin, Thioredoxinreduktase, NADPH und H2 O2; Linie Nr. GPX3, vollständige Reaktion in Abwesenheit von GPX3; und Linie No Trx, vollständige Reaktion in Abwesenheit von Thioredoxin. Abbildung 6b zeigt die Glutathionperoxidase-Aktivität des gereinigten GPX3, getrennt von Glutathion-Sepharose 4B und SnO2 /SiO2 -GSH-NSs in vitro. Es ist ersichtlich, dass das gereinigte GPX3 mit Thioredoxin als Substrat eine signifikante Peroxidaseaktivität aufweist, was darauf hindeutet, dass sich das GPX3 von SnO2 . trennte /SiO2 -GSH NSs ist im natürlichen Zustand vorhanden.
Schlussfolgerungen
Ein einfaches Verfahren zur Herstellung von silikageschütztem SnO2 . wird etabliert QD-Nanosphären (SnO2 /SiO2 NS). Das SnO2 /SiO2 NSs werden durch Glutathion weiter modifiziert, um SnO2 . zu liefern /SiO2 -GSH NSs für die Affinitätstrennung von Glutathion S -Transferase-markiertes (GST-markiertes) rekombinantes Protein. Die Ergebnisse zeigen, dass im Hinblick auf die Fähigkeit, GST-markiertes GPX3, GST-markiertes LOV und GST-markiertes ABI2 zu trennen, das präparierte SiO2 /SiO2 -GSH-NSs weisen eine spezifische Trennung, eine hohe Konzentration an Proteinbindung und gute Wiederverwendungseigenschaften auf. Außerdem behält das vom GST-markierten GPX3 getrennte GPX3 seine Redoxzustände in vitro und seine GPX-Aktivität, was bedeutet, dass das präparierte SnO2 /SiO2 -GSH-NSs könnten ein vielversprechendes Potenzial für die schnelle Trennung und Reinigung von GST-markierten Proteinen haben.
Abkürzungen
- ABI2:
-
ABA-unempfindlich 2
- CTAB:
-
Hexadecyltrimethylammoniumbromid
- DTT:
-
Dithiothreitol
- GPX3:
-
Peroxidaseaktivität von Glutathionperoxidase 3
- GSH:
-
Reduziertes Glutathion
- GST-getaggt:
-
Glutathion S -Transferase-getaggt
- MPS:
-
3-Mercaptopropyl-trimethoxysilan
- NADPH:
-
Dihydronicotinamid-Adenin-Dinukleotidphosphat
- OST1:
-
Stomata öffnen 1
- QDs:
-
Quantenpunkte
- SDS-SEITE:
-
Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese
- SEM:
-
Rasterelektronenmikroskopie
- SiO2 -SH NSs:
-
Thiol-funktionalisierte Silica-Nanosphären
- SnCl4 :
-
Zinn(IV)chlorid
- TEA:
-
Triethylamin
- TEM:
-
Transmissionselektronenmikroskopie
- TEOS:
-
Tetraethylorthosilikat
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Luftabstandshalter für 10-nm-Chips
- Zinn-Nanokristalle für zukünftige Batterien
- Nanobeschichtung für mehrere Farben
- Goldnanopartikel für Chemosensoren
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Nanodiamanten für magnetische Sensoren
- Nanobäume für farbstoffsensibilisierte Solarzellen
- Nano-Heterojunctions für Solarzellen
- Grüne Eintopf-Synthese von Ag-dekorierten SnO2-Mikrosphären:ein effizienter und wiederverwendbarer Katalysator für die Reduktion von 4-Nitrophenol
- Nukleosid-Lipid-basierte Nanoträger für die Sorafenib-Verabreichung



