Einfache Synthese und verbesserte photokatalytische Aktivität mit sichtbarem Licht von neuartigen p-Ag3PO4/n-BiFeO3-Heterojunction-Kompositen für den Farbstoffabbau
Zusammenfassung
In dieser Arbeit, Ag3 PO4 Mikropartikel wurden auf der Oberfläche von BiFeO3 . dekoriert Mikrokuboide durch ein Präzipitationsverfahren zur Gewinnung von p-Ag3 PO4 /n-BiFeO3 Heterojunction-Komposite. Die Komposite wurden für den Abbau von Säureorange 7 (AO7) unter Bestrahlung mit sichtbarem Licht eingesetzt. Es wurde festgestellt, dass die Komposite eine viel höhere photokatalytische Effizienz aufweisen als reines BiFeO3 . Inzwischen ist die intrinsische, durch sichtbares Licht getriebene photokatalytische Aktivität von Ag3 PO4 /BiFeO3 Verbundstoffe wurde außerdem durch den Abbau von Phenol bestätigt. Außerdem wurde auch die Photo-Fenton-ähnliche Katalyseeigenschaft des Verbundmaterials bewertet. Die Photostromanalyse zeigt, dass die Kombination von BiFeO3 mit Ag3 PO4 führt zur Hemmung der Rekombination von photoinduzierten Elektronen und Löchern. Die offensichtliche Verbesserung der photokatalytischen Aktivität des Komposits wird hauptsächlich der effizienten photogenerierten Ladungstrennung und der Grenzflächenladungsmigration zugeschrieben, die durch die Bildung von Ag3 . verursacht wird PO4 /BiFeO3 p-n-Heteroübergänge.
FormalPara PACS81.05.Hd82.65.+r82.50.–m
Hintergrund
In letzter Zeit hat die Halbleiterphotokatalyse als vielversprechende Technologie für die Energieumwandlung und die Behandlung von Schadstoffen große Aufmerksamkeit erregt [1,2,3]. Wie wir wissen, ist der viel untersuchte Photokatalysator TiO2 ist lediglich unter Bestrahlung mit ultraviolettem (UV) Licht aktiv, das nur etwa 5 % des Sonnenlichts ausmacht, und schränkt daher seine photokatalytischen Anwendungen unter Sonnenlicht stark ein. Folglich ist es notwendig, durch sichtbares Licht angetriebene Photokatalysatoren zu entwickeln [4,5,6,7,8].
Bismut- oder eisenbasierte Halbleiteroxide besitzen im Allgemeinen eine moderate Bandlückenenergie (~ 2,0 eV) und gelten als eine wichtige Klasse von auf sichtbares Licht reagierenden Photokatalysatoren [9,10,11,12,13,14,15,16, 17,18,19]. Darunter BiFeO3 mit einer Struktur vom Perowskit-Typ zeigt eine interessante photokatalytische Leistung für den Farbstoffabbau und die Wasserspaltung unter Bestrahlung mit sichtbarem Licht [20,21,22,23,24,25]. Seine photokatalytische Aktivität ist jedoch aufgrund der hohen Rekombinationsrate photogenerierter Elektronen (e − ) und Löcher (h + ). Glücklicherweise wurde gezeigt, dass die Kopplung von BiFeO3 mit einem Halbleiter mit schmaler Bandlücke und angepassten Bandkantenpotentialen zur Bildung eines Heteroübergangs ist eine der vielversprechendsten Strategien zur Förderung der Trennung photogenerierter Ladungen, was zu einer verbesserten photokatalytischen Aktivität von BiFeO3 . führt [26,27,28,29,30,31]. Chaiwichian et al. berichtete, dass BiFeO3 -Bi2 WO6 Nanokomposite zeigten eine erhöhte Aktivität beim Farbstoffabbau [29]. Wanget al. beobachtet, dass AgCl/Ag/BiFeO3 zeigte eine viel höhere photokatalytische Aktivität im sichtbaren Licht als reines BiFeO3 [30]. Fan und Mitarbeiter fanden heraus, dass die Kombination von g-C3 N4 mit BiFeO3 kann offensichtlich die katalytische Aktivität im Vergleich zu reinem BiFeO3 . verbessern [31].
Silberorthophosphat (Ag3 PO4 ), als ausgezeichneter durch sichtbares Licht angetriebener Photokatalysator, hat auf dem Gebiet der Photokatalyse beträchtliche Aufmerksamkeit auf sich gezogen [32,33,34,35,36,37]. Es wurde gezeigt, dass Ag3 PO4 kann eine extrem hohe Quantenausbeute (~ 90%) für die Sauerstofferzeugung aus der Wasserspaltung erzielen [32, 33]. Darüber hinaus besitzt es aufgrund seiner sehr positiven Valenzbandposition eine überlegene Photooxidationsfähigkeit für den Abbau organischer Verschmutzungen [34]. In den meisten Fällen ist Ag3 . aufgrund seiner geeigneten Energiebandposition und schmalen Bandlücke PO4 wird häufig als Cokatalysator verwendet, um sich mit anderen Photokatalysatoren zu Kompositen zu verbinden, was zu einer offensichtlichen Verbesserung des photokatalytischen Verhaltens führt, wie z. B. Ag3 PO4 /Bi2 WO6 , Ag3 PO4 /BiPO4 , Ag3 PO4 /Bi2 O2 CO3 , Ag3 PO4 /g-C3 N4 , Ag3 PO4 /BiVO4 , Bi4 Ti3 O12 /Ag3 PO4 , Ag3 PO4 /ZnFe2 O4 , Ag3 PO4 /WO3 , Ag3 PO4 /ZnO und Bi2 MoO6 /Ag3 PO4 [38,39,40,41,42,43,44,45,46,47]. Es wird berichtet, dass BiFeO3 ist ein Halbleiter vom n-Typ und Ag3 PO4 ist als p-Typ-Halbleiter bekannt [43, 48]. Der Bau von Ag3 PO4 /BiFeO3 p-n-Heteroübergang-Komposite können eine praktikable Methode sein, um einen effizienten Photokatalysator zu erhalten. Nach unserem besten Wissen wurden der Untersuchung der photokatalytischen Leistung von Ag3 . jedoch nur wenige Arbeiten gewidmet PO4 /BiFeO3 Verbundwerkstoffe.
In dieser Arbeit, Ag3 PO4 /BiFeO3 p-n-Heteroübergang-Komposite wurden leicht durch die Fällung von Ag3 . hergestellt PO4 Mikropartikel auf dem BiFeO3 Mikroquader. Säureorange 7 (AO7) und Phenol wurden als Modellschadstoffe ausgewählt, um die photokatalytische Aktivität der Komposite unter Bestrahlung mit sichtbarem Licht zu bewerten. Darüber hinaus wurde auch die Photo-Fenton-ähnliche Katalyseaktivität des Komposits untersucht. Der zugrunde liegende Mechanismus der Komposite für den Abbau organischer Schadstoffe wurde diskutiert.
Methoden
Vorbereitung von Ag3 PO4 /BiFeO3 Verbundwerkstoffe
BiFeO3 Mikrokuboide wurden über einen hydrothermalen Weg synthetisiert. 0,005 Mol Bi(NO3 )3 •5H2 O und 0,005 Mol Fe(NO3 .) )3 •9H2 O wurden in 20 ml verdünnter Salpetersäurelösung (5 ml HNO3 .) gelöst + 15 ml entionisiertes Wasser). Sechzig Milliliter KOH-Lösung mit einer Konzentration von 4,5 mol/l wurden tropfenweise unter magnetischem Rühren zu der obigen Lösung gegeben. Nach 8 Minuten Ultraschallbehandlung und weiteren 30 Minuten heftigem Magnetrühren wurde die Mischungslösung in einem mit Teflon ausgekleideten Edelstahlautoklaven mit 100 ml Fassungsvermögen versiegelt und 6 h lang einer hydrothermalen Reaktion bei 200 °C unterzogen. Nachdem der Autoklav auf natürliche Weise auf Raumtemperatur abgekühlt war, wurde der Niederschlag durch Zentrifugation gesammelt, mit entionisiertem Wasser (zweimal) und absolutem Ethanol (dreimal) gewaschen und dann 12 h bei 80 °C getrocknet, um das endgültige BiFeO . zu erhalten 3 Produkt. Ag3 PO4 Mikropartikel wurden durch ein Präzipitationsverfahren hergestellt. Drei Millimol AgNO3 wurde in 30 ml entionisiertem Wasser und 1 mmol Na3 . gelöst PO4 ·12H2 O wurde mit Hilfe von magnetischem Rühren in 30 ml entionisiertes Wasser gegeben. Nachdem die Lösung homogen war, wurde die letztere Lösung tropfenweise in die erstere unter kräftigem magnetischem Rühren für 7 h zugegeben. Während der Reaktion färbte sich die Lösung gelb. Schließlich wurde die Mischung zentrifugiert, um den Niederschlag zu sammeln. Der erhaltene Niederschlag wurde mehrmals mit entionisiertem Wasser gewaschen und dann 8 h in einem Vakuumofen bei 60 °C getrocknet.
Ag3 PO4 /BiFeO3 Komposite wurden wie folgt synthetisiert:0,1 g BiFeO3 Mikrokuboide wurden in 30 ml entionisiertem Wasser dispergiert und dann 2 h mit Ultraschall behandelt. Danach eine bestimmte Menge AgNO3 wurde in die obige Suspension gelöst. Zu dieser Mischung wurde tropfenweise eine bestimmte Konzentration an Na3 . gegeben PO4 Lösung (30 ml) unter kräftigem Magnetrühren für 7 h. Die so erhaltenen Komposite wurden durch Zentrifugation getrennt, wiederholt mit entionisiertem Wasser gewaschen und in einem Vakuumofen bei 60 °C 8 h lang getrocknet. Um die Wirkung von Ag3 . zu untersuchen PO4 der photokatalytischen Eigenschaften der erhaltenen Komposite wurde eine Reihe von Proben mit verschiedenen Ag3 . hergestellt PO4 Massenverhältnisse von 5 %, 10 %, 20 % und 40 % und die entsprechenden Proben wurden als 5 Gew.-% Ag3 bezeichnet PO4 /BiFeO3 , 10 Gew.-% Ag3 PO4 /BiFeO3 , 20wt%Ag3 PO4 /BiFeO3 , und 40 Gew.-% Ag3 PO4 /BiFeO3 , bzw. Zum Vergleich:der Verbundstoff wird als 20 Gew.-% Ag3 . bezeichnet PO4 /BiFeO3 -M wurde auch durch direktes mechanisches Mischen von BiFeO3 . hergestellt Mikroquader und Ag3 PO4 Mikropartikel, wobei Ag3 PO4 nimmt im Verbund einen Massenanteil von 20 % ein.
Photoelektrochemische Messungen
Der Photostromtest wurde am elektrochemischen Arbeitsplatz (CST 350) mit einer Drei-Elektroden-Zelle wie in der Literatur beschrieben durchgeführt [49]. In diesem Dreielektrodensystem wurden eine Platinfolie und eine Standardkalomelelektrode als Gegenelektrode bzw. Referenzelektrode verwendet. Die Arbeitselektrode wurde wie folgt hergestellt:15 mg Photokatalysatoren, 0,75 mg Ruß und 0,75 mg Polyvinylidenfluorid (PVDF) wurden zu 1-Methyl-2-pyrrolidon (NMP) gegeben, um eine Aufschlämmung herzustellen, die dann gleichmäßig auf eine 1,0" aufgetragen wurde × 1,0 cm 2 Fluorid-dotierte Zinnoxidglaselektrode. Danach wurde die Elektrode 5 h bei 60 °C getrocknet. Als sichtbare Lichtquelle wurde eine 300-W-Xe-Lampe mit einem 420-nm-Sperrfilter verwendet. Die photoelektrochemische Messung wurde in 0,1-M Na2 . durchgeführt SO4 Elektrolytlösung, und sein pH-Wert wurde mit ~ 5,3 gemessen. Die Photostrom-Zeit-Kurven (It) wurden bei einem festen Vorspannungspotential von 0,2 V gemessen. Der Test der elektrochemischen Impedanzspektroskopie (EIS) wurde unter Verwendung des sinusförmigen Spannungspulses mit Amplitude von 5 mV und im Frequenzbereich von 10 –2 bis 10 5 Hz.
Photokatalytischer Aktivitätstest
Die photokatalytische Aktivität der Proben wurde hinsichtlich des Abbaus von AO7 und Phenol unter Bestrahlung mit sichtbarem Licht bewertet. Typischerweise betrug die anfängliche AO7- oder Phenolkonzentration 5 mg/l bei einer Katalysatorbeladung von 0,5 g/l. Die pH-Werte von AO7 und Phenollösung wurden mit ~ 6,8 bzw. ~ 6,2 gemessen. Vor der Belichtung wurde die Mischung 0,5 h im Dunkeln gerührt, um das Adsorptions-Desorptions-Gleichgewicht des organischen Moleküls auf der Oberfläche der Katalysatoren zu erreichen. Diese Reaktionslösung wurde dann einer 300-W-Xenonlampe mit einem 420-nm-Sperrfilter ausgesetzt und die entsprechende Lichtintensität wurde mit ~ 50 mW cm –2 . gemessen . Während des photokatalytischen Experiments wurde in den angegebenen Zeitintervallen eine kleine Menge Reaktionslösung gesammelt und dann zentrifugiert, um die Katalysatoren zu trennen. Die Konzentration von AO7 oder Phenol wurde bestimmt, indem die Absorption des Überstands bei einer bestimmten Wellenlänge (λ AO7 = 484 nm und λ Phenol = 270 nm) mit einem UV-Vis-Spektrophotometer. Um die photokatalytische Wiederverwendbarkeit der Photokatalysatoren zu bewerten, wurde das Recyclingexperiment zum Abbau von AO7 durchgeführt. Nachdem der erste photokatalytische Test abgeschlossen war, wurden die Photokatalysatoren durch Zentrifugation gesammelt, mit destilliertem Wasser gewaschen und getrocknet. Die gesammelten Photokatalysatoren wurden für den nächsten Zyklus des photokatalytischen Experiments in die frische Farbstofflösung gegeben. Um die Photo-Fenton-ähnliche Katalysefähigkeit der Photokatalysatoren zu untersuchen, wurde H2 O2 (5 mmol/l) wurde in die Reaktionslösung gegeben. Das photo-Fenton-ähnliche Experimentverfahren war dem obigen photokatalytischen Verfahren ähnlich.
Charakterisierung
Die Phasenreinheit der Proben wurde mittels Röntgendiffraktometer (XRD, Bruker D8 Advanced) mit Cu Kα-Strahlung untersucht. Die Morphologie der Proben wurde mit einem Feldemissions-Rasterelektronenmikroskop (SEM, JEOL JSM-6701F) und einem Feldemissions-Transmissionselektronenmikroskop (TEM, JEOL JEM-2010) beobachtet. Die Zusammensetzung der Proben wurde durch energiedispersive Röntgenspektroskopie gemessen. Der chemische Zustand des Elements wurde mit Röntgen-Photoelektronenspektroskopie (XPS, PHI-5702) getestet, wobei die Bindungsenergieskala der XPS-Daten gegen den zufälligen C 1s-Peak bei der Bindungsenergie von 284,8 eV kalibriert wurde. Die ultraviolett-sichtbaren (UV-vis) diffusen Reflexionsspektren der Produkte wurden unter Verwendung eines UV-Vis-Spektrophotometers (PERSEE TU-1901) mit BaSO4 . erhalten Als Referenz. Die PL-Spektren der Proben wurden mit einem Fluoreszenzspektrophotometer (SHIMADZU RF-6000) mit einer Anregungswellenlänge von ~ 350 nm aufgenommen.
Ergebnisse und Diskussion
XRD-Analyse
Abbildung 1 zeigt die XRD-Muster von BiFeO3 , Ag3 PO4 , und Ag3 PO4 /BiFeO3 Verbundwerkstoffe mit unterschiedlichem Ag3 PO4 Inhalt. Für bloßes BiFeO3 Probe stimmen alle Beugungspeaks gut mit der rhomboedrischen Struktur von BiFeO3 . überein (PDF-Karte Nr. 74-2016) und für bloßes Ag3 PO4 Probe können die Beugungspeaks perfekt auf kubisches Ag3 . indiziert werden PO4 Phase (PDF-Karte Nr. 06-0505); dies weist darauf hin, dass hochreines BiFeO3 und Ag3 PO4 wurden erfolgreich vorbereitet. Bei den Kompositen können die XRD-Muster den charakteristischen Beugungspeaks von BiFeO3 . zugeordnet werden und Ag3 PO4 und keine Beugungspeaks von Verunreinigung erscheinen in den Mustern. Darüber hinaus ist ersichtlich, dass durch die Erhöhung des Gehalts an Ag3 PO4 , die Intensität der charakteristischen Peaks von Ag3 PO4 nimmt allmählich zu. Die Ergebnisse deuten darauf hin, dass die Komposite aus rhomboedrischem BiFeO3 . bestehen und kubisches Ag3 PO4 , und während der Herstellung der Komposite wird keine andere Phase erzeugt.
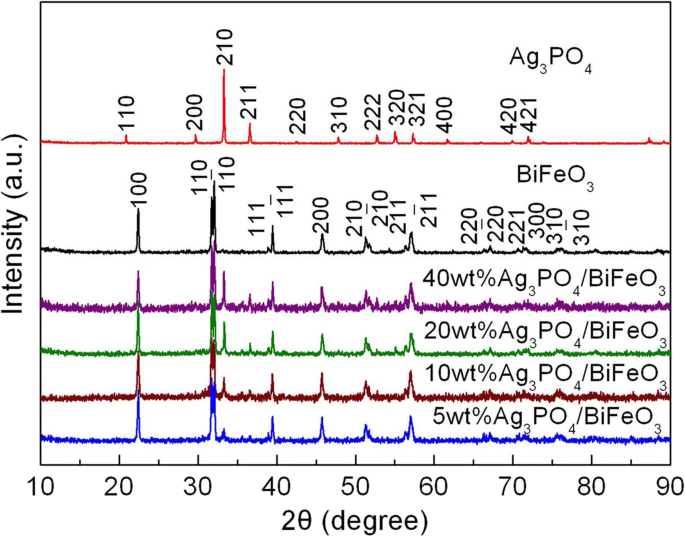
XRD-Muster von BiFeO3 , Ag3 PO4 , und Ag3 PO4 /BiFeO3 Verbundwerkstoffe
Morphologiebeobachtung
Die Morphologie der Proben wurde durch SEM und TEM beobachtet. Abbildung 2a, b zeigt das REM-Bild und das TEM-Bild von bloßem BiFeO3 , was zeigt, dass das präparierte BiFeO3 Partikel weisen eine quaderartige Form mit einer Größe von 200–500 nm auf und haben eine glatte Oberfläche. Der Einschub von Abb. 2a zeigt die Verhältnisverteilung von Länge zu Breite von BiFeO3 . Partikel, was zeigt, dass das Verhältnis von Länge zu Breite von 1,1/1 bis 2,5/1 reicht. Wie aus dem TEM-Bild in Abb. 2c ersichtlich, ist das blanke Ag3 PO4 besteht aus unregelmäßigen kugelförmigen Partikeln. Die Größenverteilung von Ag3 PO4 Partikel ist im Einschub von Fig. 2c gezeigt, was eine breite Verteilung der Partikelgröße im Bereich von 110 bis 180 nm anzeigt. Aus dem TEM-Bild des 20wt%Ag3 PO4 /BiFeO3 Komposit (Abb. 2d) sieht man, dass die unregelmäßigen Mikrokügelchen an dem quaderförmigen Partikel befestigt sind. Die hochauflösenden TEM (HRTEM)-Bilder, die von den verschiedenen Partikeln erhalten wurden, zeigen zwei unterschiedliche Sätze von Gittersäumen (Einschübe in Abb. 2d). Der Interplanarabstand von ~ 0,288 nm entspricht dem von BiFeO3 (110)-Ebenen, wobei der Interplanarabstand von ~ 0,267 nm dem Ag3 . entspricht PO4 (210) Flugzeuge. Darüber hinaus legt die EDX-Analyse nahe, dass der Verbund alle Elemente von Ag3 . enthält PO4 und BiFeO3 Phasen (Abb. 2e). Die beobachteten C- und Cu-Signale im EDX-Spektrum von Abb. 2e könnten aus dem Microgrid stammen, das zur Unterstützung der Probe verwendet wurde [50]. Diese Ergebnisse zeigen, dass Ag3 PO4 Partikel sind auf der Oberfläche von BiFeO3 . dekoriert Mikroquader, was zur Bildung von Ag3 . führt PO4 /BiFeO3 p-n-Heterostrukturen.

a SEM (der Einschub ist die Verhältnisverteilung von Länge zu Breite von BiFeO3 Mikroquader) und b TEM-Bild von BiFeO3 Mikroquader. TEM-Bild von c Ag3 PO4 Mikropartikel (der Einschub ist die Größenverteilung von Ag3 PO4 Mikropartikel) und d 20wt%Ag3 PO4 /BiFeO3 Probe; Einschub zeigt sein HRTEM-Bild. e EDX-Spektrum von 20wt%Ag3 PO4 /BiFeO3 Probe
XPS-Analyse
Die XPS-Analyse wurde durchgeführt, um die chemischen Zustände von BiFeO3 . aufzudecken und 20 Gew.-% Ag3 PO4 /BiFeO3 , wie in Abb. 3 gezeigt. Abbildung 3a zeigt das hochauflösende XPS-Spektrum von Ag 3d im Verbund. Die beiden offensichtlichen Peaks bei 373,8 und 367,7 eV werden dem Ag 3d3/2 . zugeschrieben und Ag 3d5/2 Bindungsenergien von Ag + . Abbildung 3b zeigt das hochauflösende XPS-Spektrum von P 2p des Verbundmaterials. Der Peak bei etwa 133,2 eV entspricht der charakteristischen Bindungsenergie von P 5+ Oxidationsstufe in Ag3 PO4 [51]. Abbildung 3c, d zeigen die hochauflösenden XPS-Spektren von Bi 4f bzw. Fe 2p. Für bloßes BiFeO3 , zeigt das Bi 4f-Spektrum zwei starke Peaks bei Bindungsenergien von 164,1 eV und 158,8 eV, die zum Bi 4f5/2 . gehören und Bi 4f7/2 , was darauf hinweist, dass das Bi-Ion die Oxidationsstufe + 3 besitzt. Für das Fe 2p-Spektrum wird der Peak bei 723.7 eV dem Fe 2p1/2 . zugeordnet von Fe 3+ . Ein weiteres starkes XPS-Signal bei ~ 711,6 eV kann in zwei Peaks bei 711,7 und 709,9 eV eingepasst werden. Der Peak bei 709,9 eV entspricht der Bindungsenergie von Fe 2p3/2 von Fe 2+ . Die Bindungsenergie bei 711,7 eV gehört zum Fe 2p3/2 von Fe 3+ . Darüber hinaus wird ein Satellitenpeak bei etwa 718,2 eV gefunden, der auf die gemischten Oxidationsstufen von Fe zurückgeführt wird. Aus der XPS-Analyse des Fe-Elements geht hervor, dass Fe in Form von Fe 3+ . vorliegt und Fe 2+ in bloßem BiFeO3 . Es ist erwähnenswert, dass die Bindungsenergien von Bi 4f und Fe 2p in 20 Gew.-% Ag3 PO4 /BiFeO3 zeigen eine leichte Verschiebung im Vergleich zu bloßem BiFeO3 , die hauptsächlich auf die Wechselwirkung zwischen BiFeO3 . zurückgeführt wird und Ag3 PO4 . Abbildung 3e zeigt die hochauflösenden O 1s-XPS-Spektren von BiFeO3 und 20 Gew.-% Ag3 PO4 /BiFeO3 . Für bloßes BiFeO3 , kann das O 1s-Signal in zwei Peaks bei 529,8 und 531,0 eV unterteilt werden. Die Bindungsenergie von 529,8 eV entspricht dem Gittersauerstoff, während der kleine Peak bei einer höheren Bindungsenergie von 531,0 eV durch Oberflächendefekte und chemisorbierte Sauerstoffspezies verursacht wird. Im Vergleich zu bloßem BiFeO3 , erfährt der O 1s-Peak im Komposit eine Verschiebung, die auch auf die Wechselwirkung zwischen Ag3 . zurückzuführen ist PO4 und BiFeO3 .
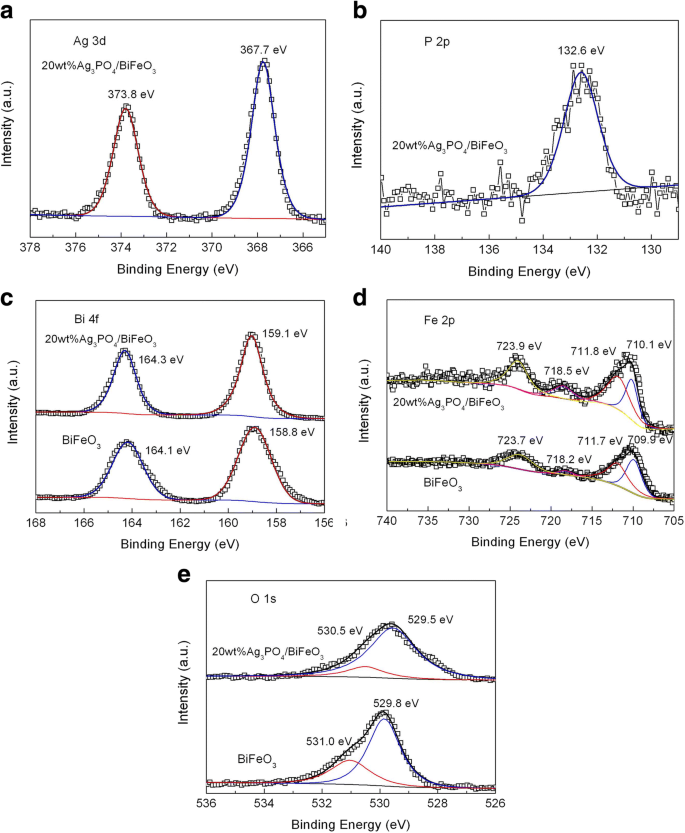
Hochauflösende XPS-Spektren von BiFeO3 und 20 Gew.-% Ag3 PO4 /BiFeO3 Probe. a Ag 3d und b P 2p von 20 Gew.-% Ag3 PO4 /BiFeO3 Probe. c Bi 4f, d Fe 2p und e O1s von BiFeO3 und 20 Gew.-% Ag3 PO4 /BiFeO3 Probe
Optische Absorptionseigenschaft
Das optische Absorptionsverhalten der Proben wurde durch Messung ihrer UV-Vis-Diffusreflexionsspektren untersucht, wie in Abb. 4a dargestellt. Die entsprechenden Absorptionsspektren, die aus den diffusen Reflexionsspektren nach der Kubelka-Munk (K-M)-Theorie transformiert wurden, sind in Abb. 4b [52] dargestellt. Es ist ersichtlich, dass alle Proben eine wichtige Lichtabsorption bei λ < 600 nm aufweisen. Um die Absorptionskante der Proben zu erhalten, wurde die erste Ableitung des Reflexionsvermögens (R) in Bezug auf die Wellenlänge λ (d. h. dR/dλ) durchgeführt, wie in Fig. 4c gezeigt. Die Absorptionskante kann aus der Peakwellenlänge in den Ableitungsspektren bestimmt werden [53]. Es ist zu erkennen, dass die Lichtabsorptionskante von bloßem Ag3 PO4 liegt bei ~ 527 nm, entsprechend der Bandlückenenergie (E g ) von ~ 2,35 eV. Bloßes BiFeO3 weist eine Absorptionskante bei etwa 567 nm auf, entsprechend dem E g von ~ 2,18 eV. Neben der Absorptionskante wird ein schwacher Peak bei ~ 700 nm beobachtet, der wahrscheinlich auf die Existenz von Oberflächenzuständen in der Mitte der Bandlücke von BiFeO3 . zurückgeführt wird . In Verbindung mit Ag3 PO4 , die Absorptionskante von BiFeO3 keine offensichtliche Änderung erfährt, was darauf hindeutet, dass die Einführung von Ag3 PO4 hat keinen offensichtlichen Einfluss auf die Bandlückenstruktur von BiFeO3 .
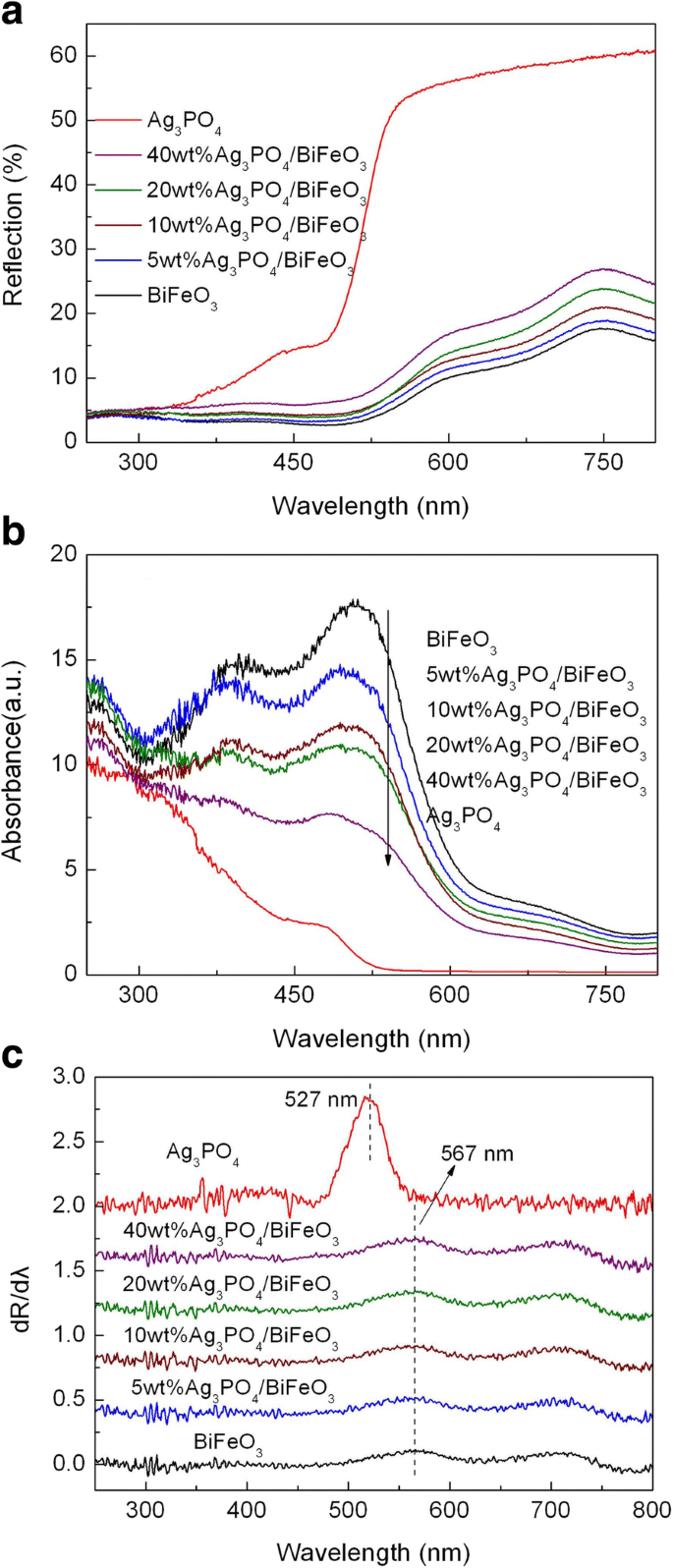
a UV-sichtbare diffuse Reflexionsspektren von BiFeO3 , Ag3 PO4 , und Ag3 PO4 /BiFeO3 Verbundstoffe. b Die entsprechenden Absorptionsspektren und c die entsprechende erste Ableitung der diffusen Reflexionsspektren
Photokatalytische Aktivitätsmessung
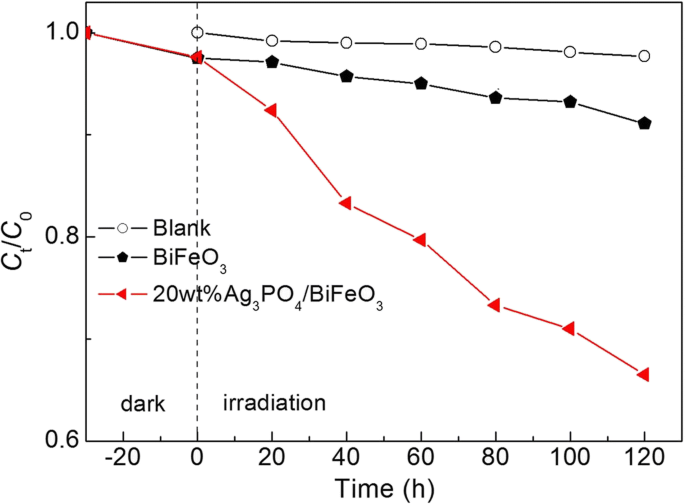
AO7 wurde als Zielschadstoff für die Bewertung der photokatalytischen Leistung der Proben ausgewählt. Der photokatalytische Abbau von AO7 wurde unter Bestrahlung mit sichtbarem Licht untersucht und das Ergebnis ist in Abb. 5 dargestellt. Vor der photokatalytischen Reaktion wurden Blind- und Absorptionsexperimente durchgeführt. Es ist ersichtlich, dass unter Bestrahlung ohne Katalysatoren oder in Gegenwart von Katalysatoren ohne Bestrahlung kein offensichtlicher Abbau des Farbstoffs nachgewiesen wird, was darauf hindeutet, dass Selbstabbau und Absorption von AO7 während des photokatalytischen Prozesses vernachlässigbar sind. Bloßes BiFeO3 hat eine schwache photokatalytische Aktivität und nur ~ 27 % von AO7 werden bei 120 Minuten Bestrahlung abgebaut. Wenn BiFeO3 Mikroquader werden mit Ag3 . kombiniert PO4 Mikropartikel, das gebildete Ag3 PO4 /BiFeO3 Komposite zeigen eine überlegene photokatalytische Aktivität gegenüber bloßem BiFeO3 . Nach 120 Minuten Exposition liegt der Abbauprozentsatz von AO7 in den Proben in der Größenordnung von 40 Gew.-% Ag3 PO4 /BiFeO3 (~ 91 %) > 20wt%Ag3 PO4 /BiFeO3 (~ 87%) > 10wt%Ag3 PO4 /BiFeO3 (~ 69%) > 5wt%Ag3 PO4 /BiFeO3 (~ 46%) > BiFeO3 (~ 27%). Es wurde festgestellt, dass die photokatalytische Leistung der Komposite mit steigendem Ag3 . einen steigenden Trend aufweist PO4 Inhalt. Unter diesen Verbundwerkstoffen ist die photokatalytische Effizienz von 40 Gew.-% Ag3 PO4 /BiFeO3 ist dem von 20 Gew.-% Ag3 sehr nahe PO4 /BiFeO3 . Daher ist in der vorliegenden Studie das am besten geeignete Massenverhältnis von Ag3 PO4 in den Verbundwerkstoffen mit 20 % angesetzt werden. Darüber hinaus ist es erwähnenswert, dass die mechanische Mischungsprobe 20 Gew.-% Ag3 PO4 /BiFeO3 -M weist eine viel geringere photokatalytische Aktivität auf als 20 Gew.-% Ag3 PO4 /BiFeO3 . Dies zeigt, dass der Aufbau des Heteroübergangs zwischen BiFeO3 und Ag3 PO4 ist für die Steigerung der photokatalytischen Aktivität notwendig. Darüber hinaus im Vergleich zu BiFeO3 /a-Fe2 O3 und BiFeO3 -Bi2 WO6 Verbundwerkstoffe [26, 29], das Ag3 PO4 /BiFeO3 Heterojunction-Komposite, die in der vorliegenden Studie hergestellt wurden, zeigen eine höhere photokatalytische Aktivität gegenüber dem Farbstoffabbau.
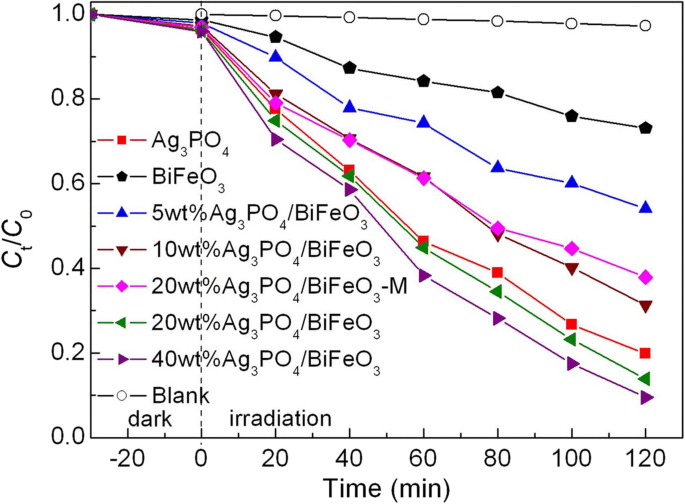
Photokatalytische Aktivitäten von BiFeO3 und Ag3 PO4 /BiFeO3 Komposite zum Abbau von AO7 unter Bestrahlung mit sichtbarem Licht, zusammen mit den Ergebnissen des Blind- und Absorptionsexperiments
Um die photokatalytische Eigenschaft der Verbundstoffe weiter zu bestätigen, wurde der photokatalytische Abbau von farblosem Phenol über 20 Gew.-% Ag3 PO4 /BiFeO3 und BiFeO3 unter Bestrahlung mit sichtbarem Licht wurde ebenfalls untersucht. Wie in Abb. 6 gezeigt, kann der Selbstabbau und die Aufnahme von Phenol aufgrund der Ergebnisse von Blind- und Absorptionsexperimenten vernachlässigt werden. Es ist ersichtlich, dass nur ~ 9% des Phenols durch BiFeO3 . katalysiert abgebaut werden nach 120 Minuten Belichtung. Wenn dagegen 20 Gew.-% Ag3 PO4 /BiFeO3 als Photokatalysator verwendet wird, kann der Abbauprozentsatz von Phenol unter den gleichen Bedingungen offensichtlich erhöht werden. Das Ergebnis deutet darauf hin, dass der Abbau des Farbstoffs auf dem mit sichtbarem Licht bestrahlten Ag3 PO4 /BiFeO3 Kompositen wird ihre intrinsische photokatalytische Aktivität anstelle der Farbstoffsensibilisierung zugeschrieben.
Photokatalytischer Abbau von Phenol über BiFeO3 und 20 Gew.-% Ag3 PO4 /BiFeO3 Probe unter Bestrahlung mit sichtbarem Licht, zusammen mit dem Ergebnis der Blindprobe und des Absorptionsexperiments
Um die Wiederverwendbarkeit der Photokatalysatoren zu bewerten, wurden die Recyclingexperimente zum photokatalytischen Abbau von AO7 über 20 Gew.-% Ag3 PO4 /BiFeO3 und Ag3 PO4 wurden unter den gleichen photokatalytischen Bedingungen durchgeführt. Wie in Abb. 7 gezeigt, weist der Verbundstoff nach drei aufeinanderfolgenden Recyclingläufen immer noch eine relativ hohe photokatalytische Aktivität auf, während die Abbaueffizienz gegenüber Ag3 PO4 einen deutlichen Rückgang erfährt. Abbildung 8a, b zeigen das TEM-Bild bzw. das XRD-Muster des Verbundmaterials nach dem Zyklenexperiment. Es ist klar, dass Ag3 PO4 Mikropartikel sind immer noch auf der Oberfläche von BiFeO3 . aufgebaut Mikroquader ohne Zerstörung der Heterostrukturen, und es wird keine offensichtliche Kristallstrukturänderung beobachtet. Dies deutet darauf hin, dass Ag3 PO4 /BiFeO3 p-n-Heteroübergang-Komposite besitzen eine gute photokatalytische Wiederverwendbarkeit.
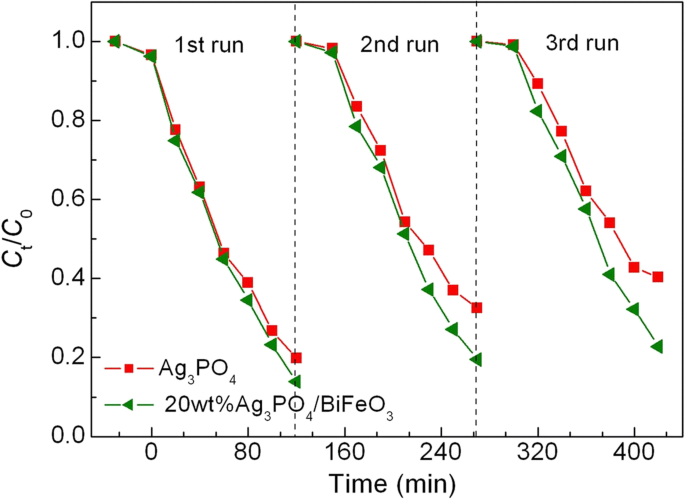
Photokatalytischer Abbau von AO7 über Ag3 PO4 und 20 Gew.-% Ag3 PO4 /BiFeO3 Probe während drei Zyklen
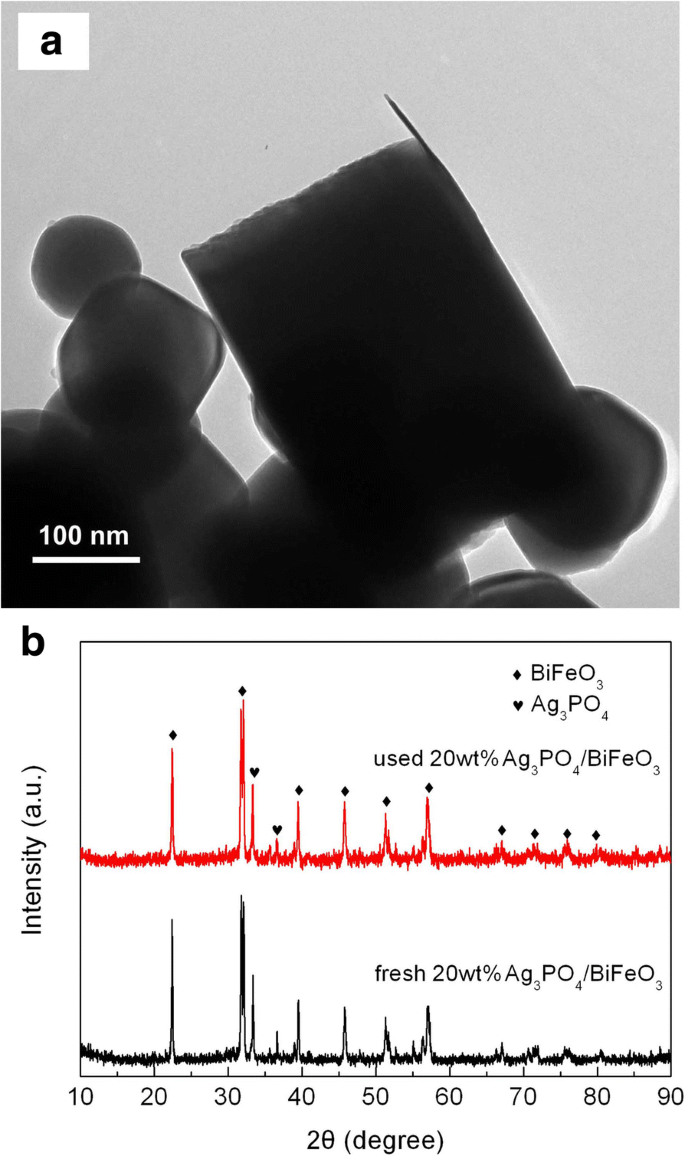
a TEM-Bild und b XRD-Muster von 20 Gew.-% Ag3 PO4 /BiFeO3 Probe nach zyklischen photokatalytischen Experimenten
Foto-Fenton-ähnliche katalytische Aktivität
Abgesehen von seiner photokatalytischen Eigenschaft ist BiFeO3 weist auch eine ausgeprägte Photo-Fenton-ähnliche Katalysefähigkeit auf [54,55,56]. Abbildung 9 zeigt den photo-Fenton-ähnlichen Abbau von AO7 über 20 Gew.-% Ag3 PO4 /BiFeO3 und BiFeO3 in Gegenwart von H2 O2 . Verglichen mit den Reaktionssystemen ohne H2 O2 , die Einführung von H2 O2 erhöht den Abbauprozentsatz des Farbstoffs merklich. Dieses Ergebnis ist hauptsächlich auf den Photo-Fenton-ähnlichen Reaktionsmechanismus zurückzuführen. In Gegenwart von sichtbarem Licht und H2 O2 , Fe 3+ auf der Oberfläche von BiFeO3 kann in Fe 2+ . umgewandelt werden unter Bildung von Hydroxyl-(•OH)-Radikalen (Gl. 1). Folglich ist Fe 2+ kann mit H2 . reagieren O2 um Fe 3+ . zu produzieren und •OH (Gleichung 2). Während der obigen Zyklusreaktion wird mehr •OH produziert, das allgemein als eine primäre aktive Spezies für den Farbstoffabbau angesehen wird (wie durch das Experiment zum Einfangen aktiver Spezies in Abb. 11 belegt). Im Fall von bloßem BiFeO3 , begrenzt die hohe Rekombinationsrate der photogenerierten Ladungen die Ausbeute an photogenerierten Elektronen, was dazu neigt, die Reduktion von Fe 3+ . zu unterdrücken in Fe 2+ (Gl. 3). Dies führt zu einer begrenzten Erhöhung des Abbauprozentsatzes. Für Ag3 PO4 /BiFeO3 Komposite können photogenerierte Elektronen und Löcher effizient getrennt werden und somit stehen mehr photogenerierte Elektronen zur Förderung der schnellen Umwandlung von Fe 3+ . zur Verfügung in Fe 2+ (Gl. 3) [57]. Dank dieser Elektronenreduktion ist der Photo-Fenton-Prozess für die Verbundwerkstoffe effizienter als der für reines BiFeO3 . Als Ergebnis Ag3 PO4 /BiFeO3 p-n-Heteroübergang-Verbundwerkstoffe weisen eine stark verbesserte Photo-Fenton-Leistung auf.
$$ {\mathrm{Fe}}^{3+}+{\mathrm{H}}_2\mathrm{O}+\mathrm{h}\upnu \to {\mathrm{Fe}}^{2+} +\bullet \mathrm{OH}+{\mathrm{H}}^{+} $$ (1) $$ {\mathrm{Fe}}^{2+}+{\mathrm{H}}_2{\ mathrm{O}}_2\to {\mathrm{Fe}}^{3+}+\bullet \mathrm{OH}+{\mathrm{O}\mathrm{H}}^{-} $$ (2) $$ {\mathrm{Fe}}^{3+}+{\mathrm{e}}^{-}\to {\mathrm{Fe}}^{2+} $$ (3)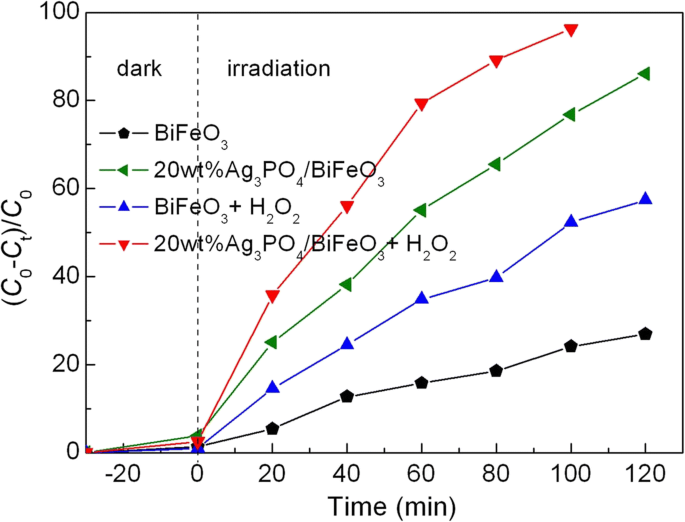
Photokatalytische Aktivitäten von BiFeO3 und 20 Gew.-% Ag3 PO4 /BiFeO3 Probe zum Abbau von AO7 unter Bestrahlung mit sichtbarem Licht in Gegenwart von H2 O2
Fotogenerierte Ladeleistung
Um das Trennungsverhalten photogenerierter Ladungen der Proben, transiente Photostromantworten, ESI-Spektren und PL-Spektren von BiFeO3 . zu bewerten und 20 Gew.-% Ag3 PO4 /BiFeO3 wurden gemessen. Abbildung 10a zeigt die Photostrom-Zeit-Kurven (I-t) der Photokatalysatoren bei intermittierender Bestrahlung mit sichtbarem Licht mit mehreren Ein-Aus-Zyklen. Es ist ersichtlich, dass der Photostromwert des Komposits viel höher ist als der von bloßem BiFeO3 , was darauf hinweist, dass die Konstruktion von Ag3 PO4 /BiFeO3 p-n-Heteroübergänge sind vorteilhaft, um die Rekombination von durch Licht erzeugten Elektronen und Löchern zu hemmen. Abbildung 10b zeigt die ESI-Spektren der Proben. Man sieht, dass der Verbund kleinere Impedanz-Bogenradien im Vergleich zu BiFeO3 . aufweist , was auf den geringeren Ladungsübergangswiderstand des Komposits schließen lässt. These results reveal that the separation and migration of the photogenerated charges can be improved in the composite, thus providing more photoinduced holes and electrons for the photocatalysis. Figure 10c shows the Mott-Schottky plot at frequency of 3000 Hz for Ag3 PO4 . The negative slope of the plot indicates that Ag3 PO4 is a p-type semiconductor, which is consistent with the report [43]. The PL spectra of BiFeO3 and 20wt%Ag3 PO4 /BiFeO3 are shown in Fig. 10d. The two samples exhibit obvious emission peaks at ~ 522 nm, which are mainly attributed to the recombination of the photogenerated electron/hole pairs. It is worth noting that the PL intensity of the composite is much smaller than that of bare BiFeO3 . This further confirms that the construction of Ag3 PO4 /BiFeO3 heterojunction promotes the separation of photoinduced charges.
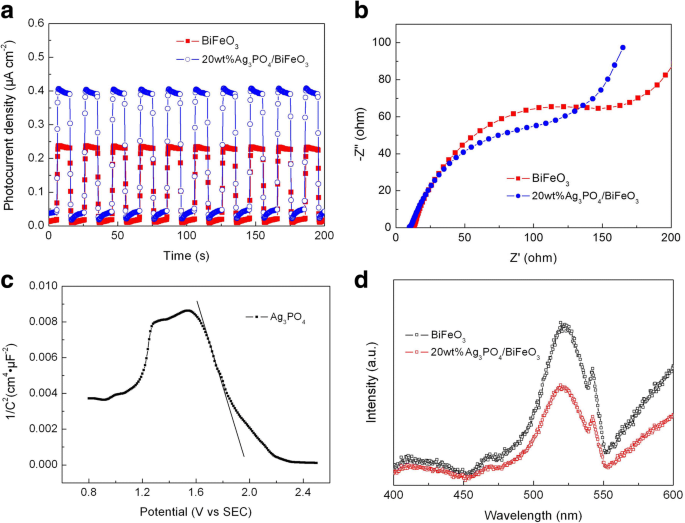
a Transient photocurrent response and b EIS spectra of BiFeO3 and 20wt%Ag3 PO4 /BiFeO3 Probe. c Mott-Schottky plot of Ag3 PO4 . d PL spectra of BiFeO3 and 20wt%Ag3 PO4 /BiFeO3 samples
Active Species Trapping
It is well known that photogenerated hole (h + ), hydroxyl (•OH), and superoxide (•O 2− ) are considered to the main active species responsible for the photocatalytic degradation of dye. In order to clarify the role of the active species in the present photocatalytic system, the active species trapping experiments were carried out, as shown in Fig. 11. It can be seen that the degradation percentage of AO7 undergoes an obvious decrease after the introduction of ethanol (scavenger of •OH, 10% by volume) or ethylene diamine tetraacetic acid (EDTA, scavenger of h + , 2 mM). This indicates that •OH and h + are the major active species involved in the photocatalytic reaction. After the addition of benzoquinone (BQ, scavenger of •O 2− , 1 mM), a slight decrease of degradation percentage is detected, suggesting that •O 2− plays a relatively minor role in the dye degradation.
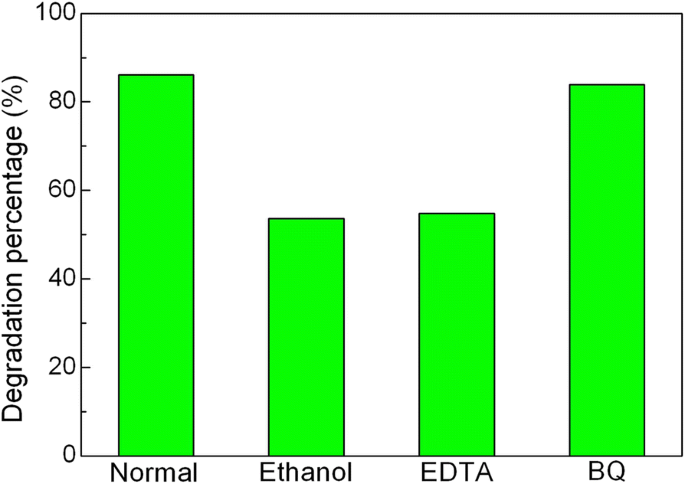
Effects of ethanol, EDTA, and BQ on the degradation percentage of AO7 over 20wt%Ag3 PO4 /BiFeO3 zusammengesetzt
Proposed Photocatalytic Mechanism
It is well known that the redox ability and migration of photogenerated charges are highly related to the energy-band potentials of photocatalysts. The valence band (VB) and conduction band (CB) of BiFeO3 and Ag3 PO4 can be obtained using the following equation [58, 59]:
$$ {E}_{\mathrm{VB}}=X-{E}^{\mathrm{e}}+0.5{E}_{\mathrm{g}} $$ (4) $$ {E}_{\mathrm{CB}}=X-{E}^{\mathrm{e}}-0.5{E}_{\mathrm{g}} $$ (5)X is the absolute electronegativity of semiconductor (calculated as the arithmetic mean of the electron affinity and the first ionization of the constituent atoms). E e is the energy of free electrons on the hydrogen scale (~ 4.5 eV). The X values of BiFeO3 and Ag3 PO4 are estimated to be 5.93 and 5.98 eV, respectively [43, 60]. Based on Eqs. (4) and (5), the CB/VB potentials of BiFeO3 and Ag3 PO4 are calculated to be 0.34/2.52 V and 0.31/2.66 V vs. NHE, respectively. The energy-band potential diagram of the two photocatalysts is shown in Fig. 12a. It is reported that BiFeO3 is an n-type semiconductor and its Fermi level lies close to the CB [48]. Ag3 PO4 is demonstrated to be a p-type semiconductor (see Fig. 10c), whose Fermi energy level is close to the VB [43].When BiFeO3 is combined with Ag3 PO4 to form p-n heterojunction (see Fig. 12b), the diffusion of electrons and holes between the two photocatalysts will build an internal electric field at the interface region of the p-n heterojunction with direction from BiFeO3 to Ag3 PO4 . Simultaneously, the energy-band potential of BiFeO3 tends to move down along with its Fermi level whereas that of Ag3 PO4 tends to raise up accompanied by its Fermi level until an equilibrium state of Fermi level of the two photocatalysts is achieved. Upon visible-light irradiation, both BiFeO3 and Ag3 PO4 can be excited to generate photoinduced electron and hole pairs. Under the promotion of the internal electric field, the photogenerated electrons in the CB of Ag3 PO4 will migrate to the CB of BiFeO3 , while the photogenerated holes will transfer from the VB of BiFeO3 to that of Ag3 PO4 . As a result, the recombination of photogenerated charges can be effectively inhibited, as evidenced by the photocurrent and PL analysis (see Fig. 10a, d). Thus, more photogenerated electrons and holes can participate in the photocatalytic redox reaction, leading to the enhancement of the photocatalytic activity for the Ag3 PO4 /BiFeO3 p-n heterojunction composites.
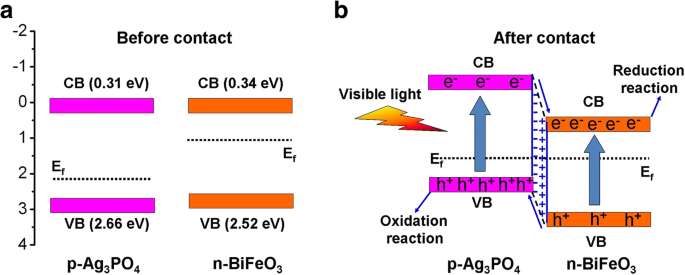
Schematic illustration of proposed photocatalytic mechanism for Ag3 PO4 /BiFeO3 zusammengesetzt. a Before contact. b After contact
Schlussfolgerungen
Ag3 PO4 /BiFeO3 p-n heterojunction composites were synthesized through the decoration of Ag3 PO4 spherical-like microparticles on the surface of BiFeO3 microcuboids. Compared with bare BiFeO3 , the as-obtained composites exhibit enhanced visible-light photocatalytic activity for the degradation of AO7 and phenol. Moreover, the composites are demonstrated to be excellent photo-Fenton-like catalysts. The improved photocatalytic activity of the composites is mainly attributed to the efficient separation of photogenerated electrons and holes owing to the formation of the p-n heterojunction between BiFeO3 and Ag3 PO4.
Abkürzungen
- AO7:
-
Acid orange 7
- CB:
-
Leitungsband
- DRS:
-
UV-vis diffuse reflectance spectra
- EDX:
-
Energy dispersive X-ray
- E g :
-
Bandgap energy
- I-t:
-
Photocurrent-time
- NMP:
-
1-Methyl-2-pyrrolidione
- PVDF:
-
Polyvinylidenfluorid
- R:
-
Reflectance
- SEM:
-
Rasterelektronenmikroskop
- TEM:
-
Transmissionselektronenmikroskop
- VB:
-
Valenzband
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgendiffraktometer
Nanomaterialien
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Fortschritte und Herausforderungen fluoreszierender Nanomaterialien für die Synthese und biomedizinische Anwendungen
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität
- Ein neuartiger Bi4Ti3O12/Ag3PO4-Heteroübergang-Photokatalysator mit verbesserter photokatalytischer Leistung
- Einfache Synthese von Wurmloch-ähnlichem mesoporösem Zinnoxid durch verdunstungsinduzierte Selbstorganisation und die verbesserten Gassensoreigenschaften
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität
- Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
- Photokatalytische Aktivität des ternären Nanokomposits Attapulgit–TiO2–Ag3PO4 für den Abbau von Rhodamin B unter simulierter Sonneneinstrahlung
- Herstellung und photokatalytische Eigenschaft neuartiger SrTiO3/Bi5O7I-Nanokomposite
- Eine einfache Methode zur Herstellung einer Cu2O-TiO2-NTA-Heteroverbindung mit sichtbarer photokatalytischer Aktivität



