Integration umweltfreundlicher Perowskite für hocheffiziente weiße Leuchtdioden
Zusammenfassung
Perowskit-Quantenpunkte (QDs) werden aufgrund ihrer hohen Quantenausbeute (QY), der einstellbaren Bandlücke und der einfachen Herstellung häufig in weißen Leuchtdioden (WLEDs) verwendet. Allerdings enthalten die rot emittierenden Perowskit-QDs normalerweise Iod (I), das bei kontinuierlicher Lichtbestrahlung nicht stabil ist. Hier wird eine WLED auf Perowskit-Basis aus bleifreien Wismut (Bi)-dotierten anorganischen Perowskiten Cs2 . hergestellt SnCl6 und weniger bleihaltiges Mn-dotiertes CsPbCl3 QDs, die weißes Licht mit Farbkoordinaten von (0,334, 0,297) emittieren. Das bidotierte Cs2 SnCl6 und Mn-dotiertes CsPbCl3 QDs zeigen beide eine ausgezeichnete Stabilität, wenn sie in der Umgebungsluft aufbewahrt werden. Als Vorteil dieser gewünschten Eigenschaft zeigt die WLED im vorbereiteten Zustand eine hervorragende Stabilität sowie Betriebszeit. Diese Ergebnisse können die Anwendung anorganischer Perowskit-QDs im Bereich der WLEDs fördern.
Einführung
Unter der Festkörperbeleuchtungstechnologie sind weiße Leuchtdioden (WLEDs) aufgrund ihrer Vorzüge der hohen Energieeinsparung, der langen Lebensdauer, der hohen Lichtausbeute und der polarisierten Emissionen ausgezeichnete Kandidaten, um Glühlampen zu ersetzen [1]. Im Allgemeinen wurden WLEDs als eine Art der sparsamen und effizienten Festkörperlichtquellen anerkannt [2, 3]. Die QD-LED-Technologie wurde in den letzten Jahren aufgrund der hohen Stabilität und der hohen Quantenausbeute (QY) von Quantenpunkten (QDs) sukzessive weiterentwickelt [4]. In letzter Zeit haben Perowskite viel Aufmerksamkeit auf sich gezogen und sie wurden in vielen verschiedenen Bereichen eingesetzt [5,6,7,8,9,10,11,12,13,14,15]. Perowskit-Solarzellen mit einem Leistungsumwandlungswirkungsgrad (PCE) von über 23% wurden aufgrund ihrer hervorragenden Absorptionskoeffizienten (Abs), ihrer langen Ladungsträgerdiffusionslängen und hohen Ladungsträgermobilitäten erreicht [5,6,7]. CsPbBr3 -verkapselte PbSe-Drähte haben eine gute optoelektronische Leistung gezeigt, einschließlich einer hohen Empfindlichkeit (~ 10 4 A W −1 ) und angemessene Reaktionsgeschwindigkeit (~ ms), was ihre große potenzielle Anwendung in Photodetektionsfeldern demonstriert [8,9,10]. Darüber hinaus wurden Perowskite in photonische Geräte eingeführt. Die bemerkenswerten Eigenschaften von Perowskit, wie z. B. reiche Phasenzusammensetzungen und die Fähigkeit, bei niedriger Temperatur in Lösung zu gehen, machen Perowskit in Transistoren anwendbar [5]. Niedrigschwellige verstärkte spontane Emission und Laser können durch CsPbX3 . realisiert werden QDs [11]. Vor allem Perowskit-QDs sind das vielversprechendste Material unter den QDs für LED-Anwendungen, aufgrund der hohen QY (bis zu> 90%), der intensiven Photolumineszenz (PL), des einfachen Herstellungsverfahrens und der hoch abstimmbaren Bandlücken (von 1,46 bis 2,50 eV). [11,12,13,14,15,16]. Allerdings schränkten die Anionenaustauschreaktion zwischen Perowskiten und die Instabilität von iod(I)-haltigen Perowskiten die Entwicklung von Perowskit-QDs in Richtung WLED-Anwendung stark ein. Sonneet al. vorgeschlagen, Silica-Einkapselung zu verwenden, um die Stabilität zu erhöhen und Anionenaustausch zu vermeiden [17]. Die Luftstabilität von Perowskit-QDs wurde stark verbessert, aber die WLED-Stabilität ist wegen des erheblichen Abfalls von rotem Licht nicht gut genug. Dann haben Shen et al. nutzten die Anthracenhülle, um rot emittierende Perowskit-QDs zu schützen, was die LED-Stabilität gegenüber Strom erhöhte [18]. Zhong und Mitarbeiter verwendeten direkt das rot emittierende K2 SiF6 :Mn 4+ Phosphor als Ersatz für jod(I)-haltige Perowskit-QDs [19]. Auch Sun und Mitarbeiter stellten die gleiche Methode zur Verbesserung der LED-Stabilität vor [20]. Aufgrund der scharfen Emissionslinien von Perowskit-QDs werden sie normalerweise in Backlight-Display-Anwendungen mit blau emittierenden LED-Chips verwendet [21, 22]. Diese WLEDs sind nicht für Festkörperbeleuchtung geeignet, da ihr CRI ziemlich niedrig ist. Kürzlich wurde in mehreren Berichten ein einphasiger Phosphor von Perowskiten hergestellt, der breite Linienbreiten besitzt. Allerdings sind die QYs dieser Art von Material relativ niedrig [23,24,25]. Ein weiteres großes Problem ist, dass die Perowskit-QDs Blei enthalten, das für Gesundheit und Umwelt giftig ist [26, 27]. Angesichts der wachsenden Besorgnis über dieses Risiko wurden Beschränkungen eingeführt, um die Verwendung von Pb in der Unterhaltungselektronik zu begrenzen. Es wurden viele Anstrengungen unternommen, um Blei zu erforschen und durch weniger toxische Elemente wie Sn, Ge, Bi und Sb zu ersetzen, die eine analoge elektronische Bandstruktur aufweisen [28,29,30]. Ihre optoelektronischen Eigenschaften sind jedoch nicht mit denen der Pb-basierten Gegenstücke vergleichbar. Die Dotierung weniger toxischer Elemente in das Perowskitgitter war ein alternativer Weg, der neue optische, elektronische und magnetische Eigenschaften einführen kann [31, 32]. Zhang et al. haben Mn-dotierte Perowskit-QDs mit QYs bis zu 54% hergestellt und das höchste Mn-Substitutionsverhältnis betrug 46% [31]. Tang und Mitarbeiter berichteten über bidotierte bleifreie anorganische Perowskite. Nach dem Dotieren von Bi, der PLQY von Bi-dotiertem Cs2 SnCl6 wird auf 78,9 % gesteigert [33].
In dieser Arbeit stellen wir Mn-dotiertes CsPbCl3 vor QDs und Bi-dotiertes Cs2 SnCl6 als oranges Emissionslicht und blaues Emissionslicht, um Hochleistungs-WLEDs herzustellen. Diese beiden Materialien können beide durch UV-Licht angeregt werden und zeigen unter UV-Licht hohe QYs. Sie enthalten auch das gleiche Anion Cl, das die Anionenaustauschreaktion während des Mischprozesses vermeidet. Außerdem ist es erwähnenswert, dass die Emissionslinienbreiten dieser beiden Perowskite sehr breit sind, was die Bildung eines kontinuierlichen Spektrums erleichtert. In einer WLED mit einem CCT von 5311K wurden die Farbkoordinaten von (0,334, 0,297) und ein CRI von 80 erreicht. Vor allem zeigte diese WLED eine ausgezeichnete Stabilität gegenüber steigenden Strömen und Arbeitszeiten.
Methoden
Materialien und Chemikalien
Cäsiumcarbonat (Cs2 CO3 , 99,9%), Blei(II)chlorid (PbCl2 .) , 99,999 %), Cäsiumchlorid (CsCl, 99,99 %), Ölsäure (OA, 90 %) und 1-Octadecen (ODE, 90 %) wurden von Alfa Aesar bezogen. Manganchlorid-Tetrahydrat (MnCl2· (H2 O)4 , 99,99 %), Oleylamin (OAm, 80–90 %) und Zinnchlorid (SnCl2 , 99,99%) wurden von Aladdin gekauft. Wismutchlorid (BiCl3 .) , 99,99%) und Polymethylmethacrylat (PMMA) wurden von Macklin bezogen. Salzsäure (HCl, 37 Gew.-% in Wasser) wurde von Sinopharm Chemical Reagent Co., Ltd. bezogen. Methanol (99,5 %) wurde von Kermel bezogen. Toluol (99,0%) und Ethylacetat (99,5%) wurden von Concord bezogen. Hexan wurde von Beijing Chemical Factory bezogen.
Syntheseprozesse
Vorbereitung von Cs-Oleat
Die Cäsium-Oleat-Lösung wurde nach dem Ansatz von Kovalenko und Mitarbeitern hergestellt [31]. Kurz gesagt, 0,8 g Cs2 CO3 , 2,5 ml OA und 30 ml ODE wurden in einen Dreihalskolben gefüllt und unter Vakuum bei 120 °C 1 Stunde lang getrocknet. Als nächstes wurde der Kolben auf N2 umgestellt Atmosphäre und erhitzt auf 150°C, bis alle Cs2 CO3 aufgelöst.
Synthese von Mn-dotiertem CsPbCl3
Das Mn-dotierte CsPbCl3 wurde durch das Heißinjektionsverfahren synthetisiert. Normalerweise 0,0615 g PbCl2 , 0,08 g MnCl2 (H2 O)4 , 1 ml OAm, 1 ml OA und 5 ml ODE wurden in einen 25 ml-Dreihalskolben gegeben und 1 Stunde bei 120 °C im Vakuum getrocknet. Dann wurde der Kolben unter Stickstoff auf 180 °C erhitzt. Bei dieser Temperatur wurden anschließend 0,5 ml getrocknetes OAm und 0,5 ml getrocknetes OA injiziert, um die Pb- und Mn-Quellen zu solubilisieren. Dann wurden 0,4 ml Cs-Oleat schnell injiziert und nach 5 Sekunden wurde die Lösung mit einem Eisbad gekühlt. Die QDs wurden mit Hexanen und Ethylacetat im Verhältnis 1:3 ausgefällt. Dann wurde die Lösung bei 5500 U/min für 5 Minuten zentrifugiert. Nach der Zentrifugation wurden die Niederschläge in Toluol dispergiert.
Synthese von Bi-dotiertem Cs2 SnCl6
Das bidotierte Cs2 SnCl6 wurde durch hydrothermale Reaktionsmethode synthetisiert. Normalerweise 0,337 g CsCl, 0,189 g SnCl2 , 0,032 g BiCl3 Pulver und 4,0 ml 37%iger Salzsäure wurden in einem mit Teflon ausgekleideten Autoklaven (30 ml) versiegelt und 20 h auf 220 °C erhitzt. Nach der Reaktion wurde der Autoklav langsam auf Raumtemperatur abgekühlt und ein weißer Kristall von Bi-dotiertem Cs2 SnCl6 konnte durch Zentrifugation (3000 rpm, 2 min) getrennt werden.
Herstellung von LED-Geräten
UV-LED-Chips mit einer bei 365 nm zentrierten Emissionspeakwellenlänge wurden von Shine On Corp. gekauft SnCl6 Pulver wurde mit PMMA/Toluol-Lösung gemischt und auf den UV-LED-Chip aufgetragen. Als nächstes Mn-dotiertes CsPbCl3 QD-Lösung wurde in eine 1 ml transparente PMMA/Toluol-Lösung gegeben. Danach wird das Mn-dotierte CsPbCl3 Lösung wurde auf den UV-LED-Chip aufgetragen, der bereits mit Bi-dotiertem Cs2 . beschichtet war SnCl6 . Das Gerät wurde dann 30 min bei Raumtemperatur ausgehärtet.
Messung und Charakterisierung
Fluoreszenzemissionsspektren wurden auf einem Spektrometer von Ocean Optics durchgeführt. Die Absorptionsspektren der Proben wurden unter Verwendung eines Shimadzu UV-2550-Spektrophotometers gemessen. Für bidotiertes Cs2 SnCl6 diffuse Reflexionsspektren (R) wurden mit einem Spektrometer von Ocean Optics gemessen, und der Abs-Koeffizient α wurde unter Verwendung der Kubelka-Munk-Theorie (1 − R ) × (1 − R )/2R . Die Anregungsspektren und die zeitaufgelöste PL-Spektroskopie (TRPL) wurden mit einem Edinburgh FLS920 Fluoreszenzspektrometer gemessen. Die Morphologie der QDs wurde mit einem FEI Tecnai G2 Spirit TWIN Transmissionselektronenmikroskop (TEM) bei 100 kV erfasst. Rasterelektronenmikroskop (REM) und energiedispersive Röntgenspektroskopie (EDX) Messungen wurden von Quanta 450 FEG durchgeführt. Röntgenbeugungsmuster (XRD) von Perowskiten wurden mit einem Bruker D8 Advance Röntgendiffraktometer (Cu Kα:λ = 1,5406 Å). Die absoluten PL QYs der Proben wurden mit einem Fluoreszenzspektrometer (FLS920P, Edinburgh Instruments) erhalten, das mit einer Ulbrichtschen Kugel ausgestattet war, deren Innenseite mit BENFLEC beschichtet war. Helligkeit und Effizienz wurden mit dem Elektrolumineszenz-Messsystem ATA-1000 (Everfine in der Volksrepublik China) gemessen.
Ergebnisse und Diskussion
Zweifach dotiertes Cs2 SnCl6 Perowskit wurde nach dem bisherigen Ansatz mit geringen Modifikationen synthetisiert [33]. Die Abs- und PL-Spektren von Bi-dotiertem Cs2 SnCl6 sind in Abb. 1a dargestellt. Wie in Abb. 1a gezeigt, konnte der scharfe Abs-Peak bei etwa 375 nm den Übergängen vom Defektband (verursacht durch Bi-Dotierung) zum Wirtsleitungsbandminimum zugeordnet werden, was in guter Übereinstimmung mit früheren Berichten ist [33]. Das XRD-Muster weist auch auf die Bildung von Sn-basiertem Perowskit hin (Abb. 3a). Alle Beugungspeaks stimmten gut mit Cs2 . überein SnCl6 Kristallstruktur (ICSD #9023), und es wurden keine Verunreinigungsphasen nachgewiesen, was in guter Übereinstimmung mit einem früheren Bericht [33] ist. Das bidotierte Cs2 SnCl6 kann durch UV-Licht (365 nm) angeregt werden und zeigt helles blaues Licht mit dem PL-Emissionspeak bei 465 nm (Abb. 1a). Die volle Halbwertsbreite (FWHM) von Bi-dotiertem Cs2 SnCl6 beträgt 65 nm, und die QY von Bi-dotiertem Cs2 SnCl6 beträgt bis zu 76 %. Das PL-Anregungsspektrum (PLE) von Bi-dotiertem Cs2 SnCl6 gemessen (bei 465 nm detektiert) und in Abb. 1a dargestellt. Im PLE-Spektrum von Bi-dotiertem Cs2 . kann ein breiter Peak bei 350 nm beobachtet werden SnCl6 , die sich im Vergleich zum Abs-Spektrum leicht verschiebt. Eine ähnliche Variation wurde in einem früheren Bericht beobachtet [33]. Darüber hinaus ist dieses Bi-dotierte Cs2 SnCl6 zeigt eine hervorragende Stabilität. Nach 300 h Bestrahlung mit UV-Licht ist die PL-Intensität nahezu konstant. Das Perowskit-Pulver kann seinen QY beibehalten, nachdem es 3 Monate lang der Luft ausgesetzt war (25 °C, relative Luftfeuchtigkeit 35–50%).
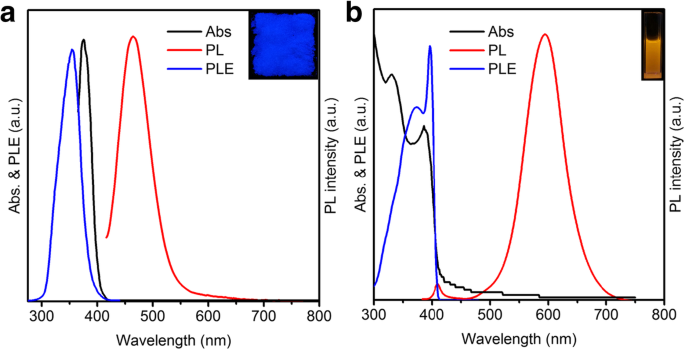
a Abs-, PL- und PLE-Spektren von Bi-dotiertem Cs2 SnCl6 QDs. Der Einschub ist die Fotografie der Probe unter UV-Anregung. b Abs-, PL- und PLE-Spektren von Mn-dotiertem CsPbCl3 QDs. Der Einschub ist das Foto der Probe unter UV-Anregung
Mn-dotiertes CsPbCl3 QDs wurden nach einem etablierten Verfahren mit geringfügigen Modifikationen hergestellt [32]. Wie in Abb. 1b gezeigt, wird der Abs-Peak bei etwa 400 nm beobachtet, der Exziton-Abs von CsPbCl3 . zugeordnet wird . Unter UV-Licht (365 nm) zeigt die QD-Lösung eine leuchtend orange Emission (Abb. 1b, Einschub). Im PL-Emissionsspektrum werden zwei Peaks beobachtet, die bei 405 nm bzw. 595 nm zentriert sind (Abb. 1b). Der Peak bei 405 nm wird dem CsPbCl3 . zugeordnet Wirt, während die breite Emissionsbande mit der FWHM bei etwa 80 nm Mn 2+ . zugeordnet wird d-d-Emission [31, 34]. Die QY unseres Produkts erreicht 52 %, was mit anderen Berichten vergleichbar ist [32, 35, 36]. Das PLE-Spektrum von Mn-dotiertem CsPbCl3 wurde gemessen (bei 595 nm nachgewiesen) und in Abb. 1b dargestellt. Das PLE-Spektrum von Mn-dotiertem CsPbCl3 folgt eng dem Abs-Spektrum, das zeigt, dass der starke PL-Peak der Mn-Emission vom Exziton von Perowskit stammt. Die so hergestellten QDs weisen eine ausgezeichnete Stabilität auf, die ihre Emissionseigenschaften unter Umgebungsatmosphären für mindestens 3 Monate (25 °C, relative Luftfeuchtigkeit 35–50 %) bewahren kann.
Die PL-Lebensdauer von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 wurden mit TRPL gemessen. Wie in Abb. 2a gezeigt, ist die Zerfallskurve von Bi-dotiertem Cs2 SnCl6 wird durch eine Exponentialfunktion gut angepasst und die Lebensdauer beträgt 375 ns, was gut mit dem vorherigen Bericht [33] übereinstimmt. Wie für Mn-dotiertes CsPbCl3 QDs, die Lebensdauer ist länger (1,7 ms), was dafür spricht, dass sie vom spinverbotenen Ligandenfeldübergang des Mn 2+ . stammt Ionen [32].
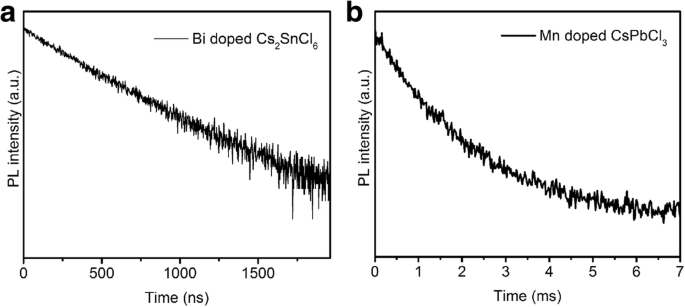
a PL-Abfall und angepasste Kurven von Bi-dotiertem Cs2 SnCl6 . b PL-Zerfall und angepasste Kurven von Mn-dotiertem CsPbCl3
Abbildung 3b zeigt das SEM-Bild von Bi-dotiertem Cs2 SnCl6 Perowskit. Das kugelförmige Bi-dotierte Cs2 SnCl6 Perowskit mit einem Durchmesser von 53 nm ist zu beobachten. EDX- und Mapping-Bilder bestätigen weiterhin das Vorhandensein von Bi in Cs2 SnCl6 (Abb. 3j, c–f). Das Verhältnis von Cs, Sn, Bi und Cl beträgt 1:0,62:0,14:3, was gut mit anderen Berichten übereinstimmt [33]. Abbildung 3g zeigt das TEM-Bild von Mn-dotiertem CsPbCl3 QDs. Wie zu sehen ist, ist das Mn-dotierte CsPbCl3 QDs zeigen eine kubische Morphologie mit einer durchschnittlichen Größe von ∼ 12 nm. Wie aus Abb. 3k ersichtlich ist, beträgt das Verhältnis von Cs, Pb, Mn und Cl 1:0,77:0,19:2,68. Das HRTEM-Bild zeigt die Gitterränder des Mn-dotierten CsPbCl3 QDs, das einen interplanaren Abstand von 3.67 Å aufweist und gut mit dem der (101)-Ebene übereinstimmt (Abb. 3h). Das SAED-Muster ist in Fig. 4c gezeigt. Wir sehen, dass die QDs eine tetragonale Kristallstruktur mit entsprechenden (101) und (200) Ebenen besitzen (Abb. 3i) [31]. XRD-Muster des Mn-dotierten CsPbCl3 QDs zeigen, dass die Beugungspeaks der tetragonalen Phase entsprechen, was mit den SAED-Ergebnissen übereinstimmt.
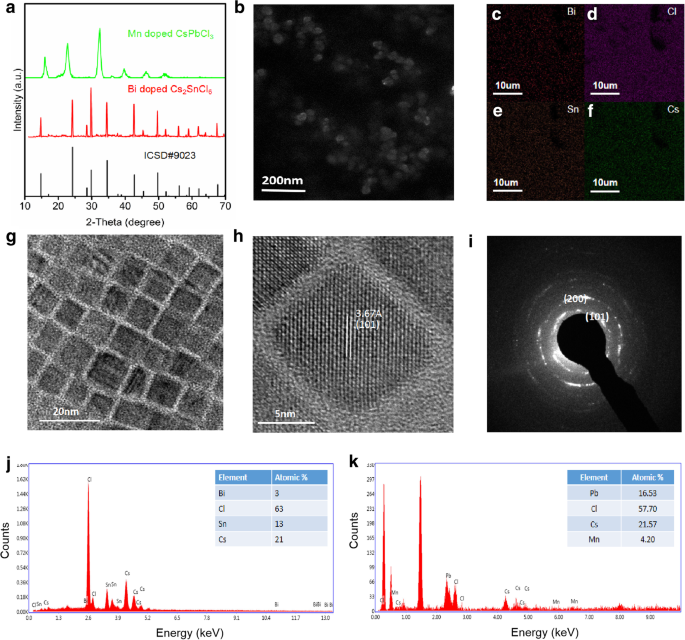
a XRD-Muster von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 QDs, b das REM-Bild von Bi-dotiertem Cs2 SnCl6 , c –f die Kartierungsbilder von Bi-dotiertem Cs2 SnCl6 , g TEM-Bild von Mn-dotiertem CsPbCl3 Perowskit-QDs, h hochauflösendes Transmissionselektronenmikroskopie(HRTEM)-Bild von Mn-dotiertem CsPbCl3 QDs, i Selected-Area-Elektronenbeugungsmuster (SAED) von Mn-dotiertem CsPbCl3 , j das EDX-Spektrum und Bi-dotiertes Cs2 SnCl6 , und k das EDX-Spektrum von Mn-dotiertem CsPbCl3
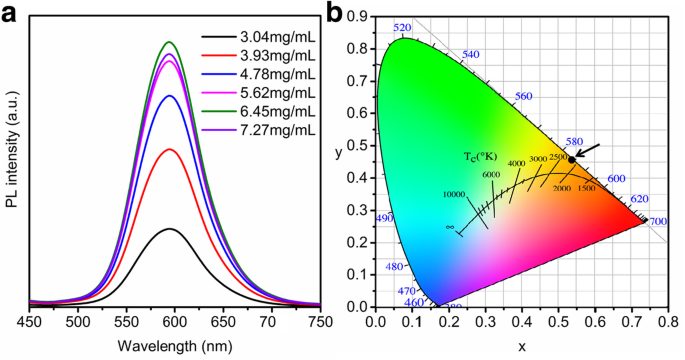
a PL-Spektren von Mn-dotiertem CsPbCl3 QDs in unterschiedlicher Konzentration. b Farbkoordinatenvariation von Mn-dotiertem CsPbCl3 QDs in verschiedenen Konzentrationen
Um die optimale Mn-Dotierungskonzentration zu erhalten, werden der Emissionspeak und die FWHM-Variation analysiert und in 4 gezeigt. Aus 4a ist ersichtlich, dass die PL-Intensität mit der Konzentration von Mn 2+ zunimmt. sup> wird von 3,04 auf 6,45 mg/ml erhöht. Mn 2+ . weiter erhöhen Konzentration führt zu einer Abnahme der PL-Intensität, was auf den Selbst-Abs-Effekt bei hoher Konzentration zurückzuführen ist. Während des gesamten Prozesses bleiben die PL-Peakposition und die FWHM gleich. Mit anderen Worten, die Änderung von Mn 2+ Die Konzentration hat keinen Einfluss auf den PL-Emissionspeak und die FWHM, die auch durch die Farbkoordinatenkarte bestätigt werden (Abb. 4b). Unabhängig davon, wie sich die Konzentration ändert, werden die Farbkoordinaten grundsätzlich bei (0,535, 0,460) (die schwarzen Punkte) gehalten. Daher wird eine Konzentration von 6,45 mg/ml als optimale Konzentration angenommen.
Eine WLED wurde durch Beschichtung von blau emittierendem Bi-dotiertem Cs2 . hergestellt SnCl6 Pulver und orange emittierendes Mn-dotiertes CsPbCl3 QDs auf einen handelsüblichen 365 nm LED-Chip (Abb. 5a). Wie in Abb. 5b gezeigt, sind im EL-Spektrum der WLED zwei offensichtliche Peaks zu erkennen, die auf Bi-dotiertes Cs2 . zurückzuführen sind SnCl6 und Mn-dotiertes CsPbCl3 . Die Beständigkeit dieser beiden Peaks weist darauf hin, dass im Herstellungsprozess kein Anionenaustausch und andere chemische Reaktionen stattfinden. In hellem Weißlicht mit Farbkoordinaten von (0,334, 0,297) kann die korrelierte Farbtemperatur von 5311 K beobachtet werden, wenn die WLED mit 15 mA betrieben wird (Abb. 5b und c). Die höchste Lichtausbeute und Leuchtdichte der WLED erreichen bis zu 20,8 lm/W und 78.000 cd m −2 , die mit anderen UV-Chip-basierten WLEDs vergleichbar sind [4, 37,38,39].
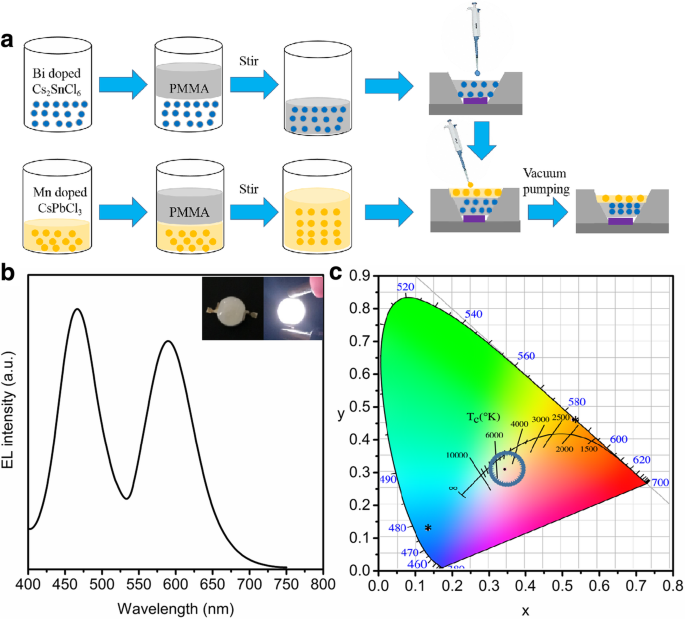
a Schema des Herstellungsprozesses der WLED; b Elektrolumineszenz-(EL)-Spektrum von WLED; c Farbkoordinaten des WLED-Geräts, Mn-dotiertes CsPbCl3 QDs und Bi-dotiertes Cs2 SnCl6。 (der schwarze Punkt innerhalb des Kreises ist die weiße Farbkoordinate und das Sternchen steht für den blauen und orangefarbenen Perowskit). Die Einsätze sind das Foto der WLED
Die Emissionsspektren der WLED im Werkszustand mit den Treiberströmen von 5 mA-120 mA sind in Abb. 6a dargestellt. Die detaillierten Charakteristika einschließlich Farbkoordinaten, CCT und CRI der WLED im Herstellungszustand sind in Tabelle 1 gezeigt. Wie in Fig. 6a gezeigt, nehmen die EL-Intensitäten beider Peaks mit zunehmendem Strom allmählich zu und zeigen keine Sättigung. Außerdem trat bei unterschiedlichen Injektionsströmen keine offensichtliche Verschiebung der Peakposition für das EL-Spektrum auf. Farbkoordinaten dieser PL-Spektren sind in Fig. 6b gezeigt. Die Farbwertkoordinaten zeigen eine geringe Verschiebung (x < 0.02, y < 0,02) nach links mit zunehmenden Antriebsströmen. Wir können beobachten, dass die EL-Intensität von Bi-dotiertem Cs2 SnCl6 steigt schneller an als die des Mn-dotierten CsPbCl3 , was dazu führen kann, dass sich die Chromatizitätskoordinaten nach links bewegen. Jedoch verursachen die FWHM-Variation und die Verschiebung des Emissionspeaks auch eine Verschiebung der Farbortkoordinaten. Wie oben besprochen, bleibt die Emissionsspitze mit der Zunahme der Ströme unverändert. Aufgrund ihrer breiten FWHM sind die Emissionspeaks von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 Überlappung, wodurch die FWHM-Variation schwer zu analysieren ist. Daher wurden monochromatische LEDs hergestellt, um jede FWHM-Variation zu analysieren. Abbildung 6c und d zeigen die Emissionsspektren von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 LEDs bzw. Im weiten Strombereich von 5 bis 120 mA tritt keine Verschiebung der PL-Emissionspeaks auf, was gut mit den WLED-Ergebnissen übereinstimmt (Abb. 6c und d). Die FWHM-Variation der beschichteten LEDs bei unterschiedlichen Strömen ist in Abb. 6e dargestellt. Wie zu sehen ist, sind die FWHMs von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 sind nahezu konstant, was darauf hinweist, dass die Variation der Farbkoordinaten der WLED nur aus der Intensitätsänderung der EL resultiert. Der Unterschied der EL-Intensitätsvariation kommt möglicherweise von der unterschiedlichen thermischen Stabilität von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 , da die Erhöhung der Ströme dazu führen kann, dass die Temperatur des LED-Chips ansteigt. Diese unbedeutende Änderung kann weiter gemildert werden, indem eine LED-Struktur vom entfernten Typ verwendet wird. Darüber hinaus ist die Langzeitbetriebsstabilität aus Abb. 6f ersichtlich. Nach einer kontinuierlichen Arbeit von 300 h sind die EL-Intensitäten der beiden Bi-dotierten Cs2 SnCl6 und Mn-dotiertes CsPbCl3 weniger als 10 % zurückgegangen sind. Tatsächlich beträgt die Halbwertszeit der WLED 3000 h, was weit besser ist als die von I-haltigen Perowskiten [15, 17, 18, 40]. Wie aus Tabelle 2 ersichtlich ist, sinkt die PL-Intensität, nachdem die WLED wie vorbereitet bei 15 mA über 50 h weiter arbeitet, auf 99% des Originals, was viel besser ist als in anderen Berichten [17, 18, 36, 40, 41,42,43,44]. Nach 100 Stunden Arbeit sinkt die PL-Intensität nur auf 97%.
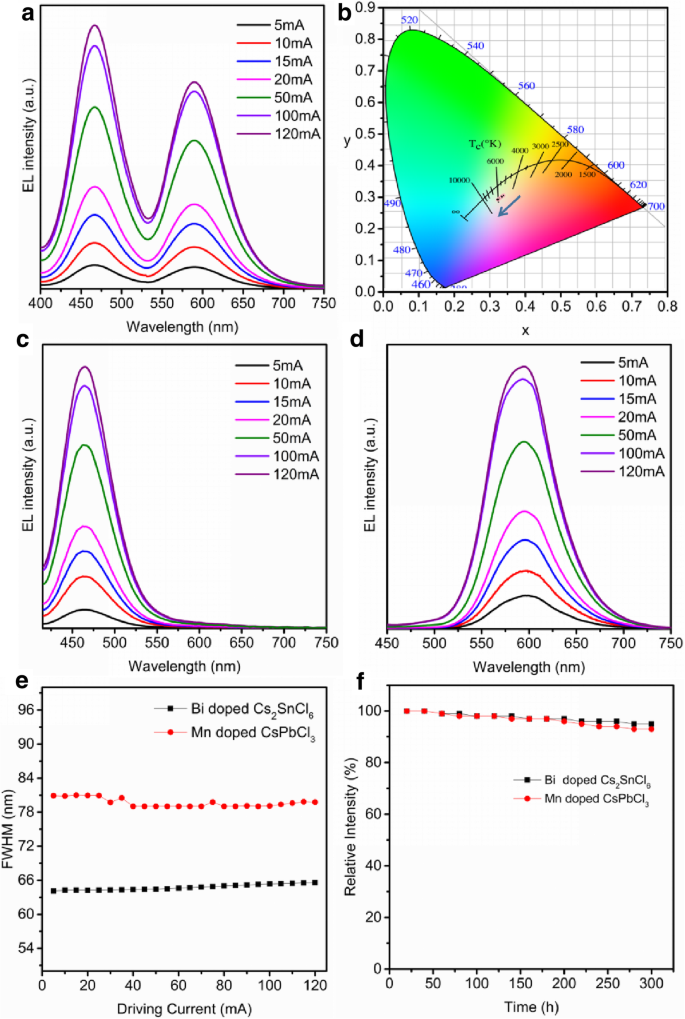
a PL-Spektren von WLED-Geräten unter verschiedenen Injektionsströmen, b Änderung der Chromatizitätskoordinaten des WLED-Geräts unter verschiedenen Injektionsströmen, c PL-Spektren von Bi-dotiertem Cs2 SnCl6 LED-Gerät unter verschiedenen Injektionsströmen, d PL-Spektren von Mn-dotiertem CsPbCl3 LED-Gerät unter verschiedenen Injektionsströmen, e die FWHM-Variation von Bi-dotiertem Cs2 SnCl6 und Mn-dotiertes CsPbCl3 , f die in verschiedenen Arbeitszeitintervallen gemessene PL-Intensitätsvariation
Heutzutage werden Perowskit-Heteroübergänge verwendet, um die physikalischen Eigenschaften von Perowskiten zu verbessern [45, 46]. Normalerweise können diese Heteroübergänge die Vorzüge beider Materialien integrieren, wie Perowskit-Polymer-Volumen-Heterostruktur, Perowskit-PbS-Kern-Schale-Struktur und Perowskit-plasmonisches Au- oder Ag-Verbundmaterial [47,48,49], was die Effizienz steigern kann. Aufgrund der geringen Stabilität von Perowskit ist es jedoch schwierig, einen Heteroübergang zu entwerfen und herzustellen. Außerdem können diese Perowskit-Heteroübergänge im Vergleich zu reinem Perowskit nicht stabil sein.
Schlussfolgerung
Zusammenfassend haben wir hochwertiges blau emittierendes Wismut-dotiertes Cs2 . kombiniert SnCl6 Perowskit mit orange emittierendem Mn-dotiertem CsPbCl3 QDs zur Herstellung von WLED. Da sie alle das gleiche Anion von Cl enthalten, kann eine Anionenaustauschreaktion vermieden werden. Außerdem orange emittierendes Mn-dotiertes CsPbCl3 QDs zeigen eine bessere Stabilität im Vergleich zu jodhaltigen Gegenstücken. Die WLED mit den Farbkoordinaten (0,334, 0,297) wird durch Abstimmung des Verhältnisses von ihnen gewonnen. Darüber hinaus weisen die WLEDs eine ausgezeichnete Langzeitbetriebsstabilität auf, die unseres Wissens bei weitem die stabilste unter den WLEDs auf Perowskit-Basis ist. Wir glauben, dass unsere Ergebnisse neue Wege für die Erforschung neuer bleifreier WLED auf Perowskit-Basis eröffnen werden.
Abkürzungen
- QDs:
-
Quantenpunkte
- WLEDs:
-
Weiße Leuchtdioden
- QY:
-
Quantenausbeute
- PCE:
-
Leistungsumwandlungseffizienz
- PL:
-
Photolumineszenz
- Cs2 CO3 :
-
Cäsiumcarbonat
- PbCl2 :
-
Blei(II)-chlorid
- CsCl:
-
Cäsiumchlorid
- OA:
-
Ölsäure
- ODE:
-
1-Oktadezän
- MnCl2· (H2 O)4 :
-
Manganchlorid-Tetrahydrat
- OAm:
-
Oleylamin
- SnCl2 :
-
Zinnchlorid
- BiCl3 :
-
Wismutchlorid
- PMMA:
-
Polymethylmethacrylat
- HCl:
-
Salzsäure
- TRPL:
-
Zeitaufgelöste PL-Spektroskopie
- TEM:
-
Transmissionselektronenmikroskop
- SEM:
-
Rasterelektronenmikroskop
- EDX:
-
Energiedispersiver Röntgendetektor
- XRD:
-
Röntgenbeugung
- PLE:
-
PL-Erregung
- FWHM:
-
Volle Breite auf halbem Maximum
- EL:
-
Elektrolumineszenz
- HRTEM:
-
Hochauflösende Transmissionselektronenmikroskopie
- SAED:
-
Ausgewählte Bereichselektronenbeugung
Nanomaterialien
- Osteoblasten-Reaktion auf kupferdotierte mikroporöse Beschichtungen auf Titan für eine verbesserte Knochenintegration
- Ein kurzer Fortschrittsbericht zu hocheffizienten Perowskit-Solarzellen
- Dielektrische Metaoberflächen höherer Ordnung für hocheffiziente Polarisationsstrahlteiler und optische Wirbelgeneratoren
- Grüne Synthese von InP/ZnS-Kern/Schale-Quantenpunkten für die Anwendung in schwermetallfreien Leuchtdioden
- Hocheffiziente invertierte Perowskit-Solarzellen mit CdSe-QDs/LiF-Elektronentransportschicht
- Sequentiell dampfgezüchteter Hybridperowskit für planare Heterojunction-Solarzellen
- Die optimale Titan-Vorstufe zur Herstellung einer kompakten TiO2-Schicht für Perowskit-Solarzellen
- Perowskit-Solarzellen, hergestellt unter Verwendung eines umweltfreundlichen aprotischen polaren Additivs aus 1,3-Dimethyl-2-imidazolidinon
- Fast Effizienz-Droop-Free AlGaN-basierte UV-Licht emittierende Dioden mit einer speziell entwickelten Übergitter-Elektronenblockierschicht vom p-Typ für eine hohe Mg-Dotierungseffizienz
- Perowskit-Leuchtdioden mit hoher Leuchtdichte mit hochpolarem Alkohollösungsmittel, das PEDOT:PSS als Lochtransportschicht behandelt



