Direktes Wachstum von Graphen auf einem Isolator unter Verwendung eines flüssigen Vorläufers über eine nanostrukturierte Kohlenstoff-Nanoröhre im Zwischenzustand
Zusammenfassung
Die Synthese hochwertiger Graphenschichten auf isolierenden Substraten ist für zukünftige graphenbasierte Hochgeschwindigkeitselektronik sehr wünschenswert. Neben der Verwendung gasförmiger Kohlenwasserstoffquellen haben sich in letzter Zeit auch feste und flüssige Kohlenwasserstoffquellen als vielversprechend für ein qualitativ hochwertiges Graphenwachstum erwiesen. Hier berichte ich über das Wachstum von ein- bis mehrschichtigem Graphen durch chemische Gasphasenabscheidung direkt auf SiO2 Substrat unter Verwendung von Ethanol als flüssigem Kohlenwasserstoff-Ausgangsmaterial. Der Wachstumsprozess von Graphen wurde als Funktion der Glühtemperatur sowie verschiedener Saatschichten systematisch untersucht. Interessanterweise wurde festgestellt, dass die durch die thermische Zersetzung von Ethanol erzeugten Kohlenstoffatome sp 2 . bilden Kohlenstoffnetzwerk auf SiO2 Oberfläche, wodurch Nanographen-Flocken über eine Kohlenstoff-Nanoröhrchen-Zwischenstufe im nanostrukturierten Zustand gebildet werden. Diese Arbeit könnte den Weg zu einem Verständnis für wirtschaftliches und katalysatorfreies Graphenwachstum ebnen, das mit aktuellen Siliziumverarbeitungstechniken kompatibel ist, und es kann auf eine Vielzahl von isolierenden Oberflächen wie Quarz, Saphir und Quarzglas angewendet werden.
Einführung
Die Synthese von hochwertigem Graphen auf Isolatoren ist für die Entwicklung von elektronischen Geräten auf Graphenbasis sehr wünschenswert, um die schädlichen Metalleffekte zu vermeiden, die durch das konventionelle metallkatalytisch unterstützte Graphenwachstum unter Verwendung von chemischer Gasphasenabscheidung (CVD) verursacht werden [1,2,3,4] . Eine der möglichen Methoden, um Graphenwachstum auf Isolatoren zu erreichen, besteht in der Einführung eines Metallkatalysators in die Dampfphase, was kürzlich von Teng et al. demonstriert wurde. [5] und Kim et al. [6]. Das Katalysatormetall in einer Dampfphase würde mit Kohlenstoffvorläufern in der Gasphase sowie auf der Oberfläche des isolierenden Substrats reagieren, was zu einer qualitativ hochwertigen, einheitlichen Graphenbildung führt. Eine andere Möglichkeit besteht darin, Graphen direkt auf dielektrischen Isolatoren zu züchten, ohne einen Metallkatalysator zu verwenden, was eine dringend benötigte Technik für seine elektronische Anwendung ist. In letzter Zeit haben viele Forschungsgruppen das direkte Wachstum von Graphen auf verschiedenen dielektrischen Substraten verfolgt, darunter hexagonales Bornitrid (h-BN) [7, 8], Glas [9,10,11], Quarz [12], Saphir [13, 14 ], Si3 N4 [15,16,17], SiO2 [18,19,20,21] und High-k-Dielektrika wie MgO [22, 23], ZrO2 [23] und TiO2 [24] unter Verwendung von CVD ohne Metallkatalysatoren. Das auf den obigen Substraten gewachsene Graphen weist jedoch eine schlechte Qualität auf, die weder mit der von Graphen auf Metallsubstraten wie Ni [1] und Cu [3] noch mit epitaktischem Graphen auf SiC [25] vergleichbar ist. Darüber hinaus ist auch der Graphen-Wachstumsmechanismus der obigen Systeme nicht gut verstanden.
Neben gasförmigen Vorläufern ist das Wachstum von Graphen unter Verwendung einer breiteren Palette potenzieller Rohstoffe wie fester und flüssiger Kohlenwasserstoffe sehr gefragt, um seine technologische Anwendung zu erreichen. Seit den letzten 5 Jahren haben viele Gruppen Graphen unter Verwendung von festem und flüssigem Kohlenwasserstoff-Ausgangsmaterial außer Methan unter Verwendung der überarbeiteten CVD-Route synthetisiert [26,27,28,29]. In den obigen Arbeiten wurden Metallkatalysatoren für die Graphennukleation verwendet. Darüber hinaus erfordert die Synthese von hochwertigem Graphen unter Verwendung der oben genannten Kohlenwasserstoff-Einsatzmaterialien ein tiefes Verständnis des Wachstumsmechanismus. Kürzlich wurde von Zhao et al. [30], wobei der Wachstumsmechanismus als selbstlimitierend beschrieben wird. Die Idee hinter der Wahl von Ethanol als Kohlenstoffquelle beruht auf den folgenden Vorteilen, darunter umweltfreundlich, vergleichsweise billiger, einfacher zu verwenden und weniger entflammbar als hochreines Methan, wodurch die Graphenherstellung leichter zugänglich wird [28]. Unter Verwendung von Ethanol als Kohlenstoffquelle wird hochwertiges Monolayer-Graphen mit einem I D /Ich G von ∼ 0.04 bei einer niedrigeren Reaktionstemperatur von ~ 800 °C wurde von Zhao et al. [30], was darauf hinweist, dass Ethanol Methan bei der CVD-Synthese von Graphen auf Cu-Folie überholt. Obwohl viele Gruppen den Wachstumsmechanismus von Graphen auf Isolatoren unter Verwendung von Methan [13, 31] und Graphen auf Metallsubstraten unter Verwendung von festen und flüssigen Kohlenwasserstoff-Ausgangsmaterialien [26, 27, 30] beschrieben haben, ist jedoch ein umfassender Wachstumsmechanismus von Graphen direkt auf Isolatoren unter Verwendung von flüssigem . bekannt Kohlenwasserstoff-Ausgangsmaterial fehlt in der hochmodernen Forschung und erfordert weitere Exploration.
In der vorliegenden Arbeit schlage ich eine neuartige Wachstumstechnik vor, die die direkte Bildung von ein- bis mehrschichtigem Graphen auf SiO2 . ermöglicht unter Verwendung von Ethanol als Kohlenstoffvorläufer in CVD und untersuchen systematisch seinen Wachstumsprozess in Abhängigkeit von der Glühtemperatur und verschiedenen Saatschichten. Das Hauptmerkmal des Wachstumsmechanismus umfasst die folgenden Schritte:(1) Zersetzung von flüssigem Kohlenwasserstoff in einer Gasphase; (2) Graphitisieren von Kohlenstoffatomen auf Siliziumoxidoberflächen, um Zwischenphasen zu bilden, einschließlich Kohlenstoff-Nanocluster und Kohlenstoff-Nanoröhrchen (CNTs); (3) Ätzen durch Wasserstoff bei erhöhter Temperatur, das zur Bildung von graphitischen Nanobändern führt, die als Keimbildungsstellen für das Graphenwachstum wirken; und (4) Kombination dieser graphitischen Nanobänder, um nach längerer Temperzeit kontinuierliche Graphenfilme hoher Qualität zu bilden.
Methoden
Wachstum von Graphen auf SiO2
Graphenwachstum auf Siliciumdioxid wurde durch chemische Gasphasenabscheidung bei Atmosphärendruck (APCVD) unter Verwendung von flüssigem Kohlenwasserstoff-Ausgangsmaterial Ethanol als Kohlenstoffquelle durchgeführt. Vor dem Wachstum SiO2 . im 300-nm-Wafermaßstab /Si-Substrate wurden mit Aceton und Isopropylalkohol (IPA) mit Ultraschall gereinigt, gefolgt von N2 Gasspülung. Diese Substrate wurden in den stromaufwärts liegenden Gasstrom eingebracht und in Gegenwart von H2 . mit einer Aufheizrate von 10 °C/min auf 1100 °C erhitzt (40 sccm) und Ar (250 sccm) bei Umgebungsdruck. Bei dieser Temperatur wurden die Substrate 5–10 min gehalten, um die Temperaturstabilität aufrechtzuerhalten, gefolgt von einer Graphen-Wachstumsphase von 5 min. Während dieser Wachstumsphase wurde Trägergas Ar (10 sccm) durch ein U-förmiges Quarzrohr geleitet, das Ethanol enthielt, um diesen Kohlenwasserstoffdampf in das horizontale Quarzrohr (Reaktionszone) in CVD zu befördern, wie in Zusatzdatei 1:Abbildung S1 gezeigt. Dieses Experiment wurde für 10-, 15- bzw. 60-minütiges Wachstum wiederholt, gefolgt von Abkühlen auf Raumtemperatur, um einen kontinuierlichen Graphenfilm auf SiO2 . zu erhalten Substrate.
Für das keimschichtunterstützte Graphenwachstum wird das SiO2 Substrate wurden vor dem Wachstum mit verschiedenen Saatmaterialien wie abgeblättertem Graphen, Holzkohle, Elektronenzyklotronresonanz(ECR)-Graphen und CVD-Graphen bedeckt, und Trägergas Ar (4 sccm) wurde bei 1100 °C für eine Stunde Wachstumszeit zugeführt. Nach dem Wachstum wurden die Proben durch Raman-Spektroskopie charakterisiert, die die charakteristischen Merkmale von gewachsenen Kohlenstoff-Nanostrukturschichten einschließlich CNT und Graphen aufdeckt und auch die Identifizierung von ein- und mehrschichtigem Graphen ermöglicht. Andere Charakterisierungsmethoden, einschließlich Transmissionselektronenmikroskopie (TEM), Rasterelektronenmikroskopie (REM) und Röntgenphotoelektronenspektroskopie (XPS), wurden verwendet, um Kristallinität, Oberflächenmorphologie und Zusammensetzungsanalyse von Graphenschichten im Zustand der Herstellung zu untersuchen.
Wachstum von ECR-CVD-Graphen für die Saatschicht
Kommerziell erhältliches 300-nm-SiO2 /Si-Substrat wurde zuerst in Aceton, Isopropylalkohol und entionisiertem Wasser gereinigt. Nach der Reinigung wurde das Substrat in die ECR-CVD-Kammer gelegt. Das Schema der ECR-CVD-Kammer ist in Zusatzdatei 1 dargestellt:Abbildung S2. Wenn das Vakuum 1 × 10 −6 . erreicht hat Torr, Ar-Fluss wurde mit einer Rate von 5 sccm eingeleitet, und das Plasma wurde bei einem Partialdruck von 6 × 10 –3 . gezündet Torr bei 400 W für 5 min, um organische Rückstände von der Substratoberfläche zu entfernen. Die Temperatur wurde dann unter Hochvakuum auf 600ºC erhöht. Wenn sich die Temperatur stabilisiert hat, fließen Argon und Ethylen (Ar:C2 H4 = 0,3:0,15 sccm) wurden für 30 s geöffnet und die Plasmaleistung wurde auf 1600 W eingestellt, gefolgt von einem Tempern in 1 sccm H2 5 min bei gleicher Temperatur fließen lassen. Schließlich wurde die Probe im Hochvakuum auf Raumtemperatur abgekühlt.
Ergebnisse und Diskussion
CVD-Wachstum von Graphen mit Ethanol
Ethanol wurde als Kohlenstoffquelle für das Wachstum von Graphen auf SiO2 . verwendet Substrat unter Verwendung eines CVD-Systems auf Ethanoldampfbasis, wie in Zusätzliche Datei 1 gezeigt:Abbildung S1. Kurz gesagt wurde das Graphenwachstum bei 1100°C in Gegenwart von H2 . durchgeführt und Ar mit einer Fließgeschwindigkeit von 40 sccm bzw. 250 sccm bei Umgebungsdruck. Abbildung 1a–d zeigt die REM-Aufnahmen verschiedener Kohlenstoff-Nanostrukturen, die auf SiO2 . gewachsen sind Substrat für verschiedene Wachstumszeiten im Bereich von 5–60 min, und ihre repräsentativen Mikro-Raman-Spektren sind in Abb. 1e–h dargestellt. Bei einer Wachstumsdauer von 5 Minuten wird beobachtet, dass Kohlenstoff-Nanopartikel gebildet werden, dargestellt durch große und kleine weiße Kreise (Abb. 1a). Diese Nanopartikel sind von Natur aus amorph, wie das Raman-Spektrum bestätigt (Abb. 1e) [32]. Der Einschub zeigt das Raman-Merkmal im Frequenzbereich von 50–300 cm −1 . Bei einer Wachstumszeit von 10 min wandeln sich einige der Kohlenstoff-Nanopartikel in CNTs um, wie in Abb. 1b zu sehen ist. Die Aufspaltung des Raman-G-Peaks tritt bei etwa 1560 cm −1 . auf (Abb. 1f) mit Sternchen markiert, was auf die spiralförmige Eigenschaft des C-Netzwerks zurückzuführen ist und vermutlich charakteristisch für CNTs ist [33, 34]. Außerdem Beobachtung eines starken radialen Atmungsmodus (RBM)-Peaks nahe 150 cm −1 bestätigt die Bildung von Single-Wall Carbon Nanotubes (SWCNTs) [35, 36]. Nach 15-minütigem Wachstum gibt es eine vollständige Umwandlung von CNTs in Graphen, die mit einigen Defektstrukturen auftrat, was durch die starke D-Peakintensität bestätigt wurde (Abb. 1g). Die weißen Bereiche im REM-Bild entsprechen ein- bis mehrschichtigem Graphen, wobei die schwarzen Bereiche das Substrat sind. Bei einer weiteren Verlängerung der Wachstumszeit auf 60 min wurde eine vollständige Bedeckung des Graphens mit weniger Defekten aus dem REM-Bild beobachtet (Abb. 1d). Darüber hinaus bestätigten Raman-Spektren auch die Bildung von Graphen mit einem relativ geringen Defekt, der aus einer reduzierten D-Peakintensität resultiert (Abb. 1h).
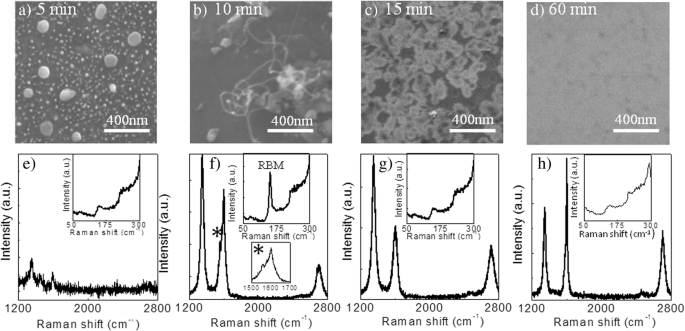
SEM-Bilder von kohlenstoffbasierten Nanostrukturen, die direkt auf Siliziumdioxid bei 1100 °C gewachsen sind, für eine Wachstumszeit von a 5 min, b 10 min, c 15 min und d 60 min. e –h Ihre jeweiligen Raman-Spektren im Frequenzbereich 1200 bis 2800 cm −1 . Die Raman-Funktionen im Frequenzbereich 50–300 cm −1 sind als Einschübe in e . dargestellt –h . G-Band-Aufspaltung in f ca. 1560 cm −1 markiert als Sternchen und das Vorhandensein des RBM-Peaks in der Nähe von 150 cm −1 zeigt die Bildung von SWCNT an
Darüber hinaus wurde das Wachstum bei einer höheren Wachstumstemperatur von 1150°C unter Verwendung eines reduzierten Trägergasstroms (Ar) von 3 sccm durchgeführt. Abbildung 2a–d zeigt die SEM-Bilder des Graphens, das für verschiedene Wachstumszeiten im Bereich von 2 bis 10 h gewachsen ist, und ihre repräsentativen Raman-Spektren sind in den Abbildungen 2e–h dargestellt. Für eine kurze Wachstumszeit (2 h) ist das Substrat mit sehr wenigen Graphenflocken bedeckt, die sowohl aus REM- als auch aus Raman-Daten beobachtet wurden. Wenn sich die Wachstumsperiode auf 4 h, 8 h und 10 h erstreckt, nimmt die Dichte der Graphenflocken zu und das Substrat wird hauptsächlich mit Monolayer-Bedeckung (Flocken mit weißem Kontrast) und wenig Doppelschicht-Bedeckung (Flocken mit weißem und schwarzem Kontrast) gefüllt, da bestätigt durch ihre Raman-Analyse (I 2D /Ich G ~ 1.5). Aber es gibt keine systematische Änderung in I 2D /Ich G Verhältnis sowie die Dichte der Flocken, die über die 4-h-Wachstumszeit hinaus beobachtet wurden. Das untere Feld Fig. 2i zeigt einige stark vergrößerte SEM-Bilder von Graphenflocken aus Fig. 2d, in denen hexagonal geformte Graphenflocken in zweischichtigen und dreischichtigen Regionen vollständig sichtbar sind. Die obige Beobachtung zeigt, dass eine längere Wachstumszeit die Graphenkeimbildungsdichte erhöht, gefolgt von einer Sättigung nach einer bestimmten Schwellenzeitdauer, was impliziert, dass die Keimstellen für die Keimbildung wenige sind und nach dem anfänglichen Wachstum eine Sättigung erreichen. Obwohl die Ausbeute des Graphenwachstums mit dieser Technik ~ 80% beträgt, was sehr geringer ist als die von CVD-Graphen, das mit gasförmigen Vorläufern gezüchtet wurde (~ 95%) [3], hat es jedoch einen Vorteil in Bezug auf katalysatorfreies Graphenwachstum direkt auf ein isolierendes Substrat, das die Notwendigkeit eines komplizierten Transferprozesses nach dem Wachstum vermeidet.
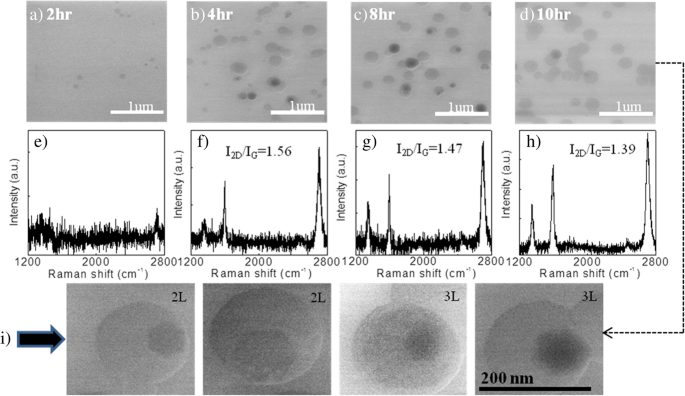
SEM-Bilder von Graphen, das direkt auf Siliziumdioxid bei 1150°C gezüchtet wurde, für eine Wachstumszeit von a 2 h, b 4 h, c 8 h und d 10 Uhr. Ihre repräsentativen Raman-Spektren sind in e . gezeigt –h . Das Ich 2D /Ich G Verhältnis für 4-h-, 8-h- und 10-h-gewachsenes Graphen wird auf 1,56, 1,47 bzw. 1,39 geschätzt. Unterseite i präsentiert einige hochvergrößerte SEM-Bilder von zweischichtigen und dreischichtigen Graphenflocken aus d . Die Körner mit größerer Größe und geringerem Kontrast sind erste Graphenschichten, und diejenigen mit kleinerer Größe und höherem Kontrast entsprechen der zweiten und dritten Schicht. Der Maßstabsbalken ist für alle gleich
Abbildung 3 zeigt das TEM-Bild mit geringer Vergrößerung einer Graphen-Flake, die 4 h lang bei 1150 °C hergestellt wurde (Abb. 2b), die sowohl aus einschichtigen als auch aus zweischichtigen Regionen mit einigen Defekten besteht. Das einschichtige Graphen (im rechten Teil gezeigt) besteht aus hexagonalen Kohlenstoffgittern, die man an der Fourier-Transformation des Elektronenbeugungsmusters (rechtes Feld) mit großem I . erkennen konnte 2D /Ich G Verhältnis (1.88) aus dem Raman-Spektrum beobachtet. Der linke Teil des TEM-Bildes enthält Moiré-Muster als Folge einer Rotationsfehlausrichtung der beiden Graphenschichten [37]. Darüber hinaus sind die Fourier-Transformation und I 2D /Ich G Verhältnis (~ 1.26), das aus dem Raman-Spektrum (linkes Feld) beobachtet wurde, veranschaulichen das Doppelschichtmerkmal der Graphenschichten.

TEM-Analyse einer CVD-gezüchteten Graphen-Flake aus Ethanol, hergestellt mit 4 h Wachstumszeit, entnommen aus Fig. 2b. Hochauflösendes TEM-Bild, das sowohl Monolayer- als auch Bilayer-Regionen zeigt, die durch eine markierte Linie getrennt sind. Der Monolayer-Bereich enthält einige Defekte, die lokalisiert sind. Moiré-Muster als Ergebnis einer Rotationsfehlausrichtung der beiden Graphenschichten sind in der Doppelschichtregion deutlich zu sehen. Die rechte und linke Tafel des TEM-Bildes zeigen die Fourier-Transformation der Elektronenbeugungsmuster von 1L- und 2L-Graphen. Sechseckige Elektronenbeugungsmuster in ausgewählten Bereichen des Monolayer- und Bilayer-Graphen zeigen die schöne Kristallinität. Ihre repräsentativen Raman-Spektren sind im unteren Feld mit I . dargestellt 2D /Ich G Verhältnis von 1,88 und 1,26 für 1L bzw. 2L
Graphen-Wachstumsmechanismus auf SiO2
Basierend auf der obigen Beobachtung schlage ich den folgenden Graphen-Wachstumsmechanismus aus Ethanol vor, wie in Abb. 4 dargestellt. Es wird festgestellt, dass sich Graphen mit bis zu wenigen Schichten für eine Wachstumszeit von 5, 10, 15 bzw. 60 min entwickelt. Schritt 1 beginnt mit der thermischen Zersetzung von Ethanoldampf bei Umgebungsdruck und erhöhter Temperatur (~ 700°C), was die Bildung von Ethylengas und Wasser gemäß der folgenden Reaktion energetisch begünstigt [38]:
$$ {\mathrm{C}}_2{\mathrm{H}}_5{\mathrm{OH}}^{\left(\mathrm{g}\right)}\to {\mathrm{C}}_2{ {\mathrm{H}}_4}^{\left(\mathrm{g}\right)}+{\mathrm{H}}_2\mathrm{O} $$ (1)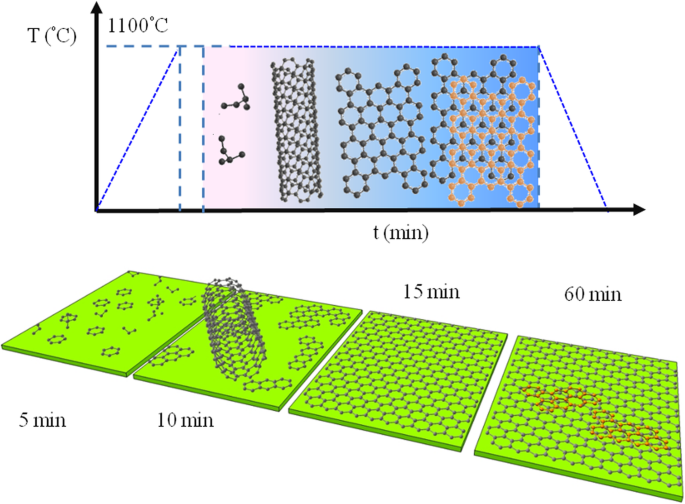
Schematische Darstellung des Graphen-Wachstumsmechanismus auf SiO2 aus Äthanol. Die untere Abbildung zeigt die Entwicklung von kohlenstoffbasierten Nanostrukturen, einschließlich Kohlenstoffnanopartikeln, Mischungen aus CNTs und Kohlenstoffnanopartikeln, mehrschichtigem Graphen (MLG) mit einigen Defekten und ein- bis mehrschichtigem Graphen für Wachstumszeiten von 5, 10, 15 und 60 min, bzw.
H2 Gas hilft bei der weiteren Zersetzung von Ethylen in Kohlenstoff- und Wasserstoffatome. Die relativ große Adsorptionsenergie des flüssigen Vorläufers im Vergleich zum gasförmigen Vorläufer legt nahe, dass der durch Einfang vermittelte Wachstumsprozess hier relevanter ist [27]. Darüber hinaus sind die Stufenkanten des SiO2 Substrat (siehe Zusatzdatei 1:Abbildung S3) möglicherweise als Defektstellen fungieren, in denen Kohlenstoffatome eingefangen werden und Keime bilden, wie bereits im Fall des Wachstums von Übergangsmetall-Dichalkogeniden diskutiert [39]. Bei kurzer Wachstumszeit (5 min) kann die Zersetzung von Ethylen zu Kohlenstoff nicht abgeschlossen sein, und es würden sich daher ungeordnete Kohlenwasserstoffstrukturen auf dem Substrat entwickeln. Wenn sich die Wachstumszeit auf 10&supmin;&sup4; erstreckt, nähert sich die Zersetzung des obigen Moleküls dem Abschluss. In diesem Fall ordnen sich einige der Kohlenstoffatome geordnet in einer spiralförmigen Konfiguration an, um CNTs zu bilden, und einige bleiben amorph. Es ist festzuhalten, dass das CNT-Wachstum meistens aus der Zersetzung von Ethanol bei einer erhöhten Temperatur mit richtigem Wasserstofffluss bevorzugt wird [40, 41].
Bei einer Wachstumszeit von 15 Minuten ist die Zersetzung möglicherweise abgeschlossen und die Kohlenstoffatome verbinden sich in einer Ebene, um C-C sp 2 . zu bilden Netzwerk namens Grapheninseln. Eine weitere Verlängerung der Wachstumszeit auf 60 min erklärt die Ausdehnung von Grapheninseln und bildet Graphenschichten. Der obige Wachstumsprozess legt nahe, dass das direkte CVD-Wachstum von Graphen auf Isolatoren im Vergleich zu denen auf metallischen Substraten eine hohe Wachstumstemperatur und eine lange Abscheidungszeit erfordert [42]. Es wird vorhergesagt, dass sowohl H2 Gas und H2 O entfernen Sie die sp 3 Netzwerk sowie dort vorhandene amorphe Kohlenstoffatome und behalten nur sp 2 Netzwerk für längere Wachstumszeit. Dieser Wachstumsmechanismus ähnelt der sauerstoffunterstützten Synthese von polykristallinem Graphen auf Siliziumdioxidsubstraten [18].
Seed-unterstütztes Wachstum von Graphen
Das keimunterstützte Wachstum von Graphen wurde bereits von mehreren Gruppen demonstriert [43, 44], um die Oberflächenkeimbildung zu kontrollieren und die Qualität von Graphenfilmen zu optimieren. Die Nukleation von CVD-Graphen auf Cu konnte unter Verwendung von Polymethylmethacrylat (PMMA) als vorstrukturierten Keimen kontrolliert werden [44]. Bei der Herstellung von Graphen direkt auf einem Isolator bleiben jedoch große Möglichkeiten, das Graphenwachstum und den damit verbundenen Mechanismus unter Verwendung verschiedener Saatmaterialien als Nukleationsstellen zu erforschen. Unter Berücksichtigung der obigen Aspekte wurden in der vorliegenden Studie vier Saatmaterialien ausgewählt, darunter abgeblättertes Graphen, Holzkohle, ECR-CVD-Graphen und CVD-Graphen, um das Graphenwachstum zu untersuchen, wie in Abb. 5 dargestellt.
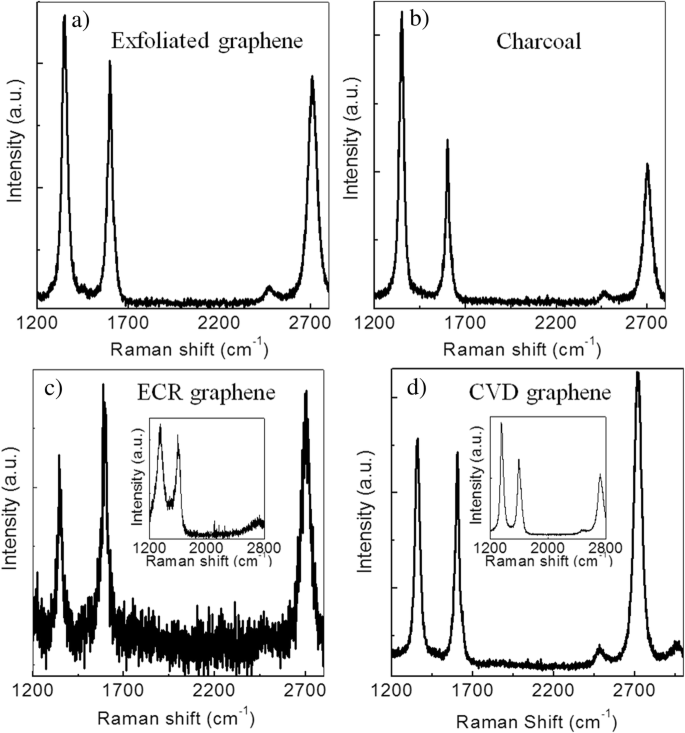
Raman-Spektren von Graphen, das durch CVD für verschiedene Saatmaterialien gezüchtet wurde, einschließlich a mechanisch abgeblättertes Graphen, b Holzkohle, c ECR-CVD-Graphen und d CVD-Graphen. Die Einschübe in Abb. 5c und d zeigen das repräsentative Raman-Spektrum von Graphen-Seeds, hergestellt durch ECR-CVD- bzw. CVD-Route
Als mechanisch abgeblättertes Graphen als Saat auf SiO2 . verwendet wurde Substrat zeigt das Raman-Spektrum (Abb. 5a) die Eigenschaften von zwei- bis dreischichtigem Graphen zusammen mit einer großen D-Band-Intensität, was darauf hindeutet, dass präpariertes Graphen eine hohe Defektdichte aufweist. Dies ist beim vorherigen Bericht [5] unwahrscheinlich, in dem der Graphenfilm eine sehr geringe Defektdichte aufwies, wenn das gleiche Saatmaterial in der CVD-Synthese verwendet wurde. Cu-Dampf fungierte in diesem Fall als Katalysator, der die Keimbildungsrate steuerte und so zu hochwertigem Graphen führte. Im vorliegenden Fall wird die Keimbildungsrate jedoch nicht kontrolliert, was zu Graphen mit hoher Defektdichte führt. Abbildung 5b zeigt das Raman-Spektrum von Graphen unter Verwendung von Holzkohle als Saatmaterial. Das resultierende Graphen hat ein ähnliches Merkmal wie das vorherige (Abb. 5a) mit großer Defektdichte.
Dann habe ich Graphen gewählt, das durch die ECR-CVD-Methode [45] als Keimmaterial für das Graphenwachstum hergestellt wurde (Abb. 5c). Im Vergleich zu mechanisch abgeblättertem Graphen und Graphen auf Basis von Aktivkohlesamen weist Graphen auf Basis von ECR-CVD-Keimen eine reduzierte D-Band-Intensität auf, was auf eine geringe Defektdichte hinweist. Es ist jedoch erwähnenswert, dass das Raman-Spektrum einen großen Rauschpegel aufweist, der wie in Abb. 2 mit dem Reinheitsgrad zusammenhängt. Es kann auch auf unvollständiges Wachstum oder partielles Wachstum zurückzuführen sein, das zu einem geringeren Signal führt. ECR-CVD-Wachstum von Nanographen wurde bei 600°C in Gegenwart von C2 . durchgeführt H2 und Ar mit der Durchflussmenge (C2 H2 :Ar = 0.15:0.3 sccm) für 30 s und Plasmaleistung von 1600 W, gefolgt von Tempern in 1 sccm H2 5 min fließen lassen. Der Abstand zwischen Substrat und Plasma wurde bei 5 cm gehalten. Die detaillierte Synthese des ECR-CVD-Nanographens wurde im experimentellen Abschnitt erwähnt, und seine Raman-Eigenschaft ist als Einschub in Abb. 5c dargestellt. Schließlich wurde CVD-Graphen als Keim für das Graphen-Wachstum gewählt, und sein Raman-Spektrum ist in Fig. 5d dargestellt. Fast einschichtiges Graphen wird mit großer symmetrischer Gaußscher 2D-Peakintensität (I 2D /Ich G ~ 1.35), was auf hochwertiges Graphen hinweist. Die Graphenkeime wurden bei 1100 °C für eine Stunde Wachstumszeit in Gegenwart von Ar und H2 . synthetisiert Durchfluss (Ar:H2 = 250:40 sccm) mit einem Trägergas-Ar-Fluss von 4 sccm, und sein Raman-Spektrum ist als Einschub in Fig. 5d gezeigt.
In dieser Arbeit wurde XPS verwendet, um die Elementaranalyse des präparierten Graphens zu untersuchen. Zusätzliche Datei 1:Abbildung S4 zeigt die XPS-Spektren des direkt auf SiO2 . gewachsenen Graphenfilms bei 1100 °C für 1 Stunde. Außer Si2s, Si2p, O1s und O2s, die der Beitrag von SiO2 . sind, werden keine anderen Peaks gefunden . Die untere Abbildung zeigt das C1s-Core-Level-Spektrum. Der einzige schmale und symmetrische intensive Peak bei 284,4 eV mit einem Halbwertsmaximum (FWHM) von 1,91 eV wird dem sp 2 . zugeordnet -gebundenes C-Atom, was die Bildung von Nanographen mit dieser metallfreien Methode anzeigt, ähnlich der vorherigen Arbeit [5].
Graphenwachstum als Funktion der Wachstumstemperatur
Ich habe das CVD-Wachstum von Graphen auf SiO2 . systematisch untersucht als Funktion der Wachstumstemperatur durch Festhalten anderer Parameter, einschließlich der Durchflussrate des verdünnten Gases (Ar:H2 =235:40 sccm) und Trägergasflussrate (Ar = 10 sccm). Drei Wachstumstemperaturen (1000 °C, 1050 °C und 1100 °C) wurden ausgewählt, und ihre repräsentativen Raman-Spektren sind in Abb. 6 dargestellt. Für niedrige Wachstumstemperaturen, 1000 °C und 1050 °C, breiter 2D-Peak mit Intensität weniger als der G-Peak wurde beobachtet, was auf die Bildung mehrerer Graphenschichten aufgrund unkontrollierter zufälliger Nukleation auf der blanken Oxidoberfläche hinweist. Darüber hinaus weist das Vorhandensein einer großen D-Peakintensität auf die Signatur von Graphen mit hoher Defektdichte hin. Die zufällige Keimbildung und die schlechte Oberflächenmigration von Kohlenstoffatomen sind vermutlich die Hauptursachen für Defekte in diesem Wachstumsprozess. Als die Wachstumstemperatur 1100°C überstieg, schien die Qualität des Graphens mit einer relativ großen und scharfen 2D-Peakintensität gut zu sein, aber der D-Peak existiert immer noch dort, was eine endliche Defektdichte darstellt. Es wird erwartet, dass eine hohe Wachstumstemperatur eine gewisse kontrollierte Nukleation fördert, die für eine verbesserte Graphenqualität verantwortlich ist. Daher wurde angenommen, dass 1100 °C die optimale Temperatur ist, um hochwertiges Graphen direkt auf SiO2 . zu synthetisieren in CVD.
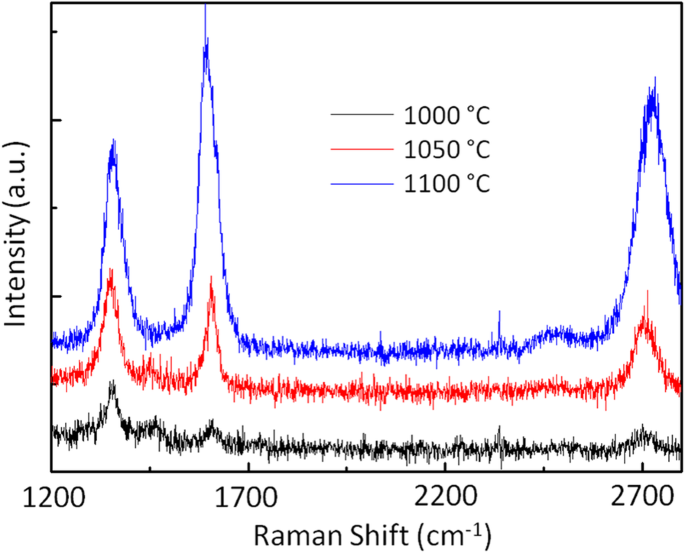
Mikro-Raman-Charakterisierung von CVD-Graphen, das direkt auf SiO2 . gewachsen ist für unterschiedliche Wachstumstemperaturen. 1000 °C (schwarz), 1050 °C (rot) 1100 °C (blau)
Mein vorgeschlagener Graphen-Wachstumsmechanismus auf Isolatoren basiert auf der thermischen Zersetzung von Ethanol, gefolgt von einer kontrollierten Nukleation von Kohlenstoff-2D-Inseln, um kontinuierliches Nanographen über ein CNT im Zwischenzustand zu bilden. Um die obige Hypothese weiter zu validieren, wurde CNT als Ausgangsmaterial für Graphen in CVD verwendet und seine Transformation als Funktion der Wachstumszeit untersucht, wie in Raman-Mapping dargestellt (zusätzliche Datei 1:Abbildung S5). Zuerst wurde CNT auf SiO2 . platziert Substrat vor dem CVD-Wachstum, wie in der oberen Abbildung schematisch gezeigt. Nach 5-minütigem Wachstum tritt eine verzerrte CNT-Struktur auf und wandelt sich schließlich in vollständiges Graphen um, wenn sich die Wachstumszeit 10 min nähert. Die RBM-, 2D/G- und D/G-Raman-Kartierung von 20 × 20 μm 2 -Region sind in der unteren Abbildung dargestellt und zeigen die Entwicklung der Graphenstruktur als Funktion der Wachstumszeit. Der RBM-Peak, der weißen Rechtecken in der Raman-Kartierung zugeordnet ist, ist die Signatur von CNT, die anfänglich vorhanden ist und nach 10 Minuten Wachstumszeit verschwindet. Der 2D/G-Peak (weiße Rechtecke) ist für CNT niedrig und nimmt mit zunehmender Wachstumszeit zu. In ähnlicher Weise ist der D/G-Peak (schwarze Rechtecke), der die Signatur von Defekten ist, für CNT hoch und für Graphen drastisch reduziert (10 Minuten Wachstumszeit).
Schlussfolgerungen
Zusammenfassend habe ich eine neuartige Graphen-Wachstumstechnik direkt auf Siliziumoxiden bei der chemischen Gasphasenabscheidung unter Verwendung von Ethanol als anderen Kohlenstoffvorläufer als Methan demonstriert. Zersetzung von Ethanol zu Ethylen und Wasser gefolgt von Keimbildung von sp 2 Netzwerkkohlenstoff auf SiO2 Oberfläche, die als Nukleationszentrum fungiert, führt über ein zwischengeschaltetes CNT im nanostrukturierten Kohlenstoffzustand zur Bildung von Nanographen-Flakes. Das Wachstum von Graphen wurde als Funktion der Glühtemperatur und der Keimschicht systematisch untersucht und schließlich sein selbstlimitierendes Verhalten diskutiert. Es wird beobachtet, dass eine höhere Wachstumstemperatur und ein niedrigerer Trägergasfluss die kristalline Qualität von Graphenflocken verbessern. CVD-Graphen wird im Vergleich zu abgeblättertem Graphen, Holzkohle und ECR-Graphen die beste Saatschicht sein, um eine hohe Qualität von Graphenflocken zu erhalten. Das vorgeschlagene Verfahren vermeidet die Notwendigkeit entweder eines Metallkatalysators oder eines komplizierten und fachmännischen Transferprozesses nach dem Wachstum und ebnet den Weg zur Entwicklung praktischer Anwendungen für Graphen, insbesondere in der Elektronik, die eine Integration in die aktuelle Si-Verarbeitungstechnologie erfordert.
Abkürzungen
- AFM:
-
Rasterkraftmikroskopie
- CNTs:
-
Kohlenstoff-Nanoröhrchen
- Lebenslauf:
-
Chemische Gasphasenabscheidung
- ECR-CVD:
-
Elektronenzyklotronresonanz-CVD
- FWHM:
-
Halbe maximale Breite in voller Breite
- MLG:
-
Mehrschichtiges Graphen
- PMMA:
-
Polymethylmethacrylat
- RBM:
-
Radialer Atemmodus
- SEM:
-
Rasterelektronenmikroskopie
- SWCNT:
-
Einwandige Kohlenstoff-Nanoröhrchen
- TEM:
-
Transmissionselektronenmikroskopie
- XPS:
-
Röntgenphotoelektronenspektroskopie
Nanomaterialien
- Neuere Veröffentlichungen beschreiben die Skalierbarkeit von Kohlenstoffnanoröhren und Durchbrüche bei der Integration
- Carbon-Nanotube-Garn, Muskel- und transparente Folien
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Direktes Wachstum von federartigen ZnO-Strukturen durch eine einfache Lösungstechnik für die Fotoerkennungsanwendung
- Entwerfen von sauberen und zusammengesetzten Kohlenstoff-Nanoröhrchen-Materialien durch porosimetrische Charakterisierung
- Herstellung und Charakterisierung eines neuen anodischen Tio2-Kohlenstoff-Nanofaser-Verbundkatalysators für eine Direkt-Methanol-Brennstoffzelle mittels Elektrospinnverfahren
- Direktes Wachstum einer gelben Leuchtdiode auf Basis von III-Nitrid-Nanodrähten auf amorphem Quarz unter Verwendung einer dünnen Ti-Zwischenschicht
- Untersuchung des nanoskaligen Reibungsverhaltens von Graphen auf Goldsubstraten mittels Molekulardynamik
- Herstellung von ultrahochmolekularem Polyethylen/Graphen-Nanokomposit In-situ-Polymerisation durch sphärische und Sandwichstruktur-Graphen/Sio2-Unterstützung
- Vorteile der Verwendung von VIA in Pads



