Instrumentelle Analyse von Stahl, Schlacke und Rohstoffen
Instrumentelle Analyse von Stahl, Schlacke und Rohstoffen
Die Instrumentenanalyse wird häufig für die qualitative und quantitative Elementaranalyse von Rohstoffen, Eisen (Roheisen), Stahl, Schlacke, feuerfesten Materialien und Schlämmen verwendet. Im Vergleich zur Nassanalyse hat die Instrumentenanalyse den Vorteil, dass sie kostengünstig und multielementar ist und außerdem sehr schnell ist. Die Sorgen um störende Elemente in der nasschemischen Analyse entfallen. Die instrumentelle Analytik vermeidet das mehrstündige Warten auf bestimmte Elemente, was bei nasschemischen Methoden notwendig ist.
Darüber hinaus bietet die Instrumentenanalyse eine ziemlich einheitliche Nachweisgrenze über eine große Liste von Elementen oder Verbindungen hinweg und ist auf einen breiten Konzentrationsbereich anwendbar, der von 100 % bis zu einigen Teilen pro Million (ppm) reicht. Die instrumentellen Methoden sind aufgrund geringerer menschlicher Eingriffe mit geringerem Umfang menschlicher Fehler reproduzierbar. Sie sind robust, zuverlässig und genau, wobei die Genauigkeit von der Kalibrierung und den für die Kalibrierung verwendeten Standards abhängt.
Die Analyse von Stahl, Schlacke und Rohstoffen ist nicht nur während des Stahlherstellungsprozesses zu Kontrollzwecken wichtig und unerlässlich, sondern auch für die große Anzahl von Proben, die für verschiedene andere Zwecke analysiert werden müssen. Die Informationen aus einer Analyse sind für verschiedene Zwecke nützlich, wie z. B. die Inspektion von Rohstoffen, Zwischenprodukten und Endprodukten, die Umweltbewertung, die Prozesskontrolle, die Fehleranalyse, die Qualitätskontrolle der Produkte und für Zwecke der Forschung und Entwicklung. P>
Geschichte
Während der Spektrograph schon seit geraumer Zeit in anderen Bereichen eingesetzt wurde, wurde das erste Instrument, das erfolgreich zur Eisenschmelzkontrolle eingesetzt wurde, 1935 in einer Gießerei installiert. Ein Baird-Spektrograph wurde 1943 im Timken-Labor für die Analyse von Proben installiert der Schmelzbetrieb. Dieses Instrument war mit einem Wood-Gitter mit einer Brennweite von drei Metern ausgestattet, das mit 15.000 Linien pro Zoll liniert und in eine Adlerhalterung eingesetzt war. Proben für die spektrographische Analyse werden in Form von Stäben mit einem Durchmesser von 5,5 mm gegossen, indem das flüssige Metall in eine Form gegossen oder in ein Glasrohr gesaugt wird. Die gegossenen Stifte werden durch ein pneumatisches Rohrtransportsystem zum Labor geschickt, wo sie sorgfältig auf einen Punkt mit einem eingeschlossenen Winkel von 140 Grad geschliffen und in die Elektrodenhalter eingesetzt werden. Es wird Strom von einer Hochspannungslichtbogen- oder Funkenquelle angelegt und Spektrallinien des emittierten Lichts werden auf Eastman-Spektralanalyseplatten Nr. 1 fotografiert. Die Platte wird dann entwickelt, gewaschen, getrocknet und in einem dunklen Raum auf Raumtemperatur abgekühlt. Die Dichte der Linie für das erforderliche Element wird auf einem Densitometer abgelesen und in Prozent berechnet, wonach sie dem Ofenbediener per Fernschreiber gemeldet wird.
Eine Weiterentwicklung in der Instrumentenanalyse war das direkt ablesbare Spektrometer. Bei diesem Instrument wurde der fotografische Tisch vollständig durch empfindliche Elektronenvervielfacher-Röhren ersetzt, die das emittierte Licht bei den verschiedenen Wellenlängen aufnehmen und innerhalb von 35 Sekunden, nachdem eine Probe in die Elektrodenhalter gelegt wurde, als Prozentsatz auf kalibrierten Uhrenzifferblättern anzeigen. Die Verwendung von Fotoröhren eliminierte alle möglichen Fehler, die mit Platten oder Filmen, Dunkelkammerentwicklung und -entwicklung, Densitometerablesungen und Berechnungstafeln verbunden sind. Das erste direkt anzeigende Spektrometer wurde im Mai 1947 im Kontrolllabor von Timken installiert und war das erste Instrument dieser Art, das in der Stahlindustrie eingesetzt wurde.
Die Instrumentenanalyse wurde weiterentwickelt und die verschiedenen derzeit verwendeten Arten der Instrumentenanalyse werden im Folgenden beschrieben.
Funkenatomemissionsspektrometrie (AES)
Die Atomemissionsspektroskopie ist eine Methode der chemischen Analyse, die die Intensität des von einem Funken emittierten Lichts bei einer bestimmten Wellenlänge verwendet, um die Menge eines Elements in einer Probe zu bestimmen. Die Wellenlänge der atomaren Spektrallinie gibt die Identität des Elements an, während die Intensität des emittierten Lichts proportional zur Anzahl der Atome des Elements ist.
Die Funkenatomemissionsspektroskopie wird zur Analyse metallischer Elemente in festen Proben verwendet. Bei nicht leitfähigen Materialien wird die Probe mit Graphitpulver gemahlen, um sie leitfähig zu machen. Bei herkömmlichen Verfahren der Lichtbogenspektroskopie wird normalerweise eine Probe des Feststoffs zerkleinert und während der Analyse zerstört. Ein Lichtbogen oder Funke wird durch die Probe geleitet und auf eine hohe Temperatur erhitzt, um die darin enthaltenen Atome anzuregen. Die angeregten Atome emittieren Licht bei charakteristischen Wellenlängen, die mit einem Monochromator gestreut und nachgewiesen werden können. Die Funkenquelle mit kontrollierter Entladung dient der quantitativen Analyse. Sowohl qualitative als auch quantitative Funkenanalysen mittels Funken-Atom-Emissionsspektrometrie werden häufig zum Zweck der Qualitätskontrolle in Stahlwerken eingesetzt.
AES kann bis zu 64 Elemente gleichzeitig in weniger als 20 Sekunden bestimmen. Die Einschränkung dieser Technik besteht darin, dass das Instrument Gase in Stahl (Sauerstoff, Stickstoff und Wasserstoff) nicht analysieren kann. Obwohl einige der modernen Instrumente eine Stickstoffanalyse ermöglichen, liegen die Reproduzierbarkeit und Nachweisgrenzen unter den Erwartungen der Stahlhersteller.
Röntgenfluoreszenz (XRF)-Spektrometrie
Dieses Spektrometer kann sowohl Metalle als auch nichtmetallische Proben analysieren. Daher wird es umfassend für die Analyse von Metallen, Schlacken, Rohstoffen und feuerfesten Proben verwendet. Es funktioniert nach folgendem Prinzip (gezeigt in Abb. 1).
Wenn eine Probe mit Röntgenstrahlen aus einer Röntgenröhre bestrahlt wird, erzeugen die Atome in der Probe einzigartige Röntgenstrahlen, die von der Probe emittiert werden. Solche Röntgenstrahlen sind als „fluoreszierende Röntgenstrahlen“ bekannt und haben eine einzigartige Wellenlänge und Energie, die für jedes Element, das sie erzeugt, charakteristisch sind. Folglich kann eine qualitative Analyse durchgeführt werden, indem die Wellenlängen der Röntgenstrahlen untersucht werden. Da die Intensität der fluoreszierenden Röntgenstrahlen eine Funktion der Konzentration ist, ist eine quantitative Analyse auch möglich, indem die Menge an Röntgenstrahlen bei der für jedes Element spezifischen Wellenlänge gemessen wird.
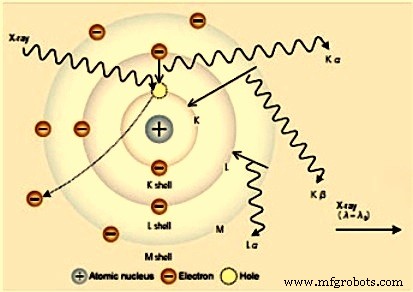
Abb. 1 Prinzip der XRF-Spektrometrie
Ein Röntgenstrahl aus der Röhre trifft auf die Probe, wo er mit einem Elektron aus einer der inneren Hüllen des A-Atoms interagiert. Es schlägt das Elektron aus seiner Bahn. Dadurch entsteht ein Hohlraum, der dann umgehend von einem Elektron aus einer äußeren Hülle gefüllt wird. Dieses Elektron hat eine höhere Energie als das Elektron, das es ersetzt. Die überschüssige Energie wird in Form eines Röntgenstrahls mit einer für das A-Atom spezifischen Wellenlänge ausgestoßen. Es gibt hauptsächlich zwei Arten von XRF-Spektrometern.
Das energiedispersive Röntgenfluoreszenz-Spektrometer (EDXRF) verwendet einen Detektor, um das gesamte Spektrum direkt in eine energiedispersive Skala zu verarbeiten. EDXRF-Spektrometer umfassen einen Hightech-Detektor, der einen gedrifteten Kristall aus Silizium-Lithium (SiLi) verwendet, der auf niedrige Temperaturen (-90 °C) gekühlt wird. Dieser Kristall ist in der Lage, Röntgenphotonen unterschiedlicher Energie zu unterscheiden (Energiedispersion). Der Detektor nimmt alle von der Probe emittierten Photonen auf und die Gesamtzählrate des Detektors beträgt etwa 50 Kilo-Zählungen pro Sekunde und ist oft gesättigt. Bestimmte Filter werden normalerweise verwendet, um einen Teil des Spektrums herauszufiltern, z. die Hauptelemente. Sekundäre Targets werden normalerweise verwendet, um nur einen Teil der Elemente des Periodensystems besser anzuregen.
Der SiLi-Kristall des Detektors absorbiert ein einfallendes Röntgenphoton, das Atome ionisiert und Elektronen- (-) und Loch- (+) Paare erzeugt. Die Menge der Elektron/Loch-Paare ist proportional zur Energie des Röntgenphotons. Detektorausgangsimpulse werden verstärkt, digitalisiert und nach ihrer Größe sortiert. Der Detektor muss auf minus 90 Grad C gekühlt werden.
Das wellenlängendispersive Röntgenfluoreszenz-Spektrometer (WDRFA) verwendet geeignete Kristalle, um das Emissionsspektrum in diskrete Wellenlängen zu trennen, bevor sie detektiert werden. Die Mikro-Röntgenfluoreszenz hat ihren Namen, weil diese Instrumente für die Analyse sehr kleiner Punktgrößen ausgelegt sind. Bei der Totalreflexions-Röntgenfluoreszenz (TRXRF) wird der Anregungsstrahl vom Substrat totalreflektiert und nur Partikel auf der Oberfläche werden angeregt, was zu Röntgenfluoreszenzemissionen führt. Auf diese Weise wird der normalerweise mit XRF-Messungen verbundene Hintergrund stark reduziert, was zu einer höheren Empfindlichkeit und niedrigeren Nachweisgrenzen führt.
Atomemissionsspektrometrie mit induktiv gekoppeltem Plasma (ICP/AES)
Atomemissionsspektrometrie mit induktiv gekoppeltem Plasma ist eine Analysetechnik zum Nachweis von Spurenelementen. Es verwendet das induktiv gekoppelte Plasma, um angeregte Atome und Ionen zu erzeugen, die elektromagnetische Felder mit Wellenlängen emittieren, die für ein bestimmtes Element charakteristisch sind. Die Intensität dieser Emission zeigt die Konzentration des Elements in der Probe an.
Das ICP-AES besteht aus zwei Teilen, nämlich (i) dem ICP und (ii) dem optischen Spektrometer. Die ICP-Fackel besteht aus 3 konzentrischen Quarzglasröhren. Der Ausgang des Hochfrequenzgenerators (RF) umgibt einen Teil dieser Quarzfackel. Zur Erzeugung des Plasmas wird normalerweise Argongas (Ar) verwendet.
Das HF-erzeugte und aufrechterhaltene Ar-Plasma, von dem Teile bis zu 10.000 Grad K heiß sind, regt die Elektronen an. Das Plasma wird verwendet, um die Elemente in der Probe zu atomisieren und zu ionisieren. Wenn die Elektronen an einer bestimmten räumlichen Position im Plasma in den Grundzustand zurückkehren, geben sie Energie bei den spezifischen Wellenlängen ab, die der elementaren Zusammensetzung der Probe eigen sind. Vom Plasma emittiertes Licht wird durch eine Linse fokussiert und durch einen Eintrittsspalt in das Spektrometer geleitet. Es gibt zwei Arten von Spektrometern, die bei der ICP-AES-Analyse verwendet werden, nämlich (i) sequentiell (Monochromator) und (ii) simultan (Polychromator).
Massenspektrometrie mit induktiv gekoppeltem Plasma (ICP-MS) ist ein sehr leistungsfähiges Werkzeug für die Elementaranalyse im Spurenbereich (ppb, Teile pro Milliarde ppm) und im Ultraspurenbereich (ppq, Teile pro Billiarde -ppb).
Atomabsorptionsspektrometrie (AAS)
Die Atomabsorptionsspektrometrie (AAS) ist eine Analysetechnik, die die Konzentrationen von Elementen misst. Die Atomabsorptionsspektrometrie wird normalerweise verwendet, um die Konzentration von über 62 verschiedenen Metallen in einer Lösung zu analysieren, und ist so empfindlich, dass sie in einer Probe bis zu Teilen pro Milliarde Gramm messen kann. Die Technik nutzt die Wellenlängen des Lichts, die von einem Element spezifisch absorbiert werden. Sie entsprechen den Energien, die benötigt werden, um Elektronen von einem Energieniveau auf ein anderes, höheres Energieniveau zu befördern.
Ein Atomabsorptionsspektrophotometer besteht aus einer Lichtquelle, einem Probenraum und einem Detektor. Bei diesem Verfahren wird Licht von einer Quelle durch die Probe zu einem Detektor geleitet. Die Lichtquelle ist eine Lampe, deren Kathode aus dem zu messenden Element besteht. Jedes Element erfordert eine andere Lampe.
Die Technik nutzt die Absorptionsspektrometrie, um die Konzentration eines Analyten in einer Probe zu bestimmen. Es erfordert Standards mit bekanntem Analytgehalt, um die Beziehung zwischen der gemessenen Extinktion und der Analytkonzentration herzustellen, und stützt sich daher auf das unten erläuterte Beer-Lambert-Gesetz.
A =eBC
Dabei ist A die Extinktion [keine Einheiten, da A =log10 (Io / I1)], e die molare Extinktion mit Einheiten von L mol¯¹ cm¯¹, B die Weglänge der Probe in Zentimetern – also die optische Weglänge, und C ist die Konzentration der Verbindung in Lösung, ausgedrückt in mol L¯¹.
Das Diagramm (Abb. 2) zeigt einen Strahl monochromatischer Strahlung der Strahlungsleistung I?, der auf eine Probenlösung gerichtet ist. Es findet Absorption statt und das aus der Probe austretende Strahlenbündel hat die Strahlungsleistung I1.
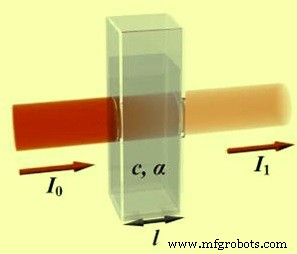
Abb. 2 Diagramm, das monochromatische Strahlung zeigt
Kurz gesagt, die Elektronen der Atome im Zerstäuber können durch Aufnahme einer definierten Energiemenge (Strahlung einer bestimmten Wellenlänge) für eine kurze Zeit (Nanosekunden) in höhere Orbitale (angeregter Zustand) befördert werden. Diese Energiemenge, d. h. Wellenlänge, ist spezifisch für einen bestimmten Elektronenübergang in einem bestimmten Element. Im Allgemeinen entspricht jede Wellenlänge nur einem Element, und die Breite einer Absorptionslinie liegt nur in der Größenordnung von wenigen Pikometern (pm, 10¯¹² m), was der Technik ihre elementare Selektivität verleiht. Der Strahlungsfluss ohne Probe und mit einer Probe im Zerstäuber wird mit einem Detektor gemessen, und das Verhältnis zwischen den beiden Werten (die Extinktion) wird mithilfe des Beer-Lambert-Gesetzes in die Konzentration oder Masse des Analyten umgewandelt.
Herstellungsprozess
- Kravox! Drahtloses, bewegungs- und berührungsempfindliches Instrument
- Einschlüsse in Stranggussstahl und deren Erkennung
- Einschlüsse in der Stahl- und Sekundärstahlerzeugung
- Einschlüsse, Einschlusstechnik und saubere Stähle
- Ökobilanz und Nachhaltigkeit von Stahl
- Eigenschaften von Stahlmaterialien und Werkzeugen, die für Stanzen verwendet werden
- Unterschiede zwischen Edelstahl und Baustahl bei Stanzmaterialien
- Verschiedene Eigenschaften und Sorten von Werkzeugstahl
- Werkzeugstahl verstehen und wie er hergestellt wird
- Rohstoffe für die Herstellung von Eisen und Stahl



