S, N codotierte Graphen-Quantenpunkt/TiO2-Komposite für eine effiziente photokatalytische Wasserstofferzeugung
Zusammenfassung
S, N kodotierte Graphen-Quantenpunkte (S, N-GQDs) gekoppelt mit P25 (TiO2 ) (S,N-GQD/P25) wurden durch einfache hydrothermale Methode hergestellt. Die so hergestellten S,N-GQD/P25-Komposite zeigten ausgezeichnete photokatalytische Wasserstofferzeugungsaktivitäten mit einem deutlich erweiterten Lichtabsorptionsbereich und überlegener Haltbarkeit ohne Beladung mit Edelmetall-Cokatalysatoren. Die photokatalytische Aktivität dieses Komposits unter sichtbarem Licht (λ = 400–800 nm) wurde im Vergleich zu reinem P25 stark verbessert. Diese bemerkenswerte Verbesserung der photokatalytischen Aktivität der S,N-GQD/P25-Komposite kann darauf zurückgeführt werden, dass S,N-GQDs eine Schlüsselrolle bei der Verbesserung der Absorption von sichtbarem Licht spielen und die Trennung und Übertragung photogenerierter Elektronen und Löcher erleichtern. Im Allgemeinen könnte diese Arbeit neue Einblicke in die einfache Herstellung photokatalytischer Komposite als Hochleistungsphotokatalysatoren liefern.
Hintergrund
Wasserstoffenergie ist eine neue grüne, schadstofffreie Energie mit vielen Vorteilen, darunter ein hoher Heizwert, einfache Lagerung und Transport, keine Umweltverschmutzung usw. Angesichts der Tatsache, dass Wasser und Sonnenlicht zwei der am häufigsten vorkommenden und am leichtesten zugänglichen Quellen in der realen Welt sind, übertragen die Sonnenenergie in H2 aus wässriger Lösung ist ein heißes Forschungsthema auf dem Gebiet der Photokatalyse und der Wasserstoffenergie. Im Vergleich zu CdS, SiC und vielen anderen Halbleitern werden diese häufig für photokatalytisches H2 . verwendet Entwicklung [1,2,3,4,5,6], TiO2 hat mehrere Vorteile, wie geringe Kosten, Ungiftigkeit, gute photochemische Stabilität und lange Lebensdauer, was seinen industriellen Anwendungen zugute kommt [7]. Die große Bandlücke (3,2 eV) von TiO2 und eine schnelle Rekombination von photogenerierten Elektronen und Löchern schränkt die Effizienz der Sonnenenergieumwandlung ein [8]. Um dieses Problem zu lösen, wurden massive Strategien verfolgt, wie die Dotierung mit Metallelementen [9, 10], die Abscheidung mit Edelmetallen [11], die Sensibilisierung mit organischen Farbstoffen [12, 13] und so weiter. In letzter Zeit hat TiO2 . großes Interesse geweckt -basierte Verbundwerkstoffe mit der Kombination metallfreier Kohlenstoffmaterialien wie Graphen und Kohlenstoffnanoröhren (CNTs), die die photokatalytische Aktivität aufgrund der überlegenen Ladungstransporteigenschaften effizient verbessern könnten, um die Rekombinationsrate photogenerierter Elektronenlöcher zu reduzieren. Du et al. [14] berichtete über eine Photokatalyse basierend auf Graphen/TiO2 Kern-Schale-Nanopartikel, und die erhöhte photokatalytische Aktivität wurde mit dem großen erweiterten photoresponsiven Bereich und der hohen Elektron-Loch-Trennungseffizienz aufgrund der synergetischen Wechselwirkungen zwischen TiO2 . in Verbindung gebracht und Graphenmaterial. Graphen ist jedoch von Natur aus ein Halbmetall mit einer Bandlücke von null, was seine Anwendung in der Photokatalyse erheblich erschwert [15]. Außerdem absorbieren sowohl Graphen als auch CNTs ein breites Spektrum an Licht und können daher andere Photokatalyse vor Lichteinstrahlung blockieren [16]. Die oben genannten Nachteile schränken die photokatalytische Leistung der auf Graphen und CNTs basierenden Kompositphotokatalyse ein.
Graphen-Quantenpunkte (GQDs) als neues aufstrebendes Kohlenstoff-Nanomaterial bestehen aus wenigen Graphenschichten mit einer lateralen Ausdehnung von weniger als 10 nm und verarbeiten einzigartige Eigenschaften, die von Graphen abgeleitet sind [17]. Im Vergleich zu herkömmlichen Halbleiter-Quantenpunkten wie ZnO [18], CdSe [19] usw. weisen GQDs eine höhere Wasserlöslichkeit, bessere chemische Stabilität, geringe Toxizität, ausgezeichnete Biokompatibilität und photoelektrische Eigenschaften auf. Daher haben sie ein breites Interesse in den Bereichen Sensorik [20, 21], Solarzellen [22, 23, 24], Bio-Bildgebung [25, 26] und Photokatalyse [27, 28, 29, 30] geweckt. Vor kurzem haben Qu et al. [31] hat GQD/TiO2 . hergestellt Nanoröhre (GQD/TiO2 NT) Kompositen durch ein einfaches hydrothermales Verfahren bei niedriger Temperatur. Die photokatalytische Aktivität von präpariertem GQD/TiO2 NT-Komposite beim Abbau von Methylorange (MO) wurden im Vergleich zu reinem TiO2 . signifikant verbessert Nanoröhren. Sudhagaret al. [32] hat GQDs/TiO2 . vorbereitet Elektrode mit hohler Nanodrähte (HNW) zur Verbesserung der Lichtsammeleffizienz und der katalytischen Aktivität für die Wasseroxidation, ohne dass Opfermittel benötigt werden, und demonstrierte den zugrunde liegenden Mechanismus des Phototrägers (e - /h + ) Übertragungseigenschaften an der Grenzfläche GQDs/Metalloxid während des Betriebs. Obwohl es mehrere Berichte gab, die das Potenzial von GQDs als durch sichtbares Licht angetriebene Photokatalysatoren nahelegen, sind das Fehlen von Emission bei langwelliger Anregung und die breite Absorption im sichtbaren Bereich (λ> 400 nm) von GQDs erfordern immer noch optimierte Methoden [33]. Kürzlich wurden mit Stickstoff und Schwefel kodotierte Graphen-Quantenpunkte (S,N-GQDs) aufgrund ihrer breiten Photoabsorption in einem breiten Spektralbereich, hoher Ladungsträgertransportmobilität und ausgezeichneter chemischer Stabilität untersucht. Qu et al. [34] haben gezeigt, dass S,N-GQDs eine viel bessere Absorption von sichtbarem Licht als reine GQDs und mehrfarbige Emission bei Anregung mit sichtbarem Licht verarbeiten. Diese Ergebnisse deuten darauf hin, dass die elementare Dotierung von GQDs vielversprechende Katalysatoren für die solare Photokatalyse ergeben könnte. Weitere Forschungen sollten sich auf die Modifikation von GQDs konzentrieren, um die Bandlücke zu regulieren, den Photoabsorptionsbereich zu verbreitern und die Photoquanteneffizienz zu verbessern. Es bleiben jedoch große Herausforderungen bei der Entwicklung kostengünstiger, stabiler und hochaktiver Photokatalysatoren auf GQD-Basis.
In diesem Artikel berichteten wir über eine hydrothermale Methode zur simultanen Synthese und Dotierung von GQDs mit S und N. Außerdem haben wir das S,N-GQD/TiO2 . hergestellt (P25) Komposite auf einem einfachen hydrothermalen Weg. Dieser Verbundstoff zeigte eine ausgezeichnete photokatalytische Leistung in H2 Herstellung aus wässriger methanolischer Lösung unter UV-vis-Bestrahlung ohne die Hilfe von Edelmetall-Cokatalysatoren. Die photokatalytischen Aktivitäten von S,N-GQD/TiO2 mit unterschiedlichen S,N-GQD-Beladungsmengen wurden ebenfalls untersucht. Schließlich wurde der Mechanismus zur Verbesserung der photokatalytischen Leistung basierend auf experimentellen Ergebnissen diskutiert.
Methoden
Synthese der S,N-GQDs
Über den detaillierten Syntheseprozess von S,N-GQDs wurde an anderer Stelle berichtet [35]. Typischerweise wurden 1,26 g (6 mmol) Zitronensäure und 1,38 g (18 mmol) Thioharnstoff in 30 ml DMF gelöst und mehrere Minuten gerührt, um eine klare Lösung zu erhalten. Dann wurde die Lösung in einen mit Teflon ausgekleideten 50 ml-Autoklaven aus rostfreiem Stahl überführt. Der verschlossene Autoklav wurde 8 h auf konstant 180 °C aufgeheizt und auf Raumtemperatur abgekühlt. Das Endprodukt wurde durch Zugabe von Ethanol in die Lösung ausgefällt und dann 15 Minuten lang bei 10.000 U/min zentrifugiert.
Synthese der S,N-GQD/P25-Verbundstoffe
Die S,N-GQD/P25-Komposite wurden durch ein hydrothermales Verfahren erhalten. Normalerweise 0,5 g P25 und 5 ml S,N-GQD (2 mg ml -1 ) wurden in 20 ml destilliertes Wasser gegeben. Die Mischung wurde 4 h bei Raumtemperatur gerührt, um eine homogene Suspension zu erhalten. Danach wurde die Suspension in einen 40 ml Teflon-versiegelten Autoklaven überführt und 6 h bei 150 °C gehalten. Dann wurden die S,N-GQD/P25-Komposite durch Zentrifugation bei 4000 U/min für 5 Minuten ausgefällt. Und schließlich wurde der Feststoff im Vakuumofen bei 50 °C über Nacht getrocknet. Um die Wirkung des S,N-GQD-Gehalts auf das photokatalytische H2 . zu untersuchen Evolutionsrate wurden die S,N-GQD/P25-Komposite mit unterschiedlichen Gehalten an S,N-GQD (0, 1, 2, 3, 5, 8 und 10 Gew.-%) hergestellt.
Charakterisierung
Transmissionselektronenmikroskopische (TEM) und hochauflösende TEM (HRTEM) Bilder wurden mit einem JEOL JEM-2100 F-Mikroskop erhalten, das bei 200 kV betrieben wurde; Röntgenbeugungsmuster (XRD) wurden auf einem Rigaku D/max-2500-Diffraktometer mit einer nickelfiltrierten Cu-Kα-Strahlung, die bei 40 kV und 300 mA betrieben wurde, aufgezeichnet; Fourier-Transformations-Infrarot-(FTIR)-Spektren wurden unter Verwendung von Nicolet 6700 (Thermo Fisher); Raman-Spektren wurden von NEXUS670 (Thermo Nicolet Corporation) durchgeführt; UV-Vis-Absorptionsspektren wurden mit einem UV-Vis-Spektrophotometer Lambda 950 (Perkin Elmer, USA) gemessen.
Photokatalytische Wasserstofferzeugung
Fünfzig Milligramm Photokatalysatorpulver wurden in einer 100 ml wässrigen Lösung dispergiert, die 10 ml Methanol als Opfermittel enthält. Die Bestrahlungen mit UV-Licht und sichtbarem Licht wurden mit einer 300 W-Xe-Lampe ohne bzw. mit einem 400 nm-Filter erzeugt. Die Menge an erzeugtem H2 wurde mit einem Online-Gaschromatographen bestimmt.
Photoelektrochemische Messungen
Die transienten Photostromantworten wurden in einer elektrochemischen Workstation mit einem herkömmlichen Drei-Elektroden-System gemessen:eine Pt-Platte als Gegenelektrode, eine gesättigte Kalomelelektrode als Referenzelektrode, und die so hergestellte Probe wurde als Arbeitsmaterial auf das ITO-Substrat aufgetragen Elektrode. Insbesondere wurde die Arbeitselektrode hergestellt, indem die Aufschlämmung aus 0,05 g Photokatalysator, 0,2 g Polyethylenglykol (PEG20000) und 1,0 ml Wasser nach dem Rakelverfahren auf ITO-Glaselektroden aufgetragen wurde, mit anschließendem Kalzinieren bei 450 °C für 30 Minuten. Die dem Elektrolyt ausgesetzte aktive Oberfläche der Arbeitselektrode betrug etwa 2 cm 2 . und die Dicke der aufgetragenen Schicht betrug etwa 8 mm. Der Elektrolyt war 0,5 M Na2 . SO4 wässrige Lösung. Die Lichtquelle war eine 300 W-Xe-Lampe.
Ergebnisse und Diskussion
Abbildung 1 zeigt die TEM-Bilder der so synthetisierten S,N-GQDs- und S,N-GQD/P25-Proben. Die TEM-Bilder zeigen, dass die S,N-GQDs eine gleichmäßige Dispersion ohne offensichtliche Aggregation aufweisen. Im HRTEM-Bild in Abb. 1a sind (0–110) Gitterstreifen mit einem Abstand von etwa 0,24 nm für S,N-GQDs sichtbar [36], was offenbart, dass die S,N-GQDs Graphitcharakter haben. Das Rasterkraftmikroskop (AFM)-Bild und das entsprechende Höhenprofil von S,N-GQDs sind in Abb. 1b bzw. c gezeigt. Die Dicken von S,N-GQDs liegen meist im Bereich zwischen 0,8–1,2 nm. Nach dem Mischen mit P25-Nanopartikeln dekorierten S,N-GQDs auf P25 und verteilten sich gut, wie das typische TEM-Bild der S,N-GQD/P25-Komposite zeigt (Abb. 1d).
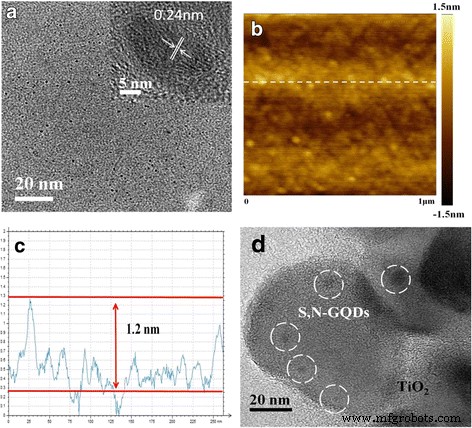
Morphologische Charakterisierungen. a TEM- und HRTEM-Bilder der S,N-GQDs. b , c Ein AFM-Bild und das Höhenprofil der S,N-GQDs. d Ein TEM-Bild der S,N-GQD/P25-Komposite
Die XRD-Muster von reinen P25-, S,N-GQDs- und S,N-GQD/P25-Kompositen sind in Abb. 2 gezeigt. P25 ist eine Mischung aus 80 % Anatas-TiO2 . und zwanzig Prozent Rutil-TiO2 . Die Beugungspeaks bei 25,28°, 36,96°, 37,8°, 48,05°, 53,89°, 55,02°, 62,69°, 70,26° und 75,03° werden (1 0 1), (1 0 3), (0 0 4 ), (2 0 0), (1 0 5), (2 1 1), (2 0 4), (2 2 0) und (2 1 5) Ebene von Anatas TiO2; und die anderen Peaks bei 36,12°, 41,18° und 56,72° gehören zur (1 0 1), (1 1 1) und (2 2 0) Ebene von Rutil-TiO2 (JCPDS-Karte Nr. 21-1272 und Nr. 21-1275). Das Spektrum der S,N-GQDs zeigt einen markanten Peak bei 25,6°, der den (0 02)-Ebenen von Graphitstrukturen entspricht (Schichtabstand von ~0,34 nm) [37]. Bemerkenswert ist, dass im XRD-Spektrum von S,N-GQD/P25 keine typischen Peaks für S,N-GQDs zu finden sind und die Lage und Intensität der aufgetretenen Peaks im Vergleich zu P25 kaum verändert sind. Dies ist auf den geringen Gehalt an S,N-GQDs in den Verbundwerkstoffen zurückzuführen, was eindeutig darauf hindeutet, dass die S,N-GQDs keinen Einfluss auf TiO2 . haben Kristallstruktur und -größe.
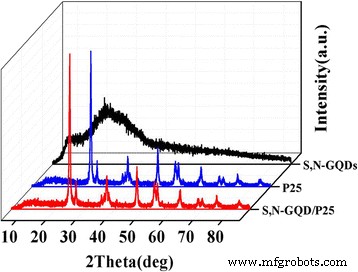
XRD-Muster der Verbundwerkstoffe P25, S,N-GQD und S,N-GQD/P25
Um die erfolgreiche Beladung der S,N-GQDs auf P25 zu demonstrieren, führten wir FTIR- und Raman-Spektrum-Messungen durch (Abb. 3). Im FTIR-Spektrum von S,N-GQDs die O-H-Streckschwingung bei 3232 cm −1 ; der Schwingungspeak von C = O bei 1753 cm −1 , asymmetrische Streckschwingungen von C = S und C–S bei 1185 und 782 cm −1 , bzw. Biegeschwingungen von N-H bei 1558 cm −1 sind sichtbar. Was den reinen P25 betrifft, so liegt der Höchstwert im Ausland bei 400–800 cm -1 entspricht den Bindungen von Ti-O und Ti-O-Ti. Im Vergleich zum P25 zeigt dieses Schwingungsband für S,N-GQD/P25 eine leichte Rotverschiebung, die durch die Kombination von S,N-GQDs und den Streckschwingungen der Ti-O-C-Vibration verursacht wird. Dies bestätigt, dass die S,N-GQDs mit P25 koordiniert sind.
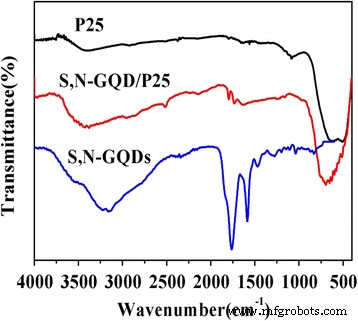
FTIR-Spektren von P25, S,N-GQDs und S,N-GQD/P25
Abbildung 4 zeigt Raman-Spektren von P25, S,N-GQDs und S,N-GQD/P25. Drei offensichtliche charakteristische Peaks bei 396, 519 und 639 cm −1 können gemäß der Symmetriegruppenanalyse Raman-aktiven Moden von P25 zugeschrieben werden. Allerdings zwei zusätzliche D- und G-Peaks bei 1357 und 1593 cm −1 kann im S,N-GQD/P25-Spektrum gesehen werden, die die Raman-aktiven Modi der S,N-GQDs sind. Basierend auf all den obigen Ergebnissen kann geschlossen werden, dass die S,N-GQDs erfolgreich auf das TiO2 . geladen wurden Nanopartikel.
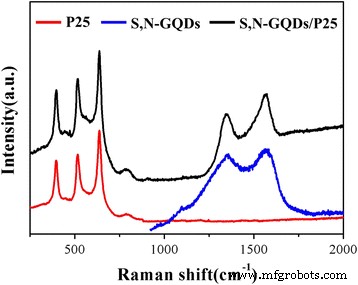
Raman-Spektren von P25, S,N-GQDs und S,N-GQD/P25
Die Lichtabsorption ist ein Schlüsselfaktor, der die photokatalytische Leistung von Photokatalysatoren beeinflusst. Die UV-Vis-Absorption von S,N-GQDs (Abb. 5 a) zeigt zwei Absorptionsbanden, die bei 345 und 462 nm zentriert sind, was sich deutlich von den traditionellen GQDs mit nur einer Absorptionsbande bei etwa 340 nm unterscheidet [38,39 ,40]. Es ist offensichtlich, dass das Dotieren von S und N in GQDs die Bandlücke ändern und zu dieser Unterscheidung führen kann. Aus der Position der Absorptionskante können die optischen direkten Bandlückenwerte der S,N-GQDs unter Verwendung der gut etablierten Tauc-Beziehung (αhυ) . bestimmt werden 2 = α 0 (hυ -E g ), wobei hυ , α 0 und E g sind Photonenenergie, eine konstante bzw. optische Bandlücke [41]. Wie in Abb. 5b gezeigt, kann eine Lückenenergie von 2,5 eV für die direkte Bandlücke für die S,N-GQDs durch Anwendung der linearen Extrapolation leicht erhalten werden. Es wird darauf hingewiesen, dass das E g von S,N-GQDs ist niedriger als TiO2 (3,2 eV), was dieser Bandlückendifferenz von 0,7 eV entspricht, damit die S,N-GQDs in der Lage sind, sichtbares Licht zu absorbieren und durch dieses angeregt zu werden [42]. Die in wässriger Lösung gemessene UV-Vis-Absorption der P25- und S,N-GQD/P25-Komposite ist in Abb. 5c dargestellt. Das reine P25 hat im sichtbaren Lichtbereich von 400–800 nm fast keine Absorption, während die Absorption von S,N-GQD/P25-Verbundstoffen bis in den sichtbaren Bereich bis 800 nm reicht. Offenbar können S,N-GQDs den Photoreaktionsbereich der S,N-GQD/P25-Komposite auf sichtbares Licht effizient erweitern, was seine durch sichtbares Licht angetriebene photokatalytische Aktivität verstärken soll.
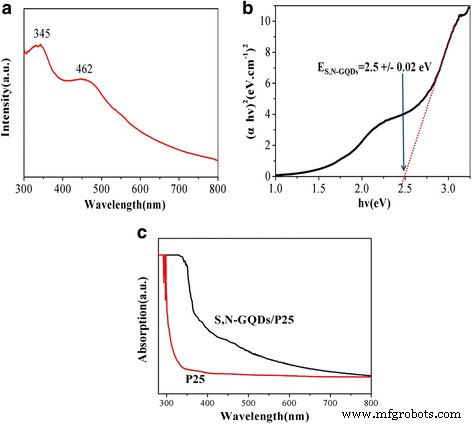
UV-Vis-Messungen. a Das UV-vis-Absorptionsspektrum der S,N-GQDs. b Der entsprechende Tauc-Plot der S,N-GQDs. c Die UV-Vis-Absorptionsspektren von P25 und S,N-GQD/P25
Abbildung 6 zeigt die photokatalytische Leistung einer Vielzahl von Proben mit unterschiedlichen Mengen an S,N-GQDs (Gew.-%) in S,N-GQD/P25 unter UV-Vis-Licht-Bestrahlung in H2 Produktion. Es ist ersichtlich, dass reines P25 ein relativ niedriges photokatalytisches H2 . aufweist Erzeugungsrate (1,7 μmol/h), wahrscheinlich aufgrund dieses TiO2 kann nur UV-Licht und die schnelle Rekombination photogenerierter Elektronen und Löcher absorbieren. Nach der Kupplung mit S,N-GQDs wird das photokatalytische H2 Die Erzeugungsrate der Verbundstoffe nimmt mit der Zunahme der Menge an S,N-GQDs allmählich zu. Die höchste Erzeugungsrate (5,7 μmol/h) wird in der 3 Gew.-% S,N-GQD-Kopplungsprobe erzielt, die 3,6-mal höher ist als die von reinem P25. Diese Ergebnisse zeigen, dass es ein möglicher Weg ist, H2 . zu verbessern Erzeugungsaktivität von reinem TiO2 durch Kopplung mit den S,N-GQDs. Dies wird hauptsächlich darauf zurückgeführt, dass im S,N-GQD-TiO2 . eine gute Energiebandanpassung vorhanden ist Heteroübergang, der eine hocheffiziente Elektron-Loch-Trennung an der Grenzfläche ermöglicht [43]. Darüber hinaus können die S,N-GQDs effizient Elektronen übertragen und die Rekombination photogenerierter Elektronen und Löcher effektiv hemmen. Mit weiterem Ansteigen des Inhalts der S,N-GQDs wird der H2 . jedoch Die Generationsrate nahm allmählich ab, was wahrscheinlich darauf zurückzuführen ist, dass die Opazität und Lichtstreuung der S,N-GQDs die Absorption von einfallendem Licht verringert und die katalytisch aktiven Zentren reduziert [44].
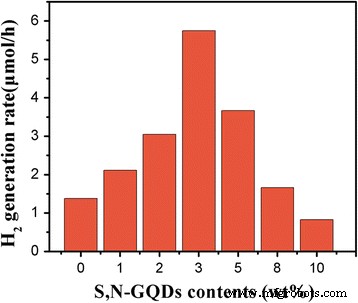
Photokatalytisches H2 Erzeugungsraten von reinen P25- und S,N-GQD/P25-Kompositen mit unterschiedlichen Mengen an S,N-GQDs unter UV-Vis-Licht
Das photokatalytische H2 Generationsrate der Photokatalysatoren wurde auch unter sichtbarem Licht untersucht (λ = 400–800 nm) Bestrahlung. Wie in Abb. 7 gezeigt, zeigt reines P25 fast keine photokatalytische Aktivität, da es im sichtbaren Licht fast keine Absorption aufweist (λ = 400–800 nm) aufgrund seiner großen Bandlücke (3,2 eV, kann es nur durch das Licht angeregt werden λ < 413 nm). Im Gegensatz dazu wird beim Laden von S,N-GQDs auf P25 das photokatalytische H2 Die Evolutionsrate nimmt unter Bestrahlung mit sichtbarem Licht allmählich zu, was zeigt, dass die S,N-GQDs durch sichtbares Licht angeregt werden könnten und eine photokatalytische Aktivität besitzen.
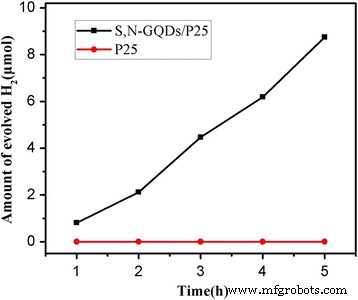
Photokatalytisches H2 Erzeugungsraten von reinem P25 und S,N-GQD/P25-Verbundwerkstoffen (3 Gew.-% S,N-GQD) unter sichtbarem Licht
Um die Praktikabilität von S,N-GQD/P25 in der Photokatalyse besser zu verstehen, haben wir seine Zyklenstabilität untersucht. Abbildung 8 zeigt, dass der S,N-GQD/P25-Komposit-Photokatalysator innerhalb von drei Wiederholungszyklen eine ausgezeichnete Stabilität aufweist, was darauf hindeutet, dass S,N-GQD/P25 eine potenzielle Anwendung im photokatalytischen Bereich haben könnte.
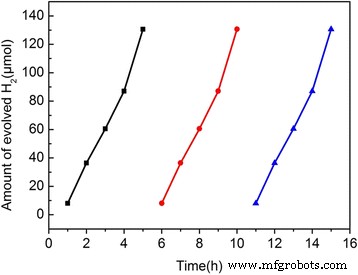
Drei Wiederholungszyklusexperimente mit 3 Gew.-% S,N-GQDs/TiO2
Um weitere Informationen über die Anregung und den Transfer von photogenerierten Ladungsträgern in Photokatalysatoren zu erhalten, wurden die transienten Photostromantworten von P25 und S,N-GQD/P25-Komposit, die auf ITO-Glas beschichtet sind, für mehrere Ein-Aus-Zyklen von UV-Vis-Bestrahlung untersucht . Wie in Abb. 9 gezeigt, zeigen alle P25-, S,N-GQDs- und S,N-GQD/P25-Elektroden empfindliche Photostromreaktionen während wiederholter Ein-/Aus-Zyklen unter der UV-Vis-Bestrahlung. Der sich ändernde Trend der Photostromdichte stimmt mit ihrem photokatalytischen H2 . überein evolutionäre Aktivitäten. Bei der P25-Elektrode gibt es selbst bei hohen angelegten Potentialen eine sehr schwache Photostromantwort auf UV-Vis-Licht. Für die S,N-GQDs-Elektrode ist die Photostromantwort stärker als die von P25 allein, wird aber viel langsamer. Dieses Photostrom-Hystereseverhalten der S,N-GQDs könnte aus einer hohen Rekombinationsrate von photogenerierten Elektronen und Löchern und einem hohen Grenzflächenwiderstand zwischen S,N-GQDs gegenüber Ladungstransfer resultieren [45]. Im Gegensatz dazu hat sich die Photostromantwort von S,N-GQD/P25 nach der Kombination der S,N-GQDs im Vergleich zu P25 allein um das Neunfache verbessert. Der signifikant erhöhte Photostrom von S,N-GQD/P25 kann darauf zurückgeführt werden, dass S,N-GQDs nanoskalige Fragmente von Graphen sind, die eine größere aktive Oberfläche bereitstellen und die Kontaktfläche mit dem TiO2 . Außerdem können S,N-GQDs wie der häufig verwendete Co-Katalysator Pt in photokatalytischem H2 . als Elektronenreservoir dienen , die für den schnellen Transfer photogenerierter Elektronen förderlich ist. Dieses Ergebnis beweist weiter, dass S,N-GQDs als Festkörper-Elektronentransferreagenz den photogenerierten Elektronentransfer beschleunigen können und zeigt, dass das S,N-GQD/P25-Komposit ein vielversprechender Cokatalysator für photokatalytisches H2<. ist /sub> Produktion.
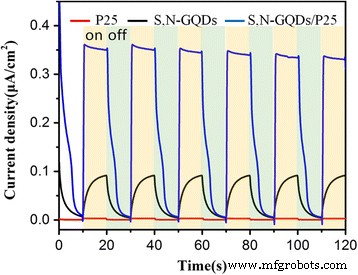
Die vorübergehende Photostromantwort von P25-, S,N-GQDs- und S,N-GQD/P25-Kompositen unter UV-Vis-Lichtbestrahlung
Darüber hinaus zeigt das PL-Spektrum von reinem P25, wie in Abb. 10 gezeigt, eine Emissionsbande im Wellenlängenbereich von 350–550 nm, die der exzitonischen Bandkantenemission von TiO2 . zugeordnet wurde . Im Vergleich zu reinem P25 zeigen alle S,N-GQD/P25-Proben eine wesentlich verringerte PL-Emission, und die Löscheffizienz der PL-Emission steigt mit steigendem S,N-GQDs-Gehalt. Diese Beobachtung zeigt, dass die Ladungsrekombination von TiO2 wurde durch Kombination mit S,N-GQDs stark verzögert. Basierend auf den obigen Ergebnissen haben wir einen möglichen Mechanismus für das verbesserte photokatalytische H2 . vorgeschlagen Produktionstätigkeit der S,N-GQD/P25-Verbundwerkstoffe. Wie in Abb. 11 gezeigt, kann der Mechanismus durch die folgenden drei Punkte beschrieben werden:Erstens können S,N-GQDs unter UV-Licht-Bestrahlung als Elektronenreservoir dienen, um photogenerierte Elektronen von P25 einzufangen und die Abtrennung photogenerierter Elektronen- Lochpaare effizient, was durch die PL-Messung bestätigt wird. Zweitens wirken die S,N-GQDs bei Bestrahlung mit sichtbarem Licht als Photosensibilisator, um P25 zu sensibilisieren und die Elektronen an das Leitungsband von P25 abzugeben, was zu dem durch sichtbares Licht angetriebenen photokatalytischen H2 . führt Produktionstätigkeit. Darüber hinaus können die S,N-GQDs mit einer schmalen Bandlücke von 2,5 eV sichtbares Licht umwandeln und besitzen eine photokatalytische Aktivität bei Bestrahlung mit sichtbarem Licht, was durch UV-Vis-Absorption und photokatalytisches H2 . bestätigt wird Erzeugung unter Messung des sichtbaren Lichts. Der gesamte photokatalytische Reaktionsprozess kann durch die folgenden Gleichungen beschrieben werden [46]:
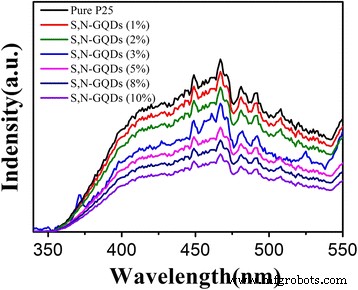
PL-Spektren von reinem P25 und S,N-GQD/P25-Kompositen mit unterschiedlichen Mengen an S,N-GQDs. Anregungswellenlänge:280 nm
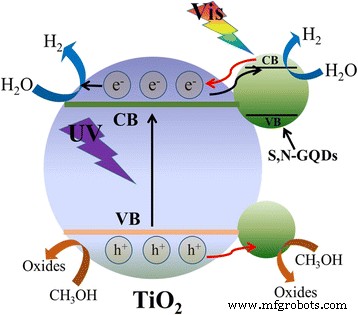
Vorgeschlagener Mechanismus für das photokatalytische H2 Entwicklung von S,N-GQD/P25-Kompositen unter UV-Vis-Lichtbestrahlung
$$ \mathrm{Photokatalysator} + hv\to\ {\mathrm{e}}^{\hbox{-} } + {\mathrm{h}}^{+} $$ (1) $$ {\mathrm{ h}}^{+} + {\mathrm{H}}_2\mathrm{O}\ \to \cdot p\mathrm{O}\mathrm{H} + {\mathrm{H}}^{+} $ $ (2) $$ {\mathrm{CH}}_3\mathrm{O}\mathrm{H} + \cdotp\mathrm{O}\mathrm{H}\\to \cdot p{\mathrm{CH}} _2\mathrm{O}\mathrm{H} + {\mathrm{H}}_2\mathrm{O} $$ (3) $$ \cdotp {\mathrm{CH}}_2\mathrm{O}\mathrm{ H}\ \to\ \mathrm{H}\mathrm{CHO} + {\mathrm{H}}^{+} + {\mathrm{e}}^{\hbox{-} } $$ (4) $ $ 2{\mathrm{H}}_2\mathrm{O} + 2{\mathrm{e}}^{\hbox{-} }\ \to\{\mathrm{H}}_2 + 2{\mathrm{ OH}}^{\hbox{-} } $$ (5) $$ \mathrm{Gesamt}\ \mathrm{Reaktion}:\ {\mathrm{CH}}_3\mathrm{O}\mathrm{H}\ \to\ \mathrm{H}\mathrm{CHO} + {\mathrm{H}}_2 $$ (6)Schlussfolgerungen
Zusammenfassend haben wir die S,N-GQD/P25-Komposite erfolgreich in wässriger Lösung hergestellt. Die Verbundstoffe wurden durch TEM-, HRTEM-, FTIR-, Raman- und XRD-Analysen untersucht. Unsere Ergebnisse zeigten, dass auf P25 dekorierte S,N-GQDs die Absorption von sichtbarem Licht von P25 offensichtlich verbreitern und die Aktivität auf photokatalytischem H2 . erhöhen können Herstellung unter UV-Vis-Licht-Bestrahlung. Insbesondere das 3 Gew. % S,N-GQD/P25 zeigte die beste photokatalytische Fähigkeit, die etwa 3,6-mal höher ist als die von reinem P25. Darüber hinaus zeigten die S,N-GQD/P25-Komposite auch effizientes photokatalytisches H2 Produktionsaktivität unter sichtbarem Licht, die einen Vorteil gegenüber P25 gewann. Insgesamt zeigten die S,N-GQD/P25-Verbundwerkstoffe eine verbesserte Nutzung von Sonnenlicht für die Wasserstofferzeugung und Energieumwandlung.
Nanomaterialien
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Hohe photokatalytische Leistung von zwei Arten von Graphen-modifizierten TiO2-Komposit-Photokatalysatoren
- Erforschung des Zr-Metall-organischen Gerüsts als effizienter Photokatalysator für die Wasserstoffproduktion
- Hierarchische Heterostruktur von ZnO@TiO2-Hohlkugeln für eine hocheffiziente photokatalytische Wasserstoffentwicklung
- CdS-Nanopartikel-modifizierte α-Fe2O3/TiO2-Nanostab-Photoanode für effiziente photoelektrochemische Wasseroxidation
- Bewertung von Graphen/WO3- und Graphen/CeO x -Strukturen als Elektroden für Superkondensatoranwendungen
- Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
- Eliminierung der bimodalen Größe in InAs/GaAs-Quantenpunkten zur Herstellung von 1,3-μm-Quantenpunktlasern
- PtNi-Legierungs-Cokatalysator-Modifikation des Eosin-Y-sensibilisierten g-C3N4/GO-Hybrids für eine effiziente photokatalytische Wasserstoffentwicklung mit sichtbarem Licht
- Einfache Synthese und verbesserte photokatalytische Aktivität mit sichtbarem Licht von neuartigen p-Ag3PO4/n-BiFeO3-Heterojunction-Kompositen für den Farbstoffabbau



