Defekte auf der Oberfläche von Ti-dotiertem MgAl2O4-Nanophosphor
Zusammenfassung
Ti-dotiertes Nano-MgAl2 O4 für weiße Emission wurde durch ein Verbrennungsverfahren synthetisiert. Extrinsische Schottky-Defekte, Al-Leerstellen und Ti 4+ Dotierstoffe in Al-Zentren, von denen angenommen wird, dass sie für die bläulich-weiße Emission verantwortlich sind, wurden durch STEM auf der Oberfläche von Ti-dotiertem Nano-MgAl2 . beobachtet O4 Pulver. Die Stabilitäten der Schottky-Defekt-Assoziationen (TiAl · –VAl ′′′)′′, wurden durch DFT-Rechnung nachgewiesen. Mit diesen Ergebnissen wurde das Emissionsverhalten interpretiert.
Hintergrund
Der Übergang vom Volumen- oder Mikrometerbereich zum Nanobereich beeinflusst ein Material stark und verändert beispielsweise seine mechanischen, optischen und elektrischen Eigenschaften [1, 2, 3, 4, 5, 6]. Diese Veränderungen werden hauptsächlich der Größe und der damit verbundenen Nichtgleichgewichtsstruktur zugeschrieben. Ein Beispiel sind die einzigartigen Phosphoreszenz- und Emissionseigenschaften, die mit Nanopartikeln erreichbar sind [2, 7]. Die Emissionseigenschaften von Nanoleuchtstoffen können zusätzlich zu den beschriebenen Quanten-Confinement-Effekten durch Dotierung moduliert werden [8, 9]. Die Ladungsvalenz eines Dotierungsmittels und die Stelle in der Struktur, die es einnimmt, beeinflussen im Allgemeinen die Emissionseigenschaften eines Leuchtstoffs. Dotierstoffe können sich in einem Nanoleuchtstoff oft an anderen Stellen (z. B. auf der Oberfläche eines Partikels) als den üblichen Stellen in einem Mikrometer-Leuchtstoff befinden. Somit werden die Oberflächen von Nanopartikeln zu wichtigen Stellen für Dotierstoffe, die solche Stellen in Massen- oder Mikrometersystemen normalerweise nicht besetzen. Die Veränderungen im Emissionsverhalten wurden aufgrund des Standorts berichtet, der mit anderen Mängeln verbunden ist [8, 9].
Reines MgAl2 O4 hat einen intrinsischen Defekt von Mg 2+ Stellenangebot, VMg ′′, das Zentrum einer roten Emission bei 720 nm. Bei Einkristallen aus Ti-dotiertem MgAl2 . wird eine starke blaue Emission beobachtet O4; das Verschwinden der roten Emission wird der Ladungskompensation durch die Zugabe von Ti 4+ . zugeschrieben [10, 11]. In unserer vorherigen Arbeit haben wir jedoch festgestellt, dass Ti-dotiertes MgAl2 . im Mikrometerbereich O4 an Luft wärmebehandeltes Pulver erzeugte eine weiße Emission [12]. Der Unterschied wurde durch das Auftreten von roten und grünen Emissionen zusätzlich zu dem Blau, das von Ti-dotiertem MgAl2 . beobachtet wurde, erklärt O4 einzelne Kristalle. Unsere frühere Arbeit [12] simulierte auch den Mechanismus der roten Emission über einen intrinsischen Schottky-Defekt-Assoziat, (VO ·· –VMg ′′) x . Die vorliegende Arbeit berichtet über die visuelle Beobachtung von extrinsischen Schottky-Defekten auf der Oberfläche von Ti-dotiertem MgAl2 O4 Nanopulver und setzt es in Beziehung zum Unterschied in den Emissionsspektren zwischen Mikron- und Nanosystemen.
Methoden
Mg(NO3 )2 ·6H2 O (Mg-Nitrat; 2,46 g, Aldrich), Al(NO3 )3 ·9H2 O (Alnitrat; 7,246 g, Aldrich), CO(NH2 .) )2 (Harnstoff; 5,231 g, Aldrich) und C10 H14 O5 Ti (Ti-Oxy-Acetyl-Acetonat; 0,1 g, Aldrich) wurde als Ausgangsmaterial für die Synthese von Ti-dotiertem Nano-MgAl2 . verwendet O4 . Mg-Nitrat und Al-Nitrat wurden bei der Synthese in einem Molverhältnis von 1:2 verwendet, und die Dotierung mit 2 Mol-% Ti wurde durch Ti-Oxy-Acetylacetonat bereitgestellt. Die Ausgangsmaterialien wurden in entionisiertem Wasser gelöst und die Mischung durch Rühren homogenisiert, bevor das Wasser auf einer Heizplatte verdampft wurde. Die verbleibende Mischung wurde in einen Aluminiumoxidtiegel gegeben und 1 h lang bei 500 000 an Luft gebrannt.
Die Phasen des synthetisierten Nanopulvers wurden durch Röntgendiffraktometrie (XRD; Rigaku) analysiert und die Photolumineszenzeigenschaften wurden durch Fluoreszenzspektrophotometrie (PSI, PL Darsa pro-5000-System) unter Verwendung von monochromatiertem 260- und 360-nm-Licht einer Xe-Lampe gemessen. Pulvermorphologie und -größe wurden durch hochauflösende Transmissionselektronenmikroskopie (TEM; JEOL, JEM-2100F) beobachtet. Bilder des Ti-Dotierstoffs und der Al-Leerstellen wurden auch durch hochauflösendes Abtast-TEM (HR-STEM; JEOL, JEM-2100F) erhalten.
Erste Prinzipien Berechnungen der Dichtefunktionaltheorie (DFT) wurden basierend auf der generalisierten Gradienten-Approximation von Perdew-Burke-Ernzerhof und projektorverstärkten Plane-Wave-Pseudopotentialen, implementiert im Vienna Ab-initio-Simulationspaket (VASP) [13,14,15] mit an . durchgeführt Energiegrenzwert von 500 eV und eine Konvergenz des Selbstkonsistenzfelds von 10 −5 eV. Die Stabilitäten verschiedener Defektassoziate wurden rechnerisch untersucht, um ihre Abhängigkeit von den Positionen der Dotierstoffe und Leerstellen und den relativen Abständen zwischen ihnen zu untersuchen.
Die Oberflächenenergie der (100)-Oberflächenebene im MgAl2 O4 Kristall wurde berechnet; seine Variation mit der Ti-Site wurde ebenfalls untersucht. Die Elementarzelle, deren Kristallstruktur zuvor optimiert wurde, um eine vollständige Relaxation des Gitterparameters, der Kristallform und der Atompositionen zu ermöglichen, wurde zu einer 4 × 1 Superzelle erweitert. {100}-Oberflächen wurden durch Einfügen einer Vakuumplatte in die Superzelle erzeugt. Die Einfügeposition der Vakuumplatte mit einer Größe von 2 × 1 Superzelle wurde variiert, um die Änderung der Oberflächenbildungsenergie mit dem Abstand zwischen der Oberfläche und dem Ti-Dotierungsmittel zu untersuchen. Ein Oberflächenabschluss mit 50 % Mg-Schicht wurde hauptsächlich in Betracht gezogen, da sich herausstellte, dass dies die stabilste (1 0 0) Oberfläche von MgAl2 . ist O4 .
Ergebnisse und Diskussion
Abbildung 1 zeigt das XRD-Muster für Ti-dotiertes MgAl2 O4 Nano-Phosphore mit TEM-Diagrammen. Abbildung 1a bestätigt eindeutig, dass MgAl2 O4 wurde bei 500 °C durch das Verbrennungsverfahren synthetisiert, da es dem JCPDS-XRD-Muster für reines MgAl2 . ähnelt O4 . Die breiten Peaks weisen auf das Vorhandensein von Nanokristalliten hin und beziehen sich auf die in Abb. 1b gezeigten Partikel mit < 20 nm. Im Gegensatz dazu ist das Ti-dotierte mikrometergroße MgAl2 O4 unserer früheren Arbeit [12] zeigt eine hohe Kristallinität, die auf die Hochtemperaturbehandlung des MgAl2 . zurückgeführt wird O4 Pulver (1300 °C für 2 h).
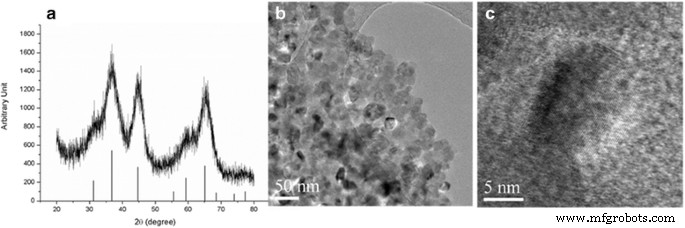
a XRD-Muster für Ti-dotiertes Nano-MgAl2 O4 Pulver synthetisiert bei 500 °C 1 h mit Referenzpeaks von MgAl2 O4 von JCPDS und b , c TEM-Bilder des Pulvers
Die Photolumineszenz-Emissionsspektren von Ti-dotiertem MgAl2 O4 zeigen weiße Emission bei 260 nm Anregung (Abb. 2a) für nano- und mikrometergroße Proben, die in Abb. 2b, c bei 500 °C für 1 h bzw. 1300 °C für 2 h synthetisiert wurden. Die beiden Emissionsbanden führen jedoch zu leicht unterschiedlichen Farben:Die des bei 500 °C synthetisierten Nanopulvers ist gegenüber der des bei 1300 °C hergestellten Pulvers im Mikrometerbereich blauverschoben. Die blaue Emission von Ti-dotiertem MgAl2 O4 Einkristalle werden Ti 4+ . zugeschrieben in Al (oktaedrischen) Zentren, die die einzige Form von Ti-Ionen in den Einkristallen war [10, 11]. Allerdings Ti-dotiertes MgAl2 O4 Es wurde gezeigt, dass mikrometergroßes Pulver sowohl Ti 3+ und Ti 4+ besetzen gleichermaßen Al (oktaedrisch) und Mg (tetraedrisch) [12].
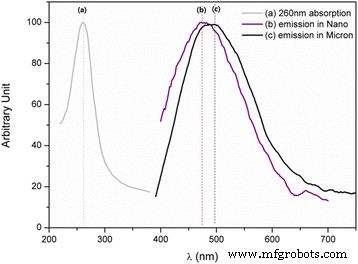
Photolumineszenz von Ti-dotiertem MgAl2 O4 :a 260 nm-Anregung, b nano und c Mikrometer [12]-Pulver, synthetisiert bei 500 °C, 1 h bzw. 1300 °C, 2 h
Abbildung 3a zeigt ein HR-STEM-Bild, das nahe der Oberfläche von Ti-dotiertem Nano-MgAl2 . aufgenommen wurde O4 . Das vergrößerte Bild in Abb. 3b zeigt, dass der Abstand zwischen den Arrays 0,2057 nm beträgt, was gut mit dem (400) planaren Abstand von MgAl2 . übereinstimmt O4 (0,202 nm). Es zeigt, dass die Atomanordnung eine relativ dunkle Leerstelle zwischen den Flecken hinterließ (siehe Pfeile in Abb. 3a, b). Die geringe Helligkeit an der Leerstelle könnte von Atomen in den unteren Schichten herrühren. Der Defektpunkt wird auch im Kontrastintensitätsdiagramm im Einschub identifiziert, das die Kontrastspitzen für die Atome innerhalb des roten Kastens von Abb. 3b zeigt. Der Leerstand wird durch die geringe Kontrastintensität der fünften Stelle von links deutlich. Um die Leerstelle zu identifizieren, haben wir die Fourier-Transformation des Bildes in Fig. 3a durchgeführt und festgestellt, dass die Strahlachse nahe bei [001] liegt (Einschub, Fig. 3a). Aus der [001] projizierten Ansicht eines MgAl2 O4 Kristall, dass Mg-Atome unabhängig voneinander in der (004)-Ebene angeordnet sind, während Al- und O-Atome in derselben Ebene überlappt erscheinen. Wenn die in der Kontrastintensität gezeigte Fluktuation nur auf die konstituierenden Atome in der Ebene zurückzuführen ist, ist es wahrscheinlicher, dass die Leerstelle von einer leeren Al-Stelle statt einer leeren Mg-Stelle stammt.
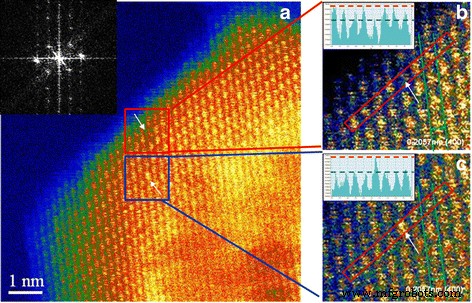
HR-STEM-Bilder von Ti-dotiertem Nano-MgAl2 O4; a . Das Bild zeigt Al 3+ Leerstand und Ti 4+ Dotierstoff in der Nähe mit Fourier-Transformation des Bildes. b Das vergrößerte Bild im roten Kasten von (a ) und Al 3+ Vakanz wird aus einem STEM-Bild mit einer entsprechenden Kontrastintensität aufgedeckt, Einschub von (b ). c Die Kontrastintensität, Einschub von (c ), bestätigt, dass Ti 4+ Dotierstoff besetzt eine Al-Stelle. Die Pfeile zeigen die Positionen von Al-Leerstellen bzw. Ti in der Al-Stelle an
In Abb. 3c ist der durch einen Pfeil im roten Kasten angezeigte Gitterpunkt viel heller als die anderen. Bedenkt man, dass Mg- und Al-Atome aufgrund ihrer ähnlichen Ordnungszahlen nicht durch z-Kontrast unterschieden werden können und Sauerstoffatome aufgrund ihrer niedrigen Ordnungszahl nur schwer nachzuweisen sind, wird dieser hellere Punkt auf den Ti-Dotierstoff geschlossen. Das entsprechende Kontrastintensitätsdiagramm (Einschub, Abb. 3c) hebt den helleren Fleck hervor, was auf das Vorhandensein eines Elements mit höherer Ordnungszahl, definitiv Ti, in diesem System hinweist. Ti in einer Al-Stelle verursacht einen Verschiebungsfehler, weil seine Ladungsvalenz und sein Ionenradius sich von denen von Al 3+ . unterscheiden . Das hellere Atom in der Abbildung erscheint größer als die anderen, in Übereinstimmung mit den größeren effektiven Ionenradien von Ti 3+ (0,081 nm) und Ti 4+ (0,0745 nm) im Vergleich zu Al 3+ (0,0675 nm) [16]. Der effektive Ionenradius von Mg 2+ wird mit 0,086 nm angegeben, was größer ist als die der Ti-Ionen. Daraus haben wir geschlossen, dass die in Fig. 3 (d. h. Fig. 3b, c) gezeigten Defekte VAl . sind ′′′ und TiAl · , in der Erwartung, dass Ti 4+ Ionen kleinerer Größe (0,0745 nm) haben eine größere Chance, freie Al-Plätze einzunehmen als Ti 3+ (0,081 nm).
Abbildung 4a zeigt die Änderung der Oberflächenenergie eines Ti-dotierten MgAl2 . O4 perfekter Kristall, berechnet in Bezug auf die Position des Dotierungsmittels. Die Oberflächenenergie, die ein Hauptfaktor für die Bildungsenergie eines Nanosystems sein kann, nimmt ab, wenn sich Ti der Oberfläche nähert, was darauf hindeutet, dass der Kristall stabiler ist, wenn sich Ti näher an der Oberfläche befindet. Das Ergebnis zeigt einen gemeinsamen Trend für Ti an einer Al-Stelle und Ti an einer Mg-Stelle; jedoch ist der Dotierstoff an einer Mg-Stelle stabiler als an einer Al-Stelle. Dies wird dem größeren effektiven Ionenradius von Mg 2+ . zugeschrieben (0,086 nm) als entweder Ti 4+ (0,0745 nm) oder Al 3+ (0,0675 nm) [16]. Daher ist der Trend wahrscheinlicher, wenn Ti-dotiertes MgAl2 O4 hat eine hohe Kristallinität. Für ein Nanosystem mit geringer Kristallinität trifft dies jedoch möglicherweise nicht immer zu, zumindest in der Nähe der Oberflächenregion.
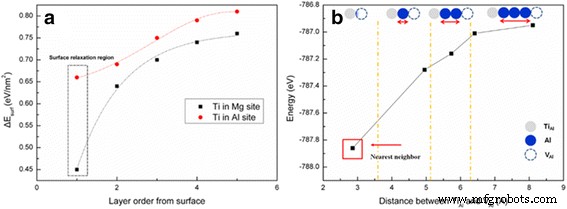
a Stabilitäten von Ti in Mg- oder Al-Leerstellen auf der Oberfläche von MgAl2 O4 :der rote Kreis zeigt die Oberflächenenergie von Ti in der Al-Stelle und der schwarze Punkt ist die von Ti in der Mg-Stelle und b die Bindungsenergie von Defektassoziaten, TiAl · –VAl ′′′ als Funktion der Entfernung
Es wurden auch DFT-Rechnungen durchgeführt, um die Positionierung des Ti-Dotierungsmittels und der Al-Leerstelle zu untersuchen. Die berechnete Energie eines Ti1 Mg15 Al31 O64 Kristall, Spinell mit einem Ti-Dotierstoff (TiAl · ) und eine Al-Leerstelle (VAl ′′′), nimmt zu, wenn das Dotierungsmittel und die Leerstelle auseinander bewegt werden, wie in Fig. 4b gezeigt. Daher wird eine größere Stabilität erreicht, wenn die beiden Defekte nahe beieinander liegen und Defektassoziationen wie (TiAl · –VAl ′′′)′′, die für die blaue Emission verantwortlich sind. Dieses Ergebnis wird der strukturellen Stabilität und der Coulomb-Kraft zwischen den beiden Punktdefekten zugeschrieben. Es entsteht jedoch ein Kompromiss zwischen diesen Faktoren und der Konfigurationsentropie, um das System bei erhöhter Temperatur zu stabilisieren, was dazu führt, dass die beiden Defekte 2–3 Atome voneinander entfernt sind, wie in Abb. 3a gezeigt.
Im Allgemeinen ist die Bildungsenergie einer Al- oder Mg-Leerstelle viel niedriger (~4,5 eV) als die eines Sauerstoffzwischengitters (~ 7,0 eV) in MgAl2 O4 [17, 18]. Auch die Bildungsenergie von intrinsischen Schottky-Defekten für MgAl2 O4 (4,15 eV/Defekt) ist viel niedriger als bei einzelnen Oxiden, MgO (7,7 eV) und α-Al2 O3 (4,2–5,1 eV). Coulomb-Schätzungen zufolge sind die Defektassoziationsenergien extrinsischer Schottky-Paare in verschiedenen ionischen Systemen kleiner als die intrinsischer Schottky-Paare [19]. Bei Ti-dotiertem MgAl2 O4 wird chemisch durch ein Verbrennungsverfahren über einen Nukleations- und Fällungsprozess synthetisiert, wie für das Nanosystem dieser Studie, anstatt durch Festkörperdiffusion, die Bildung von Defekten und Defektassoziationen, einschließlich O 2− Leerstellen, die üblicherweise bei Oxidkeramiken beobachtet werden, würden auf den Partikeloberflächen deutlich erleichtert. Die Gesamtergebnisse zeigen, dass der Defekt assoziiert, d. h. (TiAl · –VAl ′′′)′′, auf der Oberfläche von Ti-dotiertem MgAl2 . vorherrschen O4 Nanopulver, was zu einer Blauverschiebung der weißen Emission von Nanopulvern im Vergleich zu Mikrometerpulvern führt.
Schlussfolgerungen
Die Substitution von Ti in den Al-Stellen von MgAl2 O4 wurde von HR-STEM beobachtet. Eine Al-Leerstelle und ein Ti-Dotierstoff wurden nahe der Oberfläche von Ti-dotiertem Nano-MgAl2 . nachgewiesen O4 . Diese Beobachtungen zeigen das Vorhandensein von Ti 4+ in Al-Standorten. Die Blauverschiebung relativ zum Spektrum des Mikrometersystems wird dem Vorhandensein von mehr Ti 4+ . zugeschrieben Ionen in Al-Stellen an der Oberfläche. Für Ti 4+ . wäre es energetisch günstiger Ionen, um Mg-Stellen in der Spinellstruktur einzunehmen. Allerdings Ti 4+ Ionen neigen dazu, Al-Plätze im Ti-dotierten Nano-MgAl2 . einzunehmen O4 . Dieser Unterschied in der Lumineszenz des Nanosystems resultiert aus seiner geringen Kristallinität, die sich aus der niedrigen Verarbeitungstemperatur ergibt.
Abkürzungen
- Al-Nitrat:
-
Al(NO3 )3 ·9H2 O
- DFT:
-
Dichtefunktionaltheorie
- HR-MINT:
-
Hochauflösendes scannendes TEM
- Mg-Nitrat:
-
Mg(NO3 )2 ·6H2 O
- PL:
-
Photolumineszenz
- TEM:
-
Transmissionselektronenmikroskopie
- Ti-oxy-acetyl-acetonat:
-
C10 H14 O5 Ti
- Harnstoff:
-
CO(NH2 )2
- VASP:
-
Wien-Ab-initio-Simulationspaket
- XRD:
-
Röntgendiffraktometrie
Nanomaterialien
- Defekte an der Oberfläche von Titanlegierungen
- Das Design der Emissionsschicht für Elektronenvervielfacher
- Von Anfang bis Ende:Die Grundlagen der Oberflächenmessung
- Fotoinduzierte Emissionsanalyse zur Identifizierung von Oberflächenverunreinigungen
- Wie erreicht man den Null-Fehler?
- Software:Der Weg zu Null Fehlern
- Was sind die verschiedenen Arten der Oberflächenwasserentwässerung?
- Die Grundprinzipien des Flachschleifens
- Flachschleifen auf die altmodische Art
- Durchsteckmontage und Oberflächenmontage:Was ist der Unterschied?



