Auswirkung technisch hergestellter Nanopartikel auf die Freisetzung exopolymerer Substanzen aus marinem Phytoplankton
Zusammenfassung
Engineered Nanoparticles (ENPs), Produkte aus modernen Nanotechnologien, können potenziell die Meeresumwelt beeinträchtigen und eine ernsthafte Bedrohung für die Meeresökosysteme darstellen. Die zellulären Reaktionen von marinem Phytoplankton auf ENPs sind jedoch noch nicht gut erforscht. Hier untersuchen wir vier verschiedene Kieselalgenarten (Odontella mobiliensis , Skeletonema grethae , Phaeodactylum tricornutum , Thalassiosira pseudonana ) und eine Grünalge (Dunaliella tertiolecta ) für ihre Freisetzung extrazellulärer polymerer Substanzen (EPS) unter Modell-ENP-Behandlungen:25 nm Titandioxid (TiO2 .) ), 10–20 nm Siliziumdioxid (SiO2 .) ) und 15–30 nm Cerdioxid (CeO2 .) ). Wir haben SiO2 . gefunden ENPs können die EPS-Freisetzung aus diesen Algen signifikant stimulieren (200–800%), während TiO2 Die ENP-Exposition induzierte die niedrigste Freisetzung. Darüber hinaus ist der Anstieg von intrazellulärem Ca 2+ Konzentration kann durch ENPs ausgelöst werden, was darauf hindeutet, dass der EPS-Freisetzungsprozess durch Ca 2+ . vermittelt wird Signalwege. Mit einem besseren Verständnis des zellulären Mechanismus der ENP-induzierten EPS-Freisetzung können potenzielle Präventions- und Sicherheitsmaßnahmen entwickelt werden, um negative Auswirkungen auf das marine Ökosystem zu mildern.
Hintergrund
Engineered Nanoparticles (ENPs), deren Größe zwischen 1 und 100 nm (in mindestens einer Dimension) liegt, werden bei der Herstellung zahlreicher Konsumgüter verwendet, darunter Druckertinten und -farben, Reinigungsmittel, Bakterizide, Beschichtungen, Kosmetika, Sonnenschutzlotionen, Reifen, Computerbau und Medikamentenverabreichung. Angesichts der vielversprechenden Anwendung von ENPs belief sich die Finanzierung der National Nanotechnology Initiative (NNI) allein in den USA im Jahr 2017 auf fast 1,4 Milliarden US-Dollar [1,2,3]. Die Etablierung von Grundlagenwissen auf der Nanoskala war in der ersten Phase das Hauptaugenmerk der Nanotechnologie-Forschungsgemeinschaft. 2009 untermauerte dieses neue Wissen einen weltweiten Markt in Höhe von etwa einer viertel Billion US-Dollar, von denen etwa 91 Milliarden US-Dollar auf US-amerikanische Produkte entfielen, die nanoskalige Komponenten enthalten [4]. Mit der rasanten Entwicklung der Nanotechnologie ist es unvermeidlich, dass ENPs irgendwann ihren Weg in aquatische Systeme finden. Die größte Sorge bei ENPs in Bezug auf ihre potenzielle Toxizität (z. B. das Potenzial zur Produktion reaktiver Sauerstoffspezies, ROS) in der Umwelt hängt mit ihrer großen und einzigartigen Oberflächenreaktivität zusammen. Die tatsächlichen Auswirkungen auf das Meeresökosystem bleiben jedoch aufgrund der komplexen ökologischen und biologischen Faktoren natürlicher Gewässer und der Vielfalt der ENPs weitgehend unbekannt [1, 5, 6]. Frühere Studien haben gezeigt, dass ENPs dem algenbasierten marinen Ökosystem erheblichen Schaden zufügen können [7, 8]. Es hat sich gezeigt, dass marine Organismen (insbesondere Phytoplankton) mit ENPs interagieren, was zu negativen Auswirkungen führt [9,10,11]. Mit der potenziellen verstärkten Nutzung der Nanotechnologie in verschiedenen Bereichen können immer mehr ENPs in Gewässer gelangen, sodass die zellulären Reaktionen von marinem Phytoplankton auf ENPs weitere Aufmerksamkeit verdienen [12,13,14,15,16,17,18,19,20, 21].
Die meisten marinen Mikroben, ob auto- oder heterotroph, sind im Allgemeinen in der Lage, exopolymere Substanzen (EPS) zu produzieren, die verschiedene funktionelle Rollen und physikalische Eigenschaften im marinen Ökosystem haben und als Wachstumshemmer, Wachstumsförderer, Toxine, Metallfänger oder als Substrate für der heterotrophe Zyklus [22,23,24,25,26]. EPS, das aus Phytoplankton und Bakterien im Ozean freigesetzt wird, sind polysaccharidreiche anionische kolloidale Biopolymere, die für die Bildung von Meeresgelen, Meeresschnee und Biofilmen sowie für die Kolloid- und Spurenelementaufnahme und zum Schutz vor verschiedenen Umweltbedrohungen entscheidend sind. einschließlich ENPs [7, 15, 19, 20, 25, 27]. Darüber hinaus wird angenommen, dass die Sekretion von EPS eine natürliche Reaktion ist, wenn Phytoplankton verschiedenen Stress ausgesetzt ist [8].
Ca 2+ ist ein häufiger sekundärer Botenstoff, der an einer Vielzahl von intrazellulären Signalwegen beteiligt ist. Es wurde gezeigt, dass Ca 2+ wird für Chemotaxis, Motilität und Adhäsion in der Kieselalge benötigt Amphora coffeaeformis [28]. Verbessertes intrazelluläres freies Ca 2+ Spiegel führen bekanntermaßen zur Aktivierung der Proteinkinase C, die an vielen intrazellulären Signalwegen beteiligt ist [29]. Da die Freisetzung von EPS eng mit der Beweglichkeit und Adhäsion von Kieselalgen verknüpft ist, wurde vorgeschlagen, dass ein Ca 2+ -vermittelter Sekretionsprozess kontrolliert die Freisetzung von EPS aus Diatomeen [30] und der direkte Nachweis von Ca 2+ Signalübertragung, Exozytose und korrelierendes Ca 2+ In unserer vorherigen Studie wurde über eine Signalübertragung mit Exozytose berichtet [31]. Frühere Studien haben auch gezeigt, dass Wechselwirkungen mit ENPs das intrazelluläre Ca 2+ . verändern können Signalwege, die für die Zellsignalisierung essentiell sind [29, 32, 33, 34]. Spezifisches intrazelluläres Ca 2+ Konzentrationsänderungen sind wichtig bei Zellsignalen und Sekretionsvorgängen; Es gibt jedoch keine Berichte über Titandioxid (TiO2 ), Siliziumdioxid (SiO2 ) oder Cerdioxid (CeO2 ) um intrazelluläres Ca 2+ . zu verändern Niveau im Phytoplankton.
2013 haben Quigg et al. [8] fassten die direkten und indirekten toxischen Wirkungen von ENPs auf Algen zusammen. In unseren vorherigen Experimenten wurde gezeigt, dass ENPs die EPS-Aggregation erleichtern [35]. In dieser Hinsicht kann EPS die direkte ENP-induzierte Toxizität gegenüber Wasserorganismen entweder verschlimmern oder reduzieren [7, 15, 36]. Es wurde jedoch nie über eine direkte Messung der EPS-Freisetzung aus Phytoplankton unter ENPs-Stress berichtet. Ziel dieser Studie ist es, die Freisetzung von EPS aus vier verschiedenen Kieselalgenarten (Odontella mobiliensis , Skeletonema grethae , Phaeodactylum tricornutum , Thalassiosira pseudonana ) und eine Grünalge (Dunaliella tertiolecta ) unter ENP-Behandlungen. Durch das Verständnis der zugrunde liegenden Mechanismen der ENP-induzierten EPS-Freisetzung in Phytoplankton kann die Umsetzung von Präventions- und Sicherheitsmaßnahmen potenziell schädliche Auswirkungen auf Meeresorganismen mildern.
Ergebnisse und Diskussionen
ENP-Charakterisierung
Dynamische Laserstreuung (DLS) wurde verwendet, um Größenmetriken der folgenden in reinem Wasser suspendierten ENPs zu charakterisieren:TiO2 , SiO2 , und CeO2 . Die Partikelgrößenverteilung reichte von 7 bis 66 nm in TiO2 , 9 bis 66 nm in SiO2 , und 12 bis 70 nm in CeO2 . Einige größere Größen könnten auf Aggregation oder Agglomeration zurückzuführen sein, während die vorherrschende Größe für TiO2 ist 25 nm, SiO2 10 bis 20 nm beträgt und CeO2 beträgt 15 bis 30 nm, was den Herstellerangaben entspricht (Abb. 1).
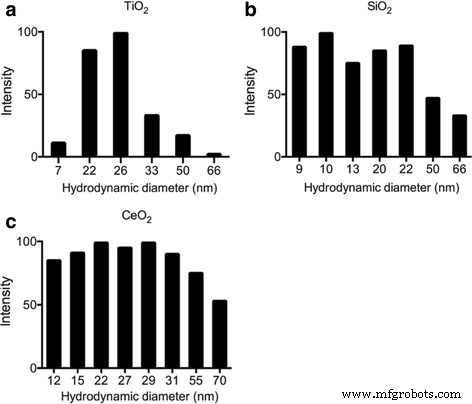
ENP-Charakterisierung durch DLS-Bewertung von a TiO2 , b SiO2 , und c CeO2 in L1-Medium nach der Beschallung zeigt ihre Größenverteilung. Die ENP-Endkonzentration in der DLS-Probe beträgt 1 μg/ml, die Messzeit beträgt 3 min direkt nach der Beschallung
ENPs induzieren intrazelluläres Ca 2+ Konzentration in Phytoplankton
Es sollte untersucht werden, ob ENPs einen Anstieg von intrazellulärem Ca 2+ . bewirken könnten Konzentration wurden Phytoplanktonzellen (OD 600 = 0,8) mit Fluo-4AM-Farbstoff beladen und 1 mg/ml 25 nm TiO2 . ausgesetzt , 10–20 nm SiO2 , und 15–30 nm CeO2 ENPs bzw. Die Veränderung des intrazellulären Ca 2+ Die Konzentration, dargestellt durch die Fluoreszenzintensität innerhalb der Phytoplanktonzellen, wurde 150 s lang überwacht. Abbildung 2a–e zeigen, dass 1 mg/ml von drei entsprechenden ENPs Ca 2+ . erhöht Konzentration in SiO2 um etwa 50–300 %, TiO2 um etwa 40 % und CeO2 um ca. 150–200 %, während die Kontrollbedingungen (L1-Medium) unverändert blieben. Die Ergebnisse zeigen, dass ENPs signifikantes intrazelluläres Ca 2+ . induzieren können Reaktionen in Phytoplankton und legen nahe, dass Phytoplankton auf verschiedene ENPs durch Ca 2+ . reagiert Signalwege. Unsere Daten zeigen nur geringfügige Veränderungen des intrazellulären Ca 2+ Niveaus bei TiO2 vorhanden ist, möglicherweise zurückzuführen auf einen erheblichen Zelltod von Phytoplankton durch TiO2 -induzierte Toxizität [37, 38]. In unserer vorherigen Studie wurde TiO2 veranlasste Erhöhung des intrazellulären Ca 2+ Konzentration [34] neben signifikanter Zellapoptose [39]. Jedoch SiO2 zeigte überraschenderweise das offensichtlichste intrazelluläre Ca 2+ Anstieg für alle Phytoplanktonarten, während CeO2 kann nur ein intermediäres intrazelluläres Ca 2+ . auslösen Konzentrationserhöhung. Frühere Untersuchungen deuteten auf das Potenzial von hohem CeO2 . hin Konzentrationen (> 50 mg/ml), um intrazellulären oxidativen Stress und eine Erhöhung des intrazellulären Ca 2+ . zu induzieren Niveaus, obwohl die Effekte gering waren, und unterstützten unsere Ergebnisse [40]. Wir haben auch das Zeta-Potential jedes ENPs in künstlichem Meerwasser gemessen, um den potentiellen Effekt zu untersuchen, der durch die Oberflächenladung verursacht werden kann; der Wert war jedoch niedrig. Die Messung ergab, dass die ENPs als ungefähr neutral gelten [41] (Zusätzliche Datei 1:Ergänzungsdaten). Dies war der erste Bericht, in dem festgestellt wurde, dass unterschiedliche ENPs intrazelluläres Ca 2+ . induzieren Konzentrationsänderungen in spezifischem Phytoplankton, was letztendlich einen neuen Weg für zukünftige Forschungen ebnet.
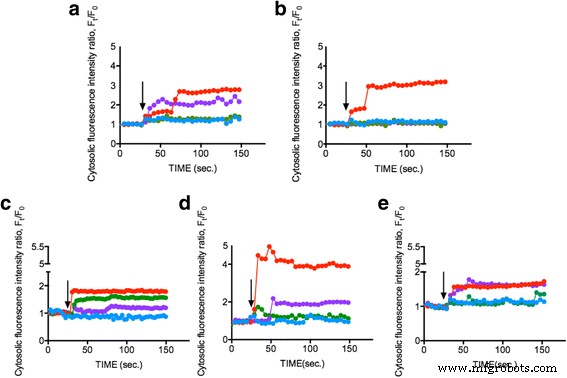
Messung von intrazellulärem Ca 2+ Konzentration nach Stimulation durch verschiedene ENPs. Verschiedene Phytoplanktonzellen a Dunaliella tertiolecta , b Thalassiosira pseudonana , c Skeletonema grathae , d Phaeodactylum tricornutum , und e Odontella mobiliensis wurden mit TiO2 . behandelt 25 nm (grün), SiO2 10–20 nm (rot), CeO2 15–30 nm (violett) mit einer Konzentration von 1 mg/ml und Kontrolle (blau). Der schwarze Pfeil zeigt den Zeitpunkt an, zu dem EPNs angewendet wurden (30 s). Die Messungen zeigen repräsentative Daten von durchschnittlich 20 Einzelzellen
ENP-induzierte EPS-Freisetzung in Phytoplankton
Enzyme-linked lectin Assay (ELLA) wurde verwendet, um die Menge der EPS-Freisetzung aus Phytoplanktonzellen bei Stimulation mit TiO2 . zu bestimmen , SiO2 , und CeO2 ENPs, Konzentrationsbereich von 1 μg/ml bis 5 mg/ml, basierend auf früheren Studien für TiO2 [42, 43] und CeO2 [44,45,46]. Die EPS-Sekretion wurde auf die gesamte Phytoplankton-DNA-Menge normalisiert (zusätzliche Datei 1:Ergänzungsdaten), um eine gleiche Vergleichsbasis zu haben. Im Vergleich zur Kontrolle haben wir festgestellt, dass 10–20 nm SiO2 kann die EPS-Freisetzung bei Dunaliella um bis zu 550 % steigern , 500 % in Thalassiosira , 1000 % bei Skelettem , 400 % in Odontella , und 900 % bei Phaeodactylum (Abb. 3). Als die Phytoplankton-Spezies TiO2 . ausgesetzt waren , gab es keine starke Wirkung auf die EPS-Sekretion, da nur Skelettema und Phaeodactylum zeigten deutliche Veränderungen. Die Daten zur Freisetzung von EPS stimmen daher mit unserem intrazellulären Ca 2+ . überein Konzentration ergibt. TiO2 keinen signifikanten Einfluss auf die EPS-Produktion, ähnlich der Tatsache, dass intrazelluläres Ca +2 Die Konzentrationen zeigten aufgrund der Toxizität von TiO2 . sehr begrenzte Veränderungen zum Phytoplankton. Die Produktion und Rückstände von ROS können zu vielen Komplikationen wie Apoptose im Phytoplankton führen [47,48,49]. In der CeO2 Behandlung zeigten die Ergebnisse eine geringfügige Wirkung bei Dunaliella , Skelettema , Odontella , und Phaeodactylum . Jedoch SiO2 zeigte die signifikanteste EPS-Induktion bei Thalassiosira pseudonana (ca. 600 %) und Skeletonema grethae (ca. 1000–1500%). Diese Daten weisen darauf hin, dass verschiedene ENPs eine spezifische EPS-Freisetzung aus Phytoplankton und intrazellulärem Ca 2+ . induzieren können Änderungen stimmen auch mit EPS-Release-Ergebnissen überein. Durch Bewertung der Veränderungen des intrazellulären Ca 2+ Konzentration ist ein direkter Zusammenhang im Ca 2+ zelluläre Wege, in denen ENPs die EPS-Sekretion von Phytoplankton hervorrufen. Die Beobachtung hier stimmt mit unseren früheren Studien auf der Grundlage von Phaeocystis . überein EPS-Veröffentlichung [31]. Die Ergebnisse liefern direkte Beweise dafür, dass Phytoplankton ENPs erkennen und unterscheiden kann, die mit unterschiedlicher EPS-Freisetzung reagieren, die durch Ca 2+ . reguliert wird Zellwege.
Die Verwendung von ELLA ermöglichte es uns, die Freisetzung von EPS über die Interaktionen des Phytoplanktons mit den ENPs zu bestimmen. Unsere Ergebnisse zeigen, dass die EPS-Sekretion signifikant erhöht wurde, als das Phytoplankton mit SiO2 . interagierte für Dunaliella tertiolecta , Thalassiosira pseudonana , und Skeletonema grethae . Es scheint, dass diese Kieselalgen darauf vorbereitet sind, SiO2 . zu erkennen Partikel. Bei Phaeodactylum tricornutum , eine starke EPS-Sekretion wurde nicht gefunden. Dieser Unterschied stellt die EPS-Freisetzung dar, die durch ENPs ausgelöst wird, die von der Phytoplanktonart und der ENP-Konzentration abhängig sind (Abb. 3). In einer früheren Studie verursachten Ölverschmutzungen große mikrobielle EPS-Freisetzungen im Meer, die vorgeschlagen wurden, um den negativen Folgen von Ölverschmutzungen entgegenzuwirken [50]. Außerdem fanden Boglaienko und Tansel heraus, dass SiO2 Partikel konnten Ölaggregate effizient entfernen [51]. Unsere Entdeckung liefert einen neuen potentiellen Mechanismus, bei dem SiO2 . mit geringer Toxizität Partikel können die EPS-Freisetzung aus spezifischem Phytoplankton induzieren, was möglicherweise die Entfernung von Ölverschmutzungen erleichtert, indem sie die EPS-Aggregation fördern. Es wurde nie berichtet, dass Cerdioxid die Meeresökosysteme auf Phytoplanktonbasis stört. Die Ergebnisse hier zeigten CeO2 ENPs können hier das gesamte Phytoplankton außer Thalassiosira pseudonana beeinflussen CeO2 ENPs können, wie SiO2, haben die Fähigkeit, die EPS-Freisetzung aus bestimmtem Phytoplankton für Anwendungen zur Ölminderung zu steigern.
Schlussfolgerungen
Die Wechselwirkung zwischen ENP und der Meeresumwelt wird aufgrund aktueller und zukünftiger Freisetzungen von Nanomaterialien immer kritischer. Hier zeigen wir eine verstärkte EPS-Sekretion als eine der Hauptwirkungen von ENPs auf Phytoplankton. Wir liefern auch Beweise dafür, dass verschiedenes Phytoplankton unterschiedlich auf verschiedene ENP-Stress reagieren kann, indem es Ca 2+ . reguliert Wege. Eine vollständige Bewertung der ENPs zu marinen Ökosystemen würde jedoch weitere Untersuchungen erfordern, um detaillierte Kenntnisse und ein Verständnis der Wechselwirkungen zwischen Nanomaterialien und Meeresorganismen zu erhalten.
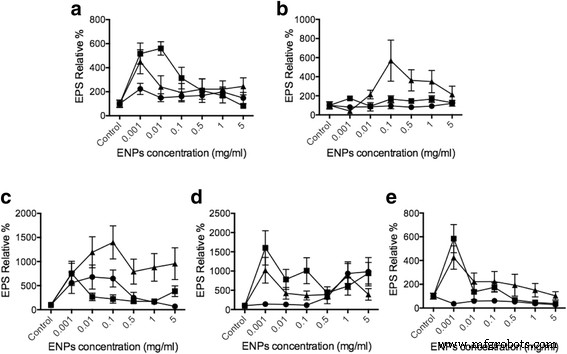
EPS-Freigabe ausgelöst durch verschiedene ENPs. Verschiedene Phytoplanktonzellen a Dunaliella tertiolecta , b Thalassiosira pseudonana , c Skeletonema grathae , d Phaeodactylum tricornutum , und e Odontella mobiliensis wurden mit TiO2 . behandelt (Kreise), SiO2 (Dreiecke), CeO2 (Quadrate) mit Konzentrationen von 5 mg/ml bzw. 1 mg/ml, 0,5 mg/ml, 0,1 mg/ml, 10 μg/ml, 1 μg/ml (n = 3)
Methoden
Phytoplankton-Kultur
Batchkulturen von Odontella mobiliensis (CCMP597), Dunaliella tertiolecta (UTEX999), Skeletonema grethae (CCMP775), Phaeodactylum tricornutum (UTEX646), Thalassiosira pseudonana (Provasoli – Guillard marine Phytoplankton Culture Collection, West Boothbay Harbor, MN, USA) wurden in L1 marinem Medium (Sigma, MO, USA) in einem 14:10 (hell:dunkel) Zyklus bei 100 μmol m −2 . gezüchtet s −1 und 24 °C unter axenischen Bedingungen. Die Wachstumsphase der Kultur wurde durch Zellzählung mit einem Hämozytometer bestimmt.
Nanopartikel und Charakterisierung
Alle ENPs, TiO2 , SiO2 , CeO2 (Sigma-Aldrich, MO, USA), wurden vor der Verwendung in reinem Wasser beschallt. ENPs wurden mit gefiltertem L1-Medium (Sigma, MO, USA) rekonstituiert, bevor sie getestet wurden. Die Größe der ENPs wurde unabhängig durch Homodyne Dynamics Laser Scattering (DLS) bestätigt. Kurz gesagt wurden Meerwasserproben durch eine 0,22-μm-Millipore-Membran (vorgewaschen mit 0,1 N HCl) erneut gefiltert und direkt in fünf 10 ml-Streuzellen gegossen, die dann im Goniometer eines Brookhaven BI-200SM-Laserspektrometers (Brookhaven Instruments, New York, USA). Die Autokorrelationsfunktion der Streuungsintensitätsfluktuationen, die bei einem 45°-Winkel detektiert wurden, wurde online von einem Brookhaven BI 9000AT Autokorrelator verarbeitet, und die Teilchengrößenverteilung wurde durch das CONTIN-Verfahren (Provencher, 1982) berechnet. Die Ergebnisse jeder Probe wurden in dreifacher Ausfertigung direkt nach der Beschallung gesammelt. Die Kalibrierung des DLS-Spektrometers wurde unter Verwendung von Standardsuspensionen monodisperser Latex-Mikrokügelchen (Polysciences, PA, USA) durchgeführt.
ENP-Behandlung
Die Phytoplanktonzellen wurden in einer 96-Well-Platte mit L1-Medium für 24 h kultiviert. Zellen wurden mit ENP-Vorräten behandelt:5 mg/ml und 1 mg/ml, 0,5 mg/ml, 0,1 mg/ml, 10 μg/ml, 1 μg/ml des TiO2 , SiO2 , und CeO2 (Sigma-Aldrich, MO, USA) oder L1-Medium (Kontrolle) für 48 h. Der sekretierte EPS enthaltende Überstand wurde gesammelt und kurz bei 4000 U/min zentrifugiert, um die restlichen ENPs zu entfernen. Dieses Protokoll wurde aus unserer vorherigen Veröffentlichung [34] übernommen. Der hier verwendete Konzentrationsbereich soll nicht die aktuellen ENP-Werte in der Umwelt darstellen oder nachahmen, sondern soll die vollständige potenzielle Wirkung von ENPs auf marines Phytoplankton abschätzen und die assoziierten zellulären Mechanismen untersuchen. Als vielversprechendes neues Nanomaterial haben ENPs noch nicht ihre volle kommerzielle Leistungsfähigkeit erreicht. Eine detaillierte Bewertung ihrer vollständigen ökologischen Auswirkungen ist dringend erforderlich, bevor ENPs auf den Markt für Handels- und Haushaltsprodukte gelangen, um mehr ENPs in die Ozeane zu bringen.
Enzyme-Linked Lektin Assay (ELLA)
Der sekretierte Polysaccharid enthaltende Überstand wurde gesammelt und kurz bei 1700 rcf (Megafuge 1.0R) zentrifugiert, um die restlichen ENPs zu entfernen. Der Überstand wurde dann in einer 96-Well-Platte (Nunc MaxiSorp, VWR, CA, USA) über Nacht bei 4 °C inkubiert. Danach wurde die 96-Well-Platte mit PBST (PBS + 0,05% Tween-20) und PBS gewaschen und dann mit 1% BSA blockiert. Die 96-Well-Platte wurde erneut mit PBST und PBS gewaschen und mit Lektin (Concanavalin A, ConA) (Sigma-Aldrich, MO, USA), konjugiert an Meerrettichperoxidase (HRP; 5 mg/ml) (Sigma-Aldrich, MO .) inkubiert , USA), bei 37 °C für 1 h. Das Substrat, 3,39,5,59-Tetramethylbenzidin (TMB; Sigma-Aldrich, MO, USA), wurde bei Raumtemperatur in jede Vertiefung gegeben, gefolgt von H2 SO4 (Sigma-Aldrich, MO, USA), um die Reaktion zu beenden. Die optische Dichte wurde bei 450 nm von PerkinElmer VICTOR3 (MA, USA) gemessen. Dieses Protokoll wurde aus unserer vorherigen Veröffentlichung [34, 52] übernommen.
DNA-Bestimmung
Das Phytoplankton enthaltende Pellet wurde gesammelt und das ZR-96 Quick-gDNA-Kit (ZYMO Research, CA, USA) erhalten. Kurz gesagt wurde 4x Lysepuffer verwendet, um Phytoplanktonzellen aufzubrechen und durch die DNA-Bindungssäule zu fließen, die am Ende durch Elutionspuffer eluiert wurde. DNA-Konzentrationen wurden mit NanoDrop ND-1000 (Thermo, CA, USA) gemessen. Das Protokoll wurde dem Protokoll des hergestellten Kits angepasst.
Messungen von intrazellulärem Ca 2+ Durch ENPs induzierte Konzentrationen
Die Phytoplanktonzellen wurden dann 60 min lang mit einem Fluo-4AM-Farbstoff (1 mM) (Kd = 335 nM, λEx = 494 nm und λEm = 506 nm, ThermoFisher, CA, USA) beladen [31]. Nach der Farbstoffbeladung wurden die Phytoplanktonzellen gespült, mit L1-Medium inkubiert und mit 1 mg/ml TiO2 . behandelt , SiO2 , und CeO2 bzw. Alle Calcium-Signalisierungsexperimente wurden an einem Nikon-Mikroskop (Nikon Eclipse TE2000-U, Tokio, Japan) durchgeführt. Protokoll und Bedingungen wurden aus früheren Veröffentlichungen angepasst [31, 34].
Zeta-Potenzial der ENP-Messung
Um die Oberflächenladungen von ENPs zu messen, wurde das Zetapotential (ζ) von ENPs mit einem Zetasizer Nano ZS, Malvern, in Gegenwart von künstlichem Meerwasser bei 25 °C gemessen. Nachdem die Daten von jeder Probe gesammelt wurden, wurden die aufgezeichneten Werte gemittelt.
Statistische Analyse
Die Daten werden als Mittelwerte ± SD angegeben. Jedes Experiment wurde unabhängig mindestens dreimal durchgeführt. Histogramme wurden von GraphPad Prism 6.0 erstellt. (GraphPad Software, Inc., San Diego, CA, USA).
Nanomaterialien
- Halbleiter-Nanopartikel
- Plasmonische Nanopartikel
- Die Wirkung des pH-Werts auf gelbe Farbstoffe aus dem Garten
- Bildungsmechanismus wohlgeordneter dicht gepackter Nanopartikel-Übergitter, die aus der Gasphase auf templatfreien Oberflächen abgeschieden werden
- Nanopartikel als Effluxpumpe und Biofilm-Inhibitor zur Verjüngung der bakteriziden Wirkung konventioneller Antibiotika
- Folatrezeptor-gerichtete Bioflavonoid-Genistein-beladene Chitosan-Nanopartikel für eine verbesserte Antikrebswirkung bei Gebärmutterhalskrebs
- Nanotechnologie:vom In-vivo-Bildgebungssystem zur kontrollierten Medikamentenabgabe
- Auswirkung der Synthesemethode von La1 − xSr x MnO3 Manganit-Nanopartikeln auf ihre Eigenschaften
- Toxizität von PEG-beschichteten CoFe2O4-Nanopartikeln mit Behandlungseffekt von Curcumin
- Wirkung des sauren Peptisierungsmittels auf das Anatas-Rutil-Verhältnis und die photokatalytische Leistung von TiO2-Nanopartikeln



