Kohlenstoff-Nanomaterialien zur Behandlung von schwermetallverseuchtem Wasser und zur Umweltsanierung
Zusammenfassung
Die Nanotechnologie ist ein fortschrittliches Wissenschaftsgebiet, das in der Lage ist, eine Vielzahl von Umweltherausforderungen zu lösen, indem die Größe und Form der Materialien im Nanomaßstab kontrolliert wird. Kohlenstoff-Nanomaterialien sind aufgrund ihrer ungiftigen Natur, ihrer großen Oberfläche, ihrer leichteren biologischen Abbaubarkeit und ihrer besonders nützlichen Umweltsanierung einzigartig. Die Schwermetallbelastung im Wasser ist ein großes Problem und stellt ein großes Risiko für die menschliche Gesundheit dar. Kohlenstoff-Nanomaterialien erhalten aufgrund ihrer überlegenen physikalisch-chemischen Eigenschaften, die für die fortschrittliche Behandlung von schwermetallverseuchtem Wasser genutzt werden können, immer mehr Aufmerksamkeit. Kohlenstoff-Nanomaterialien, nämlich Kohlenstoff-Nanoröhrchen, Fullerene, Graphen, Graphenoxid und Aktivkohle, haben aufgrund ihrer großen Oberfläche, ihrer nanoskaligen Größe und der Verfügbarkeit verschiedener Funktionalitäten ein großes Potenzial zur Entfernung von Schwermetallen aus Wasser und sind leichter chemisch zu modifizieren und recycelt. In diesem Artikel haben wir die jüngsten Fortschritte bei der Anwendung dieser Kohlenstoff-Nanomaterialien bei der Behandlung von schwermetallverseuchtem Wasser überprüft und auch ihre Anwendung bei der Umweltsanierung hervorgehoben. Toxikologische Aspekte von kohlenstoffbasierten Nanomaterialien wurden ebenfalls diskutiert.
Einführung
Verschmutzung wird als das Vorhandensein unerwünschter chemischer Einheiten bezeichnet, die den natürlichen Prozess verhindern oder nachteilige Auswirkungen auf lebende Organismen und die Umwelt haben [1,2,3]. Die Industrialisierung und der immense Bevölkerungszuwachs, der zu einer zunehmenden Urbanisierung führt, führen zu einem alarmierenden Anstieg der Umweltverschmutzung [2, 4]. Die Verbesserung der Wasser-, Boden- und Luftqualität ist eine immense Herausforderung der Neuzeit. Die Identifizierung und Behandlung von Umweltschadstoffen und deren Vermeidung ist ein wichtiger Schritt zum Schutz der Umwelt. Die Materialwissenschaft spielt eine entscheidende Rolle bei der Verwirklichung des Ziels einer sauberen Umwelt, und die Technologie der Materialwissenschaften hat sich in den letzten zehn Jahren exponentiell weiterentwickelt, insbesondere bei Nanomaterialien [1, 5]. Das reine und saubere Wasser wird aufgrund der Industrialisierung knapp, und die Welt sieht sich insbesondere in den Entwicklungsländern mit einem Mangel an sauberem Wasser konfrontiert [6]. Wasserverunreinigungen können organische Stoffe, Bakterien, Viren, Farbstoffe und Schwermetallionen wie Blei, Cadmium, Zink, Nickel, Arsen, Chrom und Quecksilber sein, da sie nicht biologisch abbaubar sind und ein großes Risiko für die menschliche Gesundheit darstellen. Schwermetallionen können viele Nebenwirkungen wie Krebs, Nierenschäden, Hepatitis, Fehlgeburten, Anämie, Enzephalopathie und nephritisches Syndrom verursachen [7,8,9,10]. Bleiionen werden im Allgemeinen aus der Metallbergbauindustrie von Bleisäurebatterien, der Papier-, Glas- und Polierindustrie in die Umwelt freigesetzt. Cadmium wird im Allgemeinen in Wasser gefunden, das beim Galvanisieren von Batterien, Photovoltaikzellen, Metallurgieprozessen und Stofffabriken ausgestoßen wird [11]. Nickelionen können Hautkrankheiten verursachen, wenn sie mit Schmuck, Reißverschlüssen, Uhren, Münzen usw. in Kontakt kommen. Chrommetallionen (VI) verursachen Krankheiten wie Leberschäden, Nephritis und Magenbeschwerden, und Cr (VI)-Ionen sind auch die Hauptursache für Nasenschleimhautulkus [12]. Abbildung 1 zeigt die Adsorption von Schwermetallionen auf dem Kohlenstoffnanomaterial (Graphen) und Abbildung 2 zeigt die verschiedenen Quellen der Schwermetallbelastung in der Umwelt. Aufgrund dieser schwerwiegenden Nebenwirkungen ist die Entfernung von Schwermetallionen aus dem Wasser von größter Bedeutung, um Menschenleben vor solchen problematischen Gesundheitsproblemen zu retten. Giftige Metallionen konnten durch zahlreiche Methoden wie Ionenaustausch, Umkehrosmose, Fällungsfiltration, Biosorption, Koagulation und Extraktion entfernt werden [13, 14]. Die Adsorption gilt als die beste Methode, da sie kostengünstig, hocheffizient und einfach zu handhaben ist, um Spuren von Schwermetallionen zu entfernen [15]. Für die Wasseraufbereitung wurden verschiedene Materialien wie Pflanzenadsorbentien und organische Naturstoffe verwendet, insbesondere Huminsäure, die weit verbreitet zur Wasserdesinfektion und zur Entfernung von Schwermetallionen verwendet wird [8, 16, 17, 18, 19]. Wanget al. haben die Huminsäure und ihr Nanokomposit in der Wasseraufbereitung umfassend untersucht [20].
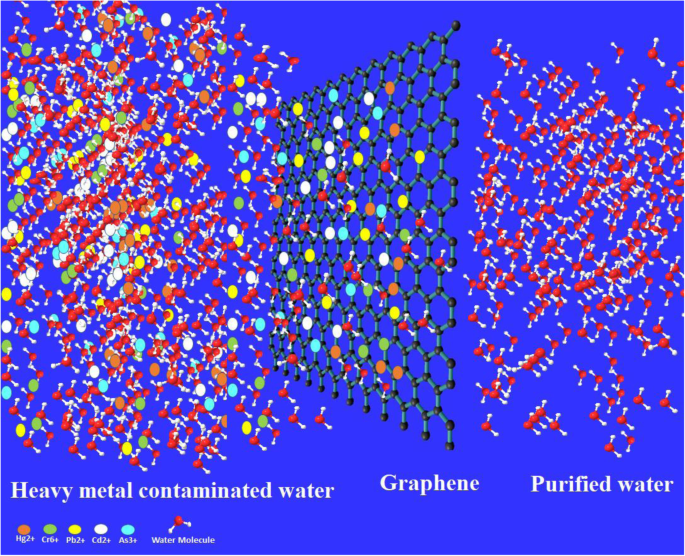
Grafische Zusammenfassung, die zeigt, dass der Reinigungsprozess von schwermetallverseuchtem Wasser unter Verwendung von Graphen und anderen kohlenstoffbasierten Materialien dasselbe bewirken kann
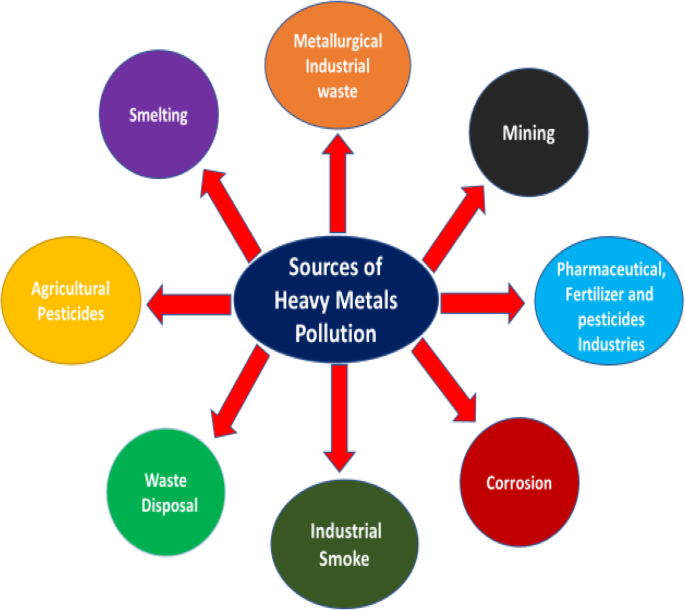
Quellen der Schwermetallbelastung in der Umwelt
Die Nanotechnologie-Plattform findet Anwendung in fast allen Bereichen wie Umweltwissenschaften, Gesundheitswissenschaften, Elektronik, industrielle Trennung, tragbare Wasseraufbereitungsanlagen für große/kleine Anlagen, Katalysatoren, Energiespeicherung und Energieerzeugung [21,22,23]. Nanomaterialien bieten aufgrund der großen Oberfläche der Nanosorbentien und ihrer Fähigkeit zur chemischen Modifizierung und leichteren Regeneration eine besondere Plattform für die Reinigung von kontaminiertem Wasser. Nanomaterialien werden mehr und mehr für die Entfernung verschiedener Arten von Schadstoffen, nämlich organische Stoffe, Metallionen, biologische Schadstoffe und Arsen, aus dem Wasser verwendet [24,25,26,27]. Kohlenstoff-Nanomaterialien, nämlich Graphen, Graphenoxid, Kohlenstoff-Nanoröhrchen, Fullerene und Aktivkohlen, werden aufgrund ihrer außergewöhnlichen chemischen, mechanischen, thermischen und Elektrische Eigenschaften. In diesem Artikel haben wir versucht, die neuesten Fortschritte bei der Anwendung von Kohlenstoffnanomaterialien, nämlich Fullerene, Kohlenstoffnanoröhren (CNTs), Graphen, Graphenoxid und Aktivkohle bei der Reinigung von mit Schwermetallionen kontaminiertem Wasser zu überprüfen.
Menschliche Gesundheit und Schwermetalltoxizität
Die Schwermetalle werden normalerweise anhand ihres Atomgewichts definiert; als Schwermetalle werden jedoch auch für Lebewesen giftige Elemente bezeichnet [28]. Bestimmte Schwermetalle sind in ihren unterschiedlichen Formen und Dosen tödlich für die menschliche Gesundheit und andere Lebewesen (Tabelle 1). Schwermetalle gelten häufig als giftig; Leichtere Metalle können jedoch ebenfalls tödlich sein, beispielsweise Beryllium und Lithium. Nicht alle Schwermetalle sind gesundheitsgefährdend, einige sind elementar, zum Beispiel Eisen und Cr(III). Die bekanntesten giftigen Metalle sind Pb, Cd, Cr, Mn, Hg, As und radioaktive Metalle. Radioaktive Metalle haben sowohl radiologische als auch chemische Toxizität. Die Toxizität von Schwermetallen hat sich als eine große Bedrohung erwiesen, und mit ihnen sind viele Gesundheitsrisiken verbunden. Die tödliche Wirkung dieser Metalle besteht darin, dass sie keine biologische Rolle spielen; sie können jedoch ein Element des Körpers nachahmen und den Stoffwechsel und andere biologische Prozesse stören. Einige Metalle wie Aluminium können leicht durch das Ausscheidungssystem eliminiert werden, während sich bestimmte Metalle in der Nahrungskette und im Körper ansammeln. Die metallinduzierte Toxizität hängt von der Dosis, dem Expositionsweg und der Kontaktzeit (z. B. akut oder chronisch) ab. Details zur Toxizität im Zusammenhang mit verschiedenen Schwermetallen sind unten aufgeführt.
Toxizität von Quecksilber (Hg)
Quecksilber (Hg) ist ein D-Block-Element mit der Ordnungszahl 80 und liegt unter Standardbedingungen in flüssiger Form vor. Quecksilber kommt in Ablagerungen von Quecksilbersulfid vor, das Zinnober genannt wird. Die Quecksilberverschmutzung wird durch die pharmazeutische Industrie, die Zellstoff- und Papierkonservierung, die Natronlaugeproduktion, die Landwirtschaft usw. verursacht [47]. Quecksilber ist das giftigste Schwermetall in der Umwelt, und eine Quecksilbervergiftung wird als rosa Krankheit bezeichnet, auch Akrodynie genannt. Quecksilber kann sich mit organischen und anorganischen Verbindungen verbinden. Erhöhte Quecksilberbelastungen in jeglicher Form können die Nieren, das Gehirn, den sich entwickelnden Fötus usw. schädigen [48]. Die Umweltschutzbehörde hat Methylquecksilber und Quecksilberchlorid als krebserregend eingestuft. Quecksilberexposition kann auch Lungenschäden, Hautausschläge, Gedächtnisprobleme und Haarausfall verursachen. Die Weltgesundheitsorganisation (WHO) hat den Standard für Trinkwasser mit niedrigerem Quecksilbergehalt auf 0,01 mg/l festgelegt [29].
Toxizität von Blei (Pb)
Blei (Pb) ist ein Element mit der Ordnungszahl 82 und gilt als Schwermetall mit silbrig-bläulichem Aussehen, das sich durch Lufteinwirkung mattgrau verfärbt [30]. Es gibt verschiedene Quellen der Bleiverschmutzung, hauptsächlich Abfälle aus der Batterieindustrie, Düngemittel und Pestizide, Metallbeschichtungs- und Veredelungsarbeiten, Abgase, Zusatzstoffe in Benzin, Pigmente in Autos und Schmelzen von Erzen. Dieses schwere giftige Metall wird aufgrund seiner weit verbreiteten Verwendung weltweit zu einem Umwelt- und Gesundheitsproblem [31]. Blei (Pb) ist ein krebserregendes Element, das von der Environmental Protection Agency (EPA) deklariert wurde. Bleivergiftung ist ein Begriff, der wegen seiner Toxizität verwendet wird und akut oder chronisch sein kann. Bleivergiftung kann geistige Behinderung, Geburtsfehler wie Autismus, Allergien, Legasthenie, Lähmung, Hirn- und Nierenschäden verursachen und auch zum Tod führen [32].
Toxizität von Arsen (As)
Arsen ist ein metalloides Element mit der Ordnungszahl 33 und kommt in mineralischer Form häufig in Kombination mit Schwefel, einigen anderen Metallen, Eisen-, Calcium-, Natrium- und Kupfersalzen sowie in reiner elementarer Form vor [33]. Das Wasser ist durch Pestizide auf Arsenbasis, Ablagerungen natürlicher Mineralien und unsachgemäße Entsorgung von Reagenzien oder Chemikalien auf Arsenbasis verunreinigt. Arsen in Form von Arsenat und Arsenit ist tödlich für Umwelt und Lebewesen. Arsen stört das Protoplasma der Zellen, indem es mit der Sulfhydrylgruppe der Zellen interagiert, was zu einer Fehlfunktion der Atmung führt und die Mitose und Zellenzyme beeinflusst [34].
Toxizität von Cadmium (Cd)
Cadmium hat die Ordnungszahl 48 und ist ein bläulich-weißes Weichmetall mit ähnlichen chemischen Eigenschaften wie Quecksilber und Zink der Gruppe 12 [30]. Sie werden durch Schmelzen seiner Erze, Galvanisieren, Batterien, Weichmacher, Legierungen, Pigmente, Nuklearindustrie und Zigarettenrauch hergestellt. Im Allgemeinen ist Cadmium in der Umwelt in geringen Mengen vorhanden; Industrieabfälle haben diese Werte jedoch stark erhöht. Cadmium-induzierte Toxizität kann Nieren, Atemwege und Skelett schädigen und ist für den Menschen krebserregend [30, 33]. Cadmium wird von der Agency for Toxic Substances and Disease Registry (ATSDR) als siebtgiftigstes Metall eingestuft [34].
Toxizität von Chrom (Cr)
Chrom (Cr) ist ein Element mit der Ordnungszahl 24 mit stahlgrauem Aussehen [35]. Chrom kommt in verschiedenen Zuständen vor, z. B. in zweiwertigen, vierwertigen, fünfwertigen und sechswertigen Zuständen; jedoch sind dreiwertige und sechswertige Formen am stabilsten. Chrom (III) ist ein essentielles Nahrungsergänzungsmittel für Mensch und Tier [35]. Die Chrom(VI)-Form ist jedoch hochgiftig und krebserregend [36, 37]. Chrom wird in Umweltmatrizen (Luft, Wasser und Boden) aus verschiedenen Quellen hergestellt, z. B. Abwasser und Luft, die hauptsächlich aus der metallurgischen und chemischen Industrie freigesetzt werden. Das sechswertige Chrom Cr (VI) ist ein Industrieschadstoff, der als krebserregend für den Menschen gilt [38, 39]. Die Konzentration von Cr (VI) im Grund- und Oberflächenwasser wird überschritten und die Weltgesundheitsorganisation (WHO) hat den Grenzwert von 50 µg pro Liter festgelegt [40].
Toxizität von Zink (Zn)
Zink (Zn) ist ein Element mit der Ordnungszahl 30 und in Gruppe 2 des Periodensystems platziert. Obwohl Zink für den Menschen ein essentielles Spurenmetall ist, kann eine übermäßige Aufnahme von Zink die Eisenaufnahme unterdrücken. Zinkionen sind hochgiftig für Pflanzen, Wirbeltiere, Wirbellose usw. [41,42,43].
Klassifizierung von Kohlenstoff-Nanomaterialien anhand ihrer Abmessungen
Die Nanomaterialien mit allen drei Dimensionen von weniger als 100 nm werden als nulldimensionales (0-D) Nanomaterial bezeichnet; Beispiele sind Fullerene und Quantenpunkte [44]. Die Nanomaterialien mit nur einer Dimension größer als 100 nm und zwei Dimensionen kleiner als 100 nm werden als eindimensionale (1-D) Nanomaterialien bezeichnet, z. B. Nanoröhren aus Kohlenstoff und Titan [45, 46]. Die Nanomaterialien, deren zwei Dimensionen größer als 100 nm sind, werden als zweidimensionale Nanomaterialien bezeichnet, ein berühmtes Beispiel ist Graphen. Dreidimensionale Materialien, deren alle Abmessungen größer als 100 nm sind, werden als dreidimensionale (3-D) Materialien bezeichnet; Beispiele sind Graphit und einige Komposite aus Nanomaterialien [46]. Abbildung 3 zeigt einige repräsentative Kohlenstoffmaterialien mit bekannter Struktur mit unterschiedlichen Abmessungen, z. B. Fulleren 0-D, einwandige Kohlenstoff-Nanoröhrchen 1-D, Graphen 2-D und Graphit 3-D.
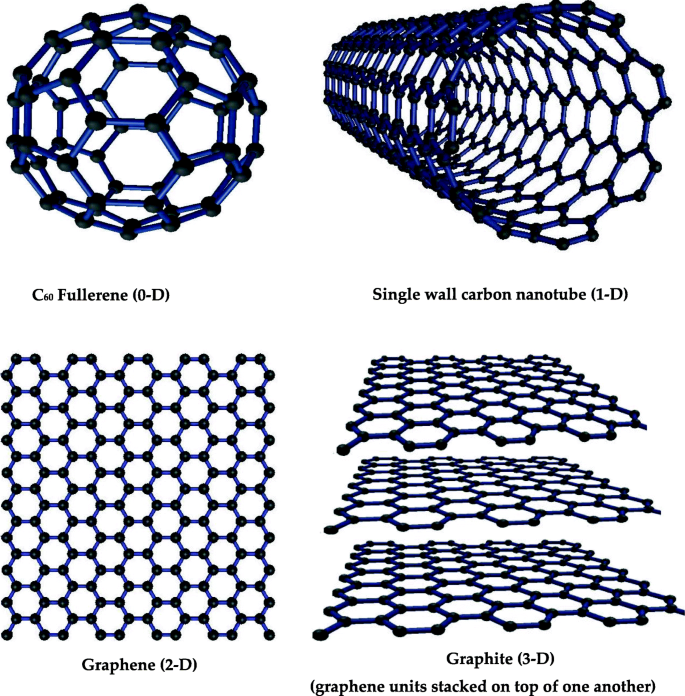
Die Beispiele für Kohlenstoff-Nanomaterialien in verschiedenen Dimensionen
Anwendung von Fullerenen in der Umweltsanierung und Wasseraufbereitung
Fullerene wurden 1985 aus interstellarem Staub entdeckt und haben eine geschlossene fünfeckige und sechseckige Ringstruktur, dargestellt durch die Formel C20 + m wo m ist eine ganze Zahl [49]. Sie haben einen hydrophoben Charakter, eine hohe Elektronenaffinität und ein hohes Verhältnis von Oberfläche zu Volumen und Oberflächendefekte. Diese einzigartigen physikalisch-chemischen Eigenschaften machen sie zu einem idealen Material für verschiedene Anwendungen wie Halbleiter, Elektronik, biomedizinische Wissenschaften, Solarzellen, Sensoren, Kosmetik, künstliche Photosynthese und Oberflächenbeschichtungen [50,51,52]. Brunet et al. zeigten, dass hydrophile funktionalisierte Fullerene (C60 ) wurden auch zum Abtöten der pathogenen Mikroorganismen in Wasser durch Anwendung eines photokatalytischen Verfahrens angewendet. Fullerene sind auch ideale saubere grüne Materialien für die Wasserstoffspeicherung, da Fullerenmoleküle aufgrund der niedrigeren Bindungsenergien von Kohlenstoff und Wasserstoff leicht in C-C-Bindungen in C-H umgewandelt werden können [27]. Die Fullerene haben aufgrund ihrer Chemie und Käfig-Molekülstruktur die maximale Wasserstoffspeicherung von 6,1%, und die Fullerenstruktur kann aufgrund der höheren CC-Bindungsenergien leicht umgekehrt werden [3, 53, 54]. Auf der Elektrodenoberfläche von Superkondensatoren werden leitfähige Kohlenstoffschichten aufgebracht, deren Kapazität von der Oberfläche, der Porengrößenverteilung und der elektrischen Leitfähigkeit abhängt [55, 56]. Kohlenstoffbasierte Nanomaterialien bieten aufgrund der größeren Oberfläche eine höhere elektrische Leitfähigkeit als konventionell verfügbare Materialien [57]. Von Fulleren-basierten Verbundmaterialien wurde berichtet, dass sie eine höhere spezifische Kapazität von 135,36 Fg − 1 . aufweisen als das reine Graphenmaterial, das nicht mit Fulleren hybridisiert wurde. Darüber hinaus zeigte Fulleren-basiertes Komposit eine bessere Retentionszeit von 92,35% selbst nach einem 1000 Lade-/Entladezyklus [58]. Fullerene wurden auch in Lithium-Ionen-Batterien als Anode verwendet und bieten einen besseren Wirkungsgrad durch den Ersatz nicht abbaubarer metallischer Anoden, wodurch sie sich als vorteilhaft in Bezug auf Effizienz und umweltfreundliches Material erweisen. Die physikalisch-chemischen Eigenschaften von Fullerenen machen sie auch zu geeigneten Kandidaten für die Extraktion verschiedener Spezies aus wässrigen Medien [59, 60]. Pickering et al. entwarfen wasserlösliche Fullerenverbindungen und setzten sie erfolgreich als Sensibilisatoren ein, um bei Bestrahlung mit sichtbarer und ultravioletter Strahlung reaktive Sauerstoffspezies (ROS) in Wasser zu erzeugen. Die ROS können die organischen Verunreinigungen im Wasser photoabbauen, außerdem wirken die wasserlöslichen Fullerene (Fullerole) auch als Antioxidantien. Am wichtigsten ist, dass Fullerole leicht aus dem Wasser entfernt werden können, nachdem sie die Funktion des Photoabbaus ausgeführt haben [53].
Es wird angenommen, dass Fullerene Spezies durch das Eindringen von Adsorbaten in die Räume/Defekte zwischen den Kohlenstoff-Nanoclustern adsorbieren, und zusätzlich zu den Defekten machen eine geringere Aggregationsneigung und eine große Oberfläche sie zu nützlichen Nanomaterialien, die für die Adsorption von Schwermetallionen aus Wasser [61, 62]. Alekseevaet al. führte vergleichende Studien von Fulleren- und Nanokomposit-Polystyrol-Filmen zur Entfernung von Cu 2+ . durch Ionen; sie fanden heraus, dass Fullerene eine bessere Effizienz zeigten [60]. Sie fanden auch, dass Fullerene dem Langmuir-Modell der Adsorption für Cu 2+ . folgen Ionen [60]. Sie stellten fest, dass das Cu 2+ Die Entfernungseffizienz von Fullerenen ist im ersten Fall höher und die Gleichgewichtsisotherme des Cu 2+ Die Adsorption am Fulleren entspricht dem Langmuir-Modell. Obwohl Fullerene ein großes Potenzial für Wasseradsorptionsanwendungen aufweisen, sind ihre Kosten zu hoch, was ihre Verwendung einschränkt. Die Spurenmengen von Fullerenen können jedoch verwendet werden, um andere Materialien wie Aktivkohle, Lignin und Zeolithe herzustellen, um deren Adsorptionseffizienz zu erhöhen [63]. Die Herstellung von Fulleren erhöht den hydrophoben Charakter, wodurch Materialien besser bei der Adsorption verwendet werden können und auch das Recycling erleichtert wird [64]. Es wurde berichtet, dass antibakterielles Material durch das Pfropfen von Fulleren C60 . gebildet wird mit Polyvinylpyrrolidon (PVP), das das Potenzial hat, in der Wasserdesinfektion eingesetzt zu werden. Der Membrantechnologie kommt bei der Reinigung von Salzen, organischen Stoffen, Partikeln und Gasen aus Wasser immer mehr Bedeutung zu. Die Membranleistung hängt von der Materialzusammensetzung ab, da sie für Reaktivität, Selektivität und mechanische Festigkeit verantwortlich ist. Fullerene haben aufgrund ihrer einfachen Funktionalisierung, ihrer hohen Elektronenaffinität, ihrer großen Festigkeit, ihrer Fähigkeit, die Größe anzupassen usw., ein großes Potenzial für die Anwendung in der Membrantechnologie. Fullerene können beim Aufpfropfen von Nanoadsorbentien zur Verbesserung ihrer Adsorptionseffizienz nützlich sein.
Biokompatibilität von Fullerenen
Fulleren-basierte Nanomaterialien wurden für biomedizinische Anwendungen genutzt und verschiedene Studien haben ihre Biokompatibilität mit lebenden Organismen gezeigt. Es wurde sowohl als Biorezeptor als auch als Biosensor verwendet und auch in der biomedizinischen Technik genutzt, und es wurde berichtet, dass es mit lebenden Systemen biokompatibel ist [65,66,67,68,69]. Fulleren ist ein ungiftiges Material, das für Filtration, Adsorptionsmittel und Membranmaterialien für Umwelt- und Wasseraufbereitungsanwendungen verwendet werden kann.
Kohlenstoff-Nanoröhren (CNTs)
Kohlenstoffnanoröhren wurden 1999 von Lijima entdeckt und können einwandig (SWCNTs) sein, z. B. geschichtetes aufgerolltes Graphen, oder mehrwandige Kohlenstoffnanoröhren (MWCNTs), z. B. mehrschichtiges aufgerolltes Graphen [70]. Die CNTs stehen aufgrund ihrer einzigartigen physikalisch-chemischen Eigenschaften seit ihrer Entdeckung im Fokus der Nanotechnologieforschung. Diese zylindrischen Nanostruktur-Allotrope aus Kohlenstoff werden in der Elektronik, Halbleiter, Feldemission, Energiespeicherung, Katalyse, Biomedizin, Luft- und Wasserfilter usw. eingesetzt. Ihr Durchmesser kann 1 nm bis mehrere Nanometer mit einer großen spezifischen Oberfläche (150– 1500 m 2 /g), und sie besitzen Mesoporen, die sie zum idealen Kandidaten für die Entfernung von Schwermetallionen durch Adsorption machen [71, 72]. Darüber hinaus können CNTs leicht mit verschiedenen organischen Molekülen funktionalisiert werden, wodurch sie spezifisch für die Auswahl von Adsorbaten werden und ihre Adsorptionsfähigkeit verbessert werden könnte [73]. Der Sorptionsmechanismus von Schwermetallen durch CNTs beruht auf der Oberflächenbeschaffenheit, dem elektrochemischen Potenzial und dem Ionenaustauschprozess [11, 73].
Umweltanwendung von CNTs/CNT-basierter grüner Technologie
Der weltweite Energiebedarf steigt immens und es werden viele Anstrengungen unternommen, um einen einfachen, kostengünstigen und umweltfreundlichen Werkstoff für zuverlässige Technologien für Energierohstoffe zu entwickeln. Solarenergie wird durch solarelektrische Umwandlung und solarthermische Umwandlung erzeugt [74]. Der geringe Wirkungsgrad der thermischen Umwandlung in Sonnenkollektoren ist jedoch die größte Hürde.
Nanofluide aus Kohlenstoff werden wegen ihrer guten Leistung als Solarabsorber in der solarthermischen Umwandlung weit verbreitet eingesetzt [75]. Auf Kohlenstoff-Nanoröhrchen basierende Photovoltaikzellen (PVCs) haben viel Aufmerksamkeit von Wissenschaftlern erregt, da sie p-Typ-Halbleiter mit ausgezeichneter Mobilität sein können und ihre Kombination mit Elektronendonatoren eine neue und einzigartige Idee ist [76, 77]. Die organischen photovoltaischen Bauelemente können leicht durch die Herstellung von CNTs mit Polymeren entworfen werden [78]. CNT-Si (p-n)-Heteroübergang-basierte Solarzellen wurden entwickelt, was zu hervorragenden leitfähigen und transparenten Filmen führt. Darüber hinaus wurde auch von CNTs mit n-Typ-Galliumarsenid (n-GaAs) mit einer besseren Effizienz von 3,8% für grünen Laser und Schreibtischlampe berichtet [79]. CNTs sind auch weit verbreitete Energiespeichergeräte, die auf den Prinzipien elektrochemischer Doppelschichtkondensatoren (EDLCs) wie Ultrakondensatoren arbeiten [80]. Der Einbau von CNTs in Elektroden von Ultrakondensatoren führte zu einer deutlichen Verbesserung der Lebensdauer mit mehr als 300.000 Zyklen [81]. Darüber hinaus wurden Superkondensator-CNTs auch in Dioden anstelle von herkömmlichen Transistoren verwendet, da sie aufgrund ihrer hervorragenden mechanischen und elektrischen Eigenschaften perfekte p-n-Übergänge herstellen können [58]. CNTs werden auch in der fortschrittlichen Sensortechnologie häufig eingesetzt, da sie die Empfindlichkeit, Selektivität, Reaktionszeit, Kosteneffizienz und Lebensdauer der chemischen und Biosensoren verbessern können [90]. Diese Ergebnisse deuten darauf hin, dass bessere CNTs ideale Materialien mit ausgezeichneter Mobilität und besserer Effizienz ohne negative Auswirkungen auf die Umwelt sind, was ein großer Nachteil bei den am häufigsten verwendeten metallbasierten p-Typ-Materialien ist.
Anwendung von CNTs in der Photokatalyse
Die Photokatalyse ist eine der fortschrittlichsten Technologien zur Abwasserbehandlung, die Halbleiter verwendet [82]. Es werden verschiedene Halbleitermaterialien verwendet, nämlich Fe3 O4 , ZnO und TiO2; die Quanteneffizienz dieser Materialien ist jedoch nicht hoch, und außerdem ist ihre ultraviolette Photoantwort auch langsam [83]. CNTs sind aufgrund ihrer verbesserten Quanteneffizienz, Nanogröße, hohen chemischen Stabilität, Hohlröhrenstruktur und des erweiterten Lichtadsorptionsbereichs aufgrund ihrer großen spezifischen Oberfläche vielversprechende fortschrittliche Materialien für die Katalyse [84]. Gaoet al. entworfene ultradünne Netzwerk-Photokatalysator-basierte SWCNTs-TiO2 und erfolgreich zur Reinigung von Wasser aus Öl eingesetzt [85]. Parket al. dekoriertes Titandioxid auf Aerogel von SWCNTs und wurde erfolgreich zur Entfernung von Methylenblau aus Wasser eingesetzt [86]. Zhao et al. hergestellte MWCNTs-TiO2 und zum Photoabbau von Methylenblau angewendet [87]. Xuet al. entwickelte Photokatalysatoren durch die Kombination von Hydroxy-MWCNTs und PbO2 nanokristalline Anode und setzte sie erfolgreich zur Entfernung von Pyridin aus Wasser ein [88].
SWCNTs in der Reinigung von schwermetallverseuchtem Wasser
SWCNTs sind eindimensionale (1-D) Kohlenstoff-Nanomaterialien, die aus einer hohlen Röhre mit einer Wanddicke von einem Atom bestehen. Dieses 1-D-Material weist aufgrund seiner einzigartigen Struktur außergewöhnliche physikalisch-chemische Eigenschaften auf. SWCNTs finden breite Anwendung in verschiedenen Bereichen wie Halbleiter, Elektronik, biomedizinische Wissenschaften, Chemie und Biosensoren [44, 89,90,91,92,93]. SWCNTs werden aufgrund ihrer porösen Struktur, ihrer großen Oberfläche, ihrer einfacheren Oberflächenfunktionalisierung und ihrer Nanogröße auch häufig für die Kontrolle der Umweltverschmutzung verwendet. Diese Eigenschaften von SWCNTs sind für ihre Anwendung in der Wasseraufbereitung sehr vielversprechend. Alijaniet al. entwarfen Nanokomposite auf SWCNT-Basis, indem sie mit Magnetit-Kobaltsulfid hergestellt wurden, und die resultierenden Nanokomposite wurden zur Entfernung von Quecksilber verwendet; Ergebnisse zeigten eine hohe Adsorption von mehr als 99,56% innerhalb eines kürzeren Zeitraums von 7 min [94]. Im Vergleich dazu wurde festgestellt, dass SWCNTs allein 45,39 % Quecksilber adsorbieren [94]. Anithaet al. führte eine molekulardynamische Simulation von nackten SWCNTs und ihren funktionalisierten Gegenstücken durch, z. B. SWCNTs-OH, SWCNTs-NH2 , und SWCNTs-COOH für die Adsorptionskapazitäten von Schwermetallionen, z. B. Cd 2+ , Cu 2+ , Pb 2+ , und Hg 2+ aus wässrigen Medien. Die Ergebnisse zeigten, dass die SWCNTs-COOH im Vergleich zu bloßen SWCNTs eine um 150–230% höhere Adsorptionskapazität aufweisen. Die SWCNTs-OH und SWCNTs-NH erwiesen sich als schwach in der Adsorption, da sie nur eine 10–47% höhere Adsorption im Vergleich zu SWCNTs zeigten [95]. SWCNTs-COOH wurde auch für die Adsorption von Pb 2+ . berichtet , Cu 2+ , und Cd 2+ Ionen mit einer Adsorptionskapazität von 96,02, 77,00 bzw. 55,89 µg/g. Im Vergleich dazu wurde festgestellt, dass nicht-funktionalisierte SWCNTs 33,55, 24,29 und 24,07 mg/g für Pb 2+ . adsorbieren Cu 2+ , und Cd 2+ Ionen bzw. [96]. Zazouliet al. entwarfen SWCNT-Nanokomposite durch Funktionalisierung mit L-Cystein. Sie wendeten die entwickelten Nanokomposite zur Entfernung von Quecksilber aus Wasser an. Die Adsorptionseffizienz des designten SWCNTs-Cysteins betrug 95 % [97]. Guptaet al. entwickelte SWCNTs-Polysulfon-Nanokomposit-basierte Membran und wurde zur Entfernung von Schwermetallen eingesetzt. Der Einbau von SWCNTs führte zu einer Verringerung der Porengröße der Membran und einer glatteren Oberfläche. Es wurde festgestellt, dass die entworfene Membran eine hohe Rückhaltefähigkeit für Metallionen aufwies und 96,8 % Cr + 6 . entfernte , 87,6 % As + 3 , und 94,2 % Pb + 2 Ionen. Die Membran ohne SWCNTs zeigte für Cr + 6 . nur 30,3 %, 28,5 % und 28,3 % Zurückweisung , As + 3 , und Pb + 2 Ionen bzw. Diese Ergebnisse zeigen die Verbesserung der Effizienz der Membran durch den Einbau von SWCNTs [98]. Dehghaniet al. angewandte SWCNTs zur Entfernung von Cr + 6 Ionen aus dem Wasser und bewertet die Wirkung verschiedener Parameter, z. B. Kontaktzeit, anfänglicher pH-Wert und anfänglicher Cr + 6 Ionenkonzentration auf die Adsorptionskapazität. Es wurde beobachtet, dass die Adsorptionseffizienz vom pH-Wert abhängt, die maximale Effizienz wurde bei pH 2,5 gefunden und die Adsorption folgt dem Langmuir-Isothermenmodell [99]. Diese Studien legten nahe, dass die einwandigen Kohlenstoff-Nanoröhrchen für die Behandlung von schwermetallverseuchtem Wasser geeignet sind.
MWCNTs bei der Reinigung von schwermetallverseuchtem Wasser
Kohlenstoffnanoröhren mit mehreren gewalzten Graphenschichten werden als mehrwandige Kohlenstoffnanoröhren (MWCNTs) bezeichnet, wie in Abb. 4 gezeigt. Die MWCNTs weisen einzigartige Eigenschaften wie große Oberfläche, hohe elektrische, thermische Leitfähigkeit und hohe Zugfestigkeit auf [100]. Aufgrund dieser physikalisch-chemischen Eigenschaften finden sie breite Anwendung in der Elektronik, Solarzellen, Sensoren und biomedizinischen Wissenschaften [101,102,103]. Die MWCNTs finden auch breite Anwendung in der Wasseraufbereitung, und insbesondere Schwermetallionen werden durch chemische Wechselwirkung mit funktionellen Gruppen von MWCNTs adsorbiert. Es wurde berichtet, dass die oxidierten MWCNTs eine hohe Adsorptionskapazität und Effizienz für das Cr 6+ . aufweisen , Pb 2+ , und Cd 2+ Ionen aus dem Wasser [104, 105]. Die Metallionenadsorption hängt auch vom pH-Wert ab, und diese Eigenschaft kann für die Desorption von Ionen durch Änderung des pH-Werts genutzt werden, und MWCNTs können wiederverwendet werden. Einige Studien haben gezeigt, dass plasmaoxidierte MWCNTs die besseren Adsorptionseigenschaften haben als chemisch oxidierte; dies kann auf eine höhere Zahl von sauerstoffhaltigen funktionellen Gruppen zurückgeführt werden, die auf der Oberfläche der Kohlenstoffnanoröhren vorhanden sind. Darüber hinaus wurde berichtet, dass plasmaoxidierte MWCNTs leicht recycelt und wiederverwendet werden können [72, 106].
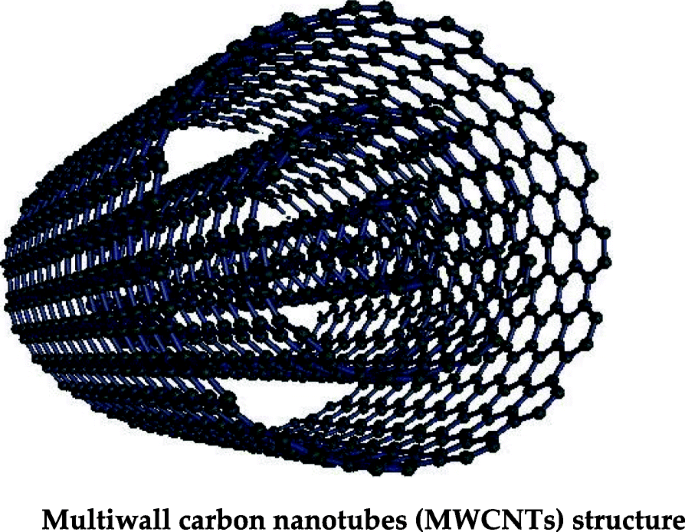
Mehrwandige Kohlenstoff-Nanoröhrchen-Struktur (MWCNT)
Das Verbundmaterial von MWCNTs wurde auch für die Adsorption von Schwermetallionen aus Wasser verwendet. Die MWCNTs-Fe2 O3 , MWCNTs-ZrO2 , MWCNTs-Fe3 O4 , MWCNTs-Al2 O3 , und MWCNTs-MnO2 -Fe2 O3 Nanokomposite wurden erfolgreich zur Entfernung der Schwerionen von Cr 6+ . eingesetzt , As 3+ , Ni 2+ , Pb 2+ , und Cu 2+ Ionen aus Wasser [107,108,109,110]. Die experimentellen Bedingungen von Lösungen, einschließlich pH- und Metallionenkonzentrationen, können die Adsorptionseigenschaften von MWCNTs beeinflussen, und das Freundlich-Adsorptionsmodell ist mit seinen experimentellen Daten zufrieden [81, 111]. Die Adsorptionseffizienz funktionalisierter MWCNTs stieg im Vergleich zu anderen Materialien organischer Oxide, und es wird auch vorhergesagt, dass funktionalisierte MWCNTs bei der Metallionenadsorption 20-mal effektiver sind als nichtoxidierte MWCNTs [112]. Es wird allgemein angenommen, dass Verbindungen zwischen Ionen und dem Auftreten polarer Kohlenstoffnanoröhren der Hauptmechanismus der Sorption sind [113, 114]. Oxidierte MWCNTs haben auch eine außergewöhnlich hohe Sorptionskapazität und Effizienz für Pb 2+ . gezeigt , Cd 2+ , und Cr 6+ aus dem Wasser. The sorption efficacy of MWCNTs with acid treatment increases the potential to remove lead, chromium, and cadmium ions with oxygen functional group making the complexes of ions or precipitates of salts on the surfaces [115]. Adsorption of MWCNTs treated with concentrated HNO3 increases significantly mainly due to oxygen functional groups created on the surface of acidified nanotubes that can react with metal ions to form complex or salt precipitates on the surface. The MWCNT composites with certain compounds like iron (III) oxide, zinc oxide, and aluminum oxide are formed by a coprecipitation method, and resulting composites are successfully applied for the removal of chromium, nickel, lead, copper, and arsenic ions. The adsorption efficiency of these nanocomposites was found to be dependent on the pH value and temperature, and the sorption process can be accomplished by changing these parameters [116, 117]. Depending on the pH and temperature, the sorption capacity of these composites varied from 10 to 31 mg/g. The adsorption process for these nanocomposites was well described by the Langmuir model [118]. The nanocomposites of oxidized multiwalled MWCNTs with manganese oxide/iron (III) oxide are reported to remove Cr 6+ ions with maximum adsorption capacity of 186.9 mg/g with the maximum removal capacity of 85% at the optimum pH 2.1 studies. Their promising adsorption was due to the surface polarity of the adsorbents. It has also been reported that plasma-oxidized MWCNTs are better in adsorption compared to chemically oxidized ones as the prior ones have more oxygenated functional groups [119]. Plasma-oxidized technique has also been reported for the formation of nanotubes with titanium oxide and manganese dioxide and utilized for the removal of lead ions from water. The results showed that these hybrid systems can act as an effective adsorbent for the lead ions in the first case; the adsorption capacity was 137 mg/g, and in the second case, it was 78.74 mg/g [120]. In a heterogeneity adsorbent surface, sites combined twice are fitted in the isotherms models of the Langmuir-Freundlich equation that was used to differentiate between two types of adsorption sites with greater and lesser energy affinities for the Ni 2+ ions [121]. It is believed that nickel ion sorption mainly occurs at the sites of energy with modified nanocomposites of MWCNTs and the nano-modification leads to a 20% increase in the adsorption capacity at small (up to 0.1 mol/l) equilibrium adsorbate concentrations. Another modification reported for MWCNTs is their functionalization with hydroxyquinoline and their application for the removal of copper, lead, cadmium, and other toxic ions [122]. The carbon nanotubes alone as well as in their oxidized and in their composite forms have tremendous ability to adsorb the heavy metal ions, and a lot of research is in progress for their applications in purification of water. Elsehly et al. applied commercial MWCNTs for the removal of the manganese and iron which could reach 71.5% and 52% respectively with a concentration in aqueous solution of 50 ppm of these metal ions [123]. In another study, CNT-based nanocomposites have been applied for the removal iron and manganese from the water [124].
Biocompatibility of CNTs
Carbon nanotubes have great potential to be applied for multidisciplinary fields like drug delivery, diagnosis, biosensors, electronics, semiconductors, and environmental remediations [125]. Different studies revealed the biocompatibility of CNTs as it has been widely exploited for biomedical applications [126, 127]. Carbon-based materials like CNTs are safe to be applied for the environmental remediation and in particularly for water treatment.
Graphene Based Material for Environmental Remediation
Graphene-based material for the adsorption of gaseous contaminants
Carbon dioxide (CO2 ) has been the environmental concern because of its immense effect in global warming [128]. Nanomaterials have been found to be promising materials as compared to conventional materials both with respect to cost and efficiency [129]. Graphene-based materials have been utilized for the adsorption of gaseous contaminants [130]. Gosh et al. showed the successful application of graphene-based nanomaterials for the capture of CO2 und H2 . A single layer of graphene has been reported to capture 37.93% of CO2 [130]. Graphene has been reported to selectively adsorb CO2 as compared to methane (CH4 ) and nitrogen (N2 ) gases. Selectivity of graphene oxide (GO) for CO2 can be attributed to higher dipole moment of carbon dioxide which can easily interact with polar oxygenated functional groups of CO2 [74, 131]. Other studies have also been reported for tuning the graphene chemistry for the improved selectivity of the desired gaseous contaminant [75, 131].
Graphene Oxide in Removal of Organic Dyes from Water
Graphene-based nano-adsorbents are excellent advanced materials for the removal of the organic contaminants from the water because of their nano-scaled size, high surface area, ability to interact via pi-pi stacking, hydrogen bonding, and electrostatic interactions [26]. In comparative adsorption studies of GO and graphite using methylene blue and malachite green as standard organic dyes, it was found that GO showed much better adsorption than graphite [26]. GO has also been utilized for the removal of cationic dyes namely methylene blue (MB), crystal violet (CV), and rhodamine B (RhB) from water. It was found that the higher the initial dye concentration, the higher will be the adsorption with adsorption capacities of 199.2, 195.4, and 154.8 mg g −1 for MB, CV, and RhB, respectively [76]. GO has also successfully applied for the removal of anionic dyes like Acid Orange 8 (AO8) and Direct Red 23 (DR23) from aqueous solutions [77].
Graphene-Based Photocatalytic Materials for Water Decontamination
Although adsorption can remove the contaminant from water, the adsorption technique is unable to destroy/degrade the contaminants and disposal step is required [77]. Photocatalysis is a useful approach for water remediation/wastewater treatment for the complete degradation and mineralization of organic/biological contaminants [78]. Graphene-based photocatalysts have been reported for their improved activity because of their high surface area, nanosize, and more electronic movements as compared to the traditionally used materials [78, 132]. Rommozzi et al. designed reduced graphene oxide (rGO) with a greener reduction method using glucose and ammonium hydroxide and successfully designed a photocatalyst which is visible by the fabrication with TiO2 . The designed rGO-TiO2 photocatalyst was successfully applied for the refractory dye named Alizarin Red S (ARS) [133]. In other studies, graphene oxide fabricated with TiO2 and ZnO exhibited much photodegradation of methylene blue as compared to TiO2 /ZnO alone [79, 80].
Graphene and Graphene Oxide-Based Adsorbents for the Purification of Heavy Metal-Contaminated Water
Graphene is one-atom-thick-layered hexagonal lattice of carbon atoms and is known as the thinnest material with the strength of 200 times than steel. Graphene was discovered in 2004 by Sir Andre Geim and Sir Konstantin Novoselov, who were awarded a Nobel prize for their discovery in 2010. Graphene (2-D) is being used widely in almost every field such as in touch screens, mobiles, LCDs, semiconductors, computer chips, batteries, energy generation, water filters, supercapacitors, solar cells, and biomedical and environmental sciences [134,135,136,137]. These 2-D graphene-based materials are getting more and more attention in water treatment due to their unique physicochemical characteristics namely electronic properties, high surface area, thermal mobility, high mechanical strength, and tunable surface chemistry [118, 134, 138, 139]. Tabish et al. designed porous graphene and applied it as an adsorbent for the removal of heavy metal ions as well as other pollutants from water. They applied this porous graphene material for As 3+ removal from water and found 80% efficiency. The material was found to retain its water treatment properties after regeneration and recycling [138]. Guo et al. designed a nanocomposite of partially reduced graphene oxide by its fabrication with Fe3 O4 via in situ co-precipitation method and applied it for the removal of Pb 2+ ions from water. The designed nanocomposite was found to be excellent in removing the Pb 2+ ions from aqueous solution with an adsorption capacity of 373.14 mg/g [140]. Zhang et al. functionalized the reduced graphene oxide with 4-sulfophenylazo (rGOs) and applied it for the removal of a variety of heavy metal ions from aqueous solution. The designed material showed the maximum adsorption capacity of 689, 59, 66, 267, and 191 mg/g for the Pb 2+ , Cu 2+ , Ni 2+ , Cd 2+ , and Cr 3+ respectively [141]. Diana et al. designed a graphene-based self-propelled microbot system whose structure was made up of nanosized multilayered consisting of graphene oxide, nickel, and platinum. Each layer performed a different function, e.g., graphene oxide captures the heavy metal Pb 2+ ions, the middle layer of Ni enables the control of microbots with the help of external magnetic field, and the inner layer of platinum helps the engine in self-propelling [142]. The designed system was found to remove the 80% of the Pb 2+ water solution. Figure 5 shows the schematic illustration of the working principle of microbots. Yang et al. designed hydrogen beads using graphene oxide and sodium alginate (GO-SA) and successfully applied them for the removal of Mn 2+ ions from the aqueous solution with excellent adsorption capacity of 56.49 mg/g [9]. Zheng et al. designed nanocomposites by fabrication of zinc oxide with tea polyphenol with reduced graphene oxide (TPG-ZnO). Designed material was applied for the removal of heavy metal ions with an added advantage of antibacterial properties [143]. They applied this material for the removal of Pb 2+ ions from aqueous solution with adsorption efficiency of 98.9%, and the adsorbent was found to possess antibacterial properties against Streptococcus mutans with 99% eradication [143]. Mousavi et al. designed nanocomposites of graphene oxide with iron oxide magnetite nanoparticles Fe3 O4 and applied them for the removal of Pb 2+ ions from water and the material showed 98% removal efficiency with a capacity of 126.6 mg/g [144]. Considering functionalized graphene as an adsorbent to remove Pb 2+ ions from an aqueous medium, the highest record of Pb 2+ ion removal over graphene is 406.6 mg/g at pH of 5.0 in 40 min [145]. Graphene-hydrogel lingo sulfonate functionalized nanocomposites having oxygenated functional groups making the surface highly polar reported to increase the rate of adsorption of Pb 2+ ions with maximum efficacy of 1308 mg/g with the equilibrium reached in 40 min. Awad et al. modified graphene oxide with chloroacetic acid (GO-COOH) and ethylenediamine (GO-amino). The designed systems were applied for the removal of mercury (Hg 2+ ) from water and found that the nanocomposites (GO-COOH) and (GO-amino) have an adsorption capacity of 122 mg/g and 230 mg/g. In addition to this, designed systems retained their adsorption efficiency after the recycling process [146]. Yan et al. designed magnet graphene oxide for the rapid removal and separation of Fe (II) and Mn (II) from micropolluted water [147]. Ali et al. designed graphene-based adsorbent successfully for the removal of noxious pollutants namely Cu (II), Pb (II), Fe (II), and Mn (II) [148].
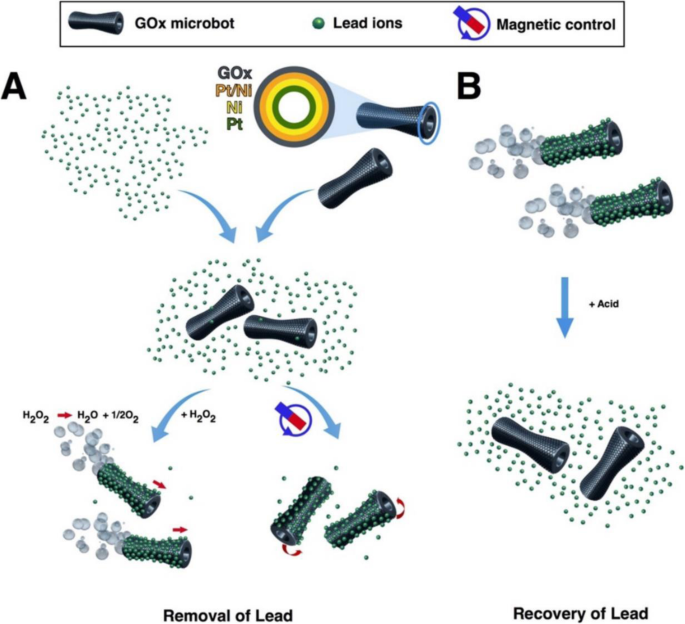
Scheme of GOx-microbot-based approach for lead decontamination and recovery. a Decontamination of polluted water using GOx-microbots fabricated by electrodeposition of nanolayers of graphene oxide (GOx), Pt/Ni layer, Ni magnetic layer, and Pt catalytic inner layer. The decontamination strategy for lead ions can be carried out by two different techniques:self-propulsion of the GOx-microbots in the presence of H2 O2 or by using an external rotating magnetic field. b Recovery of lead ions from the GOx-microbots in the presence of acidic media [117]
Biocompatibility of Graphene-Based Nanomaterial
Graphene-based nanomaterials have been applied in different fields like electronics, chemical sensors, biosensors, drug delivery, theragnostic, and other related biomedical fields. These studies also report the cytocompatibility of graphene-based materials both by in vitro as well as in vivo animal studies [122, 133, 149,150,151,152]. These findings suggest that the graphene-based materials are safe for the environmental remediation application as they are just used for the removal and degradation of pollutants and are not consumed by humans directly.
Activated Carbon in Environmental Remediation
Activated carbon is a fabulous material because of its high surface area, highly porous structure, and ease of preparation with variety of starting materials. Because of its ideal physicochemical properties, it has wide application in environmental remediations in different industries like pharmaceutics, fertilizer plants, petroleum, cosmetics, automobiles, and textiles [153] It is also widely applied for the adsorption of gases, solvent recovery, and wastewater treatment especially for the removal of organic dyes/other pollutants; not only this, but it is also used as a catalyst in biodiesel production. It is also applied as a low-cost material for the treatment and removal of water containing COD, BOD, and TSS and stabilizing and maintaining the optimum pH for biological uses [154,155,156]. Maguana et al. prepared activated carbon from the pear seed cake and successfully applied it for the removal of methylene having an adsorption capacity of 260 mg/g [157]. Antonio et al. prepared activated carbon from the kenaf plant and applied it successfully for the treatment of the wastewater of hospitals containing paracetamol as the main pollutant [158]. The above literature suggests that the activated carbon is the pretty useful economical material which can easily be prepared and it has immense application in environmental remediations.
Activated Carbon as Adsorbents in the Purification of Heavy Metal-Contaminated Water
Activated carbon (AC) is also known as activated charcoal, and this of type carbon material is formed under some treatment protocols resulting in micro/nanopores and having the large surface area of more than 3000 m 2 [159]. The AC is produced on a large scale from coal, wood, and agricultural wastes [160]. In addition to its porous nature (as shown in Fig. 6), AC also has a high mechanical strength which enables its applications in catalyst support, capacitors, electrodes, and gas storage and most importantly used as the adsorbent for removal of metal ions, organic wastes, and gases from water [160,161,162]. The high mechanical strength of activated carbon enables its periodic cleaning, regeneration, and reutilization [160]. Abeer et al. reported the preparation of AC from apricot stone and its application in removal of Zn + 2 and Al + 3 ions with removal efficiency of 92% [163]. Ebrahim et al. designed AC from sewage sludge, applied it for the removal of Cu + 2 ions from water, and found that the designed material showed maximum adsorption capacity of above 50% [164].
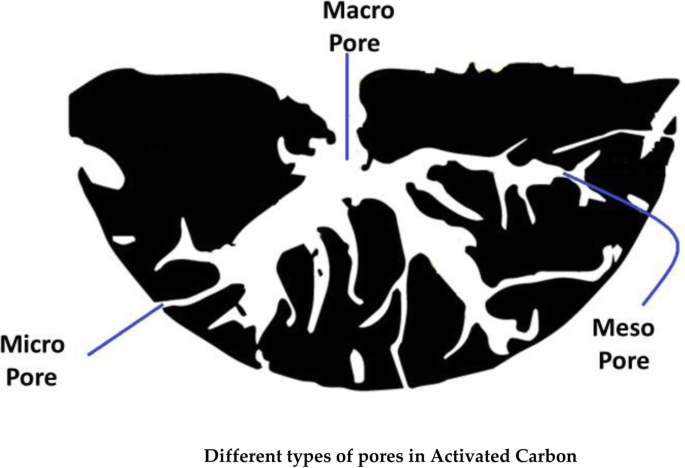
Different types of pores in activated carbon
Liet al. prepared the AC from sewage sludge produced from the wastewater treatment plant and functionalized it with sulfur [165]. They applied sulfonated AC for the removal of Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ ions from water. The adsorption capacity of metal ions were found to be 238.1 mg/g, 96.2 mg/g, 87.7 mg/g, and 52.4 mg/g for Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ respectively [165]. Cao et al. designed multipore activated carbon (MPAC) with a large surface area using the agricultural waste of long-root Eichhornia crassipes and applied it for removing heavy metal ions, e.g., Pb 2+ , Cd 2+ , Cu 2+ , Ni 2+ , and Zn 2+ . They found that at 30 °C adsorption capacity being 1.34 mmol/g, 1.07 mmol/g, 1.22 mmol/g, 0.97 mmol/g, and 0.93 mmol/g for Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ respectively [166]. Dong et al. investigated the application of spent activated carbon (AC) for heavy metal ion removal from water and found high adsorption capacity of 95% and 86% for Pb 2+ and Cd 2+ ions respectively [167]. M. Bali et al. [168] applied commercial AC for the removal of heavy metal ions and found that adsorption equilibrium of Cd 2+ ion took 15 min while for Pb 2+ , Zn 2+ , and Cu 2+ it took 45 min with percentage removal of 64% for all these ions and with Cd 2+ being the highest [10]. Kongsuwan et al. prepared the activated carbon from the agricultural waste of eucalyptus bark. They applied it for the removal of Cu 2+ and Pb 2+ from water with maximum removal capacity of 0.45 and 0.53 mmol per gram of AC respectively, with adsorption being the main mechanism of ion uptake [169]. AC poultry litter has also been reported and applied for the treatment of heavy metal-contaminated water and found that for 1 kg of poultry litter AC adsorbs 404 mmol, 945 mmol, 236 mmol, and 250–300 mmol of Cu 2+ , Pb 2+, Zn 2+ , and Cd 2+ ions respectively [170]. This adsorption is significantly higher than the commercially available AC derived from coconut and bituminous. The AC of wood saw dust of rubber plant has also been reported for the removal of heavy metal ions of Cr + 6 from water with adsorption capacity of 44 mg/g [171]. AC formed from Moso and Ma bamboo was found to be highly efficient in removing the heavy metal ions, i.e., Pb 2+, Cu 2+ , Cr 3+ , and Cd 2+ with the maximum adsorption capacity of more than 90% removal [172]. Naser et al. prepared AC from rice husk and applied them for the removal of Cu 2+ from aqueous solution, and maximum capacity was found to be 33.92%. Similar results have also been reported for the removal of Cu 2+ from the AC formed from Palm shell [173]. AC of love stones has been reported for the adsorption of Cd + 2 and Ni + 2 with adsorption capacity of 1.85 mg/g and 0.67 mg/g respectively in two different studies [174, 175]. AC prepared from olive stone using the microwave method has been applied for the removal of Fe 2+, Pb 2+, Cu 2+, Zn 2+, Ni 2+ , and Cd 2+. from wastewater. Another study reported on the olive stone AC prepared via microwave to remove a group of metal ions from synthetic wastewater:Fe 2+ , Pb 2+ , Cu 2+, Zn 2+ , Ni 2+ , and Cd 2+ with removal efficiency of more than 98% [176]. Tamarind wood AC has been reported for the highest adsorption capacity of above 97% for Pb 2+ from water [177]. Activated carbon has been applied as an adsorbent for the removal of Fe (II) and Mn (II) with great efficiency [178, 179]. The activated carbon is easy to synthesize, is cheaper, and is the most promising material for the adsorption of heavy metal ions and can be prepared at a large scale from a variety of carbon sources especially form agricultural waste. In addition to easier preparation, AC can easily be functionalized. Table 2 summarizes the effect of different parameters on the process of metal ion adsorption.
Biocompatibility of the Activated Carbon
Different studies have been conducted for the biocompatibility evaluation of the activated carbon materials prepared form different carbon sources. Activated carbon has been applied for the treatment of cystitis and was found to be effective and nontoxic compared to the antibiotics being applied [180]. Biocompatibility of activated carbon can be attributed to its inertness, and it has also been functionalized and fabricated with other materials to confer on the disinfection properties [181]. The activated carbon is also given orally to human beings as a sorbent for the removal of toxins from the human body and has also been utilized in biomedical applications [182, 183]. These studies strongly suggest the biocompatibility of the activated carbon.
Conclusion
In this review, environmental and special purification of heavy metal from heavy metal contaminants by the applications of carbon nanomaterials, namely fullerene carbon nanotubes, graphene, graphene oxide, and activated carbon discussed. These carbon nanomaterials have been utilized in the purification of heavy metal-contaminated water with great success. The reason behind the successful application is due to their fascinating properties like high surface area, ease of recycling, and easiness to desorb the adsorbed metal ions; only using mineral acid solution and regenerated material can be reused with retention of adsorption capability. In addition to these properties, the carbon nanomaterials can easily be fabricated with other nanomaterials and are easy to be functionalized resulting in multifunctional nano-adsorbent. Carbon-based materials are highly biocompatible with living organisms and environment. There is also an immense effect of different parameters such as pH, contact time, and type of adsorbents on the process of metal ion adsorption. Based on this literature review, it can be concluded that carbon nanomaterials have fascinating physicochemical properties and have great potential to be exploited in the environmental remediation and water purification.
Verfügbarkeit von Daten und Materialien
All data are fully available without restriction.
Abkürzungen
- AC:
-
Activated carbon
- GO:
-
Graphene oxide
- MWCNTs:
-
Multiwall carbon nanotubes
- r-GO:
-
Reduced graphene oxide
- SWCNTs:
-
Single-wall carbon nanotubes
Nanomaterialien
- Die perfekte Formel für die Abstimmung von Betrieb und Wartung
- Die Vor- und Nachteile von Kohlefaserringen
- Der Unterschied zwischen Kohlefaser und Glasfaser
- Materialien:Glas- und kohlenstofffaserverstärktes PP für die Automobilindustrie
- Die fünf wichtigsten Probleme und Herausforderungen für 5G
- Fortschritte und Herausforderungen fluoreszierender Nanomaterialien für die Synthese und biomedizinische Anwendungen
- Das Konzept des IoT in der Abwasserbehandlung und -bewirtschaftung verstehen
- Mondtaschenlampe zur Suche nach Wasser auf dem Mond
- Das richtige Rig für die richtigen Konfigurationen
- Die Bedeutung einer effektiven Wärmebehandlung für Stempel, Matrizen, Klingen und Werkzeugstähle



