Wiederherstellung von microRNA-499-5p schützt Mäuse mit Sepsis-induzierter Lungenverletzung durch gezieltes Targeting auf Sox6
Zusammenfassung
Hintergrund
Es ist bekannt, dass MicroRNAs (miRs) an Sepsis beteiligt sind; Daher wollen wir die schützende Wirkung von miR-499-5p auf die geschlechtsbestimmende Region Y-bezogene Hochmobilitäts-Gruppenbox 6 (Sox6) auf Sepsis-induzierte Lungenschädigung bei Mäusen diskutieren.
Methoden
Das Sepsis-induzierte Lungenverletzungsmodell wurde durch Ligatur des Blinddarms und Punktion etabliert. Das Nass-/Trockengewichtsverhältnis (W/D), miR-499-5p, Sox6, Caspase-3 und Caspase-9-Expression in Lungengewebe von Mäusen wurden getestet. Lungenverletzungs-Score, Kollagenfasern und der Grad der Lungenfibrose im Lungengewebe wurden bestimmt. Weiterhin wurde die Zellapoptose in Lungengeweben gemessen. Die Gehalte an Entzündungsfaktoren und oxidativen Stress-Indizes in bronchoalveolärer Lavageflüssigkeit (BALF) und Lungengewebe wurden über Loss- und Gain-of-Function-Assays nachgewiesen. Die Targeting-Beziehung zwischen miR-499-5p und Sox6 wurde bestätigt.
Ergebnisse
Das W/D-Verhältnis und Sox6 waren erhöht, während miR-499-5p im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung verringert war. Wiederhergestelltes miR-499-5p oder abgereichertes Sox6 milderte die Pathologie des Lungengewebes, reduzierte den Lungenverletzungs-Score, Kollagenfasern, den Grad der Lungenfibrose, TUNEL-positive Zellen, Caspase-3- und Caspase-9-Proteinexpression und den Gehalt an Entzündungsfaktoren in BALF und Lungengewebe sowie oxidative Stressreaktion im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung. miR-499-5p zielte auf Sox6 ab.
Schlussfolgerung
Eine hohe Expression von miR-499-5p kann die Zellapoptose im Lungengewebe abschwächen und die Entzündung von Mäusen mit Sepsis-induzierter Lungenverletzung durch Abbau von Sox6 hemmen, und es ist ein potenzieller Kandidat für Marker und therapeutisches Ziel für Sepsis-induzierte Lungenverletzungen.
Einführung
Sepsis ist eine systemische Entzündung, die als Folge einer Infektion entsteht und multiple Organdysfunktionen verursacht und das akute Atemnotsyndrom enthält [1]. Sie ist gekennzeichnet durch starke Hypotonie, progressive Hypoxämie, Gewebeschäden und entzündliche Veränderungen [2]. Die Lunge ist das kritischste und verletzlichste Organ bei einer Sepsis, und die akute Lungenschädigung (ALI) ist eine häufige Sepsis-induzierte entzündliche Erkrankung [3]. Die Schwere der Sepsis-induzierten ALI kann auf eine beeinträchtigte Permeabilität des alveokapillären Netzwerks zurückgeführt werden, was zu einer verminderten Sauerstoffversorgung führt [4]. Die Apoptose von Lungenzellen ist ein kritischer Faktor bei einer durch Sepsis induzierten Lungenschädigung [5]. Die Pathophysiologie der Sepsis-induzierten ALI ist unbekannt, unterstützende Maßnahmen und Antibiotika sind die einzigen verfügbaren Behandlungen bei Sepsis- und ALI-Patienten, und ihr Einfluss auf die hohen Mortalitätsraten durch Sepsis ist begrenzt [6].
MicroRNAs (miRNAs) sind kleine nicht-kodierende Segmente von endogen exprimierten RNAs, bestehend aus ungefähr 18–24 Nukleotiden, die eine Vielzahl von Zellfunktionen kontrollieren und an Zielregionen eines bestimmten Gens binden können, um ihre Expression durch Hemmung oder Aktivierung von mRNA zu kontrollieren Übersetzung/Transkription [7]. MiR-499-5p ist ein kürzlich entdecktes Mitglied von Myosin-kodierten miRNAs [8]. Eine Studie hat berichtet, dass die Serumspiegel von miR-499-5p zur Anzeige eines Organversagens bei Patienten mit Sepsis verwendet werden könnten [9]. Eine andere Studie hat gezeigt, dass die Expression von miR-499-5p an der Sepsis-induzierten kardialen Apoptose beteiligt ist [10]. Die geschlechtsbestimmende Region Y (SRY)-related high-mobility box (HMG) (SOX)-Familie wird durch einen Satz von Genen definiert, einschließlich einer DNA-Bindungsdomäne der HMG-Klasse, deren Sequenzidentität mit SRY mehr als 50 % beträgt [11] . Der Sox6-Transkriptionsfaktor ist ein Teil der SRY-verwandten HMG-Box-Familie und wird während der Progression in mehreren Geweben exprimiert, wo er eine entscheidende Rolle beim Übergang von proliferierenden Vorläuferzellen zu funktionell reifen Zellen spielt [12]. Es gibt eine Studie, die berichtet, dass erhöhtes Sox6 an einer Sepsis-induzierten kardialen Apoptose beteiligt ist [10]. Studien haben gezeigt, dass die Sox2-Expression und Sox4-Expression bei kleinzelligem Lungenkrebs beim Menschen erhöht sind [13, 14]. Aber die Beziehung zwischen Sox6 und Sepsis-induzierter Lungenverletzung muss weiter untersucht werden. Daher sollte unsere Studie die schützende Wirkung von miR-499-5p auf Mäuse mit Sepsis-induzierter Lungenverletzung untersuchen, indem es auf Sox6 abzielte.
Materialien und Methoden
Einhaltung ethischer Standards
Alle Tierversuche standen im Einklang mit dem Leitfaden für die Pflege und Verwendung von Versuchstieren der National Institutes of Health. Das Protokoll wurde vom Ausschuss für Ethik von Tierversuchen des Weihai Municipal Hospital, Cheeloo College of Medicine, Shandong University, genehmigt.
Versuchstiere
Gesunde männliche, pathogenfreie BABL/c-Mäuse (Alter 6–8 Wochen, Gewicht 18–22 g) wurden vom Versuchstierzentrum der Shandong University (Shandong, China) bezogen. Die Umgebung wurde auf 24 ± 2 °C mit 12 Hell-Dunkel-Zyklen im Wechsel eingestellt. Mäuse wurden mit freiem Zugang zu aseptischer Nahrung und sterilem Wasser behandelt. Die Experimente wurden nach einer adaptiven Fütterung für 7 Tage begonnen.
Etablierung eines Sepsis-induzierten Lungenverletzungsmodells durch Blinddarmligatur und -punktion (CLP) bei Mäusen
Die Mäuse wurden zufällig in 2 Gruppen verteilt:die Scheingruppe (n = 8) und die Modellgruppe. Mäuse wurden vor der Operation 12 Stunden lang nüchtern gehalten und dann mit 1% Pentobarbital-Natrium (70 mg/kg) durch intraperitoneale Injektion anästhesiert. Die Wirkung der Anästhesie wurde beobachtet; die Atmung und der Herzschlag von Mäusen wurden bemerkt. Kopf und Gliedmaßen von Mäusen wurden in Rückenlage fixiert und die Bauchhaut wurde präpariert und mit Jodophorwattebällchen desinfiziert. Mäuse in der Modellgruppe wurden mit einem Längsschnitt (1,0 cm) im mittleren Segment der abdominalen Medianlinie behandelt, die Bauchhöhle wurde geöffnet und der Blinddarm wurde aus der Bauchhöhle herausgezogen, um eine Verletzung von Mesenterialgefäßen zu vermeiden. Es wurde mit einem 1–0 Seidenfaden an der Hälfte des Endes des Blinddarms abgebunden und der Blinddarm wurde am kontralateralen Rand des Mesenteriums mit einer Punktionsnadel Nr. 16 punktiert. Eine angemessene Menge Darminhalt wurde extrudiert, der Blinddarm wurde zurückgelegt und der Einschnitt wurde vernäht. Nach dem Öffnen der Bauchhöhle wurde Mäusen in der Scheingruppe nur der Blinddarm herausgezogen und dann wurde der Blinddarm zurückgelegt. Mäusen wurde nach der Operation 1 ml 0,9% Natriumchloridlösung subkutan injiziert, in Käfige getrennt und routinemäßig gefüttert.
In-vivo-Transfektion
Vor der Modellierung wurden Mäuse in 7 Gruppen eingeteilt (n = 8):die Modellgruppe, die miR-499-5p-Agomir-Gruppe, die Agomir-negative Kontrollgruppe (NC), die kleine interferierende RNA (si)-Sox6-Gruppe, die si-NC-Gruppe, die miR-499-5p-Agomir + Überexpression (oe)-Sox6-Gruppe und die miR-499-5p-Agomir + oe-NC-Gruppe. Eine Stunde vor dem Modellieren wurden die Mäuse gemäß der Gruppierung behandelt. Mäuse wurden mit 1% Pentobarbital-Natrium durch intraperitoneale Injektion anästhesiert, dann in einer 45° geneigten Rückenlage fixiert und die Zunge der Mäuse wurde auf die andere Seite des Mundes bewegt, um ihre Durchgängigkeit der Atemwege sicherzustellen. Die vordere Halshaut von Mäusen wurde desinfiziert und abgeschnitten, um die Luftröhre freizulegen. Transfektionskomplex (50 µL) wurde von einem Mikrosampler aufgenommen (getropft gemäß der Gruppe, die gleiche Menge Phosphat-gepufferte Kochsalzlösung (PBS) wurde in die Modellgruppe getropft) und dann langsam in die Trachea getropft. Nach der Transfektion wurden die Mäuse vertikal gedreht und der Transfektionskomplex vollständig in der Lunge verteilt [15]. Während des Transfektionsprozesses wurden die Atmung und der Herzschlag der Mäuse beobachtet. Beim Auftreten von Atem- und Herzstillstand wurde die Transfektion sofort abgebrochen und die Atemwege frei. Die Transfektion wurde fortgesetzt, als Atem und Herzschlag der Mäuse stabil waren. MiR-499-5p-Agomir und sein NC sowie die entsprechenden Plasmide von Sox6 wurden von Shanghai GenePharma Co., Ltd. (Shanghai, China) gekauft. Nach der Transfektion wurden die Mäuse in Käfige getrennt und 1 Tag lang gefüttert und dann eingeschläfert. Mäuse wurden mit 1% Pentobarbital-Natrium durch intraperitoneale Injektion anästhesiert, in Rückenlage fixiert und dann durch Venensektion der abdominalen Aorta eingeschläfert. Die Haut der Mäuse wurde lokal desinfiziert, die Brusthöhle geöffnet, die Luftröhre und der rechte Hauptbronchial abgebunden, der rechte Hauptbronchus abgetrennt und die rechte Lunge entfernt. Der Unterlappen der rechten Lunge wurde zur pathologischen Untersuchung in 10% neutrales Formalin gelegt, der Mittellappen wurde schnell gewogen, um das Nassgewicht (W) zu berechnen und bei 56 °C gebacken, und das Trockengewicht (D) wurde nach 72 Stunden berechnet. somit wurde das W/D-Verhältnis berechnet. Der rechte obere Lappen wurde für den mRNA- und Proteinnachweis in flüssigem Stickstoff aufbewahrt. Die linke Lunge wurde dreimal mit 0,4 ml normaler Kochsalzlösung gewaschen und etwa 1 ml bronchoalveoläre Lavageflüssigkeit (BALF) wurde gesammelt, in ein 1,5 ml Eppendorf (EP)-Röhrchen überführt und auf Eis gestellt. BALF wurde 5 min bei 1500 U/min zentrifugiert und in ein neues EP-Röhrchen überführt, dann bei -80 °C zum Nachweis von Entzündungsfaktoren gelagert.
Außerdem wurden die Mäuse in 3 Gruppen (n = 10/Gruppe):Scheingruppe, Modellgruppe und miR-499-5p-Agomir-Gruppe (50 μL miR-499-5p-Agomir wurde 1 h vor der Operation in die Luftröhre instilliert). Die Überlebensrate wurde alle 12 h überwacht, insgesamt 7 Tage lang. Der Überlebensstatus der Mäuse innerhalb von 7 Tagen wurde beobachtet und die Toxizität von miR-499-5p wurde bestimmt [16].
Hämatoxylin-Eosin (H&E)-Färbung und Verletzungs-Score
Lungengewebe wurden in Paraffinschnitte präpariert, mit H&E gefärbt und unter einem optischen Mikroskop beobachtet. Lungenverletzungen (alveoläre Stauung, Blutung, Neutrophileninfiltration oder -aggregation in der Alveolarhöhle oder Gefäßwand, Alveolarwandverdickung und/oder Bildung von hyaliner Membranen) wurden durch das pathologische Bewertungssystem für Lungenverletzungen, herausgegeben von der American Thoracic Society, bewertet. 0 Punkt zeigt keine oder sehr leichte Läsionen an; 1 Punkt zeigte leichte Läsionen an; 2 Punkte zeigten mäßige Läsionen an; 3 Punkte zeigten schwere Läsionen an; 4 Punkte zeigten sehr schwere Läsionen an. Der Gesamtscore der vier Items repräsentierte den Gesamtscore der Lungenverletzung [17].
Masson-Färbung und Bewertung
Lungengewebe wurden in Paraffinschnitte (4 µm) geschnitten und mit Masson-Färbung behandelt [18]. Kollagenfasern, Schleim und Knorpel waren blau, Zytoplasma, Muskel, Zellulose und Glia waren rot und Zellkerne blau-schwarz. Im semiquantitativen Ashcroft-Scoring-System [19] bedeutete 0 Punkt eine normale Lunge; 1 Punkt zeigt eine leichte fibröse Verdickung der Alveolar- oder Bronchialwand an; 3 Punkte zeigten eine mäßige Verdickung der Alveolar- oder Bronchiolenwand ohne Schädigung der Lungenstruktur; 5 Punkte zeigten eine Verschlechterung der Fibrose, begleitet von einer Schädigung der Lungenstruktur, Bildung von Faserbändern oder -massen; 7 Punkte wiesen auf eine schwere Schädigung der Lungenstruktur und große Bereiche von Fibrose hin, die Faserbänder oder -klumpen bildeten; 8 Punkte zeigten alle regionalen Faserpackungen an.
terminale Desoxynukleotidyl-Transerase-vermittelte Desoxyuridintriphosphat-Biotin Nick End-Labeling (TUNEL)-Färbung
Die Apoptose von Lungengewebe wurde mit dem TUNEL-Kit (Roche Diagnostics GmbH, Mannheim, Deutschland) getestet und mit einem Lichtmikroskop beobachtet. Die apoptotischen Zellen waren im Kern braun gefärbt. Der Apoptoseindex zeigte den Prozentsatz der TUNEL-positiven Zellen an [20].
Immunhistochemie
Die Lungengewebeschnitte wurden mit Xylol entparaffiniert, mit 3% Wasserstoffperoxid inkubiert und mit dem Ziegenserum blockiert. Dann wurden Caspase-3 (ab13847, 1:500), Caspase-9 (ab32539, 1:250) und SOX6 (ab30455, 1:500, alle von Abcam, MA, USA) als Antikörper gegen Immunfärbungsschnitte verwendet. Ein optisches Mikroskop (Leica Microsystems, IL, USA) wurde verwendet, um Bilder aufzunehmen, die dann mit der Software Image Pro Plus 6.0 (Media Cybernetics, Rockville, MA, USA) analysiert wurden [21].
Quantitative Reverse Transkription der Polymerase-Kettenreaktion (RT-qPCR)
Das OMEGA-Kit (Solarbio Science &Technology Co., Ltd., Peking, China) wurde für die Extraktion der Gesamt-RNA in Lungengewebe und die Bestimmung der RNA-Konzentration verwendet. Die komplementäre DNA (cDNA) wurde durch reverse Transkription gemäß dem RevertAid First Strand cDNA Synthesis Kit (Thermo Fisher Scientific, Massachusetts, USA) zusammengesetzt. Die Primer wurden von Invitrogen (Carlsbad, CA, USA) entworfen, wie in Tabelle 1 gezeigt. Die PCR-Reaktion wurde gemäß dem FastStart Universal SYBR Green Master (Rox) Kit (Roche) durchgeführt. Das Experiment wurde quantitativ durch 2 −△△Ct . analysiert Methode. U6 war die Ladekontrolle von miR-499-5p und GAPDH war der interne Parameter anderer Gene [22].
Western Blot-Analyse
Das Gesamtprotein wurde unter Verwendung von Lysepuffer des Radioimmunpräzipitationsassays gesammelt, um Lungengewebe zu behandeln. Die Gesamtproteinkonzentration wurde durch das Bicinchoninsäure-Verfahren gemessen. Die Proteinprobe (30 µg) wurde durch 10 % Natriumdodecylsulfat-Polyacrylamid-Gelelektrophorese aufgearbeitet, auf die Polyvinylidenfluorid-Membran übertragen, mit 5 % Magermilchpulver blockiert und mit den Primärantikörpern Sox6 (ab30455, 1:1000, Abcam), Caspase -3 (9661, 1:1000, Cell Signaling Technology, MA, USA), Caspase-9 (9502, 1:1000, Cell Signaling Technology), Tumornekrosefaktor-α (TNF-α, ab6671, 1:1000, Abcam ), Interleukin-1β (IL-1β, 16806-1-AP, 1:500, Proteintech, USA), IL-6 (ab6672, 1:1000, Abcam) und GAPDH (sc-32233, 1:1000, Santa Cruz Biotechnologie, Inc., CA, USA). Dann wurde die Membran mit dem sekundären Antikörper inkubiert (1:2000) und durch verstärkte Chemilumineszenz entwickelt [23].
Enzyme-Linked Immunosorbent Assay (ELISA)
Die Spiegel von IL-1&bgr;, IL-6 und TNF-&agr; in BALF wurden durch einen ELISA-Kit (Boster, Hubei, China) bestimmt. Die kolorimetrische Bestimmung wurde bei 450 nm durchgeführt.
Erkennung von Indizes für oxidativen Stress
Die Lungengewebe in flüssigem Stickstoff wurden gewogen und in einem bestimmten Anteil an Kochsalzlösung bei niedriger Temperatur verdünnt, dann homogenisiert und bei 4&supmin;, 3000 U/min für 20 min bei niedriger Temperatur zentrifugiert, und der Überstand wurde zur Bestimmung entnommen. Die Aktivität der Myeloperoxidase (MPO) wurde mit dem MPO-Nachweiskit (NanJing JianCheng Bioengineering Institute, Nanjing, China) getestet und Malondialdehyd (MDA), Superoxiddismutase (SOD), Glutathionperoxidase (GSH-Px) und Katalase (CAT) wurden getestet durch Kits, die vom JianCheng Bioengineering Institute bereitgestellt werden.
Dualer Luciferase-Reporter-Gen-Assay
Sox6 könnte das Zielgen von miR-499-5p sein, das von einer biologischen Website (http://www.targetscan.org/vert_72/) vorhergesagt wurde. Es gab vier Bindungsstellen zwischen miR-499-5p und Sox6 mRNA 3′untranslated region (UTR). Die pmiR-RB-REPORT-Sox6 Wildtyp (WT) und pmiR-RB-REPORT-Sox6 Mutantentyp (MUT) Vektoren wurden von Guangzhou RiboBio Co., Ltd. (Guangdong, China) konstruiert und die entsprechenden Luciferase-Reporterplasmide wurden erzeugt. TC-1-Zellen (Lungenepithelzellen von Mäusen, 1 × 10 5 Zellen/Well, Shanghai Yiyan Biological Technology Co., Ltd., Shanghai, China) wurden in einer 24-Well-Platte ausgesät und mit miR-499-5p-Agomir oder Agomir-NC, pmiR-RB-REPORT-Sox6 WT oder . transfiziert pmiR-RB-REPORT-Sox6 MUT über Lipofectamine2000. Das duale Luciferase-Reportergen-Assay-System (Promega, WI, USA) wurde verwendet, um die Luciferase-Aktivität zu messen.
Statistische Analyse
Alle Daten wurden mit der Software SPSS 21.0 (IBM Corp. Armonk, NY, USA) analysiert. Die Messdaten wurden durch die mittlere ± ± Standardabweichung übermittelt. Vergleiche zwischen zwei Gruppen wurden von t . durchgeführt Test wurden Vergleiche zwischen mehreren Gruppen durch Einweg-Varianzanalyse (ANOVA) bewertet, und Tukeys Post-hoc-Test wurde für den paarweisen Vergleich nach der ANOVA-Analyse verwendet. Die Überlebenskurve wurde nach der Kaplan-Meier-Methode erstellt. P Wert < 0,05 war ein Hinweis auf einen statistisch signifikanten Unterschied.
Ergebnisse
W/D-Verhältnis und Sox6 sind erhöht, während miR-499-5p im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung verringert ist
Die Toxizität von miR-499-5p wurde an Mäusen getestet, um die Überlebenszeit septischer Mäuse zu bestimmen. Die Ergebnisse zeigten ( 1a ), dass die Überlebensrate der Mäuse in der Scheingruppe innerhalb von 7 Tagen 100 % betrug und die der septischen Mäuse reduziert war. Die Überlebensrate septischer Mäuse nach miR-499-5p-Behandlung wurde verbessert. Die Ergebnisse des W/D-Verhältnisses des Lungengewebes zeigten, dass (Abb. 1b):im Vergleich zur Scheingruppe war das W/D-Verhältnis in der Modellgruppe erhöht (P < 0,05). Im Vergleich zur Agomir-NC-Gruppe und der si-NC-Gruppe war das W/D-Verhältnis in der miR-499-5p-Agomir-Gruppe und der si-Sox6-Gruppe reduziert (beide P < 0,05). Das W/D-Verhältnis war in der miR-499-5p-Agomir + oe-Sox6-Gruppe im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe deutlich erhöht (P < 0.05).
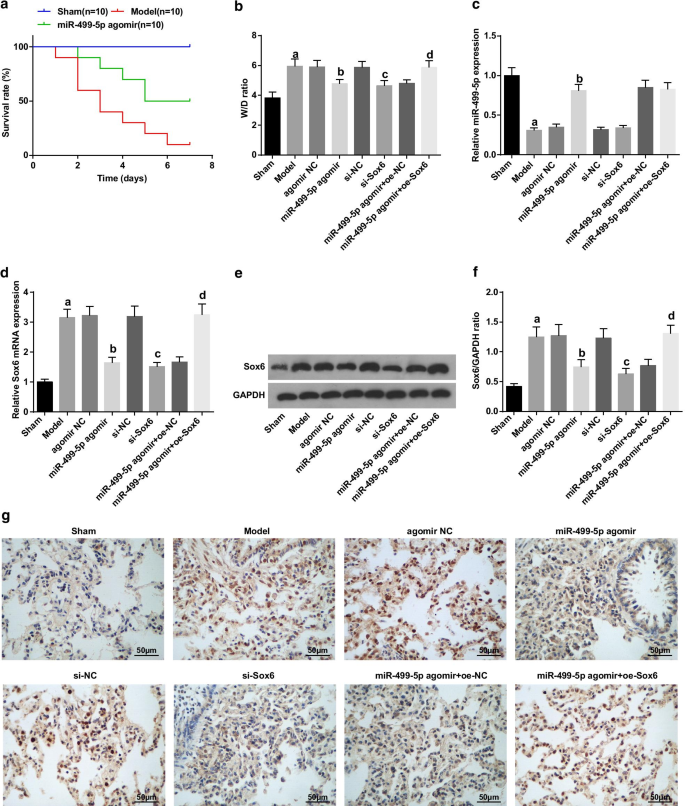
Das W/D-Verhältnis und Sox6 sind erhöht, während miR-499-5p im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung verringert ist. a Überlebenskurve von Mäusen von Kaplan-Meier. b W/D-Verhältnis von Lungengewebe in jeder Gruppe. c Expression von miR-499-5p in Lungengeweben von Mäusen. d Expression von Sox6-mRNA in Lungengeweben von Mäusen. e Proteinbande von Sox6 durch Western-Blot-Analyse. f Proteinexpression von Sox6 in Lungengeweben von Mäusen. g Sox6-Immunhistochemie von Lungengeweben von Mäusen. (a) P < 0,05 gegenüber der Scheingruppe. (b) P < 0,05 gegenüber der Agomir-NC-Gruppe. (c) P < 0,05 gegenüber der si-NC-Gruppe. (d) P < 0,05 gegenüber der miR-499-5p-Agomir + oe-NC-Gruppe. Die Messdaten wurden als Mittelwert ± ± Standardabweichung dargestellt, und die Daten wurden durch Einweg-ANOVA, gefolgt von Tukeys Post-hoc-Test bewertet
Die Expression von MiR-499-5p und Sox6 wurde nachgewiesen und wir fanden, dass (Abb. 1c–f):Im Gegensatz zur Scheingruppe reduzierte miR-499-5p und erhöhte Sox6 in der Modellgruppe (beide P < 0,05). In Bezug auf die Agomir-NC-Gruppe stieg miR-499-5p an und Sox6 nahm in der miR-499-5p-Agomir-Gruppe ab (beide P < 0,05). Im Vergleich zur si-NC-Gruppe deprimierte Sox6 in der si-Sox6-Gruppe (P < 0,05). Im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe war Sox6 in der miR-499-5p-Agomir + oe-Sox6-Gruppe dramatisch erhöht (P < 0.05).
Der Proteingehalt von Sox6 in Lungengeweben septischer Mäuse wurde durch Immunhistochemie bestimmt (Fig. 1g). Es wurde beobachtet, dass die Sox6-Proteinexpression im Vergleich zur Scheingruppe in der Modellgruppe erhöht war (P <0,05); verglichen mit der Agomir-NC-Gruppe und der Si-NC-Gruppe wurde eine geringere Sox6-Proteinexpression in der MiR-499-5p-Agomir-Gruppe und der Si-Sox6-Gruppe untersucht (beide P <0,05); Im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe war die Sox6-Proteinexpression in der miR-499-5p-Agomir + oe-Sox6-Gruppe (P < 0.05).
Restauriertes miR-499-5p oder depletiertes Sox6 lindert Pathologien des Lungengewebes, reduziert Lungenverletzungs-Score, Kollagenfasern und den Grad der Lungenfibrose bei Sepsis-induzierter Lungenverletzung Mäuse
Die Ergebnisse der HE-Färbung zeigten, dass (Abb. 2a):In der Scheingruppe war die Lungengewebestruktur intakt, das Alveolarseptum zeigte sich grundsätzlich ohne Ödem oder Entzündung und die Alveolarhöhle war klar. Im Modell der Gruppen Agomir NC, si-NC und miR-499-5p agomir + oe-Sox6 konnten Exsudation, Ödeme und Blutungen in den meisten Alveolarhöhlen des Lungengewebes beobachtet werden, und eine massive Infiltration von Entzündungszellen zeigte sich im Lungeninterstitium. In den miR-499-5p-Agomir-, si-Sox6- und miR-499-5p-Agomir + oe-NC-Gruppen war die Läsion des Lungengewebes gegenüber der Modellgruppe reduziert.
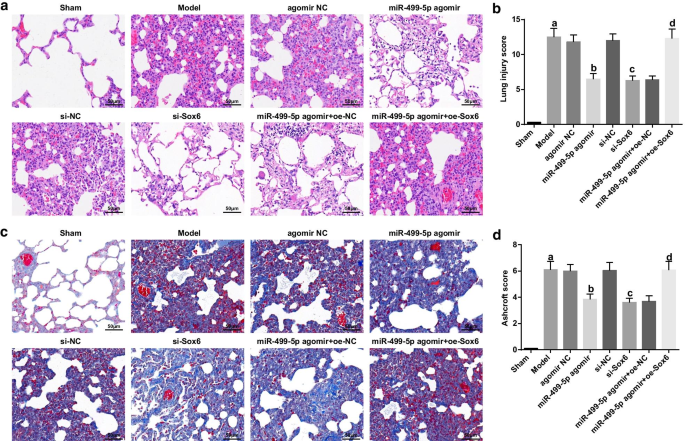
Wiederhergestelltes miR-499-5p oder erschöpftes Sox6 lindert die Pathologie des Lungengewebes, reduziert den Lungenverletzungs-Score, die Kollagenfasern und den Grad der Lungenfibrose bei Mäusen mit Sepsis-induzierter Lungenverletzung. a Ergebnisse der HE-Färbung in Lungengewebe von Mäusen. b Der Lungengewebeverletzungs-Score von Mäusen in jeder Gruppe. c Masson-Färbung von Lungengewebe bei Mäusen. d Die Lungenfibrose-Scores von Mäusen in jeder Gruppe. (a) P < 0,05 gegenüber der Scheingruppe. (b) P < 0,05 gegenüber der Agomir-NC-Gruppe. (c) P < 0,05 gegenüber der si-NC-Gruppe. (d) P < 0,05 gegenüber der miR-499-5p-Agomir + oe-NC-Gruppe. Die Messdaten wurden als Mittelwert ± ± Standardabweichung dargestellt, und die Daten wurden durch Einweg-ANOVA, gefolgt von Tukeys Post-hoc-Test bewertet
Lungenverletzungs-Score bei Mäusen und semiquantitative Ashcroft-Score-Ergebnisse zeigten, dass (Abb. 2b, d):In Bezug auf die Scheingruppe waren der Lungenverletzungs-Score und der Grad der Lungenfibrose in der Modellgruppe offensichtlich erhöht (P < 0,05). Im Vergleich zur Agomir-NC-Gruppe und der si-NC-Gruppe waren der Lungenverletzungs-Score und der Grad der Lungenfibrose in der miR-499-5p-Agomir- und der si-Sox6-Gruppe reduziert (beide P < 0,05). Im Gegensatz zur miR-499-5p-Agomir + oe-NC-Gruppe waren der Lungenverletzungs-Score und der Grad der Lungenfibrose in der miR-499-5p-Agomir + oe-Sox6-Gruppe deutlich erhöht (P < 0.05).
Die Ergebnisse der Masson-Färbung zeigten, dass (Abb. 2c):In der Scheingruppe enthielt das Lungengewebe der Mäuse eine kleine Menge blauer Kollagenfasern. Im Modell, Agomir NC-, si-NC- und miR-499-5p-Agomir + oe-Sox6-Gruppen, waren die Kollagenfasern erhöht. In der miR-499-5p-Agomir-Gruppe, der si-Sox6-Gruppe und der miR-499-5p-Agomir + oe-NC-Gruppe waren die Kollagenfasern im Vergleich zur Modellgruppe verringert.
Restauriertes miR-499-5p oder abgereichertes Sox6 reduziert TUNEL-positive Zellen, Caspase-3- und Caspase-9-Proteinexpression in Lungengewebe von Sepsis-induzierten Lungenverletzungsmäusen
Western Blot, TUNEL-Färbung und immunhistochemische Ergebnisse zeigten, dass (Abb. 3a–f):der normale Kern war blau und der apoptotische Kern war in verschiedenen Schattierungen braun. Im Vergleich zur Scheingruppe wurden TUNEL-positive Zellen, Caspase-3 und Caspase-9 Proteinexpression in der Modellgruppe (alle P < 0,05). Im Vergleich zu den Agomir-NC- und si-NC-Gruppen waren die TUNEL-positiven Zellen, die Caspase-3- und Caspase-9-Proteinexpression in den miR-499-5p-Agomir- und den si-Sox6-Gruppen (alle P < 0,05). Im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe waren TUNEL-positive Zellen, Caspase-3 und Caspase-9-Proteinexpression in der miR-499-5p-Agomir + oe-Sox6-Gruppe (alle P < 0.05).
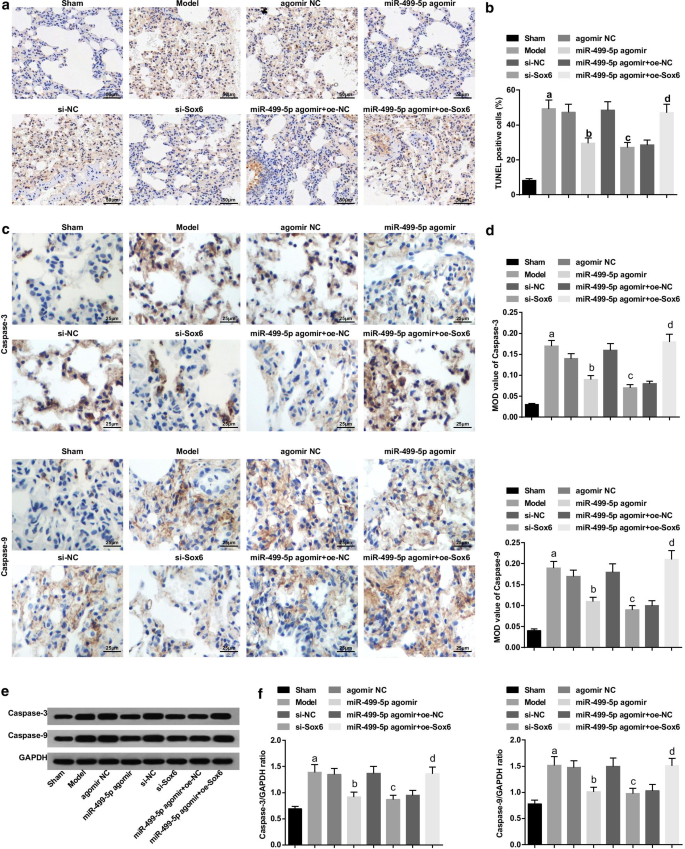
Wiederhergestelltes miR-499-5p oder abgereichertes Sox6 reduziert die TUNEL-positiven Zellen, die Caspase-3- und Caspase-9-Proteinexpression im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung. a TUNEL-positive Zellen im Lungengewebe von Mäusen. b Anzahl TUNEL-positiver Zellen im Lungengewebe von Mäusen. c Immunhistochemie von Caspase-3 und Caspase-9 in Lungengewebe von Mäusen; d Mittlerer OD-Wert von Caspase-3 und Caspase-9 im Lungengewebe von Mäusen. e Proteinbanden von Caspase-3 und Caspase-9 in Lungengeweben von Mäusen. f Caspase-3- und Caspase-9-Proteinexpression in Lungengeweben von Mäusen in jeder Gruppe. (a) P < 0,05 gegenüber der Scheingruppe. (b) P < 0,05 gegenüber der Agomir-NC-Gruppe. (c) P < 0,05 gegenüber der si-NC-Gruppe. (d) P < 0,05 gegenüber der miR-499-5p-Agomir + oe-NC-Gruppe. Die Messdaten wurden als Mittelwert ± ± Standardabweichung dargestellt, und die Daten wurden durch Einweg-ANOVA, gefolgt von Tukeys Post-hoc-Test bewertet
Wiederhergestelltes miR-499-5p oder depletiertes Sox6 verringert die TNF-α-, IL-1β- und IL-6-Gehalte in BALF- und Lungengewebe bei Sepsis-induzierter Lungenverletzung Mäuse
ELISA- und Western-Blot-Testergebnisse zeigten, dass (Abb. 4a–g):TNF-α, IL-1β und IL-6 Gehalte in der Modellgruppe im Vergleich zur Scheingruppe (alle P < 0,05). Im Vergleich zu den Agomir-NC- und den si-NC-Gruppen waren die TNF-α-, IL-1β- und IL-6-Gehalte in den miR-499-5p-Agomir- und den si-Sox6-Gruppen (alle P < 0,05). Im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe wurden die TNF-α-, IL-1β- und IL-6-Gehalte in der miR-499-5p-Agomir + oe-Sox6-Gruppe erhöht (alle P < 0.05).
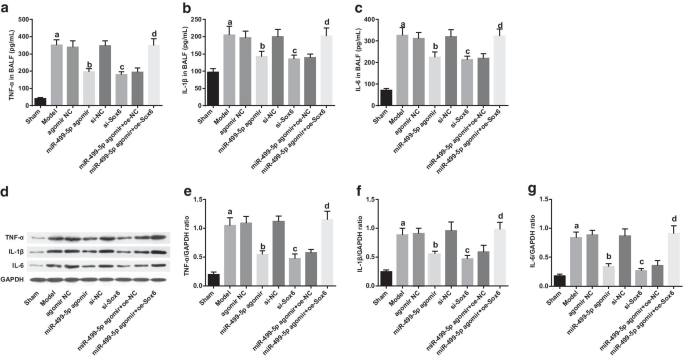
Wiederhergestelltes miR-499-5p oder abgereichertes Sox6 reduziert den TNF-α-, IL-1β- und IL-6-Gehalt in BALF- und Lungengeweben von Sepsis-induzierten Lungenverletzungsmäusen. a TNF-α-Gehalt in BALF von Mäusen in jeder Gruppe. b IL-1β-Gehalt in BALF von Mäusen in jeder Gruppe. c IL-6-Gehalt im BALF von Mäusen in jeder Gruppe. d Proteinbanden von TNF-α, IL-1β und IL-6 in Lungengeweben von Mäusen in jeder Gruppe. e Proteinexpression von TNF-α in Lungengeweben von Mäusen in jeder Gruppe. f Proteinexpression von IL-1β in Lungengeweben von Mäusen in jeder Gruppe. G Proteinexpression von IL-6 in Lungengeweben von Mäusen in jeder Gruppe. (a) P < 0,05 gegenüber der Scheingruppe. (b) P < 0,05 gegenüber der Agomir-NC-Gruppe. (c) P < 0,05 gegenüber der si-NC-Gruppe. (d) P < 0,05 gegenüber der miR-499-5p-Agomir + oe-NC-Gruppe. Die Messdaten wurden als Mittelwert ± ± Standardabweichung dargestellt, und die Daten wurden durch Einweg-ANOVA, gefolgt von Tukeys Post-hoc-Test bewertet
Restored miR-499-5p oder Depleted Sox6 erhöht die SOD-, CAT- und GSH-Px-Aktivitäten sowie reduziert den MDA- und MPO-Gehalt in Lungengewebe von Sepsis-induzierter Mäuse mit Lungenverletzung
Die Ergebnisse der Detektion von Indizes für oxidativen Stress zeigten, dass (Abb. 5a–e):im Vergleich zur Scheingruppe die SOD-, CAT- und GSH-Px-Aktivitäten beeinträchtigt waren, während die MDA- und MPO-Gehalte in der Modellgruppe (alle P < 0,05). Im Vergleich zu den Agomir-NC- und si-NC-Gruppen nahmen die SOD-, CAT- und GSH-Px-Aktivitäten zu, während die MDA- und MPO-Gehalte in den miR-499-5p-Agomir- und si-Sox6-Gruppen (alle P < 0,05). Im Vergleich zur miR-499-5p-Agomir + oe-NC-Gruppe wurden die SOD-, CAT- und GSH-Px-Aktivitäten unterdrückt, während die MDA- und MPO-Gehalte in der miR-499-5p-Agomir + oe-Sox6-Gruppe (alle P < 0.05).
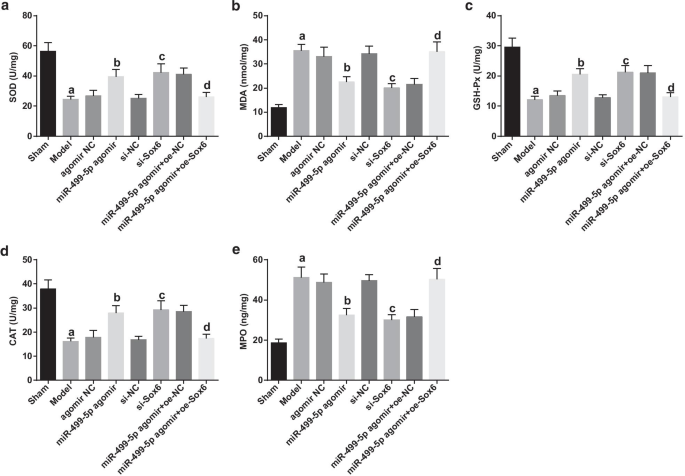
Wiederhergestelltes miR-499-5p oder abgereichertes Sox6 erhöht die SOD-, CAT- und GSH-Px-Aktivitäten sowie reduziert den MDA- und MPO-Gehalt im Lungengewebe von Mäusen mit Sepsis-induzierter Lungenverletzung. a SOD-Aktivität in Lungengeweben von Mäusen. b MDA-Gehalt im Lungengewebe von Mäusen. c GSH-Px-Aktivität in Lungengeweben von Mäusen. d CAT-Aktivität in Lungengeweben jeder Gruppe von Mäusen. e MPO-Gehalt im Lungengewebe von Mäusen. (a) P < 0,05 gegenüber der Scheingruppe. (b) P < 0,05 gegenüber der Agomir-NC-Gruppe. (c) P < 0,05 gegenüber der si-NC-Gruppe. (d) P < 0,05 gegenüber der miR-499-5p-Agomir + oe-NC-Gruppe. Die Messdaten wurden als Mittelwert ± ± Standardabweichung dargestellt, und die Daten wurden durch Einweg-ANOVA, gefolgt von Tukeys Post-hoc-Test bewertet
miR-499-5p zielt direkt auf Sox6 ab
Wir sagten über die Bioinformatik-Website TargetScan voraus, dass es gezielte Bindungsstellen zwischen miR-499-5p und SOX4/6 gab. Unter Verwendung von RT-qPCR wurde festgestellt, dass im Vergleich zur Scheingruppe die SOX2/4/6-Expression in der Modellgruppe anstieg und die SOX6-Expression hauptsächlich anstieg (alle P <0,05); im Vergleich zur Agomir-NC-Gruppe zeigte die miR-499-5p-Agomir-Gruppe keine Veränderung der SOX2-Expression, während sie eine reduzierte SOX4-Expression zeigte, hauptsächlich verringerte SOX6 (Zusätzliche Datei 1:Abb. S1a, b). Daher haben wir schließlich SOX6 als Zielgen von miR-499-5p ausgewählt. Die Website zur biologischen Vorhersage (http://www.targetscan.org/vert_72/) ergab, dass miR-499-5p auf Sox6 abzielen könnte (Abb. 6a). Der duale Luciferase-Reportergen-Assay zeigte, dass (Fig. 6b) gegenüber der Kontrollgruppe die Luciferase-Aktivität offensichtlich zerstört wurde, nachdem der pmiR-RB-REPORT-Sox6-WT-Vektor und miR-499-5p-Agomir in TC-1-Zellen (P < 0,05), während die Luciferase-Aktivität keinen deutlichen Unterschied zeigte, nachdem miR-499-5p-Agomir co-transfiziert mit pmiR-RB-REPORT-Sox6-MUT-Vektor oder Agomir-NC co-transfiziert mit pmiR-RB-REPORT-Sox6-WT-Vektor ( P> 0,05), was darauf hindeutet, dass miR-499-5p direkt an Sox6 3′UTR WT binden und dann die Luciferase-Aktivität hemmen könnte.

miR-499-5p zielt direkt auf Sox6 ab. a Die Zielbeziehung zwischen miR-499-5p und Sox6 wird von der biologischen Website vorhergesagt. b Die Verifizierungsergebnisse des dualen Luciferase-Reportergen-Assays. *P < 0,05 gegenüber der mimischen NC-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung dargestellt, und Vergleiche zwischen zwei Gruppen wurden von t . durchgeführt testen
Diskussion
Sepsis ist eine kritische Ursache für Schock und multiples Organdysfunktionssyndrom, unter denen ALI die häufigste und bedeutendste Organkomplikation ist [24]. Die Sepsis-induzierte ALI tritt nicht nur am frühesten und am häufigsten auf, sondern schreitet auch schnell fort, die Sterblichkeitsrate ist hoch und es gibt derzeit keine wirksame Therapie [25]. In einer früheren Studie wurde behauptet, dass die Hochregulierung von miR-218 die Sekretion von Entzündungsfaktoren abschwächte und eine Sepsis-induzierte Lungenschädigung verhinderte [26]. Außerdem könnte die Förderung der Spiegel von miR-146a die Entzündung bei ALI reduzieren [27] und die Wiederherstellung von miR-125b verbessert das Überleben von Mäusen mit ALI und unterdrückt Entzündungen [28]. Obwohl Studien die Rolle von miRNAs bei Lungenschäden hervorgehoben haben, wurde der detaillierte Mechanismus von miR-499-5p bei Sepsis-induzierten Lungenschäden kaum untersucht ALI. Also, a study has provided a proof that increased Sox6 was involved in sepsis-induced cardiac apoptosis [10]. Efforts should be made to deeply understand sepsis-induced lung injury. We aim to discuss the protective effect of miR-499-5p targeting Sox6 on sepsis-induced lung injury mice.
The W/D ratio of lung tissues was calculated in our study, and the expression of Sox6 and miR-499-5p in mouse lung tissues was assessed. The results showed that W/D ratio and Sox6 were increased while miR-499-5p was decreased in lung tissues of sepsis-induced lung injury mice. A recent study has proposed that miR-499-5p expression in patients with mild sepsis, severe sepsis and septic shock was dramatically decreased relative that in normal controls [9]. Another study has presented that miR-499-5p expression was markedly declined in non-small cell lung cancer (NSCLC) tissues and linked to poor clinical outcomes [29]. It is reported that the Sox6 expression was raised in lung cancer tissues in comparison with normal tissues [30]. Similarly, a previous study has revealed that the expression of Sox6 was remarkably elevated in the kidney tissues of mice with diabetic kidney disease [31]. Our study also presented that miR-499-5p directly targeted to Sox6. An important finding was that Sox6 is a target gene of miR-499 [10]. Another study provided data of that Sox6 was a target gene of miR-499-5p, and restoration of miR-499-5p suppressed the expression of Sox6 [32]. However, the target relation of miR-499-5p and Sox6 in lung tissues of sepsis-induced mice has not been uncovered yet.
In addition, it was revealed that restored miR-499-5p or depleted Sox6 alleviated lung tissues pathology, reduced lung injury score, collagen fibers and the degree of pulmonary fibrosis, and reduced TUNEL positive cells, Caspase-3 and Caspase-9 protein expression in lung tissues of sepsis-induced lung injury mice. It has been previously suggested that up-regulating miR-499-5p suppresses cell proliferation and promotes apoptosis in vivo and in vitro of NSCLC [29]. Another study has verified that restoring miR-499-5p and depleting Sox6 attenuated hypoxia/re-oxygenation-induced cell apoptosis and reduced Caspase-3 expression [32]. It was presented that down-regulating Sox6 alleviates the pathological injury and represses neuronal apoptosis in hippocampal tissues of Alzheimer’s disease [33]. Moreover, a study revealed that depletion of Sox6 inhibited high glucose-induced cell apoptosis and renal interstitial fibrosis in mouse renal mesangial cells [31]. Another study demonstrated that low expression of Sox6 declined the activity of Caspase-3 and the percentage of apoptotic cells in mouse P19CL6 cells [34]. In addition, we verified that restored miR-499-5p or depleted Sox6 declined TNF-α, IL-1β and IL-6 contents in BALF and lung tissues of sepsis-induced lung injury mice. Xiaet al. illuminated that TNF-α and IL-6 levels were dramatically raised in sepsis-induced lung injury mice [35]. A study has demonstrated that low expression of Sox6 declines the inflammatory reaction in hippocampal tissues of Alzheimer’s disease [33]. Another result in this study implied that restored miR-499-5p or depleted Sox6 raised SOD, CAT and GSH-Px activities as well as reduced MDA and MPO contents in lung tissues of sepsis-induced lung injury mice. It was presented that CLP-induced ALI was featured by inflammation in morphology, enhanced W/D ratio, raised protein concentration in BALF, higher level of MPO and MDA contents as well as lower level of SOD, GSH-Px and CAT activities in lungs after CLP [36]. It was suggested that the activity of SOD and CAT were decreased in sepsis-induced ALI in mice [37]. Furthermore, a study reported that the overexpressed miR-499-5p and low expressed Sox6 decreased the level of MDA [32].
Conclusion
In conclusion, we found that high expression of miR-499-5p can attenuate the apoptosis of lung tissues cells and inhibit inflammation of sepsis-induced lung injury mice via depleting Sox6, which may have important therapeutic implications in the treatment of sepsis-induced lung injury. Nevertheless, clinical researches are needed to detect the efficacy for the treatment of sepsis-induced lung injury.
Availability of data and material
Not applicable.
Nanomaterialien
- Vollständige Terahertz-Polarisationskontrolle mit erweiterter Bandbreite über dielektrische Metaoberflächen
- Zielgerichtete Endothelzellen mit multifunktionalen GaN/Fe-Nanopartikeln
- Evaluierung neuartiger 64Cu-markierter theranostischer Gadolinium-basierter Nanosonden in HepG2-Tumortragenden Nacktmäusen
- Verbesserte Antitumorwirksamkeit und Pharmakokinetik von Bufalin durch PEGylierte Liposomen
- Erhebliche Verbesserung von MgZnO-Metall-Halbleiter-Metall-Photodetektoren durch Kopplung mit Pt-Nanopartikel-Oberflächenplasmonen
- Verbesserung der Leistung von a-IGZO-TFT-Geräten durch einen sauberen Schnittstellenprozess durch Ätzstopper-Nanoschichten
- Abstimmung des Gleit-Roll-Bewegungsmodus von Kohlenstoffnanoröhren über Hydroxylgruppen
- In-situ-Synthese von bimetallischen Wolfram-Kupfer-Nanopartikeln durch thermisches Hochfrequenzplasma (RF)
- Wirkung von Nano-SiO2 auf die Expression und fehlerhafte Methylierung geprägter Gene in Lunge und Hoden
- Synthese und In-vitro-Studie einer Dual-Mode-Sonde, die auf Integrin αvβ3 abzielt



