Eintopfsynthese monodisperser CoFe2O4@Ag-Kern-Schale-Nanopartikel und deren Charakterisierung
Zusammenfassung
In den letzten Jahren werden monodisperse magnetische Nanopartikel mit einer Kern/Schale-Struktur für ihre breiten Anwendungen erwartet, einschließlich magnetischer Flüssigkeiten, rückgewinnbarer Katalysatoren und biologischer Analyse. Ihr Syntheseverfahren erfordert jedoch zahlreiche Prozesse wie Lösungsmittelsubstitution, Austausch von Schutzmitteln und Zentrifugation. Ein einfaches und schnelles Verfahren zur Synthese monodisperser Kern-Schale-Nanopartikel ermöglicht es, deren weitere Anwendungen zu beschleunigen. Dieses Papier beschreibt eine einfache und schnelle Eintopfsynthese von Core (CoFe2 O4 )-Schale (Ag) Nanopartikel mit hoher Monodispersität. Die synthetisierten Nanopartikel zeigten aufgrund der Ag-Schale plasmonische Lichtabsorption. Darüber hinaus wies die magnetische Eigenschaft der Nanopartikel ein weichmagnetisches Verhalten bei Raumtemperatur und ein hartmagnetisches Verhalten bei 5 K auf. Darüber hinaus zeigten die Nanopartikel eine hohe Monodispersität mit einem niedrigen Polydispersitätsindex (PDI) von 0,083 in Hexan.
Hintergrund
In den letzten zehn Jahren haben magnetische Nanopartikel mit Kern-Schale-Struktur aufgrund der Anwendungen magnetischer Flüssigkeiten [1, 2], magnetischer Separation [1, 2, 3], rückgewinnbare Katalysatoren [1, 2, 4,5,6,7], Drug-Delivery-System [1, 8,9,10] und ein verbessertes Kontrastmittel für die Magnetresonanztomographie (MRT) [7, 9,10, 11].
Unter den magnetischen Nanopartikeln wurde aufgrund seiner hervorragenden magnetischen und elektrischen Eigenschaften häufig ein Spinell-Ferrit-Nanopartikel als Magnetkern verwendet [12]. Insbesondere Kobaltferrit (CoFe2 O4 ) Nanopartikel haben ein großes maximales Koerzitivfeld (H c ), selbst bei geringer Größe sowie einer bemerkenswerten chemischen Stabilität und einer mechanischen Härte [13,14,15,16,17]. Obwohl viele verschiedene chemische Methoden zur Herstellung von CoFe2O4-Nanopartikeln entwickelt wurden, wurde die thermische Zersetzungsmethode in letzter Zeit als eines der vielversprechendsten Verfahren eingesetzt, um hochgradig, strukturell und morphologisch kontrollierte Nanopartikel mit hoher Kristallinität zu erhalten [13, 17, 18].
Magnetische Nanopartikel mit Kern-Schale-Struktur haben aufgrund ihrer Multifunktionalität einschließlich optischer, elektronischer und magnetischer Eigenschaften große Aufmerksamkeit auf sich gezogen [6, 8, 10, 19]. Insbesondere die mit Au beschichteten magnetischen Nanopartikel wurden umfassend untersucht, um nicht nur die Oberflächenplasmoneneigenschaften, sondern auch eine reaktive Oberfläche für eine starke Bindung an organische Verbindungen mit Thiolgruppen bereitzustellen [3, 20]. Typischerweise kann ein Ansatz eines kombinierten zweistufigen thermischen Zersetzungsprozesses kontinuierlich von Kernen zu Schalen synthetisieren, was zur Bildung von Au-beschichteten magnetischen Nanopartikeln mit einer hohen Monodispersität führt [20]. Auf der anderen Seite wurden trotz hervorragender plasmonischer Eigenschaften, eines höheren Extinktionskoeffizienten, einer schärferen Extinktionsbande, eines höheren Lichtstreuungs-zu-Extinktions-Effekts und starker lokaler elektromagnetischer Felder keine mit Ag-Schalen beschichteten magnetischen Nanopartikel mit diesem Ansatz synthetisiert von Ag-Schalen.
In dieser Studie ist es uns gelungen, mit einer Ag-Schale beschichtetes CoFe2 . zu synthetisieren O4 Nanopartikel durch ein einfaches und schnelles Eintopfverfahren mit zwei thermischen Zersetzungsprozessen. Es wurde bestätigt, dass unsere synthetisierten Nanopartikel eine präzise Kern-Schale-Struktur bilden, verglichen mit denen, die in einer früheren Veröffentlichung synthetisiert wurden [21, 22]. Darüber hinaus haben wir gezeigt, dass das CoFe2 O4 @Ag zeigte, dass die lokalisierte Oberflächenplasmonenresonanz (LSPR) von den Ag-Schalen stammt. Bei der Untersuchung der magnetischen Eigenschaften zeigte dieses Kern-Schale-Nanopartikel ein weichmagnetisches Verhalten mit H c von 70 Oe bei 300 k und hartmagnetischem Verhalten mit 11 k Oe bei 5 K.
Methode/Experimental
Material
Fe(acac)3 und Co(acac)2 wurden von Tokyo Chemical Industry gekauft. Diphenylether, Oleylamin (OAm) und Silber(I)acetat wurden von Wako bezogen. Ölsäure (OA) wurde von Kanto Chemical bezogen.
Synthese von CoFe2O4@Ag
Das CoFe2O4@Ag wurde durch die zweistufige hochthermische Zersetzungsmethode synthetisiert (Schema 1). Fe(acac)3 (0,353 g, 1 mmol), Co(acac)2 (0,129 g, 0,5 mmol) und OA (3,39 g, 12 mmol) wurden in 30 ml Diphenylether gelöst, der durch Erhitzen auf 180 °C für 30 Minuten vorbehandelt wurde. Eine Mischung wurde 16 h unter kräftigem Rühren auf 180 °C erhitzt. Die Farbe der Lösung änderte sich allmählich von Dunkelrot zu feinem Schwarz. Nach dem Abkühlen auf Raumtemperatur wurde eine Mischung aus OA (1,48 g, 5,2 mmol), OAm (8,13 g, 30,4 mmol) und Silberacetat (0,61 g, 3,6 mmol), gelöst in 100 ml Diphenylether, zu der Mischung gegeben. gefolgt von Erhitzen auf 180 °C für 1,5 h. Die Farbe der Mischung wurde während des Erhitzens weiter zu einem metallischen Dunkelviolett. Nach dem Abkühlen wurden 400 ml Methanol als schlechtes Lösungsmittel zu der Mischlösung gegeben, gefolgt von einer Zentrifugation (5000 U/min, 5 min) und der Redispergierung in 60 ml Hexan. Obwohl die in der Lösung dispergierten Nanopartikel möglicherweise magnetisch getrennt werden können, dauert es einige Zeit, bis sie sich wieder erholt haben. Der Zentrifugationsvorgang wurde mehrere Male wiederholt, um die nicht umgesetzten Vorläufer zu entfernen. Schließlich wurden die resultierenden Niederschläge durch Zentrifugieren der kolloidalen Hexanlösung (14.000 U/min, 20 min) entfernt. Das Nettogewicht der Nanopartikel bei dieser Methode beträgt etwa 60 mg als 1 mg/ml der kolloidalen Hexanlösung. Das CoFe2 O4 Nanopartikel als Referenz wurden hergestellt, indem nur Schritt 1 in Schema 1 durchgeführt wurde.
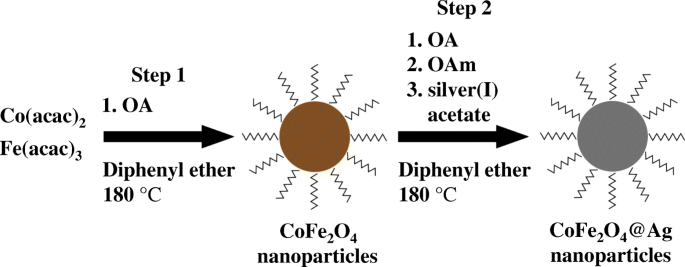
Verfahren zur Synthese von CoFe2 O4 @Ag-Nanopartikel
Charakterisierung und Berechnung
Die Morphologie von Nanopartikeln wurde unter Verwendung von Feldemissions-Transmissionselektronenmikroskopie (TEM) (Hitachi, Ltd., FE 2000) beobachtet. Die Kristallstrukturen wurden mit Röntgenbeugung (XRD) (PANalytical, X’Pert PRO MPD) im Bereich von 2θ . gemessen = 20° bis 80° unter Verwendung der CuK-α-Strahlung. Die Elementzusammensetzung von Nanopartikeln wurde durch Röntgenphotoelektronenspektroskopie (XPS) (KARATOS ESCA 3400) analysiert. Der Ätzvorgang wurde mit einer Ar-Ionenkanone durchgeführt. Die Magnetisierungsmessungen wurden mit einem supraleitenden Quanteninterferenzgerät (SQUID) (Cryogenic, S700X-R) durchgeführt. Die optischen Eigenschaften wurden auf einem UV-Vis-Spektrophotometer (Jasco, V-670) gemessen. Dynamische Lichtstreuung (DLS) (Malvern, zetasizer-nano-zs) wurde mit einer 633-nm-Laserlinie gemessen. Für die optischen Eigenschaften unserer synthetisierten Kern-Schale-Nanopartikel werden die experimentellen Daten durch Mie-Streuberechnungen gestützt, die mit der Lösung von Bohren und Huffman [23] unter Verwendung des MATLAB-Codes von Mätzler [24] durchgeführt wurden. Die dielektrischen Funktionen für Ag wurden aus Lit. [25] entnommen.
Ergebnisse und Diskussion
Abbildung 1 zeigt die TEM-Bilder von CoFe2 O4 Nanopartikel und CoFe2 O4 @Ag-Kern-Schale-Nanopartikel. Wie in den Einfügungen von Fig. 1 gezeigt, sind die Größenverteilungen beider Nanopartikel eng. Die durchschnittliche Größe (Mittelwert ± SD) von ihnen beträgt 3,5 ± ± 0,76 bzw. 5,5 ± ± 0,77 nm. Aus diesen Ergebnissen wurde die Dicke der Ag-Schale auf ca. 1 nm. Aggregation von CoFe2 O4 Partikel traten auf, aber nicht für CoFe2 O4 @Ag-Nanopartikel. Dies ist möglicherweise auf eine höhere Oberflächenenergie der CoFe2O4-Nanopartikel als die des CoFe2 . zurückzuführen O4 @Ag-Nanopartikel aufgrund eines größeren Oberfläche-zu-Volumen-Verhältnisses von CoFe2 O4 Nanopartikel [26]. Auch restliches CoFe2 O4 Nanopartikel (Kerne) konnten in der Probe von CoFe2 . nicht beobachtet werden O4 @Ag. Dieses Ergebnis legt nahe, dass fast alle Kerne gleichmäßig mit der Silber-Ag-Schale beschichtet sind.
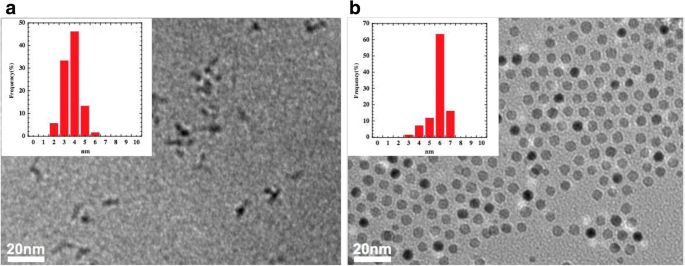
TEM-Bilder und Partikelgrößenhistogramme für Nanopartikel von a CoFe2 O4 und b CoFe2 O4 @Ag
Abbildung 2 zeigt die XRD-Muster für CoFe2 O4 und das CoFe2 O4 @Ag-Nanopartikel. Die Beugungspeaks von CoFe2 O4 Nanopartikel bei 2θ = 30,50°, 35,75°, 43,50°, 53,8°, 57,5°, 63,0° und 74,4° zeigen die Bildung einer einzelnen kristallographischen Phase, die als kubische Struktur von Spinelloxiden indiziert werden kann [17]. Andererseits sind die Beugungspeaks von CoFe2 O4 @Ag um 2θ =38,42°, 44,50°, 64,91°, 77,75° und 81,83° entsprechen denen der standardmäßigen kubisch-flächenzentrierten (fcc) Phase von Ag [10]. Die Intensität der Beugungspeaks von CoFe2 O4 sind relativ schwach und ihr Hauptpeak überlappt mit Ag; daher gehen alle in die von Ag über. Die Kristallitgröße wurde aus der Halbwertsbreite (FWHM) des Beugungspeaks mit der höchsten Intensität berechnet, die auf der Debye-Scherrer-Gleichung basiert,
$$ t=0,9l/b\ \cos\ y $$ (1)wo t ist die Kristallitgröße, l ist die Wellenlänge der Cu-Ka-Strahlung, b ist die FWHM und y ist der Beugungswinkel des stärksten Peaks. Die aus den Beugungsmustern ausgewerteten Kristallgrößen betrugen 7,1 und 3,6 nm für CoFe2 . O4 Nanopartikel und CoFe2 O4 @Ag-Nanopartikel bzw. Die Kristallgröße von CoFe2 O4 Nanopartikel waren aufgrund des Rests von CoFe2 . größer als die Größe von TEM O4 Nanopartikel außerhalb der Größenverteilung, die durch Zentrifugation in Hexan nicht entfernt werden konnten. Andererseits zeigte die Kristallgröße von XRD eine Übereinstimmung in CoFe2O4@Ag-Nanopartikeln, wenn man bedenkt, dass die Kristallgröße der Ag-Schale kleiner sein muss als die Größe des TEM. Die Größe des Kolloids nach der Silberbeschichtungsreaktion ermöglicht aufgrund seines Schwergewichts in Hexan eine Selektion durch Zentrifugation.
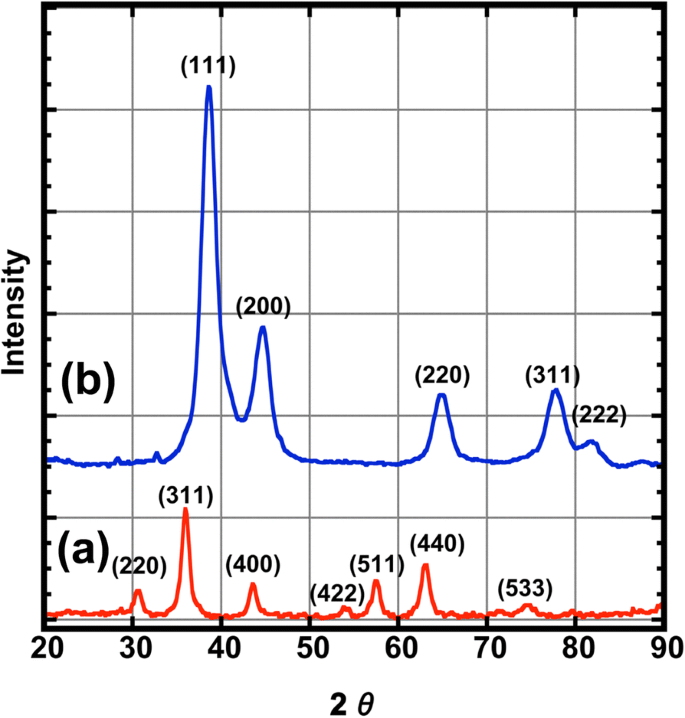
XRD-Muster von für Nanopartikel, (a ) CoFe2 O4 (rote Linie) und (b ) CoFe2 O4 @Ag (blaue Linie)
Um die innere Zusammensetzung der erhaltenen Nanopartikel mit einer Kern-Schale-Struktur zu bewerten, wurden die Nanopartikeloberflächen mit einer Ar-Ionenkanone in der Kammer geätzt [27]. Nach den bisherigen Untersuchungen sollte bei einer präzisen Kern-Schale-Struktur der Partikel die Spitzenintensität des im Kern enthaltenen Elements mit fortschreitender Ätzung erhöht werden. Wie in Abb. 3a–d gezeigt, um die Oberflächenzusammensetzung von CoFe2 . zu bestimmen O4 @Ag-Nanopartikel, wir haben die XPS-Spektren vor dem Ar-Ionenätzen gemessen. In den Anfangsoberflächen war der Peek C (1 s) in Nanopartikeln aufgrund des Vorhandenseins des Schutzmittels auf der Oberfläche der Nanopartikel leicht zu beobachten (Abb. 3a). Das Spektrum von C (1 s) wurde zerlegt und ein von C-O-C abgeleiteter Peak wurde beobachtet, der von an der Oberfläche modifizierter Ölsäure abgeleitet ist. Während die Peaks von Ag(3d) beobachtet wurden, konnten die von Fe(2p) und Co(2p) nicht beobachtet werden, was darauf hindeutet, dass der Kern vollständig mit den Ag-Schalen bedeckt war (Abb. 3b–d). Andererseits wurden die Peaks von Fe(2p) und Co(2p) in den Nanopartikeln nach dem Ätzvorgang mit Argonionen beobachtet (Abb. 3f, g). Die Peaks von Fe(2p) und Co(2p) werden zerlegt und können Fe 2+ . zugeordnet werden , Fe 3+ , Co 2+ , und Co 3+ , bzw. Die Bildung beider Arten von Ladungsträgern resultiert aus dem Sauerstoffverlust während des Hochtemperaturreaktionsprozesses [28, 29]. Für den Ladungsausgleich wird ein Teil von Fe3+ in Fe2+ und ein Teil von Co2+ in Co3+ umgewandelt. Darüber hinaus kann jeder der Ag(3d)-Peaks nach dem Ätzen aufgrund des Unterschieds im elektronischen Zustand zwischen den Nanopartikeloberflächen und der Innenseite der Schalen in zwei Peaks zerlegt werden (Abb. 3h). Diese Ergebnisse zeigen, dass die genaue Kern-Schale-Struktur gebildet wird.
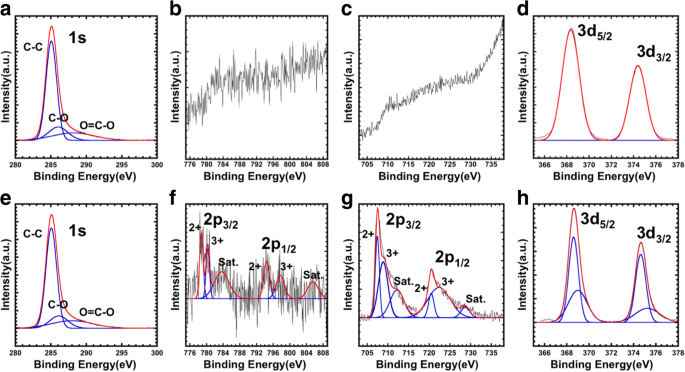
XPS-Spektren von CoFe2 O4 @Ag durch Argonionenätzung vor (a –d ) und nach (e –h ). a , e C 1 s. b , f Co 2p. c , g Fe 2p. d , h Ag 3d
Die magnetischen Hystereseschleifen von Filmen aus CoFe2 O4 und das CoFe2 O4 @Ag-Nanopartikel wurden bei 300 und 5 K gemessen, wie in Abb. 4 gezeigt. Diese Hystereseschleifen wurden als magnetische Suszeptibilität pro Einheit Kobaltgewicht normalisiert. Aufgrund der Analyse der kristallographischen Phase mit XRD (Abb. 2) wurden die Kristalldichten von CoFe2 O4 und CoFe2 O4 @Ag-Nanopartikel wurden auf 5,3 und 10,5 g/cm 3 geschätzt , bzw. Auch die Volumina von CoFe2 O4 und CoFe2 O4 @Ag-Nanopartikel wurden anhand der Ergebnisse der TEM-Beobachtung berechnet (Abb. 1). CoFe2 O4 Nanopartikel zeigten bei Raumtemperatur ein superparamagnetisches Verhalten (Abb. 4a). Wie von López-Ortega et al. [17], das CoFe2 O4 Nanopartikel mit einer Größe unter 20 nm zeigten das superparamagnetische Verhalten bei Raumtemperatur. Die magnetischen Eigenschaften jeder Probe bei den beiden Temperaturen sind in Tabelle 1 zusammengefasst. Magnetische Sättigung (M s ) des CoFe2 O4 Nanopartikel war 11 (emu/g CoFe2 O4 ), was niedriger ist als die vorherigen Ergebnisse [17, 30, 31]. Dies ist möglicherweise auf die kleinere Partikelgröße zurückzuführen, die in dieser Studie erhalten wurde. Auf der anderen Seite ist das M s des CoFe2 O4 @Ag war mit einem Wert von 3.3 noch kleiner (emu/g, CoFe2 .) O4 ). Wie in der vorherigen Literatur für Fe3 . erwähnt O4 @Ag-Nanopartikel [8,9,10, 32,33,34], das M s von CoFe2 O4 @Ag nimmt möglicherweise aufgrund des diamagnetischen Beitrags der Ag-Schale ab. Darüber hinaus ist CoFe2 O4 @Ag zeigte 77 Oe, was ein hohes H ist c Wert bei 300 k. Das H c des CoFe2 O4 @Ag unterscheidet sich auch von CoFe2 O4 unter der niedrigen Temperatur (Abb. 4b). Beide Nanopartikel zeigten trotz ihrer relativ geringen Größe Ferromagnetismus bei 5 K. Auf der Grundlage der Daten nahe Null Magnetisierung ist der Wert von H c steigt für CoFe2 O4 @Ag-Nanopartikel (7 k Oe für CoFe2 .) O4 und 11 k Oe für CoFe2 O4 @Ag). Dieses interessante Verhalten wurde auch bei anderen Kern-Schale-Nanopartikeln wie Fe@Ag [10] und Fe3 . beobachtet O4 @Au-Nanopartikel [5]. Unter Berücksichtigung dieser Tatsachen ist der Anstieg des H c des CoFe2 O4 @Ag-Nanopartikel können aus einer weniger effektiven Kopplung des magnetischen Dipolmoments abgeleitet werden [5, 20].
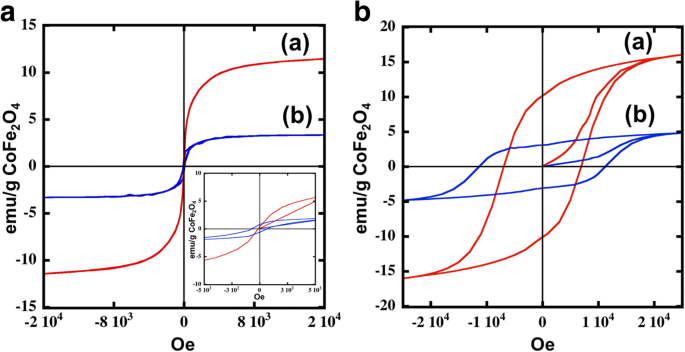
Hystereseschleifen für Nanopartikel:(a ) und (b ) sind für das CoFe2 O4 Nanopartikel (rote Linie) und CoFe2 O4 @Ag-Nanopartikel (blaue Linie) jeweils bei a 300 K und b um 5 K
Als nächstes optische Eigenschaften von CoFe2 O4 Nanopartikel wurden durch UV-sichtbare Spektralmessungen untersucht. Von Ag-Nanopartikeln ist bekannt, dass sie aufgrund der Anregung der lokalisierten Oberflächenplasmonenresonanz (LSPR) durch die Kopplung des eingestrahlten Lichts mit der kohärenten Oszillation von Oberflächenelektronen innerhalb der Ag-Nanopartikel eine signifikante Lichtauslöschung im sichtbaren Bereich zeigen. Obwohl das CoFe2 O4 Nanopartikel zeigten keine LSPR-Extinktionsbande im sichtbaren Bereich (Abb. 5), die kolloidale Lösung unseres Kern-Schale-Typs CoFe2 O4 @Ag-Nanopartikel zeigten einen scharfen Extinktionspeak bei 416 nm. Dies ist auf die Plasmonenabsorption (Dipolmodus) der Ag-Schale zurückzuführen, die theoretisch durch die Mie-Theorie unterstützt wird (siehe Zusatzdatei 1). Dieses interessante Verhalten wurde für Fe@Ag-Nanopartikel [10] und Co@Ag-Nanopartikel [7] beobachtet. Darüber hinaus sind die spektroskopischen Eigenschaften von CoFe2 O4 @Ag-Nanopartikel wurden einen Monat lang nicht gewechselt, was auf die überlegene Stabilität der Nanopartikel unter Luft hinweist.
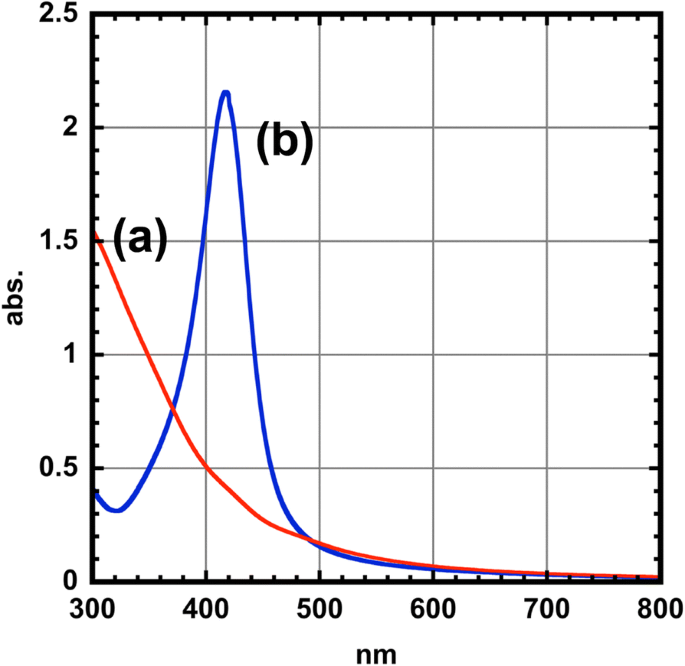
UV-Vis-Spektren für (a ) CoFe2 O4 Nanopartikel (rote Linie) und (b ) CoFe2 O4 @Ag-Nanopartikel (blaue Linie)
Die kolloidale Stabilität von CoFe2 O4 und das CoFe2 O4 @Ag-Nanopartikel wurden durch Messung der Größenverteilungen der Nanopartikel in Hexan mit DLS bewertet (Abb. 6). Die durchschnittlichen Größen von CoFe2 O4 und CoFe2 O4 @Ag-Nanopartikel wurden mit 19,67 bzw. 9,27 nm gemessen. Die Größen dieser Nanopartikel, die aus TEM-, XRD- und DLS-Messungen erhalten wurden, sind in Tabelle 2 zusammengefasst. Der Hauptunterschied der mit diesen beiden Techniken gemessenen Größen ist auf das Vorhandensein einer Adsorptionsschicht aus OA und OAm auf der Oberfläche des . zurückzuführen Partikel [35]. Organische Verbindungen wie OA und OAm erschienen aufgrund der Elektronendurchlässigkeit nicht in TEM-Bildern (Abb. 1). Da die Kettenlängen von OA und OAm ungefähr 2 nm betragen [36, 37], ist die Größe von CoFe2 O4 Das vom TEM geschätzte @Ag ist geringfügig (ca. 4 nm) größer als das vom DLS. Andererseits ist es vernünftig, dass die Größe von CoFe2 O4 durch den DLS ist weit größer als die Schätzung aus dieser Annahme. Diese Ergebnisse legen nahe, dass CoFe2O4-Nanopartikel in Hexan agglomeriert sind. Dieser Faktor beinhaltet nicht nur den Größeneffekt der oben beschriebenen Partikel, sondern auch die geringe Affinität zwischen den CoFe2 O4 Oberflächen und die Schutzmittel. Die Agglomerationstendenz des CoFe2 O4 kann nicht nur auf den Größeneffekt der oben beschriebenen Partikel zurückzuführen sein, sondern auch auf die geringe Affinität zwischen den CoFe2 O4 Oberflächen und die Schutzmittel. Ausfällung von CoFe2 O4 Nanopartikel wurden viel häufiger beobachtet als CoFe2 O4 @Ag-Nanopartikel im Prozess der Redispergierung durch Erhöhung der Anzahl der Methanolwaschvorgänge. Die hohe Monodispersität von CoFe2 O4 @Ag wird stark durch den niedrigen Polydispersitätsindex (PDI) gestützt, der durch die DLS-Messungen erhalten wurde [38]. Diese Ergebnisse zeigen, dass die Beschichtung mit Ag dem CoFe2 . nicht nur eine optische Funktion, sondern auch die Stabilität in Lösung verleiht O4 Nanopartikel.
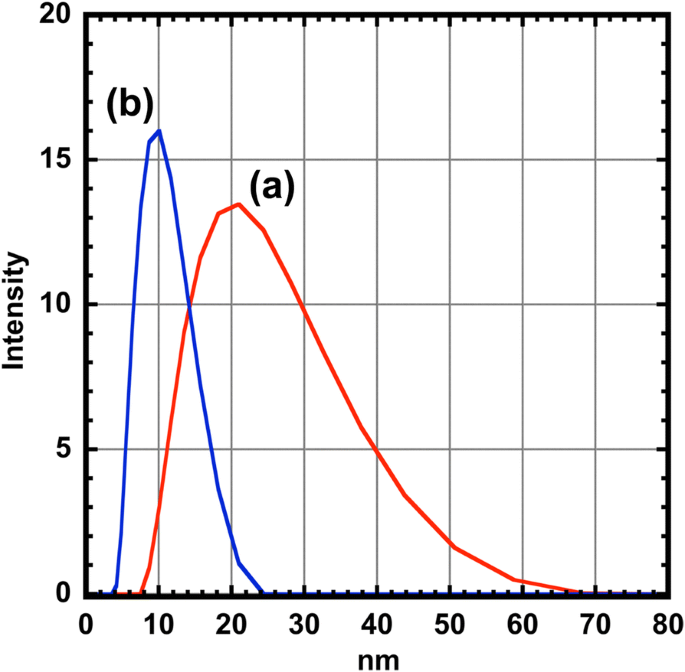
Größenverteilung (a ) des CoFe2 O4 (rote Linie) und (b ) das CoFe2 O4 @Ag-Nanopartikel (blaue Linie) gemessen mit DLS
Schlussfolgerungen
Das CoFe2 O4 Es wurde festgestellt, dass @Ag-Nanopartikel, die durch einen einfachen und schnellen Eintopfprozess synthetisiert wurden, auf einer einheitlichen Kern-Schale-Struktur mit einer engen Größenverteilung aus TEM-Bildern gebildet werden (Abb. 6). Außerdem zeigten diese Nanopartikel eine Multifunktionalität bestehend aus der plasmonischen Lichtauslöschungseigenschaft und einem superparamagnetischen Verhalten bei Raumtemperatur. Darüber hinaus zeigten die Kern-Schale-Nanopartikel ein höheres H c als CoFe2 O4 Nanopartikel bei 5 K und 300 K. Darüber hinaus behielten diese Nanopartikel in einem organischen Lösungsmittel eine hohe Monodispersität bei. Die nach dem einfachen Verfahren synthetisierten einheitlichen Nanopartikel haben aufgrund der Multifunktionalität sowie der Stabilität ein großes Potenzial in verschiedenen Bereichen.
Abkürzungen
- DLS:
-
Dynamische Lichtstreuung
- fcc:
-
Kubisch flächenzentriert
- H c :
-
Zwangsfeld
- M s :
-
Magnetische Sättigung
- OA:
-
Ölsäure
- OAm:
-
Oleylamin
- PDI:
-
Niedriger Polydispersitätsindex
- SQUID:
-
Supraleitendes Quanteninterferenzgerät
- TEM:
-
Feldemissions-Transmissionselektronenmikroskopie
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Multifunktionale Goldnanopartikel für verbesserte diagnostische und therapeutische Anwendungen:Eine Übersicht
- Herstellung und magnetische Eigenschaften von kobaltdotierten FeMn2O4-Spinell-Nanopartikeln
- Biogene Synthese, Charakterisierung und Bewertung des antibakteriellen Potenzials von Kupferoxid-Nanopartikeln gegen Escherichia coli
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Einfache Synthese von farbigen und leitfähigen CuSCN-Kompositen, die mit CuS-Nanopartikeln beschichtet sind
- Die Wirkung von Kontakt-Nichtgleichgewichtsplasma auf die strukturellen und magnetischen Eigenschaften von Mn Х Fe3 − X О4 Spinellen
- Synthese und Lumineszenzeigenschaften wasserlöslicher α-NaGdF4/β-NaYF4:Yb,Er Kern-Schale-Nanopartikel
- Nachbehandlungsmethode zur Synthese monodisperser binärer FePt-Fe3O4-Nanopartikel
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Auswirkung der Synthesemethode von La1 − xSr x MnO3 Manganit-Nanopartikeln auf ihre Eigenschaften



