Neuartige Abgabe von Mitoxantron mit hydrophob modifizierten Pullulan-Nanopartikeln zur Hemmung von Blasenkrebszellen und der Einfluss der Nanowirkstoffgröße auf die Hemmwirkung
Zusammenfassung
Die Reduzierung der Dosierung von Chemotherapeutika durch die Erhöhung der Abgabeeffizienz mit neuartigen Nanopartikeln hat großes Potenzial für die Krebsbehandlung. Hier konzentrierten wir uns auf die Verbesserung der Mitoxantronabgabe durch die Verwendung von Cholesterin-substituierten Pullulan-Polymeren (CHPs) und wählten eine geeignete Nanowirkstoffgröße aus, um das Wachstum von Blasenkrebszellen zu hemmen. Wir synthetisierten drei Arten von CHPs, genannt CHP-1, CHP-2, CHP-3. Ihre chemischen Strukturen wurden durch NMR identifiziert und der Grad der Cholesterinsubstitution betrug 6,82 %, 5,78 % bzw. 2,74 %. Ihre Durchmesser betrugen 86,4, 162,30 und 222,28 nm. Wir testeten die Freisetzungsrate von Mitoxantron in phosphatgepufferter Kochsalzlösung für 48 Stunden:Die Freisetzungsrate betrug 38,73 %, 42,35 % und 58,89 % für die drei BHKW. Der hydrophobe Substitutionsgrad im Polymer war mit dem Selbstorganisationsprozess der Nanopartikel verbunden, der sich auf ihre Größe und damit auf die Wirkstofffreisetzungsrate auswirkte. Die Freisetzung der drei arzneimittelbeladenen Nanopartikel wurde in Säurefreisetzungsmedien signifikant beschleunigt. Je größer die Nanopartikel, desto höher die Freisetzungsgeschwindigkeit des Arzneimittels. Um 24 Uhr ist der IC50 Der Wert betrug 0,25 M für die beste Hemmung von Mitoxantron auf Blasenkrebszellen.
3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazoliumbromid (MTT)-Experimente zeigten, dass arzneimittelbeladene CHP-3-Nanopartikel mit der größten Größe für Blasenkrebs am toxischsten waren Zellen. Immunfluoreszenz und Durchflusszytometrie zeigten, dass arzneimittelbeladene CHP-3-Nanopartikel mit der größten Größe die stärkste Wirkung auf die Förderung der Apoptose von Blasenkrebszellen hatten. Außerdem könnten die drei mit Wirkstoffen beladenen Nanopartikel alle die Migration von MB49-Zellen hemmen, wobei großformatige CHP-3-Nanopartikel die stärkste Hemmung aufweisen.
Hintergrund
Die Chemotherapie ist eine gängige Behandlung von Tumoren. Aufgrund der fehlenden Gewebespezifität ist die therapeutische Wirkung der Chemotherapie jedoch begrenzt und hat oft starke Nebenwirkungen [1, 2]. Daher hat die Forschung zur Verwendung von Nanopartikel-(NP)-Präparaten zur Steigerung der Zielfähigkeit von Chemotherapeutika zugenommen [3,4,5].
Nanowirkstoffe wie NP-beladene niedermolekulare Anti-Tumor-Medikamente entfalten ihre Wirksamkeit nach dem passiven Targeting von Tumorgeweben über den Effekt der verbesserten Permeabilität und Retention (EPR) hauptsächlich auf zwei Arten:(1) indem sie in Tumorgewebe freigesetzt werden und in das Zellen in freier Form, um eine Wirksamkeit auszuüben, und (2) indem sie von Zellen in Form von Mikropartikeln aufgenommen und in der Zelle freigesetzt werden, um pharmakodynamische Wirkungen auszuüben [6, 7]. Wenn ein Nanopharmazeutikum passiv auf einen Tumor gerichtet wird, welche der beiden Methoden eine große Rolle spielt oder ob beide gleichzeitig eine große Rolle spielen und ob noch andere Faktoren eine Rolle spielen, ist eine komplexe Frage. Aufgrund der metabolischen Aktivität von Tumorgeweben, Ischämie und Hypoxie und der Ansammlung von Milchsäure und weil die extrazelluläre Flüssigkeit von Tumorgeweben eine schwache Acidität zeigt, zeigen viele Nanoarzneimittel eine erhöhte Freisetzung in saurer Umgebung, um die Wirksamkeit zu verbessern [8]. Die Wirksamkeit der Wirkstofffreisetzung von Nanowirkstoffen in einer sauren Umgebung hängt eng mit den physikalisch-chemischen Eigenschaften von Nanomaterialien zusammen und wird auch von der Größe der Nanopartikel beeinflusst [9,10,11]. Nachdem die NPs passiv auf das Tumorgewebe zielen, da die Tumorzellen eine Phagozytosefunktion haben, gelangt das nanopharmazeutische Präparat hauptsächlich über Pinozytose und komplexe Prozesse, die durch die Zellmembranproteine vermittelt werden, in die Zellen [12, 13]. Unter dem Abbau von intrazellulären Lysozymen setzen Nanopharmazeutika Medikamente frei und entfalten ihre Wirkung [14].
Die Aufnahmeeffizienz von Zielzellen in Zielgewebe hängt eng mit den Eigenschaften von Nanomaterialien, Oberflächenmodifikation, Morphologie, Ladung und NP-Größe zusammen [15,16,17,18]. Die Zellaufnahme hängt in hohem Maße von der NP-Größe ab. Die Internalisierung (Endozytose) von Her-Gold-NPs hängt stark von der Größe ab, wobei die effektivste Absorption bei NPs im Bereich von 25 bis 50 nm stattfindet [19]. Extrem kleine oder große NPs haben eine ineffiziente Absorption. Die Größe von 40 bis 50 nm ist der kritische Punkt für die rezeptorvermittelte Endozytose [20]. Darüber hinaus beeinflusst die NP-Größe die Zytotoxizität. Beim Vergleich von NPs von 45 und 90 nm steht die Größe der Polymer-NPs im umgekehrten Verhältnis zur Zytotoxizität [21]. Die Größe der NPs beeinflusst die Freisetzung des Wirkstoffs im Tumorgewebe sowie die Aufnahmeeffizienz der Zellen und spielt letztendlich eine wichtige Rolle bei der Wirksamkeit des Wirkstoffs.
Die lokale Adhäsion von Polysacchariden verbessert die Lokalisierungs- und Targeting-Funktion. Die saure Umgebung externer Krebszellen führt zu einer teilweisen Freisetzung von Polysaccharid-Nanoarzneimitteln, was die duale therapeutische Wirkung von arzneimittelbeladenen NPs und freien Arzneistoffen nach passivem Targeting auf Tumorgewebe auslöst [22, 23].
Pullulan, das nicht toxisch ist, wird im Körper leicht abgebaut, und sein Cholesterin ist eine körpereigene Substanz, daher ist es sicher und als Träger für Medikamente geeignet [24, 25]. Hydrophob modifizierte Cholesteryl-Pullulan(CHP)-Polymere, die hydrophobe Cholesterylgruppen und hydrophile Zuckerketten aufweisen, können sich selbst zu nanosphärenartigen Strukturen mit hydrophoben zentralen Kernen und hydrophilen Hüllen anordnen [26, 27]. Amphiphile Polymere ordnen sich selbst zu NPs in Sphäroidstrukturen an, wobei der hydrophobe Kern von hydrophoben Gruppen wie Cholesterylgruppen gebildet wird [28].
Mitoxantron, ein krebshemmendes Breitspektrum-Anthrazyklin-Antibiotikum, das DNA interkalieren und die Topoisomerase II hemmen kann, ist ein klassisches Antitumor-Medikament. Aufgrund seiner Kardiotoxizität ist die Verwendung von Mitoxantron jedoch begrenzt. Mitoxantron wird durch hydrophobe Wechselwirkung auf das hydrophobe Zentrum von CHP-NPs geladen, um CHP-Nanometer-Präparate zu bilden, die über den EPR-Effekt einen passiven Targeting-Effekt aufweisen. Im Vergleich zu freien Arzneimitteln zeigen arzneimittelbeladene CHP-NPs reduzierte toxische Wirkungen von Arzneimitteln und eine erhöhte Wirksamkeit gegen Krebs [29, 30]. Die hydrophobe Gruppe Cholesterin im CHP-Polymer treibt die Bildung der Kernstruktur des NP an, und innerhalb eines bestimmten Bereichs gilt:Je höher der Substitutionsgrad der hydrophoben Gruppe, desto kleiner die Größe des NP [31, 32]. Die Stabilität von CHPs war für mindestens 2 Monate ohne signifikante Veränderungen der Größe und des Zetapotenzials überlegen, und Pullulan-Nanopartikel können in Tumorgewebe zielen, um Krebszellen durch EPR-Effekt abzutöten [33, 34].
In dieser Studie verwendeten wir Pullulan(CHP)-NPs, die mit Cholesterin hydrophob modifiziert wurden, als Antitumor-Wirkstoffträger, um Mitoxantron zu beladen. Verschiedene Größen von Mitoxantron-beladenen Pullulan-NPs wurden durch die Synthese von CHP-Polymeren in verschiedenen Bernsteinsäureanhydrid-Cholesterinester (CHS)-Ladungsverhältnissen erzeugt, um die Wirkung der NP-Größe auf die anhaltende Freisetzung eines Arzneimittels, die Arzneimittelfreisetzung in einer sauren Umgebung und die Toxizität für Blasenkrebs zu untersuchen Zellen, Zellaufnahmeeffizienz und Zellmigration. In diesem Experiment wurde der Größenbereich von NPs mit passivem Targeting untersucht, um einen geeigneten NP als Wirkstoffträger und eine stärkere Wirkstoffeffizienz zu screenen.
Materialien und Methoden
Reagenzien und Instrumente
Mitoxantron stammte von Aladdin Chemistry (Shanghai); der Dialysebeutel (BioSharp, USA, 8000–12.000 Da) stammte von Tianjin Junyao Biotechnology. Andere Reagenzien stammten von Beijing Xinze Technology.
Wir verwendeten das Japan F-4500 Fluorescence Spectrophotometer, J-810 Circulardichroism Chromatograph (Jasco Co., Japan), einen Partikelgrößenanalysator (MALVERN, Nano 2S-90, Japan) und ein Projektionselektronenmikroskop (JEM-100CXII, Japan). .
Synthese und Charakterisierung von CHP-Polymer und Berechnung des Substitutionsgrads von Cholesterin
Über die Synthese von Bernsteinsäureanhydrid CHS wurde bereits berichtet [35]. Eine Menge von 0,5 g Pullulanprobe wurde in 15 ml dehydratisiertem Dimethylsulfoxid als Reserve gelöst. CHS (Zuckereinheit/CHS = 0,20, 0,15, 0,05 mmol/mmol), 4-Dimethylpyridin (DMAP∕CHS = 1 mmol/mmol) und 1-(3-Dimethylaminopropyl)-3-ethyl-carbodiimid-Hydrochlorid (EDC∕ .) CHS = 1,2 mmol/mmol) wurden separat in 10 ml DMSO gelöst, bei Raumtemperatur gerührt und 1 h aktiviert; die Aktivierungsreaktion wurde in die Pullulanlösung getropft; und die Reaktion wurde nach 48 h gestoppt. Die Reaktion wurde in 200 ml absolutes Ethanol getropft und dann bildete sich ein weißer Niederschlag. Das Filtrieren erfolgte durch Absaugen und das Produkt wurde mit geeigneten Mengen an Ethanol, Tetrahydrofuran und Diethylether gewaschen und dann bei 80 °C getrocknet. Es wurden drei Arten von CHP-Polymeren mit unterschiedlichen Graden der Cholesterinsubstitution erhalten:CHP-1, CHP-2 und CHP-3 [36]. Pullulan-Polysaccharid und CHP-Polymer 10–20 mg wurden mit DMSO-d6 unter Ultraschallbedingungen gelöst und 1 H-NMR-Spektren wurden untersucht. Der Substitutionsgrad von Cholesterin im CHP-Polymer wurde auf der Grundlage der glykosidischen α-1,4- und α-1,6-Bindungen und der Fläche unter dem Methylenpeak bestimmt.
Herstellung und Charakterisierung von wirkstoffbeladenen CHP-NPs
Synthese von Mitoxantron-beladenen CHP-NPs wie beschrieben [37, 38], Wirkstoff-beladene NPs wurden durch Dialyse mit 40 mg von jedem der drei CHP-NPs, die mit verschiedenen Cholesterinwerten substituiert waren, und 4 mg Mitoxantron als Backup erhalten. Die neu hergestellten wirkstoffbeladenen NPs oder die nach der Lyophilisierung in destilliertem Wasser dispergierten Wirkstoff-beladenen NPs wurden auf ein Kupfergitter mit einem Kohlenstoffträgerfilm getropft, und das Filterpapier wurde entwässert. Gitter wurden in einen Exsikkator gelegt, dann 2% (w /w ) wurde Phosphowolframsäure (2%) zugegeben, die nach natürlicher Trocknung negativ war und durch Transmissionselektronenmikroskopie (TEM) beobachtet wurde [38]. Die Lösung neu hergestellter arzneimittelbeladener NPs oder arzneimittelbeladener NPs, die nach der Lyophilisierung in destilliertem Wasser dispergiert waren, wurde in Küvetten gegossen und zum Nachweis in einen Partikelgrößenanalysator gegeben. Jede Probe wurde dreimal verarbeitet, um eine gleichmäßige Größe und ein gleichmäßiges Potenzial von NPs zu erhalten.
Messung der Wirkstoffbeladung und Verkapselungseffizienz von Wirkstoff-beladenen KWK-NPs
Der Wirkstoffbeladungsgehalt (LC%) und die Verkapselungseffizienz (EE%) von Mitoxantron-beladenen CHP-NPs wurden wie folgt gemessen [31, 39]:
$$ \mathrm{EE}=\frac{\mathrm{Der}\ \mathrm{Betrag}\ \mathrm{of}\ \mathrm{Droge}\ \mathrm{in}\ \mathrm{der}\ \mathrm{ NPs}}{\mathrm{Gesamt}\ \mathrm{Betrag}\ \mathrm{of}\ \mathrm{Droge}} $$ $$ \mathrm{LC}=\frac{\mathrm{The}\ \mathrm{ Betrag}\ \mathrm{von}\ \mathrm{Droge}\ \mathrm{in}\ \mathrm{der}\ \mathrm{NPs}}{\mathrm{Der}\ \mathrm{Betrag}\ \mathrm{von }\ \mathrm{NPs}\ \mathrm{Gewicht}} $$Studie zur Arzneimittelfreisetzung
Die drei Arten von Mitoxantron-beladenen NPs wurden in Phosphat-gepufferte Kochsalzlösung (PBS) und in Freisetzungsmedien mit pH =6,8 und 4,0 platziert. Die Mitoxantronfreisetzung wurde in vitro durch Dialyse untersucht und der kumulierte Freisetzungsprozentsatz (Q%) wurde wie beschrieben berechnet [40].
Zelllinien und Kulturbedingungen
Die von Dr. P. Guo (Institut für Urologie, Xi'an Jiaotong University, Xi'an, Shaanxi, China) bereitgestellte Blasenkrebszelllinie MB49 wurde in DMEM (Lonza), ergänzt mit 10 % fötalem Rinderserum (Hyclone, Logan .) kultiviert , UT, USA) und 1 % Penicillin-Streptomycin bei 37 °C in befeuchteter Luft mit 5 % CO2 .
Zelllebensfähigkeitstest
Die Lebensfähigkeit der Zellen wurde durch einen auf Tetrazolium basierenden Assay bewertet. Kurz gesagt, Zellen wurden bei 2 × 10 4 . ausgesät pro Well in 96-Well-Kulturplatten und wurden 24 h anhaften gelassen. Zu Beginn der Versuche wurden unterschiedliche Saatdichten optimiert. Die Zellen wurden 24 h lang in einem Inkubator mit unterschiedlichen Konzentrationen von Mitoxantron behandelt. Mitoxantron mit 0,0078, 0,0156, 0,03125, 0,0625, 0,125, 0,25, 0,5 und 1 μM wurde in DMEM, ergänzt mit 1 % fötalem Rinderserum, gelöst. Eine Menge von 50 μL MTT-Tetrazoliumsalz (Sigma), gelöst in Hanks ausgewogener Lösung mit 2 mg/ml, wurde mit der angegebenen Behandlung in jede Vertiefung gegeben und in einem CO2 . inkubiert Inkubator für 5 h. Schließlich wurde das Medium aus jeder Vertiefung abgesaugt und 150 μL DMSO (Sigma) wurden zugegeben, um Formazankristalle aufzulösen. Die Extinktion jedes Wells wurde unter Verwendung eines Dynatech MR5000 Plattenlesegeräts bei einer Testwellenlänge von 490 nm und einer Referenzwellenlänge von 630 nm erhalten.
IC50 Werte für Mitoxantron wurden durch Dosis-Wirkungs-Kurven bestimmt. Die drei Konzentrationen von NP (0,0625, 0,125, 0,25 μM) mit drei Substitutionsgraden wurden durch MTT verglichen. Das experimentelle Verfahren war das gleiche wie für Mitoxantron.
Bewertung der Apoptose
Die Zellapoptoserate wurde durch Durchflusszytometrie mit Annexin V-FITC/Propidiumiodid (PI) bestimmt. Kurz gesagt, die behandelten Zellen wurden zweimal mit kaltem PBS gewaschen, dann in Bindungspuffer bei 2 × 10 6 . resuspendiert Zellen/ml gemäß den Anweisungen des Herstellers. Anschließend wurden 5 μL Annexin V-FITC und 5 μM PI in eine 100-μL-Zellsuspension gegeben und 30 min bei Raumtemperatur im Dunkeln inkubiert. Nach Zugabe von 300 μl Bindungspuffer wurden markierte Zellen innerhalb von 1 h durch Durchflusszytometrie nachgewiesen.
Alle frühen apoptotischen Zellen (Annexin V-FITC – positiv [grün gefärbt], PI-negativ), nekrotische Zellen (Annexin V-FITC – negativ, PI-positiv), spät apoptotische Zellen (doppelt positiv) sowie lebende Zellen ( doppelt negativ) wurden durch Durchflusszytometrie (FCM) nachgewiesen und unter Verwendung der Cell Quest Software (Becton Dickinson) analysiert. Die Anregungswellenlänge des Argonlasers betrug 488 nm und die Emissionswellenlänge 530 nm (FL-1-Kanal) für Fluoresceinisothiocyanat (FITC) und 670 nm (FL-3 c3-Kanal) für PI. Außerdem wurde die Apoptose durch Fluoreszenzmikroskopie untersucht. Zuerst 1,0 × 10 5 Zellen wurden in 96-Well-Kulturplatten ausgesät und nach 24 h wurden die Zellen wie oben behandelt, dann 24 h später 100 μL Bindungspuffer, 1 μL Annexin V-FITC und 1 μLPI wurden den Zellen bei Raumtemperatur im Dunkeln zugesetzt 15 Minuten lang bei niedriger Temperatur gehalten und fluoreszenzmikroskopisch beobachtet.
Zellmigrations-Assay
Insgesamt 8 × 10 5 Zellen wurden in Sechs-Well-Platten ausgesät und konnten volle Konfluenz erreichen. Der Monolayer wurde mit einem Cocktailstäbchen verwundet. Die Zellen wurden wie angegeben mit serumfreiem DMEM inkubiert. Digitale Bilder wurden nach 0, 6, 12, 24 und 48 Stunden aufgenommen. Die mittlere Fläche wurde unter Verwendung von Bild J berechnet und die Experimente wurden dreimal wiederholt.
Ergebnisse und Diskussion
CHP-Konjugate und Substitutionsgrad von Cholesterin
Die 1 Der H-NMR-Wert für CHP (DMSO-d6 mit TMS, ppm) betrug 2,53 ppm (2 Methylengruppen, –OCH2 .) CH2 Ö-). Abbildung 1 zeigt 1 H-NMR-Spektren, die bestätigen, dass Cholesterin über einen Bernsteinsäure-Abstandsarm chemisch an die lange Pullulankette gebunden war. Die Spektren für die drei CHP-NPs, die bei unterschiedlichen Zufuhrverhältnissen (a, b, c) synthetisiert wurden, zeigten die charakteristischen Peaks von Pullulan; α-1-4 und α-1,6 glykosidische Bindungen waren ∂4.68 (1Hα1–6 ), ∂5.05 (1Hα1–4 ) und ∂2.53 (2 Methylengruppen, –OCH2 CH2 O–), die ebenfalls leicht zu unterscheiden war. Neue charakteristische Peaks erschienen bei 0,40 bis 2,40 (Wasserstoff am cholesterischen Gerüst), was bestätigte, dass die drei CHP-Polymere erfolgreich synthetisiert wurden. Die Fläche unter dem Peak spiegelt die Anzahl der Atome wider, und der Grad der cholesterischen Substitution kann wie folgt berechnet werden [41]:
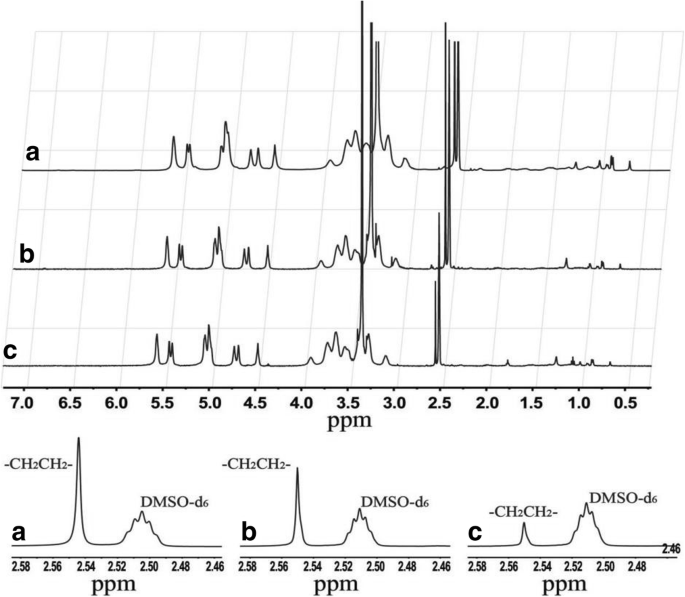
NMR-Spektren für CHP-1 (a ), BHKW-2 (b ) und BHKW-3 (c )
$$ \mathrm{DS}=\frac{A_{\partial 2.53}}{4\left({A}_{\partial 4.68}+{A}_{\partial 5.05}\right)}\mal 100\ % $$wobei die Summe von A ∂4,68 und A ∂5.05 steht für die Anzahl der Zuckereinheiten, A∂ 2,53 ist die Anzahl der Wasserstoffatome in –OCH2 CH2 O– der Cholesterylbernsteinsäure und A∂ 2,53 /4 ist die Zahl von –OCH2 CH2 O–, d. h. die Zahl der Cholesterine im Bernsteinsäureanhydrid CHS. Somit stellt die obige Formel den Grad der cholesterischen Substitution im CHP-Molekül als die Anzahl der Cholesterylgruppen pro 100 Glucoseeinheiten dar. Die berechneten Futterverhältnisse und Molverhältnisse der Cholesteryl- und Pullulanzuckereinheiten betrugen 1/5, 3/20 bzw. 1/20, und der Substitutionsgrad der drei synthetisierten CHP-1, CHP-2 und CHP-3 Polymere betrug 6,82 %, 5,78 % bzw. 2,74 %. Der Substitutionsgrad von Cholesterin an der Pullulankette nahm mit steigender Futtermenge zu. Der tatsächliche Substitutionsgrad war jedoch niedriger als bei beiden Futterverhältnissen.
Die Pullulankette kann im Lösungsmittel als flexible, gewundene Kette vorliegen, und nach Zugabe einer bestimmten Menge Cholesterin zeigt das gepfropfte Cholesterin eine größere molekulare sterische Hinderung, die die weitere direkte Veresterungsreaktion von Succinylcholesterin und der Hydroxylgruppe beeinflusst an der Pullulankette. Die Schwierigkeit der Reaktion wurde deutlich erhöht, so dass der Substitutionsgrad kleiner wurde.
Drogenbeladene KWK-NPs und ihre Größe
Die Größen der drei leeren CHP-NPs für CHP-1, CHP-2 und CHP-3 betrugen 79,1, 104,9 und 166,8 nm. Bei einem bestimmten Substitutionsgrad verstärkt sich die Hydrophobie mit steigendem Substitutionsgrad des Cholesterins. Je stärker die Hydrophobie, desto besser bildeten die selbstaggregierten CHP-NPs einen kompakteren hydrophoben Kern, was die Größe der NPs verringerte [42]. Abbildung 2 zeigt die Größe von arzneimittelbeladenen CHP-NPs. Die Partikelgrößen für CHP-1, CHP-2 und CHP-3 betrugen 86,4, 162,30 bzw. 222,28 nm. Im gleichen Verhältnis von Wirkstoffen und Materialien war die Partikelgröße des Wirkstoff-beladenen NP mit einem hohen Substitutionsgrad der hydrophoben Polymergruppe klein, aber der Partikeldurchmesser des Wirkstoff-beladenen NPs war größer als der des nicht-eingekapselten Wirkstoffs -enthaltende leere NP mit dem gleichen Substitutionsgrad. Wenn Mitoxantron in den hydrophoben Kern eindringt, wird die Partikelgröße der NPs erhöht. In Abb. 2d beträgt das Zetapotential der wirkstoffbeladenen CHP-NPs − 1,12 mV. Abb. 2e ist ein TEM-Bild, das zeigt, dass die arzneimittelbeladenen NPs kugelförmig sind.
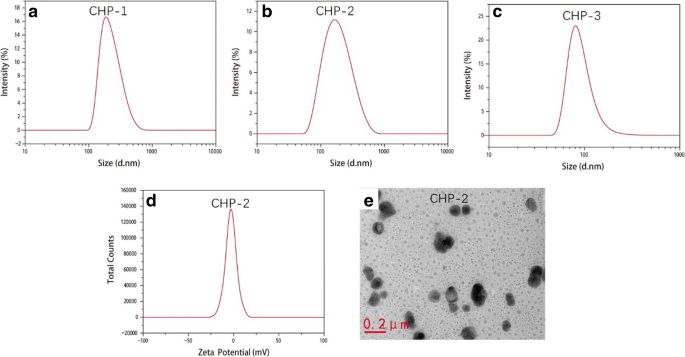
Bilder der mit Mitoxantron beladenen NP-Größe (CHP-1 (a ), BHKW-2 (b ), BHKW-3 (c )), potenzielle Bilder (CHP-2 (d )) und TEM-Bilder (CHP-2 (e ))
Wirkstofffreisetzung von NPs unterschiedlicher Größe und unter verschiedenen sauren Medien
Wenn die Verhältnisse von Wirkstoff und CHP-Polymer gleich waren, betrug die Wirkstoffbeladungs- und Einschlusseffizienz der Wirkstoff-beladenen CHP-1-, CHP-2- und CHP-3-NPs 8,17% und 88,92%; 7,62 % und 82,28 %; und 4,83% bzw. 50,67%. Je höher die cholesterische hydrophobe Substitution im CHP-Polymer ist, desto kleiner ist die gebildete Teilchengröße und desto höher die Wirkstoffbeladung und Einschlusseffizienz. Abbildung 3 zeigt die Wirkstofffreisetzungsprofile für die drei wirkstoffbeladenen CHP-NPs. Bei PBS wurde das Medikament 48 Stunden lang freigesetzt. Die Freisetzungsraten für CHP-1, CHP-2 und CHP-3 betrugen 38,73 %, 42,35 % bzw. 58,89 %. Alle drei NPs zeigten anhaltende Freisetzungseigenschaften, aber je kleiner die NP-Größe, desto stärker die Hydrophobie und desto langsamer die Wirkstofffreisetzung. Bei pH 6,8 betrugen die Wirkstofffreisetzungsraten für CHP-1, CHP-2 und CHP-3 43,82 %, 49,48 % bzw. 64,18 %. Unter schwach sauren Bedingungen setzten CHP-NPs das Medikament nachhaltig frei, die Freisetzungsrate stieg jedoch deutlich an. Bei pH 4,0 betrugen die Wirkstofffreisetzungsraten für CHP-1, CHP-2 und CHP-3 nach 48 h Wirkstofffreisetzung 51,25 %, 56,23 % bzw. 75,46 %. Die Freisetzung des CHP NP-Medikaments war bei niedrigeren pH-Werten signifikant schneller, insbesondere bei CHP-3 NP, dem größten der drei CHP NPs.
Mitoxantron (MTO)-Freisetzung aus Pullulan-NPs in phosphatgepufferter Kochsalzlösung (schwarzes Quadrat:CHP-1, weißer Kreis:CHP-2, schwarzes nach unten zeigendes Dreieck:CHP-3), bei pH 6,8 (weißes nach oben zeigendes Dreieck:CHP- 1, schwarze Raute:CHP-2, weißes Quadrat:CHP-3) und bei pH 4,0 (schwarzes Dreieck:CHP-1, weiße Raute:CHP-2, schwarzer Kreis:CHP-3) bei 37 °C in vitro
Zytotoxizität von Mitoxantron-beladenen KWK-NPs
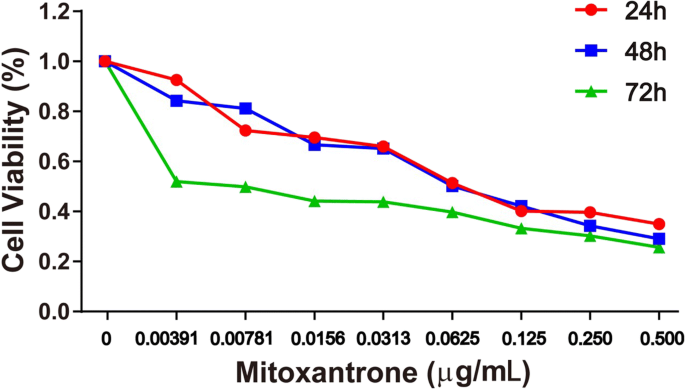
Beim MTT-Assay (Abb. 4) beträgt der IC50 die Werte für Mitoxantron zur Hemmung des Wachstums von Blasenkrebszellen betrugen 0,25, 0,20 und 0,06 μM nach 24, 48 bzw. 72 h (Tabelle 1). Als Dosierzeit haben wir 24 h angenommen.

Wirkung einer Behandlung mit Mitoxantron und NPs auf die Zellproliferation der Blasenkrebszelllinie MB49. Die Lebensfähigkeit der Zellen wurde durch einen auf Tetrazolium basierenden Assay mit 24-, 48- und 72-stündiger Behandlung mit Mitoxantron und Nano-Medikamenten von 0 bis 0,5 μg/ml an der murinen Blasenkrebszelllinie MB49 bewertet
Da die Konzentration von freiem Mitoxantron und Mitoxantron-CHP-NP bei derselben Verabreichung gleich ist, zeigen die Ergebnisse der MTT-Experimente in Abb. 5, dass die Konzentration von freiem Mitoxantron für Blasenkrebszellen toxischer war als Mitoxantron-CHP-NPs. Beim Vergleich der Mitoxantron-CHP-NPs mit den drei Cholesterin-Substitutionsgraden war die stärkste zytotoxische Wirkung CHP-3, gefolgt von CHP-2 und die schwächste war CHP-1.
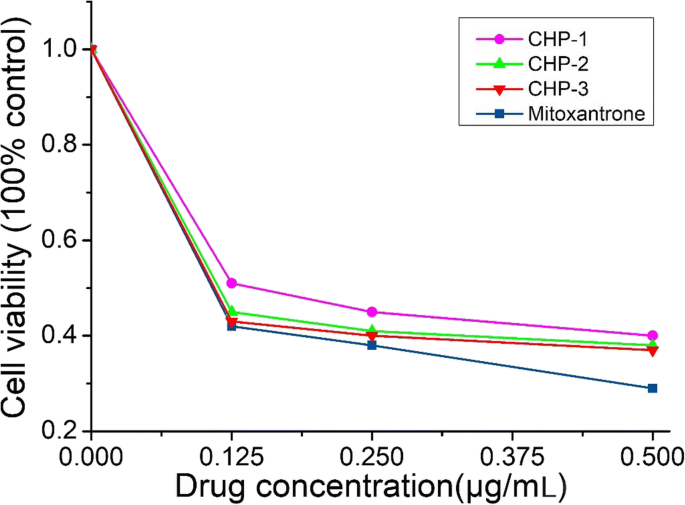
Zytotoxizität von freiem Mitoxantron und Mitoxantron-beladenen CHP-NPs nach 24 h (blaues Quadrat:Mitoxantron, rosa Kreis:CHP-1, grünes Dreieck:CHP-2, rotes nach unten zeigendes Dreieck:CHP-3)
Obwohl die toxischen Wirkungen verschiedener Konzentrationen von Mitoxantron-CHP-NPs auf Blasenkrebszellen ähnlich waren, insbesondere CHP-2 und CHP-3, war die Wirkung von CHP-1 signifikant reduziert. Jede Konzentration von CHP-1 zeigte dieses Phänomen. Somit ist die Zytotoxizität umso stärker, je größer die Mitoxantron-CHP-NP-Größe ist.
Die therapeutische Wirkung von NPs besteht aus zwei Teilen:(1) der zellulären Aufnahme von NPs und (2) der Freisetzung von NPs außerhalb der Zelle und dem freien Eintritt von Medikamenten in die Zellen, um ihre Wirksamkeit zu entfalten. Da freies Mitoxantron eine stärkere Wirkung hat als Mitoxantron-CHP-NPs, hatte CHP-3 bei gleicher Arzneimitteldosis eine stärkere therapeutische Wirkung als die anderen beiden CHP-NPs. Die Freisetzung von CHP-3 war am schnellsten, und die therapeutische Wirkung von CHP-NPs hing hauptsächlich von der Toxizität des freien Mitoxantrons in den Zellen nach Freisetzung des nanopharmazeutischen Präparats ab.
Zell-Apoptose von Mitoxantron-KWK-NPs
Wir haben Immunfluoreszenz und Durchflusszytometrie verwendet, um die Wirkung derselben Konzentration von 0,2 μg/ml Mitoxantron und der drei arzneimittelbeladenen CHP-NPs auf die Apoptose von MB49-Zellen zu vergleichen. Freies Mitoxantron war für die Apoptose stärker als die drei Mitoxantron-CHP-NPs (Abb. 6). CHP-3 hatte jedoch die stärkste Wirkung, und CHP-1 war die schwächste. Die vorherigen MTT-Ergebnisse wurden weiter bestätigt.
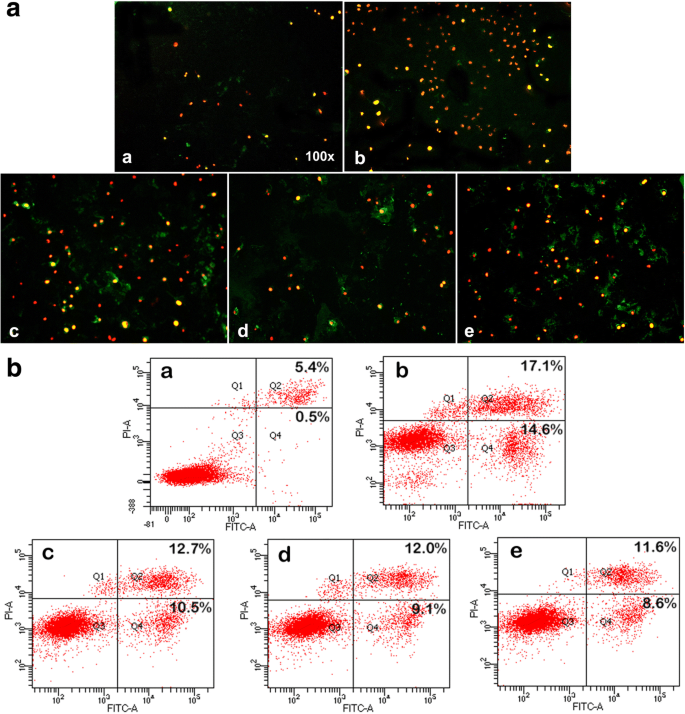
Apoptose von Mitoxantron und Nanodrugs nach 24 Stunden auf MB49-Blasenkrebszellen(a DMSO, b Mitoxantron, c BHKW-3, d BHKW-2, e CHP-1):A. Annexin V-FITC/PI-Doppelfärbung wurde durch Fluoreszenzmikroskopie nachgewiesen, frühe apoptotische Zellen zeigten Annexin V-FITC-positive Färbung (grün), nekrotische Zellen waren PI-positiv (rot) und spät apoptotische Zellen zeigte eine positive Doppelfärbung (gelb). B. Die Apoptoserate wurde durch FCM bestimmt. Lebende Zellen (Q3), frühe Apoptoserate (Q4), späte Apoptoserate (Q2), nekrotische Zellen (Q1). Je stärker die Zellfärbung, desto höher die Apoptoserate
Zellmigration von Mitoxantron-beladenen KWK-NPs
Die 24- und 48-Stunden-Fähigkeit von freiem Mitoxantron und den drei CHP-NPs, die MB49-Zellmigration zu hemmen, wurde im Vergleich mit Kontrollen beobachtet (Fig. 7). Die Migrationshemmung war für freies Mitoxantron nicht signifikant stärker als für die drei CHP-NPs. Beim MTT-Assay und Apoptose-Test war die Migrationshemmung für das freie Medikament stärker als für die drei CHP-NPs, hauptsächlich weil das freie Medikament leichter in die Zellen eindrang, um Krebszellen abzutöten. Auch im Zellmigrationsexperiment kann das freie Medikament die Zellmigration effizienter hemmen als CHP-Nanopharmazeutika, was daran liegen kann, dass einige CHP-Nanopharmazeutika nicht zwischen Zellen phagozytiert werden, was zu einer Migrationsresistenz von Krebszellen führt. Darüber hinaus unterschieden sich die drei CHP-NPs nicht in der Hemmung der Migration von Krebszellen, sodass die von den NPs gebildete sterische Resistenz eine wichtige Rolle bei der Zellmigration spielte. Daher hemmen arzneimittelbeladene CHPNPs Krebszellen auf zwei Arten:(1) Die extrazelluläre Freisetzung ist der vorherrschende Weg, wobei Nanowirkstoffe die Arzneistoffe außerhalb der Zellen freisetzen und Krebszellen als freie Arzneistoffe abtöten, wobei CHP-3-NPs toxischer sind als die anderen CHP-NPs und (2) CHP-NPs außerhalb von Krebszellen erzeugen sterische Resistenz und blockieren somit die Migration von Krebszellen.

Mitoxantron allein und mit Mitoxantron beladene KWK-NPs zeigten eine beeinträchtigte Migration bei Wundheilungstests. a DMSO, b Mitoxantron, c BHKW-3, d BHKW-2, e BHKW-1. Bilder zeigten die Lücke der zerkratzten Region zu verschiedenen Zeiten; A0 , A24 , und A48 stehen für 0, 24 bzw. 48 Stunden DMSO-Behandlung
Das Ziel dieser Studie war es, CHP-NPs geeigneter Größe als Wirkstoffträger zu screenen und experimentelle Beweise für die therapeutische Wirkung von CHP-NPs zu liefern. Wir synthetisierten drei Arten von sterolsubstituierten Pullulan-Polymeren (CHPs), CHP-1, CHP-2 und CHP-3 mit einem Cholesterin-Substitutionsgrad von 6,82 %, 5,78 % bzw. 2,74 % und einem Durchmesser von 86,4, 162,30 und 222,28 nm. Die Wirkstofffreisetzungsrate von drei Arten von Mitoxantron-CHP-NPs für 48 Stunden betrug 38,73 %, 42,35 % bzw. 58,89 %. Der hydrophobe Substitutionsgrad im Polymer wurde mit dem Selbstorganisationsprozess der NPs in Verbindung gebracht, der sich auf ihre Größe und damit auf die Wirkstofffreisetzungsrate auswirkte. In sauren Freisetzungsmedien wurde die Freisetzung signifikant beschleunigt. Je größer der NP, desto größer die Freisetzungsgeschwindigkeit des Arzneimittels. Um 24 Uhr ist der IC50 Der Wert betrug 0,25 M für die beste Hemmwirkung von Mitoxantron auf das Wachstum von Blasenkrebszellen. Arzneimittelbeladene CHP-3-NPs mit der größten Größe waren für Blasenkrebszellen am stärksten toxisch, und CHP-3-NPs hatten die stärkste Wirkung auf die Förderung der Apoptose der Zellen. Alle NPs konnten die Migration von MB49-Zellen hemmen, aber große CHP-3-NPs hatten die stärkste Hemmung.
Amphiphile Polymere können sich in wässrigen Lösungen selbst zu NPs zusammenlagern; Beispiele sind die Polysaccharide Pullulan und Chitosan, die durch hydrophobe Modifikation kleiner Moleküle zu amphiphilen Polymeren modifiziert und in wässrigen Lösungen zu kugelförmigen NPs mit hydrophoben Gruppen als Kern und hydrophilen Zuckerkettenhüllen selbstorganisiert werden können [43, 44]. Während der Selbstorganisation sind hydrophobe Gruppen die treibende Kraft für die Bildung von Nanopartikeln und der Schlüssel zur Bildung ihrer Hüllen- und Kernstruktur. Auch die Eigenschaften und das Molekulargewicht hydrophiler Gruppen haben einen wichtigen Einfluss auf die Bildung und Größe von NPs [45, 46]. Wenn das gleiche Polymer mit einem kleinen Anteil einer hydrophoben Gruppe modifiziert wird, sollte der Grad der hydrophoben Substitution moderat sein, und nur innerhalb eines bestimmten Bereichs kann die hydrophobe Substitution selbstorganisiert zu NPs werden. Wenn der Grad der hydrophoben Substitution zu hoch ist, ist die Hydrophobie des Polymers zu stark, was der Selbstorganisation nicht förderlich ist. Wenn die hydrophobe Substitution zu gering ist, ist die hydrophobe Triebkraft zu klein, um NPs zu bilden [47].
In dieser Studie synthetisierten wir erfolgreich drei Arten von CHP-Polymeren mit unterschiedlichen Substitutionsgraden von Cholesterin, indem wir ein geeignetes Zufuhrverhältnis entwickelten, und alle konnten sich selbst zu NPs einer bestimmten Größe anordnen. Während der Selbstorganisation von CHP-Polymeren können hydrophobe Wirkstoffe wie Mitoxantron in das hydrophobe Zentrum von NPs eingebettet werden, um Wirkstoff-beladene NPs zu bilden (Abb. 8). Die Größe der wirkstoffbeladenen NPs hängt vom Substitutionsgrad des Polymer-CHP ab:Je höher der Substitutionsgrad, desto kleiner die Größe. Der Substitutionsgrad von Polymeren beeinflusst auch die Menge an Wirkstoff, die nach der Selbstorganisation in die NPs geladen wird. Bei gleichem Verhältnis von Polymer zu Arzneistoff ist die Arzneistoffbelastung umso höher, je höher der Substitutionsgrad ist [48]. Auch das Verhältnis von Polymer zu Arzneimittel beeinflusst die Einkapselungseffizienz und die Arzneimittelbeladung. Nur wenn das Zufuhrverhältnis im richtigen Bereich liegt, sind die Wirkstoffbeladung und die Verkapselungseffizienz relativ hoch [31]. Die Wirkstofffreisetzung von NPs beeinflusst direkt ihre therapeutische Wirkung, die eng mit der Art der Nanomaterialien, der Oberflächenladung und der hydrophoben Gruppe der NPs, dem pH-Wert des Freisetzungsmediums und der Adsorption des Proteins Humanserumalbumin (HSA) in vivo zusammenhängt [49, 50]. Die Wirkstofffreisetzung von Mitoxantron-beladenen CHP-NPs zeigte eine langsame Freisetzung. Die Wirkstofffreisetzung von CHP-NPs mit großer Größe war schneller und die von NPs in einer sauren Umgebung war schneller. Die Wirkstofffreisetzungsrate größerer NPs war offensichtlicher und schneller.
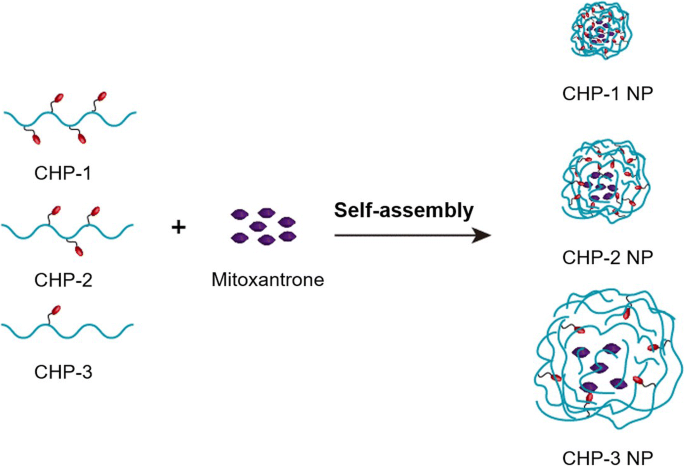
Die Selbstorganisation von Mitoxantron-beladenen CHP-Nanopartikeln (NPs)
Die Krebs-Chemotherapie ist derzeit die Hauptmethode zur Behandlung von Krebs, aber die Chemotherapeutika sind nicht gewebespezifisch und toxisch für normales Gewebe, und einige verursachen große Schäden an Immunzellen, was die Gesamtwirkung der Behandlung beeinträchtigt [51, 52]. Die Nanomedizin kann über den EPR-Effekt passiv auf Krebsgewebe abzielen, wodurch die Wirkstoffablagerung in Nicht-Zielgeweben reduziert und die Toxizität und Nebenwirkungen reduziert werden. In dieser Studie haben wir Blasenkrebszellen als Modellkrebszellen verwendet und die Auswirkungen der NPs und der NP-Größe auf Blasenkrebs diskutiert. Die Antitumorwirkung war für freies Mitoxantron stärker als für CHP-NPs; Wenn jedoch das gesamte Arzneimittel verabreicht wird, ist Mitoxantron nicht gewebespezifisch. Die Ablagerung und Verschwendung von Gewebe sowie die Toxizität und Nebenwirkungen dieser Medikamente werden nicht so wirksam sein wie Behandlungen mit Nanomedikamenten. Daher waren die toxischen Wirkungen auf Krebszellen und die Hemmung der Zellmigration mit dem freien Wirkstoff besser als mit Wirkstoff-beladenen NPs, was nicht darauf hindeutet, dass die therapeutische Gesamtwirkung von CHP-Nanometern nicht so gut ist wie die von freiem Mitoxantron. Wir weisen auf die Wirkung des hydrophoben Substitutionsgrads auf die Größe nanoskaliger Medikamente und die Wirkung der Nanogröße auf die Wirkstoffbeladung, Wirkstofffreisetzung, Zytotoxizität und Krebszellmigration hin. Nachdem die NPs über den EPR-Effekt passiv auf das Krebsgewebe gerichtet sind, wird die therapeutische Wirksamkeit von wirkstoffbeladenen NPs hauptsächlich von der Freisetzung von Wirkstoffen im Gewebe und der Freisetzung von NPs an Zellen abgeleitet (Abb. 9). Die therapeutische Wirkung von CHP-NPs besteht darin, ob ihre extrazelluläre oder intrazelluläre Freisetzung die dominierende Rolle spielt. Aus den Zellexperimenten geht hervor, dass die Größe von CHP-NPs einen starken Effekt hat:Bei größerer Größe werden mehr Medikamente freigesetzt, aber die Menge des Medikaments ist gleich. Daher kann die therapeutische Wirkung von CHP-NPs hauptsächlich von der Freisetzung im Gewebe und nicht von der Zellaufnahme abhängen.
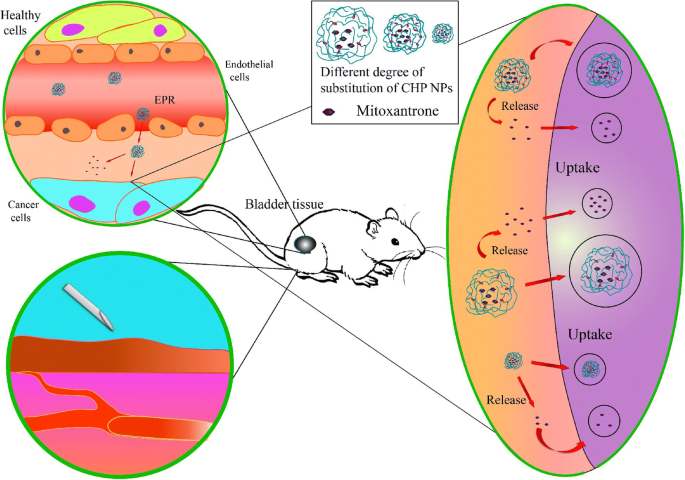
Die Behandlungswirksamkeit von Mitoxantron-beladenen CHP-NPs durch hauptsächlich lokale Freisetzung im Tumorgewebe
Viele klassische NPs werden als Wirkstoffträger verwendet, und die von uns hergestellten CHP-NPs sind anderen überlegen. Beispielsweise sind biogenetische NPs (wie Exosom, extrazelluläre Vesikel-mimetische, modularisierte extrazelluläre Vesikel) schwierig herzustellen [53]. Die Zielverteilung üblicher Liposomen ist nicht ideal und ihre Instabilität ist immer noch ein Problem [54]. Anorganische NPs wie Quantenpunkt-NPs sind sehr stabil, aber als Fremdkörper ist ihre Biokompatibilität schlecht, was beim Menschen Nebenwirkungen haben kann [55]. CHP-NPs sind einfach herzustellen und wir können ihre Größe steuern, indem wir den Grad der hydrophoben Substitution steuern [48]. Da sie in vivo direkt durch Amylase abgebaut werden können, weisen sie eine gute Biokompatibilität auf [56]. Darüber hinaus weisen CHP-NPs eine gute Stabilität und ausgezeichnete Wirkstofffreisetzungseigenschaften auf [57]. Der Nachteil besteht darin, dass sie unweigerlich zum Teil vom mononuklearen phagozytischen System verschluckt werden [58]. Weitere Forschung ist erforderlich, um die Entfernung durch das System zu reduzieren und die effektive Blutkonzentration von NPs zu verbessern.
Schlussfolgerung
Die Größe von Mitoxantron-beladenen CHP-NPs hängt vom Grad der Cholesterinsubstitution im Polymer ab. Je höher der Hydrophobie-Substitutionsgrad ist, desto kleiner ist die Größe und desto größer die Wirkstoffbeladung und Einkapselungseffizienz und desto langsamer die Wirkstofffreisetzung. Unter sauren Bedingungen ist die Freisetzung von CHP-NPs umso schneller, je stärker der Säuregehalt ist. Darüber hinaus ist die Freisetzung von NPs mit größerer Größe am besten und größere NPs können das Wachstum von Blasenzellen und deren Migration besser hemmen als kleinere NPs. KWK-NPs töten Krebszellen hauptsächlich durch die Freisetzung nanoskaliger Medikamente außerhalb der Zelle.
Nanomaterialien
- Herstellung von ICA-beladenen mPEG-ICA-Nanopartikeln und ihre Anwendung bei der Behandlung von LPS-induzierter H9c2-Zellschädigung
- Nanopartikel-Zufuhr von Artesunat verbessert die Anti-Tumor-Effizienz durch Aktivierung der Mitochondrien-vermittelten Zell-Apoptose
- Auswirkung der Verteilung von Goldnanopartikeln in TiO2 auf die optischen und elektrischen Eigenschaften von farbstoffsensibilisierten Solarzellen
- Bildung und Lumineszenzeigenschaften von Al2O3:SiOC-Nanokompositen auf der Basis von durch Phenyltrimethoxysilan modifizierten Aluminiumoxid-Nanopartikeln
- Modifiziertes hyperverzweigtes Polyglycerin als Dispergiermittel zur Größenkontrolle und Stabilisierung von Goldnanopartikeln in Kohlenwasserstoffen
- Förderung des SH-SY5Y-Zellwachstums durch Goldnanopartikel, die mit 6-Mercaptopurin und einem Neuronen-penetrierenden Peptid modifiziert sind
- Runde Goldnanopartikel:Einfluss der Partikelgröße und -konzentration auf das Wurzelwachstum von Arabidopsis thaliana
- Grüne Synthese von Metall- und Metalloxid-Nanopartikeln und ihre Wirkung auf die einzellige Alge Chlamydomonas reinhardtii
- Evaluierung der antimikrobiellen, apoptotischen und Krebszellen-Genabgabeeigenschaften von proteinbedeckten Goldnanopartikeln, die aus dem essbaren Mykorrhiza-Pilz Tricholoma crassum synthetisiert wur…
- Auswirkungen der Größe und Aggregation/Agglomeration von Nanopartikeln auf die Grenzflächen-/Zwischenphaseneigenschaften und die Zugfestigkeit von Polymer-Nanokompositen



