Fluoreszierende Nano-Biomassepunkte:Ultraschall-unterstützte Extraktion und ihre Anwendung als Nanosonde für den Fe3+-Nachweis
Zusammenfassung
Biomasse als nachhaltige und erneuerbare Ressource ist seit jeher eine der wichtigsten Energiequellen für das menschliche Leben. Hier wurden lumineszierende Nanobiomass Dots (NBDs) aus Sojabohnen durch ein Ultraschallverfahren extrahiert, das der Biomasse Fluoreszenzeigenschaften verleiht. Die so hergestellten NBDs haben eine amorphe Struktur mit einem durchschnittlichen Durchmesser von 2,4 nm und zeigen eine hellblaue Fluoreszenz mit einer Quantenausbeute von 16,7 %. Begünstigt durch die essbaren Rohstoffe und den hitzefreien Syntheseprozess zeigt der Zytotoxizitätstest, dass die Zellviabilität auch bei einer Konzentration der NBDs von 800 µg/ml noch 100 % hält, was auf die gute Biokompatibilität der NBDs hinweist. Darüber hinaus ist die Fluoreszenz der NBDs sehr empfindlich gegenüber Fe 3+ , das für Fe 3+ . verwendet werden kann Nachweis hinsichtlich ihrer gesundheitlichen Überlegenheit. Die Nachweisgrenze (LOD) des vorgeschlagenen Sensors wurde mit 2,9 μM bestimmt, was niedriger ist als der maximal zulässige Gehalt an Fe 3+ (5,37 μM) in Trinkwasser.
Hintergrund
Lumineszierende Nanomaterialien haben aufgrund ihrer einzigartigen optischen Eigenschaften eine Vielzahl von Anwendungen erreicht, insbesondere in Leuchtdioden, Detektoren, Bioimaging und Metallionendetektion [1,2,3,4,5,6]. Bisher wurde über verschiedene lumineszierende Nanomaterialien berichtet, wie Halbleiter-Quantenpunkte (QDs), Kohlenstoff-Nanopunkte und Schwefel-QDs, die in vielen Bereichen zu vielen Fortschritten geführt haben [7,8,9,10,11,12] . QDs als hervorragende Vertreter lumineszierender Nanomaterialien werden aufgrund ihrer hervorragenden optischen und elektrischen Eigenschaften in vielen Bereichen eingesetzt. Trotz alledem schränkt die Toxizität von QDs ihre Anwendung noch immer stark ein [13, 14]. Es ist immer von großer Bedeutung, grünere und nachhaltigere Nanomaterialien mit Lumineszenz zu finden. Biomasse ist eine ursprüngliche organische Substanz, die durch Photosynthese hergestellt werden kann und für ihre nachhaltigen und erneuerbaren Eigenschaften hervorgehoben wird. Konkret wird Biomasse als biologisch abbaubarer Anteil von Produkten, Abfällen und Reststoffen eines Organismus definiert [15, 16]. Im Rahmen der Nanotechnologie wird meist Biomasse als Vorstufe verwendet, die nach einer speziellen Behandlung in Nanopunkte mit bestimmten optischen Eigenschaften umgewandelt werden kann. Im Vergleich zu chemischen Vorprodukten sind die Hauptbestandteile der Biomasse, insbesondere der essbaren Biomasse, Zucker und Proteine, die in Folgebehandlungen unbedenklich sind. Daher sollten die Nano-Biomass Dots (NBDs) eine hohe Biokompatibilität aufweisen, was ihre Anwendung in biologischen und umweltbezogenen Bereichen sicherstellt, ohne schädliche Substanzen zu produzieren.
Bisher wurden nur aus Biomasse stammende fluoreszierende Kohlenstoff-Nanopunkte berichtet. Grundsätzlich wurden einige natürliche Biomassen wie Blätter, Eiweiß und Zitronensaft hydrothermal behandelt, um Fluoreszenz-Kohlenstoff-Nanopartikel zu synthetisieren [17,18,19]. Es gibt auch eine andere Art von Kohlenstoff-Nano-Punkten, die in essbaren Lebensmitteln vorkommen, die bei der Weiterverarbeitung natürlicher Biomasse entstehen [20, 21]. Bei allen handelte es sich ausnahmslos um typische Prozesse der Hochtemperaturkarbonisierung. Dieser Prozess kann lange Zeit und hohe Temperaturen erfordern, und es ist schwierig, eine Massenproduktion in großem Maßstab zu erreichen [22]. Im Vergleich zu hohen Temperaturen sind Raumtemperatur- oder Niedertemperaturbedingungen einfach durchzuführen und behalten die ursprünglichen Eigenschaften der Biomasse selbst bei.
Nanoprobe ist eine der wichtigen Anwendungen lumineszierender Nanomaterialien [23]. Aufgrund der hellen Fluoreszenz und der hohen Biokompatibilität können NBDs als eine Art Nanosonde im Bereich Biologie und Umwelt eingesetzt werden. Fe 3+ ist ein wichtiges Metallion im menschlichen Körper, für das sie eine bedeutende Rolle bei der Synthese von Hämoglobin und Myoglobin spielen [24]. Aber zu viel Fe 3+ Ansammlung im Körper kann zu Gewebeschäden und Organversagen führen. Entwicklung effektiver und umweltfreundlicher Sensorsysteme zur qualitativen und quantitativen Bestimmung von Fe 3+ ist von großer Bedeutung für klinische, medizinische und umweltbezogene Belange. Dies ermöglicht uns zu prüfen, ob Biomasse direkt aus natürlicher essbarer Biomasse ohne Verarbeitung zu Nanopunkten mit wünschenswerten Eigenschaften zugeschnitten werden kann. Nach unserem besten Wissen wurde jedoch über keine dieser lumineszierenden NBDs berichtet. Daher kann die Suche nach natürlicheren Biomassevorläufern zur Gewinnung von NBDs mit wünschenswerten Eigenschaften und hoher Biokompatibilität einen Schritt in Richtung grüner lumineszierender Nanomaterialien und Fe 3+ . machen Erkennung.
Hier wurden erstmals lumineszierende Nanobiomass Dots (NBDs) mittels Ultraschall-Extraktionsstrategie (UES) aus Sojabohnen nachgewiesen. Die Photolumineszenz (PL)-Quantenausbeute (QY) der NBDs wie hergestellt kann 16,7 % erreichen, und die NBDs zeigen eine helle Emission im Festkörper. Der Zytotoxizitätstest zeigt, dass die NBDs eine hohe Biokompatibilität aufweisen. Darüber hinaus wurden die NBDs für Fe 3+ . verwendet Detektion für seine Fluoreszenzintensitätsabhängigkeit linear vom Fe 3+ Konzentration, und die Nachweisgrenze (LOD) kann 2.9 μM erreichen.
Methoden
Materialien
Sorten von Sojabohnen aus dem Nordosten gemäß Nationalem Standard der Volksrepublik China (GB1352-2009 .) ) wurden im örtlichen Supermarkt gekauft und vor Gebrauch mehrmals mit destilliertem Wasser gewaschen. Calciumchlorid (CaCl2 ), Manganchlorid (MnCl2 .) ), Kupferchlorid (CuCl2 .) ), Kobaltchlorid (CoCl2 .) ), Bleinitrat (Pb (NO3 )2 ) und Chromnitrat (Cr(NO3 )3 ) wurden von Aladdin Ltd. (Shanghai, China) bezogen. Eisenchlorid (FeCl3 .) ), Eisenchlorid (FeCl2 .) ), Cadmiumchlorid (CdCl2 ), Quecksilberdichlorid (HgCl2 ), Natriumchlorid (NaCl) und Zinkchlorid (ZnCl2 ) wurden von Sinopharm Chemical Reagent Co., Ltd. (Shanghai, China) erhalten. Alle Chemikalien sind analytische Reagenzien (Reinheit> 99,0%) und werden wie erhalten ohne weitere Reinigung verwendet.
Synthese von NBDs
Zuerst wurden 100 Stück Sojabohnen dreimal mit einer Mischung aus Alkohol und destilliertem Wasser gewaschen, um die Verunreinigungen zu entfernen. Dann wurden die Sojabohnen in ein Becherglas mit 50 ml destilliertem Wasser gegeben, gefolgt von 2 h Ultraschall. Während dieses Prozesses änderte sich die Farbe der Lösung von transparent zu dunkelgelb, was darauf hindeutet, dass die Schale der Sojabohne auf Nanogröße zugeschnitten war, um NBDs zu bilden. Dann wurde die dunkelgelbe Lösung in Zentrifugenröhrchen überführt und bei 7000 U/min für 3 Minuten zweimal zentrifugiert, um große Partikel zu entfernen, danach wurde der Überstand durch eine 0,22-μM-Membran filtriert, um große oder agglomerierte Partikel weiter zu entfernen. Danach wurde die Lösung in einen Kühlschrank gestellt, gefolgt von einer Gefrierbehandlung bei − 5 ° C für 6 h. Dann wurde es bei − 50 ° . in einen Lyophilisator überführt C für 12 h, um die Pulver zu erhalten. Die gefrorenen Pulver wurden in Wasser dispergiert, um NBDs für die weitere Anwendung zu bilden.
Charakterisierung
Das Röntgenbeugungsmuster (XRD) der NBDs wurde unter Verwendung eines X′ Pert Pro Diffraktometers aufgezeichnet, in dem Röntgenstrahlen von einer Cu-Kα-Quelle erzeugt wurden. Ein JEM-2010 Transmissionselektronenmikroskop (TEM) wurde verwendet, um die Größe und Kristallinität der NBDs zu charakterisieren. Die Fluoreszenzspektren der NBDs wurden mit einem F-7000-Fluoreszenzspektrophotometer aufgenommen. Die UV-Vis-Absorptionsspektren der NBDs wurden unter Verwendung eines UH4150-Spektrophotometers erhalten. Die Fourier-Transform-Infrarot-(FTIR)-Spektren der Proben wurden mit einem Thermo Scientific Nicolet iS10 FTIR-Spektrometer aufgezeichnet. Die Röntgen-Photoelektronen-Spektroskopie (XPS)-Spektren der Proben wurden unter Verwendung eines Thermo Fisher Scientific ESCALAB 250Xi-Spektrometers, ausgestattet mit einer Al-Kα-Röntgenstrahlungsquelle, gesammelt.
Photolumineszenz-Quantenausbeutemessung
Der PL QY wurde mit einem F-9000 Spektrofluorometer mit Ulbrichtkugel getestet. Zunächst wurde die wässrige NBD-Lösung auf eine Absorptionsintensität von unter 0,1 verdünnt. Anschließend wurde diese wässrige Lösung in eine Fluoreszenzküvette gegeben, in die Ulbricht-Kugel eingebracht und mit monochromatischem Licht von 370 nm angeregt. Die Fluoreszenzspektren wurden im Bereich von 430–450 nm aufgenommen. Inzwischen wurden die gleichen Fluoreszenzspektren auch für reines Wasser unter identischen Bedingungen aufgenommen. Schließlich wurde der PL QY mit einer Fluoreszenzsoftware basierend auf den PL-Spektren sowohl der Probe als auch des Wassers berechnet.
Zellulärer Toxizitätstest
Die Zytotoxizität von NBDs wird durch MTT (3-(4,5)-Dimethylthiahiazo(-z-y1)-3,5-di-phenytetra-zoliu-mramide)-Methoden bewertet. Die Zellen wurden in normalem RPMI-1640 mit 10 % fötalem Rinderserum in 5 % CO2 . kultiviert und 95 % Luft bei 37 ° C in einem befeuchteten Inkubator. Für Zelllebensfähigkeitsmessungen wurden HeLa-Zellen in Platten mit 96 Vertiefungen gegeben und dann 72 h lang inkubiert. Nach 72 Stunden Inkubation von Hela-Zellen mit verschiedenen Konzentrationen von NBDs und CDs wurde die Lebensfähigkeit der Zellen aufgezeichnet.
Nachweis von Fe 3+
1 ml Lösung mit unterschiedlichen Konzentrationen von Fe 3+ wurde vor den PL-Messungen in 1 &mgr;ml NBDs mit 3 &mgr;g/l Lösung gegeben. Die Lösungen wurden gründlich gemischt und 1 min bei Raumtemperatur reagieren gelassen und dann die zugehörigen Fluoreszenzspektren aufgenommen. Die PL-Messungen wurden unter Anregung von 370 nm durchgeführt.
Ergebnisse und Diskussion
Morphologie und chemische Zusammensetzung
Die NBDs wurden mit UES-Methoden erstellt; alle Prozesse sind in Schema 1 veranschaulicht. Die Größen und Morphologie der NBDs wurden durch Transmissionselektronenmikroskopie (TEM) charakterisiert, wie in Abb. 1a und b gezeigt. Die TEM-Bilder zeigen, dass die NBDs nahezu kugelförmig waren. Die Durchmesser der NBDs reichen von 1 bis 3 nm mit einem durchschnittlichen Durchmesser von 2,4 nm, und die entsprechende Größenverteilung ist in Abb. 1c aufgeführt. Gitterränder der NBDs sind auf dem hochauflösenden TEM-Bild (Einschub von Abb. 1b) nicht zu erkennen, was auf die amorphe Natur der NBDs hinweist. Die Bilder der Hochwinkel-Dunkel-Dunkelfeld-Rastertransmissionselektronenmikroskopie (HAADF-STEM) und die entsprechende Elementarkartierung (Kohlenstoff, Stickstoff und Sauerstoff) der NBDs sind in Abb. 1d–g dargestellt. Es ist ersichtlich, dass die dominierenden Elemente der NBDs Kohlenstoff, Stickstoff und Sauerstoff sind. Darüber hinaus Festkörper 13 C-Kernresonanz(NMR)-Messungen der NBDs sind in Abb. 1h gezeigt. Die Signale reichen von 160–180 ppm, und die Peaks bei 164 ppm und 170 ppm entsprechen C=O-Bindungen, die auf sp 2 . hinweisen Kohlenstoffatome [25, 26].
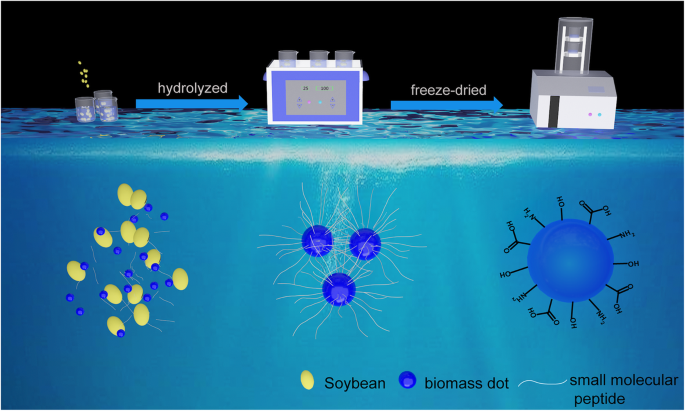
Schematische Darstellung des Herstellungsprozesses der NBDs aus Sojabohnen
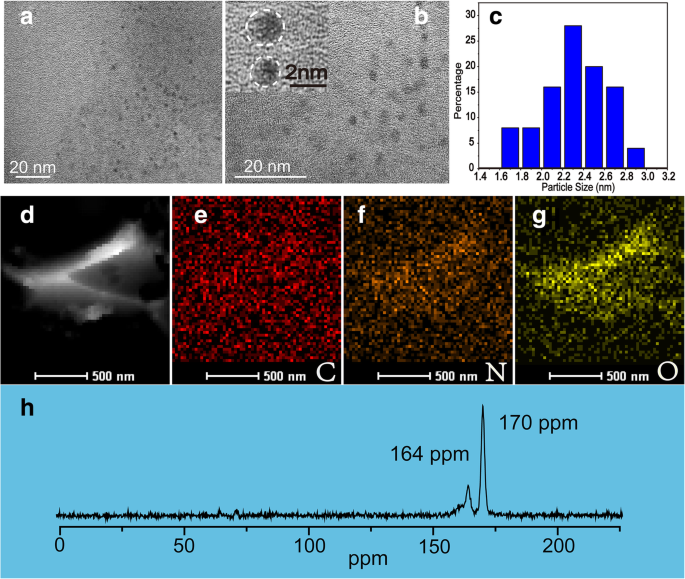
TEM-Bilder der NBDs (a ) und (b ). c Die Partikelgrößenverteilung der NBDs. HAADF-Bild (d ) und entsprechende Elementarverteilungskartierung von Kohlenstoff (e ), Stickstoff (f ) und Sauerstoff (g )
Um die strukturellen Eigenschaften der NBDs weiter zu untersuchen, wurde ein Röntgenbeugungsmuster (XRD) aufgezeichnet. Wie in Abb. 2a gezeigt, zeigt das typische XRD-Muster einen breiten Peak bei etwa 21,5 o . und eine Schulterspitze bei etwa 41,0 o , die auf die amorphe Kohlenstoffphase zurückgeführt werden kann [27]. Darüber hinaus wurden die charakteristischen Absorptionspeaks der Sojabohnen und NBDs durch Fourier-Transform-Infrarot(FTIR)-Spektroskopie untersucht, wie in Abb. 2(b) gezeigt. Die Absorptionsbanden bei etwa 3380 cm −1 kann den Streckschwingungen von O–H/–N–H zugeordnet werden, die Bande um 2906 cm −1 zu den C-H-Streckschwingungen und das Band bei etwa 1650 cm −1 zu den C=O-Streckschwingungen. Die Spitzen bei 1400 cm −1 und 1071 cm −1 entsprechen C–H- bzw. C–O-Biegeschwingungen [28]. Es gibt einen offensichtlichen Unterschied zwischen dem Spektrum von Sojabohnen und NBDs bei etwa 1750 cm −1 , das zu den Streckschwingungen von C=O-Bindungen aus den Lipiden in Sojabohnen gehört [29, 30]. Die in wässriger Lösung unlöslichen Lipide wurden beim Einweichen in Wasser von der Probe abgetrennt, was zum Verschwinden der Bindungen im FTIR-Spektrum der NBDs führte. Die reduzierten C=O-Bindungen in der Probe stammen von der Carboxylgruppe im Protein. Der Peak zentriert bei etwa 1543 cm −1 verschwand auch, was auf die Proteolyse beim Einweichen der Sojabohnen zurückzuführen ist. Beim Vergleich aller Peaks vor und nach dem Ultraschallprozess ist die Bildung von –OH, –C=O (Amid I) und –NH-Gruppen auf der Oberfläche der NBDs zu erkennen [31]. Die obigen Ergebnisse zeigen die Existenz von Hydroxyl-, Amidogen- und Carboxylgruppen auf der Oberfläche der NBDs, und diese funktionellen Gruppen spielen eine wichtige Rolle bei der Hydrophilie und Stabilität der NBDs in wässriger Lösung. Röntgen-Photoelektronenspektroskopie (XPS)-Spektren wurden durchgeführt, um die Komponenten der NBDs weiter aufzuklären, wie in Abb. 2c gezeigt. Das XPS-Spektrum zeigt drei starke Peaks bei 532,0, 401,1 und 286,1 eV, die O 1s, N 1s (Abb. 2d) bzw. C 1s (Abb. 2e) zugeschrieben werden können [32]. Diese Ergebnisse zeigen, dass die NBDs hauptsächlich C (64,33%), O (32,34 %) und N (2,72 %) sowie eine begrenzte Menge an P enthalten, und das P-Element kann aus dem Phospholipid der Sojabohnen stammen [33] . Im hochauflösenden XPS-Spektrum zeigt das C 1s-Spektrum drei Peaks bei 287,6, 285,8 und 284,6 eV, die C=O, C–O/C–N und C–C/C=C . zugeordnet werden können Gruppen, wie in Abb. 2c gezeigt. Die C=O-Bindung stammt von den löslichen Carboxylgruppen [24]. C–O/C=N und C–C/C=C stammen von den nitrosen Kohlenstoffen und sp 2 /sp 3 Kohlenstoffe bzw. [34]. Das in Abb. 2d gezeigte N 1s-Spektrum bestätigt zwei Hauptbanden bei 399,5 eV und 401,6 eV, was die Existenz von Pyridin-N und Pyrrol-N offenbart, was mit der FTIR-Analyse übereinstimmt. Das in Abb. 2f dargestellte O 1s-Spektrum weist zwei Peaks bei 531,4 eV und 533,0 eV auf, die den Gruppen C–OH/C–O–C bzw. C=O zugeschrieben werden können [9].
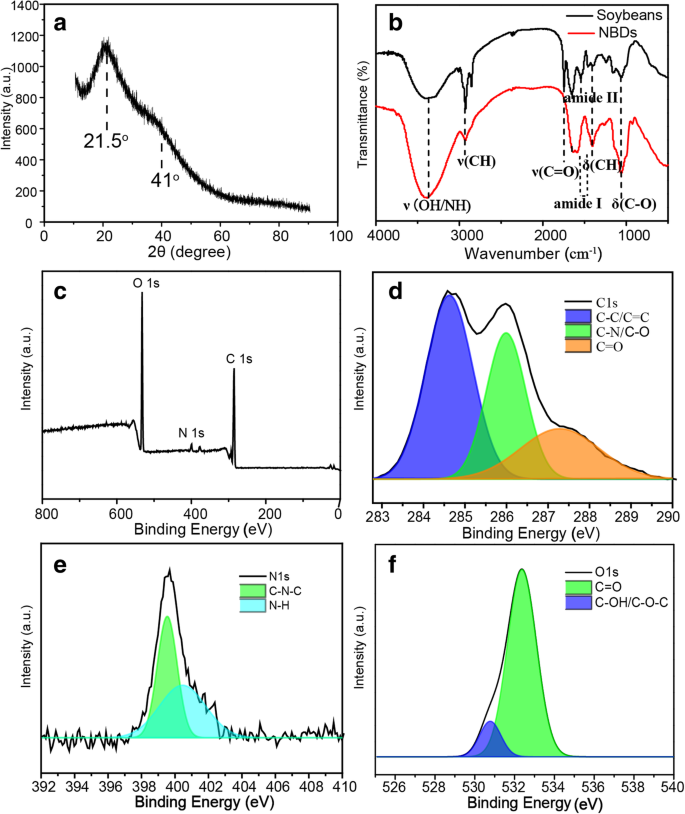
a XRD-Muster der NBDs. b FTIR-Spektren der Sojabohne und NBDs. c XPS-Spektrum der NBDs. Hochauflösende XPS-Spektren von C 1s (d ), N 1s (e ) und O 1s (f )
Basierend auf der obigen Analyse wurde ein möglicher Mechanismus für die Bildung von NBDs aus Sojabohnen vorgeschlagen. Zuerst werden einige große Partikel der in der Lösung suspendierten Biomasse durch die Ultraschallerschütterung in Nanometergröße zerbrochen. Änderungen der Lösung vor und nach der Ultraschallextraktionsbehandlung sind in Zusätzliche Datei 1:Abbildung S1 dargestellt. Dann wurde das Protein in den Sojabohnen im obigen Verfahren zu kleinmolekularen Peptiden und Aminosäuren hydrolysiert, und viele niedermolekulare Peptidketten werden an die Biomasse in Nanogröße angehängt, um die hochgradig oberflächenfunktionalisierten Biomassepunkte zu bilden. Die funktionellen Gruppen auf der Oberfläche der Biomassepunkte tragen am meisten zur Fluoreszenz bei. Dem Mechanismus entsprechend wurde die Mungbohne auch als Vorläufer verwendet und es wurden auch blau fluoreszierende NBDs erhalten, wie in Zusatzdatei 1:Abbildung S2 gezeigt.
Optische Eigenschaften
Die NBDs zeigen anregungsabhängige Fluoreszenzeigenschaften, und wenn die Anregungswellenlänge von 320 bis 520 nm variiert, verschiebt sich die Emissionsspitze allmählich rot, was darauf hindeutet, dass die Emission der NBDs durch Ändern der Anregungswellenlänge abgestimmt werden kann, wie in Abb. 3a gezeigt. Die wässrige NBD-Lösung ist bei Innenbeleuchtung transparent und zeigt bei UV-Beleuchtung blaue Fluoreszenz, wie im Einschub von Abb. 3b gezeigt. Das Photolumineszenz-Anregungsspektrum (PLE) der NBDs ist in Zusatzdatei 1:Abbildung S3 dargestellt, und die optische Anregungswellenlänge liegt im Bereich von 360 bis 420 nm. Um den PL-Ursprung der NBDs zu untersuchen, wurden die UV-Vis-Absorptionsspektren der NBDs mit unterschiedlichen Konzentrationen bei Raumtemperatur aufgenommen (die Konzentration der NBDs von unten nach oben beträgt 0,03, 0,06, 0,13, 0,25, 0,25, 0,50, 0,50 , 0,75, 1,00 und 1,50 µg/l), wie in Abb. 3b gezeigt. Die UV-Vis-Absorptionsspektren der NBDs zeigen zwei deutliche Absorptionspeaks bei 270 nm bzw. 330 nm. Ersteres kann dem π-π * . zugeschrieben werden Übergang von C–C/C=C-Bindungen, während letztere in die n-π * Übergang von C=O/N-Bindungen [35, 36]. Diese funktionellen Gruppen sind die wichtigsten chromogenen Gruppen, die zur Fluoreszenz der NBDs beitragen [37, 38]. Die PL-Spektren der Sojabohnen während der Ultraschallextraktion sind in Zusatzdatei 1:Abbildung S4 dargestellt, und die PL-Intensität nimmt mit der Zeit zu und erreicht dann das Maximum. Abbildung 3c zeigt die PL-Spektren der NBDs gemessen von 80 bis 300 K. Die NBDs zeigen ein typisches thermisches Löschverhalten, bei dem die Intensität aller Peaks mit steigender Temperatur monoton abnimmt. Dieses PL-Verhalten ist auf die Zunahme der nicht-strahlenden Rekombination und die Abnahme der Strahlen-Rekombination mit steigender Temperatur zurückzuführen [39, 40]. Um die Stabilität der NBDs zu bewerten, wurden die Photostabilität und Thermostabilität der NBDs charakterisiert, wie in Abb. 3d gezeigt. Aus Gründen der Fotostabilität wird das Messeinrichtungsbild in der zusätzlichen Datei 1 angezeigt:Abbildung S5. Die Fluoreszenzintensitätswerte sind in der zusätzlichen Datei 1 dargestellt:Abbildung S6 und S7. Die Emissionsintensität der NBDs bleibt unter der UV-Lampenbeleuchtung für 6 h über 90%, was ihre gute Photostabilität anzeigt. Aus Gründen der Thermostabilität nehmen die Fluoreszenzintensitäten der NBDs wenig ab, wenn die Temperatur zwischen 20 und 80 ° . variiert C, was ihre hohe thermische Stabilität offenbart.
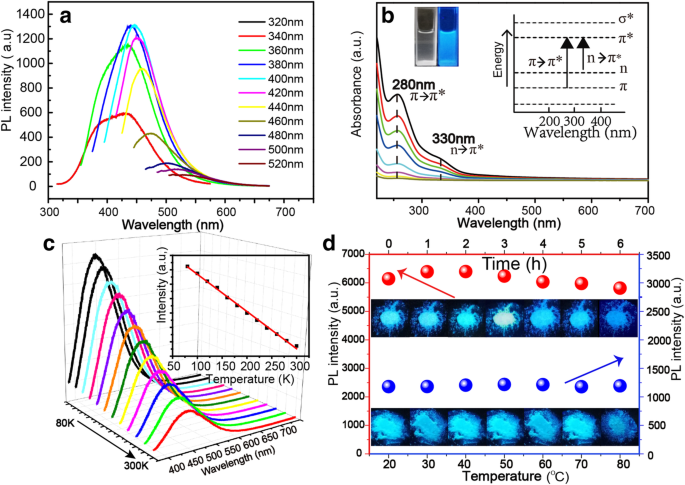
a Fluoreszenzspektren der NBDs mit Änderungen der Anregungswellenlänge von 320 bis 520 nm. b UV-Vis-Absorptionsspektren der NBDs. c Fluoreszenzspektren der NBDs bei unterschiedlicher Temperatur, der Einschub ist die Auftragung der Fluoreszenzintensität der NBDs als Funktion der Temperatur. d Fluoreszenzintensität und Bilder der NBD-Pulver unter Beleuchtung einer 365-nm-Lampe für verschiedene Dauer und die der NBD-Pulver bei unterschiedlicher Messtemperatur
Zytotoxizitätsbewertung
Die MTT-Assays wurden verwendet, um die Zytotoxizität der NBDs zu bewerten. Die Lebensfähigkeit von HeLa-Zellen, die mit den NBDs und zwei anderen Arten von CDs inkubiert wurden, die über ein hydrothermales Verfahren synthetisiert wurden, wie in Fig. 4 gezeigt NBDs erreichen 800 µg/ml. Die Zellüberlebensrate betrug 70 % und 67 %, wenn die HeLa-Zellen mit den anderen beiden Arten von CDs bei einer Konzentration von 800 µg/ml inkubiert wurden. Offensichtlich weisen die NBDs eine bessere Biokompatibilität auf als die aus chemischen Reagenzien hergestellten CDs.
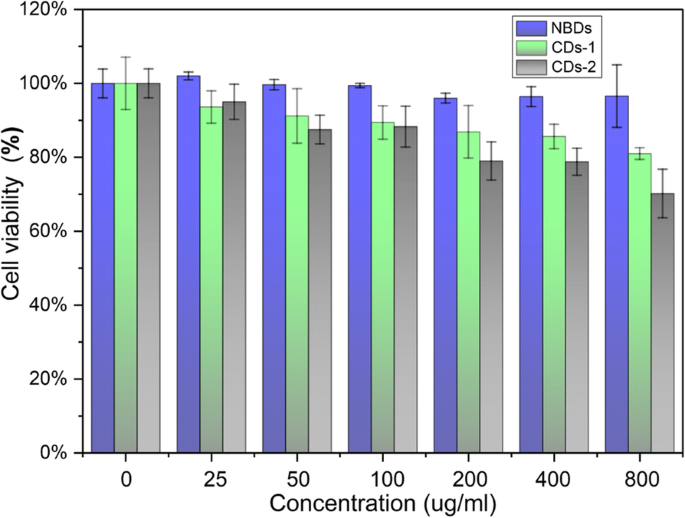
Lebensfähigkeit von HeLa-Zellen nach 72 h Inkubation mit unterschiedlichen Konzentrationen von NBDs und CDs
Erfassungseigenschaften der NBDs in Richtung Fe 3+
Interessanterweise kann die Fluoreszenz der NBDs durch Fe 3+ . effektiv gelöscht werden , wie in Abb. 5a gezeigt, und die PL-Intensität der NBDs nimmt mit der Zunahme von Fe 3+ . deutlich ab Konzentration. Darüber hinaus kann eine gute lineare Beziehung zwischen F0 /F und das Fe 3+ Konzentration von 0 bis 30 μM (R 2 = 0,99), wobei F0 und F waren die PL-Intensität der NBDs bei ex/em von 370/445 nm in Abwesenheit und Gegenwart von Fe 3+ , wie in Abb. 5b gezeigt. Die Abschreckeffizienz wurde durch die Stern-Volmer-Gleichung angepasst:
$$ \frac{{\textrm{F}}_0}{\textrm{F}}=1+{K}_{\textrm{SV}}\left[Q\right] $$ (1)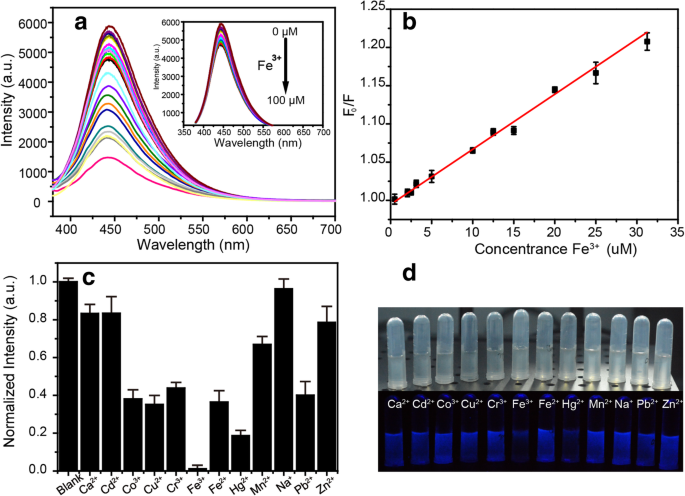
a PL-Spektren der NBDs in Gegenwart unterschiedlicher Konzentrationen von Fe 3 + . b Kalibrierkurve des Sensors in Abhängigkeit von Fe 3 + Konzentration. c Fluoreszenzintensitäten der NBDs in Gegenwart verschiedener Ionen. d Fotografische Bilder der NBDs-Lösung mit verschiedenen Metallionen unter Innen- und UV-Beleuchtung
wo K sv ist die Stern-Volmer-Löschkonstante und [Q ] ist das Fe 3+ Konzentration. Die lineare Regressionsgleichung lautet Y = 0,0072X +0,99479 , R 2 = 0,99. Die Nachweisgrenze (LOD) des vorgeschlagenen Sensors wurde mit 2,9 μM bestimmt, was niedriger ist als der maximal zulässige Gehalt an Fe 3+ (5,37 µM) in Trinkwasser, das von der United States Environmental Protection Agency (USEPA) eingerichtet wurde [24]. Die Selektivität ist ein weiterer kritischer Parameter für chemische Sensoren. Daher wurde die Fluoreszenzreaktion des Sensors gegenüber mehreren interferierenden Metallionen untersucht, darunter Ca 2+ , Cd 2+ , Co 2+ , Cu 2+ , Cr 3+ , Fe 3+ , Fe 2+ , Hg 2+ , Mn 2+ , Na + , Pb 2+ , und Zn 2+ . Metallionen jeweils in einer Konzentration von 10 −2 M wurden in 1 µl NBDs-Lösung mit einer Konzentration von 3 µg/l gegeben. In Abb. 5c ist zu sehen, dass die Fluoreszenzintensität der NBDs empfindlicher auf Fe 3+ . reagiert als andere Metallionen. Die Fotografien in Abb. 5d sind die Bilder der NBDs mit verschiedenen Ionen unter Innen- und UV-Beleuchtung, und die Konzentration der Metallionen betrug 100 μM. Offensichtlich werden die NBDs in Gegenwart von Fe 3+ . gelöscht , was darauf hinweist, dass sie zur visuellen Erkennung verwendet werden können.
Abschreckmechanismus
Der Löschmechanismus der NBDs in Gegenwart von Fe 3+ wurde basierend auf den UV-Vis-Absorptionsspektren und der Fluoreszenzlebensdauer der NBDs diskutiert. Aus den UV-Vis-Absorptionsspektren in Zusatzdatei 1:Abbildung S8 geht hervor, dass sich die Absorptionspeaks bei 270 nm und 340 nm durch die Einführung von Fe 3+ . nicht ändern , was darauf hinweist, dass das Fe 3+ beeinflusst die Struktur der NBDs nicht [41]. Abgesehen vom UV-Vis-Absorptionsspektrum ist die Wirkung von Fe 3+ zur Lebensdauer der NBD wurde ebenfalls untersucht. In Abb. 6a wird die Fluoreszenzlebensdauer nach der Zugabe von Fe 3+ . kürzer , die einen teilweisen Elektronentransfer der NBDs auf das d . beinhalten kann Orbital von Fe 3+ , vermindern somit die strahlende Rekombination der NBDs [42]. Der durch Fe 3+ . verursachte Fluoreszenzlöschmechanismus der NBDs ist in Abb. 6b gezeigt. Der empfindliche Fluoreszenzlöschungseffekt der NBDs in Gegenwart von Fe 3+ kann von der starken Wechselwirkung zwischen Fe 3+ . herrühren und die Oberflächengruppen der NBDs. Fe 3+ hat eine stärkere Bindungsaffinität und eine schnellere Chelatisierungskinetik mit Amino- und Carboxylgruppen auf den Oberflächen von NBDs. Die besondere Koordination zwischen den Fe 3+ Ionen und die phenolischen Hydroxyl-/Amingruppen von NBDs wurden häufig zum Nachweis von Fe 3+ . verwendet Ionen oder Farbreaktionen in der traditionellen organischen Chemie [43, 44]. Außerdem sind die Redoxpotentiale von Fe 3+ /Fe 2+ (Ф = 0.77) befinden sich zwischen dem niedrigsten unbesetzten Molekülorbital (LUMO) und dem höchsten besetzten Molekülorbital (HOMO) der NBDs und verursachen einen photoinduzierten Elektronentransfer vom LUMO in die komplexen Zustände von Fe 3+ [45]. Diese Ergebnisse zeigen, dass die NBDs sehr empfindlich gegenüber Fe 3+ . sind über den anderen Metallionen.
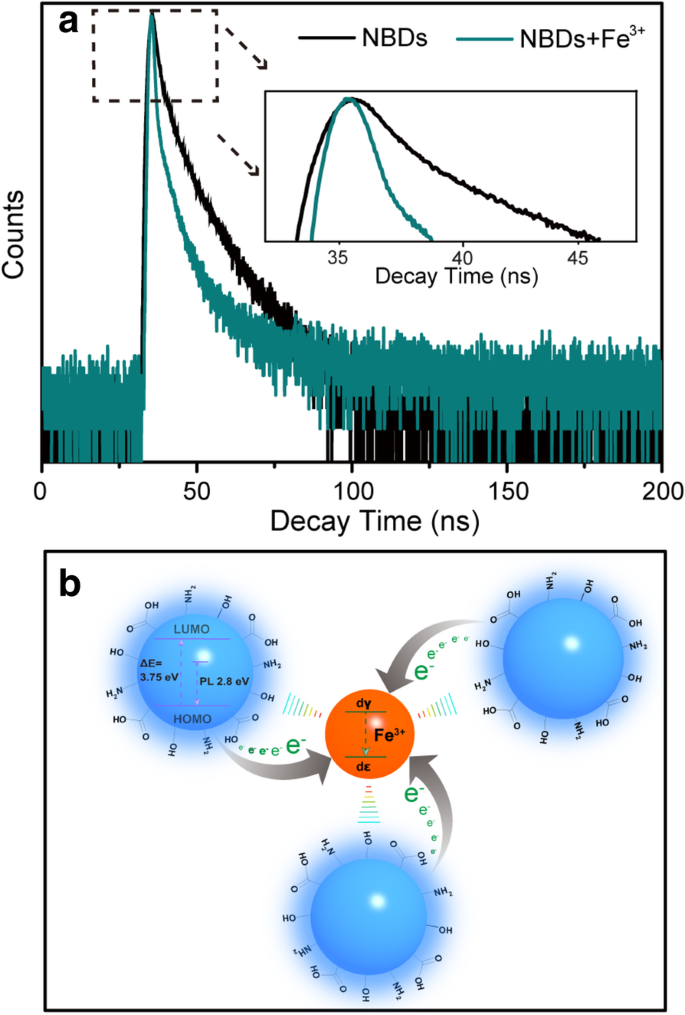
a Fluoreszenzzerfallsspuren der NCDs in Abwesenheit und Anwesenheit von Fe 3 + unter Anregung bei 370 nm und Emission bei 445 nm. b Schematische Darstellung des möglichen Fluoreszenzlöschmechanismus der NBDs in Gegenwart von Fe 3 + Ionen
Schlussfolgerung
Zusammenfassend lässt sich sagen, dass lumineszierende NBDs aus Sojabohnen über einen hitzefreien UES-Ansatz hergestellt wurden. Die NBDs zeigen eine hellblaue Fluoreszenz mit einem PL QY von 16,7%, und dank der essbaren Biomasse und des hitzefreien Syntheseprozesses bleibt die Zelllebensfähigkeit immer noch 100%, selbst wenn die Konzentration der NBDs 800 µg/ml erreicht. Darüber hinaus weist die Fluoreszenz der NBDs eine spezifische Empfindlichkeit gegenüber Fe 3+ . auf , und der LOD kann 2,9 µM erreichen. Die niedrige Toxizität und die hohe Nachweisgrenze weisen darauf hin, dass die NBDs voraussichtlich potenzielle Anwendungen in biologischen und Umweltsystemen finden werden.
Abkürzungen
- FTIR:
-
Fourier-Transformations-Infrarot
- HAADF-STEM:
-
Ringförmige Dunkelfeld-Rastertransmissionselektronenmikroskopie mit großem Winkel
- LOD:
-
Nachweisgrenze
- NBDs:
-
Nano-Biomasse-Punkte
- NMR:
-
Kernspinresonanz
- PL:
-
Photolumineszenz
- QDs:
-
Quantenpunkte
- QY:
-
Quantenausbeute
- TEM:
-
Transmissionselektronenmikroskopie
- UES:
-
Ultraschall-Extraktionsstrategie
- USEPA:
-
US-Umweltschutzbehörde
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Demonstration eines flexiblen Graphen-basierten Biosensors für den empfindlichen und schnellen Nachweis von Eierstockkrebszellen
- Multifunktionale Goldnanopartikel für verbesserte diagnostische und therapeutische Anwendungen:Eine Übersicht
- Fortschritte und Herausforderungen fluoreszierender Nanomaterialien für die Synthese und biomedizinische Anwendungen
- N,N-Dimethylformamid, das die Fluoreszenz von MXen-Quantenpunkten für die empfindliche Bestimmung von Fe3+ reguliert
- Synthese von reabsorptionsunterdrückten Typ-II/Typ-I-ZnSe/CdS/ZnS-Kern/Schale-Quantenpunkten und ihre Anwendung für Immunsorbent-Assays
- Ein einfacher Ansatz zur Synthese von fluoreszierenden Kohlenstoffquantenpunkten aus Tofu-Abwasser
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Eine wiederaufladbare Fluoreszenzsonde BHN-Fe3O4@SiO2 Hybrid-Nanostruktur für Fe3+ und ihre Anwendung in der Biobildgebung
- Umweltfreundliche und einfache Synthese von Co3O4-Nanodrähten und ihre vielversprechende Anwendung mit Graphen in Lithium-Ionen-Batterien
- Gründe für Leiterplattenverzug und ihre vorbeugenden Maßnahmen



