In-situ-Beladung von CuS-Nanoblumen in einem Schritt auf Anatas-TiO2/Polyvinylidenfluorid-Fasern und ihre verbesserte photokatalytische und selbstreinigende Leistung
Zusammenfassung
CuS-Nanoblumen wurden auf Anatas-TiO2 . geladen /Polyvinylidenfluorid (PVDF)-Fasern durch hydrothermal behandelte elektrogesponnene Tetrabutylorthotitanat (TBOT)/PVDF-Fasern bei niedriger Temperatur. Die Ergebnisse zeigten, dass die Menge an Kupferquelle und Schwefelquelle die Kristallisation und Morphologie der resultierenden Produkte bestimmt. Es wurde festgestellt, dass der Verbund von CuS die Bandlückenenergie von TiO2 . verengt und verbesserte die Trenneffizienz der photogenerierten Elektron-Loch-Paare von TiO2 . Die photokatalytische Reaktionsgeschwindigkeit von CuS/TiO2 /PVDF-Fasern zu Rhodamin B war dreimal höher als die von TiO2 /PVDF-Fasern unter Bestrahlung mit sichtbarem Licht. Aufgrund des Herstellungsprozesses, der bei niedriger Temperatur durchgeführt wurde, ist die Flexibilität von CuS/TiO2 /PVDF-Fasern wurde sichergestellt. Außerdem wurde die Selbstreinigungsleistung der Farbstofftröpfchen auf der resultierenden Produktoberfläche unter sichtbarem Licht demonstriert. Unterdessen kann das resultierende Produkt aufgrund seiner Hydrophobie automatisch Staub auf der Oberfläche des Materials unter dem Rollzustand von Tröpfchen entfernen. Daher ist das so hergestellte CuS/TiO2 /PVDF-Fasern können nicht nur die verunreinigten Verbindungen abbauen, sondern aufgrund ihrer Selbstreinigungsleistung auch die Wartungskosten senken, was eine sehr praktische Anwendungsperspektive bedeutet.
Einführung
In den letzten Jahren wurde die Umwelt des Menschen aufgrund der unangemessenen Entwicklung und Nutzung natürlicher Ressourcen ernsthaft verschmutzt, einschließlich Luft-, Boden- und Wasserverschmutzungen. Unter ihnen ist die Wasserverschmutzung zu einem der dringendsten Probleme geworden, die gelöst werden müssen, da sie eng mit dem menschlichen Leben verbunden ist. Aufgrund der wegweisenden Forschungen von Fujishima und Honda [1] hat die Halbleiter-Photokatalyse-Technologie weltweites Lob als potenzielle Lösung für den Abbau giftiger organischer Schadstoffe in Wasser gewonnen, um eine ökologische Nachhaltigkeit zu erreichen. Bisher wurden viele Halbleiter in der Wasseraufbereitung eingesetzt [2,3,4,5]. Manikandanet al. synthetisiertes MoS2 /α -MoO3 heterostrukturierte Nanoblumen durch einstufige hydrothermale Methode [6]. Das vorbereitete MoS2 /α -MoO3 heterostrukturierte Nanoblumen haben eine große Oberfläche und eine ausgezeichnete Adsorptionsleistung. Wei und Mitarbeiter stellten poröses Co3 . her O4 Nanoblätter durch hydrothermale Methode [7]. Die resultierenden Produkte weisen eine viel geringere Überspannung von 318 mV bei einer Stromdichte von 10 mA cm −2 . auf . Außerdem sind diese porösen Co3 O4 Nanoblätter weisen auch eine ausgezeichnete elektrochemische Stabilität auf. Unter vielen Halbleitern ist Titandioxid (TiO2 ) ist aufgrund seiner beispiellosen Effizienz und Stabilität zu einem bekannten Photokatalysator geworden. Die Wirksamkeit von TiO2 wird durch seine große Bandlücke (Eg ~ 3.2 eV) behindert, was es unmöglich macht, sichtbares Licht direkt zu nutzen, was zur Abwesenheit von TiO2 . führt als sichtbarer Photokatalysator. Darüber hinaus ist die schnelle Rekombination photogenerierter Ladungsträger in TiO2 reduziert seine Lichtquanteneffizienz stark.
Um diese Probleme zu lindern, wurden viele Untersuchungen durchgeführt, um die photokatalytische Fähigkeit von TiO2 . im sichtbaren Licht zu verbessern [8,9,10,11,12,13]. Die Kombination von TiO2 mit anderen Narrow-Gap-Halbleiterbauelementen, insbesondere zweidimensionalen (2D) Narrow-Gap-Halbleiterbauelementen, hat sich als erfolgreiche Strategie zur Verbesserung der Trenneffizienz photoinduzierter Ladungsträger erwiesen [14,15,16,17,18,19 ,20,21]. Ouyanget al. synthetisierte BiOCl-Nanoblätter/TiO2 Nanotube-Arrays Heterojunction durch die Kombination von Anodisierungsprozess und Imprägnierungsverfahren [22]. Die so hergestellten Produkte verbesserten die Trenneffizienz photogenerierter Ladungsträger durch die Grenzfläche zwischen den BiOCl-Nanoblättern und TiO2 Nanoröhren-Arrays. Darüber hinaus ist die Kombination von 2D-Graphen mit guter Leitfähigkeit und TiO2 kann auch eine gute photokatalytische Leistung erzielen [23]. Interessanterweise hat die Forschung zur Komplexierung mit Metallsulfiden einige Fortschritte gemacht [24,25,26,27,28,29]. Insbesondere das TiO2 Proben aus zusammengesetzten Cadmium- und Bleihalbleitern haben eine bemerkenswerte Leistung erzielt, aber auch ernsthafte Probleme mit der Sekundärverschmutzung verursacht. Daher ist die Erforschung gutartiger Halbleiterverbundwerkstoffe mit schmaler Bandlücke unerlässlich.
Kupfersulfid (CuS), ein Halbleitermaterial mit einer Bandlücke von 2,0 eV, weist eine hervorragende Leistung auf und wurde in Solarzellen, Photokatalyse, Lithiumbatterien usw. verwendet [30, 31]. Daher ist die Kopplung von CuS und TiO2 um ein CuS-TiO2 . herzustellen Komposit mit sichtbarer Lichtaktivität und hoher Trenneffizienz von photogenerierten Trägern bietet eine Möglichkeit. Yu und Mitarbeiter stellten zwei verschiedene Komposite TiO2 . her -CuS-a und TiO2 -CuS-b durch direkte Abscheidung und bifunktionelle Linker-Kopplungsmethoden auf TiO2 Nanokugeln [32]. Im Vergleich zu TiO2 -CuS-a, hergestellt durch direkte Abscheidungsmethode, TiO2 -CuS-b mit einer regelmäßigen „stacheligen Kugel-ähnlichen“ Struktur hat eine verbesserte Desinfektionsfähigkeit, die seine photokatalytische Leistung unter Sonnen- und UV-Licht verbessert. Luet al. präparierte CuS-Nanoblumen, geladen auf Rutil-TiO2 unter Verwendung von Kupfer- und Schwefelpulver durch Element-Direkt-Reaktion [33]. Im Vergleich zu reinem TiO2 oder Kupfersulfid, das wie synthetisierte CuS/TiO2 Proben zeigten eine verbesserte photokatalytische Leistung aufgrund der Bildung eines Heteroübergangs zwischen CuS und Rutil-TiO2 . Hou et al. präpariertes TiO2 Fasern durch Elektrospinnen und Nachsintern. Das präparierte TiO2 Fasern wurden in NaOH-Lösung getränkt und ließen dann CuS-Partikel auf der Oberfläche der Fasern durch hydrothermale Verfahren wachsen [34]. Die inselartigen CuS-Partikel, die an TiO2 . haften Nanofasern, die einen Durchmesser von weniger als 100 nm aufwiesen, um Heterostrukturen zu bilden. Die so hergestellten Proben zeigten eine verbesserte photokatalytische Aktivität für den Abbau des Methylblau-(MB)-Farbstoffs. Das oben erwähnte CuS-TiO2 Verbundwerkstoffe sind pulverförmige Werkstoffe oder sehr spröde Faserwerkstoffe nach einer Hochtemperaturbehandlung. Diese Materialien sind nach photokatalytischen Experimenten in Wasser schwer zu trennen und zu recyceln. Darüber hinaus leiden photokatalytische Materialien häufig unter einer Kontamination durch Zielschadstoffe, was zu einer Abnahme ihrer photokatalytischen Leistung führt.
In dieser Arbeit wurden CuS-Nanoblumen auf das TiO2 . geladen /Polyvinylidenfluorid (PVDF)-Fasern durch einstufige hydrothermale Behandlung von elektrogesponnenen Tetrabutylorthotitanat (TBOT)/PVDF-Fasern bei niedriger Temperatur. Einerseits ist der Zubereitungsprozess bequem und einfach. Andererseits garantiert der Einsatz bei niedriger Temperatur im Herstellungsprozess die Flexibilität von PVDF. Das so hergestellte CuS/TiO2 /PVDF-Faser hat eine gute photokatalytische Leistung bei sichtbarem Licht. Unter sichtbarem Licht ist die photokatalytische Reaktionsgeschwindigkeit von CuS/TiO2 /PVDF-Fasern zu Rhodamin B (RhB) ist dreimal höher als die von TiO2 /PVDF-Fasern. Außerdem wurde die Selbstreinigungsleistung des resultierenden Produkts untersucht. Daraus kann geschlossen werden, dass das so hergestellte CuS/TiO2 /PVDF-Fasern haben eine gute Trennbarkeit, Recyclingfähigkeit und Selbstreinigungsleistung. Die resultierenden Proben in dieser Arbeit bieten eine neue Perspektive für die Untersuchung der Anwendung neuartiger flexibler, recycelbarer und selbstreinigender photokatalytischer Materialien zur Kontrolle der Umweltverschmutzung.
Methoden/Experimental
Materialien
PVDF (FR904) wurde von Shanghai 3F New Materials Co., Ltd. bezogen, und N,N-Dimethylformamid (DMF, AR, 99,5%), Aceton (CP, 99,0%), TBOT (CP, 98,0%), Kupfernitrat (Cu (NO3 )2 ·3H2 O, AR, 99,0 %), Thioharnstoff (AR, 99,0 %), RhB, MB und Methylorange (MO) wurden von Sinopharm Chemical Reagent Co., Ltd. bezogen. Alle Reagenzien wurden wie erhalten ohne weitere Reinigung verwendet.
Vorbereitung von TBOT/PVDF-Fasern
In einem typischen Elektrospinnverfahren wurden 4,0 g PVDF-Pulver mit 10 g Aceton und 10 g DMF gemischt. Dann wurde die Mischung bei 40°C kräftig gerührt, bis sie klar und transparent wurde. Danach wurden 10 ml TBOT zu der oben erwähnten Lösung gegeben und 1 Stunde lang bei 40 °C gerührt, um die TBOT/PVDF-Vorläuferlösung zu bilden. Eine 5,0-ml-Spritze mit einer TBOT/PVDF-Vorläuferlösung mit einer stumpfen Metallnadel wurde auf einen Propeller gesetzt. Die Antriebsgeschwindigkeit wurde auf 1,8 ml h −1 . eingestellt . Der Fasersammler war eine in ein Stück Aluminiumfolie gewickelte Edelstahlrolle mit einer Rotationsgeschwindigkeit von etwa 250 U/min. Eine auf 9 kV eingestellte Gleichspannungsquelle wurde zwischen der Spitze und dem Kollektor in einem Abstand von 11 cm platziert. Die so hergestellten TBOT/PVDF-Fasern wurden 10 h bei 60 °C getrocknet, um jegliches restliche Lösungsmittel zu entfernen. Schließlich wurden die so hergestellten TBOT/PVDF-Fasern für die anschließende hydrothermale Behandlung in 2,5 cm × 2,5 cm große Stücke geschnitten.
Herstellung von CuS/TiO2 /PVDF-Fasern
Cu (NO3 )2 ·3H2 O und Thioharnstoff wurden in 30 ml entionisiertem Wasser in einem festen Molverhältnis (1:2) zugegeben und das Rühren wurde 30 Minuten lang fortgesetzt. Dann wurde die Lösung in den 50-ml-Edelstahlautoklaven überführt und die geschnittenen TBOT/PVDF-Stücke wurden hineingelegt. Der Edelstahlautoklav wurde in einen Elektroofen gestellt und 24 h auf 150°C erhitzt. Im hydrothermalen Prozess wird einerseits TBOT in TBOT/PVDF zu TiO2 . hydrolysiert /PVDF. Andererseits wächst CuS kontinuierlich auf der Oberfläche von TiO2 /PVDF zur Bildung von CuS/TiO2 /PVDF. Schließlich wurden die so hergestellten Fasern gründlich mit Ethanol und entionisiertem Wasser gewaschen, dann in einem Elektroofen bei 60 °C 10 h lang getrocknet und das flexible CuS/TiO2 /PVDF-Fasern wurden erhalten (siehe zusätzliche Datei 1:Abbildung S1. Zum Vergleich:die Menge an Cu (NO3 )2 ·3H2 Das zugegebene O betrug 0,1, 0,5 bzw. 1 &mgr;mMol. Dementsprechend wurden die Materialien im synthetisierten Zustand als Cu 0.1, Cu 0.5 bzw. Cu 1 bezeichnet.
Charakterisierung
Die Röntgenbeugungsmuster (XRD) wurden auf einem Rigaku SmartLab Röntgendiffraktometer im 2θ-Bereich von 10–90° unter Verwendung von Cu-Kα-Strahlung (λ = 1,54178 Å) bei einer Beschleunigungsspannung von 40 kV. Darüber hinaus wurden die Rasterelektronenmikroskopie-(SEM)-Bilder und die Transmissionselektronenmikroskopie-(TEM)-Bilder der so hergestellten Proben vom Rasterelektronenmikroskop Phenom Pro bzw. dem Transmissionselektronenmikroskop JEOL JEM-2100 Plus erhalten. Um ein detailliertes Verständnis der Informationen zur chemischen Zusammensetzung der hergestellten Produkte zu erhalten, wurden die Detektionen der Röntgenphotoelektronenspektroskopie (XPS) auf einem Thermo Scientific Escalab 250Xi-System durchgeführt. Die Lichtsammelleistung der so hergestellten Proben wurde durch diffuse Reflexionsspektren (DRS) bewertet. DRS-Untersuchungen wurden auf einem Shimadzu UV-2600-Spektrophotometer durchgeführt, das mit einem Ulbrichtkugel-Zubehör ausgestattet war und BaSO4 . verwendet als Standard für diffuse Reflexion. Die Photolumineszenzspektren (PL) der resultierenden Proben wurden auf einem Hitachi F-2500-Fluoreszenzspektrometer mit einer Xe-Lampe bei Raumtemperatur unter Verwendung einer Anregungswellenlänge von 320 nm untersucht.
Photokatalytische Aktivität
Die photokatalytische Leistung der resultierenden Produkte wurde unter einer 9-W-Weißlicht-LED-Bestrahlung bei Raumtemperatur durch Abbau von RhB (5 mg L −1 ), das direkt mit RhB-Reagenz und entionisiertem Wasser hergestellt wurde. Das Lichtspektrum dieser LED ist in der zusätzlichen Datei 1 dargestellt:Abbildung S2. Um den Einfluss der Menge an Cu-Quellen auf die Photokatalyse zu zeigen, wurden Filmphotokatalysatoren mit der gleichen Fläche in Photokatalyseexperimenten verwendet. In Photoabbauexperimenten wurde ein Stück des resultierenden Produkts in ein 100-ml-Quarzröhrchen mit 60 ml RhB-Lösung gegeben, gefolgt von 30-minütigem magnetischem Rühren im Dunkeln, um das Adsorptions-Desorptions-Gleichgewicht zwischen RhB und dem resultierenden Produkt sicherzustellen. Dann wurde das Quarzrohr mit einem Abstand von 4,0 cm unter die Lichtquelle platziert. In bestimmten Zeitintervallen wurden 3 ml Lösung aus dem Quarzröhrchen entnommen, gefolgt von einer Zentrifugation, um die Partikel zu entfernen. Dann wurde die Konzentration von RhB, die in der Lösung verblieb, und seine Absorption bei 554 nm auf einem Shimadzu UV-2600-Spektrophotometer untersucht. Um ein ungefähr äquivalentes Lösungsvolumen sicherzustellen, wurde die analysierte Lösung nach jedem Assay schnell in das Quarzrohr zurückgegossen.
Das Verhältnis der RhB-Konzentration C in jedem Intervall auf die Anfangskonzentration C 0 wurde verwendet, um die photokatalytische Abbaueffizienz anzugeben, die als C . ausgedrückt wurde /C 0 . Nach dem photokatalytischen Abbauexperiment wurde das resultierende Produkt mit Ethylalkohol und entionisiertem Wasser gewaschen, gefolgt vom Trocknen an der Luft für den nächsten photokatalytischen Abbauprozess, um die Recyclingstabilitätsleistung des resultierenden Produkts zu untersuchen.
Selbstreinigungsleistung
Benetzungseigenschaft
Die Benetzungseigenschaft von CuS/TiO2 /PVDF-Fasern wird durch Testen des Kontaktwinkels der Tröpfchen (einschließlich H2 O, RhB, MO und MB) auf dem Produkt bei Umgebungstemperatur durch ein optisches Kontaktwinkelinstrument von Theta Attension.
Selbstreinigungsleistung
Die Selbstreinigungsleistung des resultierenden Produkts wird durch Abbau von Oberflächenfarbstofftröpfchen und Entfernen von Oberflächenstaub bewertet. Die RhB-, MO- und MB-Farbstofftröpfchen mit einer Konzentration von 10 mg L −1 wurden auf das CuS/TiO2 . getropft /PVDF-Fasern und unter der 9-W-Weißlicht-LED bestrahlt. In bestimmten Zeitintervallen wurde eine optische Fotografie aufgenommen, die verwendet wurde, um die Selbstreinigungsleistung des so hergestellten Produkts gegenüber der Oberflächenverunreinigung zu untersuchen. Zur Oberflächenentstaubung des CuS/TiO2 /PVDF-Fasern wurde der Staub vor der Messung auf die Oberfläche der Probe gestreut. Dann wurde ein Tropfen Wasser auf die Oberfläche des Produkts getropft. Die Probe wurde leicht geneigt, damit sich die Tröpfchen auf der Probenoberfläche bewegen und den Staub entfernen, wodurch die Materialoberfläche sauber wird.
Ergebnisse und Diskussion
Struktur- und Morphologiemerkmale
Die XRD-Muster von TiO2 /PVDF-Fasern, Cu 0,1, Cu 0,5 und Cu 1 sind in Fig. 1 dargestellt. Es ist offensichtlich, dass außer dem Beugungspeak von PVDF und TiO2 . kein offensichtlicher Beugungspeak detektiert wird wie in Abb. 1 Kurve a dargestellt. Der Beugungspeak um 20,8° kann der β-Phase von PVDF zugeordnet werden, und der Beugungspeak bei 25,67°, 37,8°, 48,2° und 54,6° kann der (101), (004), (200), und (211) Kristallflächen der Anatas-Phase TiO2 (PDF-Karte 21-1272, JCPDS) bzw. [35,36,37]. Vergleicht man Kurve b mit Kurve a, gibt es zwei offensichtliche Beugungspeaks in der Nähe der Beugungswinkel von 29,4° und 32,6° in Kurve b, die auf die (102) und (006) Kristallflächen von hexagonalem CuS indiziert werden können (PDF-Karte 06- 0464, JCPDS). Darüber hinaus ist es erwähnenswert, dass der Beugungspeak bei 48,3 in Kurve b stärker ist als der in Kurve a, was hauptsächlich darauf zurückzuführen ist, dass die Beugungspeaks von TiO2 und CuS werden bei diesem Beugungswinkel überlagert. Diese weisen darauf hin, dass CuS erfolgreich auf dem TiO2 . gebildet wird /PVDF-Fasern. Darüber hinaus erscheint ein Beugungspeak allmählich in der Nähe des Beugungswinkels 27,7° in den Kurven c und d, verglichen mit der Kurve b, die (101) Kristallflächen von CuS entspricht. Inzwischen wird der Beugungspeak nahe 32,6° ebenfalls allmählich zu zwei unterschiedlichen Peaks bei 31,9° bzw. 32,9°, entsprechend den (103) und (006) Kristallflächen von CuS. Basierend auf den oben genannten Ergebnissen kann festgestellt werden, dass mit der Zunahme der Cu- und S-Quellen die Kristallisation von CuS besser wird.
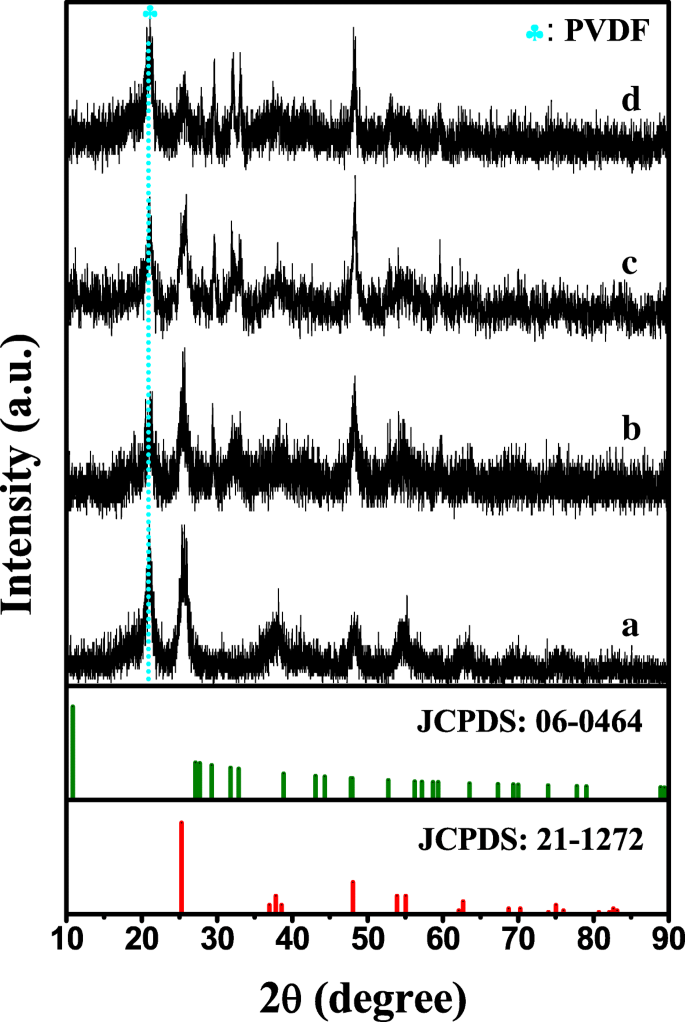
XRD-Muster von (a) TiO2 /PVDF-Fasern, (b) Cu 0,1, (c) Cu 0,5 und (d) Cu 1
Die typischen REM-Bilder von TiO2 /PVDF-Fasern, Cu 0.1, Cu 0.5 und Cu 1 sind in Abb. 2 dargestellt. Wie aus Abb. 2a ersichtlich, ist das TiO2 /PVDF-Fasern sind ungeordnet angeordnet mit einer relativ rauen Oberfläche (dargestellt im Einschub), die hauptsächlich auf die Bildung von TiO2 . zurückzuführen ist in den Fasern. Beim Vergleich von Fig. 2b mit Fig. 2a wird die Oberfläche der Fasern in Fig. 2b rauer und eine kleine Menge an CuS-Partikeln ist auf der Oberfläche der Fasern erschienen, die in der eingefügten Illustration leicht zu finden sind. Wenn die Menge der Cu-Quelle auf 0,5 mmol ansteigt, kann im Vergleich zu Fig. 2b eine sehr große Änderung festgestellt werden, dass eine große Menge an CuS-Partikeln die Oberfläche von TiO2 . bedeckt /PVDF-Fasern, wie in Abb. 2c gezeigt. Darüber hinaus ist aus der Nebenabbildung ersichtlich, dass eine kleine Menge von hexagonal geschichteten CuS-Nanoblumen auf der Oberfläche von TiO2 . erscheint /PVDF-Fasern. Wenn die Menge der Cu-Quelle auf 1 mmol ansteigt, ist offensichtlich eine große Anzahl von aggregierten CuS-Partikeln auf der Faseroberfläche erschienen (dargestellt in Abb. 2d). Durch sorgfältige Untersuchung des Einschubs von Abb. 2d bestehen diese großen CuS-Nanoblumen aus vielen hexagonalen lamellaren CuS. Basierend auf den obigen Ergebnissen kann festgestellt werden, dass die Zunahme der Cu-Quelle einerseits die Menge an CuS auf der Oberfläche der Faser kontinuierlich erhöht und andererseits die Kristallisation und das Wachstum von CuS auf der Oberfläche der Faser verbessert Oberfläche der Faser, was zu einer allmählichen Veränderung der Morphologie von CuS von Partikeln zu einer hexagonalen Lamellenstruktur führt.

REM-Bilder von a TiO2 /PVDF-Fasern, b Cu 0,1, c Cu 0,5 und d Cu 1
Die Morphologie von CuS/TiO2 /PVDF-Faser wird weiter durch TEM und HRTEM untersucht, wie in Abb. 3 dargestellt. Wie in Abb. 3a dargestellt, ist es offensichtlich, dass einige CuS-Partikel mit ungleichmäßiger Größe auf der Oberfläche von TiO2 . verteilt sind /PVDF-Faser. Die Kontaktposition zwischen CuS und TiO2 /PVDF-Faser wird vergrößert, um ein hochauflösendes Bild zu erhalten, wie in Fig. 3b gezeigt. Aus dem hochauflösenden TEM-Bild ist ersichtlich, dass CuS und TiO2 eine deutliche Kristallgrenze haben. Durch Messung des Interplanarabstands kann festgestellt werden, dass es hauptsächlich zwei Arten von Kristallflächen von TiO2 . gibt mit dem Zwischenebenenabstand von 0,35 bzw. 0,23 nm, entsprechend den (101) und (004) Kristallflächen von TiO2 . Der Winkel zwischen diesen beiden Kristallflächen beträgt etwa 68°, was mit der Literatur übereinstimmt [38]. Außerdem gibt es hauptsächlich eine Kristallfläche mit einem Kristallinterplanarabstand von etwa 0,31 nm, entsprechend der (102)-Kristallfläche von CuS. Daher stimmen die TEM- und HRTEM-Studien mit den XRD-Messungen überein.

TEM-Aufnahme von Cu 1 a und hochauflösendes TEM-Bild von Cu 1 b
Die XPS-Analyse wird verwendet, um die Informationen über die chemische Zusammensetzung und die Bindungskonfiguration der resultierenden Produkte zu untersuchen. Charakteristische Peaks von Cu, S, Ti, O, F und C sind in den XPS-Spektren deutlich zu erkennen, wie in Zusatzdatei 1 gezeigt:Abbildung S3. Die hochauflösenden XPS-Spektren von Ti 2p, O 1s, Cu 2p und S 2p sind in Abb. 4 dargestellt. Wie in Abb. 4a zu sehen ist, können die Peaks bei 459,0 und 464,7 eV Ti 2p<. zugeordnet werden sub>3/2 und Ti 2p1/2 , bzw. [39]. Der Peak von O1s kann in zwei Peaks (dargestellt in Abb. 4b) unterteilt werden, die dem Ti-O von TiO2 . entsprechen (530,2 eV) und Hydroxylgruppe (531,8 eV) im Produkt wie hergestellt [40, 41]. In Cu 2p-Profilen (Abb. 4c) sind die Peaks bei 932,0 und 952,0 eV auf 2p3/2 . indiziert und 2p1/2 von Cu 2+ , bzw. [42]. Indessen können für die Peaks des S-Elements (in Fig. 4d dargestellt) die breiten Spektren, die um 162,1 eV liegen, in zwei Peaks von 161,9 bzw. 163,5 eV unterteilt werden, entsprechend dem 2p3/2 und 2p1/2 von S 2− [43]. Darüber hinaus wird ein schwacher Peak bei 168,8 eV nachgewiesen, der die Zwischenprodukte sein können, die von Thioharnstoff bei der hydrothermalen Reaktion produziert werden [44]. Darüber hinaus ist die Atomkonzentration aus hochauflösenden XPS-Spektren in Tabelle 1 dargestellt. Es ist leicht zu erkennen, dass das Verhältnis von O- zu Ti-Atomen mehr als 2: 1 beträgt, was hauptsächlich auf die Anwesenheit von O-Atomen in PVDF zurückzuführen ist [ 45]. Das Verhältnis von S- zu Cu-Atomen beträgt etwa 1,27, also etwas mehr als 1:1. Der Hauptgrund ist, dass im Vorbereitungsprozess eine überschüssige S-Quelle (das Verhältnis von Cu-Quelle zu S-Quelle beträgt 1:2) verwendet wird, was dazu führt, dass etwas S auf der Oberfläche der Probe verbleibt. Die oben erwähnten XPS-Ergebnisse bestätigen weiter das Vorhandensein von CuS, TiO2 , und PVDF in der Cu 1 -Probe, die gut mit den XRD- und TEM-Ergebnissen übereinstimmen.
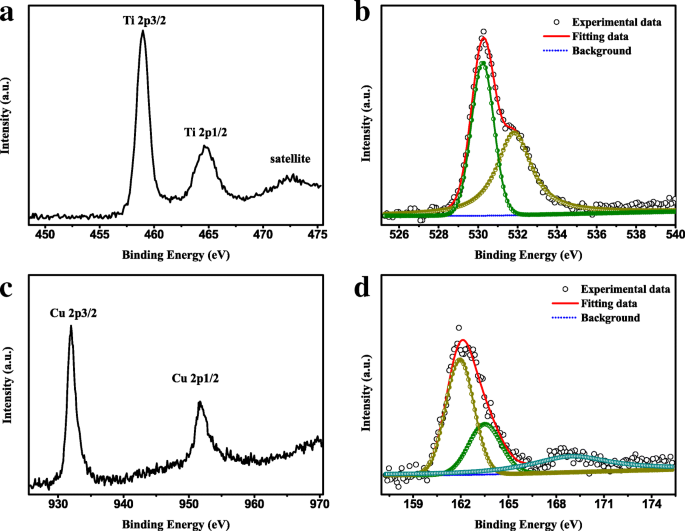
Hochauflösende XPS-Spektren von a Ti 2p, b O 1s, c Cu 2p und d S 2p in Cu 1-Probe
Optische Eigenschaften
Die optischen Eigenschaften von TiO2 /PVDF, Cu 0.1, Cu 0.5 und Cu 1 werden durch diffuse UV-Vis-Reflexionsspektren untersucht, die mit der Kubelka-Munk-Funktion [35, 46] in Absorptionswerte umgewandelt werden, wie in Abb. 5 dargestellt stellen fest, dass der Absorptionswert der mit CuS zusammengesetzten Proben viel höher ist als der von TiO2 /PVDF-Fasern im sichtbaren Lichtbereich, was darauf hindeutet, dass der CuS-Verbundstoff die Lichtsammelleistung von TiO2 . stark verbessert . Darüber hinaus steigt der Extinktionswert von Proben mit CuS-Zusammensetzung kontinuierlich mit der Zunahme der Menge an Cu-Quelle.
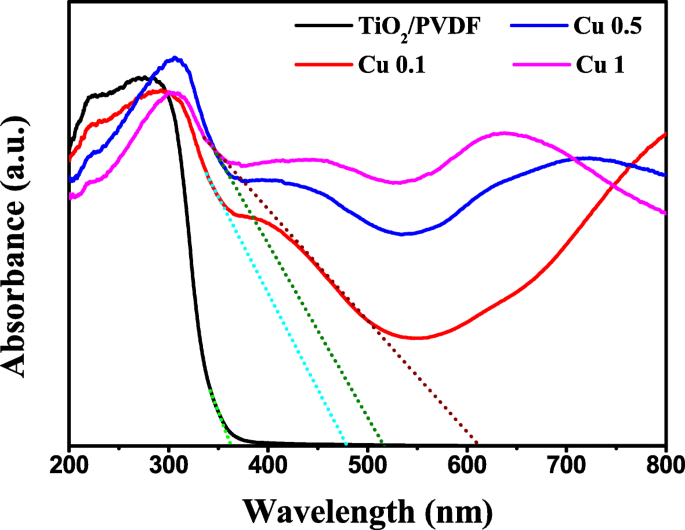
UV-Vis diffundiert Reflexionsspektren von TiO2 /PVDF, Cu 0.1, Cu 0.5 und Cu 1
Nach der bisherigen Literatur ist Anatas TiO2 gehört zu den Halbleitern mit indirekter Bandlücke, während CuS zu den Halbleitern mit direkter Bandlücke gehört [47, 48]. Ihre Energiebandlücke (Eg) wird durch die Gleichung Eg = 1240/λ . gemessen g (eV), wobei λ g ist die aus dem Schnittpunkt zwischen der Tangente der Absorptionskurve und der Abszissenkoordinate berechnete Absorptionskante [49]. Die Absorptionskante und die Energiebandlücke der resultierenden Proben sind in Tabelle 2 dargestellt.
Wie aus Tabelle 2 ersichtlich, ist die Energiebandlücke von CuS/TiO2 /PVDF-Faser ist kleiner als die in TiO2 /PVDF-Faser und die Absorptionskante von CuS/TiO2 Die /PVDF-Faser verschiebt sich mit zunehmender Menge der Cu-Quelle allmählich zu der langen Wellenlänge. Es ist möglich, dass mit zunehmender Menge an Cu-Quelle CuS immer enger auf die Oberfläche von TiO2 . gewickelt wird /PVDF-Faser (wie in REM-Bildern dargestellt), die den Grenzflächenkontakt zwischen TiO2 . herstellt und CuS werden größer, was zur Absorptionskante von TiO2 . führt Übergang zu einer langen Wellenlänge [50]. Außerdem wird mit der Zunahme der Cu-Quelle die Kristallinität von CuS besser, was die Energiebandlücke des resultierenden Produkts verringert [51, 52].
Die PL-Spektren werden üblicherweise verwendet, um die Rekombination photogenerierter Elektron-Loch-Paare im Halbleiter zu untersuchen [53, 54]. Die PL-Spektren von TiO2 /PVDF-, Cu 0.1-, Cu 0.5- und Cu 1 -Proben sind in Abb. 6 dargestellt. In Abb. 6 ist zu sehen, dass es im TiO2<. einen Emissionspeak um 394 nm (~ 3.2 eV) gibt /sub> /PVDF-Faser und Cu 0.1 weist auch hier einen schwachen Emissionspeak auf. Die Position dieses Emissionspeaks liegt nahe der Bandkantenemission von TiO2 in diesen beiden Proben und sollte die Emission von TiO2 . nahe der Bandkante sein [55, 56]. In Cu 0.5- und Cu 1 -Proben verschwinden diese Emissionspeaks. Darüber hinaus gibt es fünf Emissionspeaks im TiO2 /PVDF-Faser zwischen 449 nm (2,76 eV) und 492 nm (2,52 eV), die durch Sauerstofffehlstellen (VO ) während des Präparationsprozesses erzeugte Defekte [57, 58]. In den Proben von Cu 0.1, Cu 0.5 und Cu 1 existieren diese fünf Emissionspeaks immer noch, während die Intensität dieser fünf Emissionen stark abnimmt, hauptsächlich aufgrund der CuS-Beschichtungen auf der Oberfläche des TiO2 /PVDF-Faser und schwächt die Intensität des Emissionspeaks.
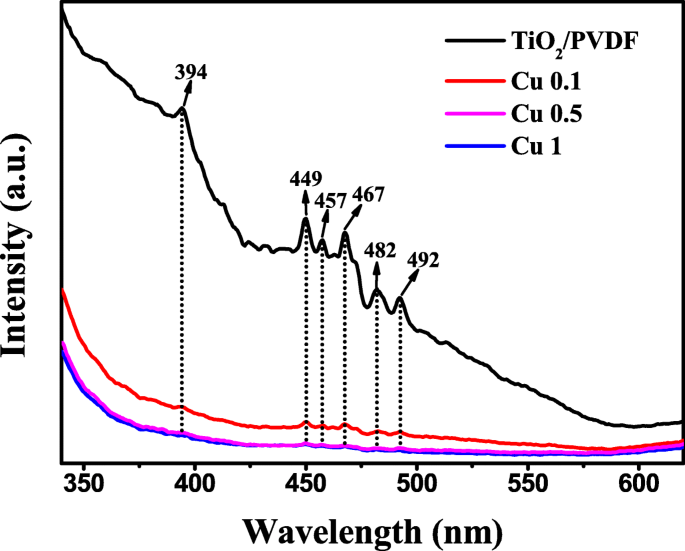
PL-Spektren von TiO2 /PVDF, Cu 0.1, Cu 0.5 und Cu 1
Außerdem ist die Intensität der PL-Spektren des CuS/TiO2 /PVDF-Fasern ist viel niedriger als die von TiO2 /PVDF-Faser, was beweist, dass der Verbund von CuS die Trenneffizienz photogenerierter Elektron-Loch-Paare erhöht und die Rekombination photogenerierter Elektron-Loch-Paare unterdrückt, was auch die photokatalytische Fähigkeit von TiO2 . bedeutet /PVDF-Faser wird verbessert.
Photokatalytische Leistungen
Die photokatalytischen Leistungen der so hergestellten Proben sind in Abb. 7 dargestellt. In Abb. 7a ist zu sehen, dass sich die Konzentration von RhB unter sichtbarem Licht nicht ändert, was bedeutet, dass es unter sichtbarem Licht ohne spontanen Abbau sehr stabil war. Interessant ist jedoch, dass TiO2 /PVDF-Faser sollte nur eine ultraviolette photokatalytische Fähigkeit aufweisen, aber eine photokatalytische Fähigkeit mit sichtbarem Licht haben, und ihr photochemischer Abbau von RhB erreichte 52,9% in 50&supmin;min. Im Vergleich zu TiO2 /PVDF-Faser haben die Cu 0.1- und Cu 0.5-Proben eine schnellere photokatalytische Geschwindigkeit und die photokatalytische Effizienz von RhB in 50 min beträgt 85,7 % bzw. 99,2 %. Wie aus Abb. 7a ersichtlich ist, weist die Cu 1 -Probe die höchste Photoabbaurate auf, die RhB in 40 Minuten vollständig abbaut.
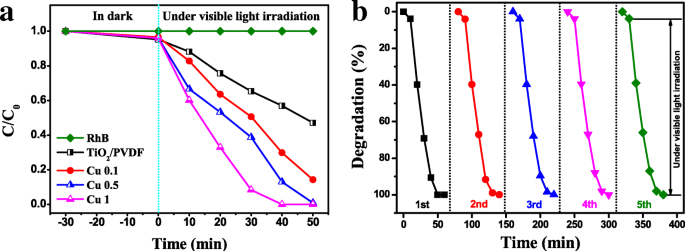
a Photokatalytische Abbaukurven von RhB über den Proben:RhB ohne Photokatalysator, TiO2 /PVDF, Cu 0.1, Cu 0.5 und Cu 1. b Das Recycling-Experiment mit der Probe Cu 1
Darüber hinaus kann der photokatalytische Abbau von RhB auch durch einen kinetischen Prozess pseudo-erster Ordnung dargestellt werden. Die Gleichung lautet wie folgt [59]:
$$ -\ln \left(C/{C}_0\right)=kt $$wo k und t sind die Reaktionsgeschwindigkeitskonstante bzw. die Messzeit; C 0 und C sind die Konzentration von RhB zu Beginn und t Zeit. Gemäß der Gleichung wird die Reaktionsgeschwindigkeitskonstante des RhB-Abbaus durch den so hergestellten Photokatalysator berechnet, wie in Zusatzdatei 1 gezeigt:Abbildung S4. Es ist ersichtlich, dass die Reaktionsgeschwindigkeitskonstante von Cu1, Cu0.5, Cu0.1 und TiO2 /PVDF ist 2,9 × 10 −2 , 1,8 × 10 −2 , 1,6 × 10 −2 , und 9,8 × 10 −3 min −1 , bzw. Es ist offensichtlich, dass die Reaktionsgeschwindigkeit von Cu1 etwa dreimal höher ist als die von TiO2 /PVDF.
Die photokatalytischen Recyclingexperimente werden an der Cu1-Probe fünfmal durchgeführt, wie in Abb. 7b dargestellt. Es ist ersichtlich, dass die photokatalytische Effizienz der Cu1-Probe bei 40 min leicht abnimmt, aber bei 50 min bei 100 % bleibt, was darauf hindeutet, dass das so hergestellte Produkt eine gewisse Recyclingstabilität aufweist.
Normalerweise sind die photoinduzierten Löcher (h + ), Superoxidanionenradikale (\( {\mathrm{O}}_2^{-\cdotp}\)) und Hydroxylradikale (OH·) werden als die wichtigsten aktiven Spezies im photokatalytischen Prozess angesehen. [60] Um hier den photokatalytischen Mechanismus des TiO2 . zu untersuchen /PVDF und CuS/TiO2 /PVDF-Fasern, Kontrollversuche mit Ethylendiamintetraessigsäure (EDTA), Stickstoff (N2 .) ) und tertiäres Butanol (tBuOH) als einzelne Radikalfänger für h + , \( {\mathrm{O}}_2^{-\cdotp } \) bzw. OH·, wie in Zusatzdatei 1 dargestellt:Abbildung S5. Es ist ersichtlich, dass \( {\mathrm{O}}_2^{-\cdotp}\) den größten Einfluss auf die photokatalytische Effizienz im TiO2 . hat /PVDF-System, gefolgt von h + und OH·. Während in CuS/TiO2 /PVDF-System, h + haben den größten Einfluss auf die photokatalytische Effizienz, gefolgt von OH· und \({\mathrm{O}}_2^{-\cdotp}\).
Es wird vermutet, dass ein möglicher Mechanismus für die photokatalytischen Mechanismen des TiO2 . verantwortlich ist /PVDF-Faser und CuS/TiO2 /PVDF-Faser unter Bestrahlung mit sichtbarem Licht, wie in Abb. 8 dargestellt. Für TiO2 /PVDF-Faser gibt es eine große Anzahl von Sauerstofffehlstellendefekten (VO ) in TiO2 /PVDF-Faser, die in den PL-Spektren bestätigt werden kann. Diese Sauerstoffleerstellendefektniveaus liegen zwischen dem Valenzband (VB) und dem Leitungsband (CB) von TiO2 . Bei Bestrahlung mit sichtbarem Licht werden die Elektronen vom VB von TiO2 . angeregt und von diesen Defekten eingefangen, wodurch ein Loch in der VB von TiO2 . zurückbleibt . Ein Teil der photogenerierten Elektronen und Löcher wandert an die Oberfläche von TiO2 und reagieren mit Sauerstoffmolekülen in der Lösung zu \( {\mathrm{O}}_2^{-\cdotp} \) oder reagieren mit Wassermolekülen zu OH·, wodurch RhB abgebaut wird.
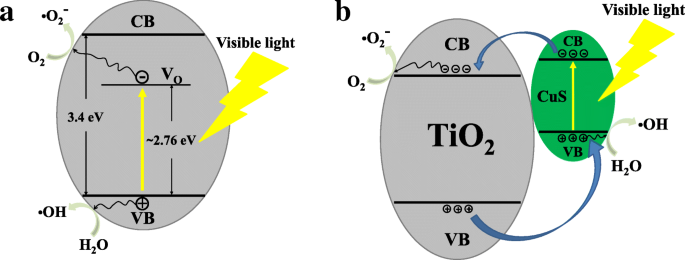
Diagramm des Trennungs- und Transmissionsprozesses eines photogenerierten Elektron-Lochs in a TiO2 /PVDF-Faser und b CuS/TiO2 /PVDF-Faser
Da die schmale Bandlücke CuS auf der Oberfläche des TiO2 . aufgetragen ist, /PVDF-Faser absorbiert das CuS sichtbares Licht, so dass Elektronen auf dem VB von CuS zu seinem CB angeregt werden und Löcher in dem VB hinterlassen. Aufgrund der CB-Energie von TiO2 niedriger als die von CuS ist, werden Elektronen von der CB von CuS auf die CB von TiO2 . übertragen , und Löcher werden von der VB von TiO2 . übertragen zum VB von CuS [40]. Die auf das CB von TiO2 . übertragenen Elektronen reagieren mit den Sauerstoffmolekülen in der Lösung zu \( {\mathrm{O}}_2^{-\cdotp}\). Und die Löcher, die zum VB von CuS wandern, reagieren mit den Wassermolekülen in der Lösung, um OH· zu bilden, wodurch RhB abgebaut wird.
Das zusammengesetzte CuS zum TiO2 /PVDF-Faser verengt einerseits die Bandlücke des Materials und vergrößert den Absorptionsbereich des Lichts. Andererseits wird die Fähigkeit des Materials, durch Licht erzeugte Elektronenlöcher zu trennen, verbessert, was bedeutet, dass die photokatalytische Fähigkeit verbessert wird.
Selbstreinigungsleistungen
Die Benetzungseigenschaft der Oberfläche entscheidet über den Selbstreinigungsmechanismus. Der statische Kontaktwinkel, also der Kontaktwinkel zwischen Festkörper und Flüssigkeit, ist ein Hauptparameter zur Untersuchung des Oberflächenbenetzungsverhaltens. Die Kontaktwinkel von H2 O, RhB, MO und MB für TiO2 /PVDF-Fasern, Cu 0.1 und Cu 1 sind in Abb. 9 und Tabelle 3 gezeigt. Es ist zu erkennen, dass die drei Proben alle Hydrophobie aufweisen. Im Vergleich zu TiO2 /PVDF-Fasern nahm die Hydrophobie von Cu 0.1 und Cu 1 leicht ab.
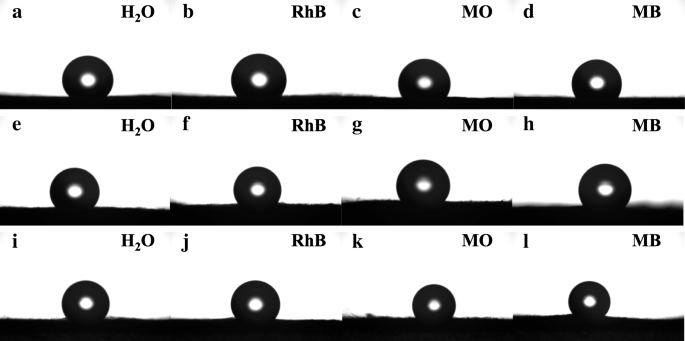
Die optischen Bilder des statischen Kontaktwinkels für a –d TiO2 /PVDF-Fasern, e –h Cu 0,1 und i –l Cu 1
Darüber hinaus wurden die Selbstreinigungseigenschaften von Cu 1 untersucht, indem 10 mg L −1 von RhB, MO und MB auf die Oberfläche des resultierenden Produkts unter Beleuchtung mit sichtbarem Licht, wie in Abb. 10 dargestellt. Es ist offensichtlich, dass die Farben dieser Farbstoffe in etwa 120 min fast verschwinden und nur transparente Tröpfchen auf der Oberfläche von das Material. Wie wir wissen, werden die Photokatalysatoren beim Photokatalyseprozess leicht an Farbstoffmoleküle angeheftet und verursachen eine Selbstverschmutzung, was ihre photokatalytische Leistung verringert. Die so hergestellten Produkte können die photokatalytische Wirkung im praktischen Einsatz aufgrund ihrer Selbstreinigungsfähigkeit stark verbessern.
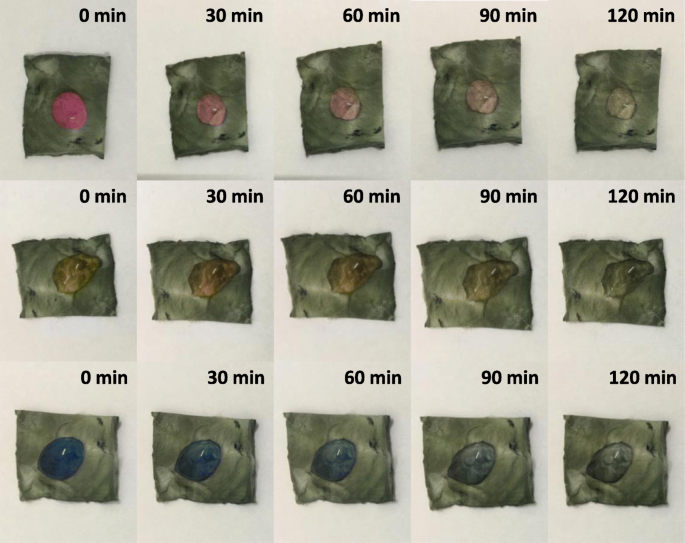
Die optische Fotografie des RhB-, MO- und MB-Tröpfchens auf der Oberfläche von Cu 1 unter Beleuchtung mit sichtbarem Licht
Darüber hinaus können aufgrund der Hydrophobie der Cu 1 -Oberfläche Wassertröpfchen auf der Produktoberfläche verbleiben. Daher kann der Staub von der Probenoberfläche durch Rollen der Wassertröpfchen auf der Oberfläche gereinigt werden, um einen Selbstreinigungseffekt zu erzielen. Wie in Abb. 11a dargestellt, zeigte die Probe, bevor Wasser auf die Oberfläche der Probe getropft wurde, eine saubere grüne Oberfläche. Um den Selbstreinigungseffekt zu zeigen, wurde eine Staubschicht auf die Probenoberfläche gestreut. Anschließend wurde ein Wassertropfen auf die Oberfläche der Probe getropft. Wird die Probe leicht geneigt, rollt der Wassertropfen auf der Probenoberfläche und bringt den Staub nach unten, um die ursprüngliche grüne Oberfläche darzustellen. Dies bedeutet, dass das zubereitete Produkt bei der tatsächlichen Verwendung die anhaftende Farbe oder den anhaftenden Staub durch Sonnenlicht oder Regen entfernen kann, wodurch die Wartungskosten gesenkt werden.

Das optische Foto eines Wassertropfens, der auf der Oberfläche von Cu 1 rollt, um Staub zu entfernen:a saubere Probe, b Probe mit staubiger Oberfläche, c Tropfen auf staubbedeckte Proben und d die Tröpfchen rollen den Staub weg und legen die saubere Oberfläche der Probe frei
Schlussfolgerungen
CuS-Nanoblumen wurden mit TiO2 . beladen /PVDF-Fasern durch einstufiges hydrothermales Verfahren auf elektrogesponnenen TBOT/PVDF-Fasern. Die Methode ist sehr einfach und bequem. Darüber hinaus ist das CuS/TiO2 /PVDF-Fasern wurden bei niedrigerer Temperatur hergestellt, um ihre Flexibilität zu gewährleisten. Im Herstellungsprozess bestimmt die Menge der Cu-Quelle die Menge und kristalline Qualität von CuS, das auf TiO2 . getragen wird /PVDF-Fasern. Wenn die Menge der Cu-Quelle 1 mmol erreicht, wird das auf TiO2 . getragene CuS /PVDF-Fasern war eine nanoblumenartige Struktur, die von einer hexagonalen Schicht gebildet wurde. Der Verbund von CuS verengt die Bandlückenenergie von TiO2 und verbessert die Lichtsammelfähigkeit von TiO2 . Außerdem erhöht der Verbund von CuS die Trenneffizienz der photogenerierten Elektron-Loch-Paare von TiO2 , entsprechend verbessert die photokatalytische Fähigkeit von TiO2 unter Bestrahlung mit sichtbarem Licht. Die photokatalytische Reaktionsgeschwindigkeit von CuS/TiO2 /PVDF-Fasern zu RhB ist dreimal höher als die von TiO2 /PVDF-Fasern unter Bestrahlung mit sichtbarem Licht. Darüber hinaus sind die photokatalytischen Eigenschaften von CuS/TiO2 . nach fünfmaligem Recycling /PVDF-Fasern nahmen nicht ab, was hauptsächlich auf ihre Flexibilität und Wiederverwendbarkeit zurückzuführen ist. Darüber hinaus hat das so hergestellte Material einen sehr guten Selbstreinigungseffekt auf die an der Oberfläche haftenden Farbstoffe und Staub, wodurch die Wartungskosten des Materials erheblich gesenkt werden können. Es kann leicht festgestellt werden, dass das so hergestellte Produkt nicht nur eine gute photokatalytische Aktivität aufweist, sondern auch eine Selbstreinigungsleistung unter sichtbarem Licht aufweist. Die in diesem Papier präsentierten Ergebnisse bieten eine neue Perspektive für die Untersuchung der Anwendung neuartiger flexibler, recycelbarer und selbstreinigender photokatalytischer Materialien für die Umweltverträglichkeit.
Verfügbarkeit von Daten und Materialien
Die während der laufenden Studie generierten und/oder analysierten Datensätze sind auf begründete Anfrage bei den entsprechenden Autoren erhältlich.
Abkürzungen
- CuS:
-
Kupfersulfid
- DRS:
-
Diffuse Reflexionsspektren
- MB:
-
Methylblau
- MO:
-
Methylorange
- PL:
-
Photolumineszenzspektren
- PVDF:
-
Polyvinylidenfluorid
- RhB:
-
Rhodamin B
- SEM:
-
Rasterelektronenmikroskopie
- TBOT:
-
Tetrabutylorthotitanat
- TEM:
-
Transmissionselektronenmikroskopie
- TiO2 :
-
Titandioxid
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Einstufige Elektrospinnroute von SrTiO3-modifizierten Rutil-TiO2-Nanofasern und ihre photokatalytischen Eigenschaften
- Hohe photokatalytische Leistung von zwei Arten von Graphen-modifizierten TiO2-Komposit-Photokatalysatoren
- Auf dem Weg zu TiO2-Nanofluiden – Teil 2:Anwendungen und Herausforderungen
- Die Auswirkungen des Li/Nb-Verhältnisses auf die Herstellung und photokatalytische Leistung von Li-Nb-O-Verbindungen
- Verstärkte photokatalytische Aktivitäten durch Au-Plasmon-Nanopartikel auf einer mit MoO3 beschichteten TiO2-Nanoröhren-Photoelektrode
- Herstellung und photokatalytische Leistung von Hohlstruktur-LiNb3O8-Photokatalysatoren
- Ein neuartiger Bi4Ti3O12/Ag3PO4-Heteroübergang-Photokatalysator mit verbesserter photokatalytischer Leistung
- Strukturelle und im sichtbaren Infrarotbereich sichtbare optische Eigenschaften von Cr-dotiertem TiO2 für farbige kühle Pigmente
- TiO2-Nanoröhren-Arrays:Hergestellt durch weiche-harte Schablone und die Korngrößenabhängigkeit der Feldemissionsleistung
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität



