Neuer Immunsensor-Fluoreszenznachweis von Tumormarker-Cytokeratin-19-Fragment (CYFRA 21-1) über Kohlenstoff-Quantenpunkte/Zinkoxid-Nanokomposit
Zusammenfassung
Die schnelle Erkennung von Lungenkrebs im Frühstadium mit dem Antigen Cytokeratin-19-Fragment (CYFRA 21-1) als Tumormarker im Humanserum spielt eine wichtige Rolle für das Überleben von Patienten und eine schnelle operative Reaktion. Diese Studie zielte darauf ab, das mit grünen synthetisierten Kohlenstoffquantenpunkten konjugierte Zinkoxid-Nanokomposit als hochempfindliche Fluoreszenz-Immunsensorlösung für die schnelle Bestimmung des CYFRA 21-1-Antigens in Humanserum einzusetzen. Die vorgeschlagene Methode wurde durch Anwendung einer hydrothermalen Methode zur Herstellung von Kohlenstoffquantenpunkten unter Verwendung von Citrus Lemon . durchgeführt Perikarp. Die gebildeten Kohlenstoff-Quantenpunkte wurden bei der Reduktion und Stabilisierung von Zinkacetat verwendet, um Kohlenstoff-Quantenpunkte-Zinkoxid-Nanokomposit zu synthetisieren. Um ein Sandwich-Capping-Antikörper-Antigen-Antikörper-Immunsensorsystem zu bilden, wurde ein CYFRA 21-1-Antigen durch Immobilisieren eines nicht-konjugierten monoklonalen Antikörpers BM 19.21 auf der Oberfläche von Kohlenstoff-Quantenpunkten-Zinkoxid-Nanokomposit und eines anderen monoklonalen Antikörpers KS 19.1 gefangen wurde auf die Mikrotiter-Well-Oberfläche aufgetragen. Dieses System verfügt über eine abstimmbare Fluoreszenzfunktion, die bei Anregung und Emission von λex . aufgezeichnet wird = 470 und λem = 520 nm. Das vorgeschlagene Nanokomposit-Fluoreszenz-Immunsensorsystem zeigte eine lineare Beziehung von 0,01–100 ng mL –1 mit einer Nachweisgrenze von 0,008 ng ml −1 . Das vorgeschlagene Immunsensorsystem basierend auf Kohlenstoffquantenpunkten-Zinkoxid-Nanokomposit bietet einen vielversprechenden Ansatz für die schnelle Diagnose von Lungenkrebs durch den Nachweis von CYFRA 21-1 in Humanserum.
Einführung
Lungenkrebs ist die öffentlichste und aggressivste Krebsart mit großen Herausforderungen in der medizinischen Behandlung. Tumorrezidive und Metastasen gelten als die häufigsten Todesursachen bei Lungenkrebspatienten [1]. Das Tumormarker-Cytokeratin-19-Fragment (CYFRA 21-1) ist ein Fragment, das in vielen normalen sowie malignen Epithelzellen vorkommt [2]. Sie kann unter Verwendung eines immunradiometrischen Sandwich-Assays abgeschätzt werden. Die frühen Studien zeigten, dass CYFRA 21-1 in malignen Stadien des Lungenkrebses in den Blutkreislauf der Patienten freigesetzt und in deren Serum erhöht ist [3]. Daher ist es möglich, das Überleben von Lungenkrebspatienten durch Früherkennung und folglich schnelle chirurgische Reaktion zu verbessern [4].
Bisher wurden nur wenige Techniken zum Nachweis von CYFRA 21-1 beschrieben, darunter Enzymimmunoassays [5], Elektrochemilumineszenz-Immunoassays [6] und immunradiometrische Assays [7]. Eine vorteilhafte Strategie zur Steigerung und Verbesserung der Sensitivität von CYFRA 21-1 in Humanserum gibt noch immer Anlass zur Sorge.
In den letzten Jahren wurden in fast allen Lebensbereichen große Fortschritte und ein explosives Wachstum der Nanotechnologie erzielt [8]. Zu diesen Bereichen gehören Drug-Delivery-Systeme [9], pharmazeutische Analyse [10], katalytische Aktivitätsreaktionen [11], medizinische Anwendungen [12], Krebstumormarker [13] und Gewebebildgebung [14].
Heutzutage haben auf Fluoreszenz (FL) basierende Sensortechniken viele Forscher aufgrund ihres einfachen Designs und ihrer hervorragenden Empfindlichkeit angezogen. Für die biologische Überwachung wurden verschiedene sensorische FL-Materialien entwickelt und synthetisiert. Die FL-Systeme zur biologischen Bestimmung sind stark lumineszierend, wasserdispergierbar, chemisch stabil und ungiftig [15]. Es gibt verschiedene immunsensorische Sonden auf Fluoreszenzbasis zum Nachweis von Biomarkern. Der heterogene kompetitive Assay wird durchgeführt, indem Fängermoleküle auf der Oberfläche immobilisiert und dann mit Fluorophor-konjugierten Biomarkern inkubiert werden. Die Konkurrenz zwischen den freien und konjugierten Biomarkern um die Bindung an die Fängermoleküle verringert die Fluoreszenzintensität mit der Biomarkerkonzentration [16]. Der heterogene Sandwich-Assay basiert auf der Inkubation von Fängermolekülen und interessierender Lösung, die einen Komplex mit Biomarkern bilden. Folglich nimmt die Fluoreszenzintensität mit der Biomarkerkonzentration zu [17].
Im homogenen kompetitiven Assay wurden zwei verschiedene Fluorophor A-konjugierte Fängermoleküle mit Fluorophor B-konjugierten Biomarkern konjugiert und die Lösung erhöht die Fluoreszenz mit Biomarkerkonzentrationen [18]. Diese Techniken zeigten jedoch bestimmte Nachteile, einschließlich ihrer langen experimentellen Zeit, des Fehlens einer Multiplex-Detektion, ihrer Komplexität und manchmal relativ falscher Ergebnisse. Fortschritte in der Nanotechnologie ermöglichten es den Forschern, neuartige Fluoreszenz-Immunsensorsonden mit einzigartigen optischen Eigenschaften zu entwickeln [19]. Seit der ersten Verwendung von Quantenpunkten in der Biomoleküldetektion haben sie großes Interesse geweckt, da ihre optischen Eigenschaften eine hohe Flexibilität bei der Auswahl der geeigneten Wellenlänge, ausgezeichnete Markierungen für die Multiplex-Detektion, Biokompatibilität und Targeting-Kapazität bieten [20].
Kohlenstoffquantenpunkte (CQDs) haben ausgezeichnete chemische, physikalische, optische, magnetische und elektrische Eigenschaften gezeigt. CQDs können mit verschiedenen Techniken synthetisiert werden, einschließlich Hydrothermal-, Elektrooxidations-, Laserablations- und Mikrowellenmethoden [21,22,23,24]. Aufgrund ihrer geringen Toxizität betrachteten wissenschaftliche Forscher CQDs als leistungsstarke Kandidaten in vielen Fluoreszenzsonden. Darüber hinaus haben sie eine starke Fähigkeit, durch verschiedene kontrollierbare chemische Reaktionen bei verschiedenen Anforderungen wie biochemischen, photochemischen, Biosensor-, Bioimaging- und Wirkstoffabgabesystemen [25, 26, 27] sowie beim Immunoassay-Nachweis [28] zu manipulieren. Frühere Studien zur Synthese von CQDs zeigten gewisse Nachteile durch die Verwendung teurer Kohlenstoffquellen, giftiger Chemikalien und Reagenzien oder der Verwendung nichtselektiver Verfahren [29]. Um diese Nachteile einzuschränken, begannen die Forscher, Fruchtsäfte als neuartige und billige Kohlenstoffquelle zu verwenden [30]. Da die Verwendung von Fruchtsäften nicht das optimale Ziel der Ressourcennutzung bietet, wurden kürzlich fluoreszierende CQDs aus Fruchtschalen gewonnen [31]. Die Verwendung von Fruchtschalen bietet einen vielversprechenden Weg für eine umweltfreundliche und grüne Synthese von CQDs.
Zinkoxid (ZnO) ist eines der wichtigsten, potenziell aktiven, stabilen und wenig toxischen Metalloxide, das in ultravioletten Lasergeräten, im biomedizinischen Bereich, in verschiedenen Arten von Sensoren und in der Photokatalyse weit verbreitet ist [32,33,34,35]. ZnO-Nanopartikel (ZnONPs) zeigten photolumineszente Eigenschaften in der Nähe des UV- und Vis-Spektrums. Dies kann auf die exzitonische Emission zurückgeführt werden, die auf der direkten Rekombination von Elektron-Loch-Paaren beruht [36] oder auf die grün-gelbe Emission bei 520 nm als Ergebnis des elektronischen Übergangs von der Leitungsbandkante auf ein Fallenniveau [37].
Im Allgemeinen sind Kohlenstoffpunkte amorphe oder nanokristalline quasi-sphärische Nanopartikel, die sp 2 . enthalten und sp 3 Kohlenstoff, O/N-basierte Gruppen und nachmodifizierte chemische Gruppen. Darüber hinaus haben CQDs die Fähigkeit, mit höheren Wellenlängen anzuregen und können die Wirksamkeit der kombinierten Oberflächen der Elektron-Loch-Paare verändern und das Quenchen in den analysierten Systemen behandeln, was die quantitative Bestimmung von Biomolekülen erleichtern kann [38]. Sie können mit Metalloxiden wie TiO2 . dekoriert werden und ZnO, um optisch aktive Nanokomposite zu bilden, die zum Nachweis von Biomarkern in Humanserum genutzt werden können. ZnO ist ein Material mit großer Bandlücke (3,37 eV), das aufgrund der hohen Dichte von Defektniveaus in der Bandlücke im UV- und blauen Bereich des sichtbaren Lichts lumineszieren kann [39]. Die Bildung von CQDs/ZnO-Nanokompositen erhöht die Absorption von sichtbarem Licht aufgrund der Hybridisierung von ZnO mit CQDs, und die Blauverschiebung der Lumineszenzabsorption auf 520 nm kann auf die strahlende Rekombination ionisierter O-Leerstellen zurückgeführt werden. Für die höhere optische Leistung der hybridisierten CQDs mit ZnO-Nanopartikeln kann neben der Erhöhung der Absorption von sichtbarem Licht eine bessere Elektron-Loch-Trennung und eine Verkürzung der Grenzflächen-Elektronentransferzeit in Betracht gezogen werden [40]. Darüber hinaus kann die signifikante Zunahme von –OH*-Radikalen, die aus CQDs/ZnO-Nanokompositen in der Wassergrenzfläche erzeugt werden, eine signifikante Erhöhung der Fluoreszenzsignale des Analysesystems verursachen. Somit verbessert das kombinierte CQDs/ZnO-Nanokomposit die Modifikation der optoelektronischen und Photolumineszenzeigenschaften der ZnO-Oberfläche und erzeugt einen starken Oberflächendefekt mit einstellbarer Photolumineszenz [41]. Darüber hinaus bieten CQDs, die mit Bio-Erkennungs-Antikörpern immobilisiert sind, die ein Antikörper-Antigen-Antikörper-FL-Sensorsystem bilden, eine brauchbare Sonde mit hoher Spezifität und Empfindlichkeit gegenüber dem Zielanalyten [42].
In der vorgeschlagenen Studie wurde ein neues einfaches und ultrasensitives Immunoassay-Fluoreszenzsensorsystem vorgeschlagen, das auf mit ZnO-Nanokomposit dekorierten CQDs basiert, um den Tumor-CYFRA 21-1-Marker in Humanserum zu bestimmen. Zitrus-Zitronen-Perikarp wurde als Kohlenstoffvorläufer verwendet, um CQDs unter Verwendung hydrothermaler Bedingungen abzuleiten. Darüber hinaus wurde es als Reduktions- und Stabilisierungsmittel für die Synthese von CQDs-konjugierten ZnO-Nanokompositen verwendet. Das hergestellte CQDs/ZnO-Nanokomposit wurde mit einem nicht-konjugierten monoklonalen Antikörper (mAb) BM 19.21 immobilisiert und die Mikrotiter-Wells wurden mit einem anderen monoklonalen KS 19.1-Antikörper beschichtet, um ein Sandwich-Capping-Immunsensorsystem zu bilden.
Methoden
Instrumente
Spektrophotometrische Spektren sowohl von CQDs als auch von CQDs/ZnO-Nanokomposit wurden unter Verwendung eines Ultrospec 2100-Biochrom-Spektrophotometers (Biochrom Ltd., Cambium, Cambridge, UK) aufgenommen. Oberflächenmorphologie und Partikelgrößenverteilung der grün synthetisierten CQDs und CQDS/Zn-Nanokomposite wurden unter Verwendung eines Transmissionselektronenmikroskops (TEM) JEOL 1200EX-Modellinstruments (JEOL Ltd., Freising, Deutschland) und eines Rasterelektronenmikroskops (SEM) JSM-7610F-Modells bewertet (JEOL, USA). Die Fluoreszenz- und Fourier-Transformations-Infrarot-(FT-IR)-Spektren des vorgeschlagenen Immunsensorsystems wurden mit dem Biotek Synergy H1-Multimode-Lesegerät (Biotek, Tokio, Japan) und dem Perkin Elmer FT-IR-Spektrophotometer (PerkinElmer Ltd., Yokohama, Japan) überprüft. , bzw. Raman-Spektren, Röntgenphotoelektronenspektroskopie (XPS) und Röntgenpulverbeugungsmuster (XRD) wurden mit einem Mikro-Raman-Spektrometer (CRAIC Technologies, CA, USA), einem Kratos Axis Ultra-Röntgenspektroskopiesystem (Kratos Analytical Ltd.) gemessen. , Manchester, UK) bzw. Siemens D-5000 Diffraktometer (Siemens, Erfurt, Deutschland).
Chemikalien und Reagenzien
Das Gerät SG-2000-10090 (Barsbüttel, Deutschland) wurde verwendet, um das bei allen Experimenten verwendete entionisierte Wasser zu gewinnen. CYFRA 21-1-nicht-konjugierte monoklonale Antikörper (mAb) BM 19.21 und KS 19.1 zur Bildung des Sandwich-Capping-Immunsensorsystems wurden von Abcam (Cambridge, UK) bezogen. Zitruszitrone Früchte wurden von lokalen Märkten geliefert. Phosphatgepufferte Kochsalzlösung (PBS) mit einem pH-Wert von 7,4 wurde unter Verwendung von Natriumchlorid, Kaliumchlorid, Natriumhydroxid, Monokaliumphosphat und Dinatriumphosphat (BHD Ltd. Co. Poole, UK) hergestellt. Randox Laboratories (Nordirland-UK) stellte freundlicherweise die handelsüblichen Normalseren zur Verfügung. Von gesunden Freiwilligen wurden zufällige Blutproben genommen, und vor Beginn dieser Studie wurde eine Einverständniserklärung eingeholt. Darüber hinaus lieferte Sigma-Aldrich (Hamburg, Deutschland) sowohl Carbodiimid-Hydrochlorid (EDC) als auch N-Hydroxysuccinimid (NHS) in reiner Qualität. Die Forschungsethikkommission der King Saud University, KSA (KSU-REC-002-E, 2019) hat die Studie genehmigt.
Grüne hydrothermale Aufbereitung von Kohlenstoffquantenpunkten (CQDs)
Zitruszitrone Perikarp wurde verwendet, um CQDs unter hydrothermalen Bedingungen zu synthetisieren. Ungefähr 20 g Zitruszitrone Perikarp und 200 ml entionisiertes Wasser wurden in einen Rundkolben überführt und bei 100 °C unter kontinuierlichem Magnetrühren für 6 Stunden unter Rückfluss erhitzt. Nach dem Abkühlen auf Raumtemperatur wurde der resultierende Extrakt bei 3500 U/min zentrifugiert und 20 ml der oberen extrahierten Lösung wurden autoklaviert und unter hydrothermalen Bedingungen im Temperaturbereich von 100 bis 200°C für verschiedene Intervalle von 6–120 h erhitzt. Nach dem Abkühlen auf Raumtemperatur stellt die obere Flüssigkeit die CQDs dar (Schema 1).
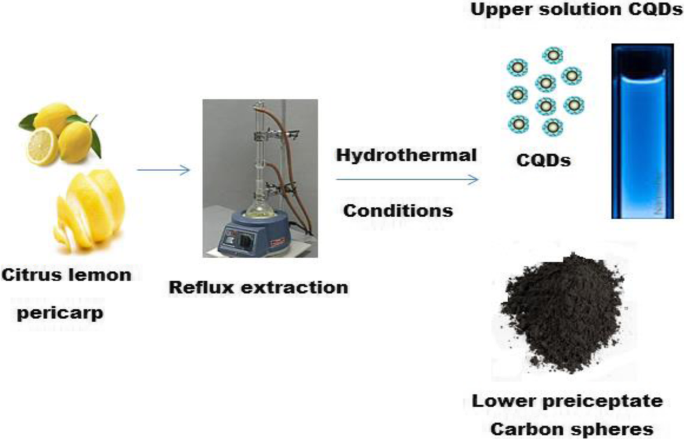
Grüne Synthese von CQDs mit Zitruszitrone Perikarp zu fluoreszierender CQD-Lösung und Kohlenstoffkugeln
Herstellung von Kohlenstoff-Quantenpunkten-Zinkoxid-Nanokomposit
Zur Herstellung von CQDs/ZnO-Nanokompositen wurde eine einfache chemische Reduktionsreaktion unter Verwendung von CQDs als Reduktions- und Stabilisierungsmittel durchgeführt. CQDs/ZnO-Nanokomposit wurde durch Zugabe von 20 mL der CQDs zu 50 mL von 5.0 × 10 −2 . erhalten mol L −1 Zinkacetat bei 60 °C unter kontinuierlichem Rühren für 10 min. Als sich die Farbe der Mischung von gelblich zu cremig änderte, wurde die Mischung 30 min beiseite gelassen, um den Reduktionsvorgang zu vervollständigen, und bei 4°C gelagert. Um die Stabilität zu gewährleisten und die Agglomeration des hergestellten CQDs/ZnO-Nanokomposits zu überprüfen, wurde UV-Vis-Spektrometrie verwendet, um die Extinktion innerhalb von 20 Tagen bei 390 nm aufzuzeichnen. Die Ergebnisergebnisse zeigten eine hohe Stabilität und keine signifikante Änderung der Absorption von CQDs/ZnO-Nanokomposit.
Charakterisierung von Kohlenstoff-Quantenpunkten-Zinkoxid-Nanokomposit
Um die Bildung von CQDs/ZnO-Nanokompositen sicherzustellen, wurden verschiedene mikroskopische und spektroskopische Techniken verwendet. Die Einheitlichkeit und Oberflächenmorphologie von CQDs und CQDs/ZnO-Nanokompositen wurden mit hochauflösendem Transmissionselektronenmikroskop (HRTEM) und SEM untersucht. Die optischen Spektren wurden mit UV-Vis-, FT-IR-, XPS- und Raman-Spektroskopie untersucht. Die Kristallstruktur der so hergestellten CQDs wurde unter Verwendung eines XRD-Musters bewertet.
Immobilisierungsprozess
Ein nicht-konjugierter monoklonaler BM 19.21-Antikörper wurde auf der Oberfläche des synthetisierten CQDs/ZnO-Nanokomposits durch eine einfache Peptidamidbindung zwischen dem Amin und den aktiven Carboxylgruppen immobilisiert. Der Immobilisierungsprozess wurde durch Zugabe von 5,0 ml jedes äquimolaren 3,0 × 10 –3 durchgeführt mol L −1 NHS und EDC zu 5,0 ml CQDs/ZnO-Nanokompositlösung unter kontinuierlichem Rühren für 1 Stunde. Ungefähr 5 mg des nicht-konjugierten monoklonalen BM 19.21-Antikörpers wurden in 1,0 ml 0,01 mol L −1 . gelöst Phosphat-gepufferte Kochsalzlösung (pH = 7,4) und zu der obengenannten Messlösung gegeben. Der nicht-konjugierte monoklonale BM 19.21-Antikörper wurde nach 12-stündiger Inkubation bei 37 °C auf der Oberfläche einer CQDs/ZnO-Nanokompositlösung immobilisiert (Schema 2). Spektrophotometrie wurde verwendet, um den Erfolg des Immobilisierungsprozesses zu bestätigen.
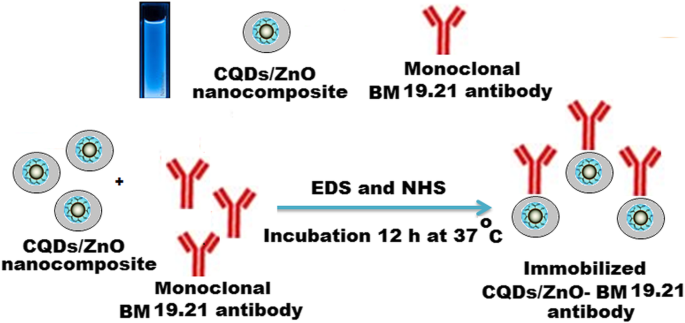
Immobilisierung des monoklonalen BM 19.21-Antikörpers auf der Oberfläche von CQDs/ZnO-Nanokomposit
Allgemeines Prinzip der Immunoassay-Methode
Eine Sandwich-Capping-Reaktion Antikörper-Antigen-Antikörper wurde unter Verwendung eines anderen monoklonalen KS 19.1-Antikörpers erhalten, der die Oberfläche von Mikrotiter-Wells beschichtete (Schema 3). Unter optimalen Immunoassay-Bedingungen wurde die Konzentration des CYFRA 21-1-Antigens als Funktion einer Zunahme der Fluoreszenzsignalintensität bestimmt.
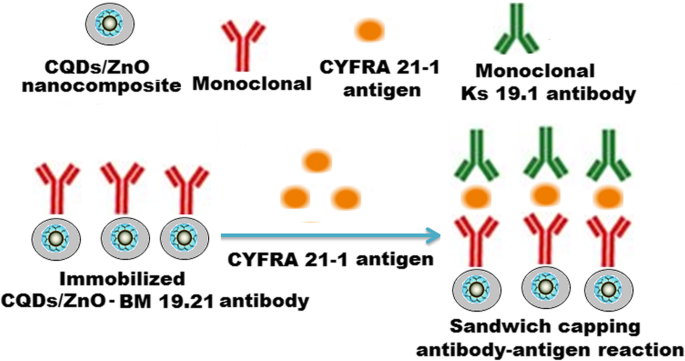
Das illustrierte Schema stellt eine Sandwich-Capping-Immunosensor-Antikörper-Antigen-Antikörper-Reaktion dar.
Das Immunsensor-Verfahren
Die Probensammlung von Humanseren wurde von zufälligen Freiwilligen bereitgestellt. Eine vollständige Gerinnung wurde vor der Zentrifugation bei Raumtemperatur sichergestellt und bei 4 °C gelagert. Die Spiking-Technik wurde verwendet, um Standardproben herzustellen, die CYFRA 21-1-Antigen im Konzentrationsbereich von 0,01–500 ng mL -1 . enthielten . Ungefähr 50 µl der dotierten Proben wurden in Mikrotiter-Wells verteilt und mit 50 µl frisch verdünntem monoklonalem KS 19.1-Antikörper unter Verwendung von phosphatgepufferter Kochsalzlösung von pH = 7,4 30 Minuten lang gemischt und dann ohne Abdeckung der Platte 1 Stunde lang bei 37 °C inkubiert. Der Inhalt der Vertiefungen wurde kräftig ausgeschüttelt und die Vertiefungen wurden dreimal mit entionisiertem Wasser (300 µl) für jede Vertiefung gespült. Etwa 50 µl der immobilisierten CQDs/ZnO-BM 19.21-Nanokompositlösung wurden in jede Vertiefung gegeben, vorsichtig gemischt und 30 Minuten bei 37 °C inkubiert. Die vorbereiteten Proben wurden einer Fluoreszenzanalyse mit einem Mikrotiter-Lesegerät unterzogen, um die Intensitäten aufzuzeichnen.
Ergebnisse und Diskussion
Morphologische Bewertung von Kohlenstoff-Quantenpunkten und ihrem Nanokomposit
Ein Transmissionselektronenmikroskop (TEM) wurde verwendet, um die Oberflächenmorphologie und die Verteilung von CQDs in den Proben zu charakterisieren. Um die Untersuchung unter TEM durchzuführen, wurden ungefähr 4 µl der vorbereiteten CQDs-Suspension auf die Oberfläche des Kohlenstoffgitters des TEM getropft. Im HRTEM-Bild (Abb. 1a) zeigten die beobachteten einheitlichen schwarzen Flecken mit Gitterabständen (0,36 nm) die Bildung von CQDs an. Ein Diagramm der Partikelgrößenverteilung wurde aufgetragen und die durchschnittliche Partikelgröße lag im Bereich von 1,5 ± 0,5 bis 5,0 ± 0,5 nm (Abb. 1b). Die erhaltene Partikelgröße bewies, dass es sich bei den gebildeten CQDs tatsächlich um Nanomaterialien mit Quantengröße handelt. Darüber hinaus wurde eine dynamische Lichtstreuung (DLS) durchgeführt, und die durchschnittliche Partikelgröße wurde mit ~ 20 ± 0.2 nm ermittelt. Es wurde ein Unterschied zwischen den beiden vorherigen Messungen beobachtet. Frühere Studien zeigten, dass HRTEM aufgrund ihrer amorphen Natur die Kristallgitterstruktur der gebildeten CQDs bei höheren Vergrößerungen nicht zeigt [43]. In ähnlicher Weise ist in dieser Studie der natürliche Vorläufer von Kohlenstoff Zitruszitrone Perikarp und die abgeleiteten CQDs wiesen ebenfalls amorphe Natur auf. Daher kann der Unterschied bei den Partikelgrößenmessungen auf die Agglomeration der gebildeten CQDs, die amorphe Natur der gebildeten Kohlenstoffpunkte, den an jedem Experiment beteiligten Mechanismus und die Hydratationsdynamik der Partikel zurückgeführt werden.
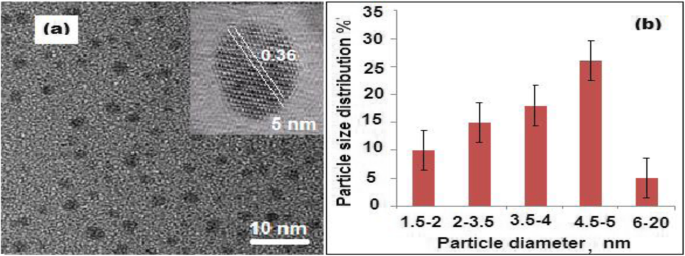
a Hochauflösendes Transmissionselektronenmikroskop (HRTEM)-Bild von CQDs mit einem Durchmesser von 5 nm und b Größenverteilungsdiagramm der CQDs basierend auf dem TEM
Das hergestellte CQDs/ZnO-Nanokomposit wurde mit TEM und REM untersucht. Im TEM-Bild (Abb. 2a) deutete das Vorhandensein von hexagonalen Partikeln, die an CQDs befestigt waren, auf die Bildung von CQDs/ZnO-Nanokomposit hin. Im SEM wurde die Nanokompositprobe mit Gold beschichtet, um die Elektronenabsorption durch die Probe und den Aufbau von Ladungen zu verhindern. Die angelegte beschleunigte Spannung betrug 15 kV bei Vergrößerung × 30.000 (Abb. 2b).

a und b repräsentieren die Transmissionselektronenmikroskop- und Rasterelektronenmikroskop-Aufnahmen von CQDs/ZnO-Nanokompositen
UV-Vis- und Fluoreszenzspektren von CQDs wurden untersucht, und die aufgezeichneten Spektren zeigten zwei signifikante Peaks bei 224 und 280 nm, die auf p . zurückgeführt werden können ~p* und n ~P* Übergang von C=C bzw. C=O. Außerdem zeigte das Fluoreszenzspektrum von CQDs zwei Signale bei maximalem λex = 360 und λem = 453 nm (Abb. 3a, b). Darüber hinaus wurde das UV-Vis-Spektrum von CQDs/ZnO-Nanokompositen untersucht. Bei 370 nm wurde ein signifikanter Absorptionspeak mit blaugrüner Verschiebung beobachtet (Abb. 4a). Die Photolumineszenz (PL)-Eigenschaften von CQDs/ZnO-Nanokompositen wurden untersucht. Die Größe und Oberflächendefekte von CQDs beeinflussen ihre Lumineszenzeigenschaften stark. In Abhängigkeit von der Anregungswellenlänge wurde die (PL)-Emission von CQDs variiert [38]. Außerdem zeigten ZnO-Nanopartikel eine defektbezogene Emission im sichtbaren Bereich der blauen bis grünen Absorption [41]. Daher erzeugten CQD-dekorierte ZnONPs ein ausgezeichnetes Nanokomposit für die PL-Emission. Wie in Abb. 4b gezeigt, wies das PL-Spektrum von CQDs/ZnO eine Blauverschiebung mit einem signifikanten Peak bei 520 nm nach der Anregungswellenlänge von 470 nm auf. Die beobachtete Verschiebung kann der Überlappung zwischen den Energiebändern von CQDs und ZnONPs zugeschrieben werden. Die angezeigte Blauverschiebung lag im Bereich der Defektemission von 2,1 eV.
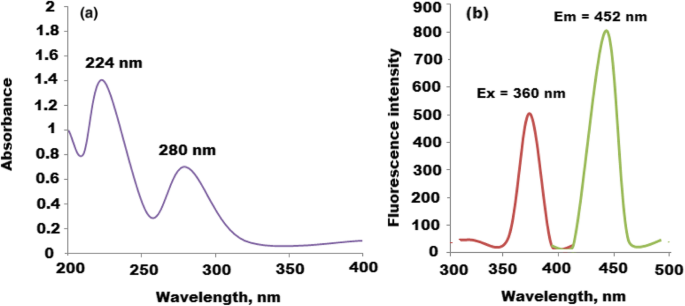
Spektroskopische Spektren von CQDs (a ) UV-Vis-Spektrum bei 224 und 280 nm und (b ) Fluoreszenzspektrum von CQDs bei λex = 360 und λem = 452 nm
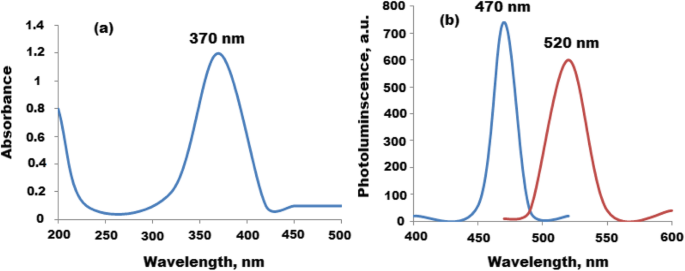
Spektroskopische Spektren von CQDs/ZnONPs a UV-Vis-Spektrum beim Absorptionspeak bei 370 nm und b Photolumineszenzspektrum von CQDs/ZnONPs bei λex = 470 und λem = 520 nm
Um die Bildung von CQDs/ZnO-Nanokomposit und immobilisiertem CQDs/ZnO-Nanokomposit mit nicht-konjugiertem monoklonalen BM 19.21-Antikörper zu bestätigen, wurde eine vergleichende FT-IR-Studie durchgeführt. Das aufgezeichnete FT-IR-Spektrum von CQDs zeigte das Vorhandensein verschiedener unterschiedlicher Peaks, die bestimmten funktionellen Gruppen entsprechen, einschließlich Streckschwingungspeaks bei 3462 cm −1 und 2932 cm −1 für C–OH- bzw. C–H-Gruppen. Darüber hinaus wurden drei Schwingungsabsorptionsbanden bei 1749 cm −1 . beobachtet , 1375 cm −1 , und 1246 cm −1 entsprechend dem Vorhandensein von C=O-, C–N- bzw. C–O–C-funktionellen Gruppen (Abb. 5a). Ein neuer Peak bei 436 cm −1 entsprechend einem sich ausdehnenden Schwingungsband von Zn–O wurde beobachtet. Die reduzierenden und stabilisierenden Eigenschaften von CQDs wurden aus der Anwesenheit von –OH- und COOH-Gruppen auf ihrer Oberfläche gewonnen. Diese funktionellen Gruppen wirken als Elektronendonatoren und haben eine starke Affinität zur Bildung von CQDs/ZnO-Nanokompositen. Daher reduzierten und stabilisierten CQDs das gebildete Nanokomposit (Abb. 5b). Wie in Abb. 5c dargestellt, wurde festgestellt, dass bei 3254 cm −1 . zwei neue Peaks gebildet wurden und 1675 cm −1 . Diese Peaks wurden der Streckschwingung von N–H bzw. C=O zugeschrieben und bestätigten die Immobilisierung von CQDs/ZnO-BM 19.21 über Peptidbindungen.
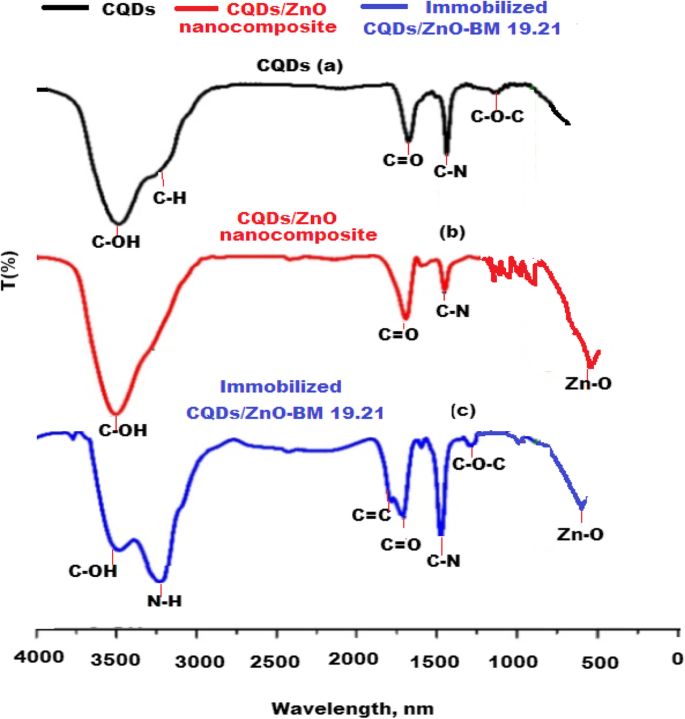
FT-IR-Spektren von a CQDs, b CQDs/ZnO-Nanokomposit und c immobilisierte CQDs/ZnO-BM 19.21 Nanokomposit
Röntgenphotoelektronenspektroskopie (XPS)-Spektren der grün synthetisierten CQDs wurden untersucht. Das erhaltene Spektrum der CQDs (Abb. 6a) zeigte unterschiedliche funktionelle Gruppen bei 288 und 286 eV für C=O bzw. COOH. Außerdem wurden zwei signifikante Bindungsenergiepeaks bei 1044,4 und 1021,5 eV für Zn 2p1/2 . beobachtet und Zn 2p3/2 , bzw. (Abb. 6b). Darüber hinaus bestätigte das hochauflösende XPS-Spektrum von CQDs/ZnO-Nanokompositen das Vorhandensein verschiedener Bindungsenergiepeaks bei 560, 385, 350, 246 und 200 eV für O 1s, C 1s, Zn 3s, Zn 3p und Zn 3d. (Abb. 6c). Alle zuvor erwähnten Daten bewiesen das Vorhandensein von ZnO auf der Oberfläche von CQDs, die CQDs/ZnO-Nanokomposit bilden.
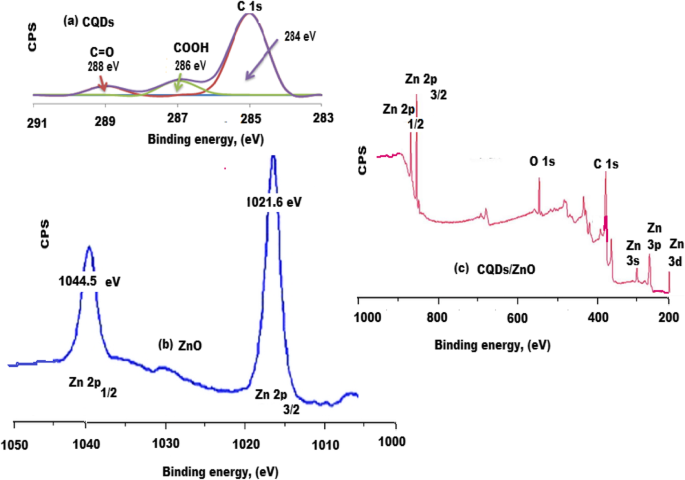
Röntgenphotoelektronenspektroskopie (XPS)-Spektren von a CQDs, b ZnO und c CQDs/ZnO-Nanokomposit
Es wurde eine Vergleichsstudie zwischen XRD-Mustern von CQDs und CQDs/ZnO-Nanokomposit durchgeführt. Im XRD-Muster von CQDs wurde ein breiter Peak bei 20° (2Ɵ) für Kohlenstoffpunkte festgestellt (Abb. 7a). Jedoch wurden bei 27°, 32°, 34°, 45°, 57°, 64°, 67°, 70°, 73°, 78° und 80° (2Ɵ) für Zn (100) unterschiedliche scharfe Peaks erkannt. (002), (101), (102), (110), (103), (200), (112), (201), (004) bzw. (202). Die beobachteten Peaks spiegeln die Verteilung von ZnO auf der Oberfläche von CQDs wider, die CQDs/ZnO-Nanokomposit bilden (Abb. 7b).
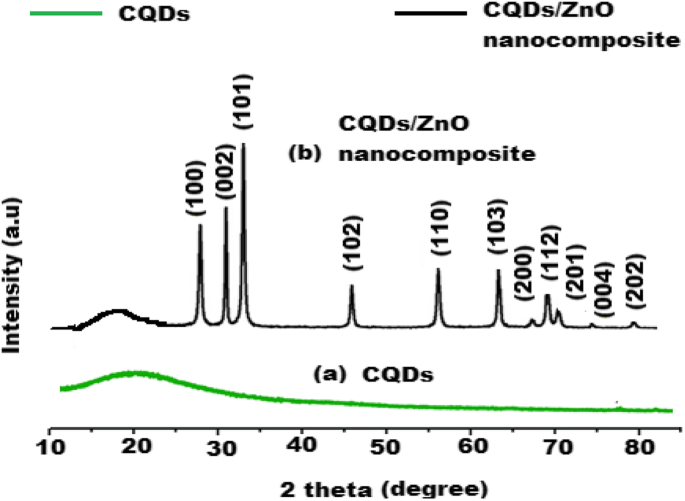
Röntgenbeugungsmuster von a CQDs und b CQDs/ZnO-Nanokomposit
Die Raman-Spektren der hergestellten CQDs, CQDs/ZnO und immobilisierten CQDs/ZnO-BM 19.21 Nanokomposit wurden untersucht. Die Raman-Signale werden häufig verwendet, um die Kristallstruktur und ihre Defekte zu untersuchen. Abbildung 8a zeigt zwei typische D- und G-Banden bei 1300 und 1520 cm −1 für Kohlenstoff-Nanopartikel bzw. Wie bereits berichtet, steht das D-Band im Allgemeinen für sp 3 Defekte und das G-Band ist ein Merkmal der ebenen Schwingung von sp 2 -gebundene Kohlenstoffe [44]. Das Ich D /Ich G Für die hergestellten CQDs wurde ein Verhältnis von 1,02 ± 0,03 berechnet. Neue scharfe Peaks wurden bei 440 und 520 cm −1 . beobachtet für ZnO-Nanopartikel und die typischen Peaks von CQDs wurden bei 1364 und 1595 cm −1 . beobachtet . Das Verhältnis von I D /Ich G wurde mit 1,2 ± 0,01 gefunden, was auf die Bildung von CQDs/ZnO-Nanokompositen hinweist (Abb. 8b). Das Raman-Spektrum von immobilisierten CQDs/ZnO-BM 19.21-Nanokompositen zeigte zahlreiche Peaks, die leicht als bestätigende Anzeichen von Sekundär- und Tertiärstrukturen erkannt werden können. Die im Bereich von 1007–1128 cm −1 . beobachteten Peaks wurden zugeordnet, um die Hauptsekundärstruktur des monoklonalen Antikörpers darzustellen. Der Raman-Gipfel liegt bei 550–682 cm −1 Regionen wurden Disulfidkonformationen zugeordnet, während die 867–797 cm −1 Einsen wurden zugeordnet, um den Wasserstoffbrückenbindungszustand von Tyrosinresten darzustellen. Auch die signifikante Verschiebung des Raman-Spektrum-Peaks auf 1630 cm −1 kann auf das Vorhandensein einer Tertiärstruktur des immobilisierten Antikörpers zurückgeführt werden [45] (Abb. 8c). Das Verhältnis von I D /Ich G wurde auf 1,4 ± 0,04 erhöht, was eine bessere Kristallstruktur aufgrund der Bildung von immobilisierten CQDs/ZnO-BM 19.21-Nanokompositen zeigt.
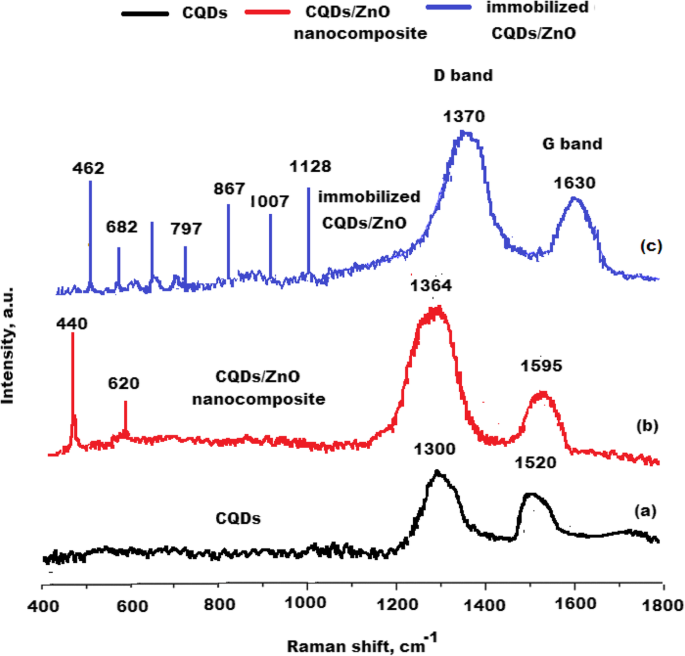
Raman-Spektrenverschiebung von a CQDs, b CQDs/ZnO-Nanokomposit und c immobilisierte CQDs/ZnO-BM 19.21 Nanokomposit
Optimierung der Fluoreszenz-Immunsensorbedingungen
Die Auswahl und Optimierung der vorgeschlagenen Fluoreszenz-Immunsensor-Bedingungen wurden durch Untersuchung verschiedener Parameter durchgeführt. Im Allgemeinen sollten die Menge des immobilisierten Nanokomposits, der pH-Wert und die Konzentration des verwendeten Puffers, die Inkubationszeit zwischen dem Zielanalyten in den Serumproben und den immunsensorischen Reagenzien untersucht und optimiert werden. Um die geeignete Menge an immobilisierten CQDs/ZnO-BM 19.21 Nanokomposit auszuwählen, wurden verschiedene Mengen im Bereich von 10–100 μL getestet. Die maximale Fluoreszenzintensität wurde durch Zugabe von 50 µl des immobilisierten CQDs/ZnO-BM 19.21-Nanokomposits beobachtet (Abb. 9a). Vier phosphatgepufferte Kochsalzlösungen mit pH-Werten von 7,2–7,5 wurden hergestellt und als Funktion der Fluoreszenzintensität getestet. Eine leichte Änderung der Fluoreszenzsignalintensität wurde durch Änderung der pH-Werte beobachtet. Bei pH 7.2 und 7.3 war das Fluoreszenzsignal aufgrund der chemischen Instabilität des immobilisierten CQDs/ZnO-Nanokomposits verringert. Das Fluoreszenzsignal wurde bei pH 7.4 bis 7.5 aufgrund der hervorragenden Wechselwirkung zwischen den monoklonalen Molekülen auf der Oberfläche des Nanokomposits erhöht (Abb. 9b). Es wurde festgestellt, dass 7,4 der am besten geeignete pH-Wert ist, um die Aktivität des Zielantigens aufrechtzuerhalten, das durch Erhöhung des pH auf mehr als 7,5 zersetzt werden kann. Daher wurde ein pH-Wert von 7,4 für weitere Studien ausgewählt.
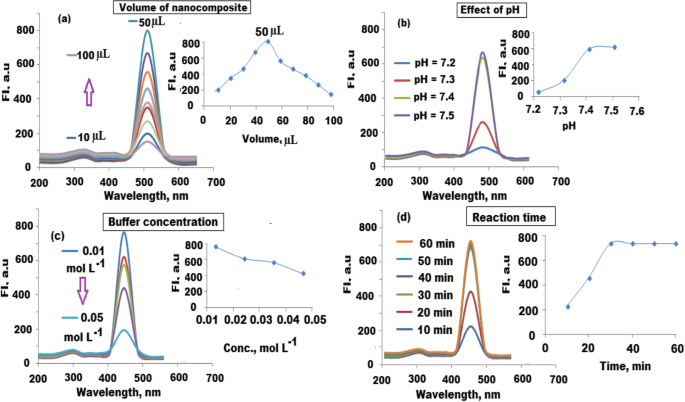
Optimierung der Fluoreszenzbestimmung von CYFRA 21-1 Antigen bei λex = 470 und λem = 520 nm. a Wirkung von zugesetzten immobilisierten CQDs/ZnO-BM 19.21 Nanokomposit, b Wirkung von phosphatgepufferter Kochsalzlösung im pH-Bereich 7,3–7,5, c Wirkung der Pufferkonzentration mit PBS im Konzentrationsbereich von 0,01–0,05 mol L −1 , und d Wirkung der Immunreaktionszeit mit 10–60 min
Der Einfluss der phosphatgepufferten Kochsalzlösung auf die Fluoreszenzintensität wurde mit einem Konzentrationsbereich von 0,01–0,05 mol L −1 . abgeschätzt . The maximum fluorescence intensity signal was obtained using the buffer concentration of 0.01 mol L −1 . At higher buffer concentrations, the immobilized CQDs/ZnO-BM 19.21 nanocomposite was aggregated, and the instability of the immunosensing solution may cause a decrease in fluorescence intensity (Fig. 9c). To calculate the immunoreaction time, the analytical procedure was repeated using reaction time ranging from 10 to 60 min. The maximum fluorescence intensity signal was observed by maintaining the reaction between the tested antigen and the immunosensing solution for at least 30 min (Fig. 9d).
Analytical Quantification
Under optimized conditions, the suggested immunoassay method was performed using 12 serum samples containing CYFRA 21-1 antigen in concentration range of 0.01–500 ng mL 1 . The outcome results were plotted to construct the calibration graph which was linear over a concentration range of 0.01–100 ng mL −1 with a detection limit of 0.008 ng mL −1 . The calculated equation was found to be I F = 7.933C + 181.24 (r 2 = 0.9992). After six repetitions, the percentage of the relative standard deviation (%RSD) was 1.3%. The acceptable results revealed a high sensitivity of the immunosensing fluorescence method for the quantification of CYFRA 21-1 antigen in serum samples.
System Suitability
System suitability was investigated by carrying out a comparative study between the suggested immobilized CQDs/ZnO-BM 19.21 immunosensing method and the previously addressed methods. The suggested fluorescence system provided significant advantages such as simplicity, eco-friendly, and easy to detect the target analyte in serum samples. The recorded results revealed high sensitivity with a wide linear detection range of 0.01–100 ng mL 1 and lower detection limit of 0.008 ng mL 1 (Table 1).
Accuracy, Precision, and Selectivity of the Immobilized Immunosensing System
To ensure the accuracy of the suggested immobilized CQDs/ZnO-BM 19.21 fluorescence immunosensing system for the determination of CYFRA 21-1 antigen in serum samples, 12 serum samples were tested. The outcome data were compared with another previously reported technique [6], which was based on electrochemiluminescence assay using tris 2,2′-bipyridyl ruthenium (II) complex to be excited by tripropylamine. Acceptable results were obtained as indicated in Table 2. Intra-day and inter-day assay were used to investigate the precision of the suggested method. The test was carried out using a serum sample containing 10 ng mL − 1 of CYFRA 21-1 antigen. The mean relative standard deviations were 1.1% and 1.3% for both intra- and inter-day assay, respectively, which revealed high precision. Furthermore, the selectivity of the suggested method towards the determination of CYFRA 21-1 antigen was evaluated using some possible interfering species such as amino acids (cysteine, lysine, serine, tyrosine, and glycine), some cations (K + , Na + , Ca 2+ , Mg 2+ , und Zn 2+ ) and some other bio-markers such as CA 15-3, CA 27-29, CA 19-9, and CA 125. The test was carried out under optimum conditions using human serum containing 10 ng mL −1 CYFRA 21-1 antigen in the presence of 10 ng mL −1 coexisting species. The outcome data were calculated as relative percentage error (Er%) and the corresponding result did not exceed ± 5% for each interfering species (Table 3). The calculated tolerance values (F-F 0 /F 0 ) were found to be with the tolerance limits (< 5%). Therefore, the suggested immobilized CQDs/ZnO-BM 19.21 immunosensing fluorescence system displayed high selectivity towards the determination of CYFRA 21-1 antigen in human serum.
Analysis of Real Specimens
In real human specimens, the suggested immunosensing fluorescence system based on immobilized CQDs/ZnO-BM 19.21 solution was exploiting to detect and quantify the percentage (%) recoveries of the tumor marker CYFRA 21-1 antigen. As previously mentioned in the immunosensing procedure, the suggested system was used to determine the CYFRA 21-1 antigen by finding the relationship between the fluorescence intensity and the concentration of CYFRA 21-1 antigen in serum samples. Certain amounts of the target antigen (0.5, 1.0, and 2.0 ng mL −1 ) were added to the estimated samples, and the increase in signal intensities was evaluated. After six determinations, the percentage relative standard deviations (%RSD) were calculated. The outcome percentage recoveries were found to be ranged from 96.7 ± 0.7 to 100.0 ± 1.3%. The calculated %RSD was in the range of 0.2–1.4%. The tested serum samples were analyzed using a previously reported method [6] and the percentage recoveries were found to be ranged from 96.1 ± 1.6 to 100.0 ± 0.4% with %RSD 0.3–1.7%. In order to ensure the suitability of the suggested immunosensing fluorescence technique using an immobilized CQDs/ZnO-BM 19.21 solution, a comparative statistical study using Student’s t test and F test [46] was carried out between the present results and those obtained by others from previously conducted methods (Table 4). The obtained t test and F test values were found to be ranged from 0.354 to 2.181 (2.228)* and 1.16 to 4.0 (5.05)* with respect to the tabulated values of P = 0.05, respectively. The results revealed good agreement between the suggested method and the previously published procedures. Also, all detected quantities of CYFRA 21-1 antigen in serum samples were within the normal limit indicating no lung cancer was diagnosed in the investigated serum samples.
Schlussfolgerung
The present study concerned with the preparation of green synthesis CQDs conjugated with ZnO nanocomposite using Citrus lemon as a precursor. The CQDs/ZnO nanocomposite was employed to form a new fluorescence immunosensing system by immobilizing a monoclonal BM 19.21 antibody through simple peptide bonds. The highly sensitive fluorescence system was used to determine the tumor marker of lung cancer (CYFRA 21-1) in human serum. CYFRA 21-1 antigen was determined via sandwich capping antibody-antigen-antibody reaction using another monoclonal antibody KS 19.1 coating the microtiter wells. The unique features and high sensitivity of the suggested system facilitate the determination of the target tumor marker with high stability and reproducibility. A comparative study was carried out and the outcome results confirmed the suitability and high sensitivity of the suggested immunosensing system, and the results were in agreement with a previously reported conventional technique.
Verfügbarkeit von Daten und Materialien
The only outcome data from this study was presented in the manuscript.
Abkürzungen
- %RSD:
-
Percentage relative standard deviation
- BM 19–21:
-
Specific monoclonal antibody
- CQDs:
-
Carbon quantum dots
- CQDs/ZnO:
-
Carbon quantum dots/zinc oxide
- CYFRA-21-1:
-
Cytikeratin-19 fragment
- DLS:
-
Dynamische Lichtstreuung
- EDC:
-
Carbodiimide hydrochloride
- eV:
-
Electron volt
- FT-IR:
-
Fourier-Transformations-Infrarot
- HRTEM:
-
Hochauflösendes Transmissionselektronenmikroskop
- KS 19-1:
-
Monoclonal cytokeratin 19-specific antibody
- Ltd. Co:
-
Limited company
- mAb:
-
Monoclonal antibody
- NHS:
-
N-Hydroxysuccinimid
- P:
-
Degree of confidence
- PBS:
-
Phosphatgepufferte Kochsalzlösung
- SEM:
-
Rasterelektronenmikroskop
- TEM:
-
Transmissionselektronenmikroskop
- UK:
-
Unite Kingdom
- USA:
-
United States of America
- UV-Vis:
-
Ultraviolett-sichtbar
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenpulverbeugung
- ZnO:
-
Zinkoxid
- ϴ:
-
Theta degree
- λmax :
-
Wavelength
Nanomaterialien
- Hocheffiziente, erregungsunabhängige blaue Lumineszenz-Karbonpunkte
- Synthese von Pyridin-reichen N,S-codotierten Kohlenstoff-Quantenpunkten als wirksame Enzymnachahmer
- Kohlenstoff-Nanodots als Dual-Mode-Nanosensoren für den selektiven Nachweis von Wasserstoffperoxid
- Wismut-Quantenpunkte in geglühten GaAsBi/AlAs-Quantenbrunnen
- Herstellung und Charakterisierung eines neuen anodischen Tio2-Kohlenstoff-Nanofaser-Verbundkatalysators für eine Direkt-Methanol-Brennstoffzelle mittels Elektrospinnverfahren
- Ein einfacher Ansatz zur Synthese von fluoreszierenden Kohlenstoffquantenpunkten aus Tofu-Abwasser
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Material und optische Eigenschaften von fluoreszierenden Kohlenstoff-Quantenpunkten, die durch hydrothermale Reaktion aus Zitronensaft hergestellt werden
- Eigenschaften von Zinkoxid-Nanopartikeln und ihre Wirkung gegen Mikroben
- Abstimmung des Gleit-Roll-Bewegungsmodus von Kohlenstoffnanoröhren über Hydroxylgruppen



