Material und optische Eigenschaften von fluoreszierenden Kohlenstoff-Quantenpunkten, die durch hydrothermale Reaktion aus Zitronensaft hergestellt werden
Zusammenfassung
Die wasserlöslichen fluoreszierenden Kohlenstoffquantenpunkte (CQDs) werden durch die Verwendung von Zitronensaft als Kohlenstoffquelle über eine einfache hydrothermale Reaktion synthetisiert. Die erhaltenen CQDs haben eine durchschnittliche Größe von 3,1 nm. Sie weisen eine einheitliche Morphologie auf und sind gut kristallin und können unter UV- oder Blaulichtbestrahlung eine helle blaugrüne Lichtemission erzeugen. Wir stellen fest, dass die Fluoreszenz dieser CQDs hauptsächlich durch das Vorhandensein sauerstoffhaltiger Gruppen auf der Oberfläche und am Rand der CQDs induziert wird. Darüber hinaus zeigen wir, dass die so hergestellten CQDs auf die Bildgebung von Pflanzenzellen angewendet werden können. Diese Studie bezieht sich auf die Herstellung, Untersuchung und Anwendung neu entwickelter Kohlenstoff-Nanostrukturen.
Hintergrund
Der Kohlenstoffquantenpunkt (CQD) ist eine neue Klasse von kohlenstoffbasierten Nanomaterialien, die normalerweise eine räumliche Größe von weniger als 20 nm aufweisen und von Xu et al. entdeckt wurden. im Jahr 2004 [1]. Die fluoreszierenden Kohlenstoff-Nanopartikel wurden von Sun et al. B. durch Laserablation von Graphitpulver im Jahr 2006 [2] und werden seitdem als „Kohlenstoffquantenpunkte (CQDs)“ bezeichnet. Die fluoreszierenden CQDs haben ein großes Potenzial für die Anwendung in der Photokatalyse, in optoelektronischen Geräten, in der Biomedizin, in Dünnfilmdisplays, in gesunder Beleuchtung und in anderen Disziplinen praktischer Anwendungen. Im Vergleich zu herkömmlichen halbleiterbasierten Quantenpunkten können die CQDs durch kostengünstige Herstellungstechniken erhalten werden und haben faszinierende und wichtige Eigenschaften wie gute Biokompatibilität, präzises biologisches Ziel, geringe Toxizität und stärkere Quantengrößenwirkung. In den letzten Jahren haben die fluoreszierenden CQDs aufgrund ihrer hervorragenden strukturellen und optischen Eigenschaften [5] große Aufmerksamkeit auf sich gezogen [3, 4]. Sie wurden als Ersatzmaterialien für konventionelle Halbleiter-Quantenpunkte in den Anwendungsgebieten einschließlich biologischer Bildgebung, biologischer Markierung, Quantenpunkt-LED (QLED), Umweltschutz und anderen verwandten Gebieten vorgeschlagen [6,7,8,9]. Die Forschung zu CQDs hat in der Physik der kondensierten Materie, in den Materialwissenschaften, in der Elektronik und in der Optoelektronik schnell zugenommen. Entsprechende Grundlagen- und Anwendungsstudien wurden weltweit umfassend durchgeführt [3,4,5,6,7,8,9].
Gegenwärtig gibt es verschiedene Techniken [10, 11], um CQDs zu synthetisieren, wie der hydrothermale Ansatz [11, 12], die Mikrowellenmethode [13] und so weiter. Die CQDs wurden aus verschiedenen Kohlenstoffvorläufern wie Glucose [14], Zitronensäure [15] und Ascorbinsäure [16] synthetisiert. Die Technik zur effizienten Herstellung biokompatibler fluoreszierender CQDs im großen Produktionsmaßstab ist jedoch immer noch erforderlich und zu einer Herausforderung für die praktische Anwendung der CQDs geworden. Es wurde festgestellt, dass die direkte Synthese der CQDs aus Nahrungsmitteln [17,18,19] und/oder Nebenprodukten [20] eine der vielversprechendsten und bedeutendsten Strategien ist. Rot emittierende Kohlenstoffpunkte (R-CDs) mit einem durchschnittlichen Durchmesser von 4 nm und einer hohen Quantenausbeute (QY) von 28 % in Wasser wurden durch Erhitzen einer Ethanollösung aus zellstofffreiem Zitronensaft synthetisiert [21]. Ein starkes Reduktionsmittel NaBH4 zu den R-CDs hinzugefügt wurde, um die Intensität der Lichtemission von den R-CDs zu erhöhen. Wir wissen jedoch, dass NaBH4 ist giftig. Vor kurzem haben wir die grün und blau emittierenden CQDs aus Tofu-Abwasser ohne Zugabe von toxischen Substanzen hergestellt [22]. Die aus Nahrungsmitteln und/oder Nebenprodukten hergestellten CQDs gelten für biologische Anwendungen als sicher, da in diesen natürlichen Kohlenstoffressourcen fast keine Toxizität bekannt ist. In letzter Zeit wurden mehrere ernsthafte Untersuchungen zur Synthese von CQDs aus ungiftigen Kohlenstoffressourcen unter Verwendung eines einstufigen Ansatzes durchgeführt, und es wurden erhebliche Fortschritte bei der Synthese, Untersuchung und Anwendung dieser CQDs erzielt. Knoblauch wurde beispielsweise als grüne Quelle zur Synthese von CQDs verwendet [23]. Detaillierte Struktur- und Zusammensetzungsstudien zeigten, [23] dass der N-Gehalt und die Bildung von C–N und C=N Schlüssel zur Verbesserung der Photolumineszenz(PL)-QY sind. Darüber hinaus weisen die CQDs eine ausgezeichnete Stabilität in einem weiten pH-Bereich und hohe NaCl-Konzentrationen auf, wodurch sie unter komplizierten und rauen Bedingungen einsetzbar sind [23].
Die Hauptmotivation der vorliegenden Arbeit ist die Entwicklung einer einfachen und effizienten experimentellen Methode zur kostengünstigen Herstellung von CQDs aus Zitronensaft durch hydrothermale Behandlung bei relativ niedrigen Temperaturen und durch einen weniger zeitaufwendigen Prozess. Es ist bekannt, dass Zitronensaft leicht und kostengünstig gewonnen werden kann und daher eine gute Kohlenstoffquelle für die CQD-basierte Proben- und Geräteherstellung ist. Im Vergleich zur vorherigen Studie [21] eignen sich die in unserer Arbeit gewonnenen nicht-toxischen CQDs besser für die biologische Bildgebung und Zellmarker. In dieser Studie untersuchen wir auch die grundlegenden materiellen und optischen Eigenschaften der aus Zitronensaft hergestellten CQDs und wenden die CQDs auf bildgebende Pflanzenzellen an.
Methoden
Vorbereitende Materialien
In dieser Studie werden die Kohlenstoffvorläufermaterialien aus frischem Zitronensaft gewonnen. Die Hauptbestandteile und ihre Prozentsätze werden durch Messung mit Hochleistungsflüssigkeitschromatographie (HPLC) erhalten, wie in Tabelle 1 gezeigt. Für die Probenvorbereitung wurden die frische Zitrone als Kohlenstoffquelle und die frische Zwiebel für die Zellbildgebung im örtlichen Supermarkt gekauft. Das Ethanol war analysenrein und wurde als Dispergiermittel verwendet. Für die Experimente wurde entionisiertes Wasser (18,25 MΩ cm) verwendet.
Synthese von CQDs
Die CQDs wurden aus Zitronensaft durch eine einfache hydrothermale Behandlung bei relativ niedrigen Temperaturen und durch einen weniger zeitaufwendigen Prozess synthetisiert. Die typischen Probenvorbereitungsprozesse sind in Abb. 1 dargestellt. Achtzig Milliliter zellstofffreier Zitronensaft wurden mit 60 ml Ethanol vermischt. Die Mischung wurde dann in einen mit Polytetrafluorethylen ausgestatteten Edelstahlautoklaven überführt und bei einer konstanten Temperatur von etwa 120 °C 3 h lang erhitzt. Nach der Reaktion wurde nach natürlichem Abkühlen auf Raumtemperatur das dunkelbraune Produkt erhalten. Die dunkelbraune Lösung wurde mit überschüssigem Dichlormethan gewaschen, um die nicht umgesetzten organischen Einheiten zu entfernen, und dieser Schritt kann 2–3 Mal wiederholt werden. Das entionisierte Wasser wurde zugegeben, bis das Volumen der braunen Lösung auf ein Drittel der Lösung angestiegen war, und 15 min bei 10000 U/min zentrifugiert, um die großen Partikel abzutrennen. So können die CQD-Proben durch Karbonisierung von Zitronensaft gewonnen werden, der als Kohlenstoffvorläufer Kohlenhydrate und organische Säuren wie Glucose, Fructose, Saccharose, Ascorbinsäure, Zitronensäure usw. enthält. Unsere einfache hydrothermale Reaktion findet bei einer niedrigeren Temperatur (120 °C) statt und benötigt weniger Zeit (3 h) als die beschriebene Methode [24].
Herstellung von CQDs aus Zitronensaft durch hydrothermale Behandlung
Charakterisierung
Die Morphologie und Mikrostruktur der aus Zitronensaft hergestellten CQDs wurden mit dem Transmissionselektronenmikroskop (JEM 2100, Japan) bei 300 KV analysiert. Die kristalline Phase der CQDs wurde durch Röntgenbeugung (Rigaku TTR-III, Japan) mit Cu-Kα-Strahlung (λ = 0,15418 nm). Das UV-Vis-Absorptionsspektrum wurde mit einem UV-Vis-Spektrophotometer (Specord200) gemessen. Die photoneninduzierte Lichtemission wurde mit einem Fluoreszenzspektrophotometer (IHR320, HORIBA Jobin Yvon, USA) für verschiedene Anregungswellenlängen im Bereich von 330 bis 490 nm untersucht. Die Spektren der Röntgen-Photoelektronenspektroskopie (XPS) wurden mit dem Photoelektronenspektrometer PHI5000 Versa Probe II mit Al Kα bei 1486,6 eV aufgenommen.
Ergebnisse und Diskussionen
Die Transmissionselektronenmikroskop-(TEM-)Bilder von CQDs sind in Abb. 2 gezeigt. Das TEM-Bild mit geringer Vergrößerung der so hergestellten Proben zeigt, dass CQDs eine gleichmäßige Dispersität aufweisen. Die CQDs sind kugelförmig mit einer engen Größenverteilung im Bereich von 2,0 bis 4,5 nm und einer durchschnittlichen Größe von 3,1 nm, wie in Abb. 2b, c gezeigt. Abbildung 2d zeigt den Gitterabstand von 0,215 nm, der der [100]-Facette von graphitischem Kohlenstoff entspricht, und das entsprechende Muster der schnellen Fourier-Transformation (FFT) der CQDs zeigt außerdem die hochkristalline Struktur, die mit dem vorherigen Bericht übereinstimmt [25]. Im Vergleich zu den vorherigen Studien [19, 21, 22, 23] weisen die in unserer Arbeit erhaltenen CQDs, wie in Abb. 2 gezeigt, nicht nur eine gute Qualität auf, sondern zeigen auch eine besser einheitliche Morphologie. Daher können CQDs mit einheitlicher abgerundeter Morphologie und guter Kristallinität durch einen einfachen hydrothermalen Behandlungsprozess hergestellt werden. Die Produktionsausbeute (PY) von CQDs kann nach der Definition PY = (m /M ) × 100 %, wobei m ist die Masse der CQDs und M ist die Masse des frischen Zitronensaftes. Die Produktionsausbeute der in dieser Studie hergestellten CQDs beträgt gemäß den Messergebnissen etwa 0,1 %, d. h. 100 g Flüssigkeit mit 6,30 % Zitronensäure können etwa 0,1 g CQDs erhalten (siehe Tabelle 1).
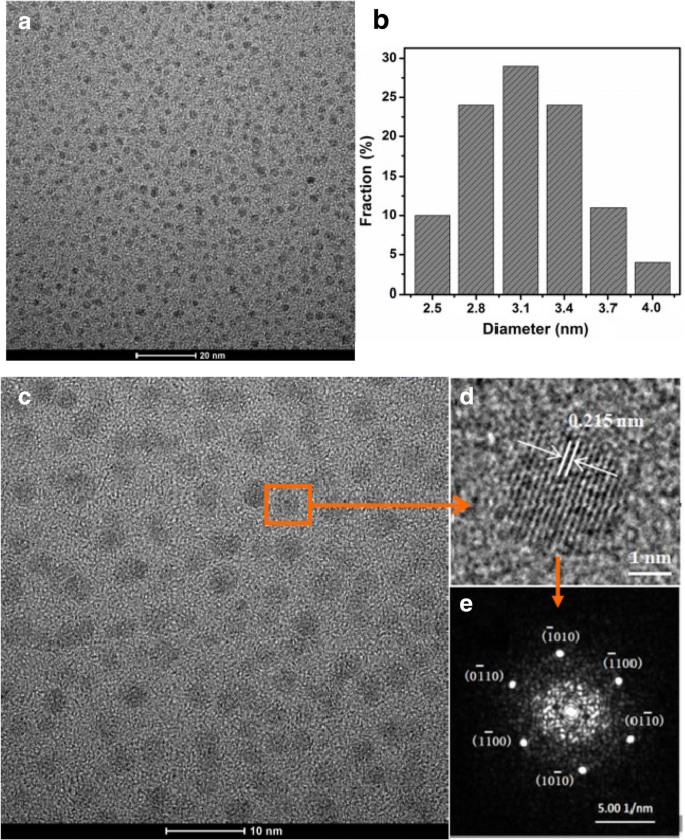
a , c , d TEM-Bild. b Partikelgrößenverteilung von CQDs. e Das entsprechende FFT-Muster von CQDs
Das typische Röntgenbeugungs- (XRD) und XPS-Profil von CQDs sind in Abb. 3 gezeigt. Es gibt einen breiten (002)-Peak, der bei 2θ . zentriert ist ~21,73°, und der Zwischenschichtabstand wurde mit 0,409 nm berechnet, entsprechend der Graphitstruktur, wie in Abb. 3a gezeigt, die den berichteten Abwertungen für CQDs ähnelt, die mit anderen Methoden hergestellt wurden [15, 26]. Die Variation des Zwischenschichtabstands kann durch die Einführung von mehr sauerstoffhaltigen Gruppen verursacht werden, z. B. durch das Vorhandensein von –OH und –COOH auf der CQD-Oberfläche und -Kante während des Verfahrens der hydrothermalen Reaktion zur Herstellung von CQDs. XPS und FTIR wurden verwendet, um die Zusammensetzung von CQDs zu erkennen. Wie in Abb. 3b, c gezeigt, zeigt das XPS-Spektrum einen dominanten graphitischen C1s-Peak bei 284,5 eV und einen O1s-Peak bei 531,4 eV von CQDs. Der typische Peak bei 284,7, 286,5 und 288,9 eV in einem hochauflösenden Scan des C1s-XPS-Spektrums (Abb. 3c wird C=C/C–C, C–O bzw. C=O/COOH zugeschrieben. Es zeigt deutlich, dass CQDs mit Hydroxyl-, Carbonyl- und Carbonsäuregruppen funktionalisiert wurden, was für die Oberflächenmodifizierung und -funktionalisierung von Vorteil ist und auch für die Löslichkeit in Wasser förderlich ist. Abbildung 3d zeigt das Fourier-Transform-Infrarotspektroskopie-(FTIR)-Spektrum von die CQDs. Das Vorhandensein von Sauerstofffunktionalitäten unterschiedlicher Art in CQDs wurde durch Peaks bei 3450 cm −1 . bestätigt (O–H-Streckschwingungen), 2927 cm −1 , 1407 cm −1 (C–H-Streckschwingungen), 1726 cm −1 (C=O Streckschwingungen), 1639 cm −1 (C=C Streckschwingungen), 1227 cm −1 (C–OH-Streckschwingungen) und 1080 cm −1 (C–O-Streckschwingungen). Es ist zu beachten, dass die FTIR-Analyse mit dem obigen XPS-Ergebnis übereinstimmt. Am wichtigsten ist, dass der C–O–C (Epoxid)-Peak bei 1290 cm −1 . vollständig verschwunden ist . Diese Ergebnisse deuten auf den Bildungsmechanismus von CQDs hin, bei dem die Epoxygruppen aufbrechen und die zugrunde liegenden C-C-Bindungen gebildet werden, woraufhin das sp 2 Domänen wurde aus niedermolekularen Vorläufern wie Glucose, Fructose, Ascorbinsäure und Zitronensäure durch weitere Dehydratisierung oder Karbonisierung extrahiert und schließlich CQDs gebildet. Daher trägt die Bindungsspaltung der umgebenden Sauerstoffgruppen zur Bildung der CQDs bei [15, 27].
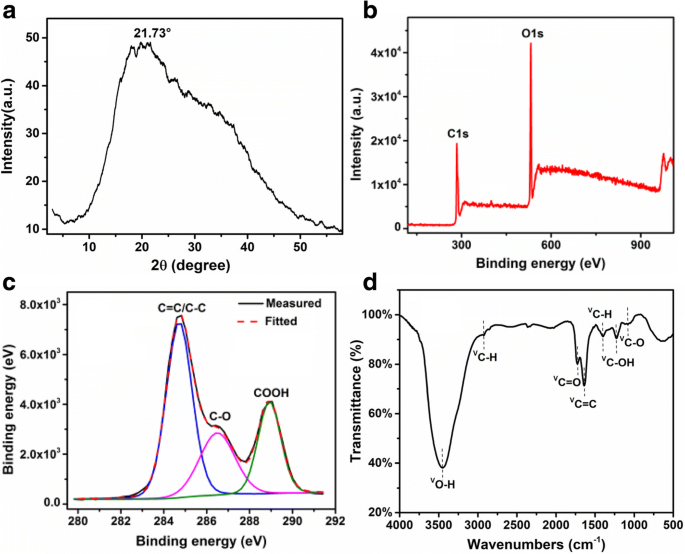
a XRD-Muster. b XPS-Spektren im unteren Bereich. c Hochauflösender XPS-Scan der C1s-Region. d FTIR-Spektren von CQDs
Derzeit werden die möglichen Mechanismen zur Bildung von CQDs aus Kohlenstoffvorläufern durch die hydrothermale Methode vorgeschlagen und untersucht [28]. Auf der Grundlage dieser veröffentlichten Ergebnisse können wir den Synthesemechanismus von CQDs aus Zitronensaft verstehen. Der fruchtfleischfreie Zitronensaft wird erhitzt und entwässert, um das Grundgerüst von C=C/C–C zu bilden, das hauptsächlich aus CQDs besteht, und der Rest der Moleküle erreicht die Oberfläche des Zellkerns, um ein neues C=C/ zu produzieren. CC-Bindung und dann in dieser Form kontinuierlich gewachsen. Mit der Verlängerung der Erhitzungszeit wird die Morphologie der CQDs allmählich gebildet. Gleichzeitig können bei der hydrothermalen Behandlung gebildeter CQDs die Oberfläche und der Rand von CQDs viel Hydroxyl (–OH), Carboxyl (–COOH) und Carbonyl (–C=O) oder anderen Sauerstoff enthalten. mit funktionellen Gruppen; ein Teil des H- und O-Atoms in diesen Gruppen könnte durch Dehydratisierung in der hydrothermalen Umgebung entfernt werden.
Um die optischen Eigenschaften von CQDs zu untersuchen, wurden die UV-Vis-(UV-Vis)-Absorptions- und Photolumineszenz-(PL)-Spektren von CQDs entsprechend gemessen. Wie in Abb. 4a gezeigt, wurde der optische Absorptionspeak der CQDs im ultravioletten Bereich mit einer maximalen Absorption bei 283 nm beobachtet, was auf n . zurückzuführen ist -π * Übergang der C=O-Bande [29]. Das PL-Spektrum in Abb. 4b zeigt, dass die PL-Emissionswellenlänge von CQDs den Peak bei 482 nm mit einer Anregungswellenlänge von 410 nm erreicht. Die Emissionswellenlänge verschob sich von 430 auf 530 nm, wenn die Anregungswellenlänge von 330 auf 490 nm erhöht wurde. Mit zunehmender Anregungswellenlänge werden fluoreszenzemittierende Peaks rotverschoben, was auf das Auftreten von Photonen-Reabsorption hinweist. Das Ergebnis zeigt, dass CQDs ein erregungsabhängiges PL-Merkmal aufweisen [30]. Die grün fluoreszierenden CQDs zeigen auch einen breiten PL-Peak, der sich mit der Änderung der Anregungswellenlänge verschiebt, was mit dem Quantenbeschränkungseffekt und Kantendefekten zusammenhängt. Bei der Standard-PL-Messung [22] beträgt die Fluoreszenzquantenausbeute der CQDs 16,7% bei einer Anregungswellenlänge von 410 nm, wobei Chininsulfat als Referenz verwendet wurde. Dieser Wert ist deutlich besser als der QY (8,95 %) von CQDs aus Zitronensaft im vorherigen Bericht [24]. Es ist bekannt, dass die QY der CQDs nach Oberflächenmodifikation oder Passivierung dramatisch verbessert werden kann [30]. Die Zugabe von Ethanol während des Syntheseprozesses kann mehr funktionelle Gruppen einführen, was zu einer höheren QY von CQDs führen kann. Allerdings ist der QY der CQDs in dieser Studie deutlich niedriger als der QY der CQDs, die unter Verwendung von Citronensäure (CA) und Ethanolamin (EA) als Modellmoleküle synthetisiert wurden. Hier führte die Pyrolyse bei 180 °C zu einer molekularen Vorstufe mit einer stark intensiven PL und einer hohen QY von 50 %, was auf die N-Dotierung während des Syntheseprozesses zurückzuführen ist [30].
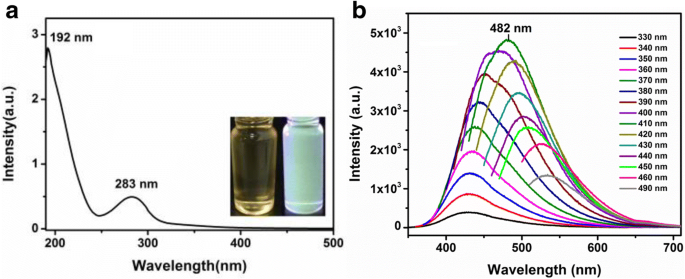
a UV-Vis-Absorptionsspektren von CQDs, Einschub:optische Bilder unter Tageslicht (links) und UV-Licht (rechts). b PL-Spektren von CQDs bei verschiedenen Anregungswellenlängen
Da sie nicht toxisch und umweltfreundlich sind, werden die CQDs als Alternativen zu Halbleiter-Quantenpunkten betrachtet, die in biologischen Systemen sowohl in vitro als auch in vivo eingesetzt werden können. Die so synthetisierten CQDs wurden in einem optischen Bild von Zwiebelepidermiszellen wie in Abb. 5 gezeigt aufgetragen. Die Fluoreszenzmikroskopie zeigt, dass die Zellwände und der Zellkern der inneren Epidermiszellen der Zwiebel klar, gut gebettet und stark im dreidimensionalen Sinne. Die Ergebnisse zeigen, dass die Färbung und Abbildung von Kohlenstoffquantenpunkten hervorragend ist und keine nachteiligen Auswirkungen auf Organismen und keine morphologischen Schäden der beobachteten Zellen hat, was weiter CQDs mit geringer Zytotoxizität demonstriert. Das konfokale Bild in Abb. 5 zeigt, dass die aus Zitronensaft synthetisierten CQDs bei der Bildgebung von Pflanzenzellen als Fluoreszenzindikatoren verwendet werden können, und zeigt außerdem die möglichen Anwendungen der biologischen Bildgebung von CQDs.
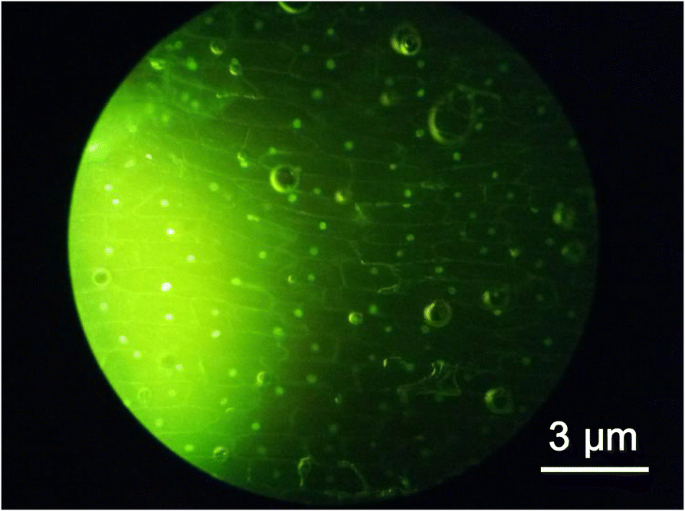
Ein optisches Bild von Zwiebelepidermiszellen, die mit CQDs gefärbt wurden, die von einer blauen Lichtquelle beleuchtet wurden
Schlussfolgerungen
In dieser Studie wurden die wasserlöslichen fluoreszierenden Kohlenstoffquantenpunkte unter Verwendung von Zitronensaft als Kohlenstoffquelle durch eine einfache hydrothermale Reaktion synthetisiert. Diese CQDs haben gute Material- und optische Eigenschaften. Sie können unter UV- oder Blaulichtbestrahlung eine helle blau-grüne Farbfluoreszenz emittieren. Wir haben gezeigt, dass die CQDs bei der Bildgebung von Pflanzenzellen verwendet werden können. Wir hoffen, dass diese wichtigen und signifikanten Erkenntnisse uns helfen können, ein tiefgreifendes Verständnis von CQDs zu erlangen und praktischere Anwendungen der neuen kohlenstoffbasierten Nanostrukturen zu erforschen.
Abkürzungen
- CQDs:
-
Kohlenstoff-Quantenpunkte
- FFT:
-
Schnelle Fourier-Transformation
- HPLC:
-
Hochleistungsflüssigkeitschromatographie
- PL:
-
Photolumineszenz
- QLED:
-
Quantenpunkt-LED
- QY:
-
Quantenausbeute
- R-CDs:
-
Rot emittierende Karbonpunkte
- TEM:
-
Transmissionselektronenmikroskop
- UV-Vis:
-
Ultraviolett-sichtbar
- XPS:
-
Röntgenphotoelektronenspektroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Die atomare Umlagerung von GaN-basierten mehreren Quantenquellen in H2/NH3-Mischgas zur Verbesserung der strukturellen und optischen Eigenschaften
- Modulation der elektronischen und optischen Anisotropieeigenschaften von ML-GaS durch vertikales elektrisches Feld
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Synthese von Pyridin-reichen N,S-codotierten Kohlenstoff-Quantenpunkten als wirksame Enzymnachahmer
- Optische und elektrische Eigenschaften von Silizium-Nanodrähten, die durch stromloses Ätzen hergestellt wurden
- Ein einfacher Ansatz zur Synthese von fluoreszierenden Kohlenstoffquantenpunkten aus Tofu-Abwasser
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
- Mikrostrukturelle, magnetische und optische Eigenschaften von Pr-dotierten Perowskit-Manganit-La0.67Ca0.33MnO3-Nanopartikeln, die über einen Sol-Gel-Prozess synthetisiert wurden
- Synthese und Eigenschaften von wasserlöslichen blau emittierenden Mn-legierten CdTe-Quantenpunkten



