Vergleichende Studien zu zweidimensionalen (2D) rechteckigen und hexagonalen Molybdändioxid-Nanoblättern mit unterschiedlicher Dicke
Zusammenfassung
Molybdändioxid (MoO2 .) ) eine Art Halbmetallmaterial weist viele einzigartige Eigenschaften auf, wie z. B. einen hohen Schmelzpunkt, gute thermische Stabilität, ein großes Oberflächen-Volumen-Verhältnis, hochdichte ungesättigte Oberflächenatome und eine ausgezeichnete Leitfähigkeit. Es besteht ein starker Zusammenhang zwischen Strukturtyp und optoelektronischen Eigenschaften von 2D-Nanoblättern. Hier die rechteckigen und sechseckigen Typen von dünnem und dickem MoO2 2D-Nanoblätter wurden erfolgreich aus MoO3 . hergestellt Pulver mittels chemischer Zwei-Zonen-Gasphasenabscheidung (CVD) mit Änderung der experimentellen Parameter, und diese hergestellten Nanoblätter zeigten unter dem Hellfeldmikroskop unterschiedliche Farben, besitzen Ränder und eine glatte Oberfläche. Die Dicke des blauen sechseckigen und rechteckigen MoO2 Nanoblätter sind ~ 25 nm bzw. ~ 30 nm, während die typische Dicke orangefarbener Nanoblätter etwa ~ 100 nm beträgt. Es wurden vergleichende Analysen und Untersuchungen durchgeführt und Mischkristallphasen in dickem MoO2 . identifiziert als Hauptmatrix durch Raman-Spektroskopie. Zum ersten Mal wurden die Emissionsbanden in dickem MoO2 Nanoblätter über ein Kathodolumineszenz(CL)-System mit besonderen Eigenschaften von Halbmetallen und Halbleitern; bei dünnen Nanoblättern wurde jedoch keine CL-Emission nachgewiesen. Die elektrischen Eigenschaften von dünnem MoO2 Nanoblätter mit unterschiedlichen Morphologien wurden verglichen, und beide zeigten unterschiedliche metallische Eigenschaften. Der Widerstand eines dünnen rechteckigen Nanoblatts betrug ~ 25 Ω bei ± 0,05 V, während 64 Ω bei ± 0,05 V für ein hexagonales Nanoblatt berichtet wurde und ein geringerer Widerstand bei einem rechteckigen Nanoblatt als bei einem hexagonalen Nanoblatt beobachtet wurde.
Einführung
Bis heute wurden verschiedene 2D-Materialien synthetisiert, wie Graphen, Übergangsmetalldichalkogenide, Antimon, schwarzer Phosphor, Mo2 C und h-BN [1,2,3,4,5,6]; veranschaulichen das unglaubliche Potenzial für neue Arten optoelektronischer Bauelemente aufgrund ihrer einzigartigen Eigenschaften und ihrer vielfältigen Möglichkeiten für die Herstellung von 2D-Materialtechnologien [7]. Sicherlich haben einige spezifische 2D-Materialien Mängel wie Null-Bandlücke, niedrige Absorptionseffizienz und Instabilität in offener Atmosphäre sind die Herausforderungen bei der Herstellung idealer nanoskaliger Bauelemente. Um diese Herausforderungen zu überwinden, haben sich Übergangsmetalloxide (TMOs) als effektive 2D-Materialien erwiesen, die eine hohe Leitfähigkeit, Piezoelektrizität, kolossalen Magnetowiderstand, bessere Stabilität in offener Umgebung und Supraleitfähigkeit usw. aufweisen [8,9,10]. Molybdändioxid ist ein typisches TMO-Material mit drei kristallinen polymorphen Formen; hexagonale Phase (P63 /mmc ) [11], tetragonale Phase (P42 /mnm ) [12] und monoklin (P21 .) /c) [13] und besitzt auch eine teilweise Rutil-Konfiguration [14] mit MoO6 , oktaedrisch verknüpftes Mo durch Sauerstoffatome in den Kanten der Elementarzelle umfasst vier MoO2 Einheiten gegenüber zwei Elementarzellen [15, 16]. Es ist bekannt, dass die Eigenschaften von Molybdänoxiden stark von ihrer kristallinen Struktur abhängen; insbesondere die Rutilstruktur von MoO2 ist interessant aufgrund der hervorragenden metallähnlichen elektrischen Leitfähigkeit [12], des geringen spezifischen elektrischen Widerstands, des hohen Schmelzpunkts [17, 18], des leichten Ionentransports [19] und der ausgezeichneten chemischen Stabilität [20]. Es wurde mit verschiedenen interatomaren Bindungen und vergleichsweise über der höchsten Zustandsdichte auf dem Fermi-Niveau in Beziehung gesetzt. Das Vorhandensein freier Elektronen erzeugt Mo 4+ in MoO2 im Gegensatz zur Generation von Mo 6+ von MoO3; daher sind alle Valenzelektronen im Molybdänmetall kovalent an die nächsten Sauerstoffatome gebunden [21, 22]. Eine kleine Variation der Mo-Valenz kann erhebliche Schwankungen der physikalischen Eigenschaften der Molybdänoxide verursachen. Zum Beispiel ist es möglich, Verbindungen anderer Oxide mit unterschiedlichen physikalischen Eigenschaften zu erhalten [23, 24].
Daher können Kristallinität, Form und Größe des Produkts glatt durch Ändern verschiedener Parameter unter gewünschten Synthesetechniken erreicht werden; beispielsweise Spevack et al. erhaltene monokline Struktur MoO2 (P21 /c) von ɑ-MoO3 durch thermische Reduktionsverfahren [25]. Alveset al. berichteten über die elektronischen und strukturellen Übergänge bei verschiedenen Temperaturen und führten zu einer Erhöhung der Wärmeausdehnung, Wärmekapazität und des spezifischen elektrischen Widerstands von einkristallinem MoO2 [26]. Jacobet al. beschrieb die Verformung in MoO2 bei hoher Temperatur und bestätigten einen Phasenübergang, der bei einer bestimmten Temperatur mit Umwandlung der verzerrten Rutilstruktur (P 21 /c ) in eine hexagonale Rutilstruktur (P 42 /mnm ) [27]. Darüber hinaus variieren die elektronische Struktur und die Eigenschaften von Molybdänoxidmaterialien mit der Dicke [16] und MoO2 Nanostrukturen werden aufgrund ihrer überlegenen Ladungstransporteigenschaften häufig in elektrochemischen Superkondensatoren [28], Katalyse [18], Sensorik [29], Energiespeicherung [30], elektrochromen Displays [31] und Energieumwandlungsregimen [32] verwendet [24]. Darüber hinaus wurden verschiedene Methoden zur Synthese verschiedener Morphologien verwendet MoO2 zur Erzielung außergewöhnlicher Eigenschaften. MoO2 hat keine Van-der-Waals-Kristalleigenschaft und kann daher nicht von der Masse zu Schichten abgeschält werden. Hauptsächlich MoO2 wurde aus ihren Vorläufern durch verschiedene Techniken synthetisiert, darunter hydrothermale und solvothermale Wege [11], thermische Zersetzung von Molybdaten [33], feste Reduktionsreaktion [34] und Elektrospinnen [35] mit unterschiedlichen Morphologien, wie Nanopartikeln [36], Nanodrähte [31], Nanostäbe [28], Nanosterne [28], Nanoblätter [37], hohle [38] und mesoporöse Partikel [39]. Diese Methoden haben sich jedoch als unwirksam erwiesen, um die Oberflächenmorphologie und -größe von Partikeln zu kontrollieren [22].
Zweidimensionales MoO2 Nanoblätter mit einer dünnen und gut homogenen Oberflächenmorphologie gelten als geeignet für eine hohe metallische Leitfähigkeit, perfekte chemische Stabilität und ermöglichen 2D-MoO2 Nanoblätter als vielversprechend für die Integration von 2D-Materialien in eine Vielzahl elektronischer Strukturen und nanoskaliger Geräte [40]. Hier haben wir eine vergleichende Studie und Synthese von zweidimensionalen (2D) rechteckigen und hexagonalen Molybdänoxid-Nanoblättern auf SiO2 . präsentiert /Si ohne Nachglühbehandlung mittels CVD-Technik:die zwei Arten von ultradünnem MoO2 Nanoblätter unterschiedlicher Dicke wurden erfolgreich hergestellt und durch Raman-, AFM- und CL- sowie I–V-Charakterisierungen charakterisiert. Das elektrische Verhalten der Molybdänoxide variiert von Halbmetall bis hin zu Halbleitern mit großer Bandlücke, da es von der Dicke und dem Oxidzustand abhängt. Die Zeiteinstellung steuert die Abscheidung, Dicke und bestimmt die Suboxidzustände [41]. Einblicke in die Phasenstabilität, Bereiche und Mischungen der Oxide sind nicht nur für das Verständnis von Molybdänoxid-Nanoblättern von Bedeutung, sondern auch für andere TMOs für optoelektronische Anwendungen wichtig [42].
Methoden/Experimenteller Abschnitt
Synthese des sechseckigen MoO2 Nanoblätter
Synthese von hexagonalen Molybdändioxiden (MoO2 .) ) Nanoblätter aus Vorläufer ~ 20 mg MoO3 Pulver (99,95%, Alfa Aesar) an einem Ende des Quarzrohres in ein Porzellanschiffchen gegeben und in einem Zweizonenofen unter Stickstoff (N2 .) erhitzt ) Atmosphäre wie in Abb. 1a gezeigt. Das Eltern-SiO2 /Si-Substrate werden nacheinander mit entionisiertem Wasser, Aceton, Ethanol und Isopropanol durch Beschallung gereinigt und die sauberen Substrate in einem Abstand von 3 cm von Vorläuferpulvern angeordnet. Am Ende des Quarzrohres wurden zwei Thermoblöcke angebracht; Vor dem Erhitzen wurde das Quarzrohr mit einem N2 . gespült (99,999 %) bei einer konstanten Gasflussrate von 200 sccm für 20 Minuten, um O2 . zu entfernen und andere Verunreinigungen und reduzierte dann die Fließgeschwindigkeit auf 20 sccm als Trägergas. Die linke Heizzone wurde mit einer Geschwindigkeit von 10 °C min −1 . auf 480 °C eingestellt Temperaturanstieg, während die rechte Zone bei gleicher Temperaturanstiegsrate auf 780 °C eingestellt und 20 Minuten in Gegenwart von N2 . gehalten wurde Umgebung. Nach Beendigung der Reaktion ließ man den Ofen auf natürliche Weise auf Raumtemperatur abkühlen und erhielt schließlich hexagonales MoO2 auf dem SiO2 . abgeschiedene Nanoblätter /Si-Substrate.
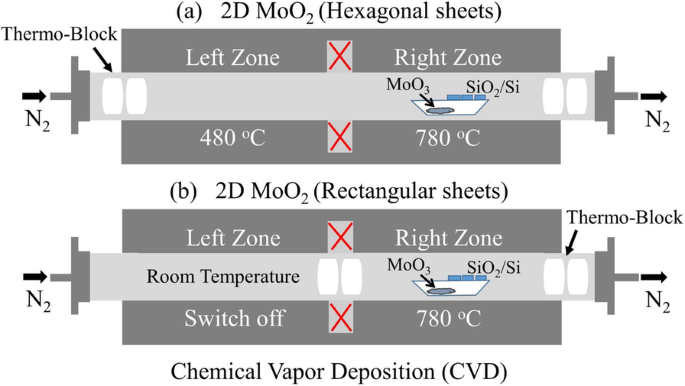
Schematischer Aufbau des CVD-Systems (das rote Kreuz repräsentiert isolierende Bereiche). a Hexagonale Molybdänoxide. b Rechteckige Molybdänoxide
Synthese des Rechtecks MoO2 Nanoblätter
In ähnlicher Weise wie oben erwähnt, ist das Rechteck Molybdändioxid (MoO2 ) Nanoblätter wurden in einem Zweizonen-Röhrenofen unter N2 . gezüchtet Atmosphäre, wie in Abb. 1b gezeigt. In diesem Aufbau wurden die Thermoblöcke nahe der Mitte des Rohres platziert:linke Zone wurde auf Raumtemperatur eingestellt und der Rest der Parameter blieb gleich wie bei der Synthese von hexagonalem MoO2 Nanoblätter, um rechteckiges MoO2 . zu züchten Nanoblätter auf dem SiO2 /Si-Substrate.
Herstellung der Geräte
Es folgte Elektronenstrahllithographie zur Herstellung von Elektroden mit Ti (10 nm)/Au (90 nm) für hexagonales und rechteckiges MoO2 Nanoblätter als Kontakt.
Charakterisierungen
AFM-Bilder wurden unter Verwendung eines Rasterkraftmikroskops, eines Dimension Edge PSS (Bruker, Inc., Karlsruhe, Deutschland) in einem kontaktlosen Modus erhalten. SEM-Bilder wurden unter einem Hitachi S-4800-Mikroskop aufgenommen, das bei 10,0 kV arbeitete. Optische Fotografien wurden mit einem optischen Mikroskop (Olympus BX51M) aufgenommen. Raman-Spektren wurden mit einem konfokalen Raman-Aufbau (basierend auf dem Spektrometer Princeton Acton SP2500) aufgenommen. Kathodolumineszenz (CL)-Spektren wurden mit einem CL-Messaufbau (Horiba Is-100-em-type2) aufgenommen. Die I-V-Kurven der Geräte wurden mit einem Mikrosondenstationssystem (Keithley 4200-SCS) gemessen.
Ergebnisse und Diskussionen
Für die Synthese von rechteckigen und hexagonalen TMO-Nanoblättern wurden unterschiedliche Bedingungen eingestellt, und die sich ändernden Parameter führten zu unterschiedlich geformten Nanoblättern, wie in Abb. 1 gezeigt. Die Literatur schlägt einige mögliche Reaktionsmechanismen für CVD-gezüchtete Nanoblätter vor; ein Teil der Stickstoffgasmoleküle wird bei einer bestimmten Temperatur durch thermische Bestrahlung in einem Röhrenofen in ionisierte Stickstoffmoleküle umgewandelt, und solche ionisierten Stickstoffmoleküle werden durch \({\mathrm{N}}_2^{\ast}\) gekennzeichnet [43] . Bei der gewünschten Temperatur werden die Moleküle von MoO3 kollidieren mit den ionisierten \({\mathrm{N}}_2^{\ast}\)-Molekülen, die in Gegenwart einer inerten Stickstoffgasumgebung eine Reihe möglicher Reaktionen hervorrufen [44,45,46].
$$ \mathrm{e}+{\mathrm{N}}_2\to {\mathrm{N}}_2^{\ast}+\mathrm{e} $$ (1) $$ {\mathrm{M} }_{\textrm{o}}{\textrm{O}}_3+\left(\frac{x}{2}\right){\textrm{N}}_2^{\ast}\to {\textrm{ M}}_{\mathrm{o}}{\mathrm{O}}_{3-\mathrm{x}}+\mathrm{xNO} $$ (2) $$ {\mathrm{M}}_{ \mathrm{o}}{\mathrm{O}}_{3-\mathrm{x}}+\left(\frac{1-x}{2}\right){\mathrm{N}}_2^{ \ast}\to {\mathrm{M}}_{\mathrm{o}}{\mathrm{O}}_2+\left(1-\mathrm{x}\right)\ \mathrm{NO} $$ ( 3) $$ {\mathrm{M}}_{\mathrm{o}}{\mathrm{O}}_2+3{\mathrm{M}}_{\mathrm{o}}{\mathrm{O} }_3\kern0.5em \to {\mathrm{M}}_{\mathrm{o}4}{\mathrm{O}}_{11} $$ (4)Die Struktur von verdampftem MoO3 Moleküle können sich in unterschiedliche Morphologien ändern Nanoblätter, entweder durch Erhöhen oder Verringern von N2 Gasfluss und die Haltezeit bei gewünschten Temperaturen [45]. Während die Moleküle zu Substraten diffundieren, beginnen sie sich zu aggregieren, um verschiedene Arten von regelmäßigem rechteckigem und hexagonalem MoO2 . zu bilden Blätter.
Abbildung 2a zeigt durch CVD hergestelltes hexagonales MoO2 Nanoblätter weit besser als die lösungsbasierte Synthese von hexagonalem MoO2 Nanoblätter [47, 48]. Darüber hinaus sind verschiedene Phasenstrukturen von rechteckigem MoO2 kann unter Verwendung der CVD-Technik mit bestimmten Steuerparametern erhalten werden; die Temperatur der Heizzonen, die Position der Thermoblöcke und die Position der Substrate, wie in Fig. 2d gezeigt. Festlegen der Temperatur der linken Heizzone auf 480 ° C war extrem wichtig für die Synthese von hexagonalem MoO2 Nanoblätter. Der grundlegende Mechanismus von hexagonalem MoO2 Nanoblätter ist ein Temperaturgradient. Xu, X. et al. berichten über eine hohe Abhängigkeit der morphologischen Variation vom thermodynamischen und kinetischen Einfluss im Kristallwachstumsprozess, der auf dem Unterschied in der thermodynamischen Stabilität und der Gitterspannung zwischen den Phasen basiert [49]. Sowohl Tief- als auch Hochtemperaturzonen spielen eine entscheidende Rolle bei der Herstellung von hexagonalen Nanoblättern; jedoch ist die Temperaturschwankung der Hochtemperaturzone sehr effektiv für das Wachstum von rechteckigem MoO2 Nanoblatt. Außerdem haben Wang, S., et al. berichteten über eine Entwicklung zweidimensionaler Nanoblätter, die stark von der räumlichen Lage der Substrate abhängen [50]. Yang, X., et al. berichteten auch über das temperaturabhängige Wachstum der regulären Nanoblattmorphologie und erklärten weiter den chemischen Dampfmechanismus mit Hilfe der KMC-Methode des ersten Prinzips [51]. Es gibt einige blau- und orangefarbene hexagonale und rechteckige Nanoblätter unterschiedlicher Dicke; blau gefärbte Nanoblätter sind dünner als orange gefärbte Nanoblätter und stimmen eng mit den Eigenschaften anderer 2D-Materialien überein [52]. Mischfarben bedeuten ein geschichtetes Nanoblatt in verschiedenen Dicken, wie in Abb. S1 und Abb. S2 in den Zusatzinformationen gezeigt. Die Dicke der Nanoblätter nahm der Reihe nach monoton ab:orange Farbe, gelbe Farbe und blaue Farbe, was von der Variation der Syntheseparameter abhängt. Abbildung 2b, e zeigt das verstärkte SEM-Bild des typischen hexagonalen und rechteckigen Nanoblatts, das eine glatte Oberfläche, klare Ränder, eine regelmäßige Form von hoher Qualität und eine Länge von 10 μm zeigt. Das AFM maß die blauen hexagonalen und rechteckigen Nanoblätter als ~ 25 nm bzw. ~ 30 nm dick, wie in Abb. 2c, f. gezeigt.

a Fotografie von hexagonalen Molybdänoxid-Nanoblättern unter dem Mikroskop. b SEM-Aufnahme eines hexagonalen Molybdänoxid-Nanoblatts, Maßstabsbalken 2 μm. c AFM-Ergebnis eines blau gefärbten hexagonalen Molybdänoxid-Nanoblatts. d Fotografie von rechteckigen Molybdänoxid-Nanoblättern unter dem Mikroskop. e SEM-Aufnahme einer rechteckigen Molybdänoxid-Nanoschicht auf einem 2 μm-Maßstab. f AFM-Ergebnis eines blau gefärbten rechteckigen Molybdänoxid-Nanoblatts
Raman-Spektren wurden aufgenommen, um die Qualität und Gleichmäßigkeit von MoO2 . im gewachsenen Zustand zu untersuchen Nanoblätter. Hier präsentieren wir Raman-Spektren von rechteckigem und hexagonalem MoO2 Nanoblätter mit unterschiedlichen Farben unter der Bestrahlung von 532 nm Laser. In Abb. 3a befinden sich die Raman-Peaks, die von einem dünnen hexagonalen Nanoblatt (blaue Farbe) erhalten wurden, bei 143,1, 184,6, 204,6, 229,6, 292,0, 311,0, 364,3, 383,3, 495,7, 570,5 und 737,6 cm −1 , bzw. Im Vergleich zum dünnen rechteckigen Nanoblatt stimmen blaue Farbpeaks mit einer kleinen Peakverschiebung bei 143,1, 185,1, 204,6, 229,2, 292,7, 311.1, 361,7, 380.2, 495,9, 569,8 und 735,1 cm −1 , bzw. Beide Arten von dünnen, blau gefärbten Nanoschichten haben die gleiche Anzahl von Raman-Peaks; jedoch wurde ein zusätzlicher starker Siliziumpeak bei 526 cm −1 . erhalten in blau gefärbtem hexagonalem Nanoblatt. Tatsächlich rührt die Peakverschiebung vom Dickenunterschied der Nanoblätter her; hexagonale Nanoblätter sind dünner als rechteckige Nanoblätter, wie in Abb. 2c, f gezeigt. Die zusätzliche Peakposition für Silizium erfolgte durch Laserpenetration, traf auf die Siliziumoberfläche, diente als Substrat und wurde der Dicke der blau gefärbten hexagonalen und rechteckigen Nanoblätter im Vergleich zu orangefarbenen dicken hexagonalen und rechteckigen Nanoblättern zugeschrieben, wie in Abb. 3a gezeigt. Für dicke hexagonale Nanoblätter wurden 13 Peaks mit der Peakposition bei 142,3, 183,5, 204,6, 229,2, 292,3, 311,0, 347,7, 361,6, 380.2, 457,8, 495,1, 570,2 und 739,7 cm –1 . erhalten , bzw. Die 13 Peaks, die für ein dickes rechteckiges Nanoblatt an den Positionen 143,3, 183,9, 204,6, 229,2, 292,2, 311,0, 346,1, 359,3, 380,2, 455,5, 495,1, 568,3 und 736,8 cm –1 . festgestellt wurden mit geringer Positionsvariation im Vergleich zu hexagonalen Nanoblättern. Die Dicke induzierte wenige zusätzliche Peaks bei anderen Wellenzahlen im Vergleich zu den blau gefärbten dünneren Nanoblättern [53]. Die Identifizierungsdetails der Raman-Peaks für dünne/dicke hexagonale und rechteckige Nanoblätter sind in Abb. S3 in der ergänzenden Datei angegeben; die Ergebnisse stimmen gut mit den berichteten Ergebnissen von monoklinem MoO2 . überein Dünnfilm, hergestellt durch verschiedene CVD-Synthesewege [54, 55]:Dicke und Verschiebung der Peaks hängen von den Wachstumsbedingungen ab [56, 57]. In der vorliegenden Arbeit berichten wir zum ersten Mal 13 Schwingungspeaks für orange Farbe, während 11 Peaks für blaues regelmäßiges hexagonales und rechteckiges MoO2 Nanoblätter, was die Existenz gemischter Strukturen in MoO2 . bestätigt Nanoblätter. Die scharfen und starken Peaks bestätigten eine bessere Kristallinität im Vergleich zu anderen berichteten Ergebnissen [15, 54, 55].
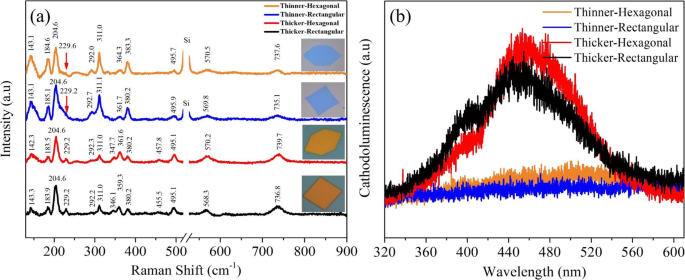
a Raman-Spektren von blauen dünnen hexagonalen und rechteckigen Molybdänoxid-Nanoblättern und orangefarbenen dicken hexagonalen und rechteckigen Molybdänoxid-Nanoblättern. b Kathodolumineszenzspektren (CL) (orange Spektren für dünne hexagonale Nanoblätter, blaue Spektren repräsentieren dünne rechteckige Nanoblätter, rote Spektren repräsentieren dicke hexagonale Nanoblätter und schwarze Spektren repräsentieren dicke rechteckige Nanoblätter)
Wir können aus diesen vier typischen Nanoschichten schließen, dass sie alle eine komplexe und gemischte Struktur enthalten, wie zum Beispiel reines MoO3 , MoO3−x , monoklines MoO2 , orthorhombisches MoO3 (α-MoO3 ) und orthorhombisches Mo4 O11 . Der Raman-Peak bei 289 cm −1 wird reinem MoO3 . zugeordnet , 142 cm −1 zu MoO3−x [58] und der Peak bei 287 cm −1 ist assoziiert mit orthorhombischem α-MoO3 [59]. Dieterle, M. berichtete über Raman-Peaks für verschiedene Molybdänoxide; orthorhombisches MoO3 , monoklines MoO2 , und orthorhombisches Mo4 O11; die Banden bei 290–292 cm −1 gelten als aus orthorhombischem MoO3 . entstanden (α-MoO3 ), während Raman seinen Höchststand bei 183, 306 cm −1 . erreicht aufgezogen aus orthorhombischem Mo4 O11 [60]. Die Peaks bei 380 cm −1 wurden MoO2 . zugeordnet [61] und 460 cm −1 zu α-MoO3 [62]. Die Ergebnisse der Raman-Spektren unserer synthetisierten Nanoblätter sind in Abb. 3a dargestellt. Ergebnisse von Raman-Spektren einzelner Nanoblätter sind in ergänzender Abb. S3 verfügbar. Daher sind die Raman-Peaks in unseren Ergebnissen mit verschiedenen Strukturphasen verschiedener Molybdänoxide verbunden:142,3 ~ 143,3 cm −1 (MoO3−x ), 183,5 ~ 185,1 cm −1 (Mo4 O11 ) und 204,6 cm −1 (MoO2 ). Darüber hinaus Peaks bei 229,2 ~ 229,6 cm −1 (MoO2 ), die in orangefarbenen Nanoblättern vorhanden sind, sind schärfer und breiter im Vergleich zu blau gefärbten Nanoblättern, was die Existenz mehrerer Spannungen in dicken Nanoblättern bestätigt. Die Peaks bei 292,0 ~ 292,7 cm −1 (α-MoO3 ) in blau gefärbten Nanoblättern sind schärfer und breiter als orange gefärbte Nanoblätter. Die Peaks bei 311,0 ~ 311,1 cm −1 (Mo4 O11 ) kommen in allen vier Arten von Nanoblättern vor; der intensivere Peak befindet sich in dünnen blau gefärbten Nanoblättern im Vergleich zu orangefarbenen Nanoblättern. Die Spitzen bei 346,1 ~ 347,7 cm −1 (MoO2 ) existieren nur in orangefarbenen Nanoblättern. Meistens sind all diese Peaks in allen Arten von Nanoblättern mit geringer Variation vorhanden; Peaks bei 359,3 ~ 364,3 cm −1 für (MoO2 ) und Spitzen bei 380,2 ~ 383,3 cm −1 (MoO2 ) waren in allen Nanoblättern vorhanden; jedoch die Peaks bei 455,5 ~ 457,8 cm −1 (α-MoO3 ) sind nur in orangefarbenen Nanoblättern vorhanden. Hauptpeaks stimmen gut mit Molybdändioxid überein und sind in allen Nanoschichten erhöht, z. B. Peaks bei 495,1 ~ 495,9 cm −1 (MoO2 ), 568,3 ~ 570,5 cm −1 (MoO2 ) und 735,1 ~ 739,7 cm −1 (MoO2 ). Die Suboxide entstanden aufgrund von Intervalenzübergängen; in Suboxiden ist der Abstand zwischen Mo-Atomen mit Sauerstoffatomen verbunden, in denen seitlich tetraedrisch c Achse nahm mit zunehmender Verzerrung der Bindung vom ungestörten Teil zur Scherebene zu. Dies betrifft die vollständig polarisierten Moden parallel zu c Achse:die polarisierten Moden senkrecht zu c Achsen werden durch die Abstände der M=O-Bindung beeinflusst. Das Entweichen von Sauerstoffatomen aus reinem MoO3 nach Behandlung mit Hochtemperatur bestätigten sich scherkristallographische Strukturen über verlängerte Scherdefekte, wodurch die Translationssymmetrie beendet wurde [58]. Die größere Anzahl zusätzlicher Peaks wird für orangefarbene hexagonale und rechteckige Nanoblätter festgestellt, die von den regulären Peaks von Molybdändioxid abweichen; die Peaks bei 142,3 ~ 143,3 cm −1 für MoO3−x , die Peaks bei 292,2 ~ 292,3 und 455,5 ~ 457,8 cm −1 für α-MoO3 , und Peaks bei 183,5 ~ 183,9 und ~ 311,0 cm −1 für Mo4 O11 .
Zur weiteren Verifizierung wird die Kathodolumineszenz (CL) durchgeführt, um den Einfluss der Strukturphase komplexer Molybdänoxid-Strukturphasen auf die metallischen Eigenschaften sowohl dicker hexagonaler als auch rechteckiger Nanoblätter zu verifizieren. Theoretisch ist das halbmetallische MoO2 wird sich teilweise in Halbleiter verwandeln aufgrund der Beteiligung von MoO3 . Es ist jedoch sehr schwierig, das PL-Spektrum von reinem MoO2 . zu messen Nanostrukturen aufgrund der metallischen Eigenschaften:MoO3 ist ein Halbleiter mit großer Bandlücke mit einer schwachen Lumineszenzintensität bis zur Umwandlung und zum Verschwinden von MoO3 zu MoO3−x , und weitere Umwandlung in MoO2 Nanoblätter [63]. Daher wurde kein Lumineszenzspektrum für hexagonale und rechteckige Molybdänoxid-Nanoblätter berichtet.
Die Kathodolumineszenz (CL)-Eigenschaften von Molybdän-Dick-Nanoblättern zeigten den elektronischen Übergang zwischen dem Leitungs- und Valenzband aufgrund der Anwesenheit von Suboxiden. Wie in Abb. 3b gezeigt, zeigen die CL-Spektren, die für dicke hexagonale und rechteckige Molybdänoxid-Nanoblätter aufgenommen wurden, kleine CL-Peaks bei 410 nm (3.02 eV), während stärkere und breitere Peaks bei 454 nm (2.73 eV) von Nanoblättern erzeugt werden. Die schwächeren Peaks bei 410 nm in beiden CL-Spektren ähneln MoO3 Spektren, und die schwache Emission kann mit einer Rekombination des Fallenzustands in Verbindung gebracht werden:454-nm-Bande, die defektbezogenen Fallenzuständen zugeordnet wird, die von Sauerstoffleerstellen stammen [64]. Die emittierte Photonenenergie für reines MoO3 liegt bei 3,02 eV anstelle von 3,2 eV für die Bandlücke zeigt die Umwandlung von MoO3 . an Pulver in MoO3−x und wurde über die Ergebnisse der Raman-Spektren verifiziert. Die Breitband-CL-Spektren, die von 3.02 bis 2.73 eV variieren, bestätigten die gemischten Nanostrukturen in dicken Nanoblättern, die ein Metall-Halbleiter-Gradientenverhalten aufweisen. Diese Molybdänoxide stehen im Zusammenhang mit der Entwicklung von Trägerkonzentrationen, Sauerstoffleerstellenkonzentrationen in reduziertem MoO3 , und Konzentration freier Elektronen in MoO2 . Diese Studien erweiterten das Wissen um strukturelle und optische Eigenschaften von substöchiometrischen Molybdänoxid-Nanoblättern und trugen zur Entwicklung fortschrittlicher optischer Geräte bei. Ähnliche CL-Spektren werden für andere Übergangsmetalloxide wie WO3 . berichtet und α-Fe2 O3 [65]. Das Problem der CL-Spektrendetektion in dünnen Nanoblättern wird beschrieben und in der Literatur beschrieben. Die CL-Intensität der Flakes nahm mit abnehmender Schichtdicke ab; dünnschichtige Flocken sind für Elektronenstrahlen transparent; erzeugte Elektronenlöcher sind direkt proportional zu ihrer Dicke [66]. Bourrellier, R., et al. verifizierte Breitband-Lumineszenzdetektion in minderwertigen Kristallen, die nicht mit extrinsischen Defekten zusammenhängt, sondern offensichtlich mit intrinsischen Defekten, die durch Elektronenbestrahlung erzeugt werden können [67]. Vor kurzem haben Zhou, N., et al. berichteten über eine starke Orientierung der CL-Intensität aufgrund einer Zunahme der Defektkonzentration und einer zunehmenden Flockendicke, aber die Intensität der CL-Emission nahm mit der Abnahme der Flockendicke ab [68]. Trotz dieses Effekts zeigen die dicken Flakes eine deutliche Lumineszenz im Vergleich zu den dünnen Flakes. Dies ist der Grund, warum CL-Spektren von reinem, dünnem MoO2 in dünnen Nanoblättern nicht nachweisbar; die CL-Spektren von dünnen hexagonalen (orangefarbenen Spektren) und rechteckigen Nanoschichten (blaue Spektren) sind in Abb. 3b dargestellt.
Die dünnen hexagonalen und rechteckigen Nanoplättchen besitzen metallische Eigenschaften, die durch I-V-Messungen bestätigt wurden, wie in Abb. 4 und unterstützende Informationen (SI) in Abb. S4 gezeigt. Wir haben zwei Terminals mit sechs Bauelementen auf blauen dünnen Nanoblättern hergestellt und I-V-Kurven mit denselben Parametern gemessen; drei davon waren rechteckige Nanoblätter und der Rest der drei waren hexagonale Nanoblätter, wie im Einschub von Fig. 4a bzw. b gezeigt. Die Kontakte wurden mit Ti/Au als Elektroden hergestellt. Das schematische Diagramm einzelner rechteckiger und hexagonaler Molybdänoxid-Nanoblätter ist in Abb. 4a, b gezeigt. In Abb. 4c, d werden die I-V-Kurven beider Arten von Nanoblättern gemessen, indem die Vorspannung mehrmals von negativ (− 0,05 V) nach positiv (+ 0,05 V) verschoben wird, ohne dass sich die Geräte ändern, und werden linear angezeigt Verhalten bei ohmschem Kontakt zwischen Nanoschichten und Elektroden von Geräten. Ohmsche Gleichung wurde für die Widerstandsmessung verwendet, R = V /Ich , wobei R steht für Widerstand, V Spannung und I Strom; Der Widerstand von rechteckigen und hexagonalen Nanoblättern wurde bei ~ 25 Ω bei ± 0,05 V bzw. 64 Ω bei ± 0,05 V gemessen, was weiter bestätigte, dass rechteckige Nanoblätter einen geringeren Widerstand als hexagonale Nanoblätter aufweisen.
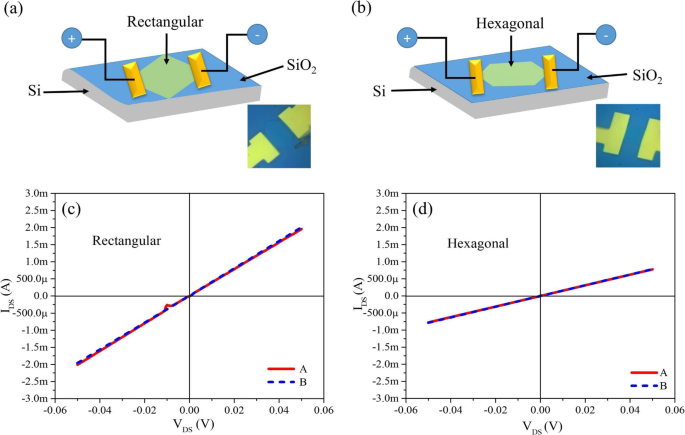
a Schematische Darstellung eines einzelnen rechteckigen Molybdänoxid-Nanoblatts. Einschub:Realbild des Geräts. b Schematische Darstellung eines einzelnen hexagonalen Molybdänoxid-Nanoblatts. Einschub:Realbild des Geräts. c I–V-Eigenschaften einzelner einzelner rechteckiger Molybdänoxid-Nanoblätter. d I-V-Eigenschaften einzelner hexagonaler Molybdänoxid-Nanoblätter
Zusätzlich ist der Widerstand (R ) blau gefärbter dünner rechteckiger Nanoblätter sind ~ 30 bei ± 0,05 V und ~ 43 Ω bei ± 0,05 V, wie in Abb. S4a, b in den unterstützenden Informationen (SI) gezeigt; jedoch Widerstand (R ) blauer dünner hexagonaler Nanoblätter sind ~ 61 Ω bei ± 0.05 V und ~ 61 Ω bei ± 0.05 V, wie in Abb. S4c, d gezeigt. Dies bestätigt, dass die blauen dünnen rechteckigen Nanoblätter einen geringeren Widerstand bei den gleichen Parametern aufweisen als blaue dünne sechseckige Nanoblätter.
Schlussfolgerungen
In dieser Arbeit berichten wir über die Kontrollsynthese von rechteckigen und hexagonalen Molybdänoxid-Nanoblättern aus einem einzelnen pulverförmigen MoO3 ohne Nachglühbehandlung durch CVD-Verfahren. Vergleichende Analysen und Untersuchungen wurden mit verschiedenen spektroskopischen Techniken durchgeführt:Raman-Spektren, optische Fotografie, Rasterelektronenmikroskopie, Rasterkraftmikroskopie und Kathodolumineszenz (CL). Der optische Kontrast hängt von der Dicke der Nanoschichten ab. Die REM-Ergebnisse bestätigten die Well-Symmetrie und die glatte Morphologie der kontrollierten Nanoblätter. Die AFM-Analyse maß ~ 30 nm Dicke dünner rechteckiger Nanoblätter und ~ 25 nm hexagonaler Nanoblätter. Ergebnisse der Raman-Spektren zeigen die Existenz gemischter Strukturen in MoO2 Nanoblätter aufgrund der komplexen kristallinen Strukturen. Eine starke Spektralempfindlichkeit und Peakverschiebung hängen von der Dicke der Nanoblätter ab. Vergleichsweise weniger Raman-Peaks wurden bei dünnen als bei dickeren Nanoschichten beobachtet und stimmen gut mit den Schwingungen des kristallinen MoO2 . überein und andere Mischkristalle; einige Peaks verschwanden jedoch in dünnen 2D-Nanoblättern. Die dicken orangefarbenen Nanoblätter enthalten aufgrund der komplexen Strukturphasen von Molybdänoxid mehr Peaks; insbesondere zusätzliches MoO3 und MoO3−x kommt in halbmetallischem MoO2 . vor , und somit zeigen die dicken Nanoblätter ein Halbleiterverhalten mit großer Bandlücke und wurden weiter durch Kathodolumineszenz(CL)-Spektren verifiziert. Zum ersten Mal wurden kombinierte metallische und Halbleitereigenschaften mit großer Bandlücke in gemischten Molybdänoxid-, dicken hexagonalen und rechteckigen Nanoblättern beobachtet. Diese Peaks in orangefarbenen Nanoblättern könnten hilfreiche photonische Materialien für praktische Anwendungen in nanoskaligen Geräten sein; bei dünnen Nanoblättern wird jedoch keine CL-Emission nachgewiesen. Die I-V-Kurven aller aus dünnen rechteckigen oder hexagonalen Nanoblättern hergestellten Bauelemente zeigten aufgrund des gut etablierten ohmschen Kontakts zwischen Nanoblättern und Elektroden ein lineares metallisches Verhalten. Das dünne hexagonale Nanoblatt zeigte einen höheren Widerstand als das rechteckige Nanoblatt. This study provides a deep comprehension of special 2D molybdenum oxide nanosheets, providing a way for modulating the properties of different types of nanosheet.
Verfügbarkeit von Daten und Materialien
All data are fully available without restriction.
Abkürzungen
- 2D:
-
Two dimensional
- MoO2 :
-
Molybdenum dioxide
- MoO3 :
-
Molybdenum trioxide
- CL:
-
Cathodoluminescence
- R:
-
Resistance
- Ω:
-
Ohm
- V:
-
Voltage
- I–V:
-
Current–Voltage
- Lebenslauf:
-
Chemische Gasphasenabscheidung
- Mo2 C:
-
Molybdenum carbide
- h-BN:
-
hexagonal-Boron nitride
- TMOs:
-
Transition metal oxides
- P:
-
Space group
- N2 :
-
Nitrogen
- \( {\mathrm{N}}_2^{\ast } \) :
-
Ionized nitrogen
- sccm:
-
Standard cubic centimeters per minute
- SiO2 /Si:
-
Silicon dioxide/silicon
- Ti:
-
Titanium
- Au:
-
Gold
- AFM:
-
Rasterkraftmikroskop
- SEM:
-
Rasterelektronenmikroskop
Nanomaterialien
- Experimentelle Forschung zur Stabilität und natürlichen Konvektion von TiO2-Wasser-Nanofluid in Gehäusen mit unterschiedlichen Rotationswinkeln
- Breitband-Perfekter Absorber mit Monolayer-MoS2 und hexagonalem Titannitrid-Nano-Disk-Array
- Einfache Synthese von Silbernanodrähten mit unterschiedlichen Aspektverhältnissen und Verwendung als flexible, transparente Hochleistungselektroden
- Auswirkungen der Doppelschichtdicke auf die morphologischen, optischen und elektrischen Eigenschaften von Al2O3/ZnO-Nanolaminaten
- Herstellung, Charakterisierung und biologische Aktivität von Avermectin-Nanoabgabesystemen mit unterschiedlichen Partikelgrößen
- Morphologie, Struktur und optische Eigenschaften von Halbleiterfilmen mit GeSiSn-Nanoinseln und gespannten Schichten
- Vergleichende Studie der elektrochemischen, biomedizinischen und thermischen Eigenschaften natürlicher und synthetischer Nanomaterialien
- Kontrollierte Synthese und selektive Adsorptionseigenschaften von Pr2CuO4-Nanoblättern:eine Diskussion des Mechanismus
- 20 verschiedene Metallarten und ihre Eigenschaften
- Verschiedene Eigenschaften und Sorten von Werkzeugstahl



