Herstellung, Charakterisierung und biologische Aktivität von Avermectin-Nanoabgabesystemen mit unterschiedlichen Partikelgrößen
Zusammenfassung
Nano-Abgabesysteme für Wirkstoffe von Pflanzenschutzmitteln können die Einsatzraten von Pflanzenschutzmitteln verbessern und ihre Bekämpfungswirkung verlängern. Dies ist auf die Nanocarrier-Hülle und die kontrollierte Freisetzungsfunktion zurückzuführen. Wirkstoffe enthaltende Partikel in Pestizidformulierungen mit kontrollierter Freisetzung sind jedoch im Allgemeinen groß und weisen breite Größenverteilungen auf. Es gab nur begrenzte Studien über die Wirkung der Partikelgröße auf die kontrollierten Freisetzungseigenschaften und die biologischen Aktivitäten von Pestizidabgabesystemen. In der aktuellen Studie wurden Nano-Abgabesysteme für Avermectin (Av) mit unterschiedlichen Partikelgrößen konstruiert und ihre Leistung bewertet. Die Av-Freisetzungsrate im Nano-Abgabesystem konnte durch Änderung der Partikelgröße effektiv gesteuert werden. Die biologische Aktivität nahm mit abnehmender Partikelgröße zu. Diese Ergebnisse legen nahe, dass Av-Nanoabgabesysteme die kontrollierbare Freisetzung, Photostabilität und biologische Aktivität signifikant verbessern können, was die Effizienz verbessert und Pestizidrückstände reduziert.
Hintergrund
Pestizide sind wichtig, um Pflanzenkrankheiten und Schadinsekten zu bekämpfen und die nationale Ernährungssicherheit zu gewährleisten. Die meisten herkömmlichen Pestizidformulierungen sind offene Systeme, die Probleme wie schlechte Dispersion, Abbau von Wirkstoffen und Tröpfchendrift aufweisen. Wirkstoffe in Pestiziden haben Verlustraten von bis zu 70–90%. Dies geschieht als Folge von Feldspritzen aufgrund von biologischem Abbau, chemischem Abbau, Photolyse, Verdunstung, Oberflächenabfluss und perkolierendem Grundwasser, die alle Bedenken hinsichtlich der Lebensmittelsicherheit und der Umwelt aufwerfen [1, 2]. Die Verbesserung der Anwendung und Abgabe von Pestiziden ist daher zu einem wichtigen Forschungsthema geworden [3,4,5].
In den letzten Jahren hat die Entwicklung von Nanotechnologie und Nanomaterialien einen neuen Ansatz zur Verbesserung der Effizienz der Pestizidanwendung geboten [6,7,8,9,10,11,12,13,14,15]. Nanopartikelformulierungen von Pestiziden wurden vorgeschlagen, um eine bessere räumliche Verteilung von Pestiziden auf Blattoberflächen zu erzeugen, aufgrund der geringen Größe und der großen Oberfläche der Nanopartikel, was eine bessere Effizienz bietet [16,17,18,19]. Nanoabgabesysteme für Pestizide beinhalten das Einschließen der Wirkstoffe von Pestiziden in polymere Nanomaterialien, um die langsame und kontrollierte Freisetzung von Wirkstoffen auf Zielkulturen zu ermöglichen [20,21,22]. Unter verschiedenen Polymeren wird Polymilchsäure (PLA) aufgrund ihrer nicht toxischen, guten Bioverfügbarkeit und Biokompatibilität und der Zulassung durch die Food and Drug Administration für den menschlichen Gebrauch in großem Umfang als Nanopartikelträger in Nanoabgabesystemen mit kontrollierter Freisetzung für viele bioaktive Moleküle verwendet. [23, 24]. Es gibt nur begrenzte Studien zu PLA als Trägermaterial im Bereich Pestizide. PLA ist aufgrund seiner Umweltfreundlichkeit, geringen Kosten und einfachen Skalierung ein sehr vielversprechendes Beschichtungsmaterial zum Einkapseln von Pestiziden.
Nano-Abgabesysteme für Pestizide bieten auch vergrößerte Kontaktflächen zwischen den Zielschädlingen und Pestizidpartikeln [25, 26].
Avermectin (Av) ist ein hochwirksames, breites und sicheres Biopestizid, das eine Vielzahl von landwirtschaftlichen Schädlingen bekämpfen kann. Av wird aufgrund von Photooxidation leicht abgebaut. Av hat auch eine kurze Halbwertszeit in Wasser, was sich auf die Schädlingsbekämpfung bei Feldanwendungen auswirkt. Der Koeffizient der Adsorption von organischem Kohlenstoff für Av ist hoch. Dies bedeutet, dass Av nicht leicht in den Boden wandert, da es sich fest mit organischem Material verbindet, was seine Schädlingsbekämpfung im Boden beeinträchtigt. Viele Anstrengungen haben sich darauf konzentriert, die biologische Aktivität von Av durch Mikroverkapselungstechnologien zu schützen [27, 28]. Die Größe von Av-enthaltenden Mikrokapseln ist jedoch schwer zu kontrollieren. Sie sind im Allgemeinen groß, mit Größen von etwa 1–5 μm und haben eine breite Größenverteilung [29, 30]. Schlechte Verteilung und Gleichmäßigkeit sowie große Größen sind nicht förderlich, um die Adhäsion von Pestiziden auf der Blattoberfläche zu verbessern oder die Durchlässigkeit für schädliche Insekten zu erhöhen. Es wurden begrenzte Untersuchungen zur Synthese und biologischen Aktivität von Pestizid-Nanoabgabesystemen für Av mit unterschiedlichen Größen durchgeführt [31,32,33,34]. Der Bau von Nano-Abgabesystemen für Av durch Einkapselung von Nanomaterialien kann seine Photostabilität signifikant verbessern, seine Bodenadsorption oder andere nachteilige Faktoren reduzieren und die Kontrollwirkung des Pestizids verbessern. Darüber hinaus haben Av-Nanoabgabesysteme auch eine bessere Penetration und ermöglichen eine langsamere und kontrolliertere Freisetzung von Wirkstoffen auf Zielkulturen im Vergleich zu herkömmlichen Mikrokapseln.
Die vorliegende Studie zielte darauf ab, verschiedene Partikelgrößen von Av-Nanoabgabesystemen durch Emulsionspolymerisation unter Verwendung von PLA herzustellen und ihre Leistung als sicherer und biologisch abbaubarer Träger zu charakterisieren. Wir untersuchten den Einfluss der Partikelgröße auf die Freisetzungseigenschaften und die biologische Aktivität des Av-Nanoabgabesystems [35,36,37,38,39]. Die Konzentrationen des Wirkstoffs und seiner Vorläufer sowie die Eigenschaften des Emulsionssystems sind die Hauptfaktoren für die Bestimmung der Größenverteilung des endgültigen Av-Nano-Liefersystems. Das Av-Nanoabgabesystem zeigte eine gute Partikeldispersion mit kontrollierter Partikelgröße, hohe Av-Beladung, effektive Größenkontrolle und verzögerte Freisetzungseigenschaften sowie gute UV-Abschirmung und Stabilität.
Experimentell
Materialien
PLA und Av wurden von Nature Works bzw. Qilu Pharmaceutical Co., Ltd. (Innere Mongolei, VR China) bereitgestellt. Polyvinylalkohol (PVA), 87–90 % hydrolysiert mit einem durchschnittlichen Mw von 30.000–70.000, wurde von Sigma-Aldrich Shanghai Trading Co., Ltd. (Shanghai, Volksrepublik China) gekauft. Gelatine wurde von Sinopharm Chemical Reagent Co., Ltd. (Beijing, Volksrepublik China) bezogen. Die Dialysemembranen wurden von Beijing Tianan Technology Co., Ltd. (Volksrepublik China) bezogen. Andere chemische Reagenzien waren von analytischer Qualität und wurden von Beijing Chemical Works (Beijing, Volksrepublik China) bezogen. Das in allen Experimenten verwendete Wasser war von Milli-Q-Qualität (18,2 MΩ cm, TOC ≤ 4 ppb) und wurde von einem Milli-Q Advantage A10-System (Millipore, Milford, MA, USA) bezogen.
Vorbereitung des Avermectin-Nanoabgabesystems
Das Av-Nanoabgabesystem wurde über ein Öl-in-Wasser (O/W)-Emulsionsverfahren in Kombination mit einem Ultraschall- und Scher-physikalischen Emulgierungsverfahren hergestellt. Kurz gesagt wurden PLA und Av in Methylenchlorid als Ölphase gelöst. Für die Wasserphase wurde Gelatine bei 40 °C in Wasser gelöst, das dann mit wässriger PVA-Lösung gemischt wurde. Dann wurde die Ölphase langsam in ein großes Volumen der Wasserphase unter Hochscheremulgierung (FA25, FLUKO, Ruhrgebiet, Deutschland) getropft, um eine grobe Emulsion herzustellen. Die grobe Emulsion wurde dann durch Ultraschallemulgierung (JY 92-IIN, SCIENTZ, Ningbo, Volksrepublik China) gleichförmig dispergiert. Die einheitliche Emulsion wurde dann über Nacht unter magnetischem Rühren verfestigt (RW20, IKA, Staufen, Deutschland). Das gehärtete Av-Nanoabgabesystem wurde durch Zentrifugation gesammelt und dreimal mit entionisiertem Wasser gewaschen. Die Produkte wurden durch Zentrifugation gesammelt und dann gefriergetrocknet (FD-81, EYELA, Tokio, Japan), um ein frei fließendes Pulver zu ergeben. Das getrocknete Pulver wurde bis zur Verwendung bei 4 °C gelagert.
Charakterisierung von Nano-Transportsystemen
Die Morphologie jedes Av-Nanoabgabesystems wurde durch Rasterelektronenmikroskopie (REM, JSM-6700 F, JEOL Ltd., Akishima-shi, Japan) mit einer Beschleunigungsspannung von 5 kV untersucht. SEM-Proben wurden tropfenweise auf die Oberfläche einer Siliziumscheibe aufgebracht. Das Tröpfchen wurde bei Raumtemperatur trocknen gelassen und wurde dann mit einer dünnen Platinschicht unter Verwendung eines Sputtercoaters (EM ACE600, Leica, Wien, Österreich) beschichtet, um eine Aufladung während der REM-Beobachtung zu verhindern. Die Partikelgrößen in den Av-Nanoabgabesystemen wurden bei 25 °C durch Laserstreuung unter Verwendung eines Zetasizers (Zetasizer NanoZS90; Malvern, Worcestershire, UK) gemessen.
Bestimmung der Avermectin-Beladung in den Nanoabgabesystemen
Die Av-Menge im Nanoabgabesystem wurde bei einer Wellenlänge von 245 nm unter Verwendung eines Ultraviolett-Vis-(UV-Vis)-Spektrophotometers (TU901, Shimadzu Corporation, Kyoto, Japan) gemessen. Im Einzelnen wurden die Av-beladenen Proben ausgewogen und über Nacht in Chloroform gelöst, wonach die Lösung durch Vakuumdestillation getrocknet wurde. Dann wurde Methanol zugegeben, um das Av aus dem getrockneten Niederschlag zu lösen. Schließlich wurde die Mischung filtriert, um eine klare Lösung zu ergeben, die durch UV-Vis-Spektrophotometrie analysiert wurde.
Kontrollierte Freisetzung von Avermectin aus den Nanoabgabesystemen
Die Freisetzungsprofile von Av aus den Nanoabgabesystemen unterschiedlicher Größe wurden wie folgt untersucht. Av-Nanoproben jeder Größe wurden in 10 ml einer Ethanol/Wasser-Mischung (1:1, v .) suspendiert /v ). Die Suspension wurde dann in einen Dialysebeutel überführt, der in einem braunen Kolben mit 90 ml Ethanol/Wasser-Gemisch (1:1, v /v ) als Freisetzungsmedium. Der Kolben wurde in einem Inkubatorschüttler bei 300 U/min bei Raumtemperatur inkubiert. Nach definierten Zeitintervallen wurden 5,0 ml Lösung entfernt und durch 5,0 ml frisches Lösungsmittel ersetzt. Die Freisetzungsrate von Av aus der Nanoabgabeprobe wurde durch Messen der Konzentrationen von im Freisetzungsmedium gelöstem Av in unterschiedlichen Intervallen berechnet und wurde verwendet, um die Eigenschaft der verzögerten Freisetzung zu bewerten. Die Konzentration von Av wurde mit einem UV-Vis-Spektrophotometer bei einer Wellenlänge von 245 nm gemessen. Als Kontrollen wurde technisches Abamectin (TC, technischer Wirkstoff) verwendet.
Photolyseverhalten von Avermectin im Nanoabgabesystem
Das photolytische Verhalten von Av im Nano-Abgabesystem wurde mit dem kommerziellen Av-WDG als Kontrolle bewertet. Die Proben wurden in Methanol/Wasser (1:1, v /v ) und gleichmäßig in Kulturschalen aufgeteilt, und die resultierenden Proben wurden für eine gewünschte Dauer bei 25 °C unter einer UV-Lampe (500 W) bestrahlt, die eine maximale Intensität bei einer Wellenlänge von 365 nm aufwies. In festgelegten Zeitintervallen (12, 24, 36, 48, 60 und 72 h) wurde die Kulturschale aus dem Reaktor genommen und die Av-Konzentration der Proben analysiert.
Stabilitätstests
Die Stabilität des Av-Nano-Fördersystems wurde nach CIPAC MT 46 und GB/T 19136–2003 getestet. Die Proben wurden in Glasröhrchen verpackt und 7 Tage bei 0 ± 2 °C und 14 Tage bei 54 ± 2 °C gelagert. Veränderungen der Av-Menge im Nano-Abgabesystem wurden dann untersucht.
Bioassays
Bioassays des Av-Nano-Abgabesystems unterschiedlicher Größe wurden mit der Leaf-Dip-Methode durchgeführt. Die Proben wurden mit wässriger Triton X-100-Lösung bei verschiedenen Av-Konzentrationen verdünnt. Kohl (Brassica oleracea .) L.) Blätter wurden in die verdünnte Av-Suspension eingetaucht, dann bei Raumtemperatur getrocknet und auf einer Petrischale befestigt. Blattlauslarven wurden in jede Schale gegeben und die behandelten Blattläuse wurden in einem Brutschrank bei 25 °C und 75 % relativer Luftfeuchtigkeit kultiviert. Zum Vergleich mit dem Kontrolltest wurden vier Wiederholungen durchgeführt. Die Sterblichkeit wurde 48 h nach der Behandlung bestimmt. Konzentrations-Mortalitätsdaten wurden mit der Statistiksoftware DPS v12.01 analysiert. Die mittleren tödlichen Konzentrationen (LC50 ) und ihre 95 %-Konfidenzgrenzen wurden berechnet. Als Kontrolle wurde kommerzielles WDG verwendet.
Ergebnisse und Diskussion
Konstruktion und Charakterisierung des Avermectin-Nanoabgabesystems
Die Av-Nano-Liefersysteme wurden gemäß dem in Abb. 1 gezeigten Verfahren konstruiert. Während des Prozesses wurden die Wasser- und Ölphasen gemäß der oben genannten Methode hergestellt. Die Ölphase wurde in einer Wasserphase (Öl-in-Wasser-Emulsion) durch Emulgieren mit hoher Scherung emulgiert, um eine grobe Emulsion herzustellen. Die grobe Emulsion wurde dann durch Ultraschallemulgierung gleichförmig dispergiert. Es folgten Rühren, Verdampfen und Zentrifugieren der resultierenden Nanopartikel. Die Partikelgröße eines Abgabesystems ist einer der wichtigsten Faktoren, die die Freisetzungseigenschaften und die biologische Aktivität des Pestizids beeinflussen. Wie in Abb. 2 gezeigt, wurden Av-Nanoabgabesysteme mit Partikelgrößen im Bereich von 344 bis 827 nm durch Steuerung der Syntheseparameter konstruiert. Die Partikelgröße ist ein wichtiger Parameter für die kontrollierte Freisetzung von Pestiziden. Die Partikelgröße der Av-Nano-Abgabesysteme konnte durch Veränderung des Konzentrationsverhältnisses PVA/Gelatine gesteuert werden. Es wurden verschiedene Av-Nanoabgabesysteme mit Größen im Bereich von 344 bis 827 nm und Av-Gehalten im Bereich von 33,4 bis 57,5 % (33,4, 44,9, 45,2 und 57,5 %) hergestellt, wie in Abb. 3 gezeigt. Alle Av-Produkte waren glatt Oberflächen und sphärische Partikelmorphologien.
Schema, das die Vorbereitung des Av-Nanoabgabesystems zeigt
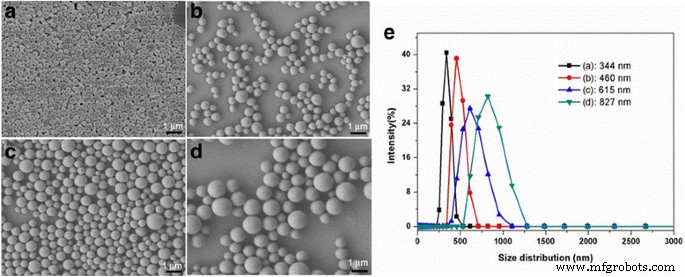
REM-Bilder (a –d ) und Größenverteilungen (e ) von Av-Nanofördersystemen mit unterschiedlichen Partikelgrößen
Av-Mengen in Av-Nanofördersystemen mit unterschiedlichen Partikelgrößen
Avermectin-Freisetzung aus dem Nano-Abgabesystem in vitro
In den letzten Jahren hat sich die Entwicklung von Pestizidfreisetzungssystemen in Richtung einer genauen und quantitativen Freisetzung im Gegensatz zu früheren langsamen und qualitativen Freisetzungssystemen entwickelt. Um eine kontrollierbare Freisetzung zu erreichen, wurden die Freisetzungsprofile der Av-Nano-Delivery-Systeme mit verschiedenen Partikelgrößen systematisch untersucht. Abbildung 4 zeigt die prozentuale Freisetzung von Av aus den Nanoabgabesystemen mit unterschiedlichen Partikelgrößen nach demselben Zeitintervall. Das technische Av hatte eine schnelle Freisetzungsrate und war nach 25 h fast vollständig freigesetzt. Die dauerhafte Gültigkeitsdauer von Pestiziden erfordert die anhaltende Freisetzung von Pestiziden, um die Wirksamkeit über einen langen Zeitraum aufrechtzuerhalten. Im Vergleich zur Burst-Freisetzung des technischen Abamectins setzten alle hergestellten Nano-Abgabesysteme Av mit relativ langsamen Geschwindigkeiten frei und hielten die anhaltende Freisetzung über längere Zeiträume aufrecht. Av-Freisetzungsprofile aus den Nanoabgabesystemen bestanden aus einer stoßartigen Freisetzung, gefolgt von einer allmählichen Freisetzung über den 240-Stunden-Zeitrahmen des Experiments. Da die Größe des Abgabesystems von 827 auf 344 nm abnahm, stieg die kumulative Freisetzung nach 240 h von 53,2 auf 79,4 %. Die Ergebnisse zeigten, dass die Av-Freisetzungsrate aus dem Nano-Abgabesystem mit abnehmender Partikelgröße allmählich zunahm. Dies war darauf zurückzuführen, dass eine größere Oberfläche der Umgebung ausgesetzt war, was die Permeation und das Austreten von Pestiziden in den Schalen des Nano-Liefersystems begünstigte. Die Ergebnisse zeigten, dass die Av-Freisetzungsrate aus dem Nano-Abgabesystem durch Modifizieren der Partikelgröße effektiv gesteuert werden konnte.
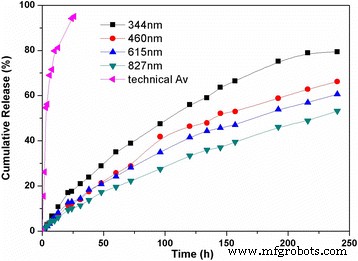
Freisetzungsverhalten von Av-Nanoabgabesystemen mit unterschiedlichen Partikelgrößen in Ethanol/Wasser (50:50, v /v ) über 200 Stunden
Biologische Aktivität
Die biologische Aktivität von Av, das aus Nano-Abgabesystemen unterschiedlicher Partikelgrößen freigesetzt wird, gegen Blattläuse ist in Abb. 5 dargestellt. Der LC50 des Av-Nanoabgabesystems nahm mit abnehmender Partikelgröße allmählich ab. Die Bioverfügbarkeit von Nanoemulsionen ist aufgrund ihrer kleineren Partikelgröße und des höheren Oberfläche-zu-Volumen-Verhältnisses angeblich höher als die von herkömmlichen Emulsionen. Daher wurden die höheren biologischen Aktivitäten von Av-Nanoabgabesystemen mit kleineren Partikelgrößen der erhöhten Dispergierbarkeit, Benetzbarkeit und Retention aufgrund von Effekten im kleinen Maßstab zugeschrieben. Alle Av-Nano-Liefersysteme hatten einen niedrigeren LC50 Werte und höhere Aktivitäten als kommerzielle Av WDG. Die hohe Wirksamkeit war auf die Nanopartikel zurückzuführen, die die Haftung und das Eindringen des Av-Pestizids auf der Oberfläche der Pflanzen verbesserten, wodurch der Verlust von Pestiziden durch Auslaufen während des Spritzens verringert wird.
Bioassay-Ergebnisse von Av-Nano-Abgabesystemen mit unterschiedlichen Partikelgrößen
UV-abschirmende Eigenschaften von Avermectin im Nano-Abgabesystem
Um die UV-abschirmenden Eigenschaften von Av im Nano-Abgabesystem zu verifizieren, wurde die photolytische Rate von Av durch künstliche Bestrahlung geschätzt. Die Analyse der Photolyserate von Av mit der Bestrahlungszeit ist in Abb. 6 dargestellt. Der photolytische Prozentsatz von Abamectin betrug 18,7 % für das Nanoabgabesystem und 46,7 % für das kommerzielle Av-WDG nach 48 h. Nach 72 h betrug der photolytische Prozentsatz von Abamectin 25,6 % für das Nanoabgabesystem und 51,5 % für das kommerzielle Av WDG. Diese Ergebnisse zeigten, dass das Nano-Abgabesystem aufgrund der schützenden Wirkung des Wandträgers eine gehemmte Photolyse von Av aufwies.
Vergleich des prozentualen Anteils der Av-Photolyse mit dem kommerziellen WDG- und Nanoabgabesystem unter UV-Bestrahlung
Speicherstabilität
Die Stabilitäten der Av-Nanoabgabesysteme mit unterschiedlichen Partikelgrößen wurden durch Messung ihres Beladungsgehalts bei Temperaturen von 0, 25 und 54 °C bewertet. Abbildung 7 zeigt, dass das Nano-Liefersystem während der Lagerung bei Raumtemperatur und niedriger Temperatur ohne größere Änderungen der Av-Beladung stabil blieb. Ein kleiner Av-Verlust wurde nach 14 Tagen bei 54 °C aufgrund des Abbaus von Av bei hoher Temperatur beobachtet. Diese Ergebnisse zeigten, dass das Av-Nano-Liefersystem eine gute Lagerstabilität aufwies.
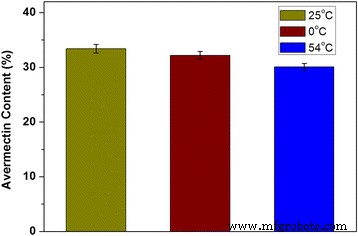
Stabilität des Av-Nano-Liefersystems bei verschiedenen Lagertemperaturen
Schlussfolgerungen
Um die kontrollierte Freisetzung, chemische Stabilität und Bioaktivität von Av zu verbessern, wurde ein Av-Nanoabgabesystem mit unterschiedlichen durchschnittlichen Partikelgrößen unter Verwendung der Emulsionspolymerisationsmethode synthetisiert. Das Av-Nano-Abgabesystem zeigte ein konsistentes Freisetzungsverhalten. Die Av-Freisetzungsrate aus dem Nano-Abgabesystem nahm aufgrund der größeren Oberfläche mit abnehmender Partikelgröße allmählich zu. Die biologische Aktivität des Av-Nano-Abgabesystems nahm aufgrund der verbesserten Haftung und Penetration mit abnehmender Partikelgröße allmählich zu. Das Av-Nano-Abgabesystem zeigte gute Anti-Photolyse-Eigenschaften und Stabilität. Das Abgabesystem überwindet die Unzulänglichkeiten gegenwärtiger Biopestizide, wie beispielsweise ihre Umweltempfindlichkeit, unerwünschte Bodenadsorption und kurze Aktivitätsdauer. Dadurch wird die Wirksamkeit von Pestiziden verbessert und die erforderliche Sprühhäufigkeit verringert.
Nanomaterialien
- Können ERP- und MES-Systeme mit dem IIoT Schritt halten?
- Experimentelle Forschung zur Stabilität und natürlichen Konvektion von TiO2-Wasser-Nanofluid in Gehäusen mit unterschiedlichen Rotationswinkeln
- Einfache Synthese von Silbernanodrähten mit unterschiedlichen Aspektverhältnissen und Verwendung als flexible, transparente Hochleistungselektroden
- Einfache Herstellung von multihierarchischem porösem Polyanilin-Komposit als Drucksensor und Gassensor mit einstellbarer Empfindlichkeit
- Herstellung, Charakterisierung und Zytotoxizität von kugelförmigen, konjugierten Gold-Cockle-Shell-abgeleiteten Calciumcarbonat-Nanopartikeln für biomedizinische Anwendungen
- Herstellung und Charakterisierung von ZnO-Nano-Clips durch das Polyol-vermittelte Verfahren
- Theranostische Wirkstoffe der nächsten Generation basierend auf mit Halbleiter-Nanokristallen kodierten Polyelektrolyt-Mikrokapseln:Entwicklung und funktionelle Charakterisierung
- Einfluss von in einer TiO2-Kompaktschicht eingebetteten Ag-Nanopartikeln unterschiedlicher Größe und Konzentration auf die Konversionseffizienz von Perowskit-Solarzellen
- Synthese und Charakterisierung von hierarchischen ZSM-5-Zeolithen mit hervorragender Mesoporosität und ausgezeichneten katalytischen Eigenschaften
- Kopplung von KI und Robotik mit mehreren Inspektionssystemen



