Herstellung und Charakterisierung von Taurin-funktionalisiertem Graphenoxid mit 5-Fluorouracil als Wirkstoffabgabesysteme gegen Krebs
Zusammenfassung
In letzter Zeit haben sich Nanocarrier-Systeme für Krebsmedikamente, insbesondere GO-basierte Drug-Delivery-Systeme, zu einem Segen für Krebspatienten entwickelt. In dieser Studie haben wir Tau gewählt, um die GO-Oberfläche zu funktionalisieren, um ihre Biokompatibilität zu verbessern. Zunächst wurde nanoskaliges GO durch das modifizierte Hummer-Verfahren und das Ultraschall-Stripping-Verfahren synthetisiert. Der Taurin-modifizierte Graphenoxid-Träger (Tau-GO) wurde durch eine chemische Methode synthetisiert, um Tau-GO zu erhalten, das eine gute Dispergierbarkeit und Stabilität in Wasser mit einem Zetapotential von − 38,8 mV und einer Partikelgröße von 242 nm aufweist. Basierend auf den Bewertungskriterien der Einkapselungseffizienz wurde die optimale Formulierung bestimmt, um Tau-GO und 5-FU durch nicht-kovalente Bindung zu kombinieren. Das 5-FU-Tau-GO war in neutraler Umgebung stabiler als in saurer Umgebung und mit einer bestimmten pH-Antwort und einem verzögerten Freisetzungseffekt. In vivo verglichen wir die orale und intravenöse Verabreichung von 5-FU bzw. 5-FU-Tau-GO unter Verwendung von pharmakokinetischen Tests und verwandten Parametern und zeigten, dass die orale oder intravenöse Verabreichung von 5-FU-Tau-GO die Wirkzeit von 5 . verlängert -FU im Körper und verbessert seine Bioverfügbarkeit. Darüber hinaus zeigte die durch den MTT-Test gemessene Hemmung von HepG2-Zellen, dass der IC50 Wert von 5-FU betrug 196 ± 8,73 μg/ml und der IC50 Der Wert von 5-FU-Tau-GO betrug 65,2 ± 0,7 μg/ml, was darauf hindeutet, dass 5-FU-Tau-GO stärker gegen HepG2-Zellen ist und eine stärkere hemmende Wirkung auf Krebszellen hat. Der mit der AO/EB-Färbung gemessene Effekt auf die Zellmorphologie zeigte auch, dass 5-FU-Tau-GO nicht nur Zellen zerstörte, sondern im Vergleich zu 5-FU auch signifikant Apoptose induzierte. Wir haben auch durch computergestütztes Design verifiziert, dass Tau-GO besser an 5-FU als an das unmodifizierte GO binden kann und dass das gebildete 5-FU-Tau-GO-System stabiler ist und der Übertragung und Freisetzung von 5- förderlich ist. FU in vivo.
Einführung
Die Chemotherapie ist nach wie vor eine gängige Methode, die bei der Behandlung verschiedener Krebsarten eingesetzt wird [1]. Ein wesentliches Hindernis der meisten Chemotherapeutika ist ihre Unfähigkeit, in wirksamen Konzentrationen in Tumorgewebe einzudringen, oder ihre unerwünschten Nebenwirkungen auf normales Gewebe [2]. Daher haben die Wissenschaftler ihre Bemühungen auf die Entwicklung eines wirksamen Wirkstoffabgabesystems konzentriert, das eine kontrollierte Wirkstofffreisetzungsrate in Tumorgewebe erreichen kann, um eine wirksame Wirkstoffabgabe und Therapie sicherzustellen.
Viele nanoskalige Materialien, darunter Liposomen [3], Polymere [4], Nanopartikel [5], Dendrimere [6], Mizellen [7] und Graphenoxid [8, 9], wurden für den Transport verschiedener Medikamente entwickelt. Unter diesen Nanomaterialien ist Graphenoxid (GO) ein neuartiges Kohlenstoff-Nanomaterial, das chemisch aus oxidiertem Graphit abgeblättert wird und mehrere faszinierende physikalische und chemische Eigenschaften aufweist, wie z Fähigkeit in Wasser [10,11,12]. Darüber hinaus zeigten die meisten in vitro-Versuchsergebnisse, dass eine niedrige GO-Konzentration als Substrat für das Zellwachstum und zur Aktivierung von Immunzellen verwendet werden könnte. Daher wird GO häufig in der Krankheitsdiagnose [13], der Bildgebung und Verfolgung von Krebszellen [14], der photothermischen Krebstherapie [15], der Gewebezüchtung [16], der gezielten Wirkstoffabgabe [17] und insbesondere als Anti- Tumormedikamententräger [18, 19]. Mehrere Forschungsgruppen haben jedoch berichtet, dass eine hohe GO-Konzentration in präklinischen und klinischen Studien offensichtliche zytotoxische Wirkungen hat. Der Mechanismus, durch den GO in vivo toxische Wirkungen hervorruft, ist durch oxidativen Stress und die Überproduktion von intrazellulären reaktiven Sauerstoffspezies, die Zellapoptose induzieren und schwere Entzündungen, Lungenödeme und Granulombildung verursachen [20]. Daher ist es von entscheidender Bedeutung, das Problem der GO-Toxizität zu lösen.
Berichten zufolge kann die Funktionalisierung kovalenter oder nicht-kovalenter Bindungen die starke hydrophobe Wechselwirkung zwischen GO und Zellen reduzieren. Dies wurde durch mehrere Studien gezeigt, die zeigten, dass die GO-Funktionalisierung seine Biokompatibilität verbessert und seine Toxizität in vivo und in vitro fast eliminiert.Yang et al. untersuchten zum ersten Mal die langfristige Bioverteilung von kovalent konjugiertem PEG-GO in Mäusen unter Verwendung einer radioaktiven Markierungsmethode, und die Ergebnisse zeigten, dass PEG-GO nach und nach von Mäusen ausgeschieden werden konnte, wahrscheinlich über Urin und Kot [21]. Zhanget al. verglichen DEX-funktionalisiertes GO mit GO und fanden heraus, dass GO-DEX die Zelltoxizität bemerkenswert reduzieren und größtenteils innerhalb einer Woche aus Mäusen eliminiert werden konnte [22]. Darüber hinaus führt die nicht-kovalente Bindung von GO an Pluronic F127 zu einer gutartigen Löslichkeit und Stabilität unter physiologischen Bedingungen und einer geringen Toxizität [23]. Obwohl mehrere Polymere oder Moleküle verwendet wurden, um GO zu funktionalisieren, wurden auf diesem Gebiet bedeutende Ergebnisse erzielt. Es sind jedoch noch Anstrengungen erforderlich, um einfache Methoden zur Konstruktion eines guten biokompatiblen GO-basierten Arzneimittelträgers zu entwickeln.
Taurin (Tau) ist eine semi-essentielle Aminosäure mit guter Stabilität und Wasserlöslichkeit. Tau kann kardiovaskulären und zerebrovaskulären Erkrankungen vorbeugen, die Sehfunktion aufrechterhalten, Zellen schützen und die Immunität regulieren. Zahlreiche Studien haben vorgeschlagen, dass Tau durch seine Hoch- oder Herunterregulierung der Expressionsfaktoren, die bei verschiedenen Krebsarten, einschließlich Lungen-, Magen-, Darm- und Brustkrebs, eine wichtige Rolle spielen, Antitumoreigenschaften besitzt [24]. Somit könnte Tau-funktionalisiertes GO eine überlegene Rolle als Träger von Antitumor-Medikamenten spielen. In diesem Artikel haben wir zum ersten Mal kovalentes Tau-funktionalisiertes GO als Nanoträger verwendet und seine Zytotoxizität in vitro untersucht. Darüber hinaus wurde 5-Fluorouracil (5-FU) als Antikrebswirkstoff verwendet, der nicht kovalent auf die Oberfläche von Tau-GO geladen wurde, um ein Wirkstoffabgabesystem aufzubauen. Das 5-FU-Tau-GO könnte nicht nur die Nebenwirkungen auf normales Gewebe reduzieren, sondern auch die Bioverfügbarkeit des Arzneimittels verbessern. Folglich wurde Tau-GO erfolgreich als neuartiges GO-basiertes Nanomaterial entwickelt, das in Zukunft bedeutende biomedizinische Anwendungen haben könnte.
Experimente und Methoden
Materialien
Das Graphitpulver, phosphatgepufferte Kochsalzlösung (PBS) und Dimethylsulfoxid (DMSO) wurden von Tianjin Laibo Chemical Co., Ltd. bezogen; Carbodiimid (EDC), N-Hydroxysuccinimid (NHS), Salzsäure (HCl) und Wasserstoffperoxid (H2 .) O2 30%) wurden von Shandong Yuwang Industrial Co., Ltd. gekauft; Taurin (Tau), 5-Fluorouracil (5-FU), menschliche Hepatomzellen (HepG2), Penicillin-Streptomycin-Lösung und fötales Rinderserum (FBS) wurden von Dalian Meilun Biotechnology Co., Ltd. bezogen; Schwefelsäure (H2 SO4 98%) und Kaliumpermanganat (KMnO4 .) ) wurden von Nanjing Chemical Reagent Co., Ltd. bezogen; Natriumnitrat (NaNO3 ) und Natriumdodecylsulfat (SDS-Na) wurden von Shanghai Jinjinle Industrial Co., Ltd. bezogen; MTT wurde von Sigma-Aldrich, Inc. gekauft; DMEM wurde von HyClone, Inc. gekauft; Die Ratten wurden vom Benxi Changsheng Experimental Animal Center gekauft. Alle anderen Reagenzien und Chemikalien waren analytisch rein und im Handel erhältlich.
GO Synthese
Das GO wurde nach einem modifizierten Hummer-Verfahren aus Graphitpulver hergestellt. Zunächst wurden 168 ml 98%ige Schwefelsäure entlang der Kolbenwand eines Dreihalskolbens zugegeben, der in ein Eisbad mit Thermometer gestellt wurde, und 5 g Graphit und 4 g Natriumnitrat wurden hinzugefügt, als die Temperatur 5 °C erreichte. Dann wurden 22,5 g Kaliumpermanganat langsam portionsweise für 1 h zugegeben und die Temperatur wurde unter 5 °C gehalten. Danach wurde der Dreihalskolben in ein Ölbad überführt und die erhaltene Mischung 30 min bei 35 °C umgesetzt, dann wurde die Temperatur auf 65 °C erhöht und die Reaktion 30 min gerührt. Nach diesem Schritt wurde die Temperatur auf 85 °C erhöht und die Mischung wurde 1 h weiter umgesetzt, um eine violett-braune Paste zu erhalten. Diese Mischung wurde 1 Woche im Raum stehen gelassen, mit 700 ml heißem Wasser in ein Becherglas überführt und das 30%ige Wasserstoffperoxid wurde tropfenweise zugegeben, bis es gelblichbraun wurde. Die Mischung wurde bei 10.000 U/min zentrifugiert, mit heißem Wasser gewaschen und dieser Vorgang wurde mehrmals wiederholt, bis der pH-Wert des Überstands 7,0 betrug. Schließlich wurde das Produkt in einem Vakuumgefriertrockner getrocknet und das nano GO wurde erhalten.
Tau-GO-Synthese
Ein genau abgewogenes 50 mg GO wurde in 50 ml destilliertem Wasser gelöst und 150 mg EDC und 100 mg NHS wurden hinzugefügt, um das GO durch Ultraschall in einem Eiswasserbad für 20 Minuten zu aktivieren. Als nächstes wurde 10 ml wässrige Tau-Lösung (0,1 g/ml) langsam (tropfenweise) in die vorbereitete wässrige GO-Lösung gegeben, und der pH-Wert wurde mit HCl auf 6–7 eingestellt und 24 h im Dunkeln im Raum kontinuierlich gerührt. Das Produkt wurde durch Zentrifugation bei 5000 U/min für 10 Minuten gesammelt und dreimal mit destilliertem Wasser gewaschen. Das Tau-GO wurde nach der Gefriertrocknung gesammelt.
5-FU Laden
Eine Menge von 20 ml Tau-GO-Lösung wurde 2 h lang mit Ultraschall behandelt. Eine genau abgewogene Menge 5-FU wurde in einer geeigneten Menge destilliertem Wasser gelöst und unter Rühren bei Raumtemperatur langsam zu der zubereiteten Tau-GO-Lösung getropft und dann 1,5 h im Dunkeln bei 30 °C beschallt. Die Produkte wurden bei 5000 U/min für 10 Minuten bei 4 °C zentrifugiert. Das untere Sediment wurde mit 20 ml destilliertem Wasser gewaschen und zentrifugiert (5000 U/min für 10 Minuten bei 4 °C) und der Vorgang wurde dreimal wiederholt. Die untere Schicht wurde gefriergetrocknet, der Überstand wurde in ein Becherglas gegeben, das Volumen gewogen, die Konzentration von 5-FU wurde durch 1200 HPLC (Agilent, USA) bestimmt. Die Nachweisbedingungen waren wie folgt:Chromatographiesäule:C18 (4,6 × 250 nm, 5 μm); Säulentemperatur:25 °C; mobile Phase:0,1 % KH2 PO4 Lösung mit pH 5,5; Flussrate:1,0 ml/min; Injektionsvolumen:20μL; und Messwellenlänge:265 nm. Das Verkapselungsverhältnis (EE) und die Wirkstoffbeladungseffizienz (LE) wurden durch die folgende Formel erhalten:
$$\begin{ausgerichtet} {\text{EE}}\left(\%\right) &=\frac{{M_{1} - C_{1} \times L_{1} }}{{M_{1 } }} \times 100\% \\ {\text{LE}}\left( \% \right) &=\frac{{M_{1} - C_{1} \times L_{1} }}{{ 20C_{0} + M_{1} - C_{1} \mal L_{1} }} \mal 100\% \\ \end{aligned}$$Die Gesamtdosis von 5-FU wurde als M1 . aufgezeichnet , die Konzentration und das Volumen von freiem 5-FU wurden als C1 . aufgezeichnet und L1 , und die Trägerkonzentration wurde als C0 . aufgezeichnet .
Charakterisierung
Um das hergestellte Nanokomposit zu charakterisieren, wurden Fourier-Transformations-Infrarotspektren (FT-IR) von 4000 bis 400 cm −1 . gescannt auf dem IRAaffinity-1-Spektrometer (Shimadzu, Japan), um die Wechselwirkungen zu bestätigen. UV-Vis-Absorptionsspektren wurden auf einem UV-3600 Scanning Spectrophotometer (Shimadzu, Japan) aufgezeichnet. Die Proben wurden in destilliertem Wasser gelöst und die Partikelgrößen, Zetapotentiale und PDI-Werte wurden auf einem Nano-ZS 90 Nano Instrument (Malvern, UK) erhalten. Die Morphologien der Proben wurden unter Verwendung eines JEM-2100-Transmissionselektronenmikroskops (TEM) (JEOL, Japan) analysiert. Thermogravimetrische Analysen (TGA) wurden mit einem thermogravimetrischen Analysator (NETZSCH, Deutschland) bei einer Heizrate von 10 °C/min von 0 auf 800 °C unter Stickstoffatmosphäre durchgeführt. Die XRD-Messung von Proben wurde mit einem Röntgendiffraktometer (Bruker, Deutschland) mit einer Kupfer-CuKα-Strahlung (λ = 1,5406 Å) in einem Weitwinkel mit 2θ-Winkel. XPS-Messungen wurden unter Verwendung einer Omicron ESCA-Sonde mit einer monochromatischen Al Karadiation (Thermo, Amerika) durchgeführt.
In-vitro-Wirkstofffreisetzung
Die In-vitro-Wirkstofffreisetzung erfolgte bei pH 1,2 (simulierte Magenumgebung), pH 6,5 (simulierte Leberkrebszellumgebung) bzw. pH 7,4 (simulierte physiologische Umgebung) bei 37 °C (simulierte Körpertemperatur). Kurz gesagt, 15 mg 5-FU-Tau-GO wurden in eine Dialysemembran gegeben, eingetaucht in 50 ml Pufferlösungen, die 0,1% SDS-Na mit einem pH-Wert von 1,2, 6,5 und 7,4 enthielten. Alle Proben wurden in ein kontinuierliches Schüttelwasserbad mit einer Geschwindigkeit von 100 U/min und einer Temperatur von 37 ° C gegeben. Zu vorgegebenen Zeitpunkten (0 min, 5 min, 10 min, 20 min, 30 min, 1 h, 1,5 h, 2 h, 2,5 h, 3 h, 4 h, 8 h, 12 h, 24 h, 48 h und 72 h) wurde 1 ml jeder Probe entnommen und durch 1 ml frische Pufferlösung mit 0,1% SDS-Na ersetzt, um das gleiche Volumen des Freisetzungsmediums beizubehalten. Das freigesetzte Medium wurde zentrifugiert und mit 1200 HPLC analysiert.
In-vitro-Zytotoxizitätsstudien
MTT-Assay
Der MTT-Assay wurde verwendet, um die Zytotoxizität von 5-FU, Tau-GO und 5-FU-Tau-GO zu bewerten. Kurz gesagt, die menschlichen Hepatom-HepG2-Zellen wurden in DEME-Medium, ergänzt mit 10 % FBS und 1 % Antibiotika (Penicillin-Streptomycin-Lösung) bei 37 °C in einer befeuchteten Atmosphäre von 5 % CO2 . kultiviert . Die Zellen wurden in einer 96-Well-Platte mit einer Dichte von 5 × 10 3 . ausgesät Zellen pro Vertiefung mit 100 μl DEME-Medium, ergänzt mit FBS und Antibiotika. Die Platte wurde für 24 Stunden in eine befeuchtete 37 °C-Kammer mit 5 % CO2 . gestellt . Danach wurde das Wachstumsmedium entfernt und mit 100 μL frischem Medium aufgefüllt, das verschiedene Konzentrationen (5, 10, 20, 40, 60, 80 und 100 μg/ml) von 5-FU, Tau-GO, 5-FU- enthielt. Tau-GO bzw. Nach einer 24 h Inkubation wurden die Zellen mit 20 μL MTT-Lösung behandelt und weitere 4 h inkubiert. Als nächstes wurde das Medium abgesaugt und die Formazankristalle in 150 μl DMSO gelöst. Schließlich wurden die Well-Platten bei 37 °C für 15 min in einem Oszillator mit konstanter Temperatur geschüttelt. Die optische Dichte (OD) jeder Probe wurde bei 570 nm unter Verwendung eines Mikroplattenlesegeräts gemessen. Die Versuche wurden in dreifacher Ausführung durchgeführt. Die Zellhemmungsrate wurde aus den Ergebnissen mit der folgenden Formel berechnet:
$${\text{Zelle}}\;{\text{Hemmung}}\;{\text{Rate}} =\frac{{{\text{OD}}_{{{\text{control}}} } - {\text{OD}}_{{{\text{behandelt}}}} }}{{{\text{OD}}_{{{\text{control}}}} }} \mal 100\ %$$wobei ODKontrolle ist die von unbehandelten Kontrollzellen erhaltene Extinktion, ODbehandelt ist die Absorption, die von behandelten Zellen erhalten wird.
AO/EB-Färbeassay
AO/EB-Doppelfärbung wurde verwendet, um die morphologischen Veränderungen der Zellen zu bewerten, die mit 5-FU, Tau-GO und 5-FU-Tau-GO behandelt wurden. Kurz gesagt, HepG2-Zellen in einer logarithmischen Wachstumsphase wurden in einer 6-Well-Platte mit einer Dichte von 10.000 Zellen pro Well ausgesät und in einem Inkubator bei 37 °C und unter 5 % CO2 . kultiviert Atmosphäre. Nach 24 h wurden die Zellen mit einer festen Konzentration von 5-FU, Tau-GO oder 5-FU-Tau-GO behandelt und weitere 24 h inkubiert. Das Medium in jeder Vertiefung wurde entfernt und die Zellen wurden zweimal mit PBS gewaschen. Als nächstes wurde 1 ml PBS, ergänzt mit 40 μL Fluoreszenzfarbstoffen (1 mg/ml AO und 1 mg/ml EB wurden im Verhältnis 1:1 gemischt) in jede Vertiefung gegeben und 10 Minuten ohne Licht inkubiert. Die gefärbten Zellen wurden unter einem Fluoreszenzmikroskop beobachtet und Bilder wurden zufällig aufgenommen.
Pharmakokinetische Studie
Alle Tierversuche wurden in Übereinstimmung mit den Richtlinien und Grundsätzen der Tierschutz- und Ethikkommission durchgeführt. Insgesamt 24 männliche SD-Ratten mit einem Körpergewicht von 230–270 g wurden 12 h lang gefastet und vor der Arzneimittelverabreichung nach dem Zufallsprinzip in 4 Gruppen eingeteilt. Den Gruppen A und B wurden 5-FU- und 5-FU-Tau-GO-Lösungen intravenös injiziert, und den Gruppen C und D wurden orale 5-FU- bzw. 5-FU-Tau-GO-Lösungen verabreicht. Alle Gruppen erhielten eine Dosis von 20 mg/kg. Nach der Arzneimittelverabreichung wurden Blutproben (ca. 0,5 ml) zu bestimmten Zeitpunkten (15 min, 1 h, 2 h, 4 h, 6 h, 8 h, 12 h, 16 h, 24 h und 48 ) in Antikoagulationsröhrchen gesammelt h). Die Plasmaproben wurden durch Zentrifugation bei 7500 U/min und bei 4 °C für 10 Minuten getrennt. Dann 200 μl Plasma und 50 mg (NH4 .) )2 SO4 wurden in einem Röhrchen (10 μl 40 μg/ml 5-BrU-interner Standardlösung) kombiniert, mit Stickstoff in einem Wasserbad bei 40 °C luftgetrocknet, 5 min gevortext und 3 min bei 10800 U/min zentrifugiert. Als nächstes wurde das Röhrchen mit 900 μl Ethylacetat/Isopropanol-Lösung (85:15, v/v) versetzt, 3 min gevortext und 15 min bei 10800 rpm zentrifugiert. Der Überstand wurde entfernt und mit Stickstoff getrocknet, 100 μl mobile Phase wurden zugegeben und die Das Röhrchen wurde 1 Minute lang gevortext. Schließlich wurde die resultierende Lösung, die aus dem Überstand gesammelt wurde, durch 1200 HPLC gemessen.
Molekulardynamiksimulation
Die Molekulardynamiksimulation wird hauptsächlich verwendet, um die Wechselwirkungskraft zwischen dem Wirkstoff und dem Träger und das Diffusionsverhalten des Wirkstoffs zu analysieren. Die chemische Struktur des 5-FU wurde mit Chemdraw des Chem Office 2014 konstruiert, und die Strukturen von Tau-GO und GO wurden im Polymer and Molecule Builders-Modul unter Verwendung der molekularen Simulationssoftware Materials Studio (Version 7.0, Accelrys Inc. , VEREINIGTE STAATEN VON AMERIKA). Alle aufgebauten Verbindungen wurden unter dem Kraftfeld COMPASS II geometrisch optimiert, und die Konformation mit der niedrigsten Energie wurde als stabile Konformation ausgewählt. Für jedes System wurde eine 10 ps-NVT-Äquilibrierung durchgeführt. Die Simulation wurde mit 100 ps MD durchgeführt, um eine ausgewogene Struktur bei 298 K und 101,325 kPa mit einer Schrittweite von 1 fs zu erhalten. Schließlich wurden die mittlere quadratische Verschiebung (MSD) und die kohäsive Energiedichte (CED) für jedes System ermittelt, und der Diffusionskoeffizient (D) wurde durch die folgende Formel angegeben:
$$D =\frac{1}{2d}\mathop {\lim}\limits_{\tau\to\infty} \frac{{\text{d}}}{{{\text{d}}\tau }}\links Links. {r\overrightarrow {\left( t\right)} - r\overrightarrow {\left( 0 \right)} } \right]} \right.^{2}$$wo die d ist die Dimension des Systems, \(r\overrightarrow {\left( t\right)}\) und \(r\overrightarrow {\left( 0 \right)}\) sind der Ortsvektor des Wirkstoffmoleküls zum Zeitpunkt t bzw. 0, \(\left[ {\left. {r\overrightarrow {\left(t\right)} - r\overrightarrow {\left( 0\right)} } \right]} \right.^{ 2}\) steht für MSD.
Ergebnisse und Diskussion
Charakterisierung
Das Tau-GO-Konjugat wurde durch eine Amidbindung von GO und Tau hergestellt. Die erfolgreiche Synthese des Nanokomposits wurde durch FT-IR-Spektren validiert (Abb. 1). Das Vorhandensein der Sauerstofffunktionalitäten auf GO wurde durch die Absorptionspeaks bei –OH (~ 3405 cm −1 ), C=O (1723 cm −1 ), C=C (1628 cm −1 ) und C–OH (1391 cm −1 .) ). Diese Ergebnisse belegen die erfolgreiche Vorbereitung von GO (Abb. 1a) [25]. Zusätzlich zu einigen charakteristischen GO-Peaks sind die neuen Peaks bei 1638 cm −1 und 3427 cm −1 entsprach der Amidgruppe und der 1164 cm −1 und 1085 cm −1 entsprach –SO. Das Tau-GO-Spektrum zeigte deutlich, dass Tau auf der GO-Oberfläche funktionalisiert wurde (Abb. 1b). In Abb. 2b der charakteristische Peak von –SO3 bei 1164 cm −1 wurde durch die Wirkung von Wasserstoffbrücken überschwemmt und war in den FT-IR-Spektren nicht sichtbar. Daher wurde 5-FU erfolgreich auf den Tau-GO geladen.
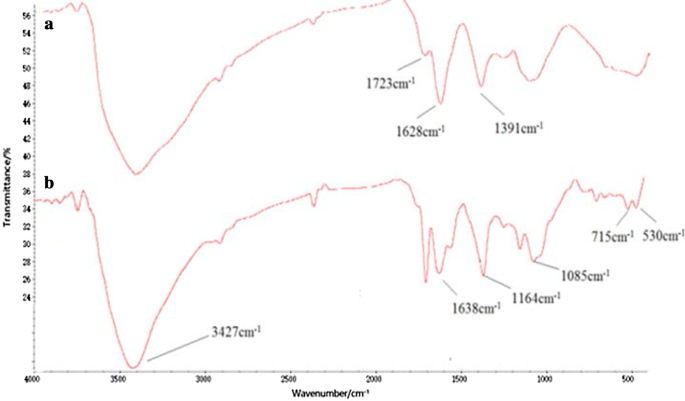
FT-IR-Spektren von GO (a ) und Tau-GO (b )
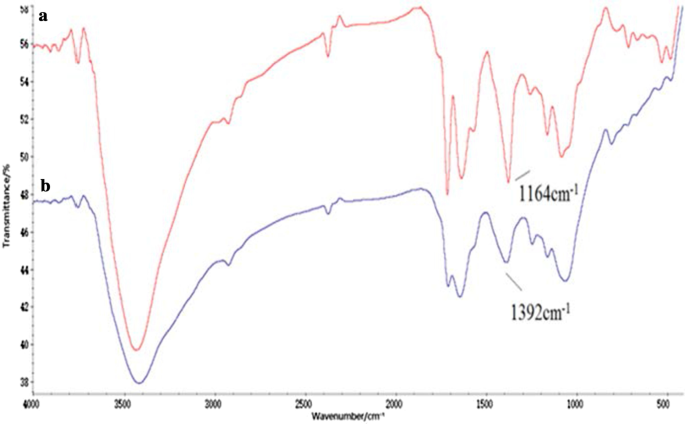
FT-IR-Spektren von Tau-GO (a ) und 5-FU-Tau-GO (b )
Die GO-UV-Vis-Absorptionsspektren sind in Abb. 3 dargestellt. Der offensichtliche Absorptionspeak bei 234 nm wurde dem π-π*-Übergang der Graphen-C=C-Bindungen zugeschrieben. Darüber hinaus wurde der 300 nm große Schulterpeak dem n-π*-Übergang der Graphenoxid-C=O-Bindungen an der Carboxyl- oder Carbonylgruppe zugeschrieben. Die beiden charakteristischen Absorptionspeaks haben sich als erfolgreiche Präparate von GO erwiesen.
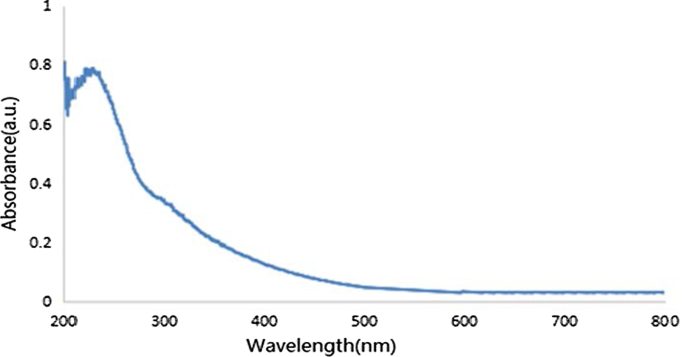
UV-Spektren von GO
Die Größe von GO, Tau-GO und 5-FU-Tau-GO ist in Abb. 4 gezeigt. Das Zetapotenzial von GO, Tau-GO und 5-FU-Tau-GO ist in Abb. 5 gezeigt. Die Größe von die GO-Blätter betrugen ungefähr 221 nm und der PDI-Wert betrug ungefähr 0,188, was darauf hindeutet, dass das hergestellte GO eine gleichmäßige Verteilung und gute Stabilität aufweist. Das Zetapotential betrug ungefähr − 33,3 mV, was darauf hindeutet, dass die negative Ladung hauptsächlich auf das Vorhandensein vieler sauerstoffhaltiger Gruppen auf der Oberfläche zurückzuführen ist. Wenn das GO mit Tau über eine Amidbindung modifiziert wurde, ersetzten die Aminogruppen einige der Carboxylgruppen und das –SO3 hatte in Lösung eine stärkere Ionisationsfähigkeit, das Zetapotential nahm ab und wurde − 38,8 mV. Die Größe und der PDI-Wert von Tau-GO betrugen ungefähr 242 nm und 0,190. Als nächstes wurde 5-FU durch eine nicht-kovalente Bindung auf Tau-GO geladen. Das Zetapotential betrug ungefähr − 26,7 mV und der Absolutwert war größer als 20 mV. Darüber hinaus lagen die Größe und die PDI-Werte von 5-FU-Tau-GO bei ungefähr 264 nm und 0,182, was darauf hindeutet, dass die elektrostatische Abstoßung zwischen den Partikeln groß ist, was keine Aggregation oder Ausfällung verursacht, und dass Tau eine gute Wasserlöslichkeit hat , GO weist auch eine gute Wasserlöslichkeit auf, da seine Oberfläche durch sauerstoffhaltige funktionelle Gruppen modifiziert ist. Die Verwendung von Tau-GO-Trägern zum Beladen von 5-FU verbessert die Wasserlöslichkeit von 5-FU erheblich, sodass 5-FU-Tau-GO stabil in wässriger Lösung dispergiert werden kann.
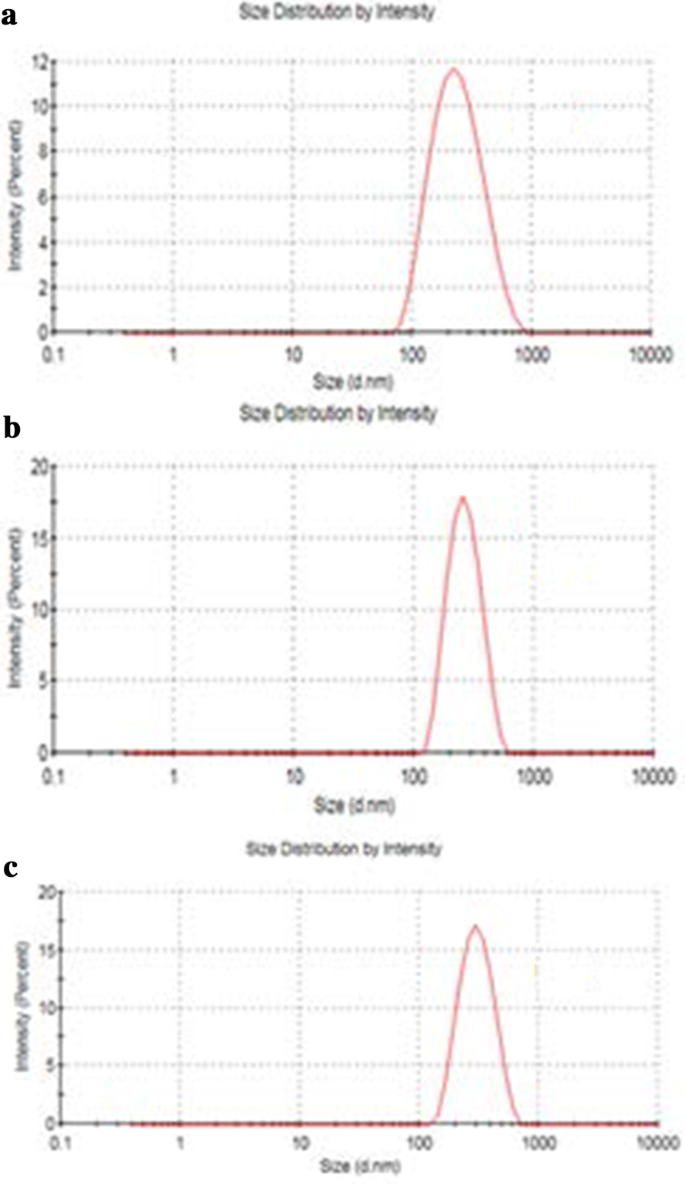
Partikelgröße von GO (a ), Tau-GO (b ) und 5-FU-Tau-GO (c )
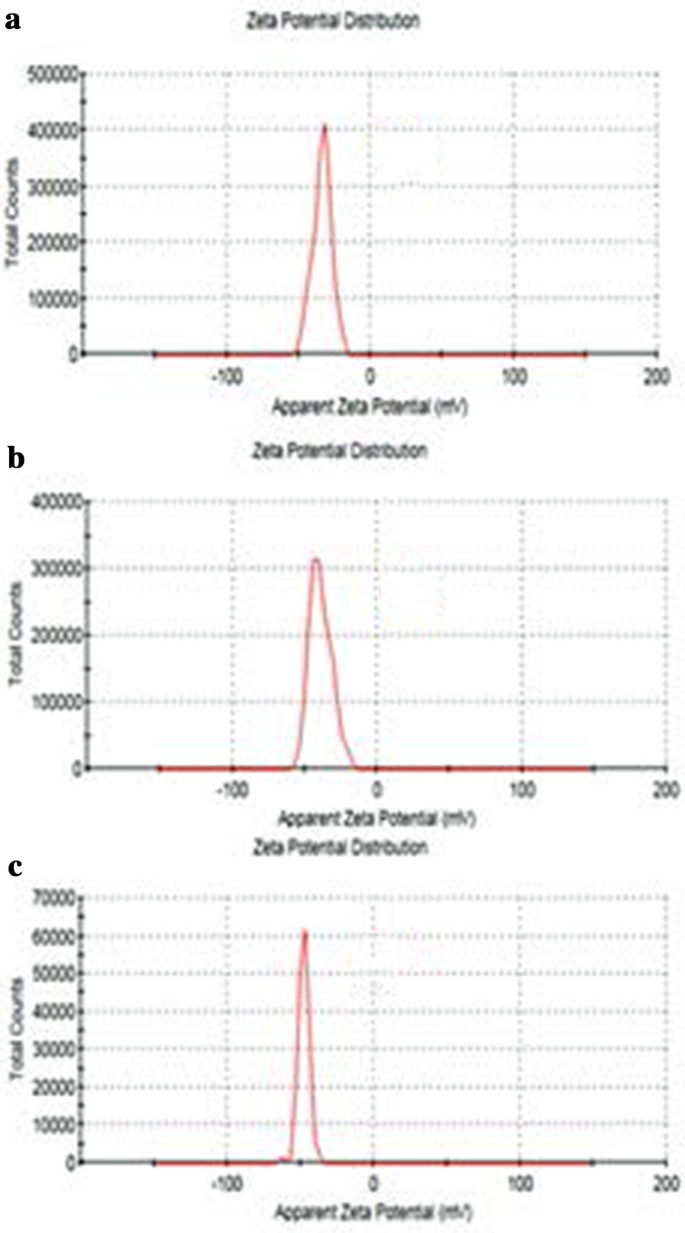
Zetapotentiale von GO (a ), Tau-GO (b ) und 5-FU-Tau-GO (c )
Die Morphologien von GO, Tau-GO und 5-FU-Tau-GO wurden durch TEM charakterisiert (Abb. 6). Das GO ist eine flache Struktur mit Falten auf der Oberfläche, die veranschaulicht, dass es sich um eine ebene zweidimensionale Struktur handelt (Abb. 6a). Im Vergleich zu GO war die Größe von Tau-GO leicht erhöht, zeigte aber immer noch eine lamellare Struktur (Abb. 6b). Das 5-FU-Tau-GO-Bild zeigte, dass die Materialien nicht aggregierten oder sich veränderten, wobei die anfängliche lamellare Struktur von GO intakt blieb (Abb. 6c). Folglich hatten Tau-GO und 5-FU-Tau-GO eine gute Stabilität.

TEM von GO (a ), Tau-GO (b ) und 5-FU-Tau-GO (c )
Die thermogravimetrische Analyse wurde verwendet, um die Zusammensetzungen der Verbundstoffe zu quantifizieren. Die TGA-Kurven von GO und Tau-GO sind in Abb. 7 dargestellt. GO und Tau-GO haben Restmassen von 39,73 % und 34,22 % in einer Stickstoffatmosphäre von 800 °C. Daher wurde beim Vergleich der Gewichtsänderungswerte der Tau-Gehalt in Tau-GO mit ungefähr 13% bestimmt.
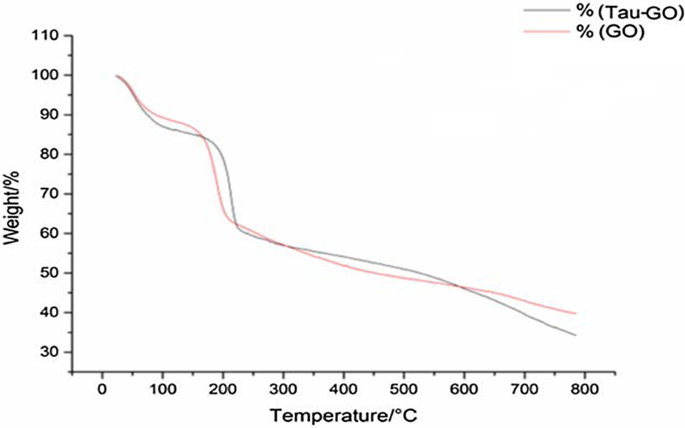
TAG von GO und Tau-GO
Die XRD-Muster von Tau, GO und Tau-GO sind in Abb. 8 gezeigt. Der charakteristische Peak von GO kann bei 10,7° des 2θ-Wertes beobachtet werden, was die Bildung von GO mit vollständiger Oxidation für einen starken chemischen Oxidations- und Abblätterungsprozess bestätigt . Nach der Funktionalisierung mit Tau auf der GO-Oberfläche nahm das Beugungsmuster des Peaks bei einem 2θ-Wert von 8,2 leicht ab. Dies bedeutet, dass GO von Tau erfolgreich funktionalisiert wurde.
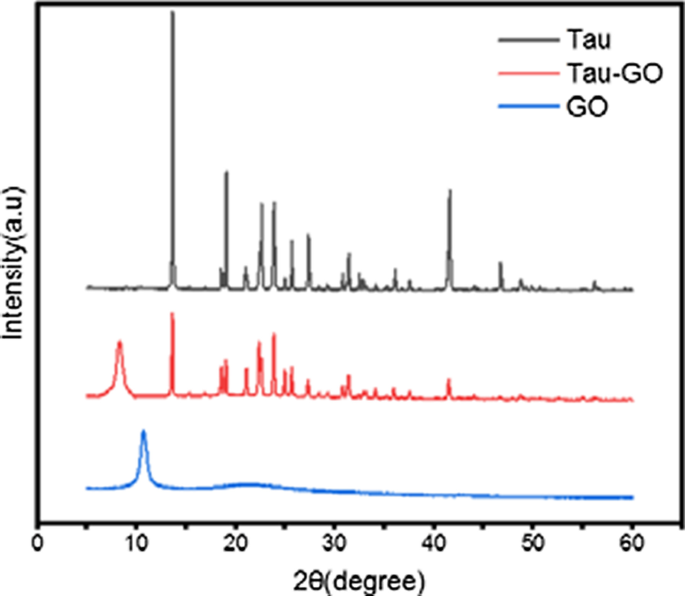
XRD-Muster von Tau, Tau-GO und GO
Die C1s-XPS-Spektren von GO und Tau-GO sind in Abb. 9 dargestellt. Die C1s-XPS-Spektren von GO weisen auf einen beträchtlichen Oxidationsgrad hin, wobei vier Kohlenstoffatome unterschiedlichen funktionellen Gruppen entsprechen. Die C1s-XPS-Spektren von Tau-GO zeigen ebenfalls dieselben Kohlenstoffatome. Darüber hinaus wurde das Auftreten von Peaks der CN-Bindungskomponente den Aminogruppen und Amidgruppen zugeschrieben. Diese Ergebnisse zeigen auch, dass GO erfolgreich von Tau funktionalisiert wird.
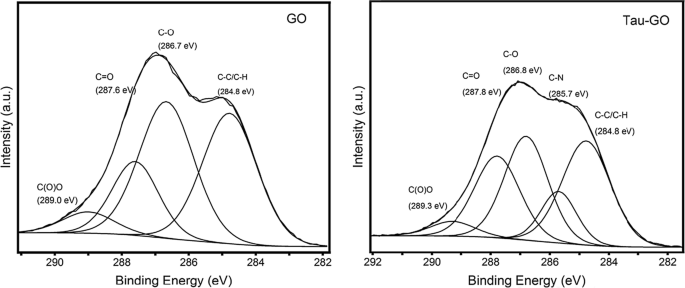
C1s XPS-Muster von GO und Tau-GO
Verhalten beim Laden und Freigeben von Medikamenten
5-FU wurde durch nicht-kovalente Wechselwirkungen an Tau-GO-Nanoträger adsorbiert. Die 5-FU-Kalibrierungskurve war y = 62.135x +21,873 (r = 0,9999) und der Bereich lag zwischen 6,5 ~ 250 µg/ml. Das Einkapselungsverhältnis (EE) und die Wirkstoffbeladungseffizienz (LE) wurden durch ungebundene Wirkstoffkonzentrationen bestimmt, um die Wirkstoffbeladungsleistung zu bewerten. Die Ergebnisse zeigten, dass EE mit steigender Wirkstoffkonzentration zunahm und dass der höchste EE-Wert 83,2 % betrug. Laut Formel betrug der LE 33,7%, d. h. 508,52 μg 5-FU können auf 1 mg Tau-GO adsorbiert werden. Daher ist Tau-GO ein vielversprechender Wirkstoffträger, der eine große Wirkstoffmenge erreichen kann. Die möglichen Mechanismen der hohen Beladungskapazität von 5-FU auf Tau-GO lassen sich durch folgende Erklärungen zusammenfassen:Erstens dient Tau dazu, GO zu funktionalisieren und aktive funktionelle Gruppen (–SO3 ). –SO3 hat eine starke Ionisationsfähigkeit in der Lösung, die die Agglomeration zwischen GO verringert und das Laden von 5-FU in Tau-GO erleichtert. Zweitens unterscheidet sich das Zeta-Potential von 5-FU-Tau-GO um 12,1 mV von dem von Tau-GO, was darauf hindeutet, dass 5-FU auf die Oberfläche von Tau-GO geladen wird und die elektrostatische Wechselwirkung eine wichtige Rolle bei der Beladung mit 5-FU. Schließlich gibt es viele Formen von Wasserstoffbrücken zwischen 5-FU und Tau-GO-Trägern, einschließlich –COOH in Tau-GO und –NH– in 5-FU, –COOH in Tau-GO und-in 5-FU C=O , –OH in Tau-GO und –NH– in 5-FU, –OH in Tau-GO und –C=O in 5-FU, –COOH und 5-FU in Tau-GO –F in Tau-GO, – COOH in Tau-GO und –F in 5-FU, diese Wasserstoffbrücken machen 5-FU-Tau-GO in Lösung stabil.
Die kumulative In-vitro-Freisetzung von 5-FU aus dem 5-FU-Tau-GO bei einer Temperatur von 37 °C in einer PBS-Lösung mit pH 1,2, 6,5 und 7,4 (simulieren Magenumgebung, Leberkrebszellumgebung bzw. physiologische Umgebung) ist in Abb. 10 dargestellt. Es wurde festgestellt, dass das freigesetzte 5-FU-Verhalten durch den pH-Wert der Umgebung beeinflusst wurde. In einem Puffer mit einem pH-Wert von 7,4 war die Wirkstofffreisetzung langsam und kontinuierlich, und die gesamte freigesetzte Wirkstoffmenge betrug nach 72 h ungefähr 70,84 %. Im Gegensatz dazu war die freigesetzte Arzneimittelmenge bei pH 7,4 signifikant niedriger als die bei pH 1,2 und pH 6,5 zum gleichen Zeitpunkt. Die gesamte Wirkstoffbeladung, die aus dem 5-FU-Tau-GO freigesetzt wurde, konnte bei ungefähr 90,29 % und 85,75 % bzw. bei pH 1,2 und pH 6,5 erreicht werden. Dies kann auf die π-π-Wechselwirkungen und Wasserstoffbrücken zwischen 5-FU und Tau-GO zurückgeführt werden. Je niedriger der pH-Wert, desto höher ist der Protonierungsgrad der Wasserstoffbrücke. Daher wurde die Stärke der Wasserstoffbrückenbindung durch den pH-Wert kontrolliert, was zur Freisetzung von 5-FU führte. Dieses pH-sensitive Wirkstoffabgabesystem spielt eine wichtige Rolle bei Antitumor-Medikamenten und kann die Freisetzung der Medikamente in die Tumorzelle erreichen.
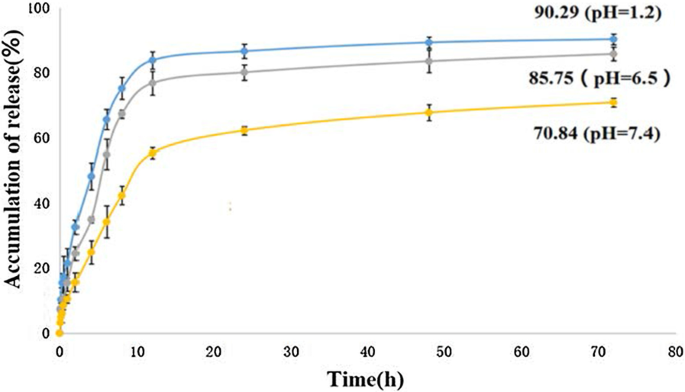
In-vitro-Freisetzungskurven von 5-FU-Tau-GO in Phosphat-Kochsalzlösung bei 37 °C
In-vitro-Zytotoxizitätsstudien
Um die potenzielle Toxizität und die Wirksamkeit von Nanocarriern in der Tumortherapie zu bewerten, wurde die In-vitro-Zelllebensfähigkeit in HepG2-Zellen unter Verwendung von MTT-Assays durchgeführt (Abb. 11). Das Tau-GO zeigte bei verschiedenen Konzentrationen keine signifikante Zytotoxizität. Nach 5-FU-Beladung zeigte das 5-FU-Tau-GO eine offensichtliche Hemmwirkung, und in dosisabhängiger Weise hatte der Nanoträger daher die Fähigkeit, Antitumor-Medikamente abzugeben. Der IC50 Der Wert von 5-FU-Tau-GO betrug 65,2 ± 0,7 µg/ml, was toxischer war als das freie 5-FU (196 ± 8,73 µg/ml). Dies kann an der Fähigkeit von Taurin liegen, Apoptose in Tumorzellen zu induzieren, wodurch indirekt die hemmende Wirkung von 5-FU auf Zellen verstärkt wird. Darüber hinaus konnte aus dem in vitro-Freisetzungsexperiment gesehen werden, dass 5-FU, das auf das Tau-GO geladen wurde, allmählich in den Zellen freigesetzt werden konnte. Daher war die Wirkzeit von 5-FU-Tau-GO auf Zellen länger als die von freiem 5-FU und bewirkte somit eine bessere Hemmung.
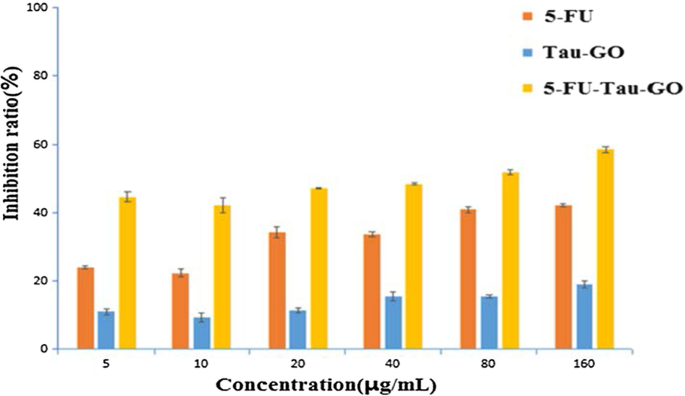
The viability of different concentrations of 5-FU, Tau-GO, and 5-FU-Tau-GO
AO fluorescent agent could emit green fluorescence when it passed through intact cell membranes and stained nuclei, while EB only marked the nucleus of damaged cells that emitted a red/orange fluorescence. The cells with early and late apoptosis presented greenish yellow or orange nuclei with the AO/EB stain, respectively. Therefore, AO/EB staining was performed to investigate whether the cells death was associated with apoptosis using characteristics of cell morphological changes. The results obtained from the AO/EB staining are presented in Fig. 12. Control cells were in spindle shape and with green nuclei. In the cell group that was cultured with Tau-GO alone, small parts of the nuclei were invaginated and with dark green or orange-red staining. Significant orange or red apoptotic cells with chromatin fragments and apoptotic bodies were observed in the 5-FU alone group. Compared with 5-FU, 5-FU-Tau-GO caused more damage to HepG2 cell morphology, which not only broke the cells, but also caused a large amount of apoptosis in cancer cells. As can be seen from the pictures, almost all the cells that were treated with 5-FU-Tau-GO, had morphological changes, a large number of cell debris and apoptotic bodies, indicating that the 5-FU-Tau-GO nano drug delivery system had a good killing effect on HepG2 cells.
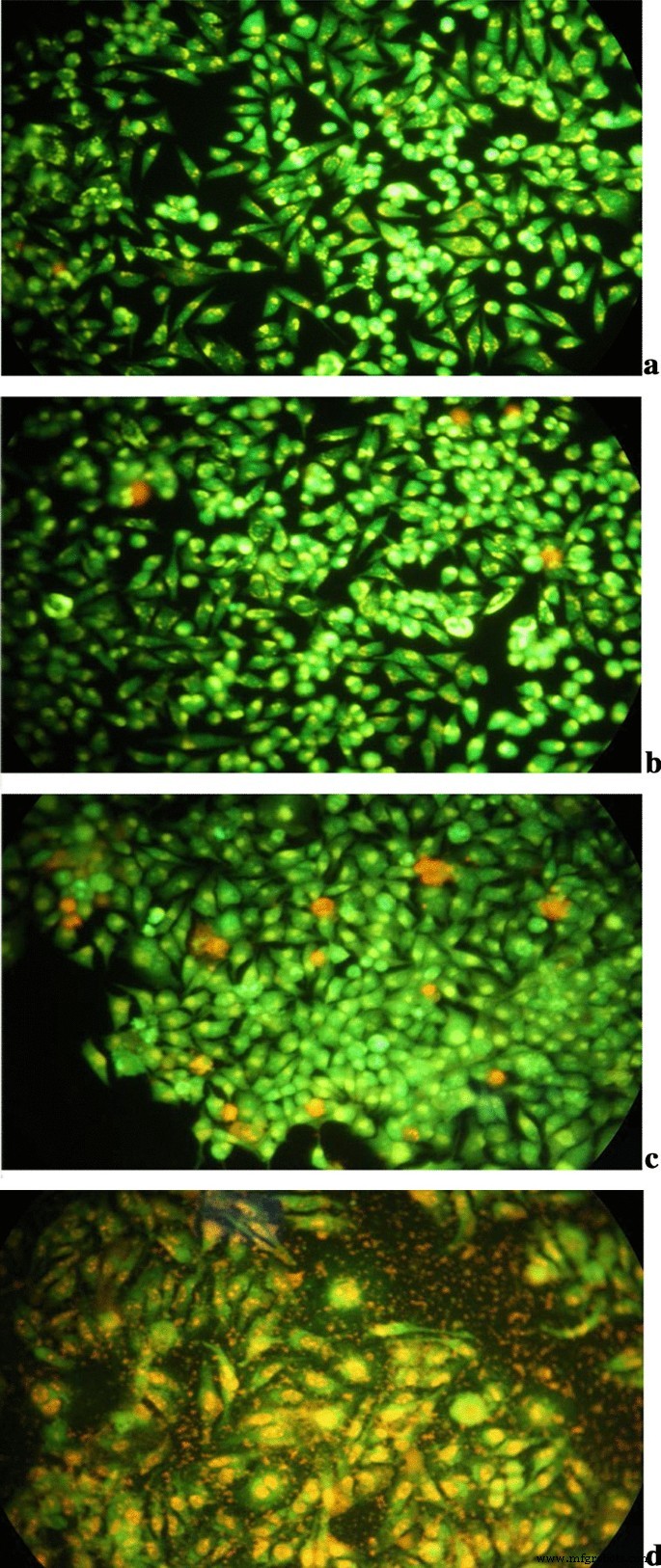
The AO/EB of control (a ), Tau-GO (b ), 5-FU (c ), and 5-FU-Tau-GO (d )
Pharmacokinetic Studies
The pharmacokinetic studies of 5-FU and 5-FU-Tau-GO were performed in SD rats. The profiles of 5-FU concentration in plasma vs. time, following oral administration, are presented in Fig. 13a. We found that the tendency of the two curves was similar, but the 5-FU plasma concentration from the 5-FU-Tau-GO nanocarrier was higher than that from the 5-FU alone and this was observed at each measured time point. Figure 13b shows the 5-FU in vivo release profiles via tail vein. The 5-FU-Tau-GO could achieve sustained drug release over 24 h, and the drug concentration gradually decreased in the first few hours, indicating that 5-FU was slowly released.
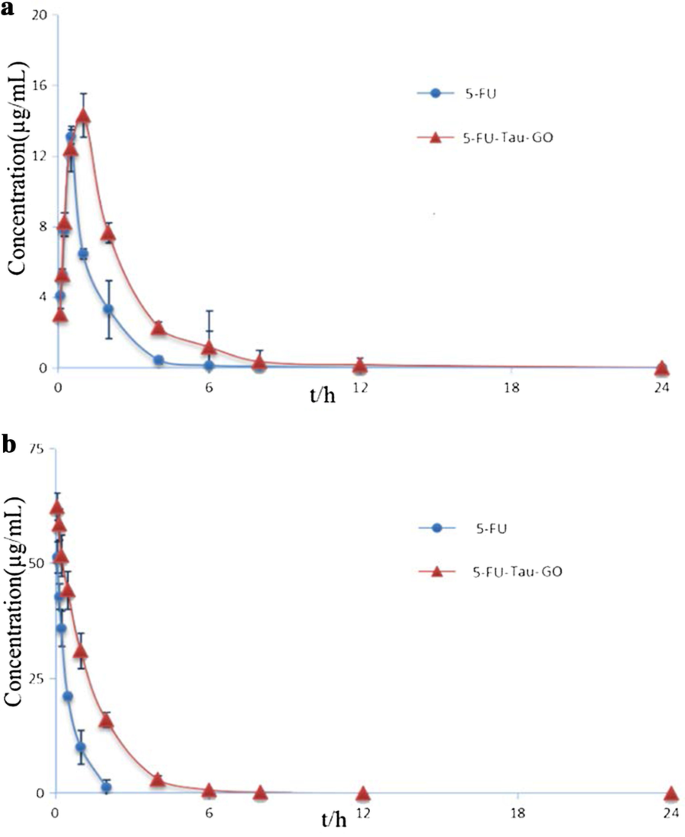
In vivo pharmacokinetic standard curves of 5-FU and 5-FU-Tau-GO through oral administration (a ). In vivo pharmacokinetic standard curve of 5-FU and 5-FU-Tau-GO through intravenous injection (b )
The two-compartment model was used to analyze the pharmacokinetic parameters of oral or intravenous administration in rats. The pharmacokinetic parameters are presented in Table 1. Compared with the 5-FU, the 5-FU-Tau-GO showed higher T1/2β that were 2.3 times by oral administration, and 3.0 times by intravenous injection, respectively. Moreover, the area under the concentration time curve (AUC0−t ) of 5-FU-Tau-GO nanocomplexes was roughy 2.1-fold higher through the oral administration, and 2.8-fold higher through intravenous injection when compared to that of the 5-FU solution, respectively. Therefore, we concluded that 5-FU-Tau-GO could significantly extend 5-FU retention time in vivo and improve bioavailability. In addition, the T1/2β of the 5-FU-Tau-GO nanocomplexes that were orally administered (1.67 ± 1.15 h), was longer than that of the intravenous injection (1.33 ± 0.64 h); however, the AUC0−t of oral administration (36.02 ± 1.83 mg/L*h) was lower than that of intravenous injection (96.50 ± 8.70 mg/L*h). These results might be due to two aspects:on the one hand, when administered by intravenous injection, the drug directly enters the blood system for circulation and without passing through the gastrointestinal barrier for redistribution; on the other hand, because 5-FU easily causes a certain damage to the gastrointestinal system, it may also affect the effective use of drugs in the body.
MD Simulations
The docking and molecular dynamics of unmodified GO, Tau-GO and 5-FU were simulated by molecular docking and molecular dynamics simulation. The molecular docking results of GO, Tau-GO and 5-FU are shown in Fig. 14, where it can be seen that the bond lengths of 5-FU and GO and Tau-GO are 3.66 Å and 2. 602 Å, respectively. Moreover, from the calculation results, the binding energies of 5-FU to GO and Tau-GO were 47.69 kcal/mol and 25.04 kcal/mol, respectively. These indicated that the binding force of Tau-GO and 5-FU was stronger than that of GO and 5-FU. This is due to Tau polar atoms, such as S and N, forming a stronger non-covalent bond with 5-FU, that makes the force between Tau-GO and 5-FU stronger.
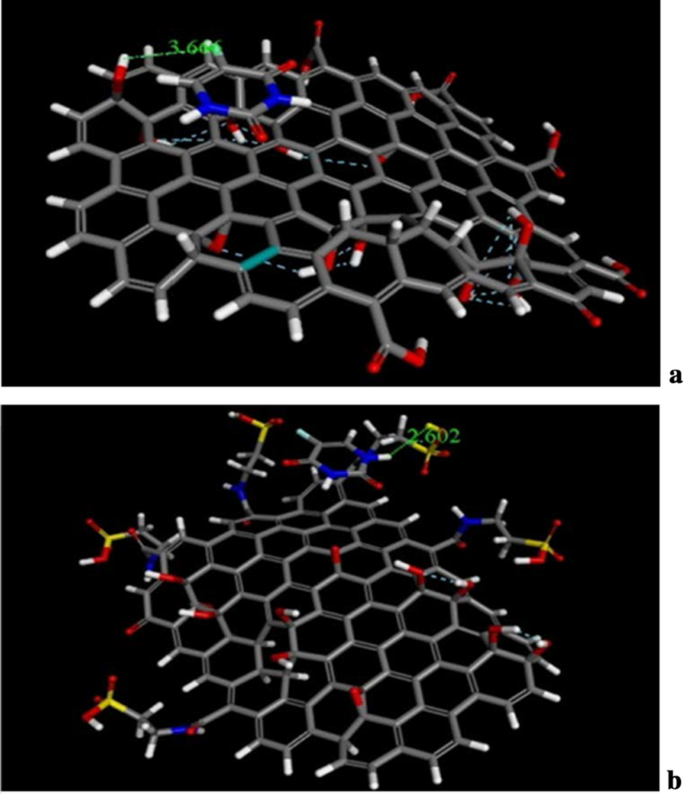
The Molecular docking of GO sheets with 5-FU (a ). The molecular docking of Tau-GO with 5-FU (b )
The diagrams of the molecular dynamics simulation of GO, Tau-GO and 5-FU were shown in Fig. 15. According to the calculation results, the CED of 5-FU-GO and 5-FU-Tau-GO were 2.67*10 8 and 2.83*10 8 , bzw. These results showed a stronger interaction between the drug and the Tau-GO. The graphs between MSD and time were plotted (Fig. 16) to obtain the diffusion coefficient via MSD. The drug diffusion coefficients were obtained by the slope divided by 6 as follows:0.094m 2 /s and 0.058 m 2 /S. These show that the force between Tau-GO and 5-FU is stronger, which is consistent with the results of the molecular docking. Therefore, the functionalized GO makes the entire carrier more abundant in atoms and groups; Therefore, making the non-covalent bond with 5-FU stronger, and the entire system more stable.
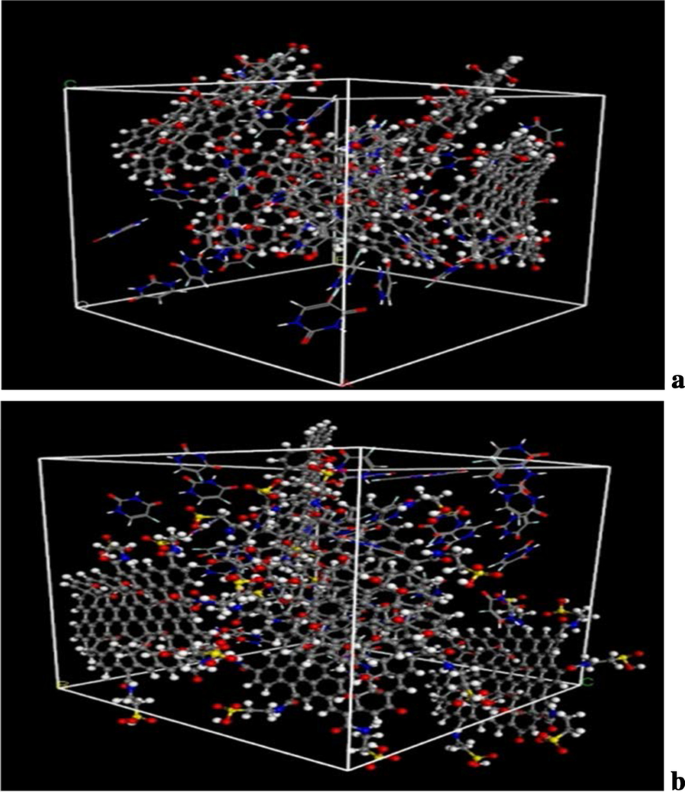
Snapshots of the GO and 5-FU at the end of the MD (a ). Snapshots of the Tau-GO and 5-FU at the end of the MD (b )
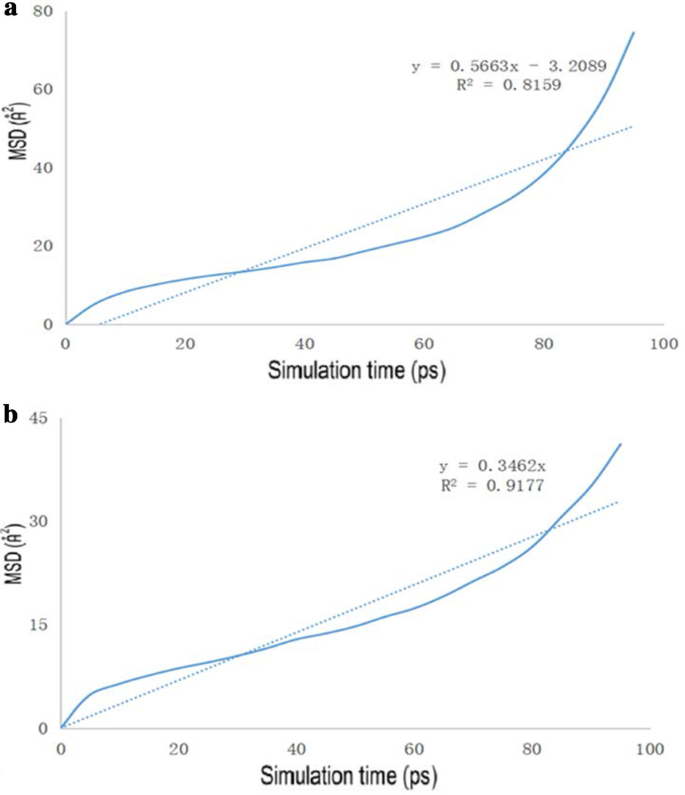
The drug MSD profiles of the GO and 5-FU (a ), Tau-GO and 5-FU (b )
Schlussfolgerungen
In summary, we successfully prepared a Tau-GO nanocomposite through a simple chemical method. GO functionalization with Tau has a good stability and improves its biocompatibility. The unique structure and brilliant properties of Tau-GO nanocarriers offer great opportunities for the loading and delivery of 5-FU. The 5-FU-Tau-GO has a potential anti-tumor ability and an excellent circulation time of drugs. Therefore, we believe that the modification of GO by the carrier Tau for 5-FU loading, is an effective and applicable tool for constructing a 5-FU-Tau-GO nano drug delivery system for the delivery of anticancer drugs and anti-tumor therapy.
Verfügbarkeit von Daten und Materialien
Die in der aktuellen Studie verwendeten und/oder analysierten Datensätze sind auf begründete Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- GO:
-
Graphenoxid
- Tau:
-
Taurine
- 5-FU:
-
5-Fluorouracil
- 5-FU-Tau-GO:
-
Taurine functionalized graphene oxide loading 5-fluorouracil
- EE:
-
Encapsulation ratio
- LE:
-
Drug-loading efficiency
- FT-IR:
-
Fourier-Transformations-Infrarot
- TEM:
-
Transmissionselektronenmikroskopie
- TGA:
-
Thermogravimetric analyses
- MSD:
-
Mean square displacement
- CED:
-
Cohesive energy density
Nanomaterialien
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Biokompatible FePO4-Nanopartikel:Wirkstofftransport, RNA-Stabilisierung und funktionelle Aktivität
- Mit Titanat-Nanoröhren dekorierte Graphenoxid-Nanokomposite:Vorbereitung, Flammhemmung und Photoabbau
- Biosicherheit und antibakterielle Wirkung von Graphen und Graphenoxid in vitro und in vivo
- RGO und dreidimensionale Graphen-Netzwerke modifizierte TIMs mit hoher Leistung gemeinsam
- Leitungsmechanismus und verbesserte Ausdauer bei HfO2-basiertem RRAM mit Nitridierungsbehandlung
- Herstellung, Charakterisierung und biologische Aktivität von Avermectin-Nanoabgabesystemen mit unterschiedlichen Partikelgrößen
- Bewertung von Graphen/WO3- und Graphen/CeO x -Strukturen als Elektroden für Superkondensatoranwendungen
- Graphen/Polyanilin-Aerogel mit Superelastizität und hoher Kapazität als hochkompressionstolerante Superkondensatorelektrode
- Herstellung und Charakterisierung von ZnO-Nano-Clips durch das Polyol-vermittelte Verfahren



