Antimikrobielle und zytotoxische Wirkungen synthetisierter Silbernanopartikel aus Punica granatum Peel-Extrakt
Zusammenfassung
Um den wachsenden Herausforderungen durch arzneimittelresistente Mikroben und das Auftreten von Tumoren zu begegnen, werden Ansätze zur Phytosynthese von Metallnanopartikeln, insbesondere Silbernanopartikeln, unternommen, um Abhilfemaßnahmen zu ergreifen. In dieser Studie wurde versucht, ein wichtiges Bioabfallprodukt, Granatapfelfruchtschalen (Punica granatum ), um Silbernanopartikel zu synthetisieren. Die Silbernanopartikel (AgNPs) wurden mit dem wässrigen Extrakt der Granatapfelschale synthetisiert. Die Bildung synthetisierter AgNPs wurde durch UV-Vis-Spektroskopie, Röntgenbeugung (XRD), Transmissionselektronenmikroskopie (TEM), Rasterelektronenmikroskopie (REM) und energiedispersive Röntgenspektroskopie (EDX) sowie durch die Umwandlung der farblosen wässrigen Lösung in eine dunkelbraune Lösung. Unter Verwendung der UV-Vis-Spektroskopie zeigte die dunkelbraune Lösung nach 24, 48 und 72 Stunden Reaktionszeit einen Peak der Plasmon-Resonanzbande bei 378 nm in der UV-Vis-Spektroskopie. Der XRD-Bericht ergab, dass die AgNPs eine kubische Struktur hatten. Der TEM- und SEM-Bericht zeigte, dass die Nanopartikel gleichmäßig in der Lösung verteilt waren, mit einer kugelförmigen Form und Größe im Bereich von 20 bis 40 nm und einer durchschnittlichen Partikelgröße von 26,95 nm. Die EDX-Bildgebung bestätigte auch das Vorhandensein von AgNPs. Es wurde festgestellt, dass die synthetisierten AgNPs gute antimikrobielle Wirkungen auf Gram-negative und Gram-positive Bakterien zeigen, insbesondere auf die Krankheitserreger Escherichia coli (ATCC 25922), Pseudomonas aeruginosa (ATCC 27584), Proteus vulgaris (ATCC 8427), Salmonella typhi (ATCC 14028), Staphylococcus aureus (ATCC 29213), Staphylococcus epidermidis (MTCC 3615) und Klebsiella-Pneumonie. Die zytotoxischen Wirkungen von AgNPs wurden auch gegen eine Dickdarmkrebszelllinie (RKO:ATCC® CRL-2577™) getestet und es wurde beobachtet, dass die Lebensfähigkeit an den Tagen 3 und 5 bei einer Exposition gegenüber 12,5 . 56% bzw. 61% betrug μg AgNPs. Diese einfache, wirtschaftliche und umweltfreundliche Methode legt nahe, dass die aus Granatapfelschalen-Extrakt biosynthetisierten AgNPs eine neuartige, wirksame Lösung für die Entwicklung eines Medikaments gegen Dickdarmkrebs sein könnten, das auch antibakterielle Wirkung hat.
Hintergrund
In den letzten Jahrzehnten gab es eine wachsende Menge an Forschung zur Nanotechnologie, insbesondere in Bezug auf die grüne Synthese und Charakterisierung von Nanopartikeln, da Nanopartikel mit einer Größe von weniger als 100 nm ideale Wirkstoffe für die Wirkstoffabgabe und biomedizinische Anwendungen sind [1]. Die Synthese von Nanopartikeln spielt in mehreren Bereichen eine einflussreiche Rolle, darunter Nanotechnologie, Biotechnologie, chemische Verarbeitung, physikalische Methodik, Systemtechnik, molekulare Motoren, Nanokristalle und Nanobiomaterialien [2]. Heute gibt es drei Methoden zur Herstellung von Nanopartikeln – chemische, physikalische und „grüne“ Routen, wobei die grüne Route den Einsatz biologischer Reduktionsmittel beinhaltet, einschließlich Pflanzenextrakten und Mikrobenfiltraten. Die ersten beiden Methoden sind oft kostspielig und erzeugen giftige Nebenprodukte, aber die grüne Nanosynthese-Methode wurde als kostengünstiges und umweltfreundliches Verfahren anerkannt [3,4,5].
Bei der grünen Synthese von Nanopartikeln werden Pflanzenbestandteile, darunter Proteine, Enzyme und Kohlenhydrate, verwendet, um Nanopartikel zu formulieren, die leicht mit Zielbiomolekülen interagieren können [6]. Dieser Ansatz zur Synthese von Silbernanopartikeln könnte eine wichtige Rolle bei zukünftigen Behandlungen für verschiedene Krebsarten oder andere Krankheiten spielen, die durch Phytonanotechnologie kontrolliert werden können [7, 8]. Gram-negative Bakterien wie Escherichia coli , Pseudomonas aeruginosa , und Proteus vulgaris , und Gram-positive Krankheitserreger wie Staphylococcus aureus und S. Epidermidis , sind für die meisten Krankenhausinfektionen verantwortlich [9]. Tatsächlich sind chirurgische Infektionen, einschließlich Lungenentzündung und Blutkreislaufinfektionen, auch auf das Vorhandensein grampositiver und gramnegativer Bakterien zurückzuführen [10]. Die pflanzenvermittelte Synthese von AgNPs kann bei der Entwicklung wirksamer antibakterieller Wirkstoffe gegen mikrobielle Krankheitserreger von Bedeutung für die öffentliche Gesundheit helfen. Kürzlich wurde festgestellt, dass synthetisierte AgNPs eine synergistische Beziehung mit dem Antibiotikum Levofloxacin aufweisen können, wodurch die antimikrobielle Gesamtaktivität erhöht wird [11]. Viele Forscher haben berichtet, dass synthetisierte AgNPs bekannte antimikrobielle Eigenschaften gegen grampositive und gramnegative Pathogene sowie zytotoxische Wirkungen auf verschiedene krebsartige und normale Zelllinien aufweisen [12,13,14]. Darüber hinaus sind AgNPs aufgrund eines großen Oberfläche-zu-Volumen-Verhältnisses hocheffizient, können leicht aufbrechen und haben im Vergleich zu Silberionen allein die Fähigkeit, Bakterienzellen zu durchdringen [13].
Die aktuelle Studie konzentriert sich auf die grüne Synthese von AgNPs unter Verwendung des wässrigen Extrakts von Punica granatum Peeling und zur Untersuchung ihrer antimikrobiellen Eigenschaften durch Verwendung von Streak-Platten und Messungen der minimalen Hemmkonzentration (MHK) nach 24 h Inkubation bei 37 °C. Die gramnegativen Bakterien E. coli (ATCC 25922), P. aeruginosa (ATCC 27584), P. vulgaris (ATCC 8427) und Salmonella typhi (ATCC 14028) sowie die grampositiven Bakterien Staphylococcus aureus (ATCC 29213), S. Epidermidis (MTCC 3615) und K. Lungenentzündung wurden untersucht, um die potenzielle Wachstumshemmung durch synthetisierte AgNPs zu testen. Darüber hinaus wurden die zytotoxischen Wirkungen auf eine Dickdarmkrebszelllinie (RKO:ATCC® CRL-2577™) getestet und zeigten eine Zellviabilitätsrate von 56 % an Tag 3 und 61 % an Tag 5 mit einer Dosis von 12,5 μg AgNPs.
Methoden
Vorbereitung des Peel-Extrakts
Ein Kilogramm saudische Granatapfelfrüchte (Punica granatum .) —angebaut in der Taif-Region des Königreichs Saudi-Arabien) wurde im Supermarkt in Riad, Saudi-Arabien, gekauft. Die Früchte wurden mehrmals mit Leitungswasser und dann mit bidestilliertem Wasser (DDH2 .) gewaschen Ö). Nach dem Waschen wurde die Schale vorsichtig entfernt. Die Granatapfelschale wurde gründlich mit DDH2 . abgespült O, um jegliche Oberflächenkontamination zu vermeiden und bei Raumtemperatur vollständig trocknen zu lassen. Schließlich wurde die Schale zu einem feinen Pulver gemahlen. Zehn Gramm des feinen Pulvers wurden in 100 ml DDH2 . eingeweicht O für 24 h bei Raumtemperatur. Die resultierende Mischung wurde unter Verwendung von Whatman Nr. 1-Filterpapier filtriert, um den wässrigen Extrakt zu erhalten. Der gesamte Prozess wurde unter sterilen Bedingungen durchgeführt.
Syntheseprozess von AgNPs
Silbernitrat (AgNO3 .); 0,1 mM) wurde mit 250 ml DDH2O gemischt. Dann wurden zehn Milliliter wässriger Granatapfelschalenextrakt zugegeben und die Lösung mit einem Schüttelinkubator 5 Minuten lang gründlich gemischt. Es wurde festgestellt, dass das Reaktionsgemisch nach 24 h seine Farbe von einer farblosen Lösung zu einer braunen Lösung änderte, was auf die Reduktion der Silberionen zu Silbernanopartikeln hinweist. Die Nanopartikellösung wurde dann bei 15.000 U/min für 15 Minuten zentrifugiert und der Vorgang wurde viermal wiederholt. Schließlich wurden gereinigte AgNPs gesammelt und weitere Assays durchgeführt, um die Eigenschaften und biologischen Aktivitäten der synthetisierten NPs zu analysieren. Der überschüssige Schalenextrakt wurde zur weiteren Analyse bei 4 °C gelagert.
Charakterisierung der AgNPs
Die Reduktion von Silberionen durch den wässrigen Granatapfelschalenextrakt wurde mit einem Perkin Elmer Lambda 950 UV/Vis/NIR-Spektrophotometer 24, 48 und 72 h nach Beginn der Reaktion von 200 auf 800 nm und bei einer Auflösung von 1 nm . überwacht . XRD-Muster wurden mit einem PANalytical-Röntgendiffraktometer erhalten, das Scangeschwindigkeiten im Bereich von 20 bis 50 mit 2θ . erreichen kann und wurden verwendet, um die kristalline Struktur der Silbernanopartikel zu bestimmen.
Oberflächentopografische und Zusammensetzungsanalysen der AgNPs wurden mit einer TEM-Analyse durchgeführt, die auf einem JEOL JEM-1230 (JEOL, Tokio, Japan) und einem JSM 6380 LA SEM mit einer Auflösung von 3,0 nm durchgeführt wurde. Die Elementaranalyse der AgNPs wurde durch energiedispersive Röntgenspektroskopie (EDX) unter Verwendung einer JED 2200-Serie (Jeol) durchgeführt.
Antibakterielle Studien
Vorbereitung der Bakteriensuspension
Bakterienstämme E. coli (ATCC 25922), P. aeruginosa (ATCC 27584), P. vulgaris (ATCC 8427), S. Typhi (ATCC 14028), S. aureus (ATCC 29213), S. Epidermidis (MTCC 3615) und K. Lungenentzündung wurden vom King Khalid Hospital in Riad, Königreich Saudi-Arabien, erhalten. Eine schnelle Identifizierung von Bakterienzellen wurde nach zuvor veröffentlichten Methoden durchgeführt [15]. Alle identifizierten Kulturen wurden auf Agarmedien übertragen und bei – 20 °C gelagert, bis sie für die Studie benötigt wurden. Zu diesem Zeitpunkt wurde jeder Bakterienstamm in sterilen Nähragar geimpft und bei 37 °C für 24 Stunden inkubiert. Die Sperre (10 6 CFU/ml) wurde hergestellt, indem eine Impföse aus der 24-h-inkubierten Kultur in 5 ml Nährbrühe überführt und 2 h bei 37 °C inkubiert wurde.
Antimikrobielle Assays
Antimikrobielle Aktivitätsassays wurden unter Verwendung einer Agar-Well-Diffusionsmethode durchgeführt [16]. Ein steriler Tupfer wurde mit frischer Bakteriensuspension befeuchtet und auf einer festen, sterilen Müller-Hinton-Agarplatte ausgestrichen. In der Agarplatte wurden mit einem Korkbohrer Vertiefungen hergestellt. In jede aufeinanderfolgende Vertiefung wurden unterschiedliche Konzentrationen (25, 50, 75 und 100 μl) der synthetisierten Nanopartikelsuspension gegossen. Alle Platten wurden 24 h bei 37 °C inkubiert. Um jede Vertiefung in jeder inkubierten Platte wurde eine Hemmzone (mm) gemessen. Für jedes Experiment wurden drei Wiederholungen durchgeführt [17].
Zellproliferationsanalyse
Die Wirkung von AgNPs auf die Zellproliferation wurde wie zuvor beschrieben mit einem Alamar Blue-Assay bewertet [12].
Kurz gesagt, 0,005 × 10 6 Zellen/Well wurden in 96-Well-Platten mit unterschiedlichen Konzentrationen (100–0,3 μg/ml) von AgNPs ausgesät und 2 bis 5 Tage bei 37 °C inkubiert. Das Medium DMEM wurde mit 4500 mg/l d-Glucose, 4 mM l-Glutamin, 110 mg/l Natriumpyruvat, 10 % fötalem Rinderserum (FBS), 1× Penicillin-Streptomycin und nicht essentiellen Aminosäuren ergänzt (alle von Gibco-Invitrogen, USA gekauft). Kontroll-Wells wurden nur mit Medium behandelt und die Zellproliferation wurde an Tag 3 und Tag 5 gemessen. Zu diesen Zeitpunkten wurde Alamar Blue (1:10) zu jedem Well hinzugefügt und die Platten wurden bei 37 °C für 4 h inkubiert; dann wurden die Platten unter Verwendung eines spektrophotometrischen Mikroplattenlesegeräts (Biotek Synergy 2; Biotek Instruments, USA) gelesen und die relative Fluoreszenzeinheit (RFU) wurde aufgezeichnet.
Zell-Apoptose-/Nekrose-Analyse
Zur Bestimmung von Apoptose/Nekrose wurden die Zellen mit AgNPs in unterschiedlichen Konzentrationen (25–1,5 μg/ml) behandelt. An Tag 5 wurden die Zellen mit einer dualen Fluoreszenz-Färbelösung (1 μl) gefärbt, die 100 μg/ml AO (Acridinorange) und 100 μg/ml EtBr (Ethidiumbromid) (AO/EtBr, Sigma, St. Louis, MO .) enthielt ). Die gefärbten Zellen wurden 1 min einer AO/EtBr (1:100)-Farbstofflösung ausgesetzt und mit einem Nikon Eclipse Ti-Fluoreszenzmikroskop beobachtet. Die Ergebnisse wurden mit der experimentellen Kontrolle verglichen. AO/EtBr, eine Kombination aus zwei Farbstoffen, hilft, Zellen mit abweichender Chromatinorganisation sichtbar zu machen. Die unterschiedliche Aufnahme von AO/EtBr ermöglicht die Identifizierung lebensfähiger und nicht lebensfähiger Zellen. Insbesondere wurde die AO verwendet, um die Anzahl der Zellen zu visualisieren, die eine Apoptose durchgemacht hatten.
Statistische Analyse
Statistische Analysen und grafische Darstellungen wurden mit Microsoft Excel 2010 und der Software GraphPad Prism 6.0 (GraphPad, San Diego, CA, USA) durchgeführt. P die Werte wurden unter Verwendung von Einweg-ANOVA-Mehrfachvergleichen berechnet. Die antimikrobielle Datenanalyse für verschiedene Konzentrationen wurde mit einem Signifikanzniveau von P . getestet < 0.05.
Ergebnisse und Diskussion
Die AgNPs wurden erfolgreich unter Verwendung des wässrigen Extrakts der Granatapfelschale als Reduktionsmittelquelle synthetisiert. Abbildung 1a zeigt 0,1 mM Silbernitrat, gelöst in 250 ml DDH2 O um eine farblose Lösung herzustellen. Dann wurden 10 ml wässriger Schalenextrakt zugegeben und gut gemischt, und die Reaktionsmischung änderte sich langsam über 24 h zu einer dunkelbraunen Farbe, wie in Abb. 1b zu sehen ist. Die bei der Synthese von AgNPs beobachtete Farbänderung wurde für ähnliche Reaktionen beschrieben, wenn verschiedene Arten von Pflanzenteilextrakten wie Blätter, Blüten, Schalen, Samen und Früchte verwendet werden. Die Farbänderung war auf AgNO3 . zurückzuführen interagiert mit pflanzlichen Quellen und wird von Silbernitrat zu elementarem Silber reduziert [18,19,20,21,22].

a 0,1 mM Silbernitrat. b Farbänderungen nach P. Granatum Schalenextrakt hinzugefügt
Abbildung 2 zeigt das UV-Vis-Spektrum von AgNPs, die mit wässrigem Granatapfelschalenextrakt synthetisiert wurden. Wie in Abb. 2 gezeigt, weist die Absorptionsbande einen Peak bei 378 nm bei Reaktionszeiten von 24, 48 und 72 h mit Intensitäten von 0,96, 1,08 bzw. 1,16 auf. Die Intensität nahm mit der Zeit zu, da die Reaktion mehr Zeit zum Ablaufen hatte, was zu höheren AgNP-Konzentrationen führte. Die Oberflächenplasmonenresonanzdaten zeigten, dass steigende Konzentrationen von AgNPs zu steigenden AgNP-Peaks führten, was mit einer erhöhten Menge an reduziertem Silber im Laufe der Zeit zusammenfiel. Als AgNO3 durch die Freisetzung von Elektronen aus dem Granatapfelextrakt zu AgNPs reagierten, begann eine gleichzeitige Reaktion, Ascorbatradikale zu oxidieren. Ein ähnliches UV-Vis-Absorptionsspektrum wurde in einer anderen Studie beobachtet, in der AgNPs aus Granatapfelschalenextrakt hergestellt wurden, mit einem Absorptionspeak bei 371 nm [23].
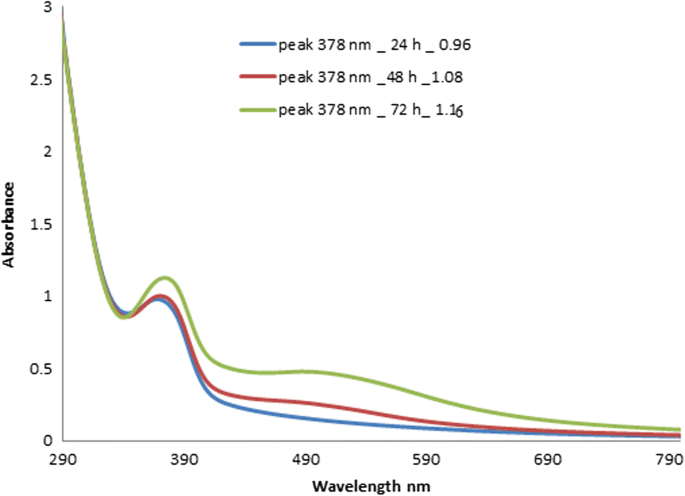
UV-Vis-Absorptionsspektren synthetisierter AgNPs nach 48 bis 72 h in Zeitintervallen
Das XRD-Muster von grün synthetisierten AgNPs ist in Abb. 3 gezeigt. Sechs intensive Beugungspeaks werden bei 2θ . beobachtet Werte im Bereich von 0 bis 90, was darauf hindeutet, dass wir die 111, 200, 220 und 311 Ebenen eines gegenüberliegenden Würfels einem zentralen Ag-Ion zuordnen könnten. Das XRD-Spektrum legt nahe, dass die synthetisierten AgNPs eine kristalline Struktur bildeten. Dieses Ergebnis stimmt mit XRD-Mustern überein, die zuvor in der JCPDS-Datenbank (Nr. 04-0783) veröffentlicht wurden. Die beobachteten nicht identifizierten kristallinen Peaks (*) entsprechen Silberoxiden [24]. Ein TEM-Bild von 0,1 mM wässrigen Granatapfel-NPs ist in Abb. 4 gezeigt. Dieses Bild zeigte Partikel mit einer kugelförmigen Form mit einem Durchmesser im Bereich von 20 bis 40 nm, wobei die durchschnittliche Partikelgröße 26,95 nm betrug. Ähnliche Berichte wurden über die Nanosynthese von Nanopartikeln unter Verwendung von Actinidia deliciosa . veröffentlicht Fruchtextrakt [25]. Die SEM-Beobachtungen der synthetisierten AgNPs (Abb. 5) zeigen eine gleichmäßige Verteilung von Silbernanopartikeln auf der Oberfläche von Granatapfelschalenzellen. Aus diesem Bild wurde festgestellt, dass die Nanopartikel eine kugelförmige Form mit Durchmessern im Bereich von 20 bis 40 nm haben, was einem früheren Bericht über kugelförmige AgNPs mit einem Durchmesser von 34 bis 50 nm ähnelt, die mit Raphanus sativus . hergestellt wurden L.-Schalenextrakt [26].
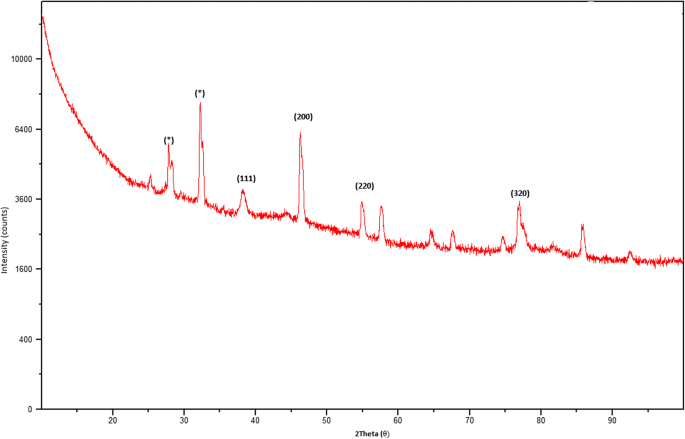
XRD-Muster synthetisierter AgNPs von P. Granatum Schalenextrakt

TEM-Aufnahme synthetisierter AgNPs von P. Granatum Schalenextrakt

SEM-Aufnahme von synthetisierten AgNPs von P. Granatum Schalenextrakt
Bei der Phytosynthese von Silbernanopartikeln unter Verwendung des hier vorgestellten Granatapfelschalenextrakts ist die Größe der erhaltenen Nanopartikel für den Wirkstofftransport recht vielversprechend. Es wird berichtet, dass die Größe der Nanopartikel mit einer Größe von weniger als 100 nm eine Rolle bei der Entwicklung intelligenter Systeme spielt, die die therapeutischen und bildgebenden Werte sowie die Wirkstoffabgabe an bestimmte Gewebe verbessern, um eine Therapie mit kontrollierter Freisetzung bereitzustellen [27]. Die Größe und Form der Nanopartikel beeinflusst die Bioverfügbarkeit des Wirkstoffs in Zielgeweben. Nanopartikel mit einer Größe von 100 nm weisen eine 2,5-fach höhere Aufnahme im Vergleich zu Partikeln mit einem Durchmesser von 1 μm auf [28, 29]. Die Größe der Nanopartikel spielt eine Schlüsselrolle bei der Partikelfunktion, wie Abbau, Gefäßdynamik, Targeting, Clearance und Aufnahmemechanismen [30]. Darüber hinaus verbessert die nanokristalline Natur der synthetisierten AgNPs die Bioverteilung und Pharmakokinetik, wie berichtet [31, 32]. Die Verwertung von Granatapfel-Bioabfall wird ein neuer Ansatz zur Abfallverwertung sein, wie bereits berichtet [33].
Die Daten der EDX-Studie lieferten eine qualitative und quantitative Analyse der in den synthetisierten Nanopartikeln gefundenen Elemente, wie in Abb. 6 gezeigt. Die EDX-Studie lieferte eine elementare Aufschlüsselung des Inhalts der synthetisierten NPs und schätzte, dass die NPs zu 70 % aus Ag nach Gewicht. Andere Elemente und Bindungen, die in den Ergebnissen identifiziert wurden, waren C-K, O, C-U, Cu und K, die jeweils einem kleinen Prozentsatz der Gesamtmasse entsprachen. Der EDX-Bericht belegt, dass die niedrige Konzentration von 0,1 mM AgNO3 führte zu einer hohen Anzahl synthetisierter AgNPs. Ähnliche Ergebnisse wurden für 0,3 mM AgNO3 . berichtet das für 3 h in destilliertes Wasser gegossen und auf 300 °C erhitzt wurde, und für 1, 2 und 3 g Granatapfelschalenextrakt mit 30 ml destilliertem Wasser vermischt und auf 80 °C erhitzt [34].
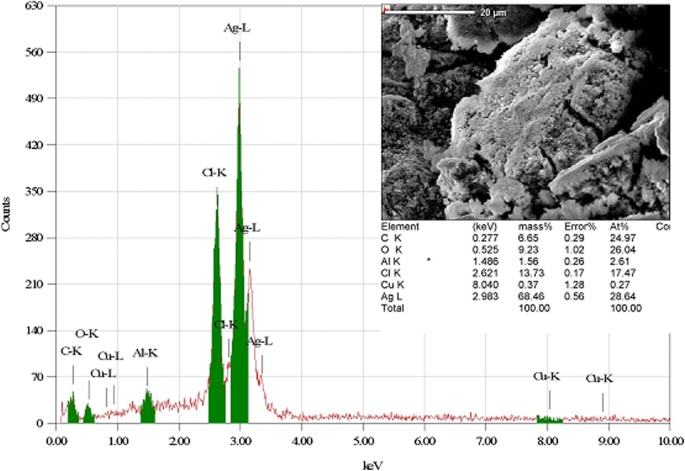
EDX-Bild synthetisierter AgNPs von P. Granatum Schalenextrakt mit quantitativer Analyse
Die antibakteriellen Eigenschaften der Granatapfel-synthetisierten AgNPs wurden mit 25, 50, 75 und 100 μg/ml-Proben sowohl gegen Gram-positive als auch gegen Gram-negative Bakterien über den Agar-Well-Diffusionstest untersucht. Agarplatten mit den gramnegativen Bakterien E. coli , S. Typhi , und P. aeruginosa und die Hemmungszonen sind in den Abb. 7a–c gezeigt. Niedrige Konzentrationen von Granatapfel-synthetisierten AgNPs (25 und 50 μl) zeigten eine inhibitorische Aktivität gegen P. aeruginosa und E. coli aber nicht gegen S. Typhi. Ähnliche antimikrobielle Wirkungen von Granatapfelprodukten wurden bereits berichtet, wobei die stärksten Hemmungen für E. coli , S. aureus , und P. aeruginosa [35,36,37].
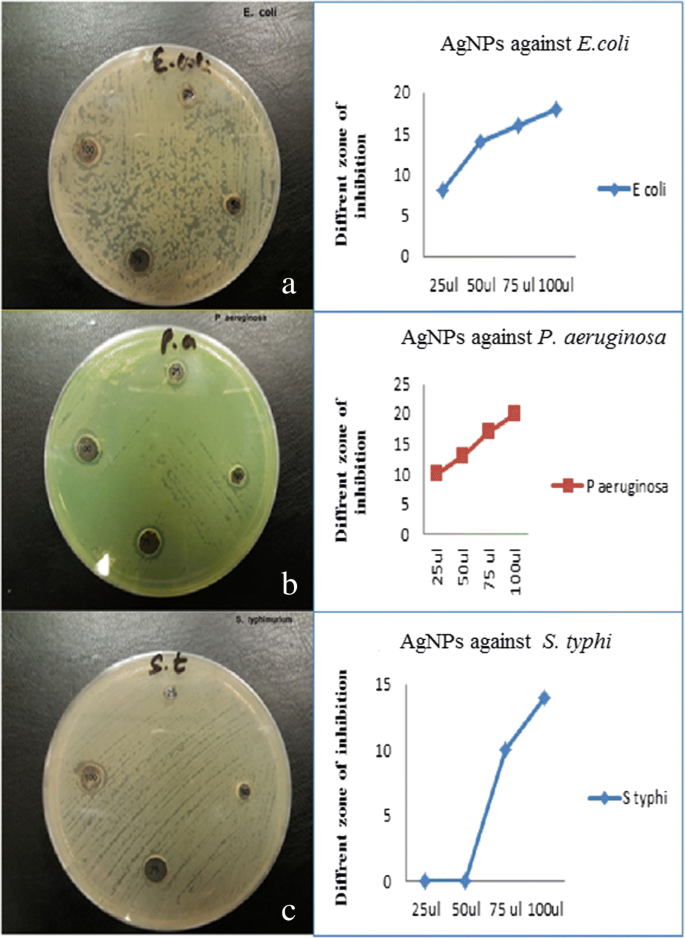
Antimikrobielle Wirkung und Hemmzone von AgNPs gramnegativer Erreger (a –c )
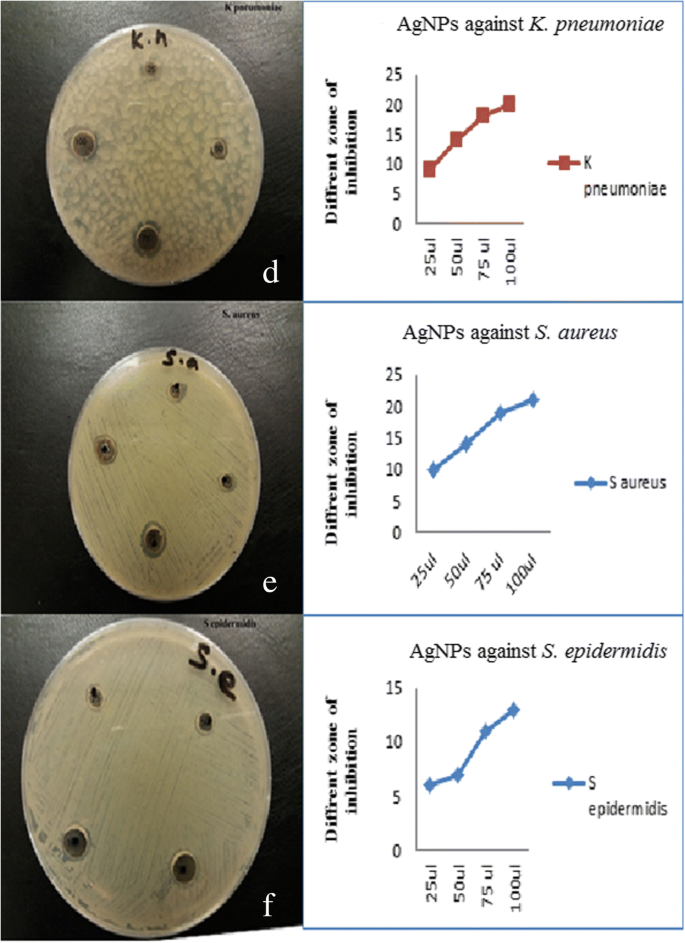
Antimikrobielle Wirkung und Hemmzone von AgNPs grampositiver Erreger (d –f )
Abbildung 8a–c zeigen die antimikrobielle Aktivität synthetisierter AgNPs gegen die grampositiven Erreger K. Lungenentzündung , S. aureus , und S. Epidermidis . Antimikrobielle Aktivität wurde selbst bei niedrigen AgNP-Konzentrationen (25 und 50 μl) für K beobachtet. Lungenentzündung, mit Hemmzonen von 9 bzw. 14 nm und gegen S. aureus , mit Hemmzonen von 6 bzw. 14 nm. Frühere Studien bestätigten auch die Wachstumshemmung von Gram-positiven Bakterien, die mit synthetisierten NPs behandelt wurden [35,36,37,38]. Die nach Exposition mit synthetisierten AgNPs bewertete antibakterielle Aktivität zeigte Hemmzonen im Bereich von 7 bis 21 mm. Abbildung 9 zeigt die Hemmwirkung verschiedener Konzentrationen (25 bis 100 μL) von P. Granatum Schälen von AgNPs auf E. coli , P. aeruginosa , S. Typhi , K. Lungenentzündung , S. aureus , und S. Epidermidis . Selbst bei niedrigen Konzentrationen von AgNPs wurde eine gute antibakterielle Aktivität für alle Mikroben mit Ausnahme von S beobachtet. Typhi , wie bereits berichtet [38].
Um die zytotoxischen Wirkungen von AgNPs zu analysieren, wurde eine Dickdarmkrebszelllinie (RKO:ATCC® CRL-2577™) verwendet. An Tag 3 fanden wir eine Lebensfähigkeit von 56 % bei einer Behandlung mit 12,5 μg und eine Lebensfähigkeit von 61 % an Tag 5. Die insgesamt signifikante Verringerung der Proliferation wurde bei> 12,5 µg beobachtet (Abb. 10a) und war konsistent mit Tag 5. Darüber hinaus bestätigten AO/EtBr-gefärbte Bilder die Proliferationsreduktion durch Visualisierung von Kolonien und Zellzahlen (Abb. 10b). Interessanterweise konnten wir Zellen mit perinukleären zytoplasmatischen Vakuolen bei 12,5 μg beobachten (Abb. 10b, c); dieser Prozess könnte ein Abbauweg in Lysosomen im Prozess der Autophagie sein, um den programmierten Zelltod zu verstärken. Es sind jedoch weitere Studien erforderlich, um die Wirkung von AgNP auf die Autophagiefunktionen zu bestätigen. In unserer vorherigen Studie zu AgNPs, die mit Pimpinella anisum synthetisiert wurden Samen fanden wir auch, dass 12 μg AgNPs für HCT116-Zellen toxisch waren, indem sie entweder Apoptose oder Nekrose verstärkten [12]. Es wurde auch berichtet, dass eine niedrige Konzentration von AgNPs in der Lage ist, Apoptose zu induzieren [39]. Die aktuellen Experimente mit AgNPs synthetisiert mit Punica granatum Schalenextrakt zeigte auch eine Toxizität von 55–62 % mit 12,5 μg. Darüber hinaus zeigte die AO/EtBr-Färbung ein klares Bild des programmierten Zelltods durch Autophagie.
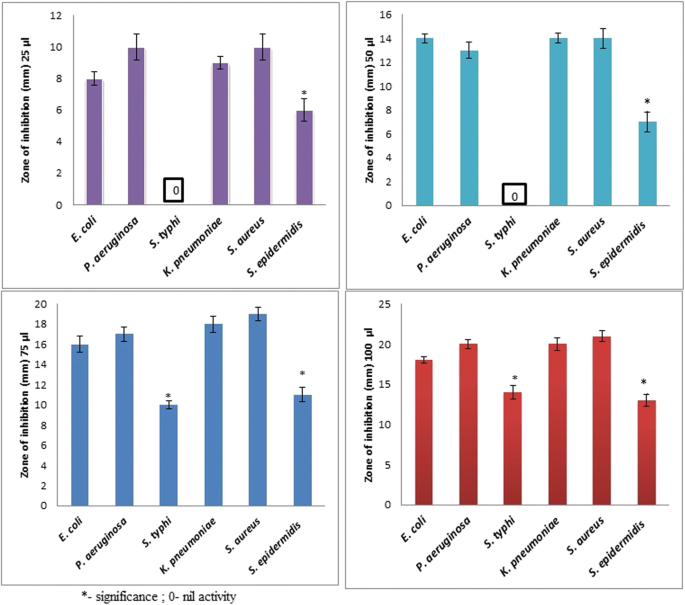
Antimikrobielle Aktivität von AgNPs gegen gramnegative und grampositive Erreger
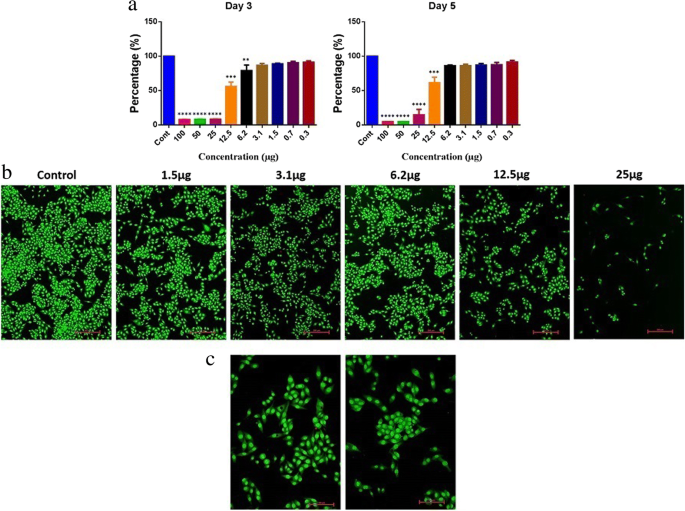
Zytotoxizität von AgNPs. a Zellproliferations- und Lebensfähigkeitsanalyse an RKO-Zellen. Einweg-ANOVA-Mehrfachvergleiche, ***P < 0,0005. b Apoptose/Nekrose-Analyse an RKO-Zellen. c RKO-Zellen, die unterschiedlichen Dosen von AgNPs ausgesetzt waren
Schlussfolgerungen
Das Ergebnis der vorliegenden Studie zeigte, dass Granatapfelschalenextrakt ein gutes Reduktionsmittel zur Synthese von Silbernanopartikeln mit einem Größenbereich von 20–40 nm (durchschnittliche Größe 26,95 nm) ist, eine ideale Voraussetzung für eine effiziente Wirkstoffabgabe und eine erhöhte Bioverfügbarkeit bei a Zielseite. Die antibakterielle Aktivität der synthetisierten AgNPs auf getestete Organismen, selbst bei niedrigen AgNP-Konzentrationen (25–100 μL), bestätigt weiter die antibiotische Wirksamkeit der grün synthetisierten AgNPs für die Entwicklung neuer antibakterieller Wirkstoffe zur Behandlung von Gram-negativen und Gram -positive Erreger. Darüber hinaus fördern die beobachteten zytotoxischen Wirkungen von AgNPs auf Dickdarmkrebszelllinien und die Verringerung der Zellproliferation bei einer Dosis von> 12,5 μg AgNPs als Erstlinienbehandlung für Tumore.
Abkürzungen
- EDX:
-
Energiedispersive Röntgenspektroskopie
- SEM:
-
Rasterelektronenmikroskop
- TEM:
-
Transmissionselektronenmikroskopie
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Biogene Synthese, Charakterisierung und Bewertung des antibakteriellen Potenzials von Kupferoxid-Nanopartikeln gegen Escherichia coli
- Wechselwirkungseffekte beim Zusammenbau magnetischer Nanopartikel
- Herstellung, Charakterisierung und Zytotoxizität von kugelförmigen, konjugierten Gold-Cockle-Shell-abgeleiteten Calciumcarbonat-Nanopartikeln für biomedizinische Anwendungen
- Grüne Kompetenz bei der Synthese und Stabilisierung von Kupfernanopartikeln:katalytische, antibakterielle, zytotoxische und antioxidative Aktivitäten
- Schwerwiegende Grenzflächeneffekte bei CoFe2O4/Fe3O4 und Fe3O4/CoFe2O4 Kern/Schale-Nanopartikeln
- Neueste Fortschritte bei Synthesemethoden und Anwendungen von Silbernanostrukturen
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Evaluierung der antimikrobiellen, apoptotischen und Krebszellen-Genabgabeeigenschaften von proteinbedeckten Goldnanopartikeln, die aus dem essbaren Mykorrhiza-Pilz Tricholoma crassum synthetisiert wur…
- Unterkühlung von Wasser durch Nanopartikel und Ultraschall gesteuert
- Mikrostrukturelle, magnetische und optische Eigenschaften von Pr-dotierten Perowskit-Manganit-La0.67Ca0.33MnO3-Nanopartikeln, die über einen Sol-Gel-Prozess synthetisiert wurden



