Biologisch abbaubare multimodale, tumormikroumgebungsempfindliche Nanopartikel für die gezielte Bildgebung von Brustkrebs
Zusammenfassung
Gasgefüllte Ultraschallkontrastmittel (US) kollabieren leicht im Körper, und das Gas kann leicht überlaufen, was die Wirksamkeit der US-Bildgebung einschränkt. Um dieses Problem anzugehen, wurde ein injizierbares, gaserzeugendes Multimode-System entwickelt, das das MR-negative Kontrastmittel Fe3 . trägt O4 , der Fluoreszenzfarbstoff Cy5.5 und das CO2 freigebender Spender (Na2 CO3 ). Die Nanopartikel können kontinuierlich Kohlendioxid (CO2 ) Gas in saurem Tumorgewebe im Körper, wodurch der Tumor unter Ultraschall ein starkes Echosignal erhält. Darüber hinaus verleihen die Nanopartikel hervorragende Effekte für die MR- und Fluoreszenzbildgebung des Tumorgewebes. Die Ergebnisse zeigen, dass dieses pH-responsive NP-System gute Effekte bei der MR/US/Fluoreszenz-Bildgebung bietet. Diese Studie bietet eine nützliche Referenz für die Multi-Mode-Tumorbildgebung.
Einführung
In der klinischen Praxis werden Mikrobläschen hauptsächlich als Ultraschallkontrastmittel für die Echtzeit-Bildgebung verschiedener Organe und Blutgefäße eingesetzt [1,2,3]. Herkömmliche Ultraschallkontrastmittel bestehen typischerweise aus Materialien wie Lipiden oder Proteinen, die Luft oder Perfluorkohlenstoffgase einschließen. Die in den Mikrokügelchen eingekapselten Gasspezies haben aufgrund der schnellen Diffusion von Mikrobläschendefekten eine geringe Stabilität im Blut und eine kurze Halbwertszeit [4,5,6]. Da darüber hinaus die Partikelgröße der gasgefüllten Mikrobläschen gewöhnlich groß ist (ungefähr 1 bis 8 µm), ist es für die Mikrobläschen schwierig, durch Gewebeextravasation in die Umgebung des Wirtstumors einzudringen. Daher ist die derzeitige Anwendung von mikrometergroßen Blasen in der intravaskulären Bildgebung begrenzt [7]. Ideale Ultraschallkontrastmittel sollten generell eine optimale Größe für den Transport durch den Gewebegefäßraum, eine ausreichende Dauer der akustischen Wirkung, eine gute Targeting und Biokompatibilität sowie eine leichte Ausscheidung aus dem Körper aufweisen [8, 9]. Das Konzept der „gaserzeugenden Nanopartikel“ wurde in früheren Forschungen vorgeschlagen, und solche Nanopartikel haben das Potenzial zur Verwendung in der Ultraschallkontrastbildgebung [10,11,12]. Diese gaserzeugenden Nanopartikel sind den derzeitigen gasgefüllten Mikrobläschen in der Leistung überlegen, und das kontinuierlich erzeugte Gas ermöglicht eine intensive Ultraschallbildgebung. Gaserzeugende Nanopartikel können die Permeation und Retention verbessern, und sie können stabil im Blut zirkulieren und sich effektiv im Tumorgewebe anreichern [13, 14].
Es bleibt eine Herausforderung, winzige und okkulte Tumore durch traditionelle bildgebende Verfahren wie Magnetresonanztomographie (MRT), Computertomographie (CT) und Ultraschall zu erkennen, die durch lange Aufnahmezeiten, hohe Strahlendosis und geringe Empfindlichkeit eingeschränkt sind [15 , 16]. Es ist notwendig, verschiedene bildgebende Verfahren zu integrieren und eine multimodale Bildgebungstechnologie zu entwickeln, um eine integrierte Synergie für die Früherkennung von Krebs zu erzielen [17,18,19]. Superparamagnetisches Eisenoxid (Fe3 .) O4 ) können Nanopartikel als negative MRT-Kontrastmittel in der T2-gewichteten Bildgebung eingesetzt werden [20, 21]. Fe3 O4 hat attraktive Gesamteigenschaften, einschließlich kleiner Partikelgröße, starker Penetration, hoher Magnetisierung, guter Metabolisierung und relativ geringer Toxizität [22, 23]. Fe3 O4 Kontrastmittel für die MRT-Diagnose von Krebs im Frühstadium wurden aufgrund ihrer hohen Relaxation und ihres Kontrasts umfassend untersucht [24,25,26]. Darüber hinaus hat die Echtzeit-Fluoreszenzbildgebung eine hervorragende Auflösung und kann eine wertvolle Methode sein, um das Tumor-Staging zu definieren, die Tumorresektion zu steuern und die Behandlungseffekte zu überwachen [27, 28].
Hierbei werden diese Nanopartikel hauptsächlich von Poly(milchsäure-co-glykol)säure (PLGA) eingekapselt, die von der Food and Drug Administration (FDA) zur Verwendung als biosicheres Material zugelassen wurde [29, 30]. Die PLGA-Partikel werden mit RGD-Peptid modifiziert, um die Bindung an αvβ3-Integrin auf der Oberfläche von Brustkrebszellen und mit Cy5.5 als Fluoreszenzfarbstoff für die in vivo-Bildgebung zu ermöglichen, und sie sind mit Fe3 . verkapselt O4 als T2-negatives Kontrastmittel in der MRT zu wirken (Schema 1a). Aufgrund der hochregulierten Glykolyse im Tumorgewebe, die in der extrazellulären Umgebung mehr Milchsäure und Protonen produzieren könnte, ist der pH-Wert von Tumorgewebe (6,8–7,2) niedriger als der von Normalgewebe (pH 7,4) [31,32,33] . Daher haben wir Natriumcarbonat (Na2 CO3 ) in der PLGA zur Produktion von CO2 Bläschen beim niedrigeren pH-Wert von Tumorgeweben für die Ultraschallbildgebung. Um ihre vielversprechende Anwendung in der Tumorbildgebung zu verifizieren, wurden die umfassenden Eigenschaften dieser Multi-Mode-Nanopartikel für die In-vitro-Bildgebung systematisch charakterisiert, einschließlich ihrer Zytotoxizität, Targeting-Spezifität und Bioverteilung im Tumorgewebe, durch drei Bildgebungsmodi.
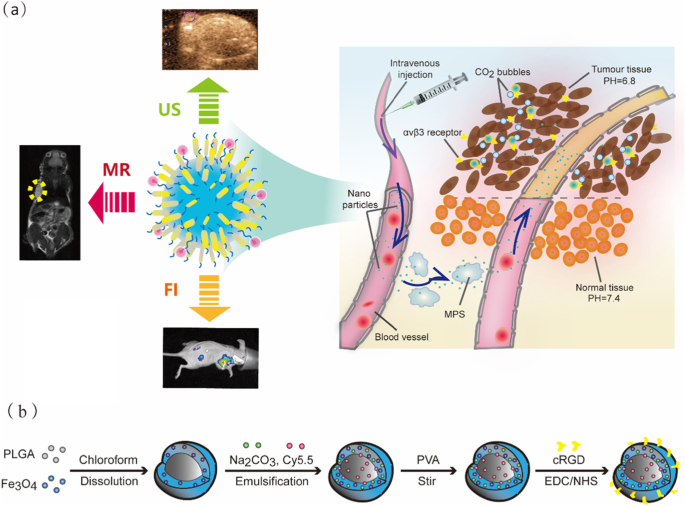
a Schematische Darstellung der Funktion in Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD NPs durch gezielte Akkumulation im Tumor und Erzeugung von CO2 Blasen in saurem Tumorgewebe, gefolgt von einer dreifach-modalen MR/US/FI-Bildgebung von Brustkrebs. b Schematische Darstellung der Herstellung des Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs.
Ergebnisse und Diskussion
Synthese und Charakterisierung von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs
Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs wurden als auf RGD ausgerichtete Multimode-Kontrastmittel entwickelt, indem ein biokompatibles Polymer von PLGA mit Fe3 . eingekapselt wurde O4 und Na2 CO3 und ein auf Integrin gerichteter Wirkstoff über eine biologisch abbaubare chemische Bindung (Schema 1b).
Transmissionselektronenmikroskopische Aufnahmen zeigten, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs waren klare Kugeln mit gleichmäßig verteilten Eisenoxidpartikeln, die in der Schale sichtbar waren (Abb. 1a). Die durchschnittliche hydrodynamische Größe der NPs wurde durch dynamische Lichtstreuung mit 117,6 nm gemessen, und der durchschnittliche Polydispersitätsindex betrug 0,234 (Abb. 1b). Die Oberflächenladung der NPs wurde durch Messungen des Zetapotentials mit −21.7 mV bestätigt (Abb. 1c). Die Messung des Fluoreszenzspektrums ergab, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD hatte die maximale Emissionswellenlänge bei 685 nm, was darauf hindeutet, dass Cy5.5 erfolgreich in den PLGA-Kern eingekapselt wurde (Abb. 1d). Die Sättigungsmagnetisierungswerte für Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD und freies Fe3 O4 Die NPs betrugen 32,6 bzw. 42,5 µEmu/g (Abb. 1e). Diese Ergebnisse zeigten die superparamagnetische Eigenschaft der Nanopartikel bei Raumtemperatur. Das FITR-Spektrum von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD zeigte, dass die N-H-Streckschwingung und der –OH-Absorptionspeak bei 3432 cm −1 . auftraten . Außerdem fanden wir eine Verbesserung (1628 cm −1 ) der C =O-Streckschwingung. Im Vergleich zu den nicht-zielgerichteten NPs ist der charakteristische Peak (das Carboxyl) bei 1735 cm −1 der anvisierten NPs wurde deutlich reduziert. Die Ergebnisse zeigten die Bindung zwischen der Carboxylgruppe an der Mikrokugeloberfläche und der Aminogruppe am RGD-Peptid. In-vitro-Bindung von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs ist in Abb. 1f dargestellt.
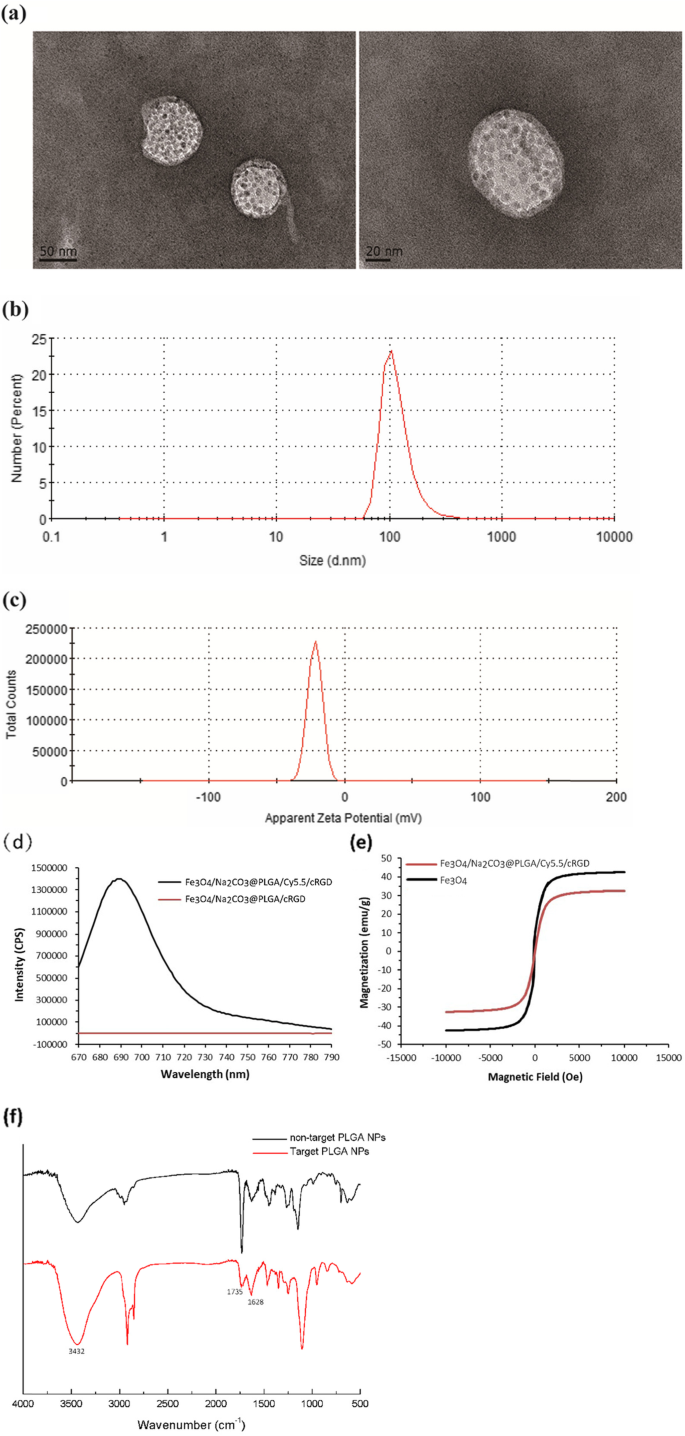
TEM-Bilder (a ) Größenverteilungen (b ) Zetapotential (c ) von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs. d Fluoreszenzemissionsspektrum von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD und Fe3 O4 /Na2 CO3 @PLGA/cRGD-NPs. e Magnetische Hysteresekurven von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD NPs und Fe3 O4 NPs. f Die FTIR der Spektren von gezieltem Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD und nicht zielgerichtete PLGA-NPs
In-vitro-Bindung von Na2CO3/Fe3O4@PLGA/Cy5.5/RGD-NPs
αvβ3-Integrin wird im Allgemeinen auf Endothelzellen von Brustkrebstumoren stark exprimiert und kann Tumormetastasen fördern [33,34,35,36]. Die zelluläre Immunfluoreszenz für die Expression von αv-Integrin in MDA-MB-231-Zellen war viel höher als die in MCF-7-Zellen; A549-Zellen dienten als positive Kontrollen (Fig. 2a). Die zelluläre Aufnahme von NPs wurde durch CLSM untersucht (Abb. 2b). Die Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs zeigten eine viel höhere Bindungsrate an MD-MB-231-Zellen als nicht zielgerichtete NPs. Die Fluoreszenzbilder zeigten auch, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs banden an das Zellzytoplasma und zusammengeführte Bilder zeigten die gleichen Stellen wie die Expression von αv-Integrin [37, 38].
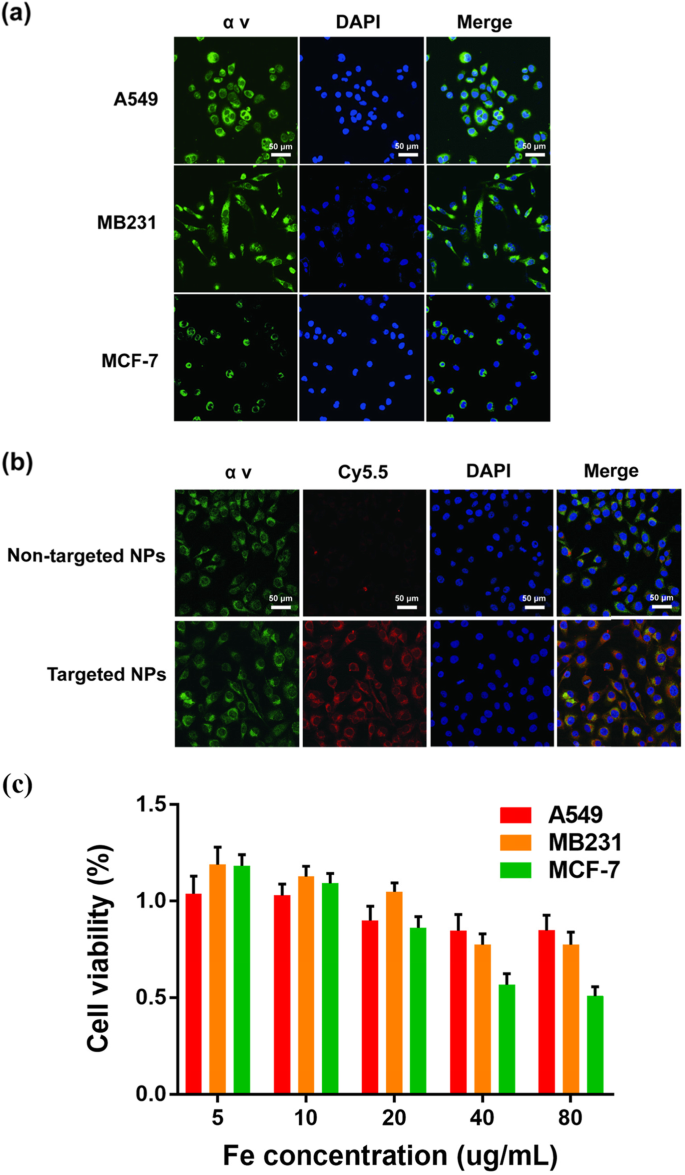
a Konfokale Fluoreszenzbilder mit der Expression von αv-Integrin auf MB231-, A549- und Mcf-7-Zellen. Blau und Grün repräsentieren DAPI- bzw. αv-Fluoreszenz. b Konfokale Fluoreszenzbilder von MB231-Zellen, die mit gezieltem Fe3 . inkubiert wurden O4 /Na2 CO3 @PLGA/Cy5.5/cRGD NPs und nicht zielgerichtete NPs. Blau, Rot und Grün repräsentieren DAPI, Cy5.5 bzw. α v Fluoreszenz. c Relative Lebensfähigkeit von MB231-Zellen, die mit unterschiedlichen Konzentrationen von Fe3 . inkubiert wurden O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs
Zytotoxizitätstest
Die In-vitro-Zytotoxizität von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs wurden in MDA-MB-231-Zellen unter Verwendung eines CCK8-Assays abgeschätzt, während mit NPs behandelte A549- und MCF-7-Zellen als Kontrollen verwendet wurden (Fig. 2c). Im Bereich der Fe-Konzentrationen von 5–80 µg/ml war die Zelllebensfähigkeit von A549- und MB231-Zellen nicht signifikant reduziert und lagen beide über 70 %. Im Gegensatz dazu zeigten MCF-7-Zellen bei Fe-Konzentrationen von mehr als 40 µg/ml eine signifikante Abnahme der Zelllebensfähigkeit auf etwa 50 %. Die CCK8-Ergebnisse zeigten, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs zeigten eine signifikant geringere Zytotoxizität in MDA-MB-231-Zellen über einen bestimmten Konzentrationsbereich.
In-vitro-Kontrastbildgebung
Wir haben ein Agargel-Phantom verwendet, um die Leistung von Na2 . zu untersuchen CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs in vitro bei verschiedenen pH-Werten (Abb. 3a). Die Ultraschallkontrastbilder von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs wurden bei schwach saurem pH (pH 6.8) im Vergleich zu pH 7,2 signifikant erhöht, wahrscheinlich weil pH 7,2 nicht genug CO2 . produziert Blasen für die Ultraschallbildgebung. Wenn sich die NPs dagegen in einer schwach sauren Umgebung befanden, konnten genügend Blasen für die Ultraschallbildgebung erzeugt werden. Diese Eigenschaft ist für Tumore relevant, die in vivo eine hohe Gewebeheterogenität und unterschiedliche pH-Werte (pH 6,8–7,2) aufweisen [32, 39, 40]. Anschließend wurde die Signalintensität des Ultraschallbildes analysiert (Abb. 3b). Die Signalintensitätsverhältnisse der Gruppen nicht zielgerichteter NP (pH =7), nicht zielgerichteter NP (PH =5), zielgerichteter NP (PH =7) und zielgerichteter NP (PH =5) im Verhältnis zur Signalintensität der Blankogruppe betrug 112 %, 145 %, 167 % bzw. 178 ± 4 %, was eindeutig darauf hindeutet, dass die NP-Zielgruppe (PH =5) das stärkste US-Signal aufwies.
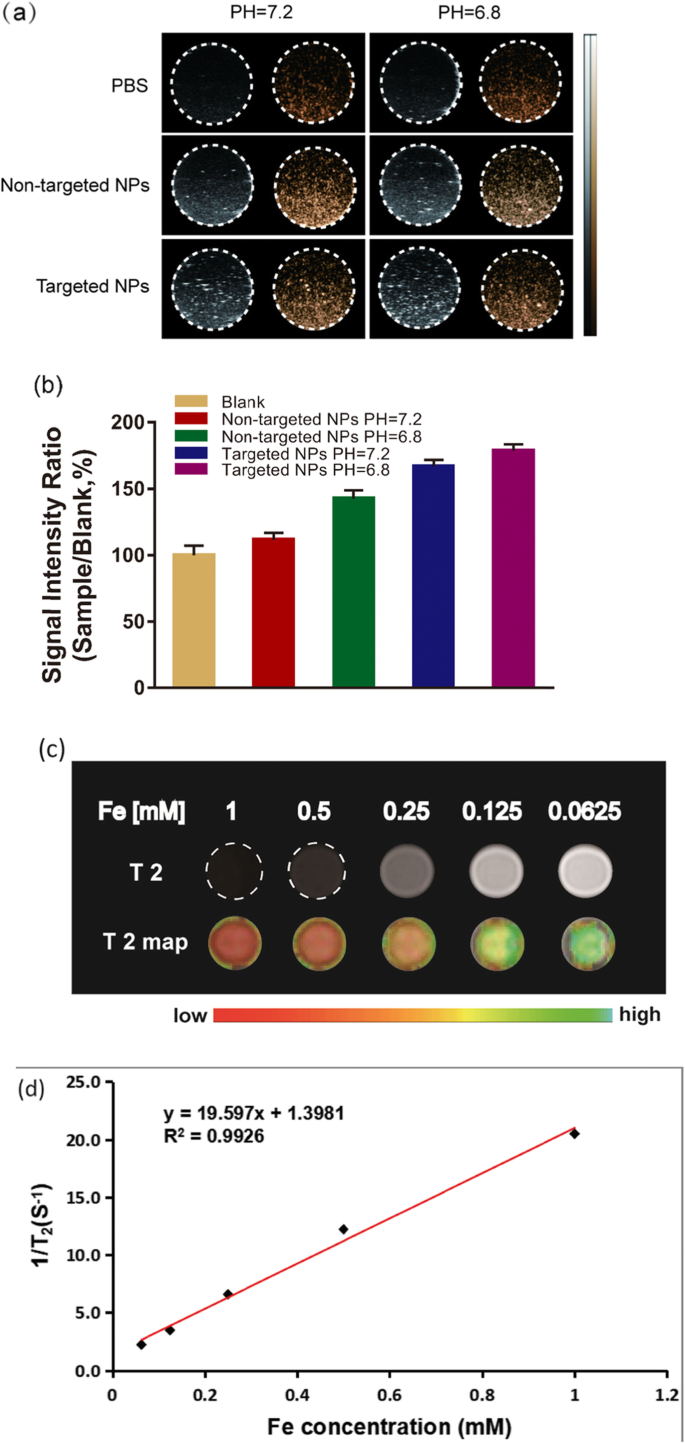
a Ultraschallbilder der gezielten NPs und der nicht gezielten NPs, aufgenommen bei verschiedenen pH-Werten (7,2 und 6,8), PBS als Kontrolle. b Die Signalintensitätsrate wird durch Sample/Blank berechnet, Sample repräsentiert die Echointensität der anvisierten und nicht anvisierten NPs und leer repräsentiert die Echointensität von PBS. c T2-gewichtete MR-Bilder von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs mit unterschiedlichen Fe-Konzentrationen (0,0625, 0,125, 0,25, 0,5 und 1 mM). d Die transversalen Relativitäten (r2) waren 19.597 mM −1 s −1 für Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs
Für die MRT-Studie in vitro, da die Konzentration von Fe im Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs stiegen an, die T2-gewichtete Signalintensität zeigte eine signifikante Abnahme, was auf die Möglichkeit dieser NPs als T2-MR-Kontrastmittel hinweist (Abb. 3c). Die transversale Relaxationsrate (r2) von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs wurden mit 19.597 mM −1 . berechnet s −1 . Obwohl die transversale Relaxationsrate (r2) von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs ist niedriger als die vieler anderer superparamagnetischer MRT-Mittel, die Zusammensetzung von Fe3 O4 kann das r2 erhöhen, das 2,94-mal höher war als das r2 von klinisch verwendeten SPIO-Partikeln.
Ultraschall-Kontrastbildgebung von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs
Um das Potenzial von Na2 . zu demonstrieren CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs für die Ultraschallbildgebung bei Tumoren haben wir eine Injektion von Na2 . in die Schwanzvene verabreicht CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs an Brustkrebs-Xenotransplantat-Nacktmäusen und überwachten die Ultraschallbilder als Funktion der Zeit (Fig. 4a). Vor der Injektion wurden Bilder des Tumors, der Leber und des subkutanen Bereichs aufgenommen. Unmittelbar nach der Injektion zeigte der Bereich des Tumorgewebes keine Kontrastverstärkung. Eine Vergrößerung des Tumorbereichs wurde 30 min nach der Injektion beobachtet und dauerte 90 min an. Die In-vivo-Ultraschallergebnisse zeigten, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/ RGD-NPs erzeugten genügend Blasen in saurem Tumorgewebe, um ein echogenes Reflexionsvermögen für die Ultraschallbildgebung zu erzeugen. Als Kontrolle erhielten wir auch Bilder der Leber und des subkutanen Gewebes zu verschiedenen Zeitpunkten nach der Injektion der gezielten NPs. Während des gesamten Beobachtungszeitraums wurde im subkutanen Injektionsbereich kein signifikantes Enhancement gefunden, und das mit der Zeit abnehmende Enhancement in der Leber war signifikant geringer als bei den Tumoren (Abb. 4b). Dieses Ergebnis zeigt an, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs, die bei physiologischem pH-Wert im Körper zirkulieren, produzieren keine nennenswerte Menge CO2 Blasen zur Kontrastverstärkung durch Ultraschall.
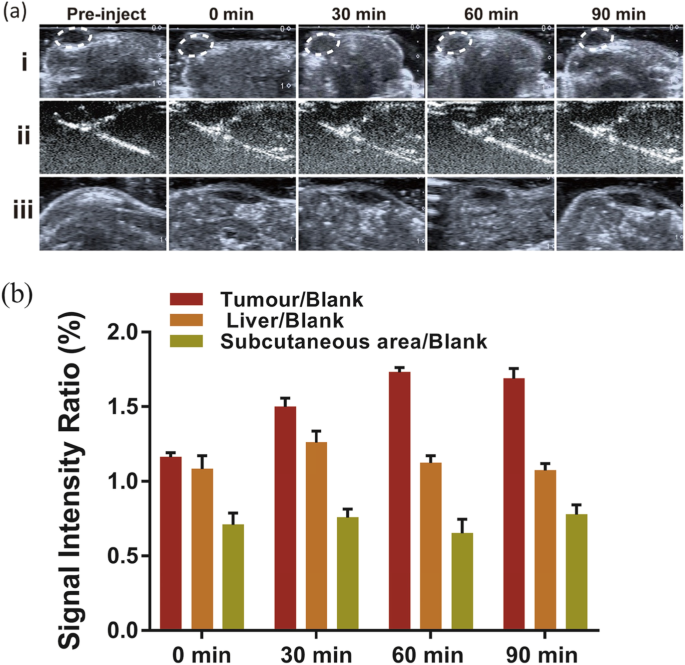
a In-vivo-Ultraschallbildgebung von Tumoren, Lebern und subkutanen Bereichen zu verschiedenen Zeitpunkten nach der Injektion von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs. b Die Echointensitätsrate als Funktion der Zeit wird nach Gewebe/Blindwert berechnet, Gewebe repräsentiert die Echointensität des Tumors, der Leber oder des subkutanen Bereichs, Leerwert repräsentiert die Echointensität vor der Injektion
MRT von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs
Für die In-vivo-MRT, um zu zeigen, dass NPs für die tumorspezifische Bildgebung verwendet werden können, Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs wurden direkt in Tumoren und Muskeln injiziert. Die Ergebnisse zeigten, dass der Tumorbereich nach Injektion der gezielten NPs eine signifikante Abnahme des T2-MR-Kontrasts aufwies und die Signalintensität signifikant von 8875 bei 0 min auf 5972 bei 120 min nach der Injektion abnahm (Abb. 5a, b). Bei gleicher Menge an injizierten Nanopartikeln zeigte der subkutane Muskelbereich jedoch eine viel geringere T2-Signalabnahme. Dieser Befund zeigt die Wirksamkeit von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs mit hypersensitiven Integrin-zielgerichteten T2-MR-Kontrastmitteln zur Verwendung in der tumorgerichteten Bildgebung. In der Gruppe mit Schwanzveneninjektion zeigte die T2-MR-Bildgebung auch eine deutliche Abnahme des Kontrasts im Tumor 24 Stunden nach der Injektion, was die hohe Tumorakkumulation von Na2 . belegt CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs (Abb. 5c, d). Darüber hinaus wurden verringerte T2-Signale in Leber und Nieren beobachtet, was darauf hindeutet, dass die Eisenionen in den NPs schnell aus dem Körper eliminiert werden konnten. Daher ergab die MRT, dass das mit PLGA umhüllte Fe3 O4 Nanopartikel zeigten ein effizientes passives Tumor-Targeting über den verbesserten Permeabilitäts- und Retentionseffekt (EPR), insbesondere das RGD-vermittelte Targeting, konnten jedoch in vivo abgebaut und schnell ausgeschieden werden.
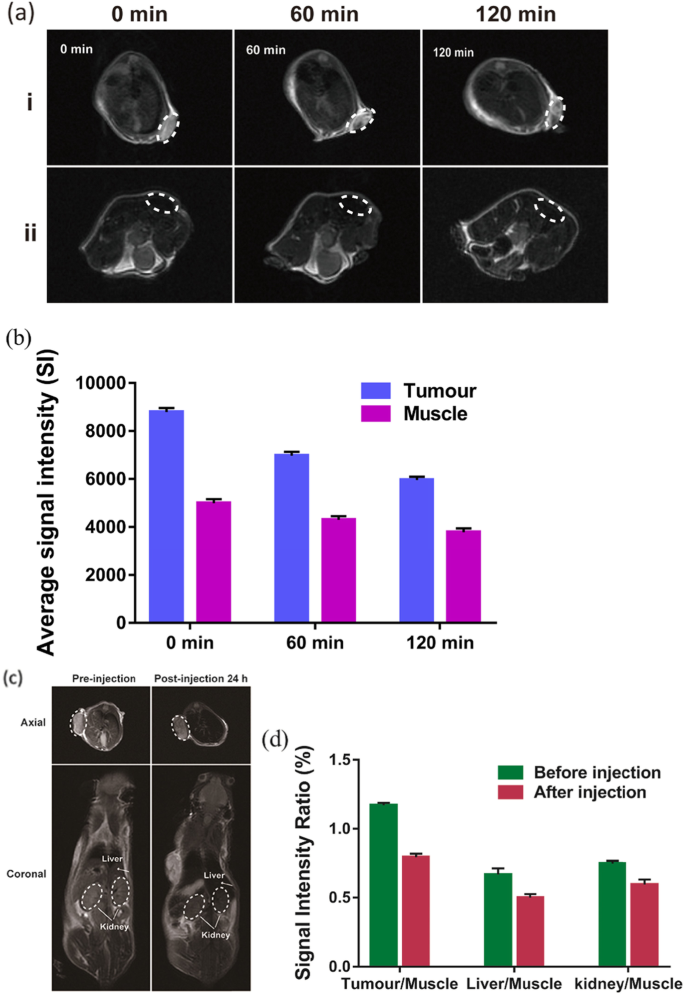
a In-vivo-T2-MR-Bilder von normalem und tumorösem subkutanem Gewebe vor und nach der Injektion von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs. b Durchschnittliche Signalintensität in Muskel und Tumor für die Injektion von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs. c T2-MR-Bilder von axialen und koronalen MDA-MB-231-Tumor-tragenden Mäusen vor und nach intravenöser Injektion von Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD-NPs. d Das Signalintensitätsverhältnis wird nach Gewebe/Muskel berechnet, Gewebe steht für die Signalintensität von Tumor, Leber und Niere vor und nach Injektion der gezielten NPs, Muskel steht gleichzeitig für die Signalintensität des Muskels
Fluoreszenzbildgebung und Histologie
Zweihundert Mikroliter NPs wurden Mäusen für die In-vivo-Fluoreszenzbildgebung intravenös injiziert. In der Gruppe, der RGD-gerichtete NPs injiziert wurden, nahm das Fluoreszenzsignal von Cy5.5 im Tumorbereich allmählich zu und erreichte 4 Stunden nach der Injektion einen Höhepunkt, was darauf hindeutet, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs können sich effektiv im Tumor anreichern. In der nicht zielgerichteten Gruppe wurden die NPs nach der Injektion im ganzen Körper verteilt und schnell abgebaut, und sie reicherten sich über einen langen Zeitraum nicht im Tumor an ( 6a ). Die Mäuse wurden dann seziert, und die wichtigsten Organe und Tumoren wurden für die in vitro-Fluoreszenzbildgebung gesammelt, die eine hohe Tumoraufnahme der angezielten NPs zeigte ( 6b , c). Die Fluoreszenzintensität von Cy5.5 in den Tumoren von Mäusen, denen gezielte NPs injiziert wurden, war 1,5-mal höher als bei Mäusen, denen nicht gezielte NPs injiziert wurden.
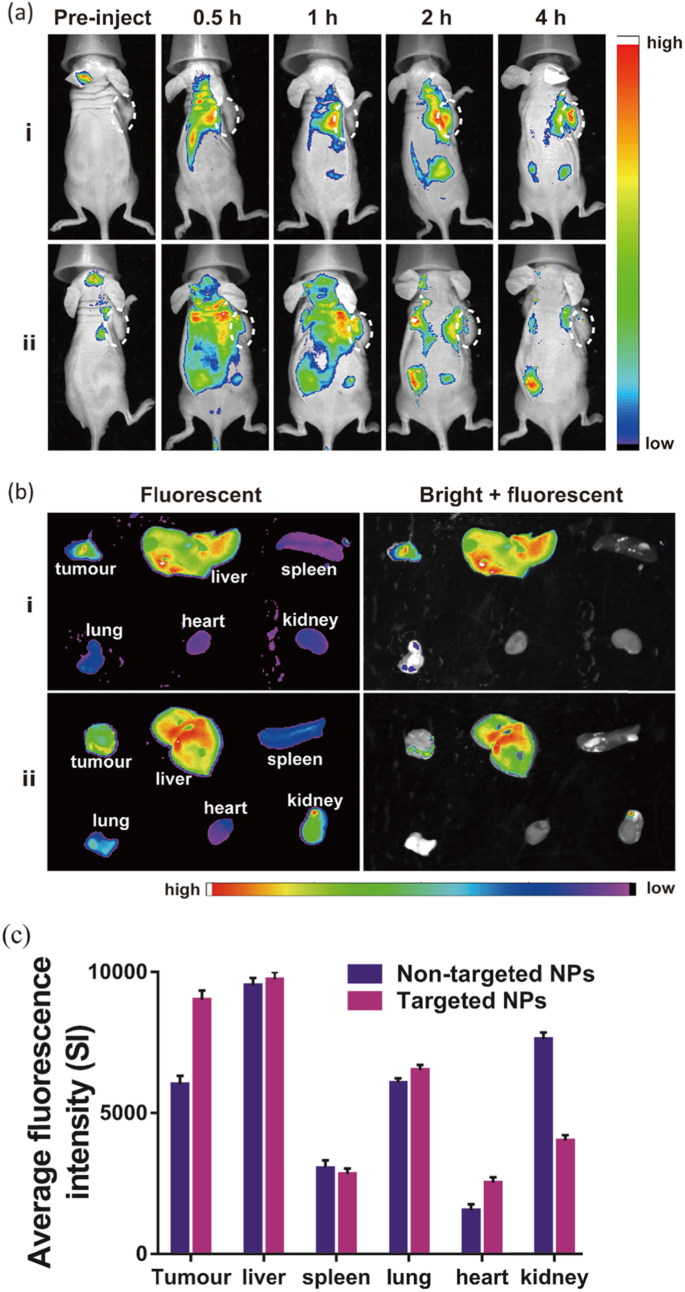
a In-vivo-Fluoreszenz-Fluoreszenz-Bildgebung von Tieren 0, 0,5, 1, 2 und 3 h nach der Injektion nach Injektion von gezielten und nicht-zielgerichteten NPs. b Ex-vivo-Fluoreszenzbilder von Tumoren und wichtigen Organen (Leber, Milz, Lunge, Herz und Niere) von Tieren. c Gemittelte Fluoreszenzintensität verschiedener Organe und Tumore
Darüber hinaus tumorspezifisches Targeting von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs wurden durch Gewebefluoreszenz-Bildgebung von gefrorenen Tumorschnitten verifiziert (Abb. 7a). Immunfluoreszenzfärbung von Tumorschnitten mit Antikörpern gegen αv- und β3-Integrin zeigte eine signifikante Expression von αvβ3-Integrin in Tumorgeweben. Die Fluoreszenz von αv- und β3-Integrin wurde mit der Cy5.5-Fluoreszenz von Na2 . zusammengeführt CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs, um ein Immunfärbungsbild zu erhalten, das eine Kolokalisation zeigt. Die Immunfluoreszenzergebnisse im Tumorgewebe zeigten, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs binden spezifisch an αvβ3-Integrin bei bösartigem MB231-Brustkrebs. Darüber hinaus ist die H&E-Färbung von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs im Vergleich mit der nicht anvisierten Gruppe zeigten, dass alle Organgewebeschnitte eine normale pathologische Morphologie und keine histopathologische Schadensantwort aufwiesen ( 7b ). Alle Ergebnisse der obigen Zytotoxizität und histologischen Analyse zeigten, dass Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs induzierten in vivo keine signifikante Toxizität für wichtige Organgewebe und ihre gute Biokompatibilität kann vernünftigerweise PLGA zugeschrieben werden.
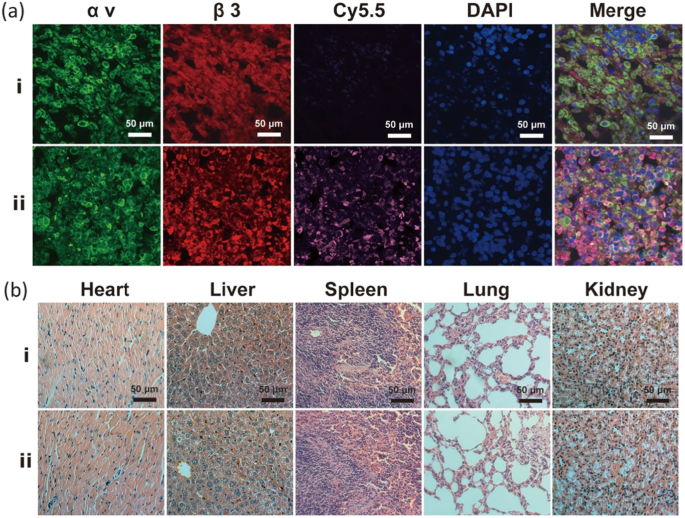
a Fluoreszenzbildgebung von MDA-MB-231-Tumor-gefrorenen Schnitten von Mäusen, denen gezielte und nicht gezielte NPs injiziert wurden. Grün, Rot, Violett und Blau stehen für αv-, β3-, Cy5.5- bzw. DAPI-Fluoreszenz. b H&E-gefärbte Tumorschnitte von Mäusen nach Injektion von gezielten und nicht gezielten NPs
Schlussfolgerungen
Zusammenfassend zeigen die obigen Ergebnisse einen kreativen und erfolgreichen Ansatz für die MRT von Brustkrebs durch ein magnetisches Targeting und ein gaserzeugendes System, das in der Tumormikroumgebung aktiviert wird. Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs weisen eine hervorragende Bildgebungsleistung und gute Biokompatibilität in MR-/Ultraschall-/Fluoreszenz-Bildgebungsmodi auf. Unsere Arbeit zeigt das große Potenzial für die Tumordiagnose mit verbesserter multimodaler Bildgebung.
Materialien und Methoden
Materialien
Poly(milchsäure-co-glycolsäure) (PLGA) (Lactid:Glycolid =75:25, Mw =20.000), Cyanine5.5-Farbstoff und Polyvinylalkohol (PVA) wurden von Sigma-Aldrich Company (Shanghai, China) bezogen. Das RGD-Peptid wurde von GenicBio BioTech Co. Ltd. (Shanghai, China) kundenspezifisch synthetisiert. Fe3 O4 Nanopartikel und Natriumcarbonat (Na2 CO3 ) wurden von Xian Ruixi Biological Technology Co. Ltd. (Henan, China) bezogen. Dichlormethan (CH2 Kl2 ) und Dimethylsulfoxid (DMSO) wurden von Solarbio Company (Beijing, China) bezogen. Alle Chemikalien waren von analytischer Qualität.
Synthese von Fe3O4/Na2CO3@PLGA/Cy5.5/cRGD-Nanopartikeln
Zuerst wurden 12,5 mg PLGA und 0,25 ml Chloroform zusammengemischt. Dann 5 μL Cy5.5, 15 μL Ölsäure-modifizierte magnetische Nanopartikel, dispergiert in Chloroform (OA@Fe3 O4 , 10 mg/ml), 5 μL Natriumcarbonat (Na2 CO3 ) und 1,5 ml einer 1%igen PVA-Lösung wurden nacheinander zugegeben und mit einem Ultraschallprozessor 2 Minuten lang emulgiert. Dann wurden 12,5 ml 0,3% PVA-Lösung zugegeben und 3-4 Stunden bei Raumtemperatur gerührt, und 12,5 ml 0,4% PVA-Lösung wurden zum Rühren (500 U/min/min) über Nacht zugegeben, um restliches organisches Lösungsmittel zu entfernen. Die obige Lösung wurde mehreren Ultrafiltrationswäschen mit ddH2 . unterzogen 0 und dann mit PB-Puffer (pH =7,4) auf ein Endvolumen von 1,25 ml verdünnt. Als nächstes wurden 0,25 mg EDC und 1,25 mg NHS zu der obigen gemischten Lösung gegeben. Die Mischung wurde 30 min bei 25 °C gerührt und dann dreimal mit Ultrafiltration gewaschen und in PB-Pufferlösung (pH =7,4) resuspendiert. Als nächstes wurden 1,25 mg cRGD zu der Lösung gegeben und über Nacht bei 4 °C gerührt. Um EDC, NHS und jegliches restliche cRGD zu entfernen, wurde die transparente Lösung durch ein Ultrafiltrationsröhrchen filtriert. Schließlich Fe3 O4 /Na2 CO3 @PLGA/Cy5.5/cRGD NPs wurden in 1,25 ml entionisiertem Wasser resuspendiert und bei 4 °C gelagert.
Nanopartikelcharakterisierung
Die dynamischen Durchmesser und das Zetapotential von Nanopartikeln wurden mit einem Zetasizer Nano-ZS (Malvern Instruments, UK) gemessen. Die Morphologie der Nanopartikel wurde unter Verwendung eines FEI Tecnai F20 Transmissionselektronenmikroskops erhalten. Die Cy5.5-Beladung wurde mit einem Hitachi F-7000-Fluoreszenzspektrometer aufgezeichnet. FTIR wurde unter Verwendung eines Fourier-Transformations-Infrarotspektrometers (Alpha II, Bruker, Schweiz) durchgeführt. Ein Vibrationsprobenmagnetometer (VSM, Lake Shore 7410) wurde verwendet, um die Hysteresekurve der Nanopartikel und des freien Fe3 . zu bestimmen O4 .
Zellen und Tiere
Humane Brustkrebs-MDA-MB-231-Zellen wurden freundlicherweise von der Stammzellbank der Chinesischen Akademie der Wissenschaften zur Verfügung gestellt. Die Zellen wurden bei 37 °C in 95 % Luft und 5 % CO2 . gehalten . Weibliche BALB/c-Mäuse (4 Wochen) wurden von Shanghai Slaccas Laboratory Animal Co. Ltd. gekauft und gemäß Protokollen gehalten, die vom Labortierzentrum der Guangxi Medical University genehmigt wurden. Auf Tierversuche folgte der Leitfaden für die Pflege und Verwendung von Labortieren, der von der Ethikkommission für Tiere des Labortierzentrums der Medizinischen Universität Guangxi herausgegeben wurde. MDA-MB-231-Brustkrebszellen wurden in die rechte Flanke von BALB/c-Mäusen (2 × 106 in 200 µl Zellen pro Maus) transplantiert und vor der Bildgebung 10–14 Tage (mittlerer Durchmesser 5 mm) wachsen gelassen.
Zellulärer Ausdruck von αv-Integrin
Zelluläre Immunfluoreszenz wurde durchgeführt, um die hohe Expression von αv-Integrin in MDA-MB-231-Zellen zu bestätigen. Als Kontrollen wurden A549- und MCF-7-Zellen verwendet. Die Zellen wurden auf 35-mm-Kulturschalen mit Glasboden (MatTek, USA) bei 2 × 10 4 . ausgesät Zellen ml −1 für 24 h. Nach der Inkubation wurden die Zellen 20 min bei Raumtemperatur mit 4% Paraformaldehyd fixiert. Dann wurden sie mit monoklonalem Kaninchen-Anti-Integrin-αv-Antikörper (ab179475, Abcam) bei 4°C über Nacht und Anti-Kaninchen-IgG-Antikörper für 1 Stunde bei Raumtemperatur inkubiert. Schließlich wurden die Zellen mit DAPI gefärbt. Die Bilder wurden durch konfokale Laser-Scanning-Mikroskopie (TCS SP8, Leica, Deutschland) aufgenommen.
Um die zielgerichtete Wirksamkeit der Nanopartikel zu beurteilen, wurde eine zelluläre Aufnahmestudie mit konfokaler Laser-Scanning-Mikroskopie (CLSM) durchgeführt. Die Zellen wurden auf 35-mm-Kulturschalen mit Glasboden (MatTek, USA) bei 2 × 10 4 . ausgesät Zellen ml −1 für 24 h. Dann wurden die Zellen mit auf RGD gerichteten NPs (30 μg mL −1 , 0,5 ml) bei pH 7,4 für 2 Stunden, und nicht-zielgerichtete NPs wurden als Kontrollen verwendet. Nach der Inkubation wurden die Zellen mit 4% Paraformaldehyd für 20 min fixiert und dann mit αv-Antikörper inkubiert. Mittels Kolokalisation haben wir die gezielte Bindung der Nanopartikel an das Integrin auf den Zellen nachgewiesen.
CCK8-Assay
Die Biokompatibilität von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-Nanopartikel wurde durch eine Zytotoxizitätsstudie bewertet. MDA-MB-231-, A549- und MCF-7-Zellen wurden auf 96-Well-Platten bei 5 × 10 3 . ausgesät Zellen ml −1 für 24 h. Dann 0,1 ml Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NP-Suspension mit Fe-Konzentrationen von 5, 10, 20, 40 und 80 µg/ml wurde in jede Vertiefung gegeben und für 24 Stunden inkubiert. Schließlich wurden 10 µl CCK8-Lösung zugegeben und die Suspension für eine weitere Stunde inkubiert. Die Ergebnisse wurden mit einem Mikroplatten-Lesegerät (Thermo Scientific, USA) bei 450 nm bestimmt.
Kontrastverstärkte Ultraschallbildgebung
Die Ultraschallbildgebung von Nanopartikeln wurde unter Verwendung eines Ultraschallsystems Vevo 2100 (Fujifilm Visual Sonics Inc., Kanada) durchgeführt. Die auf RGD gerichteten und nicht gerichteten NPs wurden dem Agarose-Modell hinzugefügt und PBS wurde als Kontrolle verwendet. Die Bilder wurden im B-Modus und CEUS-Modus mit unterschiedlichen pH-Puffern von 7,2 und 6,8 aufgenommen. Der interessierende Bereich wurde gezeichnet und der durchschnittliche Grauwert wurde in B-Modus-Bildern gemessen.
Für die in-vivo-Ultraschallbildgebung wurden Mäuse mit 2% Isofluran (Hebei Yipin Pharmaceutical Co., Ltd., China) anästhesiert und die Körpertemperatur wurde mit einem Heizkissen bei 37 °C gehalten. Über die Schwanzvene wurden insgesamt 200 µl RGD-gerichteter NPs injiziert. Kontrolltiere erhielten eine subkutane Injektion mit der gleichen Menge an NPs. Ultraschallbilder wurden unter Verwendung eines 7-MHz-Wandlers aufgezeichnet, um kontinuierlich Ultraschallbilder von Tumoren, Lebern und subkutanen Bereichen zu erfassen. Die akustische Fokuszone wurde in der Mitte des Tumors mit dem größten Querschnitt platziert, und es wurde ein Sichtfeld erhalten, das den Tumor und sein angrenzendes Gewebe enthielt.
Magnetresonanztomographie
MRT-Untersuchungen von Na2 CO3 /Fe3 O4 @PLGA/Cy5.5/RGD NPs wurden unter Verwendung eines 3.0 T MR (GE Healthcare, USA) und einer Tierspule (RF TECH LIMITED, China) durchgeführt. NPs mit unterschiedlichen Fe-Konzentrationen von 0,031, 0,063, 0,125, 0,25, 0,5 und 1 µM wurden in 1 µl Eppendorf-Röhrchen gescannt, und PBS wurde als Kontrolle verwendet. Eine T2-MRT wurde für jedes Röhrchen unter Verwendung einer T2-gewichteten FSE-Sequenz (Schichtdicke von 3 mm, TR/TE 2000/74,4 ms, 8 × 8 cm FOV und 320 × 256 Matrix) durchgeführt. Die Relaxivitäten (r2) wurden durch eine lineare Anpassung der inversen Relaxationszeit als Funktion der Fe-Konzentration berechnet.
Für die In-vivo-MRT wurden Mäuse nach dem Zufallsprinzip in zwei Gruppen (n =3) für MR-Scans, die entweder (1) lokale Injektion von Na2 . erhielten CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs in subkutanem Muskel- und Tumorgewebe oder (2) Injektion von Na2 . in die Schwanzvene CO3 /Fe3 O4 @PLGA/Cy5.5/RGD-NPs. Grundlinienbilder der Mäuse wurden vor der Injektion der Nanopartikel aufgenommen. Für Gruppe eins wurde die gleiche Menge an NPs in das subkutane Gewebe und das Tumorgewebe injiziert, und alle 30 min wurde eine MRT-Untersuchung durchgeführt, um den Signalübergang der Gewebe aufzuzeichnen. Für Gruppe zwei wurde die Tumorbildgebung in axialer und koronaler Position durchgeführt, und die MR-Parameter waren die gleichen wie für die in-vitro-Bildgebung. Die Signalintensität (SI) in der Region of Interest (ROI) wurde gemessen und zu verschiedenen Zeiten vor und nach der Injektion mit Gewebesignalen verglichen.
Tumorfluoreszenzbildgebung
Für die Fluoreszenzbildgebung in vivo wurde ein in vivo-Fluoreszenzbildgebungssystem (FX PRO, Bruker, Schweiz) zum Scannen verwendet, und die Mäuse wurden zufällig in zwei Gruppen (n =3):(1) auf RGD gerichtete NPs und (2) nicht gezielte NPs. Bilder wurden alle 30 min für einen Zeitraum von 4 h nach der Injektion aufgenommen. Anschließend wurden wichtige Organe und Tumoren entnommen und abgebildet sowie die Fluoreszenzverteilung in den Körperorganen beobachtet. Die quantitative Analyse der Fluoreszenzintensität wurde unter Verwendung einer Software für molekulare Bildgebung (Bruker, Schweiz) durchgeführt. Diese wichtigen Organe wurden dann einer H&E-Färbung unterzogen, um die Gewebetoxizität zu bewerten. Frozen tumour sections were also subjected to fluorescence immunostaining with antibodies against αv integrin and β3 integrin.
Verfügbarkeit von Daten und Materialien
Die Schlussfolgerungen in diesem Manuskript basieren auf den Daten, die alle in diesem Papier präsentiert und gezeigt werden.
Abkürzungen
- Cy5.5:
-
Sulfo-Cyanine5.5 NHS ester
- DAPI:
-
4′,6-diamidino-2-phenylindole
- EDC:
-
1-Ethyl-3-(3-dimethylaminopropyl)carbodiimid-Hydrochlorid
- FSE:
-
Fast spin echo
- MR:
-
Magnetic resonance
- NHS:
-
N-Hydroxysuccinimid
- PB:
-
Phosphate buffer
- PBS:
-
Phosphatgepufferte Kochsalzlösung
- PEG:
-
Polyethylenglykol
- PVA:
-
Polyvinylalkohol
- RGD:
-
Arginine–glycine–aspartate
- TE:
-
Echo time
- TR:
-
Repetition time
Nanomaterialien
- Goldnanopartikel für Chemosensoren
- Demonstration eines flexiblen Graphen-basierten Biosensors für den empfindlichen und schnellen Nachweis von Eierstockkrebszellen
- Nanopartikel für die Krebstherapie:Aktuelle Fortschritte und Herausforderungen
- 131I-gespurte PLGA-Lipid-Nanopartikel als Wirkstoffträger für die gezielte chemotherapeutische Behandlung von Melanomen
- Folatrezeptor-gerichtete Bioflavonoid-Genistein-beladene Chitosan-Nanopartikel für eine verbesserte Antikrebswirkung bei Gebärmutterhalskrebs
- Neuartige biokompatible Au-Nanostars@PEG-Nanopartikel für die In-vivo-CT-Bildgebung und renale Clearance-Eigenschaften
- Synthese und In-vitro-Leistung von polypyrrolbeschichteten Eisen-Platin-Nanopartikeln für die Photothermie und die photoakustische Bildgebung
- Nah-Infrarot-emittierende Cr3+/Eu3+ codotierte Zink-Gallogermanat-Persistenz-lumineszierende Nanopartikel für die Zellbildgebung
- Siliziumdioxid-Diatomeenschalen mit Au-Nanopartikeln ermöglichen eine empfindliche Analyse von Molekülen für biologische, Sicherheits- und Umweltanwendungen
- Aptamer-modifizierter magnetischer Nanosensibilisator für die In-vivo-MR-Bildgebung von HER2-exprimierendem Krebs



