Synthese und In-vitro-Leistung von polypyrrolbeschichteten Eisen-Platin-Nanopartikeln für die Photothermie und die photoakustische Bildgebung
Zusammenfassung
Die multifunktionale Nanoplattform für die Kombination von photobasierter Therapie und photoakustischer Bildgebung (PAI) zur Krebsbehandlung hat in letzter Zeit viel Aufmerksamkeit auf die Entwicklung der Nanotechnologie gelenkt. In dieser Studie haben wir Eisen-Platin-Nanopartikel (FePt-NPs) mit der Polypyrrol (PPy)-Beschichtung als neuartige Wirkstoffe für die kombinierte photothermische Therapie (PTT) und PAI entwickelt. Die erhaltenen PPy-beschichteten FePt-NPs (FePt@PPy-NPs) zeigten eine ausgezeichnete Biokompatibilität, photothermische Stabilität und eine hohe Absorption im nahen Infrarot (NIR) für die Kombination von PTT und PAI. In-vitro-Untersuchungen zeigten experimentell die Wirksamkeit von FePt@PPy-NPs bei der Abtötung von Krebszellen mit NIR-Laserbestrahlung. Darüber hinaus zeigte der Phantomtest von PAI in Verbindung mit FePt@PPy-NPs ein starkes photoakustisches Signal. Somit könnten die neuartigen FePt@PPy-NPs als vielversprechende multifunktionale Nanopartikel für weitere Anwendungen der photobasierten Diagnose und Behandlung angesehen werden.
Hintergrund
In den letzten zehn Jahren wurden viele neue therapeutische Strategien für die Krebstherapie eingeführt. Dort erlangte die photothermische Therapie (PTT) aufgrund ihrer Vorteile, einschließlich hoher Spezifität, präziser räumlich-zeitlicher Selektivität und begrenzter Nebenwirkungen, große Aufmerksamkeit [1, 2]. Die PTT verwendet Photoabsorber im nahen Infrarotbereich (NIR), um Wärme für die thermische Ablation von Krebszellen bei NIR-Laserbestrahlung zu erzeugen [2]. Die NIR-Photoabsorber nutzen den Vorteil der Laserstrahlung mit der gleichen Wellenlänge und können für die photoakustische Bildgebung (PAI)-geführte photothermische Krebstherapie verwendet werden [3, 4].
Vor kurzem haben sich Eisen-Platin-Nanopartikel (FePt-NPs) als wirksame Mittel für die duale CT/MRT-Bildgebung herausgestellt [5]. FePt-NPs zeigen eine höhere photothermische Effizienz als Gold-Nanopartikel im NIR-Bereich [6]. Kürzlich wurde auch ein stärkeres photoakustisches Signal, das durch die Verwendung von FePt-NPs erzeugt wird, im Vergleich zu Gold-Nanopartikeln gezeigt [7]. Die Oberflächenmodifizierung mit Polymer ist eine bekannte Technik zur Verbesserung der Biokompatibilität und Leistung von Nanopartikeln für die Krebsbehandlung. Trotz ihrer vielversprechenden Eigenschaften gab es einige Forschungsanstrengungen zur Oberflächenmodifizierung von FePt-NPs für die biomedizinische Anwendung [8, 9].
Die hohe Effizienz der Licht-zu-Wärme-Umwandlung der nanoskaligen Wirkstoffe ist der wichtigste Faktor für die PTT [10]. Daher sollte das ausgewählte Material für die Oberflächenmodifizierung von FePt-NPs keinen negativen Einfluss auf die Licht-zu-Wärme-Umwandlung des FePt-NP-Kerns haben. Polypyrrol (PPy), das eine starke Anregung im NIR-Bereich aufweist, hat aufgrund seiner überlegenen inhärenten Eigenschaften, einschließlich photothermischer Stabilität, geringer Kosten und Biokompatibilität, erhebliche Bedeutung in biomedizinischen Anwendungen erlangt [11, 12]. Neuere Studien haben PPy als Hochleistungswirkstoff für die Behandlung von PTT-Krebs [11, 13] und Deep-Tissue-PAI [12] beschrieben. In der vorliegenden Arbeit haben wir PPy-beschichtete FePt-NPs (FePt@PPy-NPs) als neuartige Wirkstoffe für die Kombination von PTT und PAI entwickelt. Unsere Erwartung bei der Verwendung von PPy-Polymer zum Beschichten von FePt-NPs besteht darin, den photothermischen Effekt und die Biokompatibilität der FePt-NPs zu verbessern.
Die resultierenden Nanopartikel haben eine ausgezeichnete Biokompatibilität, photothermische Stabilität und einen starken photothermischen Effekt gezeigt. Die MTT-Assay-Studie ergab, dass FePt@PPy-NPs eine wirksame Krebstherapie aufweisen. Darüber hinaus zeigte der Phantomtest des PAI in Verbindung mit FePt@PPy-NPs ein starkes photoakustisches (PA) Signal, das für weitere Anwendungen des PAI sehr vielversprechend ist.
Methoden
Material
Platinacetylacetonat (Pt(acac)2 , 97%) wurde von Acros Organics gekauft und wie erhalten verwendet. Eisenpentacarbonyl (Fe(CO)5 , 99%), Hexadecan-1,2-diol (90%), Oleylamin (80–90%), Ölsäure (70%), Dioctylether (90%), 1-Octadecen (90%), 3- Mercaptopropionsäure (3-MPA, 97%), Pyrrol (Py, Reagensqualität, 98%), Polyvinylalkohol (PVA, Mw:9000–10.000), Ammoniumpersulfat ((NH4 )2 S2 O8 , 98%), Natriumdodecylsulfat (SDS), Kaliumferrocyanid, Salzsäure und 3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromid (MTT) wurden von Sigma-Aldrich bezogen und verwendet wie bei Experimenten erhalten. Zelluläre Färbereagenzien einschließlich Trypanblau, Propidiumiodid (PI) und Hoechst 33342 wurden ebenfalls von Sigma-Aldrich bezogen. Dulbeccos modifiziertes Eagle-Medium (DMEM), fötales Rinderserum (FBS), Penicillin, Streptomycin, 1 × Trypsin und phosphatgepufferte Kochsalzlösung (PBS) wurden von HyClone (South Logan, UT, USA) bezogen. Für alle Experimente wurde destilliertes Wasser (DI) verwendet.
Synthese von FePt@PPy-NPs
Die Synthese von FePt@PPy-NPs wurde in drei Schritten durchgeführt, die in Schema 1 beschrieben sind.
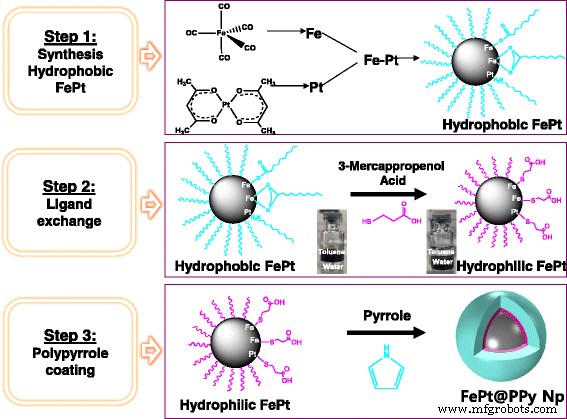
Schematische Darstellung der Synthese von FePt@PPy-NPs
Schritt 1 – Synthese hydrophober FePt-NPs
Die Synthese hydrophober FePt-NPs erfolgte nach dem beschriebenen Schema [5]. Kurz gesagt, 97 mg Pt(acac)2 , 4-ml-Dioctylether, 66-μl-Fe(CO)5 , 195 mg 1,2-Hexadecandiol, 100-ul-Oleylamin und 100-ul-Ölsäure wurden in einen 50-ml-Dreihalsrundkolben gefüllt. Die Reaktionsmischung wurde mit einer Heizrate von 15 °C/min unter Argongas auf 240 °C erhitzt. Nach 30 Minuten wurde das Produkt auf Raumtemperatur abgekühlt. Die FePt-NPs wurden durch Zentrifugation (15 000 U/min, 30 min) gesammelt und mehrmals mit Hexan gewaschen. Die endgültige Nanopartikellösung wurde in Hexan aufbewahrt.
Schritt 2 – Ligandenaustausch
Die Liganden auf der Oberfläche hydrophober FePt-NPs wurden gegen 3-Mercaptopropionsäure (3-MPA) ausgetauscht, wie in Artikeln beschrieben [14]. Darüber hinaus wurden 1 ml 3-MPA und 1 ml Cyclohexanon in ein Zentrifugenröhrchen geladen, und dann wurden 0,5 ml hydrophobe FePt-NPs, die in Hexan dispergiert waren (~ 10 mg) zu der obigen Lösung gegeben und unter Verwendung eines Vortex geschüttelt. Nach 30 min begannen die FePt-NPs auszufallen und alle Nanopartikel fielen nach 1 h aus. Die hydrophilen FePt-NPs wurden durch Zentrifugation (3500 U/min, 5 min) gesammelt. Das Produkt wurde mit Cyclohexanon, Ethanol bzw. Aceton gewaschen. Schließlich werden die hydrophilen FePt-NPs in DI unter Zugabe von NaOH verdünnt.
Schritt 3 – Beschichten hydrophiler FePt-NPs mit PPy
Fünf Milligramm hydrophile FePt-NPs wurden in 200 ml Barker mit 60 ml DI gelöst und 10 Minuten lang kontinuierlich beschallt. Dann wurden 6 ml 40-mM-SDS zu der obigen Lösung gegeben. Als nächstes wurde 1 g PVA, das vollständig in heißem Wasser gelöst war, zu der obigen Lösung gegeben. Die resultierende Mischung wurde dann bei 500 U/min gerührt. Als nächstes 10 ml 6 mM (NH4 .) )2 S2 O8 wurde zu der gerührten Lösung gegeben. Nach 1 h Äquilibrierung wurden 6 ml 100 mM Py in die obige Lösung gegeben. Nach einigen Minuten wurde die Lösung allmählich schwarz. Nach 2 h Polymerisationszeit wurden die resultierenden Nanopartikel durch Zentrifugation (12.000 U/min, 30 min) abgetrennt und mehrmals mit heißem Wasser gewaschen, um Verunreinigungen zu entfernen. Die erhaltenen FePt@PPy-NPs wurden mit PBS durch Ultraschall für 3 Minuten resuspendiert.
Charakterisierung
Die Morphologie der Nanopartikel wurde mit Feldemissions-Transmissionselektronenmikroskopie (FETEM; JEM-2100F, JEOL, Japan) beobachtet. Die atomare Zusammensetzung wurde durch energiedispersive Spektroskopie (EDS) analysiert. Die chemischen funktionellen Gruppen der Nanopartikel wurden unter Verwendung eines Fourier-Transform-Infrarotspektroskopie (FTIR)-Spektrometers (Perkin Elmer 1320 FTIR-Spektrophotometer) analysiert. Der Nanopartikeldurchmesser wurde durch das dynamische Lichtstreuungsverfahren unter Verwendung eines elektrophoretischen Lichtstreuungsspektrophotometers (ELS-8000, OTSUKA Electronics Co. Ltd., Japan) bestimmt. UV-Vis-NIR-Spektren wurden unter Verwendung von UV-Vis-NIR-Spektroskopie (Thermo Biomate 5 Spectrophotometer) gemessen. Die Laserbestrahlung erfolgte mit einem leistungsabstimmbaren 808-nm-Laser (Dauerstrich, maximale Leistung = 5 W, Hi-TechOptoelectronics Co., Peking, China).
Photothermischer Test
Zur Messung der photothermischen Leistung von NPs wie hergestellt wurde eine Suspension (1 ml), die die FePt@PPy-NPs mit spezifischen Konzentrationen (20, 30, 50, 70, 100 und 120 μg/ml) enthielt, in eine 12-Napf gegeben Platte. Dann wurde jede Vertiefung mit einem 808-nm-Laser bei einer Leistungsdichte von 1 W/cm 2 . belichtet für 5 Minuten Darüber hinaus wurde auch die Temperaturerhöhung von bestrahlten FePt@PPy-NPs bei unterschiedlichen Leistungsdichten des 808-nm-Lasers aufgezeichnet. Kurz gesagt wurde eine 50-μg/ml-FePt@PPy-NP-Lösung mit dem NIR-Laser mit der gewünschten Leistungsdichte von 0,5, 1 und 1,5 W/cm 2 . bestrahlt für 6 Minuten Die Temperatur wurde mit einem Thermometer (MASTECH, CA, USA) über eine Thermofaser aufgezeichnet.
Photostabilitätstest
50 μg/ml FePt@PPy-NPs wurden dem 808-nm-Laser bei einer Leistungsdichte von 1 W/cm 2 . ausgesetzt bis die höchste Temperatur erreicht war, und dann wurde es durch Ausschalten des Lasers auf Raumtemperatur zurückkehren gelassen. Die Heiz- und Kühlzyklen wurden sechsmal wiederholt. Das UV-Vis-Spektrum der bestrahlten Probe wurde aufgezeichnet, um es mit der bestrahlten Probe zu vergleichen.
Langzeitspeichertest
Die wässrige Suspension von FePt@PPy-NPs mit einer Konzentration von 120 μg/ml wurde 30 Tage bei 4 °C gelagert, um ihre Stabilität bei der Langzeitlagerung zu bewerten. Zum Vergleich wurden die UV-Vis-Absorptionsspektren und die Partikelgröße von FePt@PPy-NPs für den 1. Tag und den letzten Tag beobachtet. Darüber hinaus wurden FePt@PPy-NPs auf verschiedenen Medien, einschließlich DI, DMEM-Medien plus FBS und PBS, 30 Tage bei 4 °C gelagert, um die Stabilität der hergestellten FePt@PPy-NPs zu bewerten.
Zytotoxizitäts-Assay von FePt-PPy-NPs
Zur Quantifizierung der Zellzytotoxizität wurde ein Standard-MTT-Assay [15] verwendet. Die MDA-MB-231-Brustkrebszellen wurden als Modellkrebszellen verwendet, um die Biokompatibilität von FePt@PPy-NPs zu testen. Mit FePt NP behandelte Krebszellen wurden als Kontrolle verwendet. Die Zelllinie MDA-MB-231 wurde in einem DMEM-Medium mit 10 % FBS und 1 % Antibiotika in einer angefeuchteten Atmosphäre bei 37 °C und 5 % CO2 . kultiviert . Die MDA-MB-231-Zellen wurden in einer 96-Well-Mikrotiterplatte mit einer Dichte von 1 × 10 4 . ausgesät Zellen/Well. Nach 24 h wurden die DMEM-Medien, die FePt@PPy-NPs (oder FePt-NPs) mit unterschiedlichen Konzentrationen (0, 20, 30, 50, 70, 100 und 120 μg/ml) enthielten, auf Zellplatten gegeben und die behandelten Zellen wurden dann 48 h inkubiert. Beachten Sie, dass die FePt-Menge für die beiden getesteten Nanopartikel, einschließlich FePt-NPs und FePt-PPy-NPs, gleich ist. Als nächstes wurden 100 μl MTT, gelöst in PBS mit 0,5 mg/ml, in jede Vertiefung gegeben und die Zellplatten wurden weitere 4 h inkubiert. Das Dehydrogenase-Enzym, das in den Mitochondrien der lebenden Zellen vorhanden ist, wandelte das lösliche MTT in unlösliches lila Formazan um. Als nächstes wurden 100 μL DMSO zugegeben, um das unlösliche violette Formazan aufzulösen. Anschließend wurde die Absorption von violettem Formazan bei 570 nm mit einem Plattenlese-Spektrophotometer aufgezeichnet, um den Prozentsatz der Zelllebensfähigkeit zu quantifizieren.
Mobilfunkaufnahme
Mit Preußisch-Blau-Färbung wurde die zelluläre Aufnahme von FePt@PPy-NPs in die MDA-MB-231-Zelle überprüft [16]. Die Zellen wurden mit einer Dichte von 1 × 10 5 . ausgesät Zellen/ml in 12-Well-Platten und 24 h inkubiert. Als nächstes wurden 200 μg/ml FePt@PPy-NPs zu den Zellplatten gegeben und weitere 24 h inkubiert. Danach wurden die Zellen für 15 Minuten mit kaltem Formaldehyd fixiert. Und dann 10 % Kaliumferrocyanid und 20 % wässrige Salzsäurelösung (50:50 v .) /v ) wurden auf die Zellplatten gegeben und 1 h inkubiert. Das Ergebnis wurde unter Verwendung optischer Mikroskopie beobachtet.
In-vitro-Photothermie
Der MTT-Assay wurde durchgeführt, um die Wirksamkeit von FePt@PPy-NPs auf die Abtötungsfähigkeit von MDA-MB-231-Brustkrebszellen zu quantifizieren. Kurz gesagt, die MDA-MB-231-Zellen wurden in einer 96-Well-Mikrotiterplatte mit einer Dichte von 1 × 10 4 . kultiviert Zellen/Well. Am nächsten Tag wurden die FePt@PPy NP-Lösungen mit spezifischer Konzentration (0, 10, 20, 30, 50, 70 und 100 μg/ml) auf die Zellplatten gegeben und die behandelten Zellen wurden weitere 24 h inkubiert . Dann wurde PBS verwendet, um die ungebundenen Nanopartikel zu waschen. Anschließend wurden die Mikroplatten dem NIR-Laser mit einer Leistungsdichte von 1 W/cm 2 . ausgesetzt für 4 bzw. 6 Minuten. Um die Ergebnisse zu erhalten, wurden die folgenden Schritte gemäß dem Zellzytotoxizitätsassay im Abschnitt „Zytotoxizitätsassay von FePt-PPy-NPs“ durchgeführt.
Die Doppelfärbung von Hoechst 33342 und PI wurde auch verwendet, um die beschädigten und toten Zellen als Ergebnis der photothermischen Behandlung mit FePt@PPy-NPs zu erkennen. Konkret wurden die MDA-MB-231-Zellen in einer 12-Well-Platte mit einer Dichte von 1 × 10 5 . ausgesät Zellen/Well. Nach 24 h wurden die Zellen mit den FePt@PPy-NPs (0, 50, 70 und 100 μg/ml) behandelt und weitere 24 h bei 37 °C kontinuierlich inkubiert. Als nächstes wurden die ungebundenen Nanopartikel durch vorsichtiges Waschen mit PBS entfernt. Anschließend wurden die Zellplatten dem NIR-Laser mit einer Leistungsdichte von 1 W/cm 2 . ausgesetzt für 6 Minuten Als nächstes wurden die Zellkulturplatten für 24 h im Inkubator aufbewahrt und dann wurden die bestrahlten Zellen mit Hoechst 33342 und PI gefärbt. Beachten Sie, dass 1,5 ml Hoechst 33342 (10 μg/ml) in die Zellkulturplatte gegeben und dann 20 min im Inkubator aufbewahrt wurden. Dann wurden die Zellen dreimal mit PBS gewaschen, um den überschüssigen Farbstoff zu entfernen. Dann wurden die Zellen kontinuierlich mit 1,5 ml PI (10 μg/ml) gefärbt und 5 Minuten bei Raumtemperatur inkubiert. Schließlich wurden die Zellen erneut mit PBS gewaschen und die Fluoreszenzbilder wurden mit einem Fluoreszenzmikroskop (Leica Microsystems GmbH, Wetzlar, Deutschland) aufgenommen.
Tierexperiment
Um einen In-vivo-Test der photothermischen Eigenschaften von FePt@PPy-NPs durchzuführen, wurden einer 6 Wochen alten weiblichen BALB/c-Nacktmaus 100 μl 100 μg/ml FePt@PPy-NPs in PBS subkutan injiziert. Als Kontrolle wurde eine andere Nacktmaus ohne Injektion verwendet. Anschließend wurde der injizierte Bereich der Mäuse mit einem 808-nm-Laser mit 1 W/cm 2 . bestrahlt für 6 Minuten Die experimentellen Verfahren mit Tieren wurden vom Animal Care and Use Committee der Pukyong National University genehmigt und gemäß den Leitprinzipien für die Pflege und Verwendung von Labortieren durchgeführt.
Photoakustische In-vitro-Bildgebung
PAI-Einrichtung
PAI am Phantom wurde durchgeführt, um das PA-Signal von FePt@PPy-NPs auszuwerten. Unsere Gruppe hat das nichtinvasive PAI-System entwickelt, wie in der vorherigen Studie beschrieben [17]. Das schematische Diagramm des PAI-Aufbaus ist in Abb. 11 gezeigt. Es wurde ein optisches System verwendet, das in einen gepulsten Nd-YAD-gütegeschalteten Laser (Surelite III, CA, USA) eingebettet war. Der Laser wurde auf eine Wellenlänge von 808 nm und eine Frequenz von 10 Hz mit einem 5-ns-Pulsbetrieb eingestellt. Die optische Eingangsfaser mit einer Brennweite von 50 mm (Thorlabs, Newton, NJ, USA) wurde mit einer plankonvexen Linse verbunden. Die optische Ausgangsfaser wurde mit einem fokussierten Schallkopf (Olympus NDT, USA) verbunden und auf die Mitte der beleuchteten Zone ausgerichtet. Zur Aufzeichnung von PA-Signalen wurden die Daten digitalisiert und über ein in das Lasersystem integriertes DAQ-System (Data Acquisition) gespeichert. Anschließend wurden die aufgezeichneten Daten verwendet, um 2D-Bilder des Phantoms durch ein LabVIEW-Programm zu rekonstruieren.
Probenvorbereitung
Das PVA-Phantom wurde mit 8% PVA hergestellt, um das Gewebe nachzuahmen. Die vorgeimpften MBA-MD-231-Krebszellen wurden 24 h lang mit unterschiedlichen Konzentrationen von FePt@PPy-NPs (50, 100 und 200 μg/ml) behandelt. Anschließend wurden die Zellen geerntet und am Phantom mit 4% Gelatine vermischt (Abb. 12a). Dann wurde das Phantom mit einer kleinen Schicht von 4% Gelatine bedeckt und erstarren gelassen. Schließlich wurde das Phantom für die PAI-Verarbeitung auf dem Wassertank befestigt.
Ergebnisse und Diskussion
Synthese und Charakterisierung von FePt@PPy-NPs
Der Syntheseprozess von FePt-NPs ist in Schema 1 veranschaulicht. Die EDS-Analyse dieser Nanopartikel ergab, dass die endgültige atomare Zusammensetzung von Fe und Pt 20 bzw. 80 % beträgt (zusätzliche Datei 1:Abbildung S1). Hydrophobe FePt-NPs wurden mit 3-MPA modifiziert; Somit werden sie zu hydrophilen FePt-NPs mit einer durchschnittlichen Größe von 8,3 nm. Die hydrophoben FePt-NPs dispergieren in Hexan aufgrund der Anwesenheit von Ölsäure und Oleylamin auf der Oberfläche. Allerdings werden die Partikel nach dem Ligandenaustausch wasserlöslich. FTIR-Spektren von hydrophoben FePt-NPs und hydrophilen FePt-NPs zeigten die charakteristischen Banden der Absorptionsliganden von Ölsäure, Oleylamin und 3-MPA auf der Oberfläche (Abb. 3; Schema 2) [14, 18]. Die FTIR-Daten (Abb. 2) bestätigten zusammen mit der guten Löslichkeit hydrophiler FePt-NPs in Wasser (Schema 1, Schritt 2) den erfolgreichen Ligandenaustauschprozess.
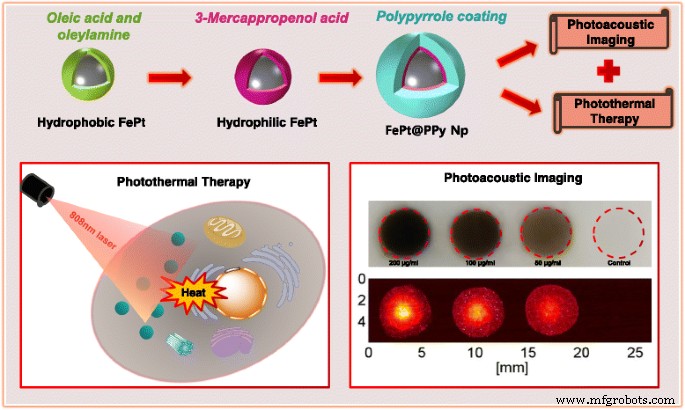
Schematische Darstellung der Synthese und Anwendung von FePt@PPy-NPs in der photothermischen Therapie und photoakustischen Bildgebung
Die FePt-NPs wurden mit PPy durch chemische Oxidationspolymerisation unter Verwendung von (NH4 )S2 O8 als Oxidationsmittel und PVA als Stabilisator. Die PPy-Schicht wurde durch TEM-Bildgebung (Abb. 1c) mit einer Dicke von etwa 10 nm deutlich beobachtet, und die durchschnittliche Größe von FePt@PPy-NPs beträgt 42 nm (Abb. 1d). Die FTIR von FePt@PPy-NPs wurde auch implementiert, um die Beschichtung von PPy-NPs durch Untersuchung der FTIR-Frequenzänderungen zu bestätigen (Abb. 3c). Die charakteristischen Peaks von PPy wurden im vorherigen Bericht [19] gut analysiert. Die FTIR-Vibrationsbänder bei 1620 und 1446 cm −1 wurden C–C- und C=C-Streckschwingungen eines PPy-Rings zugeordnet. Die Bande bei 1236 cm −1 wurde einer C-N-Streckschwingung zugeschrieben, und die Bande bei 1076 cm −1 deutete auf das Vorhandensein eines C-N-In-Plane-Deformationsmodus hin. Außerdem sind die Banden bei 798 und 600 cm −1 wurden C-H- und N-H-In-Plane-Deformationsschwingungen bzw. C-H-Außenbiegeschwingungen zugeschrieben. Das FTIR gewährleistet zusammen mit dem TEM die erfolgreiche Beschichtung von PPy äußeren FePt-NPs.
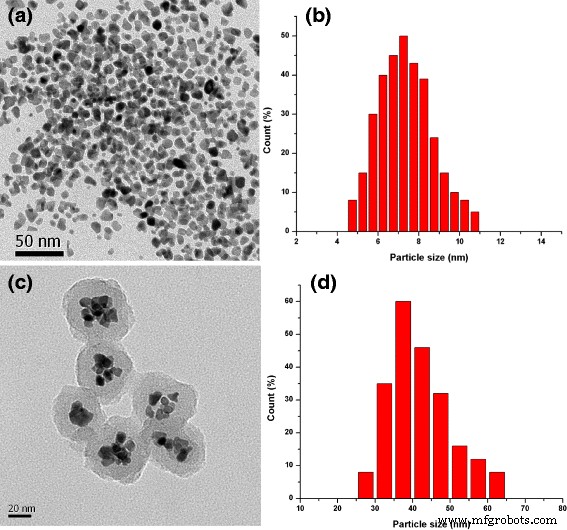
a TEM und b entsprechende Größenverteilungen reiner FePt-NPs. c TEM und d entsprechende Größenverteilungen von FePt@PPy-NPs
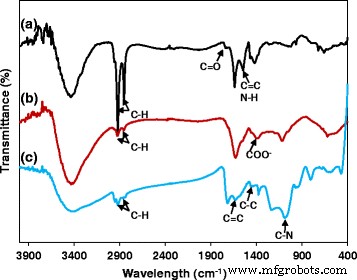
FTIR-Spektren von (a) hydrophoben FePt-NPs, (b) hydrophilen FePt-NPs und (c) FePt@PPy-NPs
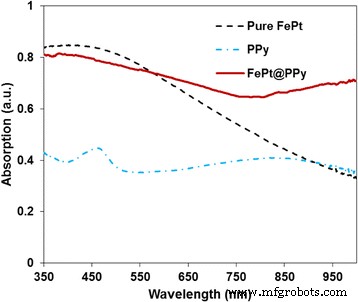
Die UV-Vis-NIR-Spektren von reinen FePt-, PPy- und FePt@PPy-NPs
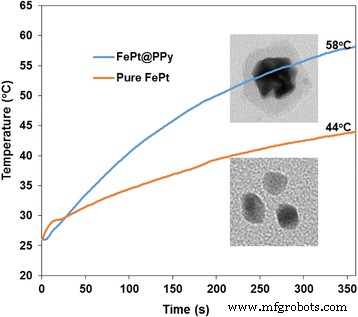
Photothermische Heizkurve von reinen FePt-NPs und FePt@PPy-NPs mit der gleichen Menge an FePt. Alle Lösungen wurden mit 1-W/cm 2 . bestrahlt 808-nm-Laser für 6 Minuten
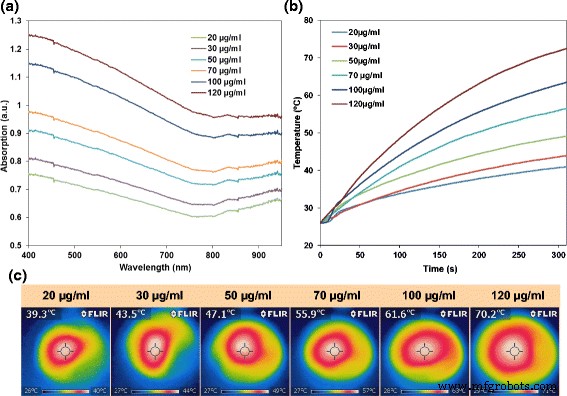
a UV-Vis-NIR-Spektren verschiedener Konzentrationen von FePt@PPy-NPs. b Der photothermische Zerfall von FePt@PPy-NPs mit unterschiedlichen Konzentrationen. c Die entsprechenden NIR-Thermografiebilder bestrahlter Proben. Alle Lösungen wurden mit 1-W/cm 2 . bestrahlt 808-nm-Laser für 5 Minuten
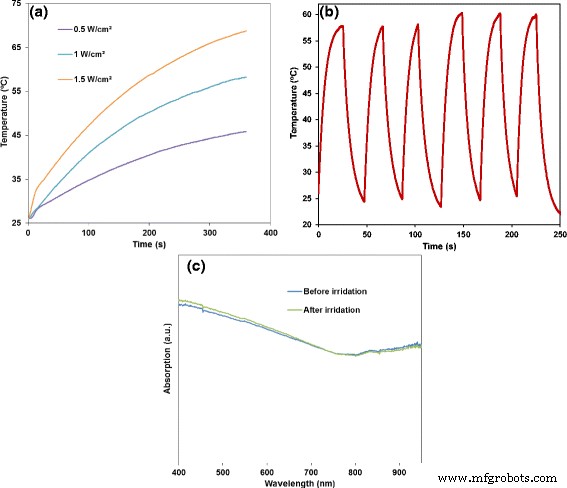
a Photothermisches Verhalten von 50 μg/ml von FePt@PPy-NPs, die unter einem 808-nm-Laser bei unterschiedlichen Leistungsdichten für 6 Minuten gehalten wurden. b Die Echtzeit-Temperaturaufzeichnung von sechs Heiz-/Kühlzyklen von 50 μg/ml von FePt@PPy-NPs unter einem Ein-/Aus-Laserexperiment (1 W/cm 2 .) ). c UV-Vis-NIR-Spektren von FePt@PPy-NPs vor und nach der Bestrahlung
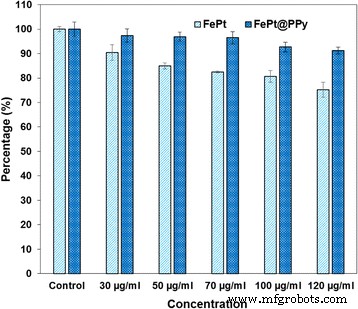
Zelllebensfähigkeit (mit MTT-Assay) von MDA-MB-231-Zellen, die mit FePt- und FePt@PPy-NPs mit unterschiedlichen Konzentrationen für 48 h inkubiert wurden
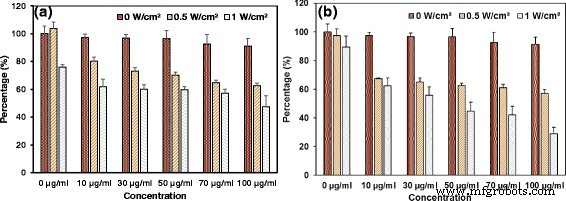
Prozentsatz der lebenden Zellen aus den mit FePt@PPy-NPs behandelten Zellen bei unterschiedlichen Laserleistungsdichten und unterschiedlichen Bestrahlungszeiten. a Die Bestrahlung wurde 4 Minuten lang durchgeführt. b Die Bestrahlung wurde 6 Minuten lang durchgeführt
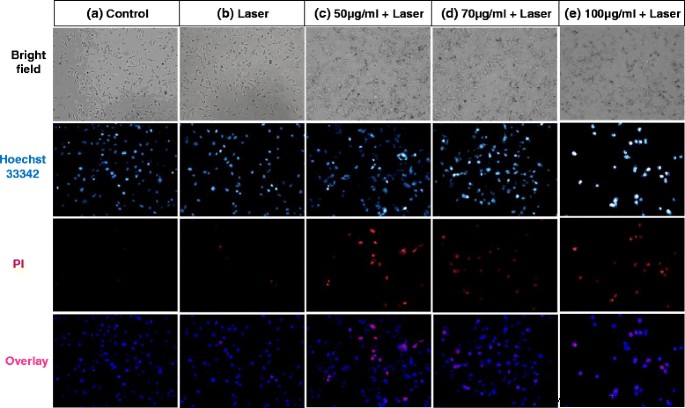
Hellfeld- und Fluoreszenzaufnahmen von MDA-MB-231-Zellen unter verschiedenen Bedingungen. a Kontrolle. b Nur Laser. c 50 μg/ml FePt@PPy-NPs + Laser. d 70 μg/ml FePt@PPy-NPs + Laser. e 100 μg/ml FePt@PPy-NPs + Laser. Alle Lösungen wurden mit 1 W/cm 2 . bestrahlt 808-nm-Laser für 6 Minuten
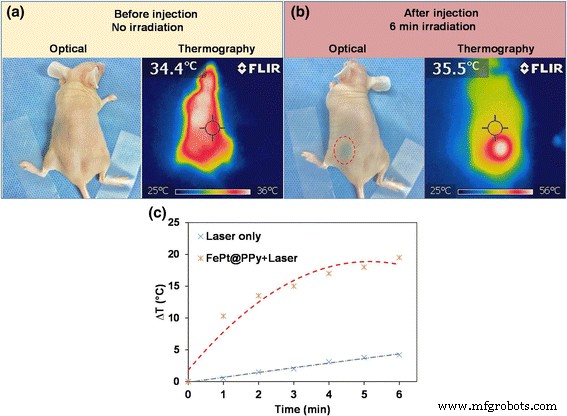
a Das optische Bild und die entsprechenden NIR-Thermografiebilder der Nacktmaus vor der Injektion von FePt@PPy-NPs. b Die linke Seite:das optische Bild der Nacktmaus mit subkutaner Injektion. Der gestrichelte rote Kreis zeigt die Injektionsstelle an. Die rechte Seite:das NIR-Thermografiebild der Nacktmaus nach 6 Minuten unter Bestrahlung mit einem 808-nm-Laser (1 W/cm 2 .) ). Beachten Sie, dass die maximale Erwärmung der Injektionsstelle entspricht. c Temperaturänderung der Hautoberfläche an der Injektionsstelle und bei den Mäusen bei Bestrahlung mit dem 808-nm-Laser (1 W/cm 2 .) ) für 6 Minuten
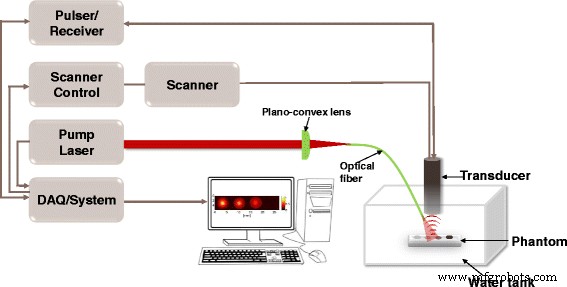
Versuchsaufbau des PAI-Systems
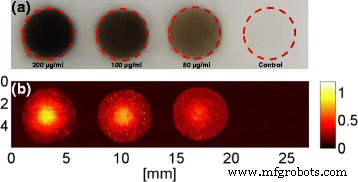
Bewertungen der PA-Reaktionen von FePt@PPy-NPs bei verschiedenen Konzentrationen:a Phantom und b entsprechende PA-Bilder
Die UV-Vis-NIR-Absorptionsspektren von reinen FePt-, PPy- und FePt@PPy-NPs sind in Abb. 3 dargestellt. Die starke Absorption im NIR-Bereich wurde für die zusammengesetzten Nanopartikel beobachtet. Die Absorptionsspektren von FePt und PPy können zusammen zu denen von FePt@PPy-NPs beitragen. Die optischen Eigenschaften von wässrigen FePt@PPy NP-Dispersionen mit unterschiedlichen Konzentrationen (von 20 bis 120 μg/mL) wurden auch durch die UV-Vis-NIR-Spektroskopie erfasst. Wie in Abb. 4a aufgetragen, nahm mit einer Zunahme der FePt@PPy-NP-Konzentration die Photoabsorptionsintensität des gesamten UV-Vis-NIR-Bereichs zu.
Photothermische Leistung von FePt@PPy-NPs
Das photothermische Verhalten von reinen FePt- und FePt@PPy-NPs wurde in Abb. 4 verglichen. Reine FePt- und FePt@PPy-NPs mit der festen FePt-Menge wurden mit einem 808-nm-Laser bei einer Leistungsdichte von 1 W/cm . bestrahlt 2 . FePt@PPy-NPs zeigten im Vergleich zu reinen FePt-NPs ein ausgezeichnetes photothermisches Verhalten. Diese Daten zeigten, dass die PPy-Schicht die photothermische Wirksamkeit des gesamten Systems verbesserte.
Wie in den Abb. 5a, unter den gleichen NIR-Laserbedingungen (5 min, 1 W/cm 2 ) stieg die Temperatur der Lösung mit 20 μg/ml FePt@PPy-NPs von 25 auf 39,3 °C, während die Temperatur der Lösung mit 120 μg/ml FePt@PPy-NPs schnell 71 °C erreichte. Darüber hinaus zeigten thermografische Bilder (Abb. 5c) die photothermische effektive Umwandlung der Probe, die bestrahlte FePt@PPy-NPs mit einem 808-nm-Laser enthielt. FePt@PPy-NPs (50 μg/ml) wurden einer NIR-Laserbestrahlung mit unterschiedlichen Laserleistungsdichten von 0,5, 1,0 und 1,5 W/cm 2 . ausgesetzt für 6 Minuten und die resultierenden Temperaturen betrugen 41,1, 51,3 bzw. 59,4 °C. Diese experimentellen Ergebnisse zeigten, dass die Belichtungszeit, die Konzentration der Nanopartikel und die Laserleistungsintensität wichtige Parameter sind, die die photothermische Leistung von FePt@PPy-NPs signifikant beeinflussen.
Photothermische Stabilitätstests von FePt@PPy-NPs
Neben der starken photothermischen Transduktion ist die Photostabilität von Nanopartikeln bei der PTT wichtig. FePt@PPy NP-Lösung mit 50 μg/ml wurde mit dem 808-nm-NIR-Laser mit 1,0 W/cm 2 . bestrahlt bis die Lösung die höchste Temperatur erreicht hat, dann durch Ausschalten des Lasers auf natürliche Weise auf Raumtemperatur abkühlen. Nach sechs Heiz- und Kühlzyklen blieb die thermische Kurve von FePt@PPy-NPs für jeden Zyklus fast gleich (Abb. 4d). Die UV-Vis-NIR-Spektren vor und nach der Laserbelichtung sind in Abb. 6c dargestellt. Für die gesamten Spektren wurde keine signifikante Änderung beobachtet. Die obigen Ergebnisse zeigten eine gute photothermische Stabilität von FePt@PPy-NPs über einen langen Zeitraum der NIR-Laserbestrahlung.
Langzeitspeichertest
Die Partikelgröße und die UV-Vis-NIR-Absorptionsspektren der präparierten Nanopartikel wurden während der 30 Tage der Lagerung überwacht. Erstens wurde in allen Lösungen, die FePt@PPy-NPs enthielten, keine Aggregation beobachtet (zusätzliche Datei 1:Abbildung S3a). Zweitens zeigten FePt@PPy-NPs in Zellkulturmedien bei einer Konzentration von 120 μg/ml keine signifikante Änderung in ihren UV-Vis-NIR-Spektren (zusätzliche Datei 1:Abbildung S3b) nach den 30 Tagen der Lagerung. Darüber hinaus blieb die durchschnittliche Partikelgröße von FePt@PPy-NPs während der Langzeitlagerung nahezu unverändert (Zusatzdatei 1:Abbildung S3c). Alle obigen Ergebnisse bewiesen eindeutig die Stabilität der hergestellten Nanopartikel.
In-vitro-Zell-Zytotoxizitäts-Assay
Für die Krebsbehandlung sollen Nanopartikel die ausgezeichnete Biokompatibilität aufweisen. Wie in Abb. 7 gezeigt, wurden die MDA-MB-231-Brustkrebszellen mit reinen FePt- und FePt@PPy-NPs mit unterschiedlichen Konzentrationen behandelt und 48 h inkubiert. Selbst bei der höchsten getesteten Konzentration (120 μg/ml) wurde keine signifikante Zytotoxizität der FePt@PPy-NPs beobachtet, und die Zelllebensfähigkeit von MDA-MB-231-Brustkrebszellen lag immer noch bei über 95 %. Bei den reinen FePt-NPs töteten 120 μg/ml bestrahlte Nanopartikel 20 % Krebszellen ab. Dieses Ergebnis zeigte, dass die Beschichtung der PPy-Schicht die Biokompatibilität von FePt-NPs verbesserte und FePt@PPy-NPs als ungiftiges Material angesehen werden können.
Mobilfunkaufnahme
Zum Nachweis der zellulären Aufnahme von FePt@PPy-NPs wurde eine Preußisch-Blau-Färbung durchgeführt, die auf der Reaktion von Eisen und Kaliumferrocyanid in saurer Lösung basiert. Wie in Zusätzliche Datei 1:Abbildung S2 gezeigt, waren die meisten Zellen im Inneren der Zellen mit blauen Flecken gefärbt, was auf die zelluläre Aufnahme von FePt@PPy-NPs hinweist.
In-vitro-Photothermie
Der Standard-MTT-Assay wurde durchgeführt, um die Wirksamkeit bestrahlter FePt@PPy-NPs auf die Abtötungsfähigkeit von MDA-MB-231-Brustkrebszellen zu bewerten. Zuerst wurden die Krebszellen mit unterschiedlichen Konzentrationen von FePt@PPy-NPs für 24 Stunden inkubiert und dann dem 808-nm-Laser bei 1 W/cm 2 . ausgesetzt für 4 Minuten Wie in Abb. 8 gezeigt, wurde der Prozentsatz der Zelllebensfähigkeit allmählich verringert, wenn die Konzentration der behandelten Nanopartikel erhöht wurde. Ungefähr 50 % der Zellen starben bei einer Konzentration von 100 μg/ml bestrahlter FePt@PPy-NPs. Um mehr Krebszellen abzutöten, wurde die Bestrahlungszeit auf bis zu 6 Minuten erhöht. With 100 μg/mL concentration, approximately 70% of dead cells were observed. A comparison of the photothermal therapy performance between the proposed system and some reported nanoparticles was conducted in Additional file 1:Table S1. It is found that the proposed system shows comparable capability in killing cancer cells (i.e., 70% cell death) with quite low nanoparticle concentration (i.e., 100 μg/mL) under relatively weak power density condition (i.e., 1 W/cm 2 ) and short irradiation time (i.e., 6 min).
In addition, by using the fluorescence imaging technique of five groups, we conducted experiments on the cancer cells to consider the killing capability of the prepared nanoparticles:the control groups (only cells), the laser-only group (cells were exposed to the 808-nm laser), the 50-μg/mL FePt@PPy NPs + 808-nm laser (cells were treated with 50-μg/mL of FePt@PPy NPs and exposed to the 808-nm laser), the 70-μg/mL FePt@PPy NPs + 808-nm laser (cells were treated with 50-μg/mL of FePt@PPy NPs and exposed to the 808-nm laser), and the 100-μg/mL FePt@PPy NPs + 808-nm laser (cells were treated with 50-μg/mL of FePt@PPy NPs and exposed to the 808-nm laser).
Double staining of Hoechst 33342 and PI was used to explore the damaged and dead cells. Hoechst 33342 is a DNA dye, which can be permeable in both dead and viable cells [20]. The changes in the size and shape of nuclei of the Hoechst 33342 stained cells can be observed under fluorescence microscopy. With the apoptosis cells, Hoechst 33342 will make the condensed chromatin brighter than that in a normal cell. PI dye also binds to DNA, but it only permeates through the membrane of damaged and dead cells [21]. Thus, double staining can differentiate between dead cells and live cells by each treatment method.
As shown in Fig. 9, the cancer cells exposed to the NIR laser in the presence of the FePt@PPy NPs emit strong fluorescence, whereas the slight fluorescence is emitted by cancer cells in the absence of the nanoparticles. Only a few dead cells with the red nuclei were observed in the control and laser-only group (Fig. 9a, b). In contrast, many cells in the FePt@PPy NPs + 808-nm laser groups died and displayed red nuclei, as observed in Fig. 9c–e. After incubation for 24 h, some dead cells lost the binding ability and were washed out of the cell disk. Therefore, the intensity of cancer cells in the 100-μg/mL of FePt@PPy NPs + 808-nm laser group was less than the others. Conclusively, almost cancer cells which were treated with 100-μg/mL of FePt@PPy NPs was destructed after being exposed to the 808-nm NIR laser at a power density of 1.0 W/cm 2 .
In Vivo Laser Heating Experiment
The potential ability of FePt@PPy NPs for laser-induced heating was finally tested in an animal model. The nude mouse was subcutaneously injected with 100 μL of an aqueous FePt@PPy (100 μg/mL) NPs in PBS. Figure 10a presents the optical and NIR thermographic images of the nude mouse before injection, pointing out the temperature of mouse surface’s skin is about 36 °C. Fig. 10b (left side) shows an optical image of the mouse in which the injection site is indicated by a dashed red circle. The injected area was irradiated with the 808-nm laser at 1 W/cm 2 for 6 min, and the NIR thermographic image of this mouse is shown in Fig. 10b (right side). The temperature of the skin’s surface was continuously monitored with an NIR thermographic camera. The time evolution of the surface temperature during the 6 min irradiation is shown in Fig. 10c, figuring out a temperature increment of the skin about 19 °C. From that, we can see clearly that the injected FePt@PPy NP area with laser irradiation produced a high temperature, as required for tumor ablation. Moreover, the heating area was found to be well localized at the injection site as shown in the NIR thermographic image (Fig. 10b, right side). Conclusively, with the excellent laser-induced heating properties, FePt@PPy could be a novel promising agent for photothermal therapy.
In Vitro Photoacoustic Imaging
The top-view image of the phantom filled with pretreated cancer cells is shown in Fig. 12a. The corresponding PAI acquired at the 808-nm laser from the sample in Fig. 12a is illustrated in Fig. 12b.
PAI is an emerging imaging modality and can be used to assist phototherapy [22]. All the samples containing pretreated cells were clearly visible, whereas the controlled samples with 4% gelatin did not produce any PA signal. The magnitude of the PA signal was increased when the concentration of nanoparticles increased. The ability to image FePt@PPy NPs inside phantom with the PAI system is very promising for image-guided photo-induced cancer therapy. The laser system for PAI, which was used in conjunction with FePt@PPy NPs, also showed the potential for future implementations.
Conclusions
In this study, we developed the photoabsorber FePt@PPy NPs and evaluated their efficiency on in vitro PTT and PAI (Scheme 2). The prepared FePt@PPy NPs showed many good properties for PTT and PAI including excellent biocompatibility, photothermal stability, and high NIR absorbance. Moreover, in vitro investigation confirmed the effectiveness of the FePt@PPy NPs in killing the cancer cells under the NIR laser. So far, the phantom test of PAI used in conjunction with FePt@PPy NPs showed a strong PA signal. Owing to their good properties, the novel FePt@PPy NPs could be considered as promising multifunctional nanoparticles for further applications in PTT and PAI.
Nanomaterialien
- Nanopartikel für die Krebstherapie:Aktuelle Fortschritte und Herausforderungen
- BSA-beschichtete Gold-Nanostäbe für die photothermische NIR-II-Therapie
- Resveratrol-beladene Albumin-Nanopartikel mit verlängerter Durchblutung und verbesserter Biokompatibilität für eine hochwirksame gezielte Pankreastumortherapie
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität
- Neuartige biokompatible Au-Nanostars@PEG-Nanopartikel für die In-vivo-CT-Bildgebung und renale Clearance-Eigenschaften
- Modifiziertes hyperverzweigtes Polyglycerin als Dispergiermittel zur Größenkontrolle und Stabilisierung von Goldnanopartikeln in Kohlenwasserstoffen
- 5-Aminolävulinsäure-Squalen-Nanoanordnungen für die Tumorphotodetektion und -therapie:In-vitro-Studien
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Antikörper-konjugierte Silica-modifizierte Goldnanostäbchen für die Diagnose und photothermische Therapie von Cryptococcus neoformans:ein In-vitro-Experiment
- Herstellung von hierarchischen porösen Silicalit-1-verkapselten Ag-NPs und ihre katalytische Leistung für die 4-Nitrophenol-Reduktion



