Umweltverträgliche Metall-organische Gerüste als Wirkstoffabgabesystem für die Tumortherapie
Zusammenfassung
Nanopartikel als Wirkstoffabgabesysteme können die Hydrophilie der Wirkstoffe verändern, um die Wirkstoffaufnahme und den Wirkstoffausfluss im Gewebe zu beeinflussen. Sie verhindern, dass Medikamente unspezifisch mit Bio-Makromolekülen binden und erhöhen die Medikamentenakkumulation an den Läsionsstellen, verbessern die Therapieeffekte und reduzieren unnötige Nebenwirkungen. Metall-organische Gerüste (MOFs), die typischen Nanopartikel, eine Klasse kristalliner poröser Materialien über selbstorganisierte organische Linker und Metallionen, weisen eine ausgezeichnete biologische Abbaubarkeit, Porenform und -größe sowie eine fein einstellbare chemische Zusammensetzung auf. MOFs haben eine starre molekulare Struktur und eine einstellbare Porengröße kann die Stabilität des Verkapselungswirkstoffs unter rauen Bedingungen verbessern. Außerdem kann die Oberfläche von MOFs mit niedermolekularen Liganden und Biomolekülen modifiziert werden und mit den Biomarkern binden, die auf der Oberfläche von Krebszellen überexprimiert werden. MOFs-Formulierungen für Therapeutika wurden entwickelt, um effektiv auf die einzigartige Tumor-Mikroumgebung (TEM) wie beispielsweise hohen H2 . zu reagieren O2 Spiegel, Hypoxie und hochkonzentriertes Glutathion (GSH). Somit sollten MOFs als ein Arzneimittelabgabesystem verhindern, dass Arzneimittel während der Blutzirkulation austreten und auf kontrollierte Weise an den Läsionsstellen freigesetzt werden. In diesem Artikel werden wir umgebungsresponsive MOFs als Wirkstoffabgabesysteme für die Tumortherapie unter verschiedenen Stimuli zusammenfassen.
Einführung
Der Tumor ist eine multifaktorielle Erkrankung mit hoher Sterblichkeits- und Rezidivrate, die die menschliche Gesundheit bedroht [1]. In Kliniken haben Chemotherapeutika und operative Eingriffe zur Tumortherapie eine Tumorhemmung erreicht, jedoch oft mit schwerwiegenden Nebenwirkungen, was uns dazu bewogen hat, überlegene Therapiemethoden zu entwickeln [2, 3]. In den letzten Jahrzehnten wurden Nanoträger für die Tumorbildgebung, Theranostik und Therapie entwickelt [4].
Bei allen Arten von Nanoträgern haben Metall-organische Gerüste (MOFs) zunehmende Aufmerksamkeit auf sich gezogen, da sie durch unterschiedliche Umgebungen stimuliert werden können [5, 6]. MOFs als eine Klasse hochkristalliner anorganisch-organischer poröser Materialien bestehen aus Metallionen oder Clustern, die durch organische Brückenliganden verbunden sind und haben in den letzten Jahren auf verschiedenen Gebieten enorme Aufmerksamkeit auf sich gezogen [7]. Anfang der 1990er Jahre wurden MOFs aufgrund ihrer fein abstimmbaren chemischen Zusammensetzung, Porenform und -größe, Morphologie, großen Oberfläche und ausgezeichneten biologischen Abbaubarkeit in der Gasspeicherung, Trennkatalyse, Energieumwandlung, Lumineszenz und chemischen Sensorik sowie im biomedizinischen Bereich weit verbreitet eingesetzt. [8, 9].
MOFs haben organische aktive Zentren und zugängliche, öffnende poröse Architekturen, chemische Stabilität und ausreichende thermische Effekte [10]. Somit können verschiedene funktionelle Gruppen über drei Strategien in MOFs integriert werden:Einkapselung, Pfropfung und Infiltration, was ihre Biokompatibilität, Löslichkeit und Interaktivität mit einem Zielmolekül verbessern kann [11]. Insbesondere der Verkapselungsansatz durch Kopräzipitation und biomimetische Mineralisierungsmethode ist der schnelle und bequeme Ansatz unter Verwendung der organischen Liganden und Metallionen, um eine einstufige Einbettung von Wirkstoffen in MOFs zu erreichen [12, 13]. Inspiriert von diesen hervorragenden Vorzügen wurden verschiedene Methoden entwickelt, um die Durchführbarkeit und Wirksamkeit der Anwendung zu ermitteln. MOFs können jedoch leicht auf verschiedenen Substraten wachsen, um multifunktionelle Komplexe zu bilden [14]. Daher können einige Therapeutika über den Synthesefortschritt direkt in MOFs eingebaut werden, was Kristallwachstumsprobleme umgehen kann, wenn präfunktionalisierte Liganden verwendet werden [15, 16]. Eine solche Strategie bietet eine hohe Atomökonomie und führt zu äußerst zufriedenstellenden Wirkstoffnutzlasten [14].
Obwohl MOFs als Wirkstoffabgabesystem für die Tumortherapie beispiellose Vorteile haben, wurde ihre Anwendung durch viele hartnäckige Nachteile eingeschränkt. MOFs sind beispielsweise ein komplizierter synthetischer Fortschritt, der vom Immunsystem des Körpers eliminiert wird und eine kurze Halbwertszeit im Blut hat [17,18,19]. In diesem Artikel werden wir einige grundlegende umgebungsstimuliresponsive MOFs zusammenfassen, um die Tumortherapie zu verbessern und den aktuellen Stand der Tumortheranostik zu überprüfen.
pH/ATP-Ansprechverhalten
Zeolithische Imidazolatgerüste (ZIFs) als spezifische Unterklasse der MOFs haben eine einstellbare Porengröße, eine extrem große Oberfläche und einen einfachen Synthesefortschritt. ZIFs werden durch biomimetische Mineralisierung und Kopräzipitation synthetisiert und als idealer Wirkstoffträger für die Tumortheranostik verwendet [20]. Darüber hinaus können ZIFs-Nanopartikel ein Entweichen von Endosomen erreichen, was der Protonierung des Imidazol-2-carboxaldehyds (2-ICA) im sauren Endosom zugeschrieben wird, das den "Protonenschwamm"-Effekt antreibt [21].
Die Gentherapie hat in den letzten Jahrzehnten sowohl in der Grundlagenforschung als auch in der klinischen Forschung zur Tumortherapie große Aufmerksamkeit auf sich gezogen [22]. Nackte Nukleinsäuren werden jedoch leicht durch die Blutserumnuklease abgebaut. Sie sind zu groß und fragil, um die Zellmembran zu passieren, was zu unbefriedigenden Therapieergebnissen führt [23, 24]. Zeolithisches organisches Gerüst-8 (ZIF-8) wird im Eintopfverfahren durch Metallionen mit geringer Toxizität (Zn 2+ ) und 2-Methylimidazol (2-Mim) unter milden Bedingungen. Es hat eine ausgezeichnete Verkapselungsfähigkeit und schützt Gene vor Enzymabbau [25]. Li und seine Mitarbeiter stellten einen einstufigen Ansatz bereit, um große Plasmid-DNA (pDNA)-Moleküle in ZIF-8- und ZIF-8-Polymersysteme durch biomimetische Mineralisierung und Copräzipitation zu laden (Abb. 1A gezeigt) [26]. ZIF-8- und ZIF-8-Polymersysteme zeigen eine ausgezeichnete Einkapselungsfähigkeit, eine gute Verteilung der beladenen pDNA gegen den enzymatischen Abbau und eine bessere pH-abhängige Freisetzung. Wichtig ist, dass das kationische Polymer (PEI)-Funktionalisierungs-MOFs-Polymer-System mit höherem Molekulargewicht (MW) die elektrostatische Wechselwirkung mit pDNA verstärkt, was die zelluläre Aufnahme und das endo-/lysosomale Entweichen verbessert, was zu einer bemerkenswerten Genexpression führt [27]. Somit bieten diese ZIF-8- und ZIF-8-Polymer-basierten Nanoträger für die Gentherapie einen wirtschaftlichen, bequemen und schnellen Ansatz zur Einkapselung von Genmolekülen für einen effektiven intrazellulären Transport und eine effektive Expression.
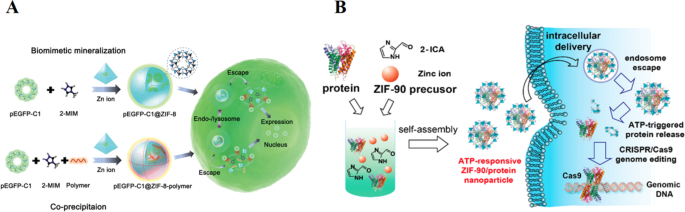
Copyright 2019 American Chemical Society. B Schematische Darstellung der Selbstorganisation von ZIF-90/Protein-Nanopartikeln und ATP-getriggerter Proteinfreisetzung aus ZIF-90-Nanopartikeln in Zellen [29]. Copyright 2019 American Chemical Society
A Schematische Darstellung der Synthese von pEGFP-C1@ZIF-8-Nanostrukturen und pEGFP-C1@ZIF-8-Polymer-Nanostrukturen über biomimetische Mineralisierungs- bzw. Copräzipitationsverfahren und deren zellulärer Abgabe- und Expressionsprozess [26].
Die Konzentration von ATP ist im Extrazellulär niedriger als 0,4 mM. Im Zytosol oder erkrankten Zellen ist die Konzentration jedoch hochreguliert (1–10 mM) [28]. Somit wird das auf ATP ansprechende Arzneimittelverabreichungssystem ein neues Fenster für eine fortschrittliche Arzneimittelverabreichung zur gezielten Behandlung von Krankheiten öffnen. Abbildung 1B gezeigt, Yang et al. berichteten über das ATP-responsive zeolithische Imidazolgerüst-90 (ZIF-90) als idealen Nanocarrier für den zytosolischen Proteintransport, das einfach durch Mischen von Zn 2+ . hergestellt wurde und Imidazol-2-carboxaldehyd (2-ICA) an der Proteinlösung [29]. An den Tumorstellen werden die ZIF-90/Protein-MOFs nach der Herstellung aufgrund der kompetitiven Koordination zwischen dem Zn 2+ . allmählich abgebaut, um das Preload-Protein freizusetzen und ATP, das ZIF-90 und das freisetzende Protein zerlegt, kann das Wachstum von Krebszellen wirksam hemmen. Somit können wir spekulieren, dass ZIP-90-MOFs molekulargewichtiges Protein unabhängig von Molekulargewicht und Proteingröße einkapseln können. Dazu gehören Superoxiddismutase und Rinderserumalbumin mit minimalen Auswirkungen auf die Proteinfunktion für die Tumortherapie.
Aufgrund der abnormalen TME erweitert dieses ATP-reaktive Proteinabgabesystem, das in diesem Abschnitt dargestellt wird, nicht nur die Chemie von MOFs in biomedizinischen Anwendungen, sondern öffnet auch ein neues Fenster für die Proteinabgabe und Genome-Editing-Techniken zur gezielten Behandlung von Krankheiten.
Leicht reagierend
Als „grüner“ Ansatz hat die photothermische Therapie eine minimale Toxizität für das umgebende Gewebe und wird häufig in der Tumortherapie eingesetzt [30, 31]. Hohe Temperaturen können schwere irreversible Gewebeschäden verursachen, wenn die Temperatur über 44 °C liegt. Es reicht aus, Zellmembranschäden, mitochondriale Dysfunktion und Störung der RNA-Synthese zu verursachen, um den Zelltod zu induzieren [32]. Anders als normales Gewebe, das Wärme ableiten und die Temperatur durch die Blutzirkulation über Neuromodulation konstant halten kann, machte die Blockierung der autonomen Regulationsfunktion Tumorgewebe zu einem Wärmereservoir. Dies bietet einen großen Vorteil für die anschließende photothermische Therapie [33].
Aufgrund dieser oben genannten Vorzüge und der schlechten Wärmeableitungsfähigkeit kann eine photobasierte Therapie für die Tumortherapie geeignet sein. Die photodynamische Therapie (PDT) ist der typische Ansatz der photothermischen Therapie, der aus drei Grundelementen besteht (nahe Infrarotlichtbestrahlung, viel Sauerstoff und Photosensibilisatoren) [34]. Nahinfrarot-Lichtbestrahlung (NIR-Licht) als externer Stimulus zeigt eine hohe räumliche und zeitliche Kontrolle der lokalen Erwärmung mit minimalen Nebenwirkungen [35, 36]. PSs nutzten umgebenden Sauerstoff, um giftige reaktive Sauerstoffspezies (ROS) zu erzeugen, um Krebszellen unter Laserbestrahlung zu zerstören [37, 38]. Wie in Fig. 2A gezeigt, haben Park et al. entwarfen ein Zr(IV)-basiertes porphyrinisches Metall-organisches Gerüst (Zr-MOF), das unter NIR-Licht ROS erzeugen kann [39]. Nach der Injektion in den Körper kann sich Zr-MOF über die Effekte der verbesserten Permeabilität und Retention (EPR) im Tumorgewebe anreichern. Die Targeting-Fähigkeit war jedoch nicht zufriedenstellend, was unnötige Nebenwirkungen verstärken könnte [40]. Daher wurde Zr-MOF mit Folsäure weiter modifiziert, wodurch die Zielfähigkeit von Zr-MOF während der Blutzirkulation verbessert und die PDT-Wirksamkeit gesteigert wurde.
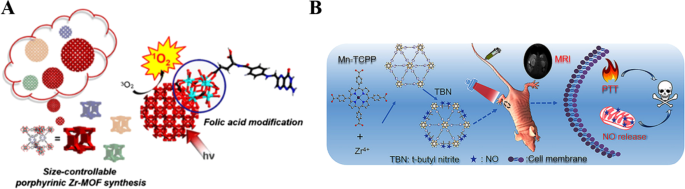
Copyright 2018 American Chemical Society. B Schema für die Synthese des NMOF-SNO-Nanokomposits und der durch NIR-Licht ausgelösten NO-Freisetzung und PTT [42]. Copyright 2018 American Chemical Society
A Abbildung der PCN-224-Struktur. 6-fach Zr6 Cluster (Zr6 O4 (OH)4 (H2 O)6 (OH)6 (COO)6 ), tetratoper Linker (Tetrakis (4-carboxyphenyl)porphyrin (H2 .) TCPP)) und 3D nanoporöses Gerüst von PCN-224. (b) Eine kubische Einheit von PCN-224 und schematische Darstellung von kugelförmigen PCN-224-Nanopartikeln auf der Grundlage der Konstruktion von kubischen Einheiten, die unterschiedliche Größen ergeben [39].
Dies kann mit Hilfe von Kontrastmitteln eine präzise Therapienavigation ermöglichen und den geeigneten Therapiezeitpunkt bestimmen [41. Wie in Abb. 2B gezeigt, entwickelten Zhang und seine Mitarbeiter Mn-Porphyrin-MOFs durch Selbstorganisation von Mn-Tetrakis(4-carboxyphenyl)porphyrin und Zr 4+ -Ionen, die Mn-Porphyrin-MOFs mit der Magnetresonanztomographie (MRT) und photothermischen Umwandlungskapazität ausstatten, ohne den langwierigen Synthesefortschritt zu erhöhen [42]. Diese neuartigen MOFs können außerdem mit dem hitzeinstabilen NO-Donor s-Nitrosothiol (SNO) konjugieren [43]. Daher kann diese MOFs-Plattform die photothermische und MRT-gesteuerte synergistische NO-Behandlung erreichen. MOFs-SNO kann sich durch intravenöse Injektion effizient in den Tumorbereichen anreichern und eine hohe photothermische Umwandlungsfähigkeit für PTT realisieren und die NO-Freisetzung für eine synergistische NO-Therapie mit weniger Photoschädigung kontrollieren. Somit sind in die MOFs integrierte Theranostika ein praktikabler Ansatz zur Verbesserung der Diagnose, ermöglichen eine präzise Therapienavigation und bestimmen den geeigneten Therapiezeitpunkt.
Aufgrund der optischen Eigenschaften von freiem Porphyrin verfügt das erhaltene Porphyrin-MOF, wenn Porphyrin in die MOFs integriert wird, über Fluoreszenzbildgebung und PDT, was neue Möglichkeiten für die Tumortheranostik der nächsten Generation eröffnet.
H2 O2 Reaktionsschnell
Hohe H2 .-Werte O2 , Hypoxie, niedriger pH-Wert und hochkonzentriertes Glutathion (GSH) sind gemeinsame Merkmale in der Tumormikroumgebung (TME) [44,45,46]. Daher kann die Verbesserung oder Veränderung einzelner TME das Tumorwachstum hemmen und die therapeutische Wirkung verstärken [47, 48]. Viele Literaturstellen haben berichtet, dass MnO2 hat Nanoenzymaktivität kann sich in Mn 2+ . zersetzen und Freisetzungsmenge O2 unter den Umständen von H2 O2 , die die Sauerstoffkonzentration in soliden Tumoren erhöhen und unter Laserbestrahlung reichlich reaktive Sauerstoffspezies (ROS) erzeugen können [49, 50]. ROS als intrazelluläres chemisches Substrat kann das Zellsignal modulieren und eine wichtige Rolle im Zellzyklus spielen [51]. Wichtig ist, dass Krebszellen empfindlicher auf hohe ROS-Spiegel und anfälliger für Apoptose sind [52]. Wie Abb. 3 zeigt, haben Sun et al. konstruiertes Rinderserumalbumin-MnO2 /chlorin e6@ZIF-8 (BSA-MnO2 /Ce6@ZIF-8) Nanosystem weist pH/H2 . auf O2 Steuerbarkeit für O2 Produktionskapazität, die einen sicheren und effizienten Behandlungsfortschritt der PDT-Therapie ermöglichte [53]. Die Beladung des ZIF-8 mit Photosensibilisator Chlorin e6 (Ce6) kann das Problem der geringen Löslichkeit in der wässrigen Umgebung lösen und ROS erzeugen, um Krebszellen unter 650-nm-Laserbestrahlung apoptotisch und nekrotisch zu induzieren. Rinderserumalbumin (BSA)-MnO2 in die Oberfläche von Ce6@ZIF-8 dekoriert, das erhaltene BSA-MnO2 /Ce6@ZIF-8 hat eine ausgezeichnete Dispergierbarkeit, geringe Toxizität, ausreichende Fähigkeit zur Sauerstofferzeugung und minimale Nebenwirkungen in vitro/in vivo. Dieses gut vorbereitete BSA-MnO2 /Ce6@ZIF-8 Nanosystem besitzt einen pH/H2 O2 -sensitive Kapazität und folgt der MRT-gesteuerten PDT, die ein enormes Potenzial für eine genauere Diagnose und Verbesserung der Antitumorwirkung birgt.
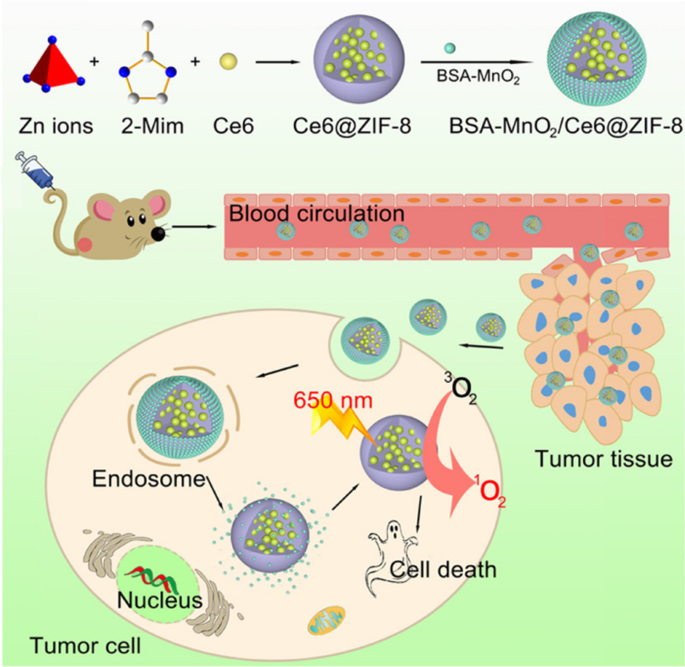
Copyright 2019 American Chemical Society
Schematische Darstellung zur Bildung eines BSA-MnO2 /Ce6@ZIF-8 Nanoplattform und schematische Darstellung der TME-Reaktionsfähigkeit und Erzeugung von ROS-Bestrahlung mit einem 650-nm-NIR-Laser für die MRT-gesteuerte photodynamische Krebsbehandlung [53].
GSH-Responsive
Einen deutlichen Vorteil hat die PDT in der Tumortherapie erreicht; eine hohe Konzentration von Glutathion (GSH) in Krebszellen (2–10 mM) widersteht nicht nur PDT, Strahlen- und Chemotherapie, sondern dient auch als Antioxidans zum Abfangen von zellulären ROS und beeinträchtigt die PDT-Anwendung stark [54, 55]. Genauer gesagt wurde berichtet, dass übermäßiges ROS eine Entzündung des Tumorgewebes und eine ernsthafte Phototoxizität für normales Gewebe verursachen kann [56, 57]. Daher ist es dringend erforderlich, ein intelligentes MOFs-System zu entwickeln, das gleichzeitig eine PSs-vermittelte ROS-Erzeugung erreichen und die negativen Auswirkungen von intrazellulärem GSH auf die Zytotoxizität von ROS in den Tumorarealen reduzieren kann.
Um diese Anforderungen zu erfüllen, haben Wan et al. stellten ein mit GSH freigesetztes Mn(III)-versiegeltes MOFs-Nanosystem zur Verfügung, das einer reduktiven Desintegration durch hochgradiges GSH in Tumorlokalisationen unterzogen wurde. Dies kann die GSH-Verarmung kontrollieren und die ROS-Erzeugung zeigte eine umfassende Tumorhemmung durch Verbesserung der therapeutischen Wirkungen der PDT (Abb. 4A gezeigt) [58]. Die größte Herausforderung von MOFs in medizinischen Anwendungen sind jedoch ihre ungünstige Biokompatibilität und kurze Bluthalbwertszeit. Daher haben viele Strategien zur Optimierung der In-vivo-Anwendung von MOFs große Aufmerksamkeit auf sich gezogen [59]. Inspiriert von zirkulierenden Blutzellen ist die biomimetische Tarnung mit der Plasmamembran ein wirkungsvoller Ansatz, um das Schicksal anorganischer Nanomaterialien in vivo zu koordinieren [60,61,62]. Wie in Abb. 4B gezeigt, veranschaulichten Min und seine Kollegen multifunktionale biomimetische MOFs-Nanopartikel mit 4T1-Brustkrebszellmembran-Tarnung für die synergetische Antikrebstherapie von PDT und Antiangiogenese [55]. Ein solches Design kann die von den Spenderzellen geerbten Oberflächenproteine behalten und mit 4T1-Zellen dekoriertes MnO2 . ausstatten beschichtete porphyrinhaltige Zr-MOF-beladene vaskuläre endotheliale Wachstumsfaktor-Rezeptor-2-MOFs (aMMTm) zusätzliche biologische Funktion, um der Makrophagenerkennung zu entgehen und Tumorgewebe über homotypische Affinität in vivo anzugreifen. Noch wichtiger ist, MnO2 in die Oberfläche von MOFs dekoriert, um hohe intratumorale Spiegel von GSH und H2 . zu neutralisieren O2 zur Verbesserung der einzigartigen Tumor-Mikroumgebung, die die PDT-Ergebnisse verbessern kann. Wenn das MnO2 Schale wurde allmählich abgebaut, das freigesetzte Mn 2+ kann als MRT-Kontrastmittel wirken und Apatinib neutralisierte die PDT-induzierte Revaskularisation und verhinderte das Fortschreiten des Tumors. Wir glauben, dass dieses multifunktionale Medikamentenabgabesystem ein enormes Potenzial für die mechanismusbasierte Anpassung der Antitumortherapie hat.
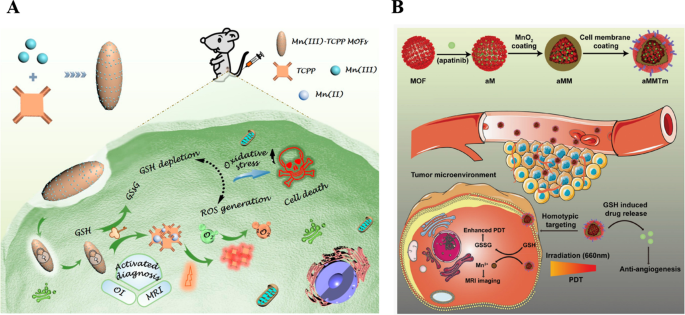
Copyright 2019 American Chemical Society. B Schematische Darstellung der aMMTm-Präparation und der vorgeschlagenen Kombinationstherapie von PDT und Anti-Angiogenese[55]. Copyright 2019 WILEY–VCH Verlag GmbH &Co. KGaA, Weinheim
Schematische Darstellung eines Endozytose-Mn(III)-versiegelten MOF-Nanosystems für MRT und OI-gesteuerte PDT durch kontrollierte ROS-Erzeugung und GSH-Abreicherung nach Entriegelung durch überexprimiertes GSH in Tumorzellen [58].
Das so hergestellte biomimetische Nanosystem für die duale bildgebungsgesteuerte synergistische Tumortherapie war ein einfaches theranostisches System, das einen neuen Weg für die Tumordiagnose und -therapie ebnen würde.
Schwefelwasserstoff (H2 S) Reaktionsschnell
Endogener Schwefelwasserstoff (H2 .) S), als dritter Gasotransmitter, wird über den Katalyseprozess aus dem Enzymsystem der Cystathionin-β-Synthase erzeugt [63, 64]. Cu-basierte MOFs haben eine starke Bindungsfähigkeit von Cu 2+ mit S 2− , und ihre inhärente Aktivität von Cu 2+ besaßen in Säure eine höhere katalytische Aktivität [65]. In den letzten Jahren wurden Cu-MOFs genutzt, um das giftige H2 . nachzuweisen S-Gas im Serum oder in der Lösung [66]. Somit ist H2 S kann als spezifisches „Zielsignal“ für die Diagnose und Therapie von Ovarial- und Dickdarmtumoren erkannt werden [67]. Wie in Abb. 5 gezeigt, stellten Li und seine Mitarbeiter endogenes H2 . bereit S-aktiviertes Cu-MOF befindet sich im "OFF"-Zustand und weist keine offensichtliche Adsorption im NIR-Bereich auf. Wenn jedoch Cu-MOFs in das Dickdarmtumorgewebe eindrangen, wo H2 S wurde überexprimiert, Cu-MOFs können durch Reaktion mit hohen H2 .-Gehalten in den „ON“-Zustand wechseln S-Konzentration, um photoaktives Kupfersulfid mit stärkerer NIR-Absorption zu erzeugen, was die photothermische Therapie (PTT) förderte [68]. Cu-MOFs haben die Peroxidase-Nachahmung und reagierten mit überexprimiertem H2 O2 zur Produktion toxischer Hydroxylradikale für die hämodynamische Therapie nach Endozytose durch die Krebszellen [69]. Somit ist H2 Die S-Triggering-Turn-On-Strategie zeigt hervorragende Antitumorergebnisse und vermeidet unnötige Nebenwirkungen bei der Tumortherapie. Dieses H2 S-getriggerte Nanocarrier können in vivo gezüchtete Dickdarmkrebszellen signifikant hemmen, und diese Biomarker-getriggerten Therapeutika zeigen ein enormes Potenzial für die Tumordiagnose und -therapie.
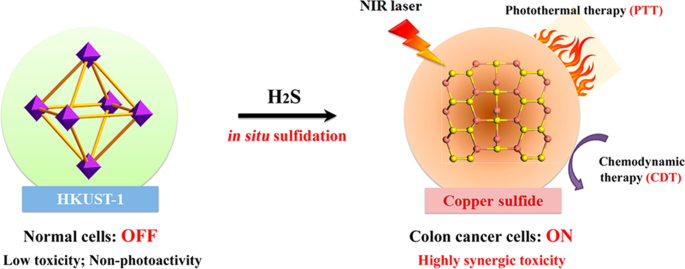
Copyright 2020 American Chemical Society
Schematische Darstellung des H2 S-getriggerte Transformation von nicht-photoaktiven Cu-MOFs-Nanoenzymen in einen Nah-NIR-aktivierbaren photothermischen Wirkstoff durch in-situ-Sulfifizierungsreaktion und ihre weitere synergetische photothermische und chemodynamische Therapie für Dickdarmkrebs [68].
Perspektiven
MOFs als Drug-Delivery-Systeme für die Tumortherapie weisen aufgrund ihrer intrinsischen Eigenschaften, einschließlich struktureller Beständigkeit, hoher Porosität, Multifunktionalität und Biokompatibilität, beispiellose Vorteile auf. Obwohl MOFs im biomedizinischen Bereich beeindruckende Fortschritte erzielt haben, müssen mehrere Schlüsselprobleme angegangen werden, bevor MOFs in die klinische Translationsphase aufgenommen werden können. Dazu gehören komplexierte Synthese, frühe Clearance durch das körpereigene Immunsystem, Systemtoxizität, unbefriedigende Pharmakokinetik und Bioverteilung, Akkumulation außerhalb des Targets und Fähigkeit zur vorzeitigen Wirkstofffreisetzung.
Um diese vielschichtigen Probleme zu lösen, ist das biomimetische Cloaking mit der Plasmamembran eine wirksame Strategie, um das Schicksal von MOFs in vivo zu steuern. Alle Arten von Zellmembranen wurden in großem Umfang zur Tarnung von MOFs verwendet. Dieser biomimetische Ansatz kann MOFs mit der Biogrenzfläche von Zellmembranen bilden, die die von der Spenderzelle geerbten Oberflächenproteine halten, ihre Elimination aus dem körpereigenen Immunsystem reduzieren, um ihre Halbwertszeit im Blut zu verlängern, und MOFs erhöhen, die an der Tumorgewebe über Permeabilitäts- und Retentionseffekte. Basierend auf diesen Vorzügen kombinierten Zellmembran und MOFs biomimetische Plattformen, um die therapeutischen Wirkstoffe für Tumorgewebe zu maximieren und eine Tumortherapie effektiv zu erreichen.
Insbesondere die verzerrten Krebsblutgefäße und die schnelle Vermehrung der Krebszellen würden eine niedrige Sauerstoffkonzentration und eine Übersäuerung in der Tumormikroumgebung (TME) verursachen. Hypoxie, niedriger pH-Wert und hohe GSH-Konzentration sind die gemeinsamen Merkmale des TEM, die Krebsmetastasen und Angiogenese fördern und zu therapeutischer Resistenz führen und die Therapieergebnisse beeinträchtigen. Die Entwicklung umweltempfindlicher und intelligenter MOFs, die durch die Tumormikroumgebung ausgelöst werden, ist ein möglicher Ansatz, um die präzise Diagnose erheblich zu verbessern und unnötige Nebenwirkungen bei der Tumortherapie zu reduzieren.
Schlussfolgerung
In diesem Artikel haben wir verschiedene Arten von MOFs basierend auf ihren einzigartigen Mechanismen und Strukturen zusammengefasst. Komplexes Design, hohe Betriebskosten und langwierige Vorbereitungsschritte sind Hindernisse, auf die MOFs bei der realen Anwendung im klinischen Bereich stoßen. Letztendlich sind eine zielgerichtete Abgabe, geringe bis keine Toxizität und herausragende therapeutische Wirkungen die entscheidenden Faktoren für eine erfolgreiche Übertragung von MOFs in die klinische Anwendung.
Verfügbarkeit von Daten und Materialien
Nicht zutreffend.
Nanomaterialien
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Zellbasierte Arzneimittelabgabe für Krebsanwendungen
- Zebrafisch:Ein vielversprechendes Echtzeit-Modellsystem für die nanotechnologisch vermittelte neurospezifische Wirkstoffabgabe
- 131I-gespurte PLGA-Lipid-Nanopartikel als Wirkstoffträger für die gezielte chemotherapeutische Behandlung von Melanomen
- Nanotechnologie:vom In-vivo-Bildgebungssystem zur kontrollierten Medikamentenabgabe
- Nukleosid-Lipid-basierte Nanoträger für die Sorafenib-Verabreichung
- 5-Aminolävulinsäure-Squalen-Nanoanordnungen für die Tumorphotodetektion und -therapie:In-vitro-Studien
- Untersuchung der physikalisch-chemischen Eigenschaften eines auf Nanoliposomen basierenden Systems für die duale Wirkstoffabgabe
- Eine neue Rolle für das IoT im Gesundheitsversorgungssystem
- 3D-gedruckte Mikroroboter versprechen Arzneimittelabgabe



