Nukleosid-Lipid-basierte Nanoträger für die Sorafenib-Verabreichung
Zusammenfassung
Obwohl die Anwendung von Sorafenib, einem kleinen Inhibitor von Tyrosin-Proteinkinasen, zur Krebsbehandlung eine weltweite Option in der Chemotherapie bleibt, sind neue Strategien erforderlich, um die Probleme mit der geringen Wasserlöslichkeit (< 5 μM), der Toxizität und den Nebenwirkungen dieses Medikaments anzugehen. In diesem Zusammenhang wird derzeit der Einsatz von Nanocarriern untersucht, um diese Nachteile zu überwinden. In diesem Beitrag berichten wir über einen neuen Typ von Sorafenib-basierten Nanopartikeln, die durch hybride Nukleosid-Lipide stabilisiert werden. Die festen Lipid-Nanopartikel (SLNs) zeigten je nach Nukleosid-Lipid-Ladung negative oder positive Zetapotentialwerte. Die Transmissionselektronenmikroskopie von Sorafenib-beladenen SLNs zeigte parallelepipedische Nanopartikel von etwa 200 nm. Biologische Studien, die an vier verschiedenen Zelllinien, einschließlich Leber- und Brustkrebs, durchgeführt wurden, zeigten eine verbesserte Antikrebsaktivität von Sorafenib-basierten SLNs im Vergleich zum freien Medikament. Wichtig ist, dass nach der Inkubation von Krebszellen in Gegenwart von SLNs in hoher Konzentration in Sorafenib (> 80 μM) aufgenommene Kontrastphasenmikroskopiebilder in allen Fällen einen vollständigen Krebszelltod zeigten. Diese Ergebnisse unterstreichen das Potenzial von SLNs auf Nukleosid-Lipid-Basis als Wirkstoffabgabesysteme.
Hintergrund
Sorafenib, das unter dem Namen Nexavar™ vermarktet wird, ist ein hydrophober medikamentöser Kinasehemmer [1], der für die Behandlung verschiedener menschlicher Krebsarten zugelassen ist, einschließlich fortgeschrittenem Nierenzellkarzinom (RCC) [2], hepatozellulärem Karzinom (HCC) [3] und fortgeschrittenem Schilddrüsenkarzinom Karzinom. Sorafenib hat mehrere bekannte Proteinkinase-Ziele, einschließlich Transmembranrezeptoren und intrazelluläre Tyrosin- und Serin-Threonin-Kinasen, und es hat auch gezeigt, dass es Apoptose induziert. In Bezug auf den Wirkmechanismus wird berichtet, dass Sorafenib das Tumorwachstum über Multi-Targets hemmt, indem es direkt auf den Tumor und/oder auf die Tumorangiogenese wirkt (durch Hemmung der VEGFR- und PDGFR-Signalgebung) [4, 5]. Seine Wirksamkeit bei der Hemmung des Wachstums maligner Zellen wurde bei vielen histologischen Krebsarten wie Melanom [6], Schilddrüse [7], Pankreas [5], Leberzellkarzinom und Leukämie [8] nachgewiesen. Die geringe Wasserlöslichkeit, die Toxizität und Nebenwirkungen schränken jedoch die Anwendung von Sorafenib in vielen klinischen Anwendungen ein. Um diese Probleme anzugehen, werden derzeit mehrere Sorafenib-Formulierungen untersucht [9, 10], darunter flüssigkristalline Nanopartikel [11], Nanoemulsion [12], Cyclodextrin-modifizierte poröse Silizium-Nanopartikel [13], Wirkstoff freisetzende Nanokomposite [14], Polyelektrolyte -basierte Nanopartikel [15] oder selbstorganisierte Curcumin-Nanopartikel [16]. Mit Sorafenib beladene Lipid-Nanopartikel (LNs) wurden jedoch nur unzureichend untersucht [17, 18].
Hier berichten wir über das erste Beispiel für Sorafenib-basierte feste Lipid-Nanopartikel (SLNs) [19] stabilisiert durch Nukleosid-Lipide [20,21,22]. Chromatographische Studien an positiv und negativ geladenen Nukleolipiden (DOTAU und diC16 .) dT) weisen darauf hin, dass diese Amphiphile die erforderliche Stabilität und Reinheit für ihre Verwendung im Rahmen von Drug-Delivery-Anwendungen besitzen [23, 24]. Ein einfaches Nanopräzipitationsverfahren ermöglicht die Bildung von SLNs mit entweder positivem (SLN + ) oder negative Ladungen (SLN − ) (Abb. 1). Es ist erwähnenswert, dass alle untersuchten SLNs die zytotoxische Wirkung von Sorafenib auf verschiedene Humankarzinome verstärkten, was zeigt, dass SLNs die Einschränkungen von Sorafenib in Bezug auf Wasserlöslichkeit und Antikrebswirkung überwinden können.
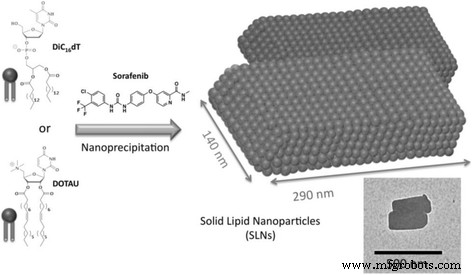
Schema der SLNs-Formulierung. Chemische Strukturen eines anionischen Nukleotid-Lipids, dem Thymidin 3′-(1,2-dipalmitoyl-sn -Glycero-3-phosphat) (diC16 dT), ein kationisches Nukleosid-Lipid DOTAU (2′,3′-Dioleyl-5′-desoxy-5′-trimethyl-ammonium-uridin) und Sorafenib, das in dieser Studie verwendet wurde (links). Schematische Darstellung von SLNs mit parallelepipedischen Formen, die nach der Nanopräzipitation eines Nukleolipids (entweder diC16 dT oder DOTAU, was zu SLN − . führt und SLN + ) mit Sorafenib (rechts). Die schematische Darstellung stammt aus dem Transmissionselektronenmikroskopie-(TEM-)Bild, das DOTAU-Sorafenib-beladene Nanopartikel zeigt (Einschub, Balken 500 nm)
Methoden
Chemikalien und Reagenzien
Methanol (MeOH), Ameisensäure (FA) und Ammoniumformiat (AFNH4) ) wurden von VWR Chemicals (Frankreich) bezogen und waren alle HPLC (Hochleistungsflüssigkeitschromatographie)-Qualität. Wasser in HPLC-Qualität (minimaler spezifischer Widerstand von 18,2 MΩ) wurde intern von ELGA Millipore System (Frankreich) hergestellt. DOTAU (CAS-Nummer:868226-06-6) und diC16 dT (CAS-Nummer:1160002-70-9) wurden im Labor gemäß dem in den Referenzen [23, 24, 25] beschriebenen Protokoll synthetisiert. Sorafenib, 4-[4-[[4-Chlor-3-(trifluormethyl)phenyl]carbamoy-lamino]phenoxy]-N -methyl-pyridin-2-carboxamid (CAS-Nummer:284461-73-0) wurde von SynVec http://synvec.fr (Ref# D114250414) bezogen.
Chromatographiestudium
Für Nukleolipid (DOTAU und diC16 .) wurde eine Umkehrphasen-UHPLC-Methode (Ultra High Performance Liquid Chromatography) entwickelt dT) und Sorafenib-Quantifizierung in SLNs. Vor der Injektion in die HPLC wurden wässrige Lösungen von Nanopartikeln mit Ethanol um Faktor 5 und 10 verdünnt, um Nukleolipide bzw. Sorafenib zu quantifizieren.
Verwendet wurde ein Chromatographiesystem UHPLC UltiMate 3000 von Dionex-Thermo Scientific (USA), bestehend aus einer Pumpe mit einem quaternären Ventilsystem zur Säulenauswahl, einem thermostatisierten Autosampler und einem thermostatisierten Säulenkompartiment. Die Trennung erfolgte mit der Säule Syncronis C18 50 × 2.1 mm, 1.7 µm. Die mobile Phase bestand aus 70/30 MeOH/25 mM Ammoniumacetat (pH =7,4) (A) und 26,5 mM Ammoniumacetat in MeOH (pH =7,9) (B). Es wurde eine Flussrate von 0,2 ml/min verwendet und das Gradientenprofil betrug 0–2 min, 0–100 % B; 2–20 min, 100 % B. Die Säulentemperatur wurde auf 25 °C eingestellt. Der Nachweis wurde bei 267 nm für Sorafenib und diC16 . durchgeführt dT und 257 nm für DOTAU. Das injizierte Volumen betrug 1 μl, was zu Quantifizierungsgrenzen von 0,6 ng für Sorafenib und 15 ng für beide Nukleolipide sowie DOTAU und diC16 . führte dT.
Standardkurven für Sorafenib, DOTAU und diC16 dT in Ethanol wird in der zusätzlichen Datei 1 angezeigt:Abbildungen SI1, SI2 bzw. SI3.
Herstellung von Sorafenib-Nanopartikeln
Zehn Milligramm Sorafenib wurden in 1 ml Ethanol gelöst und 10 mg NLs (entweder diC16 dT oder DOTAU) wurde in 1 ml Ethanol solubilisiert. Einhundert Mikroliter NLs, 100 μL Sorafenib-Lösungen und 800 μL Ethanol wurden bei Raumtemperatur zusammengemischt und tropfenweise in 10 ml destilliertes Wasser unter magnetischem Rühren gegeben. Die Lösung wurde 90 min bei 25 °C in ein Ultraschallbad gegeben. Ethanol wurde unter Vakuum bei 30 °C entfernt und das Volumen auf 1 ml eingestellt. Diese Lösung wurde zweimal mit einer Ultraschallsonde von 6 mm (Vibracell 75186) für 10 Minuten bei 100 % der Amplitude mit einem Puls von 2 Sekunden alle 5 Sekunden beschallt. Ein Milliliter wurde gegen 30 ml destilliertes Wasser für 3 × 15 min dialysiert. Dieses Volumen wird auf 2 ml eingestellt und für die Charakterisierungsquantifizierung und Stabilitätsstudien aufbewahrt. Auch Kontrollexperimente wurden mit dem gleichen Protokoll in Abwesenheit von Nukleolipiden durchgeführt.
Elektronische Transmissionsmikroskopie (TEM und EDX)
Nanopartikel wurden durch Negativfärbungsmikroskopie sichtbar gemacht. Zehn Mikroliter Nanopartikel wurden für 10 Minuten auf ein kohlenstoffbeschichtetes Kupfergitter übertragen. Die Probe wurde dann getrocknet und mit 2,5 % (w /w ) Uranylacetat in Wasser für 2 min. Die Proben wurden mit einem Hitachi H 7650 Elektronenmikroskop betrachtet. Die energiedispersive Röntgenspektroskopie wurde unter Verwendung eines TECNAI-Transmissionselektronenmikroskops in Verbindung mit Quantax-X-Flash SVE 6 durchgeführt.
Partikelgrößen- und Zeta-Bestimmung
Partikelzeta und -größe wurden unter Verwendung eines Zetasizer NanoZS, Malvern, bestimmt. Experimente wurden mit 40 μl der Nanopartikel, verdünnt in 400 μl Wasser, durchgeführt und die Messungen wurden bei 25 °C durchgeführt.
Zytotoxizitätsanalyse
HuH7 und HepG2 wurden einschichtig in DMEM-Glutamax, ergänzt mit 10 % fötalem Kälberserum, gezüchtet. MDA-MB-134 und T-47D wurden in Monolayer in RPMI gezüchtet, ergänzt mit 10 % fötalem Kälberserum (nur für T-47D, nicht essentielle AA 1X, Glukose 0,45 %, Insulin 10 mg L -1 und Natriumpyruvat 1X). Alle Kulturreagenzien stammten von Invitrogen. 10 4 Zellen/Well in 90 μl vollständigem Kulturmedium wurden in eine 96-Well-Platte ausplattiert und 24 h bei 37 °C und 5 % CO2 . inkubiert , bevor Sie dem Kulturmedium 10 μl SLN oder Sorafenib hinzufügen. Sorafenib (CAS-Nummer:284461-73-0) wurde in Kulturmedium mit 0,1% DMSO gelöst. Beachten Sie, dass unter diesen Bedingungen die maximale Konzentration von Sorafenib ohne Ausfällung 5 μM betrug, während für mit Sorafenib beladene SLNs die getestete maximale Konzentration 120 μM ohne DMSO betrug. Nach 4 Tagen Inkubation wurde die Lebensfähigkeit der Zellen mit dem auf Formazan basierenden Proliferationsassay (CellTiter 96® Aqueous One Solution Cell Proliferation Assay kit, Promega) durch Zugabe von 20 μl/Vertiefung Reagenzlösung bewertet. Nach einer 30-minütigen Inkubation bei 37 °C, 5 % CO2 , wurde die Extinktion jeder Vertiefung bei einer Wellenlänge von 492 nm unter Verwendung eines Berthold-Spektrophotometers gemessen. Die Ergebnisse werden als Prozentsatz von \( \frac{{\mathrm{OD}}_{492}\ \mathrm{of}\ \mathrm{behandelte}\ \mathrm{Zellen}-{\mathrm{OD}}_ {492}\ \mathrm{of}\ \mathrm{blank}}{\ {\mathrm{OD}}_{492}\mathrm{of}\ \mathrm{unbehandelt}\ \mathrm{Zellen}-{\mathrm {OD}}_{492}\ \mathrm{of}\ \mathrm{blank}}\).
Zelllebensfähigkeitsstudien
HuH7 wurde wie zuvor im Abschnitt „Zytotoxizitätsanalyse“ beschrieben gezüchtet. Die Lebensfähigkeit der Zellen wurde nach 4 Tagen Inkubation mit SLN + . ermittelt beladen mit Sorafenib in unterschiedlichen Konzentrationen (0, 1, 5, 10, 25, 50 und 100 μM) mit Lebend-/Totzell-Lebensfähigkeitsassay (Invitrogen). Kurz gesagt wurde das Kulturmedium entfernt und anhaftende Zellen wurden einmal mit Hanks' Balanced Salt Solution (HBSS) gewaschen. 200 Mikroliter HBSS mit 2 μM Calceinacetoxymethylester und 4 μM Ethidiumhomodimer-1 wurden in jede Vertiefung gegeben und 45 Minuten bei 37 °C und 5 % CO2 . inkubiert . Nach der Färbung wurden die Zellen einmal mit HBSS gewaschen und mikroskopisch auf einem inversen Fluoreszenzmikroskop abgebildet. Der Prozentsatz an toten Zellen wurde durch fluoreszenzaktivierte Zellsortierung (FACS)-Analyse bestimmt. Nach dem Färben mit 4 μM Ethidium-Homodimer-1-Lösung wurden die Zellen mit Trypsin behandelt und zweimal mit phosphatgepufferter Kochsalzlösung (PBS) durch Zentrifugation bei 1000 U/min für 5 Minuten gewaschen. Die Daten wurden auf einem LSRFortessa-Durchflusszytometer von Becton Dickinson erfasst und die Ergebnisse mit der DIVA-Software analysiert. Eine Probe toter Zellen wurde unter Verwendung von 70 % Methanol hergestellt und als Kontrolle verwendet.
Ergebnisse und Diskussion
Synthese und Charakterisierung von SLNs
Die Nichttoxizität und die Selbstorganisationseigenschaften der Nukleolipide machen sie zu idealen amphiphilen Adjuvantien für die Verkapselung hydrophober Medikamente wie Sorafenib. In dieser Studie wurde ein einfaches Nanopräzipitationsverfahren entwickelt, um die geringen Wasserlöslichkeitseigenschaften von Sorafenib zu berücksichtigen und seine Antikrebsaktivität zu verbessern, was in vielen Fällen seine klinische Anwendung einschränkt. Hinsichtlich der Wasserlöslichkeit stellten wir die Hypothese auf, dass der hydrophobe Charakter, die Heterocyclen und die Wasserstoffbrückenfunktionen von Sorafenib die Wechselwirkungen mit Nukleolipiden und die Bildung von Nanoobjekten begünstigen würden. Es wurde auch erwartet, dass mit Sorafenib beladene SLNs die Antitumor-Aktivitäten erhöhen sollten, indem sie die zelluläre Aufnahme von Sorafenib erhöhen. Tatsächlich haben wir in einer unserer früheren Studien zu Cisplatin-Nanopartikeln gezeigt, dass die Erhöhung der Antitumoraktivität von Cisplatin auf eine erhöhte Menge an Wirkstoff zurückzuführen ist, die in Krebszellen internalisiert wird [23] [1]. Unser Nanopräzipitationsprozess umfasst drei Schritte:(i) die Solubilisierung von Sorafenib in Ethanol bei 40 °C (10 mg/ml Sorafenib, 100 μL) und die Zugabe eines Äquivalents Nukleolipid (entweder ein anionisches Nukleotid-Lipid, das diC16 -3′-dT [Thymidin 3′-(1,2-dipalmitoyl-sn .) -Glycero-3-phosphat)] oder ein kationisches Nukleosid-Lipid DOTAU [23] [2′,3′-dioleyl-5′ -Desoxy-5′-trimethyl-ammonium-uridin], 100 μL einer Lösung mit 10 mg/ml in Ethanol; (ii) 1 ml der Ethanollösung wird tropfenweise bei Raumtemperatur zu 10 ml destilliertem Wasser gegeben; und (iii) die resultierende Suspension wurde eingedampft, um überschüssiges Ethanol zu entfernen, und beschallt.
Chromatographische Studien
Um die Wirkstoffbeladungsfähigkeiten der neuartigen Formulierungen zu bewerten, wurde eine Umkehrphasen-UHPLC-Methode entwickelt. Mit dieser HPLC-Methode wurde die gleichzeitige Trennung von Sorafenib und Nukleolipiden in 12 Minuten erreicht, was die individuelle Quantifizierung von Verbindungen in SLNs ermöglichte (zusätzliche Datei 1:Abbildung SI1–4).
Für Formulierungen, die aus Sorafenib/DOTAU (SLN + ) und Sorafenib/diC16 dT (SLN − ), bzw. Während des Kontrollexperiments, das in Abwesenheit von Nukleolipid durchgeführt wurde, gingen etwa 90 % von Sorafenib während der verschiedenen Schritte der Formulierung verloren, wahrscheinlich aufgrund der geringen Löslichkeit von Sorafenib in Wasser. Dieses Ergebnis zeigt, dass Nukleolipide notwendig sind, um Sorafenib zu solubilisieren und die SLNs zu stabilisieren.
Physikochemische Studien
Dynamische Lichtstreuung (DLS) Experimente wurden durchgeführt, um die Bildung von SLNs zu charakterisieren. Sowohl negative als auch positive Nukleolipide (diC16 .) dT und DOTAU) bilden in wässriger Lösung ähnliche nichtsphärische Nanopartikel mit parallelepipedischer Form mit einer Monodispersität (Polydispersitätsindex, PDI = 0,202 und 0,289; Größe =335,2 bzw. 304,4 nm, Abb. 2 und Zusatzdatei 1:Abbildung SI7). Erwartungsgemäß hängen die Zetapotentiale von SLN-basierten Objekten von den Nukleolipid-Polköpfen ab (ζ = + 59,1 und − 54,9 mV für SLN + und SLN − , siehe Zusätzliche Datei 1:Abbildung SI10). Das Vorhandensein von Sorafenib im NP wurde durch TEM-Bildgebung validiert und EDX-Aufnahmen eines SLN− wurden mit EDX-Aufnahmen realisiert. Abb. 2e, f zeigt I- und II-Punkte. Fleck I in Abb. 2f zeigt die Emission von Chloratomen (Spot I, Abb. 2e, f), was die Anwesenheit von Sorafenib anzeigt (siehe chemische Struktur Abb. 2f). Beachten Sie, dass Chlor nur in Punkt I und nicht in Punkt II vorhanden ist (Abb. 2f).
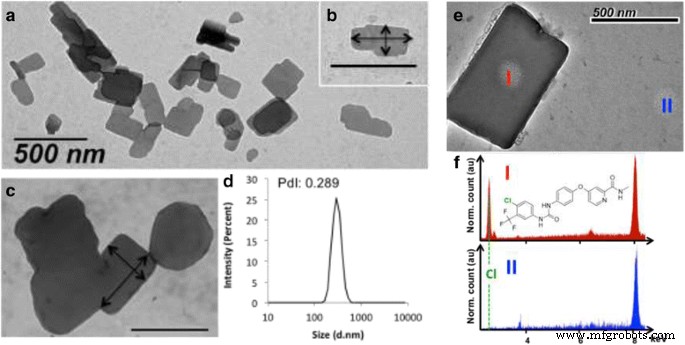
Charakterisierung von SLNs. Transmissionselektronenmikroskopie (TEM)-Bilder, die die Morphologie von Sorafenib-Nanopartikeln mit DOTAU zeigen (a ) und Einschub (b ). Beispiel für ein DOTAU-basiertes SLN mit einer Größe von 327 x 172 nm (Pfeile), das eine durchschnittliche Größe von 304 nm bestätigt, gemessen mit DLS (d ). c Beispiel für ein TEM-Bild mit diC16 dT-SLNs (Pfeile 330 x 500 nm). (e ) TEM-Aufnahme eines SLN-. I &II Spots sind die Lokalisierungen, an denen EDX-Erfassungen durchgeführt wurden. (f ) EDX-Spektren an den Positionen I &II. Die gestrichelte Linie betont die Emission von Chloratomen, die nur in I vorhanden sind. Die chemische Struktur des Sorafenib-Moleküls ist ebenfalls dargestellt. Beide Spektren wurden mit der Cu-Atom-Emission bei 8 keV (aufgrund des TEM-Cu-Gitters) normalisiert
Wichtig ist, dass in Kontrollexperimenten die Nanopräzipitation von Sorafenib in Abwesenheit von Nukleolipiden zu keinem Nanoobjekt führte, was zeigt, dass die Nukleolipide die Bildung und Stabilisierung der SLNs ermöglichen.
Stabilitätsstudien
Kolloidale Stabilität von SLN + und SLN − wurden durch DLS und Zetapotential bei zwei Temperaturen gemessen (Abb. 3a und zusätzliche Datei 1:Abbildung SI10). Im Fall von diC16 dT-basierte Formulierungen, die Größe von SLN − wurde nach 30 Tagen bei 4 und 37 °C nicht verändert, was auf eine hohe Stabilität dieser Nanopartikel hinweist (zusätzliche Datei 1:Abbildung SI9). Diese Stabilität kann durch die Natur der Wechselwirkungen erklärt werden (mit H-Brücken, π -π Stapeln, Ladung/Ladungs-Wechselwirkung), die zwischen den diC16 . auftritt dT und Sorafenib. Für DOTAU-basierte Formulierungen jedoch SLN + waren nur bei 4 °C für 30 Tage stabil, wie DLS-Studien zeigten (Abb. 3a), während bei 37 °C eine Zunahme sowohl der Größe als auch des PDI beobachtet wurde (Abb. 3a). Diese relative Instabilität wurde bei 37 °C im Fall von SLN + . beobachtet könnte durch abstoßende Coulomb-Wechselwirkungen zwischen den positiven Ladungen von Sorafenib und DOTAU erklärt werden. Interessanterweise weisen die Studien zur kolloidalen Stabilität darauf hin, dass es möglich ist, die Stabilität, also die Abgabe von Sorafenib aus den SLNs in die physiologische Umgebung, abhängig von dem zur Stabilisierung der SLNs verwendeten Nukleolipid zu modulieren. Die Stabilitätsmodulation könnte abhängig von der benötigten Freisetzungskinetik attraktiv sein.
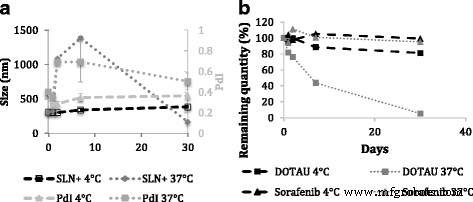
Stabilitätsstudien von SLNs. Kolloidale Stabilität von SLN + (a ) und chemische Stabilität von Sorafenib und DOTAU bei SLN + gegen die Zeit bei 4 und 37 °C (b ). PDI, Polydispersitätsindex
Parallel zur kolloidalen Stabilität ist die chemische Stabilität von Sorafenib, DOTAU und diC16 dT in den SLN-basierten Formulierungen wurde als Funktion der Zeit bei 4 und 37 °C mit einer neuen chromatographischen Methode untersucht (siehe Zusatzdatei 1:Abbildung SI4). Kinetische Studien bei beiden Temperaturen sind in Abb. 3b und Zusatzdatei 1 dargestellt:SI5 für DOTAU-SLNs und diC16 dT-SLNs bzw. Die Ergebnisse zeigen, dass Sorafenib und diC16 dT-Moleküle in Formulierungen bleiben über mindestens 1 Monat stabil, was im Fall von SLN − . auf eine langfristige chemische Stabilität bei beiden Temperaturen hinweist . Im SLN + . wurde jedoch eine Abnahme von DOTAU im Laufe der Zeit beobachtet Formulierungen. Zunächst wurden bei 4 °C Verluste von etwa 12 % über 7 Tage und 20 % über 30 Tage gemessen. Wenn die Temperatur erhöht wurde, nahm die DOTAU-Stabilität mit einem Verlust von 55 % über 7 Tage und auf 95 % über 30 Tage bei 37 °C ab. Solche Unterschiede in der chemischen Stabilität zwischen Nukleolipiden wurden bereits in früheren Stabilitätsstudien nachgewiesen (siehe zusätzliche Datei 1:Abbildung SI6).
Biologische Studien
Die Zytotoxizität von SLN wurde anhand der Stoffwechselaktivitäten und Morphologien der Zellen bewertet. Der MTT-Assay ermöglichte den Vergleich von freiem Sorafenib (in 0,1 % von DMSO) und mit dem Arzneimittel beladenen SLNs (Abb. 4) auf vier Zelllinien, darunter zwei Hepatokarzinome (HuH7 und HepG2) und zwei luminale Brustkrebsarten (MDA-MB-134 und T-). 47D). Erstens bei Konzentrationen nahe der maximalen Löslichkeit von freiem Sorafenib (5 μM Sorafenib in 0,1 % DMSO, 2,8 μM für Sorafenib/DOTAU und 4 μM für Sorafenib/diC16 .). dT-Nanopartikel) hemmten beide SLNs die Lebensfähigkeit der Zellen besser als freies Sorafenib. Wie in Abb. 4b gezeigt, zeigte eine an MDA-MB-134-Zellen durchgeführte Zelllebensfähigkeitsstudie, dass die Aktivität von freiem Sorafenib durch seine Wasserlöslichkeit (100 % der Zelllebensfähigkeit bei [Sorafenib] = 5 μM) begrenzt ist, während IC50 Werte von 15 und 50 μM wurden für SLN + . beobachtet und SLN − , bzw. (Abb. 4b). In einer FACS-Studie mit HuH7 wurde ein IC50 . erreicht von ungefähr 50 μM wurde erhalten (Zusatzdatei 1:Abbildungen SI12 und SI13). Bilder der Phasenkontrastmikroskopie zeigen tatsächlich eine verringerte Dichte der Zellschichten, die entweder mit SLN − . behandelt wurden und SLN + im Vergleich zu unbehandelten oder mit Sorafenib behandelten Zellen ohne Veränderung der Zellmorphologie (zusätzliche Datei 1:Abbildung SI11). Zweitens wurden ähnliche Experimente bei höheren Konzentrationen von SLNs durchgeführt ([Sorafenib] = 120 und bei 84 μM für SLN − und SLN + ) und verglichen mit freiem Sorafenib an seiner Löslichkeitsgrenze (Konzentration von 5 μM). Unter diesen Bedingungen zeigen beide SLNs eine starke zytotoxische Wirkung auf die vier Krebszelllinien, wie in Abb. 5 gezeigt. Wie die Phasenkontrastmikroskopie-Bilder zeigen, wurden Zelltrümmer für beide SLN − . beobachtet (Abb. 5C1–4) und SLN + (Abb. 5D1–4), die den Zelltod bestätigt, während die Zellen im Fall von freiem Sorafenib am Leben bleiben (Abb. 5B1–4). Es ist erwähnenswert, dass bei luminalen B-Brustkrebszellen starke zytotoxische Effekte für beide SLNs beobachtet wurden (Abb. 5C1–2 und D1–2). Eine solche antitumorale Wirkung, die bisher nicht berichtet wurde, eröffnet dank der SLNs neue mögliche therapeutische Anwendungen von Sorafenib.
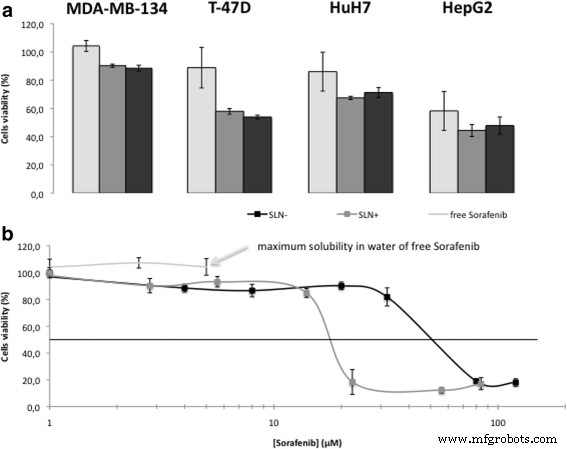
Zytotoxizitätswirkung von Sorafenib oder SLNs. a ) Vergleich der Zytotoxizität mit freiem Sorafenib oder SLNs von Sorafenib in 4 Zelllinien (2 luminaler B-Brustkrebs und 2 Hepatokarzinome) nach Quantifizierung mit MTS-Assay auf 3 Wells mit 5 μM freiem Sorafenib, 2,8 μM NPs Sorafenib/DOTAU (SLN+ .) ) und 4 μM der NPs Sorafenib/diC16dT (SLN-). b ) Zellviabilitätsassay (MDA-MB-134-Zellen) in Gegenwart von freiem Sorafenib (begrenzte Löslichkeit), SLN+ (grau) oder SLN- (schwarz)
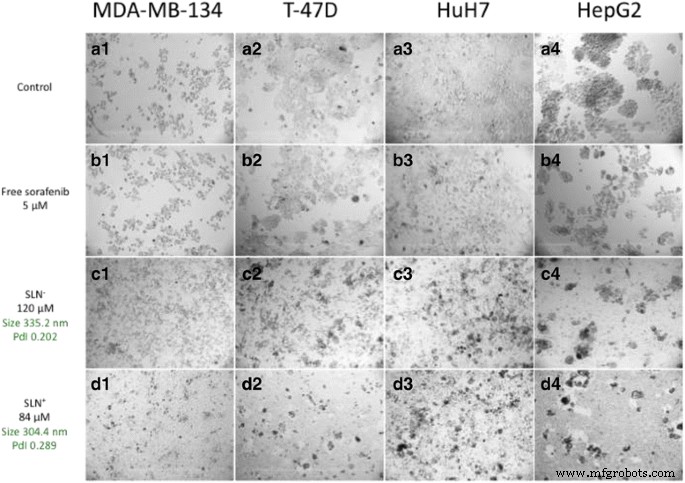
Vergleich der Zellmorphologien zwischen Kontrolle, freiem Sorafenib oder SLNs. Phasenkontrastmikroskopiebilder, die Zytotoxizität unter verschiedenen Bedingungen an vier menschlichen Karzinomzelllinien (den Hepatokarzinomen, HuH7, HepG2 und dem luminalen Mammakarzinom MDA-MB-134, T-47D) zeigen. A) In Abwesenheit von Sorafenib (Kontrollexperimente, A1 –A4 für MDA-MB-134, T-47D, HuH7, HepG2 bzw. Zelllinien). B) Zellen wurden 4 Tage lang in Gegenwart von 5 μM freiem Sorafenib inkubiert. C und D) Zellen inkubiert in Gegenwart von SLN − und SLN + bei 84 bzw. 120 μM Sorafenib-Konzentration
Schlussfolgerung
Wir berichten über einen neuartigen Ansatz, der auf Nukleolipiden basiert und die effiziente Verkapselung und Abgabe von Sorafenib ermöglicht. Unsere Untersuchungen zeigen die Bildung von zwei Arten von Festlipid-Nanopartikeln (SLNs), die hoch mit Sorafenib beladen sind. Diese SLNs, die entweder negative oder positive Zetapotentialwerte aufweisen, weisen parallelepipedische Formen auf. Wie die DLS- und HPLC-Studien gezeigt haben, kann die Stabilität der SLNs je nach verwendetem Nukleolipid moduliert werden. Wichtig ist, dass sowohl SLN + und SLN − Formulierungen sind in der Lage, die Wasserlöslichkeit von Sorafenib (Konzentrationen höher als 120 μM) dramatisch zu verbessern. Solche SLNs zeigen bessere antitumorale Aktivitäten auf vier Krebszelllinien (Leber- und Brustkrebs) im Vergleich zu freiem Sorafenib, das aufgrund seiner fehlenden Wasserlöslichkeit eingeschränkt ist. Kontrastphasenmikroskopie-Bilder, die von den vier Krebszelllinien aufgenommen wurden, zeigen eine drastische Zellsterblichkeit, wenn sie mit 120 μM SLN − . inkubiert wurden oder 84 μM SLN + . Somit könnte dieses Medikament als neue Therapieoption bei Leberkrebs (z. B. Anwendung von Sorafenib in der intraarteriellen Chemotherapie) oder Brustkrebs eingesetzt werden. Unseres Wissens ist dieser Bericht das erste Beispiel einer Studie, in der Sorafenib gegen luminales B-Brustkrebs eingesetzt wurde und die Nützlichkeit des SLN-Ansatzes demonstriert. Insgesamt unterstreichen die in diesem Beitrag berichteten Ergebnisse das Potenzial von SLNs auf Nukleosid-Lipid-Basis als Wirkstoffabgabesysteme.
Abkürzungen
- AFNH4 :
-
Ammoniumformiat
- DLS:
-
Dynamische Lichtstreuung
- FA:
-
Ameisensäure
- HCC:
-
Hepatozelluläres Karzinom
- HPLC:
-
Hochleistungsflüssigkeitschromatographie
- LNs:
-
Lipid-Nanopartikel
- MeOH:
-
Methanol
- PDI:
-
Polydispersitätsindex
- RCC:
-
Nierenzellkarzinom
- SLNs:
-
Feste Lipid-Nanopartikel
- UHPLC:
-
Ultra-Hochleistungs-Flüssigkeitschromatographie
Nanomaterialien
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Nano-Heterojunctions für Solarzellen
- Umweltverträgliche Metall-organische Gerüste als Wirkstoffabgabesystem für die Tumortherapie
- Drei Grundlagen der Routenplanung für große Einzelhändler
- So verbessern Sie die Zustellung auf der letzten Meile für kleine Sendungen
- Sechs Möglichkeiten, sich auf sperrige Bestellverzögerungen vorzubereiten
- Versand am selben Tag aus dem Geschäft? Fünf Tipps für eine schnellere Lieferung
- Die Zukunft der kontaktlosen Lieferung
- Eine neue Rolle für das IoT im Gesundheitsversorgungssystem
- 3D-gedruckte Mikroroboter versprechen Arzneimittelabgabe



