Verbesserte plasmonische Biosensoren von Hybrid-Goldnanopartikel-Graphenoxid-basiertem markierungsfreiem Immunoassay
Zusammenfassung
In dieser Studie schlagen wir ein modifiziertes Gold-Nanopartikel-Graphenoxidblatt (AuNP-GO)-Nanokomposit vor, um zwei verschiedene Wechselwirkungen zwischen Proteinen und hybriden Nanokompositen für den Einsatz in biomedizinischen Anwendungen zu erkennen. GO-Faltblätter haben eine hohe Bioaffinität, die die Bindung von Biomolekülen an Carboxylgruppen erleichtert und zu ihrer Verwendung bei der Entwicklung von Sensormechanismen geführt hat. Wenn GO-Schichten mit AuNPs dekoriert sind, führen sie lokalisierte Oberflächenplasmonenresonanz (LSPR) in den Resonanzenergietransfer spektraler Änderungen ein. Unsere Ergebnisse legen eine vielversprechende Zukunft für AuNP-GO-basierte markierungsfreie Immunoassays nahe, um Krankheitsbiomarker zu erkennen und Infektionskrankheiten schnell zu diagnostizieren. Die Ergebnisse zeigten den Nachweis von antiBSA in 10 ng/ml hCG-unspezifischem Störprotein mit dynamischen Reaktionen im Bereich von 1,45 nM bis 145 fM und einer LOD von 145 fM. Angesichts des breiten Anwendungsspektrums von GO-Plättchen als Wirtsmaterial für eine Vielzahl von Nanopartikeln kann der hier entwickelte Ansatz für die zukünftige Integration von Nanopartikeln mit GO-Nanoblättern für die Blutsensorik von Vorteil sein. Die hervorragenden Anti-Interferenz-Eigenschaften ermöglichen den Einsatz des Biosensors in der klinischen Analyse und Point-of-Care-Testing (POCT)-Diagnostik von Schnellimmunoassay-Produkten, und er kann auch ein potenzielles Werkzeug für die Messung von Biomarkern in Humanserum sein.
Hintergrund
Auf Kohlenstoffmolekülen basierende Materialien wie Kohlenstoffnanoröhren [1, 2], Kohlenstoffkugeln (Buckminsterfulleren, C60) [3], zweidimensionales Graphen [4,5,6] und Graphenoxid (GO) [7,8,9 ,10,11] sind in Biosensoren weit verbreitet. Unter ihnen ist die zweidimensionale Schichtstruktur von Graphen ein ideales Material, um dünne Filme mit hoher Leitfähigkeit [12, 13] und ausgezeichneter optischer Permeabilität [14] und hoher Biokompatibilität [15, 16] zu ermöglichen. Aus diesen Gründen wird Graphen-basiertes Material in der biomedizinischen und elektrochemischen Sensortechnologie häufig verwendet [17, 18]. Darüber hinaus basiert der photoelektrische Typ der biologischen Sensortechnologie hauptsächlich auf GO [19,20,21]. Da Oxidgruppen so eingestellt werden können, dass sie eine Lichtbandlücke absorbieren und abstrahlen [22, 23], werden sie häufig in der Fluoreszenz [24], Oberflächenplasmonenresonanz (SPR) [8,9,10,11, 19,20,21 . verwendet ] und lokalisierte Oberflächenplasmonenresonanz (LSPR) [25, 26] Sensortechnologie. Insbesondere hat GO einzigartige chemische funktionelle Gruppen (Epoxidbrücken, Hydroxylgruppen, paarweise Carboxylgruppen (Carboxyl und Carbonyl)), die die Affinität und kovalente Bindung von Biomolekülen verbessern.
Die Synthese von Graphenmaterial in Kombination mit Nanopartikeln (wie Pt, Au, Ag, Pd und ZnO) wurde für die Entwicklung neuer Nanokomposit-Technologien umfassend untersucht. Insbesondere die Verwendung von Goldnanopartikeln (AuNPs) wurde als Mechanismus für den Energietransfer in der kolorimetrischen und Absorptionsspektroskopie verwendet. Darüber hinaus hat die Forschung an AuNPs im sichtbaren Licht während des letzten Jahrzehnts die einzigartigen plasmonischen Resonanzeigenschaften hervorgehoben. Da die Anpassung der Größe und Form von AuNPs die Wellenlängenverschiebung der optischen Absorption ändern kann, können AuNPs für eine verbesserte Plasmaabsorption und Signalverstärkung verwendet werden [27, 28]. Daher werden AuNPs aufgrund ihrer speziellen optischen und optoelektronischen Eigenschaften in einem breiten Anwendungsspektrum wie optoelektronischen Komponenten zur Verbesserung der Lichtextraktion [29, 30] und Lichtabsorptionsreaktionen [31, 32, 33] umfassend eingesetzt. Darüber hinaus sind AuNPs biokompatibel und wurden auf ihre Verwendung in der chemischen Sensorik, biomedizinischen Bildgebung, Krebstherapie [34, 35], Wirkstoffträger [32, 33], photothermische Therapie [36, 37, 38] untersucht. Kontrastmittel [39], Radiosensibilisator [40] und Biosensorik [33, 41, 42, 43] Anwendungen.
Die Funktionalität der AuNPs wurde durch Hinzufügen des Crosslinkers modifiziert, um Oxidation zu vermeiden und als Träger von sekundären Pflanzenstoffen oder Vektoren zu fungieren; somit kann diese Kombination die Biokompatibilität und Bioaktivität erhöhen [44,45,46]. Crosslinker wie Cystamin (Cys) oder 8-Mercaptooctansäure (MOA) werden durch selbstorganisierte Monoschichten (SAMs) mit Carbonsäure-terminierten Thiolen auf einer modifizierten Au-Oberfläche aktiviert. MOA bindet über den Thiollinker (-SH-Ende) an die Au-Oberfläche, was zu Monoschichten führt.
Darüber hinaus wurde auch viel über die Forschung zu Plasmonmetallmaterial berichtet. Beispielsweise wurde gezeigt, dass plasmonische Metallkern-Schale-Nanopartikel [47], Nanosterne [48] und fluordotierte Zinnoxid-Nanopartikel [49] die Energiebandlücke erhöhen, was sie in Solarzellen- und Sensoranwendungen wünschenswert macht.
Darüber hinaus wurde über die Verwendung von AuNP-GO-Hybriden basierend auf chemischer Synthese [50,51,52] und elektrostatischer Selbstorganisation [53] in Sensor-, Energie- und katalytischen Anwendungen berichtet. In den letzten Jahren hat sich die Forschung zunehmend auf die Verwendung von AuNP-GO-Hybriden in Biosensoren konzentriert. Diese Hybride haben sich bei der Entwicklung der elektrochemischen [54,55,56,57,58,59] und der oberflächenverstärkten Raman-Streuung (SERS) [56, 59] als nützlich erwiesen, um die Anwendung in biologischen Assays zu verbessern. Derzeit gibt es jedoch keine relevanten Berichte über die Verwendung von Biosensor-Technologie mit bloßem Auge oder kolorimetrischer Schnellimmunoassay. So wurden beispielsweise elektrochemische DNA-Biosensoren auf Basis von AuNP-GO-Hybriden zum Nachweis von Brustkrebs-Biomarkern verwendet, um eine frühzeitige Diagnose zu ermöglichen. Mit diesem Biosensor wurde die Nachweisgrenze (LOD) von 0,16 nM bei einer Sensitivität von 378 nA/nM für den Biomarker ERBB2 erreicht [54]. Darüber hinaus wurde ein elektrochemischer Aptasensor auf der Basis von AuNP auf Nanokomposit-Nanokomposit-Basis mit punktierter Reduktion aus Graphenoxid (rGO-AuNP) verwendet, um selektiv eine Konzentration von 3,3′4,4′-polychlorierten Biphenylen (PCB77) zwischen 1 pg L – . nachzuweisen 1 und 10 μg L − 1 , mit einer LOD von 0,1 pg L − 1 [55]. Darüber hinaus wurden AuNP-GO-Hybride als elektrochemischer Biosensor zum Nachweis von Wasserstoffperoxid (H2 O2 ), mit einer Lebensmitteldynamik von 0,1 bis 2,3 mM und einer LOD von 0,01 mM [57]. Ein weiteres gutes Beispiel ist die Verwendung von AuNP-GO [56, 59] und AuNP-Graphen [59] Hybriden für SERS-basierte Biosensoren in verschiedenen Anwendungen sowie SERS-gemessene Biobildgebung.
In dieser Studie schlagen wir eine alternative Methode der chemischen Synthese und elektrostatischen Selbstorganisation von AuNP-GO-Hybriden mit schichtweiser Selbstorganisation vor. Wir analysieren auch die biologische Nachweisempfindlichkeit der modifizierten kombinierten AuNPs und GO-Faltblätter und ihre Protein-Immunantwort. Wir haben zwei Arten von AuNP-GO-basierten proteinmarkierungsfreien Immunoassays entwickelt und ihre Reaktionszeit und Sensitivität bei Antigen-Antikörper-Wechselwirkungen untersucht. Zu den hervorragenden Sensoreigenschaften von Graphen-AuNP-Kompositen zählen die ultrahohe Sensitivität und die Affinität von Biomolekül-Wechselwirkungen, die den Nachweis einer Vielzahl von Biomolekülen mit hoher Spezifität beeinflussen. Diese Eigenschaften implizieren, dass diese Verbundwerkstoffe eine vielversprechende Rolle in zukünftigen Anwendungen spielen und das Potenzial haben, der bevorzugte Weg zur Erkennung von Krankheiten in klinischen Diagnoseanwendungen zu sein.
Methoden/Experimental
Materialien
Graphit wurde von Graphene Supermarket (Graphene Laboratories Inc., Reading, MA, USA) bezogen. GO-Blätter wurden aus Graphitflocken erhalten, indem eine modifizierte Hummer-Methode [60] verwendet wurde, gefolgt von einer Ultraschallzertrümmerung für 5 h für eine Flockengröße von 0,1–1 μm und eine Dicke von 1,1 nm. Cystamindihydrochlorid (Cys, 96%), Hydrogentetrachloroaurat(III)-trihydrat (HAuCl4 ·3H2 O), ACS, 99,99 % (Metallbasis) und Au 49,5 % min wurden von Alfa Aesar Co. (USA) bezogen. Natriumcitrat (HOC(COONa)(CH2 .) COONa)2 ·2H2 O) wurde von J.T. Baker Chemical Co. (USA). Rinderserumalbumin (BSA, SI-B4287, Sigma-Aldrich, USA), Anti-Rinderalbumin-Antikörper, hergestellt in Kaninchen (antiBSA, SI-B1520, Sigma-Aldrich, USA), N -Hydroxysuccinimid (NHS) und 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimid (EDC) wurden von Sigma-Aldrich Inc. (USA) bezogen. Die Immunglobuline (Ig) mit Anti-BSA-Antikörperstruktur wurden von B-Lymphozyten produziert und in das Plasma sezerniert. Die monomeren Formen von Ig-Molekülen waren Glykoproteine mit einem Molekulargewicht von etwa 150 kDa. Jedes Ig-Monomer war in der Lage, zwei Antigenmoleküle zu binden. Alle Reagenzien und Lösungsmittel wurden ohne weitere Reinigung verwendet.
Wir verwendeten drei verschiedene Temperaturbedingungen bei 550, 400 und 100 °C mit Siedezeiten von 5, 5 bzw. 120 Minuten, um die Reduktion der Nanopartikel zu kontrollieren. Diese unterschiedlichen Temperaturen reduzierten die Nanopartikel, um das gleiche Absorptionsspektrum bei 520 nm zu erhalten, wie in der zusätzlichen Datei 1:Abbildung S1 deutlich zu sehen ist.
Synthese von AuNPs
Die zur Gewinnung von AuNPs verwendete Methode basierte auf der Verwendung von Natriumcitrat als Reduktionsmittel, um Tetrachloraurat-Taurin-Ionen in Wasser zu reduzieren. Ein Volumen von 15 ml HAuCl4 ·3H2 O-Lösung mit 1 mM Au wurde unter Rückfluss erhitzt und 1,8 ml 38,8 mM Natriumcitrat (Na3 C6 H5 O7 )-Lösung wurde zu der siedenden (550 °C, 1100 U/min) Lösung gegeben. Die Reduktion der Goldionen durch die Citrat-Ionen war nach 5 min abgeschlossen, und die Lösung wurde 30 min weiter gekocht (400 °C, 900 U/min) und dann auf Raumtemperatur abkühlen gelassen [36, 61, 62]. Diese Methode liefert kugelförmige AuNPs mit einem durchschnittlichen Durchmesser von etwa 15 nm, und eine reduzierte Konzentration von 0,8 ml von 38,8 mM Natriumcitrat kann verwendet werden, um AuNPs mit einem durchschnittlichen Durchmesser von etwa 60 nm herzustellen [63, 64]. Die chemische Reaktion ist wie folgt:HAuCl4(aq) + C6 H5 O7 Na3(aq) → Au(s) + CO2 + HCOOH.
Vorbereitung von GO basierend auf einem Antigen-Ziel
Wir haben eine Immunoassay-Methode entwickelt, um GO-Faltblätter herzustellen, wie in Abb. 1 gezeigt. Wir verwendeten eine 200-μl-GO-Faltblattlösung mit einer Konzentration von 0,1 g/l und die Aktivierung von Carboxylendgruppen auf der Oberfläche von GO-Faltblättern für kovalente Bindungen Die Bildung zur Immobilisierung von Kohlenwasserstoffketten wurde mit einer Mischung aus 400 μM (EDC)/100 μM (NHS) in einem Volumenverhältnis von 1:1 durchgeführt. Das BSA-Protein wurde mit EDC/NHS an den Enden von GO-Faltblättern immobilisiert, um kovalente Bindungsreaktionen zwischen Carboxylgruppen auf GO und –HN2 . zu aktivieren und zu fördern von BSA. Die aktivierte –COOH-Oberfläche wurde dann einer starken kovalenten Immobilisierung über ein Amin (NH2 )-Kopplungsreaktion mit 20 μl BSA-Protein in einer Konzentration von 100 μg/ml. Schließlich haben wir eine Zentrifuge verwendet, um wiederholt nicht immobilisiertes BSA-Protein auf der GO-Oberfläche zu entfernen. Das GO-BSA-Antigenzielverfahren ist in Abb. 1 dargestellt.
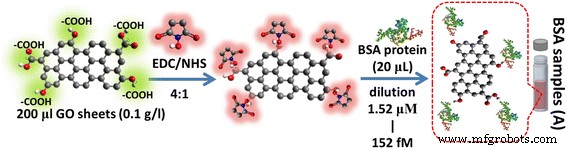
GO-BSA-Interaktion. Die Carboxylgruppe von GO-Blättern kann durch EDC/NHS-Reaktion und Herstellung des GO basierend auf dem Antigen-Target für GO-BSA aktiviert werden
Herstellung von AuNPs und AuNP-GO basierend auf einer Antikörpersonde
Wir führten eine Oberflächenfunktionalisierung mit Cys mit 15-nm-AuNPs in einem Volumen von 200 μL durch. Die AuNPs wurden unter Verwendung einer derivatisierten, selbstorganisierten Thiol-Monoschicht von Cys chemisch modifiziert. Die AuNPs wurden 2 h bei Raumtemperatur in eine Lösung von Cys (10 mM) getaucht. Aufgrund der starken AuNP-S-Bindung (Thiolbindung) kann Cys leicht mit AuNPs und –NH2 . verbinden auf der Oberfläche von AuNPs–Cys–NH2 . exponierte Gruppen . Anschließend fügten wir 20 μl Antikörper (antiBSA) von 100 μg/ml Protein hinzu, um die Oberfläche der AuNPs zu immobilisieren, gefolgt von einer wiederholten Zentrifugation, um nicht immobilisiertes Cys auf der Oberfläche der AuNPs zu entfernen. Entionisiertes Wasser wurde dann verwendet, um alle nicht immobilisierten AuNPs zu entfernen (Cys ist eine Aminothiolstruktur, die nicht durch EDC/NHS aktiviert werden muss). Das an die AuNPs gebundene Cys hatte Amin (–NH2 )-Gruppen, die kovalent mit Carboxylgruppen (–COOH) auf der Oberfläche von antiBSA gekoppelt sind. Schließlich verwendeten wir wiederholte Zentrifugation, um nicht-immobilisiertes Anti-BSA-Protein von der Oberfläche der AuNPs zu entfernen. Eine Reihe von Anti-BSA-Proteinkonzentrationen wurde durch serielle Verdünnung von 100 μg/ml auf 1 pg/ml hergestellt. Die Herstellung der AuNP-antiBSA-Sonde bei verschiedenen Antikörperkonzentrationen ist in Abb. 2a gezeigt.
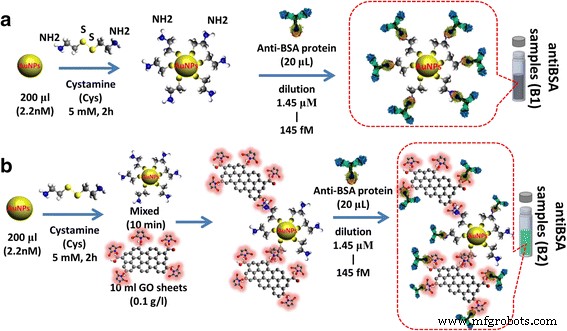
AuNP-antiBSA- und AuNP-GO-antiBSA-Wechselwirkungen. Vorbereitung der a AuNPs und b AuNP-GO basierend auf Antikörpersonde
Wir verwendeten AuNPs, die mit der GO-Faltblatt-Methode hergestellt wurden, um das AuNP-GO-Nanokomposit zu modifizieren. Die AuNPs wurden mit der Natriumcitrat-Reduktionsmethode hergestellt und die Größe der 60-nm-AuNPs wurde mit Cys (5 mM) modifiziert. Anschließend verwendeten wir EDC/NHS, um die –COOH-Gruppen auf der Oberfläche der GO-Blätter zu aktivieren. Die an die AuNPs gebundenen Cys enthalten –NH2 kovalent mit –COOH-Gruppen gekoppelte Gruppen auf der Oberfläche der GO-Faltblätter. Die AuNPs auf der Oberfläche der GO-Schichten wurden mithilfe eines Cys-Linkers immobilisiert, um kovalente Bindungsreaktionen zwischen den AuNPs und GO zu fördern. Die kovalente Kopplung bietet eine stabile und einfache Methode zur Bindungsoberflächenfunktionalisierung auf GO-Schichten. Die GO-Blätter wurden gründlich mit entionisiertem Wasser gespült, um ungebundenes GO an der AuNP-Linker-Oberfläche zu entfernen. Das AuNP-Cys bildete einen neuen Verbund von AuNP-GO, gefolgt von einer Immobilisierung mit verschiedenen Verdünnungskonzentrationen von 100 μg/ml bis 1 pg/ml Antikörper-(antiBSA)-Sondenprotein, um AuNP-GO-antiBSA zu bilden, wie in Abb. 2b.
Charakterisierung von AuNPs und GO Sheets
Die Dispersion und Morphologie von AuNP-GO-Schichten wurden unter Verwendung eines 300-kV-Feldemissionskanonen-Transmissionselektronenmikroskops (FEG-TEM; Tecnai G2F30S-Twin, Philips-FEI, Amsterdam, Niederlande) und eines hochauflösenden Transmissionselektronenmikroskops ( HR-TEM) auf einem FEI Tecnai G20 System (Hillsboro, OR, USA). Die Dispersion und Morphologie der AuNP-GO- und GO-Schichten wurden unter Verwendung eines extrem auflösenden analytischen Feldemissions-Rasterelektronenmikroskops JEOL JSM-7800F Prime (JEOL Inc., USA) charakterisiert. Das UV-Vis-Transmissionsspektrum (UV-vis) eines Doppelstrahl-Spektrophotometers wurde mit einem UV-Vis-Spektrophotometer (U-2900, Hitachi High-Technologies Corporation, Tokio, Japan) mit einer Wellenlänge von 200 bis 1100 nm bei Raumtemperatur beobachtet . Raman-Messungen wurden unter Verwendung eines mikroskopischen Raman-Systems (MRI, Protrustech Co., Ltd., Taiwan) durchgeführt. Als Detektor wurde ein luftgekühltes Spektrometer (AvaSpec-ULS2048L) mit 1800 Linien/mm Gitter und 50 µm Spalt verwendet. Fourier-Transform-Infrarotspektrometer (FTIR)-Messungen wurden mit einem Bruker Vertex 80v-Spektrometer im abgeschwächten Totalreflexionsmodus (ATR) und einem DTGS-Detektor (64 Scans) mit einer Auflösung von 2 cm − 1 . durchgeführt auf einem KBr-Pellet im Vakuum bei einem Druck von etwa 6 Pa. Das Instrumentation Center der National Tsing Hua University unterstützte diese Arbeit. Röntgenphotoelektronenspektroskopie (XPS) wurde unter Verwendung der Einrichtungen des National Synchrotron Radiation Research Center, Hsinchu, Taiwan, durchgeführt. Die Photoelektronenspektroskopie-Experimente wurden mit einer 09A2 U5-Spektroskopie-Beamline für XPS durchgeführt. Photonen mit festen Energien von 380 und 900 eV wurden für C (1s) und Co (2p) während der gesamten Photoelektronenspektroskopie-Experimente auf Kernebene verwendet. Die Experimente wurden im Total-Electron-Yield-Mode an einem 6-m-Hochenergie-Kugelgitter-Monochromator durchgeführt. Die Photonen trafen auf die normale Oberfläche und Photoelektronen wurden in einem Winkel von 58° von der normalen Oberfläche gesammelt. Die Bindungsenergien in allen Spektren bezogen sich auf das Au 4f 7/2 Kernstufe bei 84,0 eV. Nach Subtraktion des linearen Hintergrunds wurden die Spektren mit gemischten Gauß-Lorentz-Funktionen basierend auf einem nichtlinearen Least-Square-Algorithmus angepasst [65].
Ergebnisse und Diskussion
Struktur- und Morphologieanalyse
Die Größe der AuNPs hing von der Art des Reduktionsmittels und den Bildungs- und Lagerungsbedingungen ab. Die SEM-Analyse zeigte, dass die GO-Blätter und AuNPs mit einer durchschnittlichen AuNP-Größe von 60 nm gleichmäßig auf der GO-Oberfläche befestigt waren (Abb. 3). Abbildung 3a zeigt SEM-Bilder der GO-Blätter auf dem Au-Film und dass die GO-Blätter weniger als 1 μm groß waren. Beim Vergleich von GO und AuNP-GO konnte im AuNP-GO-Verbund ein Goldelement beobachtet werden. Dies deutete darauf hin, dass die AuNPs erfolgreich auf der faltigen GO-Oberfläche adsorbiert wurden. Die synthetisierten AuNP-GO-Hybride wurden mit TEM charakterisiert, wie in Abb. 3b gezeigt. Abbildung 3b, c zeigt die Synthesebedingungen. Die Konzentration von 10 ml GO-Blattlösung betrug 0,1 g/l und 200 μl AuNP-Lösung hatten eine Konzentration von 2,2 nM. Die TEM-Bilder in Abb. 3a mit einem 100-nm-Maßstabsbalken und Abb. 3b mit einem 0,5-μm-Maßstabsbalken zeigen unterschiedliche Vergrößerungen der Größe und zeigen deutlich, dass die AuNPs auf der Oberfläche der GO-Blätter immobilisiert waren. Die AuNPs hatten eine Kugelform, was darauf hindeutet, dass die Carboxylfunktionalität auf der Oberfläche der GO-Faltblätter eine wichtige Rolle bei der Bildung chemischer kovalenter Bindungen mit den AuNPs spielen könnte, wie in Abb. 2b gezeigt.

Oberflächenmorphologieanalyse des Nanokomposits. a SEM-Bilder eines GO-Blatts und b TEM-Bild des AuNP-GO-Verbundmaterials. c Das TEM-Bild des ERGO AuNP-GO Films
Charakterisierungen von GO durch XPS-, Raman- und FTIR-Spektroskopie
Abbildung 4a zeigt die hochauflösende C 1s XPS-Spektralanalyse der GO-Blätter. Die C1s mit der höchsten Intensität bei einer Bindungsenergie von 284,6 eV entsprachen funktionellen Carbonylgruppen für C–C (sp2), und die Peaks bei 285,6, 286,6, 288,2 und 289,4 eV entsprachen C–C (sp3) in aromatischen Ringen , C–O in Hydroxyl- und Epoxygruppen, C=O in Carbonylgruppen bzw. O–C=O in Carboxylgruppen. Die C 1s XPS-Spektren der GO-Schichten auf einem Goldfilmsubstrat zeigten, dass die relativen Atomprozentsätze von C–C (sp2), C–C (sp3), C–O, C=O und O–C=O 77,44, 2,16, 18,14, 1,77 bzw. 0,49 % [66]. Abbildung 4b zeigt die Raman-Spektralanalyse der GO-Schichten in NaCl-Lösung mit spektralen Merkmalspeaks bei 1614 cm − 1 (G-Band), 1355 cm − 1 (D-Band), 2714 cm − 1 (2D-Band), 2947 cm − 1 (G + D-Band) und ~ 3240 cm − 1 (2D’-Band) [38, 67]. Die Bildung der GO-Faltblätter wurde weiter analysiert, um die Eigenschaften verschiedener sauerstoffhaltiger Spezies unter Verwendung von ATR-FTIR-Spektren aufzuklären, wie in Abb. 4c gezeigt. Diese ATR-FTIR-Spektren zeigten auch mehrere charakteristische Peaks von GO; C–O bei 850 cm − 1 aufgrund von (C–O–C) Epoxidschwingungen, C–O bei 1080 cm − 1 aufgrund von (C–O)-Alkoxy-Streckschwingungen, C=C bei 1500~1600 cm − 1 aufgrund aromatischer C=C-Bindungen und C–O bei 1260 cm − 1 aufgrund von (C–O–C)-Epoxid-asymmetrischen Schwingungen. Die Carboxylgruppen an den Kanten der GO-Schichten zeigten –COOH-Streckschwingungen mit Peaks bei 1652 und 1731 cm − 1 entsprechend C=O-Streckschwingungen von Carbonylgruppen. Die Spektren zeigten außerdem drei Peaks bei 2900 cm − 1 bezogen auf asymmetrische und symmetrische Streckschwingungen von –CH2 und ein Deformationspeak bei 1462 cm − 1 aufgrund von Alkengruppen (C–H), die sich auf der Ebene von GO befinden. FTIR-Spektren von GO zeigten einen großen Bereich von Absorptions-Breitbandpeaks von C-OH und H2 O-Vibrationen bei 3370 cm − 1 durch Dehnungsschwingungen [67].
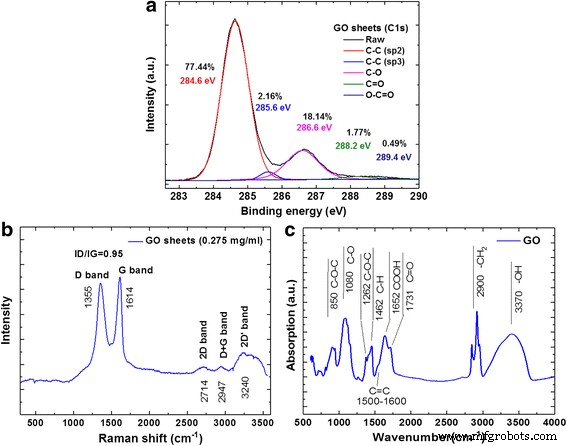
Spektralanalyse von GO-Blättern. a Hochauflösender XPS-Scan in der C1s-Region, b Raman und c FTIR
Analyse von GO und AuNP mit Proteinwechselwirkungseigenschaften
UV-Vis-Spektren von wässrigen GO und AuNPs mit Proteinwechselwirkungsdispersionen sind in Abb. 5 dargestellt. Die AuNPs hatten hohe Extinktionskoeffizienten und eine einzigartige Größe in Abhängigkeit von den Oberflächenplasmonen(SP)-Absorptionsbanden. Die modifizierten AuNPs mit zwei unterschiedlichen Abmessungen waren 15 und 60 nm für 520 und 540 nm der SP-Absorptionsspektren [68, 69]. Abbildung 5a zeigt die mit Cys in einer Konzentration von 5 mM modifizierte AuNP-Lösung (520 nm) mit der AuNP-Cys-Extinktionsbande [69]. Die UV-vis-Spektren wässriger GO-Dispersionen ergaben zwei Absorptionspeaks:das Maximum bei 230 nm entsprechend dem π-π*-Plasmonenpeak aromatischer C-C-Bindungen in aromatischen sp2-Clustern unterschiedlicher Größe und die Schulter bei 300 nm entsprechend dem n–π*-Plasmonenpeak aufgrund der Anwesenheit von Epoxid- und Carbonyl(C=O)-Bindungen (Abb. 5b) [9, 20]. Die UV-Vis-Spektren der GO-EDC/NHS- und GO-EDC/NHS-BSA-Lösung (Abb. 5b) zeigten, dass GO-EDC/NHS und GO-EDC/NHS-BSA einen Peak bei etwa 270 nm zeigten, was war wahrscheinlich aufgrund starker Wechselwirkungen zwischen GO und Amingruppen [70, 71]. Abbildung 5c zeigt die Absorptionsspektren der Bindungen für verschiedene Konzentrationen von antiBSA mit AuNPs (60 nm). Abbildung 1b zeigt die Syntheselösung der AuNP-antiBSA-Sonde (Probe B1). Die Wellenlängen hatten offensichtliche Absorptionspeaks bei 540 und 755 nm, wobei die Wellenlänge bei 540 nm hauptsächlich durch die AuNPs (60 nm) verursacht wurde und der Peak bei 755 nm einem kombinierten Absorptionspeak aus AuNP+Cys+antiBSA entsprach. Dieses Ergebnis zeigte, dass ein Anstieg der Anti-BSA-Konzentration einen allmählichen Anstieg der Absorption bei 540 nm und einen kontinuierlichen Anstieg der Nahinfrarot-Absorption bei 755 nm induzierte. Die unterschiedlichen antiBSA-bindenden Wechselwirkungen an der Oberfläche der AuNPs verursachten Änderungen des Oberflächenbrechungsindex, der wiederum in die Absorptionsintensität des LSPR umgewandelt wurde. Die LSPR-Bande wurde durch die Partikelgröße beeinflusst. Die AuNPs zeigten starke SPR-Banden im sichtbaren Bereich. Mit Erhöhungen des Brechungsindex der mittelgroßen Partikel konnte die Verschiebung der SPR-Peakpositionen vom sichtbaren zum nahen Infrarot eingestellt werden. In den experimentellen Ergebnissen der Proteinwechselwirkung haben wir AuNP-antiBSA gemischt, wie in Abb. 5d gezeigt. Die Empfindlichkeit wurde bestimmt, indem die LSPR-Wellenlänge des 500–760 nm-Bands als Funktion des gemessenen Brechungsindex aufgetragen wurde. Wir haben dann unterschiedliche Konzentrationen von Anti-BSA-Protein von 1,45 nM bis 145 fM verdünnt und in einem 200-μl-Volumen gemischt. Die Änderungen der 540- und 760-nm-Absorption wurden durch die unterschiedlichen Konzentrationen von antiBSA und AuNP verursacht. Spektralmessungen wurden dann 5 min später durchgeführt, die unterschiedliche Konzentrationen der Lichtintensitätsabsorption zeigten, und ein Absorptionspeak von 60 nm für die AuNPs wurde bei 540 und 755 nm beobachtet. Diese Ergebnisse stimmten mit den AuNP-antiBSA-Absorptionskalibrierungskurven überein. Die Kalibrierungskurven wurden von y . angepasst = 2,43 + 0,25× (Korrelationskoeffizient, R 2 = 0,91) für den 540-nm-Absorptionspeak und y = 2,56 + 0,31× (Korrelationskoeffizient, R 2 = 0,96) für den 760-nm-Absorptionspeak, wobei x ist die Konzentration von antiBSA und y ist die optische Extinktion.
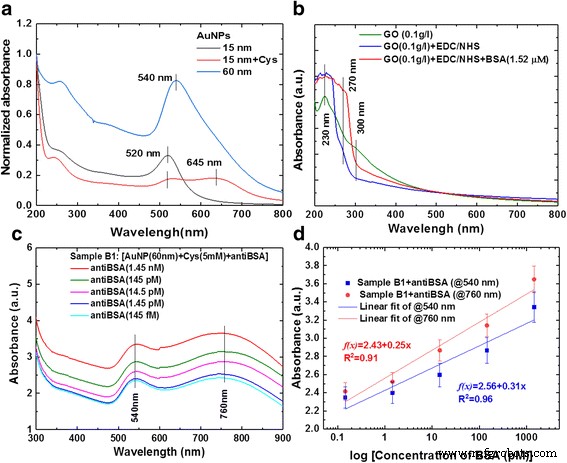
Analyse von UV-Vis-Absorptionsspektren für AuNP mit antiBSA-Interaktionsantwort. a SP-Absorptionsspektren von AuNPs, b GO-gebundenes BSA, c AuNP-anti-BSA-Sonde und d Kalibrierungskurven für AuNP mit Anti-BSA-Interaktionsreaktion bei Verdünnung verschiedener Konzentrationen von Anti-BSA-Protein von 1,45 nM bis 145 fM
Analyse von AuNP-antiBSA und AuNP-GO-antiBSA basierend auf Immunoassay-Interaktionen
Um den immunologischen Nachweismechanismus von GO- und AuNP-GO-Nanokompositen zu verstehen, wurde eine Spektralanalyse für Bindungsreaktionen durchgeführt, wie in Abb. 6 gezeigt. Abbildung 6a zeigt die UV-Vis-Absorptionsspektren der AuNP-GO- und GO-BSA-Nanocomposites. Für die GO-Blatt-Lösung (0,1 g/l) gab es einen Peak bei etwa 230 nm [70] und eine Schulter bei etwa 300 nm, und die GO-BSA-Konjugate zeigten einen Absorptionspeak bei etwa 270 nm und einen Peak bei etwa 230 nm [9, 20, 70]. In der Kombination von AuNP-GO-Nanokompositen wurden drei Absorptionspeaks bei 230, 300 bzw. 540 nm festgestellt. Die π-π-Stapelung oder kovalente Bindungswechselwirkungen zwischen AuNPs und der GO-Faltblattoberfläche waren die treibende Kraft für die Verankerung der AuNPs auf den hoch biokompatiblen GO-Materialien. Die GO-Schichten wurden dazu gebracht, sich in den AuNPs anzusammeln, was zu einer starken Absorptionsbande von 200–300 nm führte. Daher war die Absorption der GO-Schichten viel größer als die Absorption von AuNPs im sichtbaren Lichtband. Abbildung 6b zeigt, dass die UV-Vis-Spektren des AuNP-Absorptionspeaks bei 540 nm lagen [50, 68, 69]. Die Absorptionspeaks lagen bei 540 und 660 nm für AuNP+Cys-Konjugate; 230, 300, 540 und 660 nm für AuNP+Cys+GO-Konjugate; und 230, 270, 540 und 660 nm für AuNP+Cys+GO+antiBSA-Konjugate. Die GO-Blätter hatten zwei Absorptionspeaks bei 230 nm (π–π*-Plasmonenpeak) und 300 nm (n–π*-Plasmonenpeak). Es wurde eine Verschiebung der Absorptionswellenlänge festgestellt, und diese Absorptionsverschiebung wurde als Bestätigung der antiBSA (0 fM ~ 1,45 nM)-Absorption auf der AuNP+Cys+GO-Oberfläche angesehen. Abbildung 6c zeigt die Synthese der Lösung der AuNP+Cys+GO+antiBSA-Sonde (Probe B2) wie in Abbildung 2b. Der Anstieg der Anti-BSA-Konzentration war mit 540 nm relativ hoch. Abbildung 6c zeigt verschiedene Konzentrationen der Lichtintensitätsabsorption, und ein Absorptionspeak von 60 nm für die AuNPs wurde bei 540 nm beobachtet. Der Anstieg der Anti-BSA-Konzentration war mit 540 nm relativ hoch. Dieses Ergebnis zeigte, dass AuNP-GO die Plasmonenabsorptionseigenschaften bei 540 nm verbessern konnte, wenn die Anti-BSA-Konzentration erhöht wurde. Darüber hinaus haben wir im Immunoassay-Experiment das GO-BSA (1,52 μM) Target (Probe A) und die AuNP+Cys+GO+antiBSA-Sonde gemischt, wie in Abb. 6d gezeigt. Neben hydrophoben und π-π-Wechselwirkungen der GO-Faltblätter unterstützten auch kovalente Bindungen zwischen Proteinen und Carboxylgruppen auf den GO-Faltblättern die Oberflächenadhäsion. Dieses Ergebnis war wahrscheinlich darauf zurückzuführen, dass die AuNP+GO-antiBSA-Hybridstruktur eine stabile Immunantwort mit anderen Proteinen auf GO-BSA bildet. Die Wellenlängen hatten einen offensichtlichen Absorptionspeak bei 260 nm. Neben hydrophoben und π-π-(π-π*-Plasmonenpeak)-Wechselwirkungseigenschaften der GO-Faltblätter unterstützten auch kovalente Bindungen zwischen Proteinen und Carboxylgruppen auf den GO-Faltblättern die Oberflächenadhäsion. Vor und nach der BSA- und antiBSA-Bindung waren die π-π*-Plasmonenpeakwerte von GO (230 und 270 nm) signifikant verschoben, was bewies, dass BSA und antiBSA positiv gebunden waren.
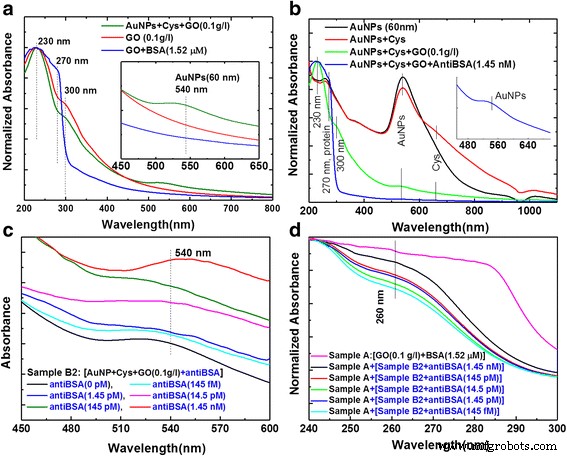
Analyse von UV-Vis-Absorptionsspektren für die Immunantwort. a AuNP-gebundenes GO und GO-gebundenes BSA, b AuNPs und GO-gebundenes Anti-BSA, c AuNP-GO-antiBSA-Sonde und d AuNP-GO-antiBSA-Sonde und GO-BSA-Target für die Immunantwort
Abbildung 7 zeigt, dass diese Ergebnisse gut mit den Kalibrierungskurven übereinstimmten. Eine detaillierte Analyse der obigen experimentellen Ergebnisse (Abb. 6c, d) zeigte, dass die Wahrnehmungsreaktionen auf die entsprechenden durchschnittlichen Extinktionsungenauigkeiten 1,3487, 1,1776, 1,0698, 0,8755 und 0,8588 (Abb. 7a) und 0,9226, 0,8535, 0,7649, 0,7243 . betrugen und 0,695 (Fig. 7b), entsprechend den Proteinkonzentrationen von 1,45 nM, 145 pM, 14,5 pM, 1,45 pM bzw. 145 fM. Abbildung 7a zeigt, dass die lineare Regression der Kalibrierungskurven f(x) . war = 0,918 + 0,124× (Korrelationskoeffizient, R 2 = 0,94) für die AuNP-GO-Sonde mit antiBSA-Wechselwirkungen, wobei x ist die Proteinkonzentration und y ist die optische Extinktion. Außerdem zeigt Abb. 7b, dass die lineare Regressionsgleichung der angepassten Kurve f(x) . war = 0,791 + 0,057× (Korrelationskoeffizient, R 2 = 0,954) für GO und AuNP-GO basierend auf dem Immunoassay.
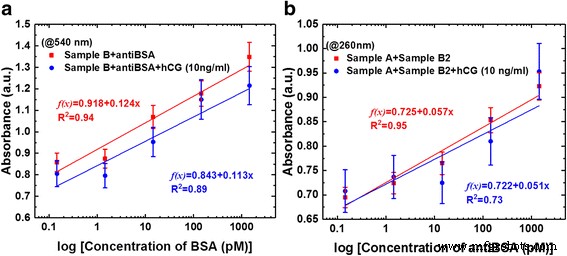
Vergleich der Kalibrierungskurven von Sensing-Antworten, die bei verschiedenen Proteinkonzentrationen erhalten wurden. a Kalibrierkurven für AuNP-GO-Sonde mit antiBSA-Wechselwirkungen. b Kalibrierkurven für GO und GO-AuNPs basierend auf einem Immunoassay
Während des Quantifizierungsexperiments fügten wir eine feste Konzentration von 10 ng/ml des Proteins humanes Choriongonadotropin (hCG) hinzu, um als Störer zu wirken. Die Ergebnisse zeigten, dass das fixierte interferierende hCG-Protein auf den Immunoassay-Kalibrierungskurven durch f(x) . angepasst wurde = 0,843 + 0,113× (Korrelationskoeffizient, R 2 = 0,89) für die AuNP-GO-Sonde mit antiBSA-Wechselwirkungen (Abb. 7a) und f(x) = 0.722 + 0.051× (Korrelationskoeffizient, R 2 = 0,73 für GO und AuNP-GO basierend auf dem Immunoassay (Abb. 7b).
Darüber hinaus zeigten unsere experimentellen Ergebnisse, dass die Detektionsstrategie eine Oberflächenregeneration ohne Spezifitätsverlust (vier Regenerationen) ermöglicht und auch zum Nachweis von antiBSA-Protein mit dynamischen Reaktionen im Bereich von 1,45 nM, 145 pM, 14,5 pM, 1,45 pM . verwendet werden kann , 145 fM und 0 fM. The results demonstrated that with a decreased concentration of antiBSA (from 1.45 nM to 145 fM) and even without the presence of antiBSA (0 fM), the spectral absorption intensity did not change the minimum level of quantitation. The hCG protein interfered with the antibody recognition in the immunoassay to a limited extent, possibly due to non-specific adsorption. This implies a very low cross-reactivity of the hCG protein and non-specific interactions at a low adsorption. In the practical quantitative analysis with immunoassays, a LOD of 145 fM for antiBSA was achieved in both buffer and interference protein samples.
Schlussfolgerungen
We successfully demonstrated a GO-bound AuNP biocompatible nanocomposite in a biosensing mechanism in a rapid and label-free immunoassay for biomolecule interactions. The results showed that the AuNP-GO nanocomposite was biocompatible and exhibited LSPR extinction to biomolecules, which could promote the absorption spectra characteristic peaks, accelerate the reaction of molecules, and enhance the stability of chemical covalent bonds during immobilization. For the detection of antiBSA protein, the limit of detection of the GO and AuNP-GO based on the immunoassay was as low as 145 fM. Among the AuNP-GO biosensors, GO immobilized in the AuNP-GO nanocomposite showed the highest bioaffinity, with good sensitivity, low detection limit, and fast response toward the protein immunoassay. The results of our experiments showed that a fixed concentration 10 ng/ml of hCG protein as an interferer did not affect the test response. Given the growing trend of applying biosensors in POCT, LSPR for AuNP-GO nanocomposite technology is a highly promising and versatile tool for use in immunoassays. Combining the properties of AuNPs and GO sheets to develop new nanocomposites for the synthesis of smart materials shows promise for the development of user-friendly diagnosis applications. In the future, AuNP-GO nanocomposites may be used in innovative immunoassays, rapid detection reagents, and miniaturization, which may in turn make LSPR technology an irreplaceable tool for routine clinical analysis and POCT diagnostics.
Abkürzungen
- Ag:
-
Silver
- AntiBSA:
-
Bovine serum albumin antibody
- Au:
-
Gold
- AuNP:
-
Gold nanoparticle
- BSA:
-
Bovine serum albumin
- Cys:
-
Cystamine
- EDC:
-
1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide
- FEG-TEM:
-
Field-emission gun transmission electron microscope
- FTIR:
-
Fourier-transform infrared spectrometer
- GO:
-
Graphene oxide sheet
- HR-TEM:
-
High-resolution transmission electron microscope
- LOD:
-
Limit of detection
- LSPR:
-
Lokalisierte Oberflächenplasmonenresonanz
- MOA:
-
8-Mercaptooctanoic acid
- NHS:
-
N -Hydroxysuccinimide
- Pd:
-
Palladium
- POCT:
-
Point-of-care testing
- Pt:
-
Platinum
- RGO:
-
Reduction graphene oxide
- SAMs:
-
Self-assembled monolayers
- SERS:
-
Surface-enhanced Raman scattering
- UV-Vis:
-
Ultraviolet-visible
- XPS:
-
Röntgenphotoelektronenspektroskopie
- ZnO:
-
Zinc oxide
Nanomaterialien
- Nanogoldcluster sind ein wunderbarer Katalysator
- Plasmonische Nanopartikel
- Goldnanopartikel für Chemosensoren
- Nanofasern und Filamente für eine verbesserte Wirkstoffabgabe
- Multifunktionale Goldnanopartikel für verbesserte diagnostische und therapeutische Anwendungen:Eine Übersicht
- BSA-beschichtete Gold-Nanostäbe für die photothermische NIR-II-Therapie
- Verbesserter nichtlinearer optischer Effekt in hybriden Flüssigkristallzellen basierend auf photonischen Kristallen
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität
- Erhöhte Biokompatibilität in anodischen TaO x Nanotube-Arrays
- Erhöhte Stabilität magnetischer Goldnanopartikel mit Poly(4-styrolsulfonsäure-co-maleinsäure):Maßgeschneiderte optische Eigenschaften für die Proteindetektion



