Humatunterstützte Synthese von MoS2/C-Nanokompositen über die gemeinsame Fällungs-/Kalzinierungsroute für Hochleistungs-Lithium-Ionen-Batterien
Zusammenfassung
Es wurde ein einfacher, kostengünstiger, ungiftiger und tensidfreier Weg zur Synthese von MoS2 . entwickelt /Kohlenstoff (MoS2 /C) Nanokomposite. Kaliumhumat besteht aus einer Vielzahl von sauerstoffhaltigen funktionellen Gruppen, die als vielversprechende Kandidaten für die Funktionalisierung von Graphen gelten. Verwendung von Kaliumhumat als Kohlenstoffquelle, zweidimensionales MoS2 /C-Nanoblätter mit unregelmäßiger Form wurden über einen stabilisierten Kopräzipitations-/Kalzinierungsprozess synthetisiert. Die elektrochemische Leistung der Proben als Anode einer Lithium-Ionen-Batterie wurde gemessen und zeigte, dass das MoS2 /C Nanokomposit kalziniert bei 700 °C (MoS2 .) /C-700)-Elektrode zeigte eine hervorragende Leistung mit einer hohen Entladekapazität von 554,9 mAh g − 1 bei einer Stromdichte von 100 mA g − 1 und die Coulomb-Effizienz der Probe blieb nach den ersten 3 Zyklen auf einem hohen Niveau von ungefähr 100 %. Gleichzeitig wird das MoS2 /C-700-Elektrode zeigte eine gute Zyklenstabilität und Geschwindigkeitsleistung. Der Erfolg bei der Synthese von MoS2 /C-Nanokomposite über die gemeinsame Fällungs-/Kalzinierungsroute könnten einen neuen Weg ebnen, um vielversprechende Anodenmaterialien für Hochleistungs-Lithium-Ionen-Batterien zu realisieren.
Hintergrund
Aufgrund ihrer hohen Energiedichte, langen Lebensdauer und Umweltfreundlichkeit werden Lithium-Ionen-Batterien (LIBs) häufig in tragbaren elektronischen Geräten [1] (z. B. Mobiltelefonen und Uhren), Elektrofahrzeugen [2, 3] und erneuerbaren verwendet Energiespeicherung [4,5,6,7,8]. Graphit ist das am häufigsten verwendete Anodenmaterial in kommerziellen LIBs und profitiert von seiner niedrigen Arbeitsspannung, guten Leitfähigkeit und geringen Kosten [9,10,11]. Die charakteristische Struktur von Graphit führt jedoch zu einer machbaren Erzeugung von LiC6 , was nur eine Lithiumionen-Interkalation in jeweils sechs Kohlenstoffatomen ermöglicht, was zu einer niedrigen theoretischen spezifischen Kapazität von 372 mAh g − 1 . führt , was weit von den aktuellen Geschäftsanforderungen entfernt ist [12].
Gegenwärtig wird es bevorzugt, geeignete Elektrodenmaterialien in LIBs für eine höhere Batteriekapazität, eine längere Zykluslebensdauer und eine bessere Leistungsfähigkeit zu erhalten. Daher werden in LIBs häufig Anodenmaterialien auf Li-Legierungsbasis [13], Übergangsmetalloxide [14], Oxysalze und Übergangsmetallsulfide [15] als Anodenmaterialien verwendet, da diese Materialien alle notwendigen Eigenschaften für eine geeignete Elektrode aufweisen Materialien. Unter diesen Materialien sind Übergangsmetallsulfide (z. B. CuS2 [16], WS2 [17] und MoS2 [18,19,20] waren ein spannendes Thema in der Forschung, da sie reichlich erdreich sind und eine hohe spezifische Kapazität aufweisen, wenn sie als Anodenmaterialien in LIBs verwendet werden [21]. Als typischer Vertreter ist MoS2 hat aufgrund seiner besonderen S-Mo-S-Schichtstruktur [22], der hohen theoretischen spezifischen Kapazität im Vergleich zu herkömmlichen Graphitanoden und der Übertragungsreaktion von vier Elektronen bei Verwendung als Anodenmaterial in LIBs viel Aufmerksamkeit auf sich gezogen [23, 24]. Darüber hinaus sind die Van-der-Waals-Kräfte zwischen den MoS2 Schichten sind sehr schwach und erlauben eine Lithium-Ionen-Diffusion ohne signifikante Volumenänderung zu verursachen [25, 26]. MoS2 ist aufgrund seiner geringen elektrischen Leitfähigkeit immer noch ein unbefriedigendes Anodenmaterial, was zu einer schlechten Zyklen- und Geschwindigkeitsleistung führt [27]. Um dieses Problem zu lösen, wurde eine Reihe von Strategien entwickelt, um die elektrische Leitfähigkeit zu verbessern, wie zum Beispiel der Einbau von MoS2 mit Kohlenstoffmaterialien [28,29,30].
Bis heute ist eine Vielzahl von MoS2 /Kohlenstoff-Komposite wurden als Anodenmaterialien in LIBs synthetisiert, nämlich geschichtetes MoS2 /Graphen-Komposite [31], MoS2 /C mehrschichtige Nanokugeln [32], MoS2 -CNT-Komposit [33], mehrschichtiges Graphen/MoS2 Heterostrukturen [34] oder blütenblattartiges MoS2 Nanoblätter, die in hohlen mesoporösen Kohlenstoffkugeln raumbegrenzt sind [35]. Trotz erfreulicher Fortschritte bei elektrischer Leitfähigkeit, Zyklen und Geschwindigkeitsleistung der Elektrode bestehen einige andere Konflikte in der Synthesemethode fort. Derzeit ist die am häufigsten verwendete Synthesemethode der hydrothermale Ansatz, gefolgt von einem Glühprozess, der eine Kohlenstoffmatrix mit einigen Tensiden wie Natriumoleat oder Oleyamin und Schwefelelement mit etwas L-Cystein im ersten Verfahren einbringen kann. Darüber hinaus waren teure und giftige organische Reagenzien während des Syntheseprozesses im Vergleich zu Copräzipitationsverfahren immer unverzichtbar und unvermeidbar. Derzeit gewinnt die Co-Präzipitationsmethode aufgrund ihrer kostengünstigen, ungiftigen, vertrauenswürdigen und stabilen Methode gerade erst an Popularität in der Synthese anorganischer nanostrukturierter Materialien zu gewinnen [36, 37]. Nach unserem besten Wissen gibt es nur wenige Berichte über die Synthese von MoS2 /C-Nanokomposit durch Co-Präzipitations-/Kalzinierungs-Prozess, insbesondere mit Kaliumhumat.
Als funktionalisierter Graphenkandidat kann Kaliumhumat angesehen werden, eine Art aromatisches Hydroxycarboxylat, das aus einer Vielzahl von sauerstoffhaltigen funktionellen Gruppen besteht [38]. Im Allgemeinen wurde viel geforscht, um Kaliumhumat als Kohlenstoffquelle zu verwenden, um Kohlenstoffmaterialien unter extrem rauen Bedingungen zu synthetisieren [38, 39]. Huang [38] berichtete, dass Kaliumhumat eine einfache Karbonisierung sein kann, um reduzierte Graphitoxidmaterialien herzustellen. In diesem Artikel wird MoS2 /C-Nanokomposite wurden über eine gemeinsame Fällungs-/Kalzinierungsroute unter Verwendung einer organischen Substanz (Kaliumhumat) und einer anorganischen Substanz ((NH4 )6 Mo7 O24 ) als Reagenzien. Die elektrochemische Leistung der Proben als LIBs-Anode wurde gemessen und die Ergebnisse zeigten, dass die Probe bei 700 °C kalziniert wurde (MoS2 /C-700) zeigte eine bessere Zyklenfähigkeit und ein besseres Geschwindigkeitsverhalten. Die Entladekapazität der Probe blieb bei 554,9 mAh g − 1 nach 50 Zyklen bei der Stromdichte von 100 mA g − 1 , was viel besser ist als die anderen beiden Proben, die bei 600 °C bzw. 800 °C kalziniert wurden. In der Zwischenzeit wird das vorbereitete MoS2 /C-700 zeigt eine vergleichbare elektrochemische Leistung [40, 24].
Methoden/Experimental
Kaliumhumat wurde von Double Dragons Humic Acid Co., Ltd. Xinjiang (China) bezogen, und die Analyse der Zusammensetzung von Kaliumhumat wurde in Zusatzdatei 1:Tabelle S1 gezeigt. Alle chemischen Reagenzien (außer Kaliumhumat) waren von reiner analytischer Qualität und wurden ohne weitere Reinigung verwendet.
Synthese von MoS2 /C
Die Vorstufe wurde durch gemeinsame Fällung aus (NH4 )6 Mo7 O24 und Kaliumhumat in Gegenwart von HNO3 gefolgt von einem gefriergetrockneten Prozess für 2 Tage. In einem typischen Verfahren wurden 4 g Kaliumhumat in 40 ml 0,25 M (NH4 )6 Mo7 O24 Lösung. Anschließend wurde die oben genannte Lösung tropfenweise zu 100 ml 0,5 M HNO3 . gegeben Lösung unter kräftigem Magnetrühren. Die Dauer des magnetischen Rührens betrug mehrere Stunden. Der untere Niederschlag wurde dann von der Mischlösung abgetrennt, gefriergetrocknet und als Mo-HA-Vorläufer markiert. Die Vorstufe wurde mit wasserfreiem Na2 . gemischt SO4 (im Verhältnis 1:10) und im Mörser zu einer homogenen Masse vermahlen. Anschließend wurde die Mischung 3 h bei 700 °C kalziniert (mit einer Heizrate von 10 °C min − 1 ) und dann natürlich auf Raumtemperatur abgekühlt. Schließlich wurden die Produkte dreimal mit entionisiertem Wasser und Ethanol gewaschen, gefolgt von einem gefriergetrockneten Verfahren, um das MoS2 . zu erhalten /C-Pulver. Parallel dazu wurden auch die bei 600 und 800 °C kalzinierten Proben synthetisiert.
Charakterisierung
Die organischen funktionellen Oberflächengruppen von Kaliumhumat wurden mit einem Fourier-Transformations-Spektrophotometer (FT-IR, VERTEX 70, Bruker) mit KBr als Referenzprobe gemessen. Struktur und Morphologie verschiedener Proben wurden durch Röntgenbeugung (XRD, BRUKER D8 Advance) mit Cu Kα-Strahlung (λ = 1,54178 Å), Transmissionselektronenmikroskopie (TEM, Hitachi H-600), hochauflösende Transmissionselektronenmikroskopie . charakterisiert (HRTEM, JEM-2100F), LEO 1450VP Rasterelektronenmikroskop (REM), energiedispersives Röntgenspektrometer (EDX) und Röntgenphotoelektronenspektroskopie (XPS, ESCALAB 250Xi Spektrometer). Thermogravimetrische Analysen (TGA) wurden auf einem thermogravimetrischen Analysator (Netzsch TGA 409) durchgeführt. Das Raman-Spektrum wurde auf Bruker Senterra mit einer Wellenlänge von 532 nm durchgeführt.
Elektrochemische Messungen
Elektrochemische Messungen wurden an Knopfzellen durchgeführt. Die Arbeitselektroden wurden durch Mischen von 80 Gew.-% des so hergestellten MoS2 . hergestellt /C aktive Materialien, 10 Gew. % Acetylenruß und 10 Ge % Polyvinylidenfluorid (PVDF) in N-Methyl-2-pyrrolidinon (NMP)-Lösungsmittel, um eine homogene Aufschlämmung zu bilden. Die Aufschlämmung wurde auf die Kupferfolie aufgetragen und im Vakuum bei 110 °C 12 h getrocknet. Die Knopfzellen wurden in einem mit Argon gefüllten Handschuhfach zusammengebaut. Bei der Messung wurde Lithiumfolie als Gegenelektrode und Referenzelektrode verwendet, und eine Polypropylenfolie (Celgard-2400) wurde als Separator verwendet. Die Elektrolytlösung war 1 mol L − 1 LiPF6 in Ethylencarbonat (EC), Dimethylcarbonat (DMC) und Diethylcarbonat (DEC) (EC/DMC/DEC, 1:1:1, Volumenverhältnis). Die galvanostatischen Ladungs-Entladungs-Messungen wurden in einem Potenzialbereich von 0,01–3,0 V mit einem Batterietestgerät LAND CT2001A (Wuhan) bei Raumtemperatur durchgeführt. Zyklische Voltammetrie (CV)-Messungen wurden an einer elektrochemischen Workstation (CHI 660D) mit einer Abtastrate von 0,1 mV s − 1 . durchgeführt zwischen 0,01 und 3,0 V.
Ergebnisse und Diskussion
Die Oberflächenchemie von Kaliumhumat wurde mit dem FTIR-Spektrum untersucht. In Abb. 1a sind die breiten Peaks bei 3400 cm – 1 . zentriert wurden den Streckschwingungen von −OH, −COOH und H2 . zugeschrieben O-Bindungen, die Peaks bei 1627, 1413 und 1050 cm − 1 wurden den Streckschwingungen der −COO-Gruppen und −CH, −OH usw. zugeschrieben [41], was auf die reichhaltigen sauerstoffhaltigen funktionellen Gruppen auf der Oberfläche von reinem Kaliumhumat hinweist, die für die Komplexbildungsreaktion oder Adsorption von Vorteil sind . TGA-Kurve der homogenen Mischung aus Mo-HA-Vorstufe und wasserfreiem Na2 SO4 (mit einem Anteil von 1:10) in einer Argonatmosphäre mit einer Aufheizrate von 10 °C min − 1 ist in Abb. 1b gezeigt. Es ist ersichtlich, dass es in der TGA-Kurve drei Stufen der Gewichtsabnahme gibt. Der erste Gewichtsverlust beträgt 1,59 % von Raumtemperatur bis 250 °C, was auf die Zersetzung des Wassers in der Oberfläche der Mo-HA-Vorstufen zurückzuführen sein kann. Es gibt zwei weitere aufeinander folgende Schritte des Gewichtsverlusts, mit einem Gewichtsverlust von 1,35 % von 250 bis 500 °C und einem Gewichtsverlust von 3,17 % von 500 bis 800 °C, und dann bleibt die Masse konstant, was darauf hindeutet, dass die Vorstufe bei 800 °C vollständig zersetzt. Für ein solches System wählen wir diese drei Temperaturen für die Kalzinierung als 600, 700 und 800 °C, bezeichnet als MoS2 . /C-600, MoS2 /C-700 und MoS2 /C-800 bzw.
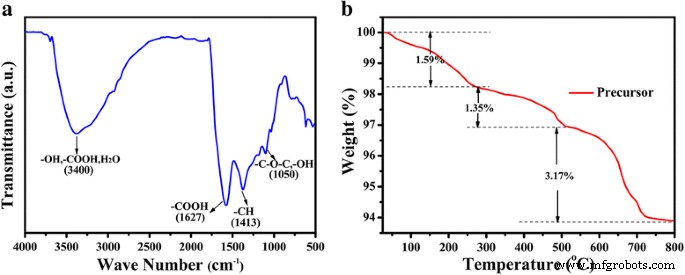
a FT-IR-Spektren von reinem Kaliumhumat. b TGA-Kurve der homogenen Mischung aus Mo-HA-Vorstufe und wasserfreiem Na2 SO4 (mit einem Anteil von 1:10)
Gemäß der Literatur [34] wurde ein möglicher Mechanismus des Reaktionsprozesses vorgeschlagen und in Schema 1 schematisch dargestellt. Darüber hinaus sind die entsprechenden Formeln in Zusatzdatei 1 aufgeführt:Gleichungen 1–5. In diesen Gleichungen wurde Kaliumhumat als K-HA abgekürzt. Beim Auflösen von Kaliumhumat in (NH4 .) kann es zu einer Komplexbildung kommen )6 Mo7 O24 Lösung unter Beteiligung von HNO3 Lösung, die zur Erzeugung von Mo-HA führt. Nach dem Erhitzen der Mischung aus der Mo-HA-Vorstufe und wasserfreiem Na2 SO4 in einer Argonatmosphäre bei einer relativ hohen Temperatur würde die Mo-HA-Vorstufe karbonisiert, um das Zwischenprodukt aus amorphem Kohlenstoff zu bilden, und dann würde das Zwischenprodukt wasserfreies Na2 . reduzieren SO4 um Na2 . zu erzeugen S, weiter zu Wasserstoff-Schwefel hydrolysiert. Schließlich kann Schwefelwasserstoff mit MoOx . reagieren , was zur Bildung von MoS2 . führt /C-Nanokomposite.
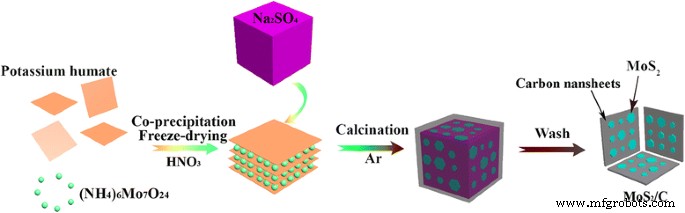
Schematische Darstellung des Herstellungsverfahrens von MoS2 /C-Nanokomposit
Abbildung 2a–b zeigen die XRD-Muster und Raman-Spektren des MoS2 /C-Nanokomposite, die bei verschiedenen Temperaturen kalziniert wurden. Abbildung 2a zeigt, dass fast alle Beugungspeaks von MoS2 /C-600 und MoS2 /C-700 kann gut auf das hexagonale MoS2 . indiziert werden Phase (JCPDS-Karte Nr. 86-2308), die mit denen des vorherigen Berichts übereinstimmt [42]. Es gibt noch einige andere Peaks, die nicht mit der Standardkarte im MoS2 . übereinstimmen /C-800-Beispiel. Wir spekulieren, dass das Kristallin von MoS2 /C wurde bei hoher Temperatur zerstört. Aus den Raman-Spektren (Abb. 2b) ist ersichtlich, dass die Peaks zwischen 379 und 400 cm − 1 . liegen gehörte zu E 1 2g (die Verschiebung der Mo- und S-Atome in der Ebene) und A 1g (symmetrische Verschiebung von Mo- und S-Atomen außerhalb der Ebene) Raman-Moden [24, 43]. Die Banden erschienen bei 1347 und 1589 cm − 1 waren das charakteristische D- und G-Band und der Wert von I D /Ich G 0,96, 0,91 und 0,94, wenn die Temperatur von 600 auf 800 °C steigt. Ersteres entspricht dem amorphen Kohlenstoff oder sp 3 -hybridisierter Kohlenstoff (D-Band) und letzterer dem sp 2 . zugeordnet -hybridisierter Kohlenstoff (G-Band) [44]. Obwohl es keinen großen Unterschied zwischen dem Grad der Graphitisierung gibt, ist das MoS2 /C-700-Probe ist bis zu einem gewissen Grad immer noch etwas höher als die anderen beiden Proben, was darauf hindeutet, dass der Kohlenstoff in dieser Probe nicht nur in Form von amorphem Kohlenstoff, sondern auch in Form von graphitischem Kohlenstoff vorliegt. Daher haben wir uns auf das MoS2 . konzentriert /C-700-Probe in den folgenden Untersuchungen.
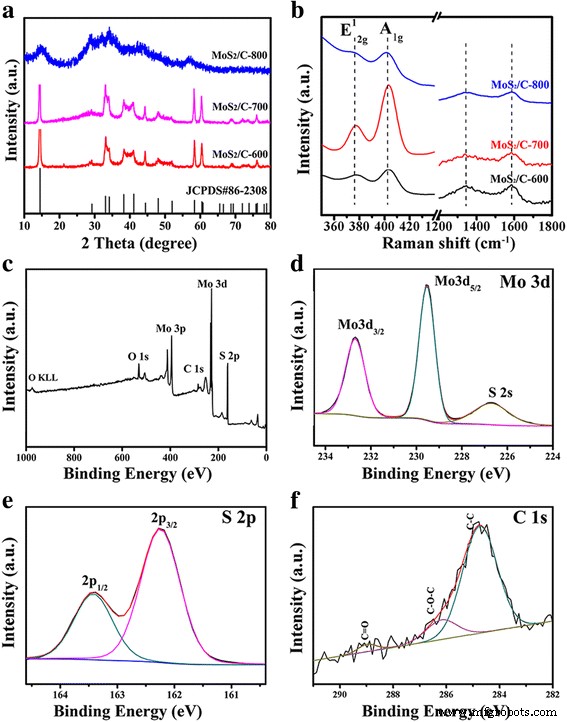
a XRD-Muster. b Raman-Spektren von MoS2 /C-Nanokomposite, die bei verschiedenen Temperaturen kalziniert wurden. c Vermessung der XPS-Spektren von MoS2 /C-700. d Hochauflösende XPS-Spektren von Mo 3d. e S 2p. f C 1 s
Um die chemische Zusammensetzung und die chemischen Bindungen von MoS2 . weiter zu untersuchen /C-700, wurde eine Röntgen-Photoelektronenspektroskopie-(XPS)-Analyse durchgeführt. Das XPS-Spektrum (Abb. 2c–f) zeigt das Vorhandensein von Mo-, S-, C- und O-Elementen im MoS2 /C-700 Nanokomposit. Die hochauflösenden XPS-Spektren von Mo 3d und S 2p sind in Abb. 2d bzw. e dargestellt. Die Peaks bei 229,4 und 232,6 eV werden dem Mo 3d5/2 . zugeordnet und Mo 3d3/2 , was die Existenz von Mo in MoS2 . bestätigt /C-700 [45, 46]. Das Vorhandensein eines weiteren XPS-Peaks bei 226,5 eV ist auf S 2 s indiziert, das sich aus der Oberfläche des MoS2 . ergibt /C-700 [47]. Darüber hinaus sind die XPS-Peaks bei 162,3 und 163,4 eV in S 2p-Spektren charakteristische Peaks von S 2p3/2 und S 2p1/2 von MoS2 , bzw. Abbildung 2f zeigt, dass das Spektrum von C1 in drei Peaks unterteilt werden kann, die als C–C-, C–O- bzw. C=O-Gruppen bezeichnet werden.
Das EDX-Spektrum zeigt, dass die bei 700 °C kalzinierte Probe Mo-, S- und C-Elemente enthält, wie in Abb. 3a gezeigt. Abbildung 3b, c zeigen die SEM-Bilder der Probe von MoS2 /C-700. Zum Vergleich die REM-Bilder von MoS2 /C-600 Nanokomposit und MoS2 /C-800-Nanokomposit wurden auch in der zusätzlichen Datei 1 gezeigt:Abbildung S1. Um die entsprechende Elementverteilung in der Probe von MoS2 . zu untersuchen, /C-700 wurden die entsprechenden Elementar-Mapping-Analysen durchgeführt. Wie in Abb. 4a–d gezeigt, sind die elementaren Kartierungsbilder von MoS2 /C-700 demonstrierte die gleichmäßige Verteilung von Mo, S und C über das gesamte MoS2 /C-700 Nanokomposit, was mit den EDX- und XPS-Ergebnissen übereinstimmt.

a EDX-Spektrum von MoS2 /C-700. b , c SEM-Bilder von MoS2 /C-700 Nanokomposit

a -d Elementarkartierungsbilder von MoS2 /C-700; (e ) TEM-Bild, (f ) der SAED und (g ) Hochauflösendes TEM-Bild von MoS2 /C-700 Nanokomposit, (h ) Vergrößertes HR-TEM-Bild des markierten Bereichs in Abbildung (g )
Wie in Abb. 4e–h dargestellt, sind die Morphologie und Struktur des so synthetisierten MoS2 /C-Nanokomposite wurden durch Transmissionselektronenmikroskopie (TEM), Selected Area Electron Diffraktion (SAED) und hochauflösende Transmissionselektronenmikroskopie (HRTEM) untersucht. Das TEM-Bild (Abb. 4e) und die SEM-Bilder (Abb. 3b, c) zeigen deutlich, dass die Struktur von MoS2 /C-700-Nanokomposit sind zerknitterte zweidimensionale Nanoblätter mit einer Breite von ~ 800 nm und einer Dicke von ~ 20 nm. Das SAED-Muster in Abb. 4f zeigt, dass die hexagonale Gitterstruktur von MoS2 ist gut kristallisiert. Darüber hinaus wurden die Kristallgitter der Probe bei HRTEM-Profilen ((Abb. 4g, h) und Zusatzdatei 1:Abbildung S2) gezeigt. Die Profile zeigten hochkristallines MoS2 Nanoblätter mit einem Zwischenschichtabstand von 0,27 nm entsprechend der (100)-Ebene von hexagonalem MoS2 [24, 34]. Darüber hinaus zeigt zusätzliche Datei 1:Abbildung S2 deutlich, dass die Kohlenstoff-Nanoblätter mit MoS2 . dekoriert wurden Nanoblätter.
Abbildung 5a zeigt die CV-Kurven der ersten 3 Zyklen von MoS2 /C-700-Elektrode bei einer Abtastrate von 0,1 mV s − 1 im Potenzialfenster von 0,01–3,00 V vs. Li + /Li. Während des ersten Zyklus weist der Reduktionspeak bei 1,0 V auf den Mechanismus der Lithiumeinfügung hin, der auf die Einfügung von Lithiumionen in das MoS2 . zurückzuführen ist Schichten zu Lix MoS2 . Gleichzeitig fand ein Phasenübergang von 2H (trigonal-prismatisch) zu 1T (oktaedrisch) statt [48]. Ein weiterer Reduktionspeak bei 0,4 V wird der Umwandlung von Lix . zugeschrieben MoS2 in metallisches Mo und Li2 S. Der breite Oxidationspeak bei 2,35 V repräsentiert die Deinterkalation von Li2 S bis S. Während der nachfolgenden Zyklen verschwinden die beiden kathodischen Peaks bei 1,0 und 0,4 V mit dem Auftreten von drei neuen Peaks bei 2,0, 1,2 und 0,3 V, was auf die Verringerung von MoS2 . hinweist und die Umrechnung von S8 zu Polysulfiden und dann zu Li2 S [24].
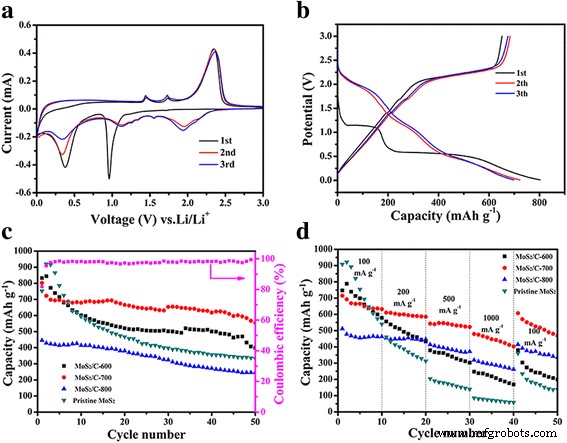
a CV-Kurven der ersten drei Zyklen von MoS2 /C-700-Elektrode bei einer Abtastrate von 0,1 mV s − 1 . b Entlade- und Ladekurven der ersten 3 Zyklen von MoS2 /C-700-Elektrode bei einer Stromdichte von 100 mA g − 1 . c Fahrleistung MoS2 /C-Elektrode und das makellose MoS2 Elektrode bei einer Stromdichte von 100 mA g − 1 , und Coulomb-Effizienz von MoS2 /C-700-Elektrode. d Leistung von MoS2 . bewerten /C und das unberührte MoS2 Elektrode bei Stromdichten von 100 bis 1000 mA g − 1
Die Entlade- und Ladekurven der ersten 3 Zyklen von MoS2 /C-700-Elektrode wurden aufgezeichnet, und die entsprechenden Ergebnisse sind in Abb. 5b gezeigt. Im ersten Zyklus werden die Entlade- und Ladekapazitäten von MoS2 /C-700-Elektrode sind 802,8 und 651,4 mAh g − 1 mit einem Coulomb-Wirkungsgrad von 81,14 %. Der irreversible Kapazitätsverlust kann auf eine irreversible Reaktion wie die Zersetzung des Elektrolyten und die Bildung eines Festelektrolytgrenzflächenfilms (SEI) zurückzuführen sein [49, 50].
Die Zyklenstabilität des gesamten MoS2 /C-Elektrode und das makellose MoS2 Elektrode bei einer Stromdichte von 100 mA g − 1 sind in Abb. 5c dargestellt. Gleichzeitig ist die Coulomb-Effizienz von MoS2 /C-700 wird ebenfalls aufgezeichnet. Nach 50 Zyklen sind die Entladekapazitäten von MoS2 /C-600, MoS2 /C-700, MoS2 /C-800 und makelloses MoS2 Elektrode bei einer Stromdichte von 100 mA g − 1 bleiben bei 399,7, 554,9, 245,7 und 332,9 mAh g − 1 , bzw. Wie in Zusatzdatei 1:Tabelle S1 gezeigt, wurden die Entladekapazitäten nach 50 Zyklen von MoS2 . zusammengefasst -basierte Elektrode, die in anderer Literatur vorgestellt wird, die so hergestellte MoS2 /C-700 zeigen vergleichbare elektrochemische Leistungen im Vergleich zu den vorherigen Arbeiten. Daraus wird geschlossen, dass die MoS2 /C-700-Elektrode zeigt die herausragendste Zyklusleistung und die Coulomb-Effizienz der Probe blieb nach den ersten 3 Zyklen auf einem hohen Niveau von etwa 100 %. Es kann von der geringen Menge an graphitischem Kohlenstoff in dieser Probe profitieren, was zu einer verbesserten elektrischen Leitfähigkeit des Nanokomposits führt.
Neben der Zyklenfestigkeit ist auch die High-Rate-Performance ein wichtiger Faktor für High-Power-Anwendungen. Abbildung 5d zeigt die Ratenleistung von MoS2 /C und das unberührte MoS2 Elektrode bei Stromdichten von 100 bis 1000 mA g − 1 . Bei 1000 mA g − 1 , die Entladekapazität von MoS2 /C-700 kann immer noch einen relativ hohen Wert von ~ 450 mAh g − 1 . halten , das höher ist als das andere MoS2 /C-Elektroden und makelloses MoS2 Elektrode, die wir bei der gleichen Stromdichte hergestellt haben. Wenn die Stromdichte wieder auf 100 mA g − 1 . geändert wird , die Kapazität von MoS2 /C-700-Probe kann bis zu ~ 500 mAh g − 1 . erholen nach 50 Zyklen bei unterschiedlichen Stromdichten, was die gute Ratenfähigkeit der Probe zeigt.
Die elektrochemischen Impedanzspektren (EIS)-Messungen am MoS2 /C und das unberührte MoS2 Elektrode wurden durchgeführt, um ein weiteres Verständnis über die hervorragende elektrochemische Leistung des MoS2 . zu erlangen /C-700-Probe (Abb. 6). Auf diesen Nyquist-Plots befindet sich im Hochfrequenzbereich ein Halbkreis, gefolgt von einer Steigungslinie im Niederfrequenzbereich. Es ist zu erkennen, dass der Halbkreis im Hochfrequenzbereich des MoS2 /C-700 Sample ist offensichtlich kleiner als das der anderen drei Samples, was mit dem Ladungsübergangswiderstand zusammenhängt (R ct ) trat an der Elektrolyt- und Elektrodengrenzfläche auf. Daher impliziert dieses Ergebnis weiter, dass der Einbau von Kaliumhumat die Leitfähigkeit von MoS2 . deutlich verbessert , was zu einer weiteren Verbesserung der elektrochemischen Leistung führt.
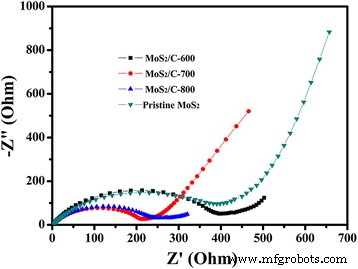
Nyquist-Plots des MoS2 /C-Elektrode und das makellose MoS2 Elektrode in einem Frequenzbereich von 0,01 Hz bis 100 kHz getestet
Schlussfolgerungen
In dieser Arbeit wird zweidimensionales MoS2 /C-Nanoblätter wurden erfolgreich über eine gemeinsame Fällungs-/Kalzinierungsroute synthetisiert, indem eine organische Substanz (Kaliumhumat) und eine anorganische Substanz ((NH4 )6 Mo7 O24 ) als Reagenzien. Strukturelle Charakterisierungen zeigen, dass MoS2 . wie hergestellt /C-700-Nanokomposit ist zweidimensionales (2D) MoS2 /C-Nanoblätter mit unregelmäßiger Form. Das 2D-MoS2 /C-Nanoblätter zeigten eine verbesserte elektrochemische Leistung, wenn sie als Anodenmaterial für LIBs hergestellt wurden. Weiterhin wurde ein möglicher Reaktionsprozess vorgeschlagen. Die derzeitige Synthesestrategie kann auf die Synthese anderer Nanokomposite ausgeweitet werden, die als Anodenmaterialien für Hochleistungs-Lithium-Ionen-Batterien dienen können.
Abkürzungen
- 2D:
-
Zweidimensional
- Lebenslauf:
-
Zyklische Voltammetrie
- DEZ:
-
Diethylcarbonat (DEC)
- DMC:
-
Dimethylcarbonat
- EC:
-
Ethylencarbonat
- EDX:
-
Energiedispersives Röntgenspektrometer
- EIS:
-
Elektrochemische Impedanzspektroskopie
- FT-IR:
-
Fourier-Transformations-Spektrophotometer
- HRTEM:
-
Hochauflösende Transmissionselektronenmikroskopie
- I D :
-
Die Intensität des D-Bandes
- I G :
-
Die Intensität des G-Bandes
- LIBs:
-
Lithium-Ionen-Akkus
- Mo-HA:
-
Die Vorläufer
- MoS2 /C:
-
MoS2 /Kohlenstoff
- MoS2 /C-600:
-
MoS2 /C Nanokomposit kalziniert bei 600 °C
- MoS2 /C-700:
-
MoS2 /C Nanokomposit kalziniert bei 700 °C
- MoS2 /C-800:
-
MoS2 /C Nanokomposit kalziniert bei 800 °C
- NMP:
-
N-Methyl-2-pyrrolidinon
- PVDF:
-
Polyvinylidenfluorid
- R ct :
-
Ladungsübergangswiderstand
- SEM:
-
Rasterelektronenmikroskop
- TEM:
-
Transmissionselektronenmikroskopie
- TGA:
-
Thermogravimetrische Analysen
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Zinn-Nanokristalle für zukünftige Batterien
- MoS2 mit kontrollierter Dicke für die elektrokatalytische Wasserstoffentwicklung
- Einfache Synthese von auf MWNT verankerten SiO2@C-Nanopartikeln als Hochleistungsanodenmaterialien für Li-Ionen-Batterien
- Synthese und elektrochemische Eigenschaften von LiNi0.5Mn1.5O4 Kathodenmaterialien mit Cr3+ und F− Verbunddotierung für Lithium-Ionen-Batterien
- Temperaturabhängige Kristallisation von MoS2-Nanoflocken auf Graphen-Nanoblättern für die Elektrokatalyse
- MoS2/Acetylene Black Composite mit wenigen Schichten als effizientes Anodenmaterial für Lithium-Ionen-Batterien
- Na4Mn9O18/Carbon Nanotube Composite als elektrochemisches Hochleistungsmaterial für wässrige Natrium-Ionen-Batterien
- Einfache Synthese von oberflächenfunktionalisierten magnetischen Nanokompositen zur effektiven selektiven Adsorption kationischer Farbstoffe
- Umwandlung von Schlamm-Si in Nano-Si/SiOx-Struktur durch Sauerstoffeindringung als Vorläufer für Hochleistungsanoden in Lithium-Ionen-Batterien
- Synthese und Untersuchung von CuGeO3-Nanodrähten als Anodenmaterialien für fortschrittliche Natrium-Ionen-Batterien



