Fortschritte bei kohlenstoffbasierten Elektrokatalysatoren für flexible Zink-Luft-Batterien in den letzten 5 Jahren:aktuelle Strategien für Design, Synthese und Leistungsoptimierung
Zusammenfassung
Die zunehmende Popularität tragbarer elektronischer Geräte hat zur schnellen Entwicklung flexibler Energieumwandlungssysteme geführt. Flexible wiederaufladbare Zink-Luft-Batterien (ZABs) mit hohen theoretischen Energiedichten zeigen ein erhebliches Potenzial als flexible Energiegeräte der nächsten Generation, die in tragbaren elektronischen Produkten eingesetzt werden können. Das Design hocheffizienter und luftstabiler Kathoden, die sowohl die Sauerstoffreduktionsreaktion (ORR) als auch die Sauerstoffentwicklungsreaktion (OER) elektrochemisch katalysieren können, ist sehr wünschenswert, aber auch eine Herausforderung. Flexible Katalysatoren auf Kohlenstoffbasis für die ORR/OER-Katalyse können grob in zwei Typen eingeteilt werden:(i) selbsttragende Katalysatoren basierend auf der in-situ-Modifikation flexibler Substrate; (ii) nicht selbsttragende Katalysatoren auf Basis von Oberflächenbeschichtungen von flexiblen Substraten. Zu den Methoden zur Optimierung der katalytischen Leistung gehören die Dotierung mit Atomen und die Regulierung der elektronischen Struktur und der Koordinationsumgebung. Dieser Aufsatz fasst die zuletzt vorgeschlagenen Strategien für die Synthese von Designer-Elektrokatalysatoren auf Kohlenstoffbasis und die Optimierung ihrer elektrokatalytischen Leistung in Luftelektroden zusammen. Und wir konzentrieren uns maßgeblich auf die Analyse der inhärenten aktiven Zentren und ihrer elektrokatalytischen Mechanismen, wenn sie als flexible ZABs-Katalysatoren verwendet werden. Die Ergebnisse dieser Überprüfung können bei der Entwicklung wertvollerer kohlenstoffbasierter Luftelektroden und ihrer entsprechenden flexiblen ZABs für die Anwendung in tragbaren elektronischen Geräten hilfreich sein.
Einführung
Die derzeitige übermäßige Nutzung nicht erneuerbarer Energien hat Bedenken hinsichtlich der Energiekrise aufkommen lassen. Um die aktuelle Energieknappheit zu lindern, müssen daher effizientere und umweltfreundlichere Stromversorgungsgeräte etabliert werden. Darüber hinaus hat das Aufkommen und die Popularisierung von dehnbaren, faltbaren und biegsamen tragbaren elektronischen Geräten das schnelle Wachstum und die Entwicklung flexibler Energiespeichersysteme ausgelöst [1,2,3]. Zink-Luft-Batterien (ZABs) weisen eine theoretische Energiedichte von 1086 Wh kg −1 . auf , das ist ungefähr das Fünffache der weit verbreiteten wiederaufladbaren Lithium-Ionen-Batterien. Darüber hinaus hat Zink die Vorteile reichlich vorhandener Reserven und großer Verfügbarkeit [4, 5]. Typische ZABs verwenden Zink als negative Elektrode, Sauerstoff als positive Elektrode und Kaliumhydroxid als Elektrolyt. Durch die Einführung hochstabiler Zinkanoden und wasserbasierter Elektrolyte sind ZABs ungiftig, umweltfreundlich und sicher und haben als vielversprechende Energiespeichersysteme breite Aufmerksamkeit gefunden [6]. Das grundlegende Funktionsprinzip von ZABs beinhaltet eine elektrochemische Reaktion zwischen Zink an der negativen Elektrode der Batterie und dem OH − in der Elektrolytlösung, was zur Freisetzung von Elektronen führt. Gleichzeitig kommen die Katalysatoren in der Gasdiffusionselektrode oder Luftkathoden-Reaktionsschicht mit dem Elektrolyten und dem Luftsauerstoff in Kontakt, und dann findet der Ladungstransfer statt. Beim Betrieb von wiederaufladbaren ZABs erfolgt die Umwandlung zwischen Sauerstoff und Wasser an der Luftelektrode; dazu gehören ORR und OER, die beide Mehrelektronen-Rekombinationsprozesse sind. Die spezifischen Reaktionen, die in alkalischen Lösungen auftreten, sind wie folgt:
$${\text{ORR}}:\,{\text{O}}_{2} \left( {\text{g}} \right) + 2{\text{H}}_{2} { \text{O}}\,\left( {\text{l}} \right) + 4{\text{e}}^{ - } \to 4{\text{OH}}^{ - }$$ (1) $${\text{OER}}:\,4{\text{OH}}^{ - } \to {\text{O}}_{2} \left( {\text{g}} \right) + 2{\text{H}}_{2} {\text{O}} \left( {\text{l}} \right) + 4{\text{e}}^{ - }$ $ (2)Es wurden verschiedene kinetische Modelle entwickelt, um die Reaktionswege während der ORR zu verstehen. Das erste Modell, entwickelt von Damjanovic et al. [7, 8], beinhaltet die Bildung von Wasserstoffperoxid in einem Reaktionsweg parallel zu dem, in dem O2 ohne die Bildung von Wasserstoffperoxid als Zwischenprodukt zu Wasser reduziert. Dies wird schematisch durch Gl. 1 und 2.
$${\text{O}}_{{2}} \to ^{{{\text{I}}_{{1}} }} {\text{H}}_{{2}} {\ text{O }}$$ (1) $$\begin{array}{*{20}c} {{\text{O}}_{{2}} \mathop{\longrightarrow}\limits^{{{ \text{I}}_{{2}} }}{\text{H}}_{{2}} {\text{O}}_{{2}} \mathop{\longrightarrow}\limits^{ {{\text{I}}_{{3}} }}{\text{H}}_{{2}} {\text{O}}} \\ { \downarrow {\text{I}}_ {4} } \\ {{\text{zu}}\,{\text{Lösung}}\,{\text{und}}\,{\text{Ring}}\,{\text{Elektrode}} } \\ \end{array}$$ (2)Wasserstoffperoxid, das als Reaktionszwischenprodukt in Weg 2 gebildet wird, wird teilweise an derselben Scheibenelektrode wie Wasser reduziert und teilweise durch konvektive Diffusion von der Scheibenelektrode in die Lösung und die Ringelektrode überführt. Ich1 , I2 und ich3 repräsentieren die jeweiligen Strömungen. Ich4 stellt die Geschwindigkeit dar, mit der Wasserstoffperoxid als Strom von der Scheibenelektrode wegdiffundiert. Das erzeugte Peroxid-Zwischenprodukt ist jedoch instabil, was den Reaktionsprozess komplizieren, die Elektrolytmembran beschädigen und die Aktivität des Katalysators sowie die Ausgangsspannung und die Energieumwandlungsrate der Brennstoffzelle verringern kann [9]. Daher die direkte 4e – Pfad (Gl. 1) wird als der ideale Pfad für die ORR angesehen, da er eine höhere Ausgangsspannung und Energieumwandlung hat als der 2e – Pfad (Gl. 2).
Da ein beträchtliches Überpotential der ORR erforderlich ist, um die mit dem mehrstufigen Elektronentransfer verbundenen Energiebarrieren zu überwinden [10], besteht die größte Herausforderung bei der Entwicklung flexibler wiederaufladbarer ZABs, die in großem Maßstab angewendet werden können, in der Verwendung von Luftkathoden in den ZABs, die ein übermäßiges Potenzial [11] und eine schlechte Sauerstoffreversibilität aufweisen, die durch die langsame ORR und OER während des Ladens und Entladens verursacht werden [12]. Die Pt/C-Elektroden zeigen die beste katalytische Leistung für die ORR, während IrO2 /RuO2 zeigt eine hervorragende katalytische Leistung in der OER. Diese Katalysatoren haben jedoch auch mehrere Nachteile, wie knappe Reserven, hohe Kosten, einzelne katalytische Aktivität und geringe Stabilität, die ihre Anwendung im großen Maßstab stark behindern [13]. Daher ist die Entwicklung eines erschwinglichen Katalysators mit hervorragenden bifunktionellen ORR/OER-Katalysatorleistungen für die Kommerzialisierung flexibler ZABs von entscheidender Bedeutung. Nichtedelmetalle, insbesondere Übergangsmetalle, haben aufgrund ihrer hohen Aktivität und ausgezeichneten thermischen Stabilität breite Aufmerksamkeit auf sich gezogen. Darüber hinaus besitzen Katalysatoren auf Kohlenstoffbasis bedeutende Vorteile, einschließlich struktureller Flexibilität, ausgezeichneter elektrischer Leitfähigkeit, guter chemischer und thermischer Stabilität und einfacher chemischer Funktionalisierung, zusätzlich zu ihrem geringen Gewicht. Daher gelten sie als vielversprechende Materialkandidaten für den Einsatz in tragbaren elektronischen Produkten. Es gibt mehrere ausgezeichnete Luftkathoden auf CC-Basis (Kohlenstoffgewebe); Eine der größten Herausforderungen ist jedoch die Identifizierung von Materialien mit hervorragender Leitfähigkeit, die gleichmäßig auf CC wachsen können. Wachsen die Materialien auf dem CC ungeordnet, verringert sich die Zahl der aktiven Zentren auf dem Katalysator. Herkömmliche ZABs verwenden eine wässrige Lösung als Elektrolyt, die die Anforderungen von flexiblen Festkörper-ZABs nicht erfüllen kann. Daher verwenden die meisten Festkörper-ZABs, die eine hervorragende Leistung aufweisen, Gelelektrolyte zum Leiten von Elektrizität, wie Polyvinylalkohol, Polyethylenoxid (PEO), Polyacrylamid (PAM) und Polyacrylsäure (PAA). Diese Gelelektrolyte werden zunehmend in ZABs eingesetzt, da sie eine starke Plastizität und eine gute Leitfähigkeit besitzen. Insbesondere Natriumpolyacrylat ist aufgrund seiner Pufferwirkung in alkalischen Elektrolyten in der praktischen Anwendung von Gelelektrolyten auf Wasserbasis stabil. [1]
In den letzten Jahren hat die Zahl der Studien zu flexiblen ZABs zugenommen, die einige theoretische Grundlagen für die praktische Herstellung und Anwendung von flexiblen ZABs liefern. Obwohl Zhu et al. veröffentlichten einen ausführlichen Überblick über eindimensionale Batterien [14] und Shi et al. bifunktionelle Katalysatoren im Detail vorstellten [15], wurde über die jüngsten Fortschritte, insbesondere in den letzten fünf Jahren, bei flexiblen ZABs mit kohlenstoffbasierten Katalysatoren nicht berichtet. Daher fasst diese Arbeit die Strategien für die Synthese von Kohlenstoff-basierten Katalysatoren und die Optimierung ihrer elektrokatalytischen Leistung in Luftelektroden zusammen, mit einem signifikanten Fokus auf der Analyse ihrer inhärenten aktiven Zentren und ihres elektrokatalytischen Mechanismus bei Anwendung als flexible ZABs-Katalysatoren.
Designer-Elektrokatalysatoren auf Kohlenstoffbasis
Kohlenstoffbasierte Materialien werden aufgrund ihrer hervorragenden Eigenschaften häufig in ZABs-Katalysatoren verwendet. Bei diesen Materialien handelt es sich hauptsächlich um Materialien auf Graphenbasis (einschließlich funktionalisiertem Graphen und Graphenprofilen); es werden jedoch auch Graphit, Fulleren und Carbon Nanotubes (CNTs) verwendet [16]. Dennoch leiden kohlenstoffbasierte Materialien bei der praktischen Anwendung von ZABs immer noch unter vielen Mängeln. Daher ist es notwendig, die Behandlung von Kohlenstoffmaterialien zu optimieren. Ein Beispiel hierfür sind N-dotierte poröse Kohlenstoffmaterialien, die außergewöhnliche bifunktionelle elektrokatalytische Leistungen in der ORR und OER aufweisen [17, 18]. Unter den verschiedenen Methoden zur Modifizierung von Kohlenstoffmaterialien kann die Dotierung mit einzelnen Atomen wie N, P und S die Katalysatoraktivität deutlich verbessern. In Anbetracht dessen haben einige Forscher N- und P-Co-Dotierung verwendet und festgestellt, dass der co-dotierte Katalysator eine ausgezeichnete Aktivität aufweist. Darüber hinaus wirken sich andere Methoden wie die Einzelmetalldotierung, Bimetalldotierung und Nanomaterialien eindeutig positiv auf die Katalysatorleistungsoptimierung von Kohlenstoffmaterialien aus. Methoden zur Entwicklung von Hochleistungselektrokatalysatoren für ZABs wurden jedoch kaum erforscht. Studien haben gezeigt, dass die Modifizierung von Kohlenstoffmaterialien wie Graphen und CNTs durch Dotierung die Oberflächeneigenschaften der Kohlenstoffmaterialien optimieren kann. Die typischste Strategie zur Optimierung der Katalysatorleistung besteht darin, heteroatomdotierte Kohlenstoff-Nanomaterialien mit Übergangsmetall-basierten Materialien (Oxide, Chalkogenide wie Ni-basierte Sulfide usw. [19,20,21], Übergangsmetallphosphiden (TMP [ 22]) und Nitrid) Verbundwerkstoffe. Da ZABs-Elektrokatalysatoren noch zahlreiche Mängel aufweisen, ist es von entscheidender Bedeutung, ihre katalytische Struktur zu optimieren. Derzeit werden elektronische Strukturanpassungen, Sauerstoffdefekte, Metall-Sauerstoff-Bindungen, Grenzflächenspannungen und atomare Dotierung häufig beim Design von ZABs-Katalysatoren verwendet.
Aufbau hocheffizienter Katalysatoren auf flexiblen Elektroden
Die flexible Elektrode wird in flexiblen ZABs durch die Gasdiffusionsschicht repräsentiert. Die Luftkathode wird durch direktes Aufwachsen eines hocheffizienten Katalysators auf der flexiblen Elektrode gebildet, was die Vorteile hat, selbsttragend zu sein und eine große Elektrodenkontaktfläche und eine starke Faltbarkeit zu haben. Selbsttragend bedeutet, dass kein nichtleitender Klebstoff erforderlich ist, wodurch eine Verschlechterung der Elektrodenleistung und ein Verlust des Katalysators bei wiederholter Verformung der Elektrode vermieden werden. Darüber hinaus wird die Verringerung der aktiven Stellen und die Erhöhung der Grenzflächenimpedanz durch die Verwendung nicht leitender Klebstoffe vermieden. Das Wachstum des Katalysators auf der expandierbaren Elektrode kann mit anderen Verfahren kombiniert werden, wie der Elektroabscheidung, dem hydrothermalen Verfahren und der Vulkanisation bei Raumtemperatur. Zu den häufig verwendeten flexiblen Elektroden gehören stickstoffdotierter Kohleschaum, Kohlefasergewebe, Kohlepapier und Kohlefilz, die eine ausgezeichnete elektrische Leitfähigkeit aufweisen.
Wachstum hocheffizienter Katalysatoren auf Kohlefasergewebe
Kohlefasergewebe, ein aus Kohlefasern aufgebautes Gewebe, ist das am häufigsten verwendete flexible Trägermaterial. Das Aufwachsen von hocheffizienten Katalysatoren direkt auf Kohlefasergewebe ist eine einfache und effektive Methode, die durch Lösungsreaktionen (Abb. 1a–c), Elektroabscheidung und eine Kombination anderer Methoden, z. B. auf engstem Raum, Wärmebehandlung [2], erreicht werden kann. (Abb. 1d, e), Carbonisierungs-Oxidation-CC und Ligand-unterstützte Kalzinierung (Herstellung eines ultradünnen CoOX Schicht [23]). Ein Beispiel für die Karbonisierungs-Oxidation ist das Wachstum verschiedener Kristallstrukturen, Morphologien und Partikelgrößen von 3D- und 2D-MOFs auf Kobaltbasis auf CC zur Herstellung einer bindemittelfreien Kathode, gefolgt von der Verankerung des geschichteten Co3 O4 Nanopartikel in Stickstoff-dotierten Kohlenstoff-Nanoarrays [24]. Das Nanofasernetzwerk wurzelt auf CC in einer Stickstoffatmosphäre, um eine bifunktionelle Luftkathode mit hervorragender katalytischer Leistung und bemerkenswerter Flexibilität zu erhalten [25]. Obwohl das Elektroabscheidungsverfahren weit verbreitet ist, um Elektrodenmaterialien herzustellen, ist aufgrund der inhärent schlechten Leitfähigkeit von Co3 O4 , weisen konventionelle Elektroabscheidungsverfahren Einschränkungen bei der Bildung eines Co3 . auf O4 Schicht mit großer Kontaktfläche auf einem leitfähigen Träger. Co3 O4 kann in situ auf dem Kohlefasergewebe aufgewachsen werden, um ein gleichmäßig gewachsenes ultradünnes Co3 . zu bilden O4 Schicht. Insbesondere das ultradünne Co3 O4 Schichten haben eine maximale Kontaktfläche auf dem leitfähigen Träger, was einen schnellen Elektronentransport erleichtert und eine Aggregation der ultradünnen Schichten während des Elektrodenpräparationsprozesses verhindert [26]. Darüber hinaus ist Co3 O4 kann in ein Nano-Mikroarray mit Schichtstruktur umgewandelt werden [24], wie in Abb. 1f dargestellt. Diese ultradünne Kobaltoxidschicht kann auch als Elektrokatalysator in ZABs verwendet werden [23], wie in Abb. 1g dargestellt.
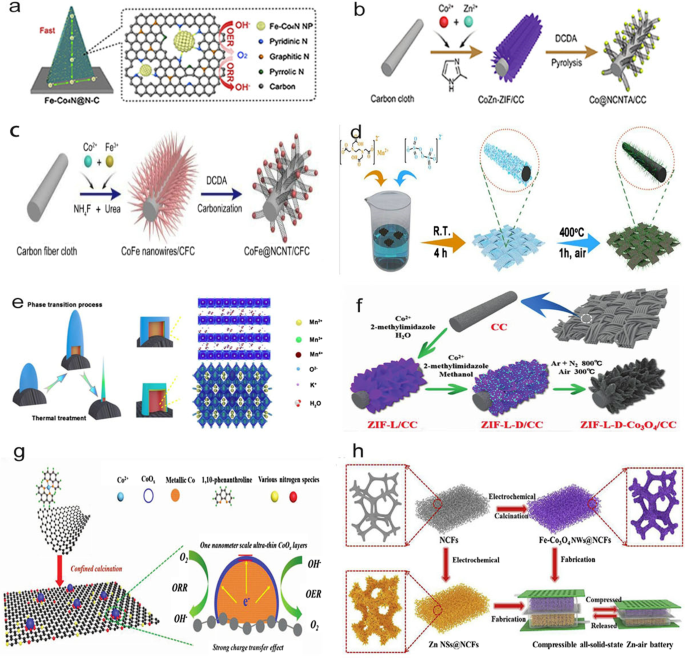
a Schema des Fe-Co4 Auf CC gewachsenes N@N–C-Nanoblatt zur Anwendung in der bifunktionellen Sauerstoffreaktion [56]. b Schematische Darstellung des Syntheseprozesses für Co@NCNTAs [85]. c Schema des Syntheseprozesses für CoFe@NCNT/CFC [98]. d Schema der Herstellung von MnOx -CC-400 [2]. e Vorgeschlagener Phasenübergang von Manganoxid auf CC über eine thermische Behandlung [2]. f Schema des ZIF-L-D-Co3 O4 /CC-Bildungsprozess [24]. g Schema eines 1 nm-CoOx Schicht auf dem metallischen Substrat aus Co/N-RGO [23]. h Schema der Herstellungsverfahren für die quetschbaren und wiederaufladbaren Festkörper-ZABs [27]
Wachstum effizienter Katalysatoren auf selbst hergestellten Schaumstoffen
Bei selbstgefertigten Schaumstoffen handelt es sich hauptsächlich um Carbonschaum und Nickelschaum. Panet al. verwendeten einen Melaminschwamm, der bei einer Temperatur von 800 °C geglüht wurde, um ein flexibles geschäumtes Kohlenstoffmaterial zu bilden, das dann als Arbeitselektrode verwendet wurde, um die Vorstufe für Fe-Co3 . galvanisch abzuscheiden O4 NWS@NCFs über ein skalierbares Elektroabscheidungsverfahren. Folglich könnte das flexible geschäumte Kohlenstoffmaterial in vollfesten Schwammbatterien verwendet werden [27], wie in Abb. 1h gezeigt. Das Nickelschaummaterial ist eine Art vernetzter Metallschwamm. Jianget al. zeigten, dass das Aufwachsen von Katalysatorelektroden in situ auf einem flexiblen Substrat Unordnung verursachen und dichte unregelmäßige Bereiche bilden würde, was die katalytische Aktivität verringern würde. Daher konstruierten sie eine geordnete mehrdimensionale Anordnung von 1D-CNTs, die mit 0D-Kobalt-Nanopartikeln (genannt MPZ-CC@CNT) und 2D-Kohlenstoff-Nanorippen auf einem Nickelschaummaterial dekoriert sind. Während der Pyrolyse des bimetallischen 2D-ZnCo-Koordinationsgerüsts wurden CNTs mit einem hohen Gehalt an N-Dotierung in situ aus dem hochdispersen Kobalt gezüchtet, wodurch eine offene und geordnete Anordnung gebildet wurde [28], wie in Abb. 2a dargestellt.
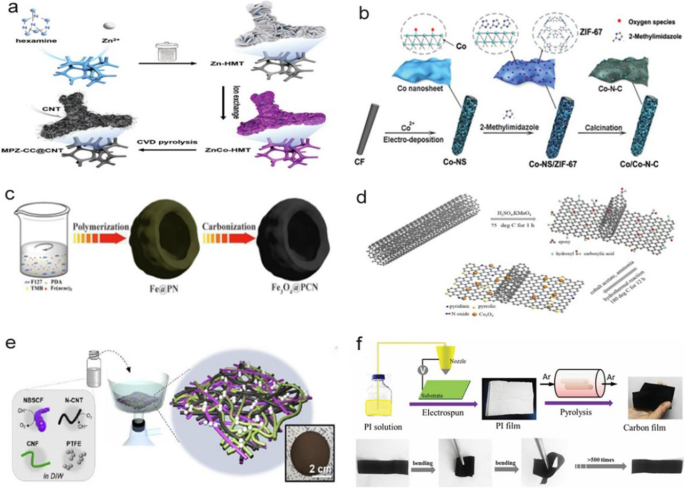
a Schematische Darstellung des Herstellungsprozesses für MPZ-CC@CNT [28]. b Synthese des Co/Co-N-C-Katalysators [29]. c Schema der Herstellung des Fe3 O4 @PCN-Katalysatoren [40]. d Schema der Co3 O4 /N-p-MCNTs-Kompositkatalysatorsynthese [41]. e Schema des Herstellungsverfahrens für die MH-Papierluftkathode, zusammen mit ihrer Fotografie [43]. f Schematische Darstellung des Herstellungsverfahrens für den NCNF und Fotos des resultierenden flexiblen NCNF [44]
Synthese hocheffizienter Katalysatoren auf Kohlefilz
Carbonfilz ist ein Vliesstoff. Yuet al. [29] entwickelten eine neuartige Strategie zur Synthese von Co-N-C-Nanoblättern auf Kohlenstofffilz (Co/Co-N-C), die Co-Nanoinseln mit einer 3D-Schichtstruktur enthalten, wie in Abb. 2b dargestellt. Diese ungewöhnliche Struktur führt zu einem guten Kontakt zwischen den Co-Nanoinseln und den Co-N-C-Nanoblättern. Darüber hinaus ist die Koexistenz von Co 0 und Co 2+ verbesserte die elektrokatalytische Leistung des bifunktionellen (ORR/OER) Katalysators. Daher kann die insgesamt einzigartige Schichtstruktur den effektiven Elektronen-/Ionentransport in ORR und OER weiter fördern [29]. Neben dem Aufwachsen von 3D-Nanoelektroden auf Kohlenstofffilz kann auch eine nanoskalige ultradünne Kobaltoxid (CoOx)-Schicht auf Kohlenstofffilz (d. h. einem metallischen Co/N-dotierten Graphensubstrat) hergestellt werden [23]. Diese ultradünne Struktur bietet günstige Voraussetzungen für die Anwendung in ZABs.
Synthese hocheffizienter Katalysatoren auf Kohlepapier
Kohlefaserpapier (CFP) besteht aus Kohlefasern und wird durch den Papierherstellungsprozess hergestellt. CFP kann verwendet werden, um die ORR- und OER-Leistungen von nichtmetallischen Elektrokatalysatoren wie g-C3 . zu verbessern N4 . G-C3 N4 hat einen hohen Stickstoffgehalt und kann somit eine ausreichende Anzahl aktiver Zentren für elektrokatalytische Reaktionen bereitstellen und das ORR-Potential reduzieren [30]. Seine elektrokatalytische Leistung ist jedoch aufgrund seiner Nichtleitfähigkeit, die zu einer schlechten Elektronenübertragungsfähigkeit führt, erheblich eingeschränkt [30]. G-C3 N4 mit unterschiedlichen Morphologien können mit unterschiedlichen Wärmebehandlungsmethoden hergestellt werden [30]. Die ORR- und OER-Leistungen des Katalysators können optimiert werden, indem g-C3 . behandelt wird N4 , wie zum Beispiel 1) die Synthese eines hocheffizienten Katalysators unter Verwendung von g-C3 N4 als Vorlage [31, 32], 2) Anwendung eines g-C3 N4 -unterstützte Pyrolysestrategie [33,34,35] oder 3) Einführung von g-C3 N4 in Kohlenstoff. Phosphordotiertes g-C3 N4 kann direkt auf CFP wachsen, das als flexible Sauerstoffelektrode ausgeführt werden kann. Dies ist der erste nichtmetallische bifunktionelle ORR/OER-Elektrokatalysator, der durch die Kombination von blütenartigem Pg-C3 . gebildet wird N4 bestehend aus dünnen Nanoschichten von g-C3 N4 und CFP. Der Elektrokatalysator enthält ein 3D-Hybridnetzwerk mit hohem N-Gehalt und hoher P-Dotierung, das eine hervorragende ORR- und OER-Aktivität und Haltbarkeit [36] sowie eine gute Lade- und Entladeleistung auch bei Biegeverformung bewirkt .
Synthese hocheffizienter Katalysatoren auf engstem Raum
Die Synthese hocheffizienter Katalysatoren auf engstem Raum kann die Dotierungseffizienz erhöhen, den Wärmeverlust reduzieren und die mesoporösen Eigenschaften verbessern, wodurch ihre ORR-Leistung verbessert wird. Die begrenzten Räume können Molekularsieb-Nanokanäle sein, wie Montmorillonit, 2–4-6 Tripyridyltriazin, CNTs, Kohlenstoff-Nanoblätter und dotierte Kohlenstoffschichten. Zahlreiche Versuche haben auch gezeigt, dass auf engstem Raum hergestellte Katalysatoren eine verbesserte katalytische Wirkung aufweisen. Das Dotieren von Übergangselementen und nichtmetallischen Elementen auf engstem Raum kann die katalytische Effizienz erheblich verbessern. Es wurde über N- und S-Codotierung [13], N- und P-Codotierung [12], zweidimensionale Stickstoffdotierung [37, 38] usw. berichtet. Darüber hinaus wurde festgestellt, dass bei einer plasmaunterstützten Dotierungsstrategie auf engstem Raum der Ätzeffekt des Plasmas dem engen Raum Porosität verleihen kann, wodurch mehr aktive Zentren freigelegt werden, was langfristig förderlich ist Haltbarkeit und effektiver Elektronentransport des Elektrokatalysators [39]. Zhanget al. verwendeten eine Weichmembranmethode, um Fe3 . herzustellen O4 in eine poröse Kohlenstoff-Nanoschale gehüllt, die eine ausgezeichnete katalytische Leistung und langfristige Haltbarkeit zeigt [40], wie in Abb. 2c gezeigt. Die Co3 O4 Nanopartikel wurden auf den mit Stickstoff dotierten, teilweise abgeblätterten mehrwandigen CNTs verankert, was zu einer hervorragenden katalytischen Leistung führte [41], wie in Abb. 2d gezeigt.
Kombination hocheffizienter flexibler Katalysatoren
Ein kombinierter Katalysator umfasst einen einzelnen funktionellen Katalysator, der aus demselben Material in verschiedenen Formen besteht, oder einen bifunktionellen Katalysator, der aus verschiedenen Materialien besteht. Xuet al. erreichten eine ORR-Luftkathode mit einer einzigen Funktion durch gleichzeitiges Entwerfen ausgerichteter, kreuzweise gestapelter und poröser CNT-Folien, wobei die CNT-Folien als Gasdiffusionsschicht, Katalysatorschicht und Stromkollektor fungierten, und synthetisierte neue faserige, flexible und dehnbare ZABs [42]. Der Luftkathodenkatalysator in flexiblen ZABs weist typischerweise eine unzureichende katalytische ORR/OER-Aktivität auf und erfordert harte Synthesebedingungen, einschließlich hoher Temperaturen/hoher Drücke und saurer (oder alkalischer) Lösungen. Neben den Problemen bifunktioneller Luftkatalysatoren hängen die mechanischen Eigenschaften der Luftkathode stark von den mechanischen Eigenschaften ihres Substrats ab, was zu einem Mangel an Formvielfalt und Verformbarkeit des Luftkathodenblechs führt. Auf dieser Grundlage haben Lee et al. verwendeten einen kombinierten hocheffizienten flexiblen Katalysator für die OER und stickstoffdotierte CNTs für die ORR [43], wie in Abb. 2e gezeigt. Die monolithische hetero-nanomatte Papierluftkathode besteht aus einem bifunktionellen 1D-Katalysatorgemisch, Cellulose-Nanofasern und Polytetrafluorethylen-Nanopartikeln, ohne dass herkömmliche Stromkollektoren und Gasdiffusionsschichten erforderlich sind [43]. Zhanget al. synthetisierte eine neue Art von NiCo2 O4 /N-dotierter Kohlenstoff-Nano-Mesh-bifunktioneller Elektrokatalysator bestehend aus hohlem NiCo2 O4 Nanosphären und N-dotiertes Kohlenstoff-Nanonetz [40]. Der bifunktionelle Elektrokatalysator wurde durch Flüssigphasensynthese synthetisiert und anschließend wärmebehandelt, wonach er zu einer Batterie zusammengebaut wurde.
Selbstgemachte flexible Kathodenfolie
Liuet al. stellten einen nanoporösen Kohlenstoffnanofaserfilm (NCNF) her, indem ein elektrogesponnener Polyimid(PI)-Film unter einer Ar-Atmosphäre pyrolysiert wurde. Wie in Abb. 2f gezeigt, besitzt das NCNF Flexibilität und eine hohe mechanische und Zugfestigkeit. Die Zugfestigkeit des NCNF beträgt 1,89 MPa und der Zugmodul beträgt 0,31 GPa. NCNF weist eine nanoporöse 3D-Kohlenstoffnetzwerkstruktur und eine große spezifische Oberfläche auf, die kurze und schnelle Elektronen-/Ionenpfade und reichlich Gasdiffusionskanäle bereitstellen kann. Noch wichtiger ist, dass das Elektrodendesign auch die Vorteile hat, Polymerbindemittel zu eliminieren und den Herstellungsprozess zu vereinfachen sowie Batteriegröße und -kosten zu minimieren. Die flexiblen, vollfesten wiederaufladbaren ZABs mit der NCNF-Luftkathode weisen eine hohe Entladungsspannung auf (~ 1,0 V @ 2 mA cm −2 ), niedrige Ladespannung (~ 1,8 V @ 2 mA cm −2 ), hohe Energiedichte von 378 Wh kg −1 und ausgezeichnete mechanische und zyklische Stabilität. Diese Ergebnisse legen die Möglichkeit groß angelegter Anwendungen der ZABs nahe [44].
Optimierungsstrategien für die Leistung des ZAB-Katalysators
In den letzten Jahren hat sich die Forschung an kostengünstigen und hocheffizienten Elektrokatalysatoren für ORR und OER rasant entwickelt. Obwohl es viele Kontroversen bezüglich des spezifischen katalytischen Prozesses gibt, der während der Elektrokatalyse abläuft, ist es sicher, dass eine größere Anzahl effektiver aktiver Zentren im Katalysator zu einer besseren katalytischen Aktivität führt. Im Prozess der Leistungsoptimierung von ZABs-Katalysatoren kann die atomare Dotierung auf Kohlenstoff zu Synergien und strukturellen Defekten sowie zur Anpassung der elektronischen Struktur, der Koordinationsumgebung und der Katalysatorstruktur führen. Daher kann die elektrokatalytische Wirkung des Katalysators durch Dotieren der Kohlenstoffmaterialien mit bestimmten Atomen verbessert werden. Atomare Dotierung kann in Einzelatom-Dotierung und Multiatom-Dotierung eingeteilt werden, wobei die Atome entweder Metallatome oder Heteroatome sein können. Sowohl die Einzelatom-Dotierung als auch die Mehratom-Dotierung können die elektrokatalytische Leistung des Katalysators verbessern.
Atom-Doping
Durch Kompositionsanalyse und Dichtefunktionaltheorie-Berechnungen haben Yu et al. festgestellt, dass eine N-Dotierung die Leitfähigkeit und die Sauerstoffaufnahmekapazität des Katalysators effektiv verbessern kann; eine übermäßige N-Dotierung führt jedoch zu einer Abnahme der Reaktionskinetik [45]. Synergistischer Effekt und strukturelle Defekte können durch Dotierung mit Heteroatomen erreicht werden.
Einzelatom-Dotierung
Zur Einzelatomdotierung können Heteroatome (N, P, S etc.) und Metalle (Fe, Co, Mn etc.) verwendet werden. Unter diesen ist die N-Dotierung die am häufigsten verwendete Einzelatomdotierung auf Kohlenstoff. Die N-Dotierung kann die Elektronentransporteffizienz und die Sauerstoffadsorptionsstärke erhöhen sowie die Reaktionskinetik des Katalysators verbessern, was zu Defekten und der Freilegung aktiverer Zentren führt. Yu et al. gezeigt, dass eine N-Dotierung die elektronische Leitfähigkeit und O2 . signifikant verbessern kann Adsorptionsfähigkeit von Co3 O4 Nanodrähte durch experimentelle Untersuchungen und Dichtefunktionaltheorie (DFT)-Rechnungen [45]. Aufgrund der Lücke zwischen den Blechen können Übergangsmetalle wie Co [5], Ni, Mn [46, 47] (wie in Abb. 3b, c), Fe und Cu auf aktiven Substratmaterialien, wie z als Kohlenstoffmaterialien (Graphen, CNTs usw.). Es wurde auch bestätigt, dass 2D-Heteroatome einzigartige Strukturen und physikalische und chemische Eigenschaften aufweisen, wie N, P, S [22, 48] und B [49,50,51,52,53,54] (wie in Abb. 3d, e), kann die elektrochemische und elektrokatalytische Leistung der Katalysatoren verbessern.
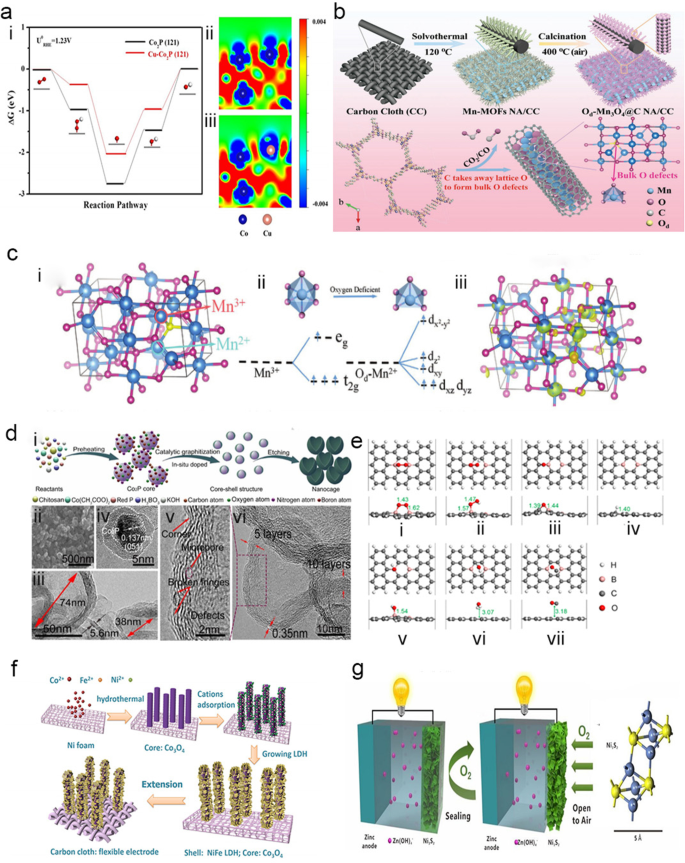
a (i) Freie-Energie-Diagramm der ORR über Co2 P- und Cu-dotiertes Co2 P-Oberflächen. Die unterschiedlichen Ladungsdichten von (ii) Co2 P (121) und (iii) Cu-dotiertes Co2 P (121). Die blauen und roten Bereiche zeigen getrennt die Verarmung und Ansammlung von Elektronen an [22]. b Darstellung des Syntheseverfahrens des Od-Mn3 O4 @CNA/CC-Nanostruktur und ihre Bildungsmechanismen auf atomarer Ebene. Die blauen, rosa, grauen und gelben Kugeln repräsentieren die Mn-, O-, C- bzw. Od-Atome [46]. c (i) Superzellenmodell von Mn3 O4 . (ii) oktaedrische und pyramidale Mn-O-Kristallfelder und die d-Orbitalaufspaltungskonfigurationen. (iii) Elektronendichteunterschiede von Od-Mn3 O4 (rosa Kreis steht für Mn 3+ , himmelblauer Kreis steht für Mn 2+ ) [47]. d Synthese und morphologische Charakterisierung von NB-CN [52]. (i) Illustration des Bildungsmechanismus des graphitischen Kohlenstoff-Nanokäfigs. (ii) SEM-Bild und (iii) TEM-Bild von NB-CN. (iv) HR-TEM-Bild von NB-CN vor dem Waschen mit Säure und (v) HR-TEM-Bild von NB-CN. e Optimierte Adsorptionsstrukturen der ORR-Zwischenstufen und CO auf BGNR [54]:(i) O2 , (ii) OOH, (iii) O, (iv) H, (v) OH, (vi) H2 O und (vii) CO. f Schematische Darstellung des Syntheseprozesses des Co3 O4 @NiFe-LDH-Hybrid-Nanodraht-Arrays auf Ni-Schaum bzw. flexiblem Kohlenstoffgewebe [24]. g Schematische Darstellung von Zn-Ni3 S2 Batterie und Zink-Luft-Batterie und Strukturdiagramm von Ni3 S2 molekular bzw. [23]
Mehratom-Dotierung
Multiatom-Dotierung umfasst sowohl Heteroatom-Co-Dotierung (NS, NP, NB usw.) als auch Heteroatom- und Metall-Co-Dotierung [55] (Fe-Co-N [56], Mn-N [57], Fe- N [58], Co-Fe-NP [12], Co-Fe-N [39], Co-Mn-NP [59], Co-Cu-N [60, 61], Co-Cu-P usw. .). Einerseits kann die Dotierung mit Heteroatomen effektiv synergistische Defekteffekte im Katalysator erzeugen, die zu einer höheren katalytischen Aktivität führen [62, 63]. Andererseits wurde bestätigt, dass die Co-Dotierung mit Übergangsmetallatomen und Heteroatomen die Sauerstoffreduktionsleistung des Katalysators effektiv verbessern kann [64, 65]. Außerdem besteht ein synergistischer Effekt zwischen Multimetallen und Heteroatomen, der die elektrokatalytische Aktivität des Katalysators erhöht. Multimetalle können die Leitfähigkeit und den Oxidationszustand des Katalysators verbessern und dadurch den Ladungstransfer des Katalysators [66] und die elektrokatalytische Leistung des Katalysators erhöhen [60]. Diao et al. durch DFT festgestellt, dass Cu-Dotierung zu positiveren Zentren neben Co führen und die Bindungskraft zwischen den oberflächenaktiven Zentren und den adsorbierten Zwischenprodukten schwächen kann, wodurch die Massen- und Ladungstransferraten und die Freilegung aktiver Zentren erhöht werden [61]. Wie in Fig. 3a gezeigt, in Cu-dotiertem Co2 P, an den Co-Zentren, die den Cu-Atomen benachbart sind, tritt eine deutliche Elektronenverarmung auf, was darauf hindeutet, dass eine Cu-Dotierung die Elektronenverteilung von Co2 . verändern kann P [22].
Synergistischer Effekt
Ein synergistischer Effekt in der Katalyse kann als signifikante Steigerung der katalytischen Aktivität definiert werden, wenn mehrere Elemente (Metalle oder Nichtmetalle) oder Verbindungen kombiniert werden, im Vergleich zu einer alleinigen Verwendung dieser Elemente oder Verbindungen. Der synergistische Effekt kann die Regulierung der elektronischen Struktur des Katalysatorsubstrats unterstützen, die elektrokatalytische Aktivität erhöhen [37, 67] und kann eine starke Koordination erzeugen, um aktivere Zentren zu erzeugen [56]. Diese Zusammenarbeit kann in die folgenden Kategorien eingeteilt werden:
-
Hochaktive Metall-/Nichtmetall-Gruppen erfahren einen Synergismus mit den leitfähigen dotierten Kohlenstoff-/Stickstoff-Substraten. Ein Beispiel für diese Kategorie sind Metall-Stickstoff-Kohlenstoff (M-N-C)-Verbindungen [68,69,70], wie beispielsweise Co-N-C-Verbindungen. An der Grenzfläche zwischen Co und dem N-dotierten Kohlenstoff können aktive Co-N-C-Zentren vorhanden sein, was die Bildung/Abscheidung von O* erleichtern kann. Darüber hinaus wurde gezeigt, dass das Co-Nx Zentren und das in die Kohlenstoffmatrix eingebettete N sind aktive Zentren in Nichtedelmetall-ORR-Hybridkatalysatoren [68]. Andere Beispiele sind Übergangsmetalle (Co und Fe) auf N-dotiertem Kohlenstoff [39, 71, 72], Pyridin-N [58], Graphitisierung-N [71], Co-Azo-Spezies [71], N, P co- dotierte Materialien, geschichtete N-dotierte heteroporöse Kohlenstoffnanofasern mit ausgezeichneten Elektronentransportwegen und einer hohen spezifischen Oberfläche [10] und Graphen-Nanokomposite. Graphen-Nanokomposite wurden durch hydrothermales in-situ-Wachstum von CoSe- und Nickelselenid-Nanopartikeln auf Graphen-Nanoblättern (GNs) synthetisiert. Der synergistische Effekt zwischen den Komposit-Nanopartikeln und Graphen verbessert die elektrochemische Leistung des Katalysators [73, 74]. Am wichtigsten ist, dass bewiesen wurde, dass die starke Koordination zwischen dem Metallzentrum und Pyridin-N die Bildung aktiver Pyridin-NM-Zentren fördern kann und das elektronenreiche Pyridin-N den Ladungstransfer zum Metallzentrum effektiv beschleunigen kann, wodurch die ORR-Aktivität stark verbessert [75, 76].
-
Die Synergie zwischen Metallen verleiht den Katalysatoren einen Legierungseffekt, der die elektronische Struktur des Systems anpasst und die Sauerstoffkombination optimiert [74, 77]. Die synergistische Wirkung bimetallischer aktiver Zentren auf die Sauerstoffelektrokatalyse wurde bereits untersucht. Für das NiCo2 S4 @g-C3 N4 -CNT integrierte flexible Elektrode, Elektronen werden vom bimetallischen Ni/Co-Aktivzentrum auf das reichlich vorhandene Pyridin-N in g-C3 . übertragen N4 und kooperieren mit dem gekoppelten leitfähigen CNT, um eine reversible Sauerstoffelektrokatalyse zu fördern. Theoretische Berechnungen zeigen, dass die Pyridinmetall-N-Spezies (Ni, Co-N2 ) hat einen einzigartigen Co-Aktivierungseffekt auf das bimetallische Ni/Co-Atom. Es reduziert sein d-Band-Zentrum und erleichtert die Adsorption/Desorption von Sauerstoffzwischenprodukten, wodurch die Reaktionskinetik beschleunigt wird. In einem codotierten Fe-O4 N@NC-Nanoblatt-Array kann das Metallzentrum einen starken Koordinationseffekt mit dem Pyridin-N erzeugen, und die Co-Dotierung mit Fe und N fördert die Bildung einer großen Zahl aktiver Pyridin-NM-Zentren in der ORR [78,79 ,80,81]. In hybridisiertem porösem Co3 O4 verankert auf MnO2 , Co und Mn erzeugen einen Kopplungseffekt, beschleunigen dadurch die Elektronentransportrate, bilden eine Pufferzone und beschleunigen die Trennung der Katalysatoroberflächenprodukte [82]. Ein weiteres Beispiel sind Cu- und Co-modifizierte N-dotierte GNs mit Co-Nanopartikeln [60]. Darüber hinaus ist die ausgezeichnete elektrokatalytische Aktivität von Co2 P@CNF kann durch die starke Wechselwirkung zwischen dem Co2 . erklärt werden P-Nanokristalle und die poröse Kohlenstoffbeschichtung co-dotiert mit CoNx und N und P, was zu einem verbesserten Grenzflächenladungstransport und einer Regulierung des Co2 . führt Elektrokatalytische Aktivität von P [83]. Ein neues 2D-MoSe2 -Ni(OH)2 Material wurde auch durch eine einfache einstufige hydrothermale Synthese hergestellt. Das 2D-MoSe2 -Ni(OH)2 Nanohybrid mit einer einzigartigen vertikal ausgerichteten Nanoblattstruktur bietet eine große elektroaktive spezifische Oberfläche, verkürzt die Diffusionslänge der Elektrolytionen und verbessert dadurch die elektrochemische Reaktionskinetik [84].
Strukturmängel
Es wird angenommen, dass sich Defekte, einschließlich Gitterverzerrungen, gebrochene Streifen und Kantenstellen an den Ecken, positiv auf die katalytische Aktivität auswirken. Es wurde festgestellt, dass Defekte an den Kanten von DG (defektes Graphen) die Änderungen der freien Energie von ORR und OER reduzieren können, wodurch die katalytische Aktivität und Leitfähigkeit von DG verbessert werden [85]. Beispielsweise kann die Einführung von P-Atomen in die N-dotierte Kohlenstoffmatrix effektiv einen synergistischen Defekteffekt und eine N-P-Struktur erzeugen, wodurch die katalytische Leistung in der OER und ORR optimiert wird [12]. Inzwischen H2 [86] und Ar-Plasmaätzen können auch verwendet werden, um Materialien mit reichen Defektstrukturen zu bilden.
Anpassung der elektronischen Struktur und Koordinationsumgebung
Bezüglich der elektronischen Struktur des Katalysators wurde allgemein geschätzt, dass die Oberflächenladungsverteilung des Katalysators durch Einbringen von Defekten, wie etwa dotierten heterometallischen Kationen, eingestellt werden kann. Die Defekte, einschließlich Sauerstofffehlstellen (VO) [77], können die Zahl der katalytisch aktiven Zentren erhöhen oder dem Katalysator eine neue katalytische Aktivität verleihen [87]. VO kann durch Ar-Plasmaätzen erreicht werden [88]. In alkalischen Medien sollte ein effizienter ORR-Katalysator in der Lage sein, Sauerstoff durch den Vier-Elektronen-Reduktionsprozess vollständig zu Hydroxid zu reduzieren, während ein schwächerer ORR-Katalysator die Reaktionssequenz mitten im Zwei-Elektronen-Transferprozess beendet. Lian et al. bewiesen, dass eine 3D-Orbitalkonfiguration des Metallzentrums die ORR durch Anpassung des Oxidationszustands und des elektronischen Zustands des Metallzentrums fördert. Darüber hinaus kann eine lokale Koordination die Umwandlungsrate der Ziel-Redoxsubstanzen weiter beschleunigen [10]. Auch Co-Atome besitzen aufgrund ihrer unterschiedlichen möglichen Valenzzustände eine ausgezeichnete Aktivität. Co 2+ und Co 3+ besetzen die tetraedrischen und oktaedrischen Plätze von Co3 O4 , die bei der Förderung des Elektronentransfers in der OER hilft [11]. Darüber hinaus wurde die Abscheidung von ultradünnen NiFe-geschichteten Doppelhydroxiden (NiFe-LDHs) auf der Oberfläche von Co3 O4 kann die chemische Oberflächenvalenz von Co, Ni und Fe durch Änderung des Elektronendonor- und/oder Elektronenabsorptionseffekts einstellen, was zu einem Gleichgewicht und einer Optimierung der ORR- und OER-Leistung führt [89], wie in Abb. 3f gezeigt.
Erhöhung der Anzahl der Porenstrukturen
Nanostrukturierte Materialien haben reiche Porenstrukturen und eine große Anzahl mesoporöser Kanäle, die eine entscheidende Rolle bei der Modifizierung von Sauerstoffübertragungskanälen [11] spielen, die Einfangzeit von Sauerstoffmolekülen verlängern und ihre Wechselwirkung mit den katalytisch aktiven Zentren verstärken. Einige nanostrukturierte Materialien weisen eine 2D/3D-Struktur auf [90], die eine größere spezifische Oberfläche aufweist und die Zahl der Dreiphasengrenzflächen erhöht. Durch rationales Design kann ein nanostrukturiertes poröses Material mit großer Oberfläche und hoher Leitfähigkeit konstruiert werden, um sicherzustellen, dass mehr Nanopartikel in direktem Kontakt mit dem Elektrolyten stehen, was zu einem geringeren Widerstand zwischen dem Aktivmaterial und dem Elektrolyten führt [83]. Eine reiche Porenstruktur kann den Ladungstransfer und die Diffusion zwischen Ladungen beschleunigen und den Massentransfer erhöhen, wodurch die Leistung des Katalysators verbessert wird [11, 39]. Die Oberflächen nanostrukturierter Materialien haben einen stabilen niedrigen Brechungsindex und können Sauerstoffadsorptionsenergien ähnlich der Oberfläche von Pt aufweisen [91]. Diese Eigenschaft ist Teil der Bedingungen, die für die hocheffiziente katalytische Leistung des Katalysators erforderlich sind. Nanostrukturierte Materialien, die als Luftkathode von ZABs verwendet werden können, umfassen Ni3 C/NC-Nanoblätter (2D), Ni3 S2 /Ni-Nanoblatt-Arrays [1] (wie in Abb. 3g gezeigt), einheitliches poröses Co3 O4 Nanopartikel/Nanosheets [11, 45], N-dotierte CNTs (normalerweise als aktives Substrat verwendet), hohles NiCo2 O4 Nanosphären, N-dotierte CNTs [92] und MoSe2 /G-Nanohybride [93].
Anpassung der Katalysatorstruktur
Um eine Reaktion zu katalysieren, ist ein Katalysator mit einer vernünftigen Struktur erforderlich. Übergangsmetalloxide mit Spinellstruktur können helfen, Überpotentiale zu reduzieren und dadurch die Energieumwandlungseffizienz des Katalysators zu verbessern [82, 94]. Die 2D/3D-Struktur des Katalysators kann aufgrund der vergrößerten Kontaktfläche zwischen dem aktiven Zentrum und dem Elektrolyten zu einer hervorragenden katalytischen Aktivität führen. Zum Beispiel Co-dotierte, nanoporöse NiO-Blüten, bei denen der synergistische Effekt zwischen dem 2D-hexagonalen Rahmen und einer großen Anzahl von Nanoporen auf der Seite des Nanoblatts die Anzahl der effektiven katalytisch aktiven Zentren für O2 . erhöht Adsorption/Diffusion [5]; und die einzigartige 3D-geschichtete Co/Co-NC-Systemstruktur, die eine effiziente Anzahl aktiver Zentren bereitstellen kann [29]. Andere Beispiele sind ein neues Graphen-Wasserstoff/B-dotiertes Quantenpunkt-Verbundmaterial mit einer einzigartigen 3D-Struktur, hoher Porosität und großer spezifischer Oberfläche, das eine Fülle von katalytisch aktiven Zentren und einen verbesserten Elektrolytmassentransport und Ionendiffusion aufweist [95], und ein 2D-Co-MOF, das direkt auf CC gezüchtet wird und dem 3D-Co-MOF-Wachstum ausreichend Platz bietet, um eine geschichtete 3D-auf-2D-MOF-Systemstruktur zu bilden. Im Vergleich zu einem ausschließlich 3D- oder 2D-MOF werden mehr katalytisch aktive Zentren exponiert [24]. Darüber hinaus erleichtert das 3D-Gerüst die vollständige Durchdringung des Elektrolyten und fördert den Elektronentransport in der porösen Netzwerkstruktur [41]. Außerdem kann die Miniaturisierung des Volumens des katalytischen Materials auch die katalytische Effizienz verbessern. Auf atomarer Ebene beispielsweise ein ultradünnes CoOx Schicht beschleunigt effektiv die Elektronenleitung und bietet reichlich aktive Zentren. Dies ist auf die Einführung der Co-Oxidation in die Nanoblätter zurückzuführen, die die Zahl der exponierten aktiven Zentren erhöhen kann [23]. Ein weiteres Beispiel ist ein 2D-La(OH)3 . -Graphen-Nanohybrid, hergestellt durch eine einfache und wirtschaftliche solvothermale Reduktionstechnik, die elektrostatisch auf 2D-GNs verankert wird, um die Aggregation von Lanthanhydroxid zu verhindern und mehrere elektroaktive Zentren für die Reaktion bereitzustellen [96].
Schlussfolgerungen und Zukunftsaussichten
Obwohl die aktuelle Forschung zu ZABs erhebliche Fortschritte gemacht hat, gibt es noch große Herausforderungen, darunter die Entwicklung neuer Methoden zur Synthese selbsttragender flexibler Kathoden, die Untersuchung elektrokatalytischer Mechanismen und die Identifizierung geeigneter Materialien zur Synthese flexibler Kathoden mit hervorragender katalytischer Leistung. Als eines der wichtigen Katalysatormaterialien für ZABs haben kohlenstoffbasierte Katalysatoren aufgrund ihrer großen spezifischen Oberfläche, der zahlreichen aktiven Zentren und der guten elektrischen Leitfähigkeit große Aufmerksamkeit auf sich gezogen. Kohlenstoffmaterialien leiden jedoch immer noch unter einigen Nachteilen, wie etwa der unsicheren Toxizität von CNTs, höheren Kosten als andere flexible Elektrokatalysatormaterialien und schlechter Wiederholbarkeit auf verschiedenen Substraten; Kohlenstoffmaterialien, die aus natürlichen Biomaterialien gewonnen werden, weisen eine relativ geringe Flexibilität und Leitfähigkeit auf, was die Leistung der tragbaren elektronischen Geräte, in denen sie verwendet werden, einschränkt. Es wird erwartet, dass eine umfassende Untersuchung der Katalysatormikrostruktur und des Effekts der atomaren Dotierung sowie der internen Beziehung zwischen der elektronischen Verteilung des Katalysators und seiner elektrokatalytischen Sauerstoffreduktionsleistung eine entscheidende Rolle bei der effektiven Identifizierung der tatsächlichen Rolle von Metallionen spielt. N, S und P sowie andere Dotierungselemente an den aktiven Zentren und vertiefen das Verständnis des ORR-Prozesses der Kohlenstoffkatalysator-Elektrokatalyse. Wir erwarteten, zur Entwicklung erschwinglicher, leistungsstarker kohlenstoffbasierter Nichtedelmetall-ORR-Katalysatoren beizutragen. Ein flexibles elektronisches Produkt auf Kohlenstoffbasis wurde verwendet, um den menschlichen Puls und die Atemfrequenz zu erfassen [97]. Es wird davon ausgegangen, dass in Zukunft mehr multifunktionale flexible elektronische Geräte auf der Grundlage von flexiblen ZAB-Katalysatoren auf Kohlenstoffbasis kommerzialisiert werden.
Verfügbarkeit von Daten und Materialien
Unzutreffend. Alle Bilder im Artikel wurden zitiert.
Abkürzungen
- ZABs:
-
Zink-Luft-Batterien
- ORR:
-
Sauerstoffreduktionsreaktion
- OER:
-
Sauerstoffentwicklungsreaktion
- CC:
-
Carbontuch
- PEO:
-
Polyethylenoxid
- PAM:
-
Polyacrylamid
- PAA:
-
Polyacrylsäure
- CNTs:
-
Kohlenstoff-Nanoröhrchen
- TMP:
-
Übergangsmetallphosphide
- CFP:
-
Kohlefaserpapier
- DFT:
-
Dichtefunktionaltheorie
- DG:
-
Defektes Graphen
- VO:
-
Sauerstoff offene Stellen
- NiFe-LDHs:
-
NiFe-geschichtete Doppelhydroxide
Nanomaterialien
- Hygienisches Design für die Lebensmittel- und Verarbeitungsindustrie
- Nanopartikel für die Krebstherapie:Aktuelle Fortschritte und Herausforderungen
- Fortschritte und Herausforderungen fluoreszierender Nanomaterialien für die Synthese und biomedizinische Anwendungen
- Das Design der Emissionsschicht für Elektronenvervielfacher
- Tauchbeschichtungsverfahren und Leistungsoptimierung für elektrochrome Drei-Zustands-Bauelemente
- Synthese und elektrochemische Eigenschaften von LiNi0.5Mn1.5O4 Kathodenmaterialien mit Cr3+ und F− Verbunddotierung für Lithium-Ionen-Batterien
- Herstellung von PPy-beschichteten MnO2-Hybrid-Mikromaterialien und ihre verbesserte zyklische Leistung als Anode für Lithium-Ionen-Batterien
- Effizientes und effektives Design von InP-Nanodrähten für maximale Sonnenenergiegewinnung
- Auswirkung verschiedener Bindemittel auf die elektrochemische Leistung einer Metalloxidanode für Lithium-Ionen-Batterien
- Sechs Lieferkettenstrategien für Öl und Gas in Zeiten des Coronavirus



