Herstellung von thermoresponsiven Polymer-Nanogelen aus Oligo(Ethylenglycol)diacrylat-Methacrylsäure und deren Eigenschaftscharakterisierung
Zusammenfassung
Stimuli-responsive Polymere haben in den letzten Jahren aufgrund ihrer breiten Anwendung in verschiedenen Bereichen zunehmende Aufmerksamkeit erfahren. Ein neuartiges stimuliresponsives Polymer, basierend auf Oligo(ethylenglycol)diacrylat (OEGDA) und Methacrylsäure (MAA), P(OEGDA-MAA), wird durch Fällungspolymerisation hergestellt und weist nachweislich einen LCST-Typ-VPTT (Volumenphase Übergangstemperatur) bei 33 °C in Wasser und eine VPTT vom UCST-Typ bei 43 °C in Ethanol, alle bei einer Konzentration von 1 mg/ml. Beide VPTTs sind stark konzentrations- und pH-abhängig, was eine einfache Möglichkeit bietet, die Phasenübergangstemperatur einzustellen. Das Polymer wird hinsichtlich seiner Zusammensetzung und seiner Morphologie in Wasser und in Ethanol in unterschiedlicher Konzentration charakterisiert. Die beiden Übergänge werden anhand der Ergebnisse untersucht und interpretiert. Diese Arbeit bietet einen neuen Weg zur Herstellung eines neuen Typs von stimuliresponsiven Polymeren mit großem Potenzial für verschiedene Anwendungen, insbesondere in biomedizinischen Bereichen, da bekannt ist, dass PEG-basierte stimuliresponsive Polymere nicht toxisch und nicht immunogen sind.
Hintergrund
Stimuli-responsive Polymere sind in der Lage, auf externe Stimuli mit erheblichen Veränderungen ihrer physikalisch-chemischen Eigenschaften zu reagieren [1,2,3]. Dank dieser Reaktionsfähigkeit wurde eine große Vielfalt ihrer Anwendungen entwickelt, einschließlich Aktuatoren, Wirkstoffabgabe, Gentransfer und Stofftrennung [4,5,6,7]. Unter den üblichen äußeren Reizen wie Temperatur, pH, Ionenstärke, elektrisches Feld und Ultraschall haben Polymere, die auf Temperaturänderungen reagieren, nämlich wärmeempfindliche Polymere, seit Jahrzehnten große Aufmerksamkeit erfahren [1,2,3,4,5,6, 7,8,9], von denen die Polymere mit einer Volumenphasenübergangstemperatur (VPTT) oder einer niedrigeren kritischen Lösungstemperatur (LCST) für unvernetzte lösliche Polymere mit Abstand am häufigsten untersucht wurden. Dies gilt insbesondere für P(N -Isopropylacrylamid), PNIPAM, ein wärmeempfindliches Polymer, das aufgrund seiner VPTT in Wasser bei etwa 32 °C, nahe der menschlichen Körpertemperatur, umfassend auf seine potenziellen biomedizinischen Anwendungen untersucht wurde [2, 9,10,11,12].
Es ist allgemein anerkannt, dass PNIPAM-basierte Materialien eine erkennbare Hysterese aufweisen, starke Wasserstoffbrücken-Wechselwirkungen mit Proteinen aufweisen und während der Hydrolyse Amine mit niedrigem Molekulargewicht produzieren. All diese Eigenschaften haben ihre Anwendungen im Bereich der Biotechnologie eingeschränkt [13]. Vor kurzem wurde eine neue Familie von Polymeren (PEG) basierend auf Oligo(ethylenglycol) (OEG) mit thermoresponsiven Eigenschaften entwickelt [14,15,16,17]. Allerdings ist PEG in Wasser nur bei erhöhter Temperatur und unter Druck thermoresponsive [18], was PEG für viele Anwendungen ungeeignet macht. Um seine Anwendungen als thermoresponsive Materialien zu erweitern, besteht die gängige Praxis darin, funktionelle Gruppen an einem oder beiden seiner OEG-Enden zu befestigen, wodurch ein OEG-Makromonomer entsteht, das dann durch verschiedene Prozesse polymerisiert wird, darunter beispielsweise anionische [19], kationische [20] , Gruppentransferpolymerisation [21, 22]; konventionelle radikalische Polymerisation [23]; eine Vielzahl von lebenden Polymerisationen auf Basis freier Radikale, einschließlich ATRP [24], RAFT [25, 26] und NMP [27]; und diverse andere Polymerisationsverfahren [28, 29]. Es ist mittlerweile bekannt, dass die VPTT oder LCST der OEG-basierten Polymere durch Änderung der experimentellen Bedingungen ihrer Synthese angepasst werden kann, um ihre Strukturen zu ändern, einschließlich beispielsweise des Molekulargewichts, der Architektur und der Länge des EG-Segments, das Verhältnis und die Struktur der Comonomere und die Natur der Endgruppen. All dies wurde in aktuellen Übersichtsartikeln [1, 17] gut dargestellt.
Es ist bemerkenswert, dass die absolute Mehrheit der berichteten Studien zu OEG-basierten responsiven Polymeren mit einem Ende des OEG-Monomers, das durch (Meth)acrylat funktionalisiert ist, während das andere Ende mit einem Ether abgeschlossen ist, hergestellt wurde. Die so hergestellten Polymere bestehen daher aus einem Rückgrat der (Meth)acrylsegmente mit den OEG-Ketten als anhängende Gruppen, was das OEG-Polymer zu einer kammartigen Kette macht. Ein weiteres gemeinsames Merkmal der bisher berichteten OEG-basierten Polymere ist, dass diese Polymere meist durch Polymerisation eines einzelnen OEG-Makromonomers [19] oder Copolymerisation von zwei oder mehr OEG-Makromonomeren unterschiedlicher OEG-Länge oder -Struktur hergestellt wurden [14,15, 16], in beiden Fällen nicht vernetzt. Vor diesem Hintergrund wird in dieser Arbeit ein neuartiges OEG-basiertes Polymer, P(OEGDA-MAA), durch Copolymerisation von Oligo(ethylenglycol)diacrylat (OEGDA) mit Methacrylsäure (MAA) durch Fällungspolymerisation in Wasser. Das so gebildete Polymer ist daher aufgrund der Diacrylatstruktur vernetzt und reagiert nachweislich mit einer VPTT in Wasser, die dem allgemein berichteten Phasenübergang vom LCST-Typ ähnelt, während dieses Polymer in Ethanol eine VPTT vom UCST-Typ zeigt. Beide VPTTs sind stark konzentrationsabhängig. Diese Phasenübergänge werden hinsichtlich Polymerzusammensetzung und Morphologie in Dispersion bei unterschiedlicher Konzentration charakterisiert. Diese Arbeit liefert daher einen neuartigen Typ von stimuliresponsiven Polymeren mit großem Potenzial für verschiedene Anwendungen, insbesondere in biomedizinischen Bereichen.
Methoden
Materialien
Oligo(ethylenglycol)diacrylat (OEGDA, Mn = 575) wurde von Aladdin (Shanghai, China) bezogen. Methacrylsäure (MAA) stammte von Tianjin Guangcheng Chemicals (Tianjin, China), wobei die Inhibitoren entfernt wurden, indem sie durch basisches Al2 . geleitet wurden O3 (Sinopharm Chemical Regent Co. Ltd., Shanghai, China). Ammoniumpersulfat (APS) wurde von Tianjin Hedong Hongyan Chemicals (Tianjin, China) geliefert. Die Dialysebeutel (MWCO 3500) stammten von Union Carbide Corporation (Shanghai, China).
Vorbereitung von P(OEGDA-MAA)
Das Copolymer aus OEGDA und MAA, P(OEGDA-MAA), wurde durch Fällungspolymerisation in Wasser hergestellt. Für ein typisches Verfahren wurden MAA (0,1834 g, 2,11 mmol) und OEGDA (0,8166 g, 1,43 mmol, Molverhältnis von OEGDA/MAA = 40/60) in 500 ml entionisiertes Wasser, das zuvor in einem Glaskolben mit 1 l Liter Fassungsvermögen. Nach dem Spülen mit Stickstoff, um Sauerstoff zu entfernen, wurde APS-Lösung (10 Gew.-%, 300 μl) zugegeben. Der Kolben wurde schnell verschlossen und in ein Wasserbad bei 70 °C gestellt, um die Polymerisation normalerweise für 4 h zu starten. Der klare Inhalt in der Flasche wurde nach der Initiierung schnell trübe, was auf die Ausfällung des Polymers hinweist. Am Ende der Polymerisation wurde das Reaktionssystem auf Raumtemperatur abgekühlt und die trübe emulsionsartige Mischung verwandelte sich in eine klare Polymerdispersion, zu der eine bestimmte Menge NaCl-Lösung (2 M) mit einem pH-Wert von 1,0 vor- mit Salzsäure eingestellt, zugegeben. Die Zugabe von NaCl-Lösung provozierte die Ausfällung des Polymers, das durch Zentrifugation bei 10.000 U/min gesammelt, in Wasser redispergiert und schließlich 72 h bei Raumtemperatur gegen entionisiertes Wasser dialysiert wurde, um NaCl zu entfernen.
Charakterisierung
1 Die H-NMR-Analyse der Polymere wurde auf einem 400-MHz-NMR-Spektrometer (Avance III, Bruker, Schweiz) unter Verwendung von Dimethylsulfoxid-d . durchgeführt 6 (DMSO-d 6 ) als Lösungsmittel. Die Morphologie des getrockneten Polymers wurde unter Verwendung eines Rasterelektronenmikroskops (SEM, FEI Quanta Feg-250, US) beobachtet. Der OEGDA-Gehalt des Polymers wurde durch potentiometrische Titration bestimmt, wie zuvor beschrieben [30]. Eine Dispersion des Polymers in entionisiertem Wasser (1,0 mg/ml) wurde mit einer kalibrierten NaOH-Lösung von etwa 0,1 M auf pH 11,5 titriert. Der pH-Wert der Dispersion wurde gemessen und mit einem pH-Meter (Metrohm 808 Titrandio, Schweiz) aufgezeichnet. Der Äquivalenzpunkt wurde verwendet, um den MAA-Gehalt im Copolymer zu bestimmen. Die VPTT von P(OEGDA-MAA) in einer Magendispersion (pH = 1,0, 150 mM NaCl) wurde wie zuvor beschrieben gemessen [30]. Die VPTT von P(OEGDA-MAA) in seiner Ethanoldispersion wurde bestimmt, indem die Transmission der Dispersion bei einem Licht von 565 nm unter Verwendung eines Spektrophotometers (UV3101PC, Shimadzu, Japan) verfolgt wurde. Die Polymerdispersion wurde zunächst auf 70 °C oberhalb der Übergangstemperatur erhitzt, 5 min äquilibriert und anschließend von 65 °C auf 10 °C im Abstand von 5 °C mit ebenfalls einer Gleichgewichtszeit von 5 min bei jeder Temperatur abgekühlt . Die Durchlässigkeit gegen die Temperatur wurde aufgezeichnet und die Temperatur, bei der 50% der maximalen Durchlässigkeit erreicht wurden, wurde als VPTT genommen. Die Größe und Größenverteilung von P(OEGDA-MAA)-Hydrogelen in Ethanol und in Wasser wurde durch dynamische Lichtstreuung (DLS, Nano-ZS, Malvern Instruments, UK) gemessen.
Ergebnisse und Diskussion
Zusammensetzungsanalyse von P(OEGDA-MAA)
Es ist bemerkenswert, dass in den berichteten Präparaten verschiedener OEG-basierter thermoresponsiver Polymere die überwiegende Mehrheit der OEG-Makromonomere nur an einem Ende funktionalisiert ist und für die meisten davon Methacrylat als Endgruppen verwendet wird, während für die Comonomere niedermolekularer Gewicht wird eine Vielzahl von (Meth)Acrylaten und Acrylamiden verwendet und MAA wird selten verwendet [3, 13,14,15,16,17]. Um einen neuartigen Typ von OEG-basierten thermoresponsiven Polymeren herzustellen, wurde ein neuer Typ von OEG, bei dem beide Enden mit Acrylat funktionalisiert sind (OEGDA), in Wasser mit MAA, ebenfalls einem selten verwendeten Monomer, copolymerisiert (siehe zusätzliche Datei 1:Abbildung S1). Die Polymerisation wurde mit 40 % OEGDA in Mol durchgeführt. Die Zusammensetzung des erhaltenen P(OEGDA-MAA) wurde von 1 . analysiert H-NMR (Abb. 1). Die Zuordnung der Peaks erfolgte anhand der verwendeten Monomere (siehe Zusatzdatei 1:Abbildung S2) und der berichteten Polymere mit ähnlicher Struktur [31]. Die Gruppe der Peaks bei einer chemischen Verschiebung von 1,2 ppm oder einer niedrigeren Zone wurde den Methylprotonen in der MAA-Einheit im Polymer zugeordnet; der große und scharfe Peak bei 2,0 ppm wurde den Protonen in der aus MAA- und Acrylsegmenten bestehenden Hauptkette zugeordnet, während die Gruppe der großen Peaks von 3,2 bis 3,9 ppm den Protonen des Ethylens des Rückgrats zugeordnet wurde. Die charakteristischen Peaks bei chemischen Verschiebungen von 12,35 und 4,11 ppm (Abb. 1), die dem Carboxylproton von MAA (Ha) und den Oxyethylenesterprotonen (Hb) unmittelbar benachbart zu den Acrylateinheiten zugeschrieben werden, wurden verwendet, um die Zusammensetzung der Copolymer. Der OEGDA-Gehalt im P(OEGDA-MAA)-Copolymer wurde nach Gl. 1:
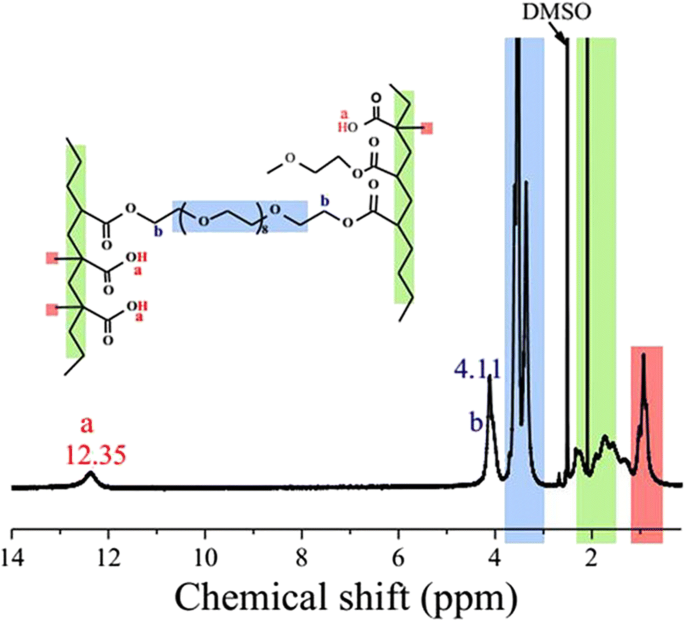
1 H-NMR-Spektrum von P(OEGDA-MAA)
$$ \left[\mathrm{OEGDA}\right]\ \mathrm{in}\ \mathrm{das}\ \mathrm{Copolymer}\ \left(\mathrm{mol}\%\right)=\left({ S}_{\textrm{b}}/4\right)/\left({S}_{\textrm{a}}+{S}_{\textrm{b}}/4\right) $$ ( 1)wo S a ist die integrierte Oberfläche des Peaks bei 12,35 ppm, die die Carboxylprotonen und S . darstellt b ist der Peak bei 4,11 ppm [30]. Somit wurde ein OEGDA-Gehalt im Copolymer von 40,9 Mol-% erhalten. Derselbe OEGDA-Gehalt wurde auch durch potentiometrische Titration geschätzt (siehe Zusätzliche Datei 1:Abbildung S3), was 38,8 Mol-% für den OEGDA-Gehalt ergab. Verglichen mit dem Verhältnis der für die Polymerherstellung verwendeten Monomere (40 Mol-% OEGDA) kann man schlussfolgern, dass die beiden Monomere OEGDA und MAA vollständig copolymerisiert wurden.
Morphologie von P(OEGDA-MAA)
Zur Herstellung der wässrigen Dispersion von P(OEGDA-MAA) wurde das getrocknete Polymerhydrogel bekannter Menge in einer bestimmten Menge Wasser bei Raumtemperatur dispergiert, eine klare lösungsartige Dispersion wurde durch einfaches Schütteln des Fläschchens erhalten, da dies wurde unterhalb der VPTT des Polymers in Wasser durchgeführt, im Folgenden als niedrige VPTT bezeichnet. Für die Dispersion von P(OEGDA-MAA) in Ethanol wurde eine bekannte Menge des Polymers zu Ethanol einer bekannten Menge in einer Glasflasche mit Schraubverschluss gegeben, die zuvor in einem Wasserbad bei 70 °C unter magnetischem Rühren angeordnet war. Unter leichtem Rühren bildete sich je nach Polymerkonzentration innerhalb von 30 min bis 1 h eine quasi-klare Dispersion. Für alle Dispersionen in Ethanol mit unterschiedlicher Polymerkonzentration wurden sie 1 h lang auf 70 °C erhitzt, um die äquilibrierte Quellung für das Polymer zu erreichen, gefolgt von einem Abkühlen auf Raumtemperatur, was die quasi-klaren Dispersionen trübe. da diese Raumtemperatur weit unter der VPTT des Polymers in Ethanol lag. Die klare wässrige Dispersion und die trübe Suspension des Polymers in Ethanol wurden herausgenommen und auf den Probenträger getropft, um die Morphologie durch SEM zu beobachten. Ausgewählte Bilder sind in Abb. 2 dargestellt. Es ist ersichtlich, dass für die aus der wässrigen Dispersion hergestellte Probe (1,0 mg/ml, Abb. 2a ). Es ist bemerkenswert, dass die Polymerisation bei 70 °C durchgeführt wurde, einer Temperatur, die deutlich über der niedrigen VPTT des Polymers liegt, bei der Polymerpartikel gebildet wurden. Obwohl das gebildete Polymer nicht wasserlöslich war, müssen sie stark hydrophil sein, da sie hauptsächlich aus Ethoxylat und Methacrylsäure bestehen. Vor diesem Hintergrund ist es denkbar, dass das Polymer in einem späteren Stadium der Polymerisation ausfällt, da beobachtet wurde, dass die klare Lösung ca. 33]. Außerdem war die Monomerkonzentration sehr niedrig (0,2 Gew.-%) und das gebildete Polymer P(OEGDA-MAA) war vernetzt. All dies zusammengenommen war die Bildung von Nanogel-Partikeln mit sehr kleiner Größe, etwa 40 nm im getrockneten Zustand, nicht überraschend. Bei Raumtemperatur in Wasser, entweder durch Abkühlen des Polymerisationssystems am Ende der Polymerisation oder durch erneutes Dispergieren des getrockneten Polymers in Wasser, werden diese Hydrogelteilchen vermutlich auf molekularer Ebene nicht wirklich gelöst, weil das Polymer vernetzt war, sie wurden stattdessen durch Wasser so stark gequollen, dass das Polymerisationssystem wie eine veritable Polymerlösung mit einer Transmission von 100 % aussah (Abb. 3). Tatsächlich ist eine hydrodynamische Partikelgröße (R h , der Radius) von ca. 12 nm wurde in diesem System am Ende der Polymerisation durch DLS nachgewiesen (Zusatzdatei 1:Abbildung S4). Im Vergleich zur Größe (Durchmesser, 40 nm) der Partikel im trockenen Zustand (Abb. 2a) war die DLS-Größe der Hydrogelpartikel noch kleiner, was darauf hindeutet, dass die Hydrogelpartikel während der Wasserverdampfung in der REM-Probe aggregiert haben müssen. Dies ist leicht zu verstehen, da die Hydrogelpartikel mit 100 % Transmission in ihrer wässrigen Dispersion stark gequollen sein müssen und im trockenen Zustand viel kleinere Partikel als die DLS-Größe erwartet worden wären, wenn sie unabhängig voneinander gehalten worden wären und bildeten feste Partikel, wenn das Lösungsmittel entfernt wurde. In dem Wissen, dass das vernetzte Polymer vollständig gequollen war, wobei ihre hydrophilen Kettenenden weitgehend in die umgebende Wasserphase verlängert waren, sollten ihre hydrophilen Ketten und Enden bis zu einem gewissen Grad durchdringt werden. Dies machte die gesamte Dispersion sehr homogen. Die 100 % Transmission der Dispersion war ein Hinweis auf die Homogenität. Unter diesen Umständen war eine gewisse Aggregation der Hydrogelteilchen bei der Wasserverdampfung nicht unerwartet; es sollte eigentlich unvermeidlich sein.

SEM-Bilder von P(OEGDA-MAA), die aus ihrer Dispersion bei Raumtemperatur und unterschiedlicher Konzentration in Wasser bei 1 mg/ml erhalten wurden (a ) und in Ethanol mit 5 mg/ml (b ) und 10 mg/ml (c )
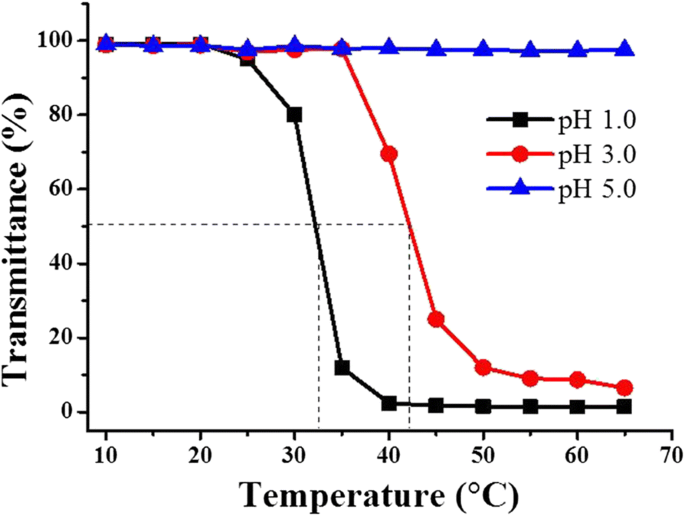
Abhängigkeit der Lichtdurchlässigkeit der P(OEGDA-MAA)-Dispersion (1,0 mg/ml, 150 mM NaCl) von der Temperatur bei verschiedenen pH-Werten
Bezüglich der trüben Mischung von P(OEGDA-MAA) in Ethanol bei Raumtemperatur wurde die Probe auf die gleiche Weise hergestellt, indem sie auf den Probenträger getropft und die Morphologie unter SEM beobachtet wurde. Für die Probe mit einer Konzentration von 5 mg/ml wurde festgestellt, dass die Nanopartikel, die in Wasser beobachtet wurden, wie in Abb. 2a gezeigt, verschwanden (Abb. 2b). Stattdessen traten aggregierte Körnchen des Hydrogel-Polymers auf, und die Größe der Körnchen war signifikant größer als die der Partikel, die aus ihrer Wasserdispersion erhalten wurden (Abb. 2a). Dies ist ein starker Hinweis darauf, dass die Entquellung bei den beiden Dispersionstypen recht unterschiedlich war.
Es ist am wahrscheinlichsten, dass die Hydrogel-Polymerketten in Ethanol oberhalb der hohen VPTT des UCST-Typs stärker durchdringt waren als in Wasser unterhalb der niedrigen VPTT des LCST-Typs. Dies ist sehr wahrscheinlich, da Ethanol in Struktur und Hydrophilie P(OEGDA-MAA) ähnlicher ist. Durch Abkühlen auf Raumtemperatur verklebten die ursprünglichen Nanopartikel der Hydrogel-Polymere, die bei ihrer Synthese gebildet und weitgehend über dieser UCST-Typ-hohen VPTT aufgequollen waren, und wurden daher die Granulate bzw. deren Aggregation beobachtet. Bei einer höheren Konzentration (10 mg/ml, Abb. 2c) in Ethanol schien es, dass die Hydrogel-Polymerketten weiter durchdringt wurden, sodass ein kontinuierlicher Hydrogelfilm mit zufällig verteilten kleinen Körnchen gebildet wurde.
Niedrige VPTT von P(OEGDA-MAA) Hydrogel in Wasser
Dieses Polymer, P(OEGDA-MAA), wie oben synthetisiert, reagierte auf Wärme (Fig. 3), und die Reaktionsfähigkeit war auch stark vom pH-Wert abhängig. Eine VPTT von 33 °C wurde in Wasser bei einer Konzentration von 1 mg/ml und einem pH-Wert von 1,0 nachgewiesen, und diese VPTT verschob sich bei 42 °C und pH 3 zu einer höheren Temperatur, ein deutlicher Anstieg mit steigendem pH-Wert. Bei einer weiteren Erhöhung des pH auf 5 zeigte das Polymer keine Änderung der Lichtdurchlässigkeit, d. h. die VPTT verschwand. Diese Beobachtungen legen nahe, dass die Anwesenheit von Wasserstoffionen notwendig war, damit das Hydrogelpolymer thermoreaktiv ist, ganz anders als die meisten der OEG-basierten Materialien, die mit carbonsäurefreien Monomeren hergestellt wurden und die bei pH = 7 oder höher reagieren [34] . Es ist bekannt, dass ein responsives Polymer bei Raumtemperatur durch unterschiedliche Wechselwirkungen zwischen ihren Ketten und Wassermolekülen solubilisiert oder gequollen wird, wenn sie vernetzt sind, dh ihr VPTT-Verhalten kann als Folge der Konkurrenz zwischen hydrophilen Polymer-Wasser-Wechselwirkungen und hydrophoben Polymer-Polymer-Wechselwirkungen [1, 2, 7, 16, 35]. Unterhalb dieser VPTT werden die Wechselwirkungen zwischen dem hydrophilen Anteil des Polymers und Wasser begünstigt, Wassermoleküle sind um die Polymerketten herum angeordnet und bilden Wasserstoffbrücken mit den hydrophilen EG-Segmenten, was zur Solubilisierung des Polymers führt, wenn es linear ist, und zur Quellung, wenn es vernetzt wird, während oberhalb von VPTT , wird diese Wechselwirkung von Wasser-Polymer synchron mit erhöhten Wechselwirkungen zwischen dem hydrophoben Polymer selbst reduziert, was zur Dehydratisierung der Polymerketten und deren Selbstaggregation führt. Bei den meisten OEG-basierten Polymeren ohne Carboxylgruppe gibt es keinen starken Wasserstoffbrückendonor in ihren Ketten, sondern schwache Van-der-Waals-Wechselwirkungen. Die pH-Abhängigkeit von VPTT ist relativ moderat. Die Situation ändert sich jedoch dramatisch, wenn Carboxylgruppen in die Polymerketten eingebaut werden, wie im vorliegenden Fall für P(OEGDA-MAA). Bei niedriger Temperatur (< VPTT) in Kombination mit einem niedrigen pH-Wert unterhalb des pKa (4,8) der Carbonsäure [1, 3] werden die Carbonsäuregruppen protoniert und können die Rolle des Protonendonors für den Ethersauerstoff des Polymers spielen, um . zu bilden Wasserstoffbrückenbindung, und eine solche Komplexierung führt zu einer Art Schrumpfung des Hydrogels, weil die Wechselwirkung von Wassermolekülen mit den Polymerketten auf diese Weise reduziert wird, obwohl die Polymerketten hydratisiert bleiben und das Polymer mit hoher Transmission solubilisiert erscheint. Bei hohem pH-Wert werden die Carboxylgruppen ionisiert, was zu einer elektrostatischen Abstoßung zwischen den negativ geladenen Polymerketten führt. Diese Abstoßung ist viel größer als alle Wechselwirkungen, die durch die Nichtelektrolyt-Polymerketten untereinander oder mit Wasser erreicht werden können, dh Van-der-Waals- und Wasserstoffbrückenbindungen, und bringt die Polymerketten in ihren möglichst ausgedehnten Zustand:eine vollständige bei den nicht vernetzten Polymeren wird eine Auflösung erreicht, und bei den chemisch vernetzten Polymeren werden die Ketten weitgehend verlängert, wobei das Polymer weitgehend gequollen ist [3]. In Abb. 3 war das Verschwinden von VPTT bei pH 5 der Fall, wenn eine große Anzahl der Polymerketten ionisiert wurde, was als Folge eine Abstoßung zwischen den Polymerketten erzeugte, wodurch sie auch bei einer höheren Temperatur gequollen bleiben, ohne dass das Kollabieren Zustand beobachtet. Bei einem niedrigeren pH (z. B. pH 3) gab es weniger ionisierte Carboxylgruppen an derselben Polymerkette, die bei einer gegebenen Temperatur weniger verlängert wurde; die Wechselwirkungen von nichtelektrolytischen Polymerketten, wie Van-der-Waals- und Wasserstoffbrückenbindungen, gewannen an Bedeutung, und daher wurde eine verzögerte VPTT bei einer höheren Temperatur nachgewiesen. Offensichtlich ist der pH-Wert umso niedriger; die niedrigere ist die VPTT, genau wie in Abb. 3. Außerdem gilt dies nur für Polymerketten, die bei hohem pH-Wert negativ geladen werden. Für Polymere, die bei hohem pH-Wert kationisch werden (z. B. solche mit Amingruppen), ist das Gegenteil der Fall:VPTT erscheint bei höheren pH-Werten und verschwindet bei niedrigeren pH-Werten [3, 36].
Dieser VPTT-Übergang wurde durch die Größenvariation der Hydrogelpartikel gut demonstriert, bestimmt durch DLS bei verschiedenen Temperaturen (Abb. 4) an einer wässrigen Dispersion von P(OEGDA-MAA) bei einer Konzentration von 1 mg/ml und einem pH-Wert von 1,0. Bei einer Temperatur unterhalb der VPTT (33 °C) wurden sehr kleine Partikel nachgewiesen. Die Größe nahm mit dem Temperaturanstieg langsam und kontinuierlich zu, von etwa 15 nm bei 10 °C auf etwa 20 nm bei 25 °C. Ein abrupter Anstieg der Partikelgröße wurde mit dem Temperaturanstieg über die VPTT festgestellt, ein Durchmesser der Partikel von etwa 600 nm wurde bei 35 °C, knapp über der VPTT (33 °C), festgestellt; sobald die Temperatur die VPTT überschritten hat, wurde eine weitere langsame und allmähliche Zunahme der Größe der dispergierten Polymerhydrogele beobachtet. Es war ziemlich offensichtlich, dass die hier nachgewiesenen Größen, etwa 600 nm bei 35 °C und 1100 nm bei 60 °C, die der aggregierten Hydrogelpartikel waren, im Vergleich zu denen, die unterhalb der VPTT erhalten wurden. Abbildung 4 zeigt, dass die Dehydratisierung des thermoresponsiven Polymers viel früher vor der VPTT begann; es war bei der VPTT oder in einem Temperaturbereich sehr nahe daran, dass die Dehydration stark beschleunigt wurde, was das Schrumpfen und Aggregat der Partikel aufgrund der Dehydratation förderte, und dass eine starke Abnahme der Transmission festgestellt wurde, wie in Abb. 3 dargestellt Die Größenvariation der Hydrogel-Partikel zeigte auch, dass sich die durch Dehydration verursachte Aggregation der Hydrogel-Partikel noch nach der VPTT entwickelte; es war nicht einfach durch Lichtdurchlässigkeit nachweisbar, da die Abnahme der Durchlässigkeit dadurch im Vergleich zur hohen Opazität in diesem Zustand recht minimal war.
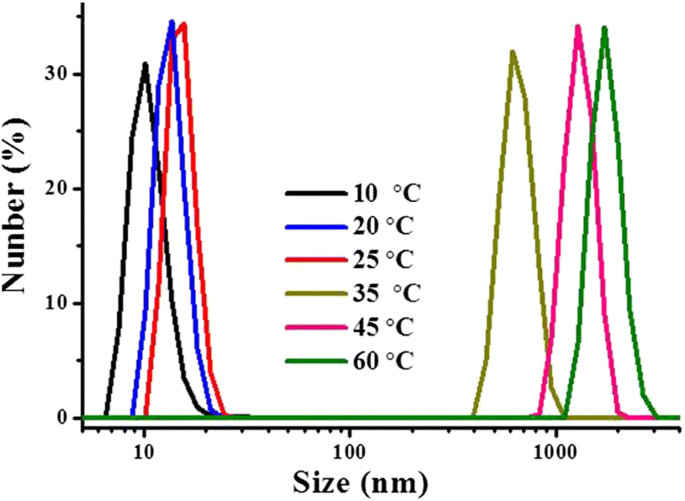
Durchmesser des thermoresponsiven P(OEGDA-MAA)-Hydrogels in wässriger Dispersion (1 mg/ml, pH 1,0) bei unterschiedlicher Temperatur
Neben der Abhängigkeit der Reaktionsfähigkeit vom pH-Wert, wie in Abb. 3 zu sehen, hängt das thermoresponsive Verhalten des Materials auch eng mit der Ionenstärke, der Konzentration und der Erwärmungs-/Abkühlgeschwindigkeit zusammen. Von verschiedenen Autoren wurde gezeigt, dass die VPTT von OEG-basierten Polymeren eher konzentrationsunempfindlich ist [14, 37]. Wu et al. berichteten in einer Studie an einem Copolymer von 2-(2-Methoxyethoxy)ethylmethacrylat mit Oligo(ethylenglycol)methylethermethacrylat, dass ein geringfügiger Unterschied beobachtet wurde und vermutlich auf eine höhere Konzentration (10 Gew.-%) als in anderen Studien zurückgeführt wurde [16]. Der Einfluss der Polymerkonzentration auf die VPTT wurde kurz untersucht, wobei die Konzentration zwischen 1,0 und 5,0 mg/ml variierte (siehe Zusatzdatei 1:Abbildung S5). Es wurde festgestellt, dass im Vergleich zu der VPTT, die bei 33 °C für das Hydrogel bei einer Konzentration von 1,0 mg/ml beobachtet wurde, die VPTT bei einer Konzentration von 2,0 mg/ml zu einer niedrigeren Temperatur von 29 °C und zu einem weiteren verschoben wurde niedrigere Temperatur von etwa 27 °C, wobei die Konzentration auf 5,0 mg/ml erhöht wurde. Dies ist einfach auf den Konzentrationseffekt des Copolymers zurückzuführen. Bei dem vorliegenden Erhitzungsverfahren weit unterhalb der VPTT waren alle oder die meisten Polymerketten unabhängig und weitgehend in ihrer Dispersion gequollen; um VPTT herum begannen sie zu aggregieren, und nach VPTT waren alle Polymere aggregiert, um eine heterogene Suspension der Polymere im Lösungsmittel (im vorliegenden Fall Wasser) zu bilden, was zu einer Lichtdurchlässigkeit von 0% führte. VPTT ist der Zeitpunkt, an dem die Polymerketten massiv zu aggregieren beginnen. Es ist leicht vorstellbar, dass die Polymerketten leicht aufeinandertreffen und in einer Dispersion mit höherer Konzentration aggregieren, und es ist eine kürzere Zeit erforderlich, um eine Verringerung der Transmission zu erreichen, die der in einer verdünnten Dispersion entspricht.
VPTT von P(OEGDA-MAA) Hydrogel in Ethanol
Im Gegensatz zu VPTT vom LCST-Typ wurden Studien an den Polymeren mit UCST oder VPTT vom UCST-Typ in deutlich geringerem Umfang berichtet [38]. Polysulfobetain [39] und Poly(N -Acrylolyglyciamid) [40,41,42] sind die Polymere, die Berichten zufolge mit UCST in Wasser vorliegen, während Polyacrylamid [43] und Poly(acetoacetoxyethylmethacrylat) [44] Berichten zufolge eine UCST in binärem Ethanol/Wasser-Lösungsmittelgemisch aufweisen. Rothet al. zeigten, dass Poly[oligo(ethylenglycol)methylethermethacrylat] (POEGMA) in einer Vielzahl von aliphatischen Alkoholen UCST aufweist und dass die UCST-Phasenübergangstemperatur von der Struktur, dem Molekulargewicht und der Konzentration von POEGMA abhängt, da sowie das Lösungsmittel Co-Solventien [45]. Es wurde auch berichtet, dass P(NIPAM) ein UCST-Verhalten in einer Ethanol/Wasser-Mischung zeigt [46].
Anders als der Test mit VPTT vom LCST-Typ in Wasser wurde die Untersuchung von VPTT vom UCST-Typ dieses Materials in Ethanol durchgeführt. Die Transmission wurde von 70 °C bis 15 °C mit einer Gleichgewichtszeit von 5 min bei jeder Temperatur aufgezeichnet (Abb. 5). Bei einer Temperatur von 70 °C oder höher war die Hydrogel-Ethanol-Dispersion homogen und transparent mit einer Durchlässigkeit von 100 % für alle Proben, außer derjenigen mit der höchsten Konzentration von 30 mg/ml, deren Durchlässigkeit . war etwa 95 %. Wir glauben, dass mit einer verlängerten Gleichgewichtszeit eine Durchlässigkeit von 100 % erreicht werden würde. Diese hohe Transmission war ein Hinweis darauf, dass das Hydrogelpolymer stark gequollen war und die Dispersion wie eine authentische Lösung aussah. Mit abnehmender Temperatur wurde bei allen Proben eine Abnahme der Transmission beobachtet, die eindeutig konzentrationsabhängig war. Bei einer Temperatursenkung auf 60 °C blieb die Durchlässigkeit für die beiden Proben mit niedrigerer Konzentration (1 und 2 mg/ml) bei 100 %, und eine erkennbare Abnahme der Durchlässigkeit wurde nur beobachtet, wenn die Temperatur unter 60 °C fiel, während für Bei den drei Proben mit höherer Konzentration (5, 10 und 30 mg/mL) wurde ab 70 °C eine deutliche Abnahme der Transmission festgestellt, und die Abnahme war bei der Probe mit höherer Konzentration signifikanter. Bei 60 °C fiel die Transmission der Proben auf 87, 80 bzw. 70 %, streng geordnet nach ihrer Konzentration von niedrig bis hoch. Dies war genau das gleiche, das bei der niedrigen VPTT in Wasser beobachtet wurde und durch den Konzentrationseffekt leicht verständlich. Der einzige Unterschied bestand darin, dass es sich hier um Ethanol statt Wasser handelte und durch die Temperaturabsenkung die intra- und intermolekularen Wechselwirkungen der Hydrogel-Polymere an Bedeutung gewannen, diese Wechselwirkungen die zwischen Polymer und Ethanol überholten. Ethanolmoleküle, die mit Polymerketten oberhalb der VPTT assoziiert waren, wurden nach und nach dissoziiert, wenn die Temperatur verringert wurde, und die Polymerketten begannen sich selbst zu aggregieren, wenn die Temperatur nahe der VPTT lag, was zu einer Abnahme der Lichtdurchlässigkeit führte, wie in Abb. 5 gezeigt.
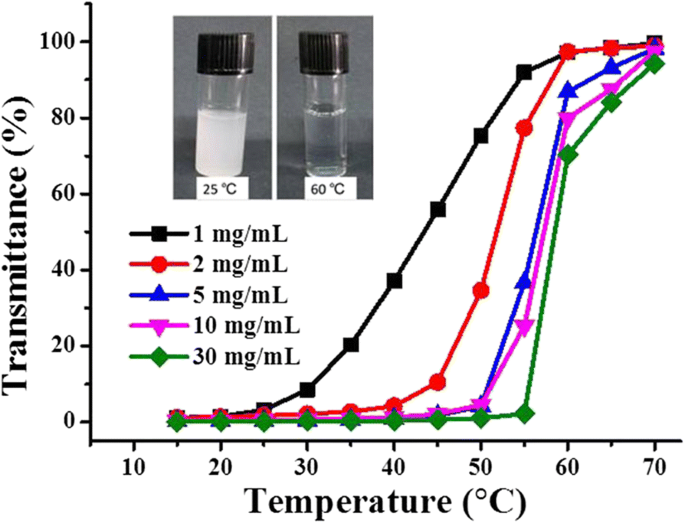
Transmission von P(OEGDA-MAA) in Ethanol mit unterschiedlicher Konzentration. Die Einschübe sind die optischen Bilder der Hydrogele in Ethanol (1 mg/ml) bei 25 bzw. 60 °C
Phasenübergangsmechanismus
Um den Mechanismus dieses VPTT vom UCST-Typ besser zu verstehen, wurde die Größe der Hydrogelpartikel bei einer Konzentration von 1 mg/ml im Kühlprozess bei unterschiedlicher Temperatur (Zeit) mit DLS gemessen, genau wie beim VPTT vom LCST-Typ. Die Ergebnisse sind in Abb. 6 dargestellt. Eine sehr kleine Partikelgröße mit einem Radius von etwa 8 nm (R h ) wurde bei 60 °C erhalten, obwohl die Probe homogen und transparent aussah. Die geringe Größe der Hydrogelpartikel stimmte mit der Größe des Nanogels in Wasser unterhalb dieser niedrigen VPTT bei 10 °C (Durchmesser 15 nm, Abb. 4) überein, was ein Hinweis darauf sein kann, dass das vernetzte Hydrogel weitgehend auf aufgequollen war ein Zustand, der bei einer so niedrigen Konzentration auf molekularer Ebene einzeln gelöst wäre und die hydrophilen Kettenenden (hauptsächlich Carboxylgruppen) vollständig in Richtung des umgebenden Lösungsmittels verlängert sind; das ganze System war in der Tat homogen und erschien völlig transparent. Angesichts der verwendeten Menge an MAA (60 Mol-%) und seiner hohen Löslichkeit in Wasser ist es nicht ausgeschlossen, dass einige Kettensegmente und insbesondere Kettenenden, die nur aus MAA bestehen, in den Polymeren gut vorhanden waren. These chain ends would be the most exposed towards the surrounding solvent in their fully swelled state, i.e., towards water below the LCST-type VPTT and towards ethanol above the UCST-type VPTT. Owing to the limited number of the hydrophilic chain ends and their high hydration, the size of the hydrogel particles detected might be only the size of the crosslinked core, as shown by the encircled area in Fig. 7. In fact, hydrogel particles with their R h around 10 nm, determined by DLS, were often reported. Diverse examples are available, such as polyacrylamide above its UCST in aqueous alcohol solutions [43] and 4-propoxyazobenzene-terminated PNIPAM in aqueous solution below its LCST [47]. And R h as small as 2 to 3 nm was reported for an OEG-based responsive polymer below its LCST [48]. For the present polymer, by decreasing the temperature from 60 to 45 °C, very close to the VPTT, the R h of the hydrogel particle size slightly increased to about 7 nm. This increase might be caused by the collapse of the hydrophilic chain ends, which were extended into ethanol at temperature above the UCST-type VPTT as discussed above. At this stage, the crosslinked core of the hydrogel particles was largely shrunk because the ethanol molecules were squeezed out of the polymer inner, owing to a decrease in the interaction of the polymer chains with ethanol molecules by decreasing the temperature, accompanied by an increase in the interaction of the polymer chains between themselves. By further decreasing the temperature to 40 °C just across the UCST (43 °C), the radius of the hydrogel particles abruptly increased to a significantly large size of 150 nm, very similarly to what observed for the aqueous dispersion shown in Fig. 4 when the temperature was increased across the LCST-type VPTT. This size here is no more that of a single crosslinked nanogel as above but rather that of the aggregate of the nanogel particles, as illustrated in Fig. 7. The radius of the particle aggregates further grew to 270 nm with the temperature further decreased to 25 °C. This suggests that, before reaching the UCST-type VPTT, the transmittance decrease was due to mainly the change in polymer chain conformation, i.e., the hydrophilic chains (ethylene oxide segments, and particularly carboxylic groups) were changed from their full extension in the solvent to coils on the surface of the individual hydrogel polymer particles with a crosslinked core for each, whereas the transmittance decrease around the VPTT was caused by self-aggregation of the nanogel particles (unimers), in accordance with further disassociation of ethanol molecules from the polymer chains. This has been named as a two-step process including dehydration of the particles (unimers) and their aggregation [16, 35, 37, 49]. In characterization of LCST or VPTT by varying temperature, the disassociation of the hydrophilic chains from the solvent molecules leads to the formation of a core-shell structure, with the hydrophobic polymer chains as the core and the dehydrated chains as the shell, this mechanism is also described as formation of core-shell micelles followed by their aggregation [16, 37]. A schematic illustration is given in Fig. 7 for this mechanism.
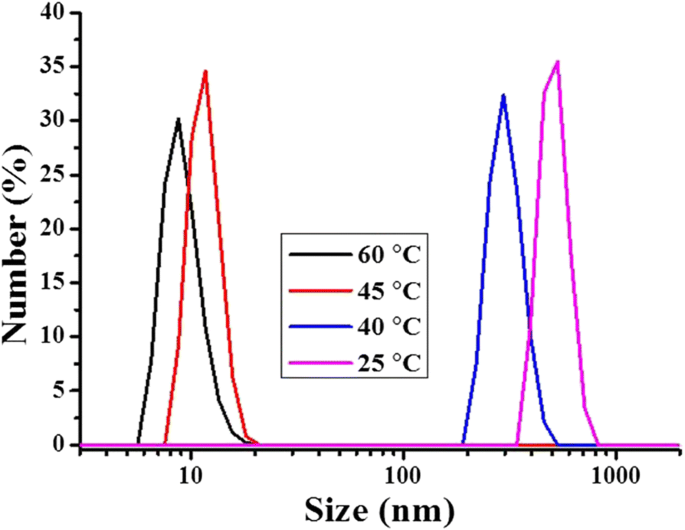
Diameter of P(OEGDA-MAA) hydrogels in ethanol (1 mg/mL) at different temperature
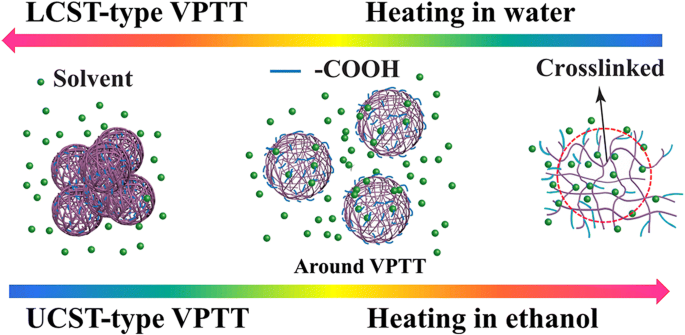
Schematic illustration of the VPTT mechanism for the UCST-type VPTT of P(OEGDA-MAA) in ethanol
Schlussfolgerungen
A novel responsive polymer based on OEG, P(OEGDA-MAA), is prepared through precipitation copolymerization of OEGDA with MAA. The polymer prepared with 40 mol% of OEGDA was chemically crosslinked and showed a distinct LCST-type VPTT of 33 °C in water at pH 1.0 and concentration of 1.0 mg/mL. This VPTT was closely concentration and pH dependent. It shifted towards lower temperature with increased concentration, whereas a shift towards higher temperature was observed with increased pH, and the VPTT completely disappeared at pH 5. This same polymer exhibited also a UCST-type VPTT in ethanol at 43 °C, which was equally concentration dependent. The size evolution of the hydrogel particles versus temperature was measured for the two types of dispersions across their VPTT. For the LCST-type VPTT in water, a slight size increase was detected with increased temperature as long as the temperature was below this VPTT; and a dramatic size increase was observed once the temperature was increased to above this LCST-type VPTT. For the UCST-type VPTT in ethanol, the opposite was observed, i.e., a slight size increase with decreased temperature as long as the temperature was above this VPTT, and a dramatic size increase once the temperature was lowered below the UCST-type VPTT. These results suggest that the responsiveness of the polymer follows a two-step process, including a transition of polymer chain conformation from extended status to coil-form due to the dehydration of the hydrophilic chains from the largely swelled state, followed by an aggregation of the individual particles. This work provides therefore a novel type of candidate materials for potential applications in biomedical fields.
Abkürzungen
- APS:
-
Ammonium persulfate
- ATRP:
-
Atom transfer radical polymerization
- DLS:
-
Dynamische Lichtstreuung
- EG:
-
Ethylene glycol
- LCST:
-
Lower critical solution temperature
- MAA:
-
Methacrylic acid
- OEG:
-
Oligo(ethylene glycol)
- OEGDA:
-
Oligo(ethylene glycol) diacrylate
- P(OEGDA-MAA):
-
Poly(oligo(ethylene glycol) diacrylate-methacrylic acid)
- PEG:
-
Poly(ethylene glycol)
- PNIPAM:
-
P(N -isopropylacrylamide)
- POEGMA:
-
Poly[(oligo(ethylene glycol) methyl ether methacrylate]
- RAFT:
-
Reversible addition-fragmentation chain transfer polymerization
- R h :
-
Hydrodynamic particle radius
- UCST:
-
Upper critical solution temperature
- VPTT:
-
Volume phase transition temperature
Nanomaterialien
- Herstellung und magnetische Eigenschaften von kobaltdotierten FeMn2O4-Spinell-Nanopartikeln
- Herstellung von ICA-beladenen mPEG-ICA-Nanopartikeln und ihre Anwendung bei der Behandlung von LPS-induzierter H9c2-Zellschädigung
- Auf dem Weg zu TiO2-Nanofluiden – Teil 1:Vorbereitung und Eigenschaften
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Paramagnetische Eigenschaften von Fulleren-abgeleiteten Nanomaterialien und ihren Polymerverbundstoffen:Drastischer Pump-Out-Effekt
- Synthese von ZnO-Nanokristallen und Anwendung in invertierten Polymersolarzellen
- Herstellung und photokatalytische Leistung von Hohlstruktur-LiNb3O8-Photokatalysatoren
- Herstellung von PPy-beschichteten MnO2-Hybrid-Mikromaterialien und ihre verbesserte zyklische Leistung als Anode für Lithium-Ionen-Batterien
- Synthese und Charakterisierung von modifiziertem BiOCl und ihre Anwendung bei der Adsorption von Farbstoffen niedriger Konzentration aus wässriger Lösung
- Herstellung und Charakterisierung von ZnO-Nano-Clips durch das Polyol-vermittelte Verfahren



