Tuning hierarchischer Eisen(III)-Nanostrukturen-dekorierter Kieselgur für Superkondensatoren
Zusammenfassung
FeOOH-Nanoblätter auf porösem Kieselgur wurden erfolgreich durch einen einfachen zweistufigen hydrothermalen Ansatz für Superkondensatoren hergestellt, und dann α-Fe2 O3 und γ-Fe2 O3 Nanostrukturen werden durch Kalzinieren unter verschiedenen Atmosphären und Temperaturen erhalten. Die Morphologien und Strukturen aller Proben werden im Detail untersucht, um die hierarchische Architektur deutlich zu machen. Außerdem werden systemische Tests in 1 M Na2 . durchgeführt SO4 Elektrolyt, um die elektrochemischen Eigenschaften dieser Materialien zu charakterisieren. Unter den eisenbezogenen Verbundelektroden besitzt Diatomit@FeOOH die höchste spezifische Kapazität (157,9 F g −1 bei einer Stromdichte von 0,5 A g −1 ) und beste Zyklenleistung (98,95 % Retention nach 1000 Zyklen), was als potenzielles Material für Hochleistungs-Superkondensatoren angesehen wird. Darüber hinaus kann die Synthesestrategie auf die Herstellung anderer von Metalloxiden abgeleiteter funktioneller Materialien zur Energiespeicherung und -umwandlung ausgeweitet werden.
Hintergrund
Bisherige große Herausforderungen für Superkondensator-Technologien sind die niedrige Energiedichte und die hohen Produktionskosten. Einige Forschungsanstrengungen wurden unternommen, um seine Nachteile zu verbessern [1]. Einige Übergangsmetalloxide oder -hydroxide wie MnO2 [2,3,4], FeOOH [5], NiO [6] und CuO [7] gelten als potenzielle Kandidaten für aktive Elektrodenmaterialien. Unter diesen Übergangsmetalloxiden haben Eisen(III)-oxide/-hydroxide aufgrund ihres natürlichen Vorkommens, ihrer variablen Oxidationsstufen und ihrer Umweltfreundlichkeit große Aufmerksamkeit auf sich gezogen [8,9,10]. Außerdem wurden Eisenoxide/Hydroxide als besonders wünschenswerte Elektrodenmaterialien für Superkondensatoren angesehen, da ihre Struktur (wie FeOOH vom Tunneltyp) den Ionentransport beschleunigen kann. Allerdings besitzen Eisenoxide/Hydroxide immer noch zwei Haupthindernisse (kleine Oberfläche und geringe elektrische Leitfähigkeit). Nanostrukturen können die Hindernisse ändern und enorme Vorteile in Energiespeichersystemen bieten, die als hohe Lade-Entlade-Raten durch Beschleunigung hoher spezifischer Oberflächen, schnelle Redoxreaktionen und kurze Diffusionswege für Elektronen und Ionen gelten [11]. Untersuchungen haben jedoch gezeigt, dass Eisenoxid-Nanostrukturen dazu neigen, Aggregate zu bilden und sich in große Partikel umzuwandeln, was zu einem starken Verlust der spezifischen Oberfläche führt, was sich ernsthaft auf die elektrochemischen Eigenschaften auswirkt [12]. Daher besteht das Hauptproblem derzeit darin, einen einfachen und praktikablen Weg zu finden, um die Nanostrukturen von Eisen(III)-oxiden effektiv zu dispergieren, beispielsweise durch die Herstellung von Eisen(III)-Metalloxiden auf der Oberfläche poröser Template.
Als wichtiges natürliches poröses Nanomaterial ist Kieselgur aufgrund seiner hohen Porosität, geringen Volumendichte, stabilen chemischen Eigenschaften und großen spezifischen Fläche ein attraktives poröses Templat [13,14,15]. Kieselgur-Templat kann die geringe Oberfläche vergrößern und die Aggregation von Nanostrukturen vermeiden. Obwohl die Eigenschaften ihrer Strukturen offensichtlich und vielversprechend sind, wurden Kieselgur-Komposite auf der Basis von Eisenoxiden/Hydroxiden zur Bildung einer hierarchisch porösen Struktur bisher nur selten in Superkondensatoren untersucht.
In diesem Artikel berichten wir über die erfolgreiche Herstellung von Eisenoxiden/-hydroxiden auf Kieselgur als Superkondensator-Elektrodenmaterialien durch einen effektiven zweistufigen hydrothermalen Ansatz. Unser Ziel war es, Kieselgur als Templat zu verwenden, um Eisenoxid/Hydroxid-Nanostrukturen gleichmäßig auf der Kieselgur-Oberfläche zu verteilen Zusatzdatei 1:SI-5. Bemerkenswerterweise zeigte das endgültige Komposit Diatomit@FeOOH mit dem synergistischen Effekt von Kieselgur und Eisenoxiden/-hydroxiden vielversprechende elektrochemische Eigenschaften in Superkondensatoren.
Experimenteller Abschnitt
Materialsynthese
Alle chemischen Reagenzien waren von analytischer Reinheit und wurden ohne weitere Reinigung verwendet. Synthetische Verfahren sind wie folgt (Abb. 1; mehr Details in Zusatzdatei 1:SI-1).
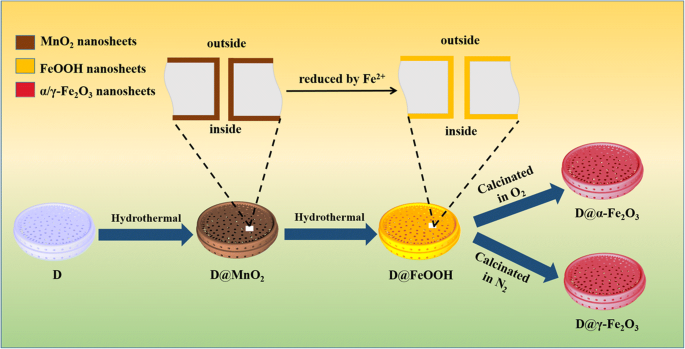
Präparative Route von Kieselguren auf Basis von Eisenoxiden/-hydroxiden
Anfänglich wurde die natürliche Kieselgur über ein einfaches Ölbadverfahren nach den folgenden Verfahren gereinigt. Dann wird das MnO2 -dekorierte Kieselgur wurden nach einem hydrothermalen Verfahren hergestellt. Normalerweise ist der KMnO4 Lösung (30 &mgr;l, 0,05 &mgr;M) wurde mit der gereinigten Kieselgur (30 mg) gemischt. Danach wurde die Mischung in einen mit Teflon ausgekleideten Autoklaven (50 ml) überführt, der 24 h bei 160 °C wärmebehandelt wurde. Die so hergestellte Kieselgur wurde zentrifugiert, mit destilliertem Wasser gewaschen und dann bei 60 °C getrocknet. Danach MnO2 -dekorierte Kieselgur wurde erhalten.
Außerdem eine Lösung von FeSO4 ·7H2 O (0,01 M, 30 mL) wurde zur vollständigen Umwandlung der vorbehandelten Kieselgur@MnO2 . verwendet (30 mg) bei 120°C für 2 h. Am Ende werden die unterschiedlichen Kristallformen (α-Fe2 O3 und γ-Fe2 O3 ) aus mit Eisenoxid dekorierter Kieselgur wurden durch Calcinieren bei 350 °C für 2 h unter O2 . hergestellt Atmosphäre und 500 °C für 2 h unter N2 Atmosphäre.
Charakterisierung
Zur Beobachtung der Morphologien wurde eine fokussierte Ionenstrahl-Rasterelektronenmikroskopie (Zeiss Auriga FIB/SEM) verwendet. Und die Phasenanalyse und Struktur wurden durch Pulver-Röntgenbeugung (XRD; D/max 2500, Cu Kα) ermittelt.
Elektrochemische Messungen
Elektrochemische Untersuchung der Materialien in einem Drei-Elektroden-System:Alle elektrochemischen Eigenschaften der so erhaltenen Kieselgur-Komposite wurden durch eine konventionelle Drei-Elektroden-Ausrüstung, die mit 1 M Na2 . gefüllt war, charakterisiert SO4 Elektrolyt. Vor den Messungen wurden die Arbeitselektroden mit Mischaktivmaterial (Kieselgur@MnO2 , Kieselgur@FeOOH, Kieselgur@α-Fe2 O3 , und Kieselgur@γ-Fe2 O3 ), Acetylenruß und Polyvinylidenfluorid (PVDF) in einem Gewichtsverhältnis von 7:2:1 in N -Methyl-2-pyrrolidon (NMP). Die Aufschlämmung wurde auf Stücke aus geschäumtem Nickelschaum (1 × 1 cm 2 .) aufgetragen ), das erhitzt wurde, um das Lösungsmittel zu verdampfen (120 °C für 12 h). Der Nickelschaum wurde mit etwa 2 mg Elektrodenmaterial beladen. Die elektrochemischen Leistungen und Kapazitätswerte der Verbundelektroden wurden mit zyklischer Voltammetrie (CV), galvanostatischer Aufladung/Entladung (CC) und elektrochemischer Impedanzspektroskopie (EIS) charakterisiert.
Die spezifische Kapazität (C m ) wird durch die folgende Gleichung berechnet:
$$ {C}_m=\frac{I\Delta t}{m\Delta V} $$wo ich ist der Entladestrom, △t ist die Entladezeit, △V ist das potentielle Fenster während der Entladung und m ist das Gewicht der aktiven Materialien.
Ergebnisse und Diskussion
Abbildung 2 zeigt REM-Bilder von MnO2 , FeOOH und α-Fe2 O3 /γ-Fe2 O3 Nanoarrays auf der Kieselgur. Abbildung 2a zeigt das einheitliche und diskrete MnO2 Nanoblätter (Kieselgur@MnO2 ) auf der Kieselgur über ein einfaches hydrothermales Verfahren gezüchtet. Durch Säurebehandlung und Kalzinierung wird MnO2 kann sich durch die Wechselwirkungskraft fest mit Kieselgur verbinden, was Reaktionen zwischen MnO2 . erleichtert und Fe 2+ . Währenddessen erhöhen viele Poren von Kieselgur die Diffusion von Ionen. Abbildung 2b zeigt, dass Kieselgur@FeOOH eine ähnliche Morphologie aufweist wie MnO2 Arrays. Tatsächlich ist MnO2 wird um Fe 2+ . reduziert Ionen und Fe 2+ Ionen in Lösung treten an die Stelle von Mn. Darüber hinaus ist die Vorbehandlung zur Stabilisierung des Kristalls MnO2 und die Unterstützung von Ethylenglykol erzeugen wahrscheinlich die ähnliche Morphologie der Nanoblätter. Die Größe von α-Fe2 O3 Nanoblätter (Abb. 2c) ist größer, und der Abstand zwischen den Blättern ist bei derselben starken Vergrößerung größer als bei γ-Fe2 O3 (Abb. 2d). Die Morphologie der Proben bei geringer Vergrößerung ist in Zusatzdatei 1:SI-2(a–d) ersichtlich. Zusätzlich zeigt Zusatzdatei 1:SI-2(e, f) die entsprechenden EDS-Zuordnungen von Kieselgur@MnO2 und Kieselgur@Fe2 O3 und weiter die Existenz konvictiver Elemente (Mn, Fe und O) beweisen, was die Bildung von MnO2 . bestätigt und Fe2 O3 Nanoblätter. Außerdem zeigt zusätzliche Datei 1:SI-2(f), dass kein Mn-Element in dem auf Kieselgur geladenen FeOOH vorhanden ist, was darauf hindeutet, dass das MnO2 Nanoblätter wurden vollständig in Eisenhydroxide überführt.
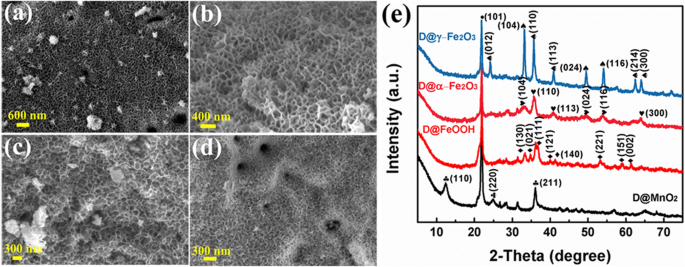
REM-Aufnahmen von Kieselgur@MnO2 Nanokomposit (a ), Kieselgur@FeOOH-Nanokomposit (b ), Kieselgur@α-Fe2 O3 Nanokomposit (c ), Kieselgur@γ-Fe2 O3 Nanokomposit (d ); XRD-Muster der vier Proben (e )
XRD-Muster der so erhaltenen Proben sind in Fig. 2e gezeigt, um die Phasenzusammensetzung und Struktur der Produkte zu bestätigen. Es ist anzumerken, dass die stärksten Peaks der vier mit einem Punktsymbol gekennzeichneten Proben in allen Kurven die charakteristischen Peaks des Kieselgursubstrats sind. Die Kieselgur@MnO2 Probe zeigte Beugungspeaks bei 2θ = 12,784°, 25,711° und 37,522°, entsprechend den (110), (220) und (211) Kristallebenen (JCPDS-Karte Nr. 44-0141). Bei FeOOH-Nanoblatt-Arrays wurden drei Beugungspeaks des MnO2 verschwinden in der roten Kurve, während einige gut definierte Beugungspeaks gut mit dem Standard-XRD-Muster von FeOOH (JCPDS-Karte Nr. 29-0713) übereinstimmen, das mit (130), (021), (111) übereinstimmt, ( 121), (140), (221), (151) und (002) Ebene. Die XRD-Ergebnisse der Eisenoxid-/Hydroxid-Proben zeigen, dass das MnO2 Peaks verschwanden und zeigen, dass es kein MnO2 . gibt Nanoblätter vorhanden. Daher zeigen sowohl die EDS-Kartierung als auch die XRD-Ergebnisse, dass MnO2 wird komplett durch Fe 2+ . ersetzt Ionen in dieser Arbeit. Darüber hinaus sind die Beugungspeaks von α-Fe2 O3 sind schwächer als die von γ-Fe2 O3 etwa 24,138° und 62,449°, den (012)- und (214)-Ebenen des Eisenoxidkristalls vom Hämatit-Typ zugeordnet (beide sind JCPDS-Karte Nr. 33-0664). Es bestätigt erneut, dass der Austausch zwischen MnO2 und Fe 2+ Ionen treten erfolgreich an den Grenzflächen von Kieselgur und Lösung auf.
Um die elektrochemischen Eigenschaften der vier Proben zu untersuchen, wurde ein Drei-Elektroden-System in 1 M Na2 . durchgeführt SO4 wässriger Elektrolyt. Die Unterschiede in Morphologie und Struktur dieser vier Proben können zu unterschiedlichen elektrochemischen Leistungen führen. Kieselgur dient als Substrat und trägt aufgrund seiner porösen Strukturen zum effizienten Transport von Ionen bei.
Wie in Zusatzdatei 1 gezeigt:SI-3(a, b), die CV- und CC-Kurven von Kieselgur@MnO2 Elektroden sind quasi-rechteckig bzw. nahezu symmetrisch dreieckig. Es gibt keine deutlichen Redoxpeaks, die von dem idealen Rechteck abweichen, was die faradische pseudokapazitive Natur der Elektrode manifestiert. Wie in Zusatzdatei 1 gezeigt:SI-3(c, d), hat Kieselgur@FeOOH die besseren kapazitiven Eigenschaften als die anderen beiden Proben (Kieselgur@α/γ-Fe2 O3 ). Die spezifische Kapazität von Kieselgur@FeOOH-Elektroden beträgt etwa 157,9 F g −1 bei einer Stromdichte von 0,5 A g −1 , was zeigt, dass die hochporöse Struktur mehr Ionen in ihre Oberfläche übertragen und mehr redox-faradische Reaktionen fördern kann. In Übereinstimmung mit den REM-Ergebnissen sind die Abstände von α-Fe2 O3 Nanoblätter sind so groß, dass die Oberfläche des aktiven Materials die Kationen weniger nutzt, während γ-Fe2 O3 kann die kleinste spezifische Fläche für Ionen unter den drei Eisenoxidproben bereitstellen. Daher ist der Abstand der Nanoblätter der Proben sehr wichtig. Außerdem hat die Kieselgur@FeOOH-Elektrode in dieser Arbeit, wie in Tabelle 1 gezeigt, eine höhere spezifische Kapazität unter diesen Elektroden auf Eisenoxid/Hydroxid-Basis im Vergleich zu früheren Arbeiten.
Daher werden systematische Tests durchgeführt, um die elektrochemischen Eigenschaften der Kieselgur@FeOOH-Elektrode besser zu untersuchen. Abbildung 3a zeigt typische CV-Kurven einer FeOOH-Probe im Potentialbereich von − 1 bis 0 V bei unterschiedlichen Abtastraten. Galvanostatische Ladungs-Entladungs-Kurven einer Kieselgur@FeOOH-Elektrode bei verschiedenen Stromdichten sind in Abb. 3b dargestellt. Die Form der CV- und CC-Kurven der Kieselgur@FeOOH-Elektrode zeigt die Pseudokapazitätseigenschaften von Kieselgur@FeOOH. Abbildung 3c veranschaulicht weiter die Beziehung zwischen spezifischer und Stromdichte. Die Zyklenfähigkeit der Kieselgur@FeOOH-Elektrode wurde einem Langzeittest für aufeinanderfolgende 1000 Zyklen unterzogen (Abb. 3d), und die Kapazitätserhaltung nach 1000 Zyklen beträgt etwa 98,95 %. Die CC-Kurven der letzten 10 -Zyklen deuten auf keine größeren Strukturvariationen während der Lade-Entlade-Prozesse hin. Außerdem enthalten die Nyquist-Plots für die FeOOH-Probenelektrode (Zusatzdatei 1:SI-4) einen Halbkreis im Hochfrequenzbereich und eine Gerade im Niederfrequenzbereich. Der Innenwiderstand (R s ) der Elektrode beträgt etwa 3,0 und 3,5 vor und nach 1000 Zyklen ohne große Schwankungen, während der Ladungsübergangswiderstand (R ct ) beträgt etwa 1,2 und 4,0 Ω vor und nach 1000 Zyklen. Diese Erkenntnisse könnten für die guten elektrochemischen Eigenschaften der Kieselgur@FeOOH-Elektrode verantwortlich sein.
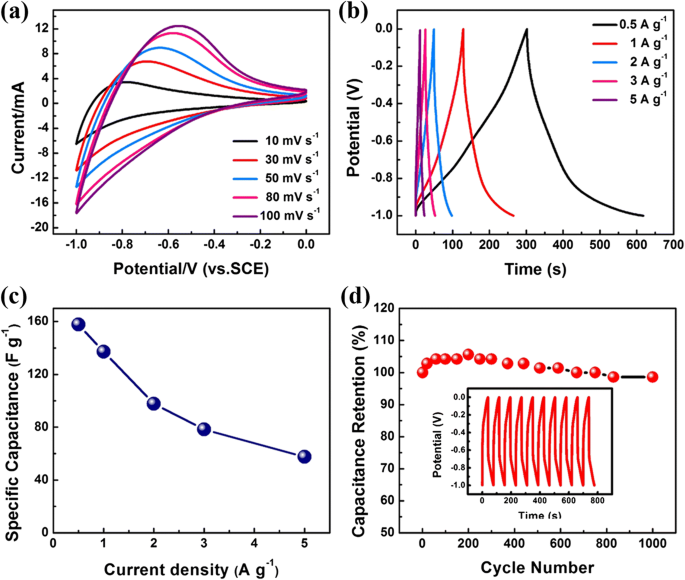
a CV-Kurven von Diatomite@FeOOH, gemessen bei verschiedenen Scanraten. b CC-Kurven von Diatomit@FeOOH, gemessen bei verschiedenen Stromdichten. c Spezifische Kapazität gemessen bei verschiedenen Stromdichten. d Zyklenleistung der Elektrode bei einer Stromdichte von 1 A g −1 (der Einschub zeigt die Lade-Entlade-Kurven der letzten 10 Zyklen)
Schlussfolgerungen
Zusammenfassend stellen wir mit Eisenoxiden dekorierte Kieselgur in Kombination mit einem anschließenden Austauschprozess durch einen einfachen und effektiven hydrothermalen Ansatz her. Diese Eisenoxide/Hydroxide besitzen fein kontrollierte Morphologien und Nanoblattstrukturen. Diatomit@FeOOH-Material weist vielversprechende elektrochemische Eigenschaften auf, die anderen Eisenoxidmaterialien überlegen sind. Die spezifische Kapazität von Kieselgur@FeOOH beträgt 157,9 F g −1 bei einer Stromdichte von 0,5 A g −1 , und seine Zyklenleistung ist gut (98,95 % Retention nach 1000 Zyklen). Tatsächlich könnte die hierarchische und poröse Kieselgur@FeOOH ein vielversprechendes aktives Material für Superkondensatoren sein. Darüber hinaus kann eine solche Synthesestrategie auf die Herstellung anderer von Metalloxiden abgeleiteter funktioneller Materialien zur Energiespeicherung und -umwandlung ausgeweitet werden.
Abkürzungen
- CC:
-
Galvanostatisches Laden/Entladen
- Lebenslauf:
-
Zyklische Voltammetrie
- EIS:
-
Elektrochemische Impedanzspektroskopie
- FIB/SEM:
-
Fokussierte Ionenstrahl-Rasterelektronenmikroskopie
- NMP:
-
N -Methyl-2-pyrrolidon
- PVDF:
-
Polyvinylidenfluorid
- XRD:
-
Pulver-Röntgenbeugung
Nanomaterialien
- Luftabstandshalter für 10-nm-Chips
- Nanobeschichtung für mehrere Farben
- Nanodiamanten für magnetische Sensoren
- Nanobäume für farbstoffsensibilisierte Solarzellen
- Nano-Heterojunctions für Solarzellen
- Aktivkohlefasern mit hierarchischer Nanostruktur aus Baumwollhandschuhabfällen als Hochleistungselektroden für Superkondensatoren
- Miniaturisierte dehnbare und hochfrequente lineare Superkondensatoren
- Monodisperse Kohlenstoff-Nanosphären mit hierarchischer poröser Struktur als Elektrodenmaterial für Superkondensatoren
- Hierarchische Heterostruktur von ZnO@TiO2-Hohlkugeln für eine hocheffiziente photokatalytische Wasserstoffentwicklung
- Nukleosid-Lipid-basierte Nanoträger für die Sorafenib-Verabreichung



